–≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—П, –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—П –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–∞—П —Б–≤—П–Ј—М –Т–У–І-6 —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є
–Т–Є—А—Г—Б –≥–µ—А–њ–µ—Б–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ 6 —В–Є–њ–∞ (–Т–У–І-6) –≤–њ–µ—А–≤—Л–µ –±—Л–ї –Њ–±–љ–∞—А—Г–ґ–µ–љ –≤ 1986 –≥. —Г –Т–Ш–І-–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞, –Ї–Њ—В–Њ—А—Л–є —Б—В—А–∞–і–∞–ї –Њ—В –ї–Є–Љ—Д–Њ–њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [1].
–Ґ–∞–Ї –ґ–µ –Ї–∞–Ї —Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б –Є –≤–Є—А—Г—Б –≥–µ—А–њ–µ—Б–∞ 7 —В–Є–њ–∞, –Т–У–І-6 –Њ—В–љ–Њ—Б—П—В –Ї –±–µ—В–∞-–≥–µ—А–њ–µ—Б–≤–Є—А—Г—Б–∞–Љ. –Ш–Љ–µ—О—В—Б—П –µ–≥–Њ –і–≤–µ —А–∞–Ј–ї–Є—З–љ—Л–µ –њ–Њ–і–≥—А—Г–њ–њ—Л: –Т–У–І-6–Р –Є –Т–У–І-6–Т, –Ї–Њ—В–Њ—А—Л–µ –љ–∞ 95% –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є —В–Њ–ґ–і–µ—Б—В–≤–µ–љ–љ—Л. –І–µ—А–µ–Ј 20 –ї–µ—В –њ–Њ—Б–ї–µ –Њ—В–Ї—А—Л—В–Є—П –Т–У–І-6 —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –µ–≥–Њ –≤–∞—А–Є–∞–љ—В–∞–Љ–Є –і–Њ—Б—В–Є–≥–ї–Є —В–∞–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є, —З—В–Њ –Є—Е —Б—В–∞–ї–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –Ї–∞–Ї –і–≤–∞ —А–∞–Ј–љ—Л—Е –≤–Є–і–∞.
–Т–У–І-6 —Б–Њ—Б—В–Њ–Є—В –Є–Ј –Ї–∞–њ—Б–Є–і–∞ –Є–Ї–Њ—Б–∞—Н–і—А–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л, –Њ–Ї—А—Г–ґ–µ–љ–љ–Њ–≥–Њ —В–µ–≥—Г–Љ–µ–љ—В–Њ–Љ –≤ –ї–Є–њ–Є–і–љ–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ –і–Є–∞–Љ–µ—В—А–Њ–Љ –Њ–Ї–Њ–ї–Њ 200 –љ–Љ [2].
–С–Њ–ї–µ–µ 90% –ї—О–і–µ–є –њ—А–Є–Њ–±—А–µ—В–∞—О—В –Т–У–І-6–Т –≤ —А–∞–љ–љ–µ–Љ –і–µ—В—Б—В–≤–µ –≤ –≤–Є–і–µ –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Н–Ї–Ј–∞–љ—В–µ–Љ—Л –Љ–µ–ґ–і—Г 6 –Љ–µ—Б. –Є 2 –≥–Њ–і–∞–Љ–Є –њ–Њ—Б–ї–µ —Г—В—А–∞—В—Л –Љ–∞—В–µ—А–Є–љ—Б–Ї–Є—Е –њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е –∞–љ—В–Є—В–µ–ї. –Ш–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ –Т–У–І-6–Р –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–µ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –Є –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Ї–∞–Ї–Є–Љ–Є-–ї–Є–±–Њ —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є. –Р–љ—В–Є—В–µ–ї–∞ –Ї –Т–У–І-6 –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В –±–Њ–ї–µ–µ —З–µ–Љ —Г 90% –љ–∞—Б–µ–ї–µ–љ–Є—П —А–∞–Ј–≤–Є—В—Л—Е —Б—В—А–∞–љ [3]. –Я–Њ—Б–ї–µ –њ–µ—А–≤–Є—З–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Т–У–І-6–Р –Є –Т–У–І-6–Т –њ–Њ–ґ–Є–Ј–љ–µ–љ–љ–Њ –Њ—Б—В–∞—О—В—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –≤ –ї–∞—В–µ–љ—В–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –Є –Љ–Њ–≥—Г—В —А–µ–∞–Ї—В–Є–≤–Є—А–Њ–≤–∞—В—М—Б—П, –≤—Л–Ј—Л–≤–∞—П –ї–Є—В–Є—З–µ—Б–Ї—Г—О –Є–љ—Д–µ–Ї—Ж–Є—О. –Т –Љ–∞–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Т–У–І-6–Р –Є –Т–У–І-6–Т –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —В–Ї–∞–љ—П—Е –Є –Њ—А–≥–∞–љ–∞—Е: –≤ –Ї–ї–µ—В–Ї–∞—Е –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –≤ –Љ–Є–љ–і–∞–ї–Є–љ–∞—Е, —Б–ї—О–љ–љ—Л—Е –ґ–µ–ї–µ–Ј–∞—Е, –њ–Њ—З–Ї–∞—Е, –њ–µ—З–µ–љ–Є, –ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є—Е —Г–Ј–ї–∞—Е, —П–Є—З–Ї–∞—Е, –≤ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е, –Љ–Њ–љ–Њ—Ж–Є—В–∞—Е –Є –Љ–∞–Ї—А–Њ—Д–∞–≥–∞—Е. –Т–У–І-6–Р –Є –Т–У–І-6–Т вАФ –Ґ-–ї–Є–Љ—Д–Њ—В—А–Њ–њ–љ—Л–µ –≤–Є—А—Г—Б—Л, –љ–Њ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–Љ–Є –ї–Њ–Ї—Г—Б–∞–Љ–Є –ї–∞—В–µ–љ—В–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —П–≤–ї—П—О—В—Б—П –Ї–ї–µ—В–Ї–Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л (–¶–Э–°), –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–∞—А—Л –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є [4]. –Ы–∞—В–µ–љ—В–љ—Л–є –≤–Є—А—Г—Б –Љ–Њ–ґ–µ—В —А–µ–∞–Ї—В–Є–≤–Є—А–Њ–≤–∞—В—М—Б—П —Г –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ–µ—В–µ–љ—В–љ—Л—Е, –Є, —З—В–Њ –±—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —З–∞—Й–µ, —Г –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ—А–Њ–Љ–µ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –ї–Є—Ж. –†–µ–∞–Ї—В–Є–≤–∞—Ж–Є—П –Т–У–І-6 –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–∞ —Б —Н–њ–Є–ї–µ–њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Є–њ–∞–і–Ї–∞–Љ–Є, —Н–љ—Ж–µ—Д–∞–ї–Є—В–Њ–Љ –Є –Њ—В—В–Њ—А–ґ–µ–љ–Є–µ–Љ —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—В–∞ [5вАУ7].
–Т–У–І-6 –Є–љ—Д–Є—Ж–Є—А—Г–µ—В CD4+-–ї–Є–Љ—Д–Њ—Ж–Є—В—Л, –њ—А–Є–≤–Њ–і—П –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Є—Е —Г—А–Њ–≤–љ—П, —З—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М –Ї–Њ—Д–∞–Ї—В–Њ—А–Њ–Љ –њ—А–Њ–≥—А–µ—Б—Б–Є–Є –°–Я–Ш–Ф–∞, –Њ–і–љ–∞–Ї–Њ –і–ї—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ —В—А–µ–±—Г—О—В—Б—П –і–∞–ї—М–љ–µ–є—И–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П [8].
–Т–У–І-6 –Њ–±–ї–∞–і–∞–µ—В —В—А–Њ–њ–Є–Ј–Љ–Њ–Љ –Ї –љ–µ–є—А–Њ–љ–∞–Љ –Є –і–µ–љ–і—А–Є—В–љ—Л–Љ –Ї–ї–µ—В–Ї–∞–Љ –¶–Э–°. –Ш–Ј –і–≤—Г—Е –≤–∞—А–Є–∞–љ—В–Њ–≤ –±–Њ–ї–µ–µ –љ–µ–є—А–Њ–≤–Є—А—Г–ї–µ–љ—В–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –Т–У–І-6–Р, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –µ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–µ–є –≤ –±–ї—П—И–Ї–∞—Е –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –њ—А–Є —А–∞—Б—Б–µ—П–љ–љ–Њ–Љ —Б–Ї–ї–µ—А–Њ–Ј–µ. –Ф—А—Г–≥–Є–µ –≥–µ—А–њ–µ—Б–≤–Є—А—Г—Б—Л —З–µ–ї–Њ–≤–µ–Ї–∞ –њ—А–Є –ї–∞—В–µ–љ—Ж–Є–Є –љ–∞—Е–Њ–і—П—В—Б—П –≤ –≤–Є–і–µ –Ї–Њ–ї—М—Ж–µ–≤–Є–і–љ–Њ–є —Н–њ–Є—Б–Њ–Љ—Л –≤ —П–і—А–µ –Ї–ї–µ—В–Њ–Ї —Е–Њ–Ј—П–Є–љ–∞. –Ю–і–љ–∞–Ї–Њ –Т–У–І-6–Р –Є –Т–У–І-6–Т –Љ–Њ–≥—Г—В –Є–љ—В–µ–≥—А–Є—А–Њ–≤–∞—В—М—Б—П –≤ —Е—А–Њ–Љ–Њ—Б–Њ–Љ—Л –Є –њ–µ—А–µ–і–∞–≤–∞—В—М—Б—П –≤–µ—А—В–Є–Ї–∞–ї—М–љ–Њ —З–µ—А–µ–Ј –≥–µ—А–Љ–Є–љ–∞—В–Є–≤–љ—Л–µ –Ї–ї–µ—В–Ї–Є. –І–∞—Б—В–Њ—В–∞ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ–Њ–є –Є–љ—В–µ–≥—А–∞—Ж–Є–Є –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–љ–Њ—А–Њ–≤ –Ї—А–Њ–≤–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 0,8вАУ1,5% [9]. –Ш–љ—В–µ–≥—А–Є—А–Њ–≤–∞–љ–љ—Л–є –≥–µ–љ–Њ–Љ –≤–Є—А—Г—Б–∞ –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –≤ –Ї–Њ–љ—Ж–µ–≤—Л—Е –Њ–±–ї–∞—Б—В—П—Е —Е—А–Њ–Љ–Њ—Б–Њ–Љ вАФ —В–µ–ї–Њ–Љ–µ—А–∞—Е. –£ –ї–Є—Ж, –Ї–Њ—В–Њ—А—Л–µ —Г–љ–∞—Б–ї–µ–і–Њ–≤–∞–ї–Є —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ—Г—О –Є–љ—В–µ–≥—А–∞—Ж–Є—О –Т–У–І-6, –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В –Њ–і–љ—Г –Ї–Њ–њ–Є—О –≤–Є—А—Г—Б–∞ –љ–∞ –Ї–ї–µ—В–Ї—Г –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Я–Њ–і–Њ–Ј—А–µ–≤–∞—В—М –≤–Є—А—Г—Б–љ—Г—О –Є–љ—В–µ–≥—А–∞—Ж–Є—О —Б–ї–µ–і—Г–µ—В –њ—А–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤–Є—А—Г—Б–∞ 105 –Ї–Њ–њ–Є–є/–Љ–ї –Є –≤—Л—И–µ.
–Ф–∞–љ–љ—Л–µ –Ј–∞ —Г—З–∞—Б—В–Є–µ –Т–У–І-6 –≤ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –±–Њ–ї–µ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ –љ–µ–Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л. –Ґ–∞–Ї, –Р. Krumina et al. [10] —Б–Њ–Њ–±—Й–∞—О—В –Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Т–У–І-6 —Б —Д–Є–±—А–Њ–Љ–Є–∞–ї–≥–Є–µ–є. –£ 23 –Є–Ј 43 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Н—В–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –Ф–Э–Ъ –Т–У–І-6 –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –≥—А—Г–њ–њ–µ –Ї–Њ–љ—В—А–Њ–ї—П –Є–љ—Д–µ–Ї—Ж–Є—О –≤—Л—П–≤–ї—П–ї–Є –ї–Є—И—М —Г 3 –Є–Ј 50 —З–µ–ї–Њ–≤–µ–Ї. –Я—А–Є —Н—В–Њ–Љ —Г 29 –Є–Ј 43 –±–Њ–ї—М–љ—Л—Е —Д–Є–±—А–Њ–Љ–Є–∞–ї–≥–Є–µ–є –Є–Љ–µ–ї–Є—Б—М —А–∞–Ј–ї–Є—З–љ—Л–µ —Б—В–µ–њ–µ–љ–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Р-–і–µ–ї—М—В–∞- –Є –°-–љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –љ–∞—А—Г—И–µ–љ–Є—П —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–є –Є –±–Њ–ї–µ–≤–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є.
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Г–ґ–µ –±–Њ–ї–µ–µ 25 –ї–µ—В –Њ–±—Б—Г–ґ–і–∞—О—В —А–Њ–ї—М –Т–У–І-6 –њ—А–Є —А–∞—Б—Б–µ—П–љ–љ–Њ–Љ —Б–Ї–ї–µ—А–Њ–Ј–µ [11, 12]. –°—А–µ–і–Є –њ—А–Њ—З–Є—Е –њ—А–Є—З–Є–љ –Т–У–І-6 —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В –≤ –Ї–∞—З–µ—Б—В–≤–µ –Њ–і–љ–Њ–≥–Њ –Є–Ј —Б–∞–Љ—Л—Е –Ј–љ–∞—З–Є–Љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е —В—А–Є–≥–≥–µ—А–Њ–≤, –Ј–∞–њ—Г—Б–Ї–∞—О—Й–Є—Е –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –њ—А–Є —Н—В–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є. –Т–Є—А—Г—Б—Л –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є –≤ –њ—А–Њ–±–∞—Е —В–Ї–∞–љ–µ–є –¶–Э–°, –∞ —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ –≤—Л—П–≤–ї–µ–љ–Є—О –∞–љ—В–Є-–Т–У–І-6 –∞–љ—В–Є—В–µ–ї —Б—Л–≤–Њ—А–Њ—В–Ї–Є –Ї—А–Њ–≤–Є –Є –ї–Є–Ї–≤–Њ—А–∞ —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—О —Н—В–Њ–≥–Њ –≤–Є—А—Г—Б–∞ —Б —А–∞—Б—Б–µ—П–љ–љ—Л–Љ —Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ in situ –і–µ—В–µ–Ї—Ж–Є–Є –≤–Є—А—Г—Б–љ–Њ–є –Ф–Э–Ъ. –Я—А–Є —Н—В–Њ–Љ —З–∞—Б—В–Њ—В–∞ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–≤ —В–Њ–Љ —З–Є—Б–ї–µ —В–∞–Ј–Њ–≤–Њ–≥–Њ) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞—Б—Б–µ—П–љ–љ—Л–Љ —Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ –і–Њ—Б—В–Є–≥–∞–µ—В 50вАУ80%.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞—В—М –Є–љ—Д–µ–Ї—Ж–Є—О –Т–У–І-6 –љ–∞ –Њ—Б–љ–Њ–≤–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ј–∞—З–∞—Б—В—Г—О —В—А—Г–і–љ–Њ, —З—В–Њ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –љ–∞–Ј–љ–∞—З–µ–љ–Є—О —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П. –Ы–∞–±–Њ—А–∞—В–Њ—А–љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г –Є–љ—Д–µ–Ї—Ж–Є–Є –Т–У–І-6 –њ—А–Њ–≤–Њ–і—П—В —Б –њ–Њ–Љ–Њ—Й—М—О —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ-–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є. –Э–∞–Є–±–Њ–ї–µ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –≤–Є—А—Г—Б–љ–Њ–є –Ф–Э–Ъ –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є –Є –≤ –і—А—Г–≥–Є—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –ґ–Є–і–Ї–Њ—Б—В—П—Е —Б –њ–Њ–Љ–Њ—Й—М—О –њ–Њ–ї–Є–Љ–µ—А–∞–Ј–љ–Њ–є —Ж–µ–њ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є (–Я–¶–†) –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є. –Ґ–∞–Ї –Ї–∞–Ї –њ—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Ј–∞—А–∞–ґ–µ–љ–Є–Є –Є –і–∞–ґ–µ –њ—А–Є —А–µ–∞–Ї—В–Є–≤–∞—Ж–Є–Є –Т–У–І-6 –Є–љ—Д–µ–Ї—Ж–Є—П –Љ–Њ–ґ–µ—В –њ—А–Њ—В–µ–Ї–∞—В—М –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ, —Г—Б–ї–Њ–≤–љ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ—Л –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ф–Э–Ъ –Т–У–І-6, –Ї–Њ—В–Њ—А—Л–µ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В –∞–Ї—В–Є–≤–љ—Г—О, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –≤—Л—А–∞–ґ–µ–љ–љ—Г—О –Є–љ—Д–µ–Ї—Ж–Є—О вАФ 1000 –Ї–Њ–њ–Є–є/–Љ–ї –Є –≤—Л—И–µ.
–Я—А–Њ—В–Є–≤ –≥–µ—А–њ–µ—Б–≤–Є—А—Г—Б–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є, –≤—Л–Ј—Л–≤–∞–µ–Љ—Л—Е –∞–ї—М—Д–∞-, –±–µ—В–∞- –Є –≥–∞–Љ–Љ–∞-–Т–У–І, –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —В–∞–Ї–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Ї–∞–Ї –≤–∞–ї–∞—Ж–Є–Ї–ї–Њ–≤–Є—А, –≥–∞–љ—Ж–Є–Ї–ї–Њ–≤–Є—А, —Д–Њ—Б–Ї–∞—А–љ–µ—В (–љ–µ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ –≤ –†–§) –Є —Ж–Є–і–Њ—Д–Њ–≤–Є—А (–љ–µ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ –≤ –†–§). –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –і–ї—П –ї–µ—З–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є, –≤—Л–Ј–≤–∞–љ–љ—Л—Е –Т–У–І-6, –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Њ—Д–Є—Ж–Є–∞–ї—М–љ–Њ –љ–µ —Г—В–≤–µ—А–ґ–і–µ–љ—Л.
–Т —Б–≤—П–Ј–Є —Б —В–µ–Љ —З—В–Њ –Љ–љ–Њ–≥–Є–µ –≤–Њ–њ—А–Њ—Б—Л –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–є –Т–У–І-6 –њ–Њ–Ї–∞ –љ–µ —А–µ—И–µ–љ—Л, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Є–љ—В–µ—А–µ—Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ —Б —Г—Б–њ–µ—И–љ–Њ–є –њ–Њ–њ—Л—В–Ї–Њ–є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ —А–µ—И–µ–љ–Є—П –і–∞–љ–љ—Л—Е –≤–Њ–њ—А–Њ—Б–Њ–≤.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ
–Я–∞—Ж–Є–µ–љ—В –Ю., 49 –ї–µ—В, –Њ–±—А–∞—В–Є–ї—Б—П —Б –ґ–∞–ї–Њ–±–∞–Љ–Є –љ–∞ –ґ–ґ–µ–љ–Є–µ –≤ —Г—А–µ—В—А–µ, –±–Њ–ї—М –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ –≤ –њ—А–Њ–Љ–µ–ґ–љ–Њ—Б—В–Є, –Љ–Њ—И–Њ–љ–Ї–µ, –љ–µ–њ—А–Є—П—В–љ—Л–µ –Њ—Й—Г—Й–µ–љ–Є—П –њ—А–Є –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–Є, –≤–Њ –≤—А–µ–Љ—П –Є –њ–Њ—Б–ї–µ —Н—П–Ї—Г–ї—П—Ж–Є–Є.
–Ш–Ј –∞–љ–∞–Љ–љ–µ–Ј–∞: –≤ —В–µ—З–µ–љ–Є–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –±–Њ–ї–µ–µ—В —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—Б—В–∞—В–Є—В–Њ–Љ. –Х–ґ–µ–≥–Њ–і–љ–Њ –њ—А–Њ—Е–Њ–і–Є–ї —В–µ—А–∞–њ–Є—О –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–Љ–Є –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, —Д–Є–Ј–Є–Њ–ї–µ—З–µ–љ–Є–µ вАФ —Б –≤—А–µ–Љ–µ–љ–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ. –Т —О–љ–Њ—Б—В–Є –Њ—В–Љ–µ—З–∞–ї —З–∞—Б—В—Л–µ —А–µ—Ж–Є–і–Є–≤—Л –≥–µ–љ–Є—В–∞–ї—М–љ–Њ–≥–Њ –≥–µ—А–њ–µ—Б–∞. –Ф—А—Г–≥–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –њ–µ—А–µ–і–∞–≤–∞–µ–Љ—Л–µ –њ–Њ–ї–Њ–≤—Л–Љ –њ—Г—В–µ–Љ, –Њ—В—А–Є—Ж–∞–µ—В.
–°–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П: –±–Њ–ї–µ–Ј–љ—М –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞, –њ—А–Є–љ–Є–Љ–∞–µ—В –ї–µ–≤–Њ–і–Њ–њ—Г 200 –Љ–≥/—Б—Г—В, –±–µ–љ—Б–µ—А–∞–Ј–Є–і 50 –Љ–≥/—Б—Г—В. –Я–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –≤—А–∞—З–∞-–љ–µ–≤—А–Њ–ї–Њ–≥–∞ –≤—Л–і–µ—А–ґ–Є–≤–∞–µ—В —А–µ–ґ–Є–Љ –њ–Њ–≤—Л—И–µ–љ–љ—Л—Е —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е –љ–∞–≥—А—Г–Ј–Њ–Ї (–µ–Ј–і–∞ –љ–∞ –≤–µ–ї–Њ—Б–Є–њ–µ–і–µ 25вАУ40 –Ї–Љ –≤ –і–µ–љ—М). –С–Њ–ї–µ–Ј–љ—М –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Є –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–Љ —В—А–µ–Љ–Њ—А–Њ–Љ –њ–∞–ї—М—Ж–µ–≤ —А—Г–Ї.
–Я–∞–ї—М—Ж–µ–≤–Њ–µ —А–µ–Ї—В–∞–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ: –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–∞—П –ґ–µ–ї–µ–Ј–∞ 4√Ч4 —Б–Љ, –±–Њ–ї–µ–Ј–љ–µ–љ–љ–∞—П, –Љ—П–≥–Ї–Њ-—Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–Њ–і–љ–Њ—А–Њ–і–љ–Њ–є –Ї–Њ–љ—Б–Є—Б—В–µ–љ—Ж–Є–Є, –∞—Б–Є–Љ–Љ–µ—В—А–Є—З–љ–∞ –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–љ–Њ–є –њ—А–∞–≤–Њ–є –і–Њ–ї–Є, –±–µ–Ј –Њ—З–∞–≥–Њ–≤—Л—Е —Г–њ–ї–Њ—В–љ–µ–љ–Є–є, —Б–ї–Є–Ј–Є—Б—В–∞—П –љ–∞–і –ґ–µ–ї–µ–Ј–Њ–є –њ–Њ–і–≤–Є–ґ–љ–∞.
–Ш–љ–і–µ–Ї—Б —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Б—В–∞—В–Є—В–∞ (chronic prostatitis symptom index) CPSI вАФ 15 (–±–Њ–ї—М вАФ 8, –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є—П вАФ 2, –≤–ї–Є—П–љ–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–∞ –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ—Г—О –ґ–Є–Ј–љ—М вАФ 5), –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є (quality of life) QoL вАФ 4, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В —Г–Љ–µ—А–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є.
–Ь–µ—В–Њ–і–Њ–Љ –Я–¶–† Chlamydia trachomatis, Mycoplasma genitalium, Trichomonas vaginalis, Neisseria gonorrhoeae, Ureaplasma spp., Mycoplasma hominis, –≤–Є—А—Г—Б –њ—А–Њ—Б—В–Њ–≥–Њ –≥–µ—А–њ–µ—Б–∞ (–Т–Я–У) 1, 2 —В–Є–њ–∞ –љ–µ –≤—Л—П–≤–ї–µ–љ—Л.
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–µ–Ї—А–µ—В–∞ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (–°–Я–Ц) —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ 0вАУ4 –≤ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П, –ї–µ—Ж–Є—В–Є–љ–Њ–≤—Л–µ –Ј–µ—А–љ–∞ вАФ —Б–Ї—Г–і–љ–Њ. –Ю–±—Й–Є–є –∞–љ–∞–ї–Є–Ј –Љ–Њ—З–Є –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–Њ—А–Љ—Л, –≤ –Љ–∞–Ј–Ї–µ –Є–Ј —Г—А–µ—В—А—Л –≤—Л—П–≤–ї–µ–љ—Л –ї–µ–є–Ї–Њ—Ж–Є—В—Л 0вАУ1вАУ0 –≤ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П.
–Я—А–Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –і–Њ –њ–Њ—Б—В–Љ–∞—Б—Б–∞–ґ–љ–Њ–є –њ—А–Њ–±—Л –Љ–Њ—З–Є: Staphylococcus epidermidis 104 –Ъ–Ю–Х/–Љ–ї –≤ –Њ–±–µ–Є—Е –њ—А–Њ–±–∞—Е, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –∞–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–Љ—Г –•–Я/–°–•–Ґ–С.
–Т –§–У–С–£ ¬Ђ–Э–Ш–¶–≠–Ь –Є–Љ. –Э.–§. –У–∞–Љ–∞–ї–µ–Є¬ї –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є –њ—А–Њ–≤–µ–і–µ–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–µ—В–Њ–і–Њ–Љ –Я–¶–† –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є (–Я–¶–†—А–≤) –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ф–Э–Ъ –њ—П—В–Є –Т–У–І: –Т–Я–У-1, –Т–Я–У-2, –≤–Є—А—Г—Б–∞ –≠–њ—И—В–µ–є–љ–∞ вАФ –С–∞—А—А, —Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б–∞, –Т–У–І-6. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –љ–∞–±–Њ—А—Л —А–µ–∞–Ї—В–Є–≤–Њ–≤ –і–ї—П –Я–¶–† ¬Ђ–Р–Љ–њ–ї–Є–°–µ–љ—Б HHV1/HHV2-c–Ї—А–Є–љ-FL¬ї –Є ¬Ђ–Р–Љ–њ–ї–Є–°–µ–љ—Б EBV/CMV/HHV6-c–Ї—А–Є–љ-FL¬ї, (–Ю–Ю–Ю ¬Ђ–Ш–љ—В–µ—А–Ы–∞–±–°–µ—А–≤–Є—Б¬ї, –†–Њ—Б—Б–Є—П). –Т –Ї–∞—З–µ—Б—В–≤–µ —Н–љ–і–Њ–≥–µ–љ–љ–Њ–≥–Њ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є ќ≤-–≥–ї–Њ–±–Є–љ–Њ–≤—Л–є –≥–µ–љ.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Љ–∞—В–µ—А–Є–∞–ї–Њ–Љ —Б–ї—Г–ґ–Є–ї–Є: —Ж–µ–ї—М–љ–∞—П –Ї—А–Њ–≤—М, —Б–Њ—Б–Ї–Њ–± –Є–Ј —Г—А–µ—В—А—Л (–°–£), –°–Я–Ц, —Н—П–Ї—Г–ї—П—В. –Я–Њ–ї—Г—З–µ–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л: –Ф–Э–Ъ –Т–Я–У-1, –Т–Я–У-2, –≤–Є—А—Г—Б–∞ –≠–њ—И—В–µ–є–љ–∞ вАФ –С–∞—А—А –Є —Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б–∞ –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞. –Ф–Э–Ъ –Т–У–І-6 –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –≤ –≤—Л—Б–Њ–Ї–Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е –≤–Њ –≤—Б–µ—Е –Є–Ј—Г—З–µ–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е: –≤ –°–£ вАФ —Б–≤—Л—И–µ 4 –Љ–ї–љ –Ї–Њ–њ–Є–є/–Љ–ї, –≤ –°–Я–Ц вАФ 925 —В—Л—Б. –Ї–Њ–њ–Є–є/–Љ–ї, –≤ —Н—П–Ї—Г–ї—П—В–µ вАФ 177 —В—Л—Б. –Ї–Њ–њ–Є–є/–Љ–ї. –Т—Л—Б–Њ–Ї–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Т–У–І-6 –≤ –Ї—А–Њ–≤–Є (600 —В—Л—Б. –Ї–Њ–њ–Є–є/–Љ–ї) –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ—Г—О –Є–љ—В–µ–≥—А–∞—Ж–Є—О –≤–Є—А—Г—Б–∞.
–Я—А–Є —Г—А–Њ—Д–ї–Њ—Г–Љ–µ—В—А–Є–Є: –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П —Б–Ї–Њ—А–Њ—Б—В—М –њ–Њ—В–Њ–Ї–∞ –Љ–Њ—З–Є (Qmax) вАФ 17,3 –Љ–ї/—Б, —Б—А–µ–і–љ—П—П —Б–Ї–Њ—А–Њ—Б—В—М (Qav) вАФ 8,6 –Љ–ї/—Б, –њ—А–Є –Њ–±—К–µ–Љ–µ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є—П вАФ 157 –Љ–ї. –Я—А–Є –Ґ–†–£–Ч–Ш: –Њ–±—К–µ–Љ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л вАФ 46 —Б–Љ3 –±–µ–Ј –Њ—З–∞–≥–Њ–≤ —Г–Ј–ї–Њ–≤–Њ–є –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є–Є, –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А—Г—О—В—Б—П –Ї–∞–ї—М—Ж–Є–љ–∞—В—Л –≤–і–Њ–ї—М —Г—А–µ—В—А—Л.
–Я—А–Є –њ–Њ–ї—Г—З–µ–љ–Є–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –≤–Є—А—Г—Б–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В –њ–Њ–і—В–≤–µ—А–і–Є–ї, —З—В–Њ —А–∞–љ–µ–µ —Г –љ–µ–≥–Њ —Г–ґ–µ –≤—Л—П–≤–ї—П–ї–Є –Т–У–І-6 –Є –Њ–љ –њ—А–Њ—Е–Њ–і–Є–ї –ї–µ—З–µ–љ–Є–µ –≤ –Њ–і–љ–Њ–є –Є–Ј –Ї–ї–Є–љ–Є–Ї –≥. –Ь–Њ—Б–Ї–≤—Л –Ј–∞ 2 –≥–Њ–і–∞ –і–Њ –Њ–±—А–∞—Й–µ–љ–Є—П –њ–Њ –і–∞–љ–љ–Њ–Љ—Г –њ–Њ–≤–Њ–і—Г.
–Ф–Є–∞–≥–љ–Њ–Ј: —Б–Є–љ–і—А–Њ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є III–Т, —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –≥–µ—А–њ–µ—Б–≤–Є—А—Г—Б–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П 6 —В–Є–њ–∞.
–Я—А–Њ–≤–µ–і–µ–љ–Њ –ї–µ—З–µ–љ–Є–µ: –≤–∞–ї–∞—Ж–Є–Ї–ї–Њ–≤–Є—А 500 –Љ–≥ –њ–Њ 1 —В–∞–±–ї–µ—В–Ї–µ 2 —А/—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 3 –Љ–µ—Б., –Т–Ш–§–Х–†–Ю–Э¬Ѓ (–Є–љ—В–µ—А—Д–µ—А–Њ–љ ќ±-2b —Б –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–∞–Љ–Є вАФ –≤–Є—В–∞–Љ–Є–љ–∞–Љ–Є –Х –Є –°) –≤ —Д–Њ—А–Љ–µ —А–µ–Ї—В–∞–ї—М–љ—Л—Е —Б—Г–њ–њ–Њ–Ј–Є—В–Њ—А–Є–µ–≤, –њ–Њ 1 —Б—Г–њ–њ–Њ–Ј–Є—В–Њ—А–Є—О 3 –Љ–ї–љ –Ь–Х 2 —А/—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 10 –і–љ–µ–є, –Ј–∞—В–µ–Љ 3 —А/–љ–µ–і. –µ—Й–µ –≤ —В–µ—З–µ–љ–Є–µ 3 –љ–µ–і.
–Т —Е–Њ–і–µ –ї–µ—З–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–∞ –і–≤—Г–Ї—А–∞—В–љ–Њ –њ—А–Њ–≤–Њ–і–Є–ї–Є –њ–Њ–≤—В–Њ—А–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –°–Я–Ц вАФ —З–µ—А–µ–Ј 2 –љ–µ–і. –Є 4 –љ–µ–і. –Њ—В –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П. –°–Њ–і–µ—А–ґ–∞–љ–Є–µ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 40вАУ60 –≤ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П, –≤–≤–Є–і—Г —З–µ–≥–Њ –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј –±—Л–ї –Є–Ј–Љ–µ–љ–µ–љ –љ–∞ –•–Я/–°–•–Ґ–С III–Р.
–Ъ –Ї–Њ–љ—Ж—Г —В–µ—А–∞–њ–Є–Є —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є–µ —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ —Г–ї—Г—З—И–Є–ї–Њ—Б—М. –Э–∞–Є–±–Њ–ї–µ–µ –Ј–∞–Љ–µ—В–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ—А–Њ—П–≤–ї—П–ї–Њ—Б—М –≤ –≤–Є–і–µ —Б–љ–Є–ґ–µ–љ–Є—П –ґ–ґ–µ–љ–Є—П —Г—А–µ—В—А—Л, —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–µ–є –≤–Њ –≤—А–µ–Љ—П –Є –њ–Њ—Б–ї–µ —Б–µ–Љ—П–Є–Ј–≤–µ—А–ґ–µ–љ–Є—П. –Ю—Ж–µ–љ–Ї–∞ –њ–Њ —И–Ї–∞–ї–µ CPSI –љ–∞ 90-–є –і–µ–љ—М —Б–Њ—Б—В–∞–≤–Є–ї–∞ 8 (4+1+3) –±–∞–ї–ї–Њ–≤, –њ–Њ —И–Ї–∞–ї–µ QoL вАФ 2 –±–∞–ї–ї–∞, —В. –µ. –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –≤—Б–µ—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є.
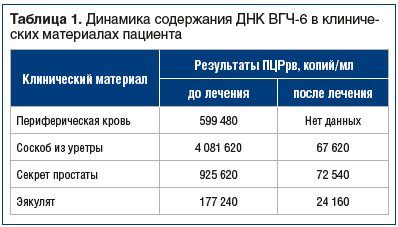
–Ь–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—П –°–Я–Ц: –ї–µ–є–Ї–Њ—Ж–Є—В—Л 10вАУ15 –≤ –њ–Њ–ї–µ –Ј—А–µ–љ–Є—П, —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –ї–µ—Ж–Є—В–Є–љ–Њ–≤—Л—Е –Ј–µ—А–µ–љ вАФ —Г–Љ–µ—А–µ–љ–љ–Њ. –Т–Є—А—Г—Б–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Т–У–І-6 (—В–∞–±–ї. 1).
–Я–∞–ї—М—Ж–µ–≤–Њ–µ —А–µ–Ї—В–∞–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ: –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–∞—П –ґ–µ–ї–µ–Ј–∞ 4√Ч4 —Б–Љ, –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –±–µ–Ј–±–Њ–ї–µ–Ј–љ–µ–љ–љ–∞—П –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є, –Љ—П–≥–Ї–Њ-—Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ–љ—Б–Є—Б—В–µ–љ—Ж–Є–Є, –∞—Б–Є–Љ–Љ–µ—В—А–Є—З–љ–∞—П –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П –њ—А–∞–≤–Њ–є –і–Њ–ї–Є, –±–µ–Ј –Њ—З–∞–≥–Њ–≤—Л—Е —Г–њ–ї–Њ—В–љ–µ–љ–Є–є, —Б–ї–Є–Ј–Є—Б—В–∞—П –љ–∞–і –ґ–µ–ї–µ–Ј–Њ–є –њ–Њ–і–≤–Є–ґ–љ–∞.
–°—Г–±—К–µ–Ї—В–Є–≤–љ–Њ —В–µ—З–µ–љ–Є–µ –Є–Љ–µ—О—Й–µ–≥–Њ—Б—П –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Њ—Б—М –Ј–∞ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–µ–љ–Є—П.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г –њ–∞—Ж–Є–µ–љ—В–∞ –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –≤–µ—А–Њ—П—В–љ—Л–Љ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –∞–≥–µ–љ—В–Њ–Љ –•–Я/–°–•–Ґ–С III–Р —П–≤–Є–ї—Б—П –Т–У–І-6. –Э–∞ —Д–Њ–љ–µ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ—В–Є–≤–Њ–≥–µ—А–њ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Є –Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–Њ–ї–Є, —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –і–Є–Ј—Г—А–Є–Є, —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є (–Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤–Є—А—Г—Б–∞, –Њ—Ж–µ–љ–Ї–∞ –њ–Њ —И–Ї–∞–ї–µ CPSI). –Т—Л—Б–Њ–Ї–Є–µ –Ї–Њ–љ–µ—З–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Т–У–І-6 –њ—А–Є —Е–Њ—А–Њ—И–µ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Њ—В–≤–µ—В–µ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ–Њ–є –Є–љ—В–µ–≥—А–∞—Ж–Є–µ–є –≤–Є—А—Г—Б–∞, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –Ї–∞–ґ–і–∞—П –Ї–ї–µ—В–Ї–∞ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —Б–Њ–і–µ—А–ґ–Є—В –µ–≥–Њ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є –Љ–∞—В–µ—А–Є–∞–ї.
–Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Њ—Б–љ–Њ–≤–љ–Њ–є –ґ–∞–ї–Њ–±–Њ–є –њ–∞—Ж–Є–µ–љ—В–∞ –±—Л–ї–Њ –ґ–ґ–µ–љ–Є–µ –≤ —Г—А–µ—В—А–µ, –њ—А–Є —Н—В–Њ–Љ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤–Є—А—Г—Б–∞ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –Є–Љ–µ–љ–љ–Њ –≤ —Н—В–Њ–Љ —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–Љ –ї–Њ–Ї—Г—Б–µ. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤–Ї–ї—О—З–∞–≤—И–µ–є –њ—А–µ–њ–∞—А–∞—В –Т–Ш–§–Х–†–Ю–Э¬Ѓ (–Є–љ—В–µ—А—Д–µ—А–Њ–љ ќ±-2b —Б –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–∞–Љ–Є вАФ –≤–Є—В–∞–Љ–Є–љ–∞–Љ–Є –Х –Є –°) –≤ —Д–Њ—А–Љ–µ —А–µ–Ї—В–∞–ї—М–љ—Л—Е —Б—Г–њ–њ–Њ–Ј–Є—В–Њ—А–Є–µ–≤, —Г–і–∞–ї–Њ—Б—М —Б–љ–Є–Ј–Є—В—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –≤–Є—А—Г—Б–∞ –≤ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–Љ —Г—А–µ—В—А—Л –љ–∞ –і–≤–∞ –њ–Њ—А—П–і–Ї–∞, —З—В–Њ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ –і–ї—П —Г—Б—В—А–∞–љ–µ–љ–Є—П —Г—А–µ—В—А–∞–ї—М–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤.
–Я–Њ—Б–ї–µ–і—Г—О—Й–Є–µ –≥–Њ–і—Л –љ–∞–±–ї—О–і–µ–љ–Є—П –Ј–∞ –і–∞–љ–љ—Л–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Б–Є–Љ–њ—В–Њ–Љ—Л –•–Я/–°–•–Ґ–С –Є–Љ–µ–ї–Є –ї–µ–≥–Ї—Г—О —Б—В–µ–њ–µ–љ—М —В—П–ґ–µ—Б—В–Є –Є –љ–µ –Ј–∞—Б—В–∞–≤–ї—П–ї–Є –њ–∞—Ж–Є–µ–љ—В–∞ –Њ–±—А–∞—Й–∞—В—М—Б—П –Ј–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й—М—О. –Т –±—Г–і—Г—Й–µ–Љ –±–Њ–ї–µ–µ –і–µ–є—Б—В–≤–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є –≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –≥–µ–љ–Њ–Љ–љ–Њ–µ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞–љ–Є–µ —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ—А–Њ—В–Ї–Є—Е –њ–∞–ї–Є–љ–і—А–Њ–Љ–љ—Л—Е –њ–Њ–≤—В–Њ—А–Њ–≤, —А–µ–≥—Г–ї—П—А–љ–Њ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –≥—А—Г–њ–њ–∞–Љ–Є, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ —Е–Њ—А–Њ—И–Є–є –∞–љ—В–Є–≤–Є—А—Г—Б–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–∞ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е [13].
–Ф–∞–љ–љ—Л–є —Б–ї—Г—З–∞–є, –љ–∞—Б–Ї–Њ–ї—М–Ї–Њ –љ–∞–Љ –Є–Ј–≤–µ—Б—В–љ–Њ, —П–≤–ї—П–µ—В—Б—П –њ–µ—А–≤—Л–Љ —Б–Њ–Њ–±—Й–µ–љ–Є–µ–Љ –Њ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ–Њ –Є–љ—В–µ–≥—А–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Т–У–І-6, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —Б –•–Я/–°–•–Ґ–С.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–®–Є—А–Њ–Ї–Њ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –Т–У–І-6 –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –µ–≥–Њ –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Я–¶–† –њ–Њ—Б–ї—Г–ґ–Є–ї–Є –љ–∞—З–∞–ї–Њ–Љ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–≥–Њ –Є–Ј—Г—З–µ–љ–Є—П —Н—В–Њ–≥–Њ –≤–Є—А—Г—Б–∞. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –Т–У–І-6 –Љ–Њ–ґ–µ—В –±—Л—В—М –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ —Б —Н–љ—Ж–µ—Д–∞–ї–Є—В–Њ–Љ, —Н–њ–Є–ї–µ–њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Є–њ–∞–і–Ї–∞–Љ–Є, –±–Њ–ї–µ–≤—Л–Љ–Є —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –µ–≥–Њ –љ–µ–є—А–Њ—В—А–Њ–њ–Є–Ј–Љ–Њ–Љ. –Ю—Б–Њ–±–µ–љ–љ–Њ –±–Њ–ї—М—И–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Т–У–І-6 –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≤ —Б–ї—Г—З–∞–µ –µ–≥–Њ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–љ–Њ–є –Є–љ—В–µ–≥—А–∞—Ж–Є–Є –≤ –Њ–Ї–Њ–ї–Њ—В–µ–ї–Њ–Љ–µ—А–љ—Г—О –Њ–±–ї–∞—Б—В—М. –Я—А–Є —Н—В–Њ–Љ –≤–Є—А—Г—Б –љ–∞—З–Є–љ–∞–µ—В –њ–µ—А–µ–і–∞–≤–∞—В—М—Б—П –њ–Њ –љ–∞—Б–ї–µ–і—Б—В–≤—Г –њ–Њ –Ј–∞–Ї–Њ–љ–∞–Љ –Ь–µ–љ–і–µ–ї—П.
–Т –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ —Б–ї—Г—З–∞–µ –Т–У–І-6 —П–≤–Є–ї—Б—П –≤–µ—А–Њ—П—В–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –∞–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Б—В–∞—В–Є—В–∞. –Я—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ–∞—П —В–µ—А–∞–њ–Є—П, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П –љ–∞ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ —А–µ–њ–ї–Є–Ї–∞—Ж–Є–Є –Т–У–І-6 –Є –∞–Ї—В–Є–≤–∞—Ж–Є—О –∞–љ—В–Є–≤–Є—А—Г—Б–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –њ–Њ–Ї–∞–Ј–∞–ї–∞ —Е–Њ—А–Њ—И–Є–є –≤–Є—А—Г—Б–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –≤ –≤–Є–і–µ —Б–љ–Є–ґ–µ–љ–Є—П –≤–Є—А—Г—Б–љ–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —А–µ–Љ–Є—Б—Б–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–∞ —Б —В–∞–Ј–Њ–≤—Л–Љ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ.
–С–ї–∞–≥–Њ–і–∞—А–љ–Њ—Б—В—М
–†–µ–і–∞–Ї—Ж–Є—П –±–ї–∞–≥–Њ–і–∞—А–Є—В –Ї–Њ–Љ–њ–∞–љ–Є—О –Ю–Ю–Ю ¬Ђ–§–µ—А–Њ–љ¬ї –Ј–∞ –Њ–Ї–∞–Ј–∞–љ–љ—Г—О –њ–Њ–Љ–Њ—Й—М –≤ —В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–є —А–µ–і–∞–Ї—В—Г—А–µ –љ–∞—Б—В–Њ—П—Й–µ–є –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є.












