В настоящее время кардинально изменился образ жизни большинства населения земли: хронический стресс, малоподвижный образ жизни и переедание характерны для населения развитых стран, в то же время недоедание и недостаток белковых компонентов рациона – для жителей развивающихся стран. Изменение климата, вырубка лесов, загрязнение окружающей среды, урбанизация и другие агрессивные факторы также отражаются на здоровье обитателей земли, в результате чего у наших современников мутации в геноме происходят чаще, чем у предков. Это ведет к нарушению гомеостаза, снижению резистентности организма. У многих людей развиваются хронические патологические состояния, включая вторичный иммунодефицит, что сопровождается высоким риском развития различных заболеваний, преимущественно инфекционных (вирусных). Такие индивиды часто и долго болеют, трудно выздоравливают и, таким образом, составляют контингент «проблемных» пациентов, в том числе и часто болеющих детей (ЧБД).
Профилактика и лечение заболеваний дыхательных путей, включая ОРВИ и грипп, у контингента «проблемных» пациентов с иммунодефицитом, особенно ЧБД, является актуальной проблемой современного здравоохранения. Это обусловлено затруднениями при проведении вакцинации у таких лиц, отсутствием адекватных лечебных противовирусных средств и изменчивостью вирусов. В большинстве случаев этиологическими факторами заболеваний дыхательных путей являются вирусы или их сочетания с условно–патогенной или патогенной бактериальной флорой. Так, известно около сотни различных вирусных возбудителей, включая представителей 5 семейств РНК–содержащих вирусов (ортомиксо–, парамиксо–, корона–, пикорна–, реовирусы) и 3 семейств ДНК–содержащих вирусов (адено–, парво– и герпесвирусы), которые могут вызывать острые заболевания дыхательных путей [Давидовская, 2006; Львов, 2008; Царев, 2009]. При этом спектр противовирусных средств для эффективного лечения этих заболеваний ограничен, особенно осложненных форм ОРВИ и гриппа, которые нередко сопровождаются тяжелыми последствиями для иммунокомпрометированных пациентов. Более того, на их фоне часто развиваются рецидивирующие и хронические поражения верхних и нижних отделов респираторного тракта с формированием вторичного иммунодефицита, поэтому отмечается повышенный интерес практических врачей к иммуномодулирующим средствам. Многочисленные публикации по данной проблеме свидетельствуют о широком применении различных иммуномодуляторов при ОРВИ и гриппе как у взрослых, так и у детей, что представлено в Кохрановском обзоре [Del–Rio–Navarro et al., 2006] и в других публикациях.
Другой аспект проблемы иммунотерапии связан с агрессивной маркетинговой технологией фармацевтических компаний. На лекарственном рынке стран СНГ циркулируют многочисленные препараты, рекомендуемые для повышения иммунитета, порой сомнительного происхождения, с отсутствием клинически доказанных результатов их эффективности. Это затрудняет практическим врачам выбор оптимального иммуностимулятора для лечения и профилактики вирусных инфекции у пациентов с нарушениями в иммунной системе.
Инозин Пранобекс (ИП) – синтетический аналог инозина, получен путем соединения инозина со вспомогательной молекулой, которая повышает доступность инозина для лимфоцитов и таким образом усиливает его иммуностимулирующие свойства. За более чем 38–летний период применения лекарственных аналогов ИП не зарегистрированы случаи серьезных побочных эффектов. Существуют многочисленные данные клинических испытаний, свидетельствующие об эффективности ИП как иммуностимулирующего и противовирусного агента у «проблемных» или «трудных» пациентов с иммунодефицитом. Это, по–видимому, связано с отсутствием у ИП выраженного плейотропного эффекта, характерного для цитокинов (в частности интерферонов), что обусловливает непредсказуемость фармакологического поведения цитокинов. Более того, применение экзогенных цитокинов лимитировано у контингента «проблемных» пациентов, особенно ЧБД, со сниженным иммунитетом, в связи с отсутствием соответствующих эффекторных клеток или наличием патогномоничных факторов заболевания, препятствующих активации лимфоцитов. Короткий период полураспада экзогенных цитокинов и необходимость применения их для достижения терапевтического эффекта в высоких дозах стимулирует исследователей к поиску наиболее приемлемого и адекватного иммунопотенциатора, принимающего участие в регуляции иммунных процессов в организме, но не обладающего побочными эффектами цитокинов. К таким иммуностимуляторам можно отнести ИП, предшественниками которого являются природные пурины.
Ранее мы проанализировали эффективность применения ИП при урогенитальных заболеваниях, связанных с вирусами простого герпеса и папилломы человека [Елисеева и соавт., 2009; Елисеева и Мынбаев, 2009; Мынбаев и соавт, 2009]. Настоящий обзор является логическим продолжением предыдущих работ с целью проведения систематизации и метаанализа эффективности вспомогательной иммунотерапии у контингента пациентов с нарушениями в иммунной системе и ЧБД при рецидивирующих ОРВИ.
Методы исследования
Методы поиска
Информационный поиск источников, опубликованных с 1999 по 2009 г., был проведен с использованием ключевых слов: «острые респираторные вирусные инфекции (ОРВИ)», «часто болеющие дети», «заболевания дыхательных путей», «грипп», «иммуномодуляторы», «пурины», «синтетический аналог инозина», «инозин», «Инозин Пранобекс», «Гроприносин», «Изоприносин», «Инозиплекс», «Иммуновир», «Метизопринол» в электронных англо– и русскоязычных базах данных, включая www.medline, www.pubmed.com, www.google.ru, http://elibrary.ru.
Критерии отбора источников
Методологические подходы для изучения эффективности вспомогательной иммунотерапии при ОРВИ остаются недостаточно ясными. Это связано с трудностью организации подобного рода исследований и отсутствием четких критериев отбора больных. Порою трудно определить показания к применению вспомогательной иммунотерапии. Возникают проблемы при рандомизации с двойным ослеплением, поскольку для адекватной оценки эффективности препарата требуется длительное наблюдение за индивидами, получавшими иммуностимулирующие препараты. Так, в Кохрановском обзоре только 6 (17,6%) из проанализированных 34 работ выполнялись с адекватной двойной слепой рандомизацией [Del–Rio–Navarro et al., 2006].
Другая проблема связана с популяцией, которая участвует в исследовании. Иммунностимуляторы в основном назначают в амбулаторных условиях, при этом участники могут не явиться на повторные приемы или не соблюдать предписанный режим. Это ведет к недостатку данных и гетерогенности отдаленных результатов. Критерии оценки эффективности иммунностимуляторов также неопределенны и неточны, часто приблизительны и косвенны.
Учитывая вышеуказанные факторы, при определении критериев отбора мы исходили из того, что при заболеваниях дыхательных путей (ОРВИ и грипп) у контингента пациентов с нарушениями в иммунной системе применялись аналоги ИП (Гроприносин и Изопринозин), при этом режим приема препарата не учитывался. Следовательно, в данный обзор были включены доступные источники, в которых оценивалась эффективность вспомогательной иммунотерапии с применением аналогов ИП в профилактике и лечении респираторных инфекционных заболеваний, включая ОРВИ и грипп у контингента пациентов с нарушениями в иммунной системе, в том числе и ЧБД.
Материалы систематического обзора и дизайн выбранных нами работ для метаанализа
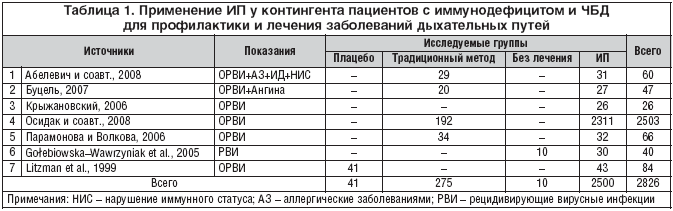
На начальном этапе были доступны 14 ссылок, в которых имелись сочетания ключевых слов, использованных нами в поиске литературы. На следующем этапе произведена сортировка обзоров и малоинформативных публикаций, выделены 7 работ для систематического анализа (табл. 1). В этих источниках описаны данные 2826 индивидов. Из них 2500 индивидам (дети и взрослые), преимущественно из контингента пациентов с нарушениями в иммунной системе и ЧБД, назначали ИП в лечебно–профилактическом режиме, а только в лечебном режиме ИП назначали больным с ОРВИ, ангиной и другими респираторными заболеваниями. 41 индивиду назначали плацебо и 275 больных получали традиционное лечение.
Чтобы определить пригодность результатов выбранных нами источников для метаанализа, изучали дизайн исследования и качество изложения результатов исследования в этих работах. При этом только 1 работа являлась проспективным плацебо–контролируемым сравнением с двойной рандомизацией [Litzman et al., 1999]. Открытое контролируемое сравнительное клиническое исследование проведено в 3 источниках [Абелевич и соавт., 2008; Парамонова и Волкова, 2006], включая данные широкомасштабного многоцентрового постмаркетингового исследования с участием 121 врача в 13 городах РФ по изучению лечебно–профилактической эффективности ИП [Осидак и соавт., 2008]. Одну работу мы считаем условно контролируемой, поскольку в контрольной группе результаты традиционного лечения ангины, протекающей без ОРВИ, сравнивались с основной группой, где ИП применяли дополнительно для лечения ангины, протекающей на фоне ОРВИ [Буцель, 2007]. В 2 работах контрольная группа отсутствовала [Golebiowska–Wawrzyniak et al., 2005; Крыжановский, 2006]. При этом клинические и иммунологические показатели детей с иммунодефицитом и рецидивирующими респираторными инфекциями сравнивались в динамике с показателями 10 здоровых детей [Golebiowska–Wawrzyniak et al., 2005], а в другой работе ИП был назначен в первой группе для профилактики часто и длительно болеющих пациентов, а во второй группе был включен в комплекс лечения ОРВИ [Крыжановский, 2006]. По стилю описания результатов две статьи идентичны – описание практического опыта [Буцель, 2007; Крыжановский, 2006], но в одной из них дополнительно представлен обзор литературы в виде лекционного материала [Крыжановский, 2006]. Исходя из качества изложения результатов исследования для метаанализа были использованы результаты 4 источников [Осидак и соавт, 2008; Парамонова и Волкова, 2006; Golebiowska–Wawrzyniak et al., 2005; Litzman et al., 1999], причем в 2 из них были обобщены данные лечебно–профилактического режима применения ИП у детей [Осидак и соавт, 2008; Парамонова и Волкова, 2006].
Особенности популяции в источниках,
включенных в метаанализ
Показаниями для применения ИП являлись нарушение иммунного статуса (НИС) у больных с заболеваниями дыхательных путей: повышенная заболеваемость ОРВИ, сочетание вирусных и бактериальных инфекций, тяжелые затяжные бактериальные инфекции [Абелевич и соавт, 2008]. Лечение ОРВИ на фоне ангины [Буцель, 2007] и только ОРВИ [Крыжановский, 2006]. В других работах ИП был использован в лечебно–профилактическом режиме ОРВИ и гриппа преимущественно ЧБД с неблагоприятным преморбидным фоном [Осидак и соавт, 2008; Парамонова и Волкова, 2006] и для профилактики рецидивирующих вирусных инфекций у детей [Golebiowska–Wawrzyniak et al., 2005; Litzman et al.,1999]. При этом группа здоровых детей, которые нуждались в легкой хирургической коррекции (без уточнения), составили контрольную группу [Golebiowska–Wawrzyniak et al., 2005]. Таким образом, основным контингентом в большинстве работ являлись часто болеющие дети с нарушениями иммунного статуса (табл. 2).
Критерии включения и исключения пациентов
в анализированных источниках
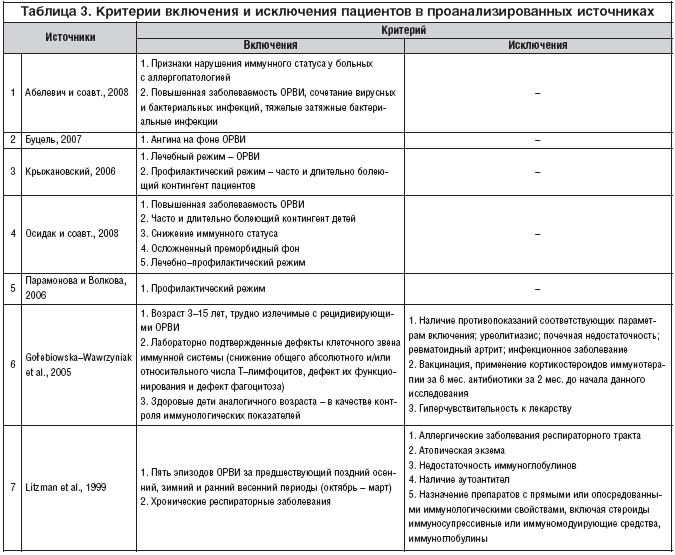
Критерии включения при назначении ИП в большинстве анализируемых работ были связаны с нарушениями иммунного статуса и частыми острыми или рецидивирующими ОРВИ у контингента пациентов (табл. 3). При этом лечение ОРВИ у этого контингента было трудным из–за неблагополучного преморбидного фона и сочетания различных сопутствующих инфекций. ИП назначали как для профилактики ОРВИ и сезонного гриппа, так и для лечения ОРВИ.
Режим и цель назначения Инозина Пранобекса
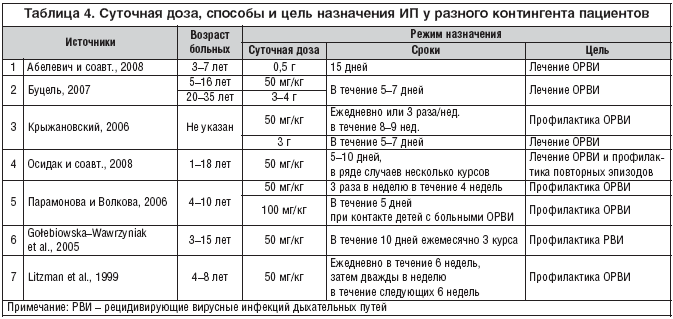
В большинстве случаев ИП назначали по стандартной схеме: в суточной дозе по 50 мг/кг массы тела или по 3 г. В то же время, по данным некоторых источников, назначали по 3–4 г/сут. (табл. 4).
Режим назначения ИП разнообразен: с длительностью назначения от 5 дней до 3 мес., однократно или с многократными повторениями, 5– или 10–дневными курсами.
В большинстве источников оценка эффективности ИП производилась комплексными клинико–лабораторными методами, включающими иммунологические тесты для изучения морфологической и функциональной состоятельности клеточного звена иммуннитета. При этом наблюдение за состоянием участников проводилось до и после назначения ИП в течение различного периода времени (от 2 нед. до 1 года). В двух работах информация о сроках наблюдения отсутствовала, а по результатам исследования можно считать, что авторы наблюдали больных во время лечения ОРВИ [Буцель, 2007; Крыжановский, 2006].
Методы статистической обработки
Статистическая обработка выполнена с помощью программ Graph Pad Prism 4 и GraphPad InStat. Значение р получено с помощью непараметрических тестов (paired/unpaired T tests).
Принцип структурирования
систематического обзора
Популяция, представленная в данном обзоре, включает детей и взрослых, здоровых и больных, поэтому на первом этапе проводили метаанализ, включив результаты работ, выполненных для изучения лечебно–профилактической эффективности применения ИП у детей с отягощенным преморбидным фоном, а также у контингента пациентов, преимущественно с нарушениями в иммунной системе и ЧБД [Осидак и соавт, 2008; Парамонова и Волкова, 2006; Golebiowska–Wawrzyniak et al., 2005; Litzman et al., 1999].
На втором этапе проводили обобщенный анализ побочных эффектов применения ИП в лечебно–профилактическом режиме при ОРВИ и воспалительных респираторных заболеваниях из всех источников, проанализированных в этом обзоре.
В разделе «дискуссия» мы обобщили данные литературы и результаты проанализированных нами источников в метаанализе, в том числе данные работ, исключенных из него, в которых контингент состоял из больных с хронической болезнью легких [Крыжановский, 2006] и ангиной [Буцель, 2007] на фоне ОРВИ.
Результаты исследования
Метаанализ результатов
лечебно–профилактического применения ИП при респираторных инфекциях
Метаанализ эффективности применения ИП в лечебно–профилактическом режиме по частоте и характеру эпизодов ОРВИ при сравнении с показателями контрольной группы и/или с исходными данными до приема ИП был проведен по результатам 4 работ (табл. 5). Обобщенные результаты этих источников свидетельствуют о том, что частота и продолжительность эпизодов ОРВИ значительно сокращается у детей после профилактического приема ИП по сравнению с аналогичными показателями в контрольной группе, а также исходными показателями, полученными до приема ИП [Осидак и соавт, 2008; Парамонова и Волкова, 2006; Golebiowska–Wawrzyniak et al., 2005], и только результаты одной работы не подтвердили наличие лечебно–профилактической эффективности у ИП при рецидивирующих респираторных инфекциях [Litzman et al., 1999].
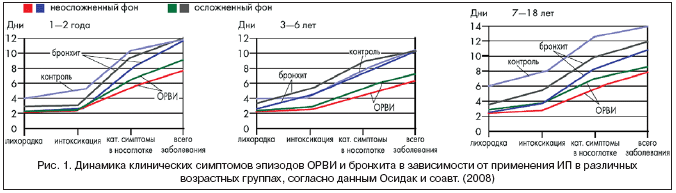
Согласно данным Осидак и соавт. (2008), применение ИП у детей, включая лиц с неблагополучным преморбидным фоном, способствовало сокращению продолжительности практически всех симптомов заболевания, в том числе температурной реакции, интоксикации и катаральных явлений в носоглотке (рис. 1). При этом продолжительность эпизодов ОРВИ не превышала 6–8 дней у 64–70% детей, принимавших ИП, что существенно превосходит аналогичный показатель у детей контрольной группы (4–25%).
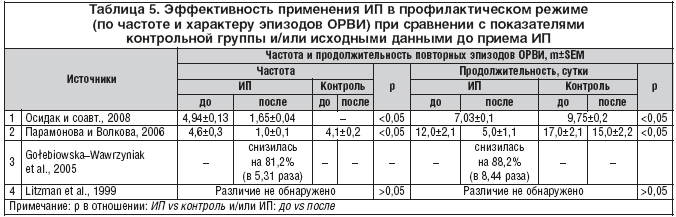
В аналогичной по принципу работе с меньшим количеством детей Парамонова и Волкова (2006) также показали профилактическую эффективность ИП в отношении снижения частоты и продолжительности эпизодов ОРВИ (рис. 2). После применения ИП число детей, перенесших первичные и повторные эпизоды ОРВИ, уменьшилось в 3,5 раза по сравнению с аналогичным показателем в контрольной группе.
Парамонова и Волкова (2006) считают, что подтверждением лечебно–профилактической эффективности ИП является сравнительно более легкое течение ОРВИ, снижение в 3–4 раза частоты развития таких осложнений, как острый бронхит, пневмония и отит. Проведя сравнительные клинические и углубленные иммунологические исследования у детей с рецидивирующими респираторными инфекциями, получивших лечение ИП, Golebiowska–Wawrzyniak et al. (2005) подтверждают такие выводы российских ученых, как сокращение частоты эпизодов рецидивов респираторных инфекции на 81,2%, или в 5,31 раза, по сравнению с показателями до применения ИП. При этом форма тяжести ОРВИ стала более легкой на 60,3%, или в 2,52 раза, продолжительность эпизодов ОРВИ сократилась на 88,2%, или в 8,44 раза, а так называемый общий индекс клинических симптомов снизился на 72,5%, или в 3,64 раза, по сравнению с аналогичными показателями до применения ИП. В результате применения ИП Golebiowska–Wawrzyniak et al. (2005) удалось сократить частоту применения антибиотиков у детей на 93,5%, или в 15,3 раза, а других неантибактериальных препаратов – на 78,3%, или в 4,51 раза. Вместе с тем, в плацебо–контролируемой работе, выполненной с целью профилактики острой рецидивирующей респираторной инфекций у детей 4–8 лет, Litzman et al. (1999), не обнаружили существенного различия между ИП и плацебо. Эффективность ИП оценивалась по частоте и продолжительности эпизодов ОРВИ, по тяжести развивающихся симптомов (по продолжительности кашля и повышенной температуры тела), а также по развитию осложнений. Тем не менее Litzman et al. (1999) отмечают повышение числа Т–лимфоцитов (CD3+, CD4+ и CD8+ клеток) в крови на фоне применения ИП.
Обобщенный анализ
побочных эффектов применения ИП
Анализ свидетельствует, что в 2 работах побочные эффекты не описаны [Абелевич и соавт, 2008; Парамонова и Волкова, 2006], в 4 источниках вообще отсутствует информация о нежелательных реакциях [Буцель, 2007; Крыжановский, 2006; Golebiowska–Wawrzyniak et al., 2005]. В других 4 исследованиях авторы детально указали спектр и характер «нежелательных явлений», связанных с приемом ИП [Осидак и соавт., 2008; Litzman et al., 1999]. При этом, согласно данным Осидак и соавт. (2008), развитие таких эффектов, как тошнота, боль в эпигастрии, сухость кожи, аллергическая реакция, сонливость и повышение концентрации трансаминаз печени (АЛТ), в ответ на применение ИП было нечастым и не сопровождалось отменой препарата (табл. 6).
Кроме того, Litzman et al. (1999) отмечает появление позитивного противонуклеарного титра, равного 1:40 при отсутствии клинических симптомов и других лабораторных изменений, включая повышение концентрации мочевой кислоты (МК) и печеночных проб.
Дискуссия
Актуальность проблемы связана с тем, что в настоящее время у многих индивидов, особенно у детей, обнаруживают вторичный иммунодефицит, обусловленный изменением образа жизни, воздействием агрессивных факторов внешней среды, малоподвижного образа жизни, чрезмерного стресса и других причин. В результате люди становятся уязвимыми для возбудителей инфекции, не только патогенных, но и оппортунистических. Они часто и долго болеют, трудно выздоравливают и составляют контингент иммунокомпрометированных пациентов и ЧБД. Профилактика и лечение ОРВИ и гриппа у них представляет определенные трудности из–за отсутствия адекватных лечебных противовирусных средств, особенно в случаях развития осложнений. Более того, на фоне ОРВИ и гриппа часто формируется вторичный иммунодефицит, в связи с чем отмечается повышенный интерес практических врачей к иммуномодулирующим средствам.
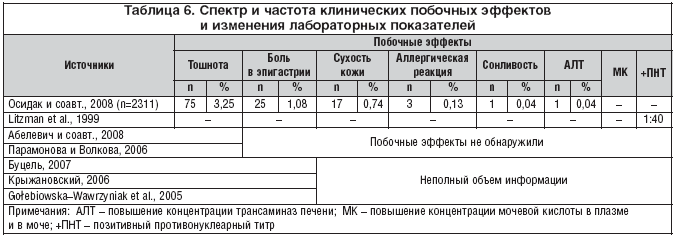
Существуют множественные трактовки механизмов противовирусной активности ИП. Так, например, оценив противовирусный эффект ИП в отношении 4 штаммов вируса гриппа А и В на культуре МДСК клеток, Сергиенко и соавт. (2009) показали, что ИП обладает противовирусным действием в отношении штаммов вируса гриппа А и В без выраженной типовой специфичности как в лечебном, так и профилактическом режимах применения препарата (табл. 7).
Согласно данным Сергиенко и соавт. (2009), ИП обладает противовирусным действием в отношении вирусов гриппа А и В. Ингибирующее влияние препарата на репродукцию вирусов гриппа выявлено как при предварительной обработке культуры клеток (профилактический режим), так и при внесении препарата непосредственно после инфицирования клеток (терапевтический режим). При этом был выявлен дозозависимый эффект: увеличение концентрации препарата сопровождалось потенцированием противовирусного действия независимо от типа вируса. ИП ингибировал репродукцию как вирусов гриппа типа А (H1N1 и H3N2), так и гриппа типа В. Следует отметить, что ингибирующее влияние ИП на репродукцию вирусов гриппа типа А было выражено сильнее, чем на репродукцию вируса гриппа типа В (табл. 8).
Абелевич и соавт. (2008) продемонстрировали изменение показателей клеточного и гуморального иммунитета до применения ИП, затем спустя 2 нед. и 2 мес. после лечения. При этом на раннем этапе отмечена активация В–клеточного звена иммунитета с увеличением IgA и IgM, а также возрастание концентрации CD8+ лимфоцитов и HLA–DR+ клеток, на позднем этапе – переключение синтеза иммуноглобулинов с IgM на IgG, нормализацию и/или повышение концентрации HLA–DR+ клеток и снижение количества CD3+ клеток. Такие же изменения в иммунологическом статусе у детей с рецидивирующими респираторными инфекциями, получивших лечение ИП, согласно данным Golebiowska–Wawrzyniak et al. (2005), привели к повышению эффективности лечения детей с неблагоприятным преморбидным фоном и рецидивирующими респираторными инфекциями.
В порядке обсуждения считаем уместным ссылаться на работы, исключенные из метаанализа, где ИП использовался для профилактики и лечения ОРВИ у больных с хронической болезнью легких (ХБЛ) [Крыжановский, 2006] и ангиной [Буцель, 2007]. В наблюдениях Крыжановского (2006) ИП был использован у 12 индивидов (часто и длительно болеющих) в качестве профилактики ОРВИ по 50 мг/кг массы тела в сутки в течение 8–9 нед. и у 14 больных с ХБЛ для лечения ОРВИ по 3 г/сут. в течение 5–7 дней. Из выводов автора следуют, что применение ИП в профилактическом режиме способствует уменьшению частоты развития и облегчению течения ОРВИ, продлевает период ремиссии. В лечебном режиме прием ИП способствует сокращению длительности таких клинических проявлений, как боль в горле, насморк, кашель, более быстрой нормализации повышенной температуры тела, ликвидации симптомов интоксикации и ускоряет обратное развитие воспалительных процессов, предотвращает формирование осложнений.
В клиническом опыте использования ИП Буцель (2007) назначал ИП в суточной дозе детям по 50 мг/кг массы тела в сутки и взрослым по 3–4 г/сут. в течение 5–7 дней, что способствовало значительному уменьшению интенсивности головных болей, «сглаженному» проявлению ринофарингита и сокращению лихорадочного периода.
В дальнейшем лечебно–профилактическая эффективность ИП была продемонстрирована при изучении частоты эпизодов гриппа и ОРВИ в широкомасштабном многоцентровом постмаркетинговом исследовании с участием 121 врача в 13 городах РФ [Осидак и соавт., 2008], а также в открытой контролируемой работе с меньшим количеством детей [Парамонова и Волкова, 2006].
Однако Litzman et al., (1999), проведя плацебо–контролируемое исследование у детей 4–8 лет с целью профилактики острой рецидивирующей респираторной инфекций, не обнаружили существенного различия между ИП и плацебо–контролем. Тем не менее авторы отмечают повышение числа Т–лимфоцитов в виде CD3+, CD4+ и CD8+ клеток в крови после применения ИП. Следует отметить, что клинические результаты Litzman et al. (1999) были получены на основании записей в дневниках родителей, которые регистрировали клинические признаки ОРВИ. При этом некоторые критерии включения являются спорными. Так, например, новым эпизодом ОРВИ считали появление не менее двух признаков, таких как кашель, насморк, боль в горле, боль в ухе, повышение t тела ≥38,0°С продолжительностью не менее 4 дней при регистрации 4 дневного бессимптомного периода после перенесенного ранее эпизода ОРВИ.
Интерпретируя эти данные, считаем, что клинические результаты профилактической эффективности ИП, продемонстрированные клиницистами [Крыжановский, 2006; Осидак и соавт., 2008; Парамонова и Волкова, 2006; Golebiowska–Wawrzyniak et al., 2005], по–видимому, являются следствием ингибирующего влияния ИП на репродукцию вирусов, вызывающих ОРВИ [Сергиенко и соавт., 2009].
В проанализированных нами источниках существуют также негативные факторы, снижающие достоверность представленных в них результатов, заключающиеся в разнообразии дизайна и бедности методологических подходов. Из этого следует, что для подтверждения эффективности вспомогательной иммунотерапии с использованием ИП у контингента иммуннокомпрометированных пациентов с рецидивирующими ОРВИ необходимо проведение рандомизированных плацебо–контролируемых исследований.
Заключение
Представлен обобщенный анализ данных из 7 источников литературы, посвященных оценке эффективности вспомогательной иммунотерапии с ИП, который был назначен 2500 индивидам (детям/взрослым) с нарушениями в иммунной системе и рецидивирующими ОРВИ.
Результаты данного метаанализа свидетельствуют о значительном снижении частоты новых эпизодов ОРВИ у индивидов после лечебно–профилактического курса с ИП, особенно у контингента с иммунодефицитом и ЧБД, с отягощенным преморбидным фоном. Прослеживается тенденция сокращения длительности и облегчение тяжести ОРВИ на фоне лечения с ИП.
Обнадеживающие результаты применения ИП в проанализированных нами источниках литературы позволяют сделать вывод о целесообразности вспомогательной иммунотерапии при лечении ОРВИ у лиц с теми или иными нарушениями иммунного статуса.

![Рис. 2. Частота и продолжительность эпизодов ОРВИ до и после приема ИП по сравнению с контрольной группой [Модифирован из данных Парамоновой и Волковой, 2006]](/data/articles/Image/t18/n5/313-7.gif)
![Таблица 7. Влияние ИП на репродукцию вирусов гриппа А и В в культуре клеток МДСК [Сергиенко и соавт., 2009]](/data/articles/Image/t18/n5/313-9.gif)
![Таблица 8. Характеристика противовирусного действия ИП в отношении вирусов гриппа А и В [Сергиенко и соавт., 2009]](/data/articles/Image/t18/n5/313-10.gif)
Литература
1. Абелевич М.М., Иванова Е.Л., Лукушкина Е.Ф. Этиопатогенетическая терапия инозином пранобексом у детей с осложненным течением аллергических заболеваний. НМЖ, 2008; 1: 60–64.
2. Буцель А.Ч. Клиническое обоснование применения лекарственного средства «Гроприносин» в лечении больных ангиной на фоне острой респиртаорной вирусной инфекции. Медицина, 2007; 2: 90–91.
3. Давидовская Е.И. Рациональная фармакотерапия респираторных вирусных инфекций. Мед. Нов. 2006; 12: 1–5.
4. Елисеева М.Ю., Мынбаев О.А. Вспомогательная иммунотерапия ВПЧ–ассоциированных поражений слизистых оболочек и кожи урогенитальной и перианальной локализации (Систематический обзор литературы и МЕТА–анализ применения Инозина Пранобекса). Гинекология 2009; 11(5):22–33.
5. Елисеева М.Ю., Мынбаев О.А., Мaсихи К.Н., Манухин И.Б., Тыщенко Е.А., Кундохова М.С. Современные взгляды на герпетическую инфекцию. Проблемы репродукции. 2009; 1:25–35.
6. Крыжановский В.А. Применение Гроприносина для профилактики и лечения ОРВИ у больных хронической обструктивной болезнью легких. Медицина, 2006; 3: 74–78.
7. Микробиология, вирусология и иммунология. Учебник для мед. вузов / Под ред. В.Н.Царева – М.:Практическая медицина, 2009; 581 с.
8. Медицинская вирусология. Руководство / Под. ред. Д.К. Львова. – М.:ООО «Медицинское информационное агенство», 2008. – 656 с.
9. Мынбаев О.А., Елисеева М.Ю., Доорбар Дж., Манухин И.Б. Эпидемиология, молекулярная биология, патофизиология и принципы иммунотерапии папилломавирусной инфекции. Вопросы гинекологии, акушерства и перинатологии, 2009; 8(3): 69–79.
10. Мынбаев О.А., Елисеева М.Ю., Масихи К.Н., Манухин И.Б., Царев В.Н. Гроприносин – высокоэффективный иммуностимулятор для «трудных» пациентов с нарушениями в иммунной системе. Трудн. пациент. 2009; 7 (8): 27–34.
11. Осидак Л.В., Зарубаев В.В., Образцова Е.В., Эрман Е.С., Дриневский В.П. Изопринозин в терапии ОРВИ у часто болеющих детей. Дет. Инф. 2008; 7 (4): 35–41.
12. Парамонова Н.С., Волкова О.А. Проблемы острых респираторных вирусных заболеваний в педиатрии. Медицина 2006; 4: 66–67.
13. Сергиенко Е.Н., Шмелева Н.П., Германенко И.Г., Грибкова Н.В. Грипп у детей: клинико–эпидемиологические особенности и новые возможности терапии. Мед.Новости 2009; 14:1–4.
14. Del–Rio–Navarro BE, Espinosa Rosales F, Flenady V, Sienra–Monge JJL. Immunostimulants for preventing respiratory tract infection in children (Review).The Cochrane Coll.2006.
15. Golebiowska–Wawrzyniak M, Markiewicz K, Kozar A, Derentowicz P, Siwinska–Golebiowska H. The study on therapeutic efficacy of inosine pranobex in children. Pol. J.Food Nutr Sci. 2004; 46(13/54 SI2): 33–36.
16. Golebiowska–Wawrzyniak M, Markiewicz K, Kozar A, Derentowicz P, Czerwinska–Kartowicz I, Jastrzebska–Janas K, Waclawek J, Wawrzyniak ZM, Siwinska–Golebiowska H. Immunological and clinical study on therapeutic efficacy of inosine pranobex. Pol Merkur Lekarski. 2005;19(111):379–82.
17. Litzman J, Lokaj J, Krejci M, Pesak S, Morgan G. Isoprinosine does not protect against frequent respiratory tract infections in childhood. Eur J Pediatr 1999; 158:35–37.
18. Saker L, Lee K, Cannito B, Gilmore A, Campbell–Lendrum D. Globalization and infectious diseases: a review of the linkages. Social, Economic and Behavioural Research. Special Topics WHO. 2004. No.3TDR/STR/SEB/ST/04.2 http://apps.who.int/tdr/svc/publications/tdr–research–publications/globalization–infectious–diseases












