–Т–≤–µ–і–µ–љ–Є–µ
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Љ–µ–і–Є—Ж–Є–љ—Л –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ґ–Є–Ј–љ–Є –ї—О–і–µ–є, —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (–°–°–Ч) –Њ—Б—В–∞—О—В—Б—П –≤–µ–і—Г—Й–µ–є –њ—А–Є—З–Є–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –≤–Њ –≤—Б–µ–Љ –Љ–Є—А–µ [1]. –°–Њ–≥–ї–∞—Б–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–Љ –і–∞–љ–љ—Л–Љ –Т—Б–µ–Љ–Є—А–љ–Њ–є –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П –°–°–Ч –Ї–∞–ґ–і—Л–є –≥–Њ–і —Г–љ–Њ—Б—П—В –њ–Њ—А—П–і–Ї–∞ 17 –Љ–ї–љ –ї—О–і—Б–Ї–Є—Е –ґ–Є–Ј–љ–µ–є [2]. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –°–ї—Г–ґ–±—Л –≥–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ–Њ–є —Б—В–∞—В–Є—Б—В–Є–Ї–Є –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є –≤ 30% —Б–ї—Г—З–∞–µ–≤ –°–°–Ч —П–≤–ї—П—О—В—Б—П –њ—А–Є—З–Є–љ–Њ–є —Б–Љ–µ—А—В–Є –Љ—Г–ґ—З–Є–љ –Є –ґ–µ–љ—Й–Є–љ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ [3].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Њ –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –љ–Њ–≤—Л—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Љ–∞—А–Ї–µ—А–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥–ї–Є –±—Л —Б–ї—Г–ґ–Є—В—М –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–Љ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–Њ–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П —В–µ—З–µ–љ–Є—П –°–°–Ч, –љ–Њ —В–Њ–ї—М–Ї–Њ –Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–∞—В—А–Є–є—Г—А–µ—В–Є—З–µ—Б–Ї–Є–є –њ–µ–њ—В–Є–і (BNP), –µ–≥–Њ –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–Є (proBNP, NT-proBNP) –Є —Б–µ—А–і–µ—З–љ—Л–µ —В—А–Њ–њ–Њ–љ–Є–љ—Л (cTnI –Є cTnT) –љ–∞—И–ї–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ [4вАУ7].
–Т –і–∞–љ–љ–Њ–є —Б—В–∞—В—М–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –Њ–±–Ј–Њ—А–∞ –ї–Є—В–µ—А–∞—В—Г—А—Л, –Ї–∞—Б–∞—О—Й–µ–≥–Њ—Б—П –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–∞—А–Ї–µ—А–∞ –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–∞ 15 (–Ш–Ы-15) –≤ –∞—Б–њ–µ–Ї—В–µ –°–°–Ч.
–С–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –∞—Б–њ–µ–Ї—В—Л –Ш–Ы-15
–Ш–љ—В–µ—А–ї–µ–є–Ї–Є–љ 15 –±—Л–ї –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ –≤ 1994 –≥. –і–≤—Г–Љ—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ–Є –љ–∞—Г—З–љ–Њ-–Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–Є–Љ–Є –ї–∞–±–Њ—А–∞—В–Њ—А–Є—П–Љ–Є [8, 9]. J. Burton et al. [8] –Њ–њ–Є—Б–∞–ї–Є –љ–Њ–≤—Л–є —Ж–Є—В–Њ–Ї–Є–љ (–¶–Ъ) –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ –Ш–Ы-T, –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ—Л–є –ї–Є–Љ—Д–Њ–Љ–љ–Њ–є –Ґ-–Ї–ї–µ—В–Њ—З–љ–Њ–є –ї–Є–љ–Є–µ–є HuT-102. –£—З–µ–љ—Л–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є, —З—В–Њ —Б—Г–њ–µ—А–љ–∞—В–∞–љ—В (supernatant вАФ –њ–ї–∞–≤–∞—О—Й–Є–є –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є), –њ–Њ–ї—Г—З–µ–љ–љ—Л–є –Њ—В –і–∞–љ–љ–Њ–є –Ї–ї–µ—В–Њ—З–љ–Њ–є –Ї—Г–ї—М—В—Г—А—Л, –њ—А–Є –њ–µ—А–µ–љ–Њ—Б–µ –µ–≥–Њ –≤ –Ш–Ы-2-–Ј–∞–≤–Є—Б–Є–Љ—Г—О –Ї—Г–ї—М—В—Г—А—Г –Љ—Л—И–Є–љ–Њ–є –Ї–ї–µ—В–Њ—З–љ–Њ–є –ї–Є–љ–Є–Є CTLL-2 —Г—Б–Є–ї–Є–≤–∞–ї –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –Ґ-–Ї–ї–µ—В–Њ–Ї –Є –∞–Ї—В–Є–≤–∞—Ж–Є—О –±–Њ–ї—М—И–Є—Е –Ј–µ—А–љ–Є—Б—В—Л—Е (–≥—А–∞–љ—Г–ї—П—А–љ—Л—Е) –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤, –њ—А–Є —Н—В–Њ–Љ –∞–љ—В–Є—Б—Л–≤–Њ—А–Њ—В–Ї–∞ –Ї –Ш–Ы-2 –љ–µ —Г–Љ–µ–љ—М—И–∞–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –Ґ–∞–Ї–ґ–µ –і–ї—П –њ—А–Њ—П–≤–ї–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ш–Ы-T —В—А–µ–±–Њ–≤–∞–ї–∞—Б—М —Н–Ї—Б–њ—А–µ—Б—Б–Є—П ќ≤-—Ж–µ–њ–Є —А–µ—Ж–µ–њ—В–Њ—А–∞ (R) –Ш–Ы-2 (–Ш–Ы-2R). –Ш–Ы-T –±—Л–ї –Њ—Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–љ –Ї–∞–Ї –Ґ-–Ї–ї–µ—В–Њ—З–љ—Л–є —А–Њ—Б—В–Њ–≤–Њ–є —Д–∞–Ї—В–Њ—А.
–Э–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є –Љ–µ—Б—П—Ж–∞–Љ–Є –њ–Њ–Ј–ґ–µ J. Giri et al. [9] –і–Њ–ї–Њ–ґ–Є–ї–Є –Њ–± –Њ—В–Ї—А—Л—В–Є–Є –¶–Ъ —Б –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —Б—Е–Њ–ґ–µ–є —Б –Ш–Ы-2, –Ї–Њ—В–Њ—А—Л–є —В–∞–Ї–ґ–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–ї –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –Ш–Ы-2R.
K. Grabstein et al. [10] –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞ –љ–∞ –Ї–ї–µ—В–Ї–∞—Е —Н–њ–Є—В–µ–ї–Є—П –њ–Њ—З–Ї–Є –≤—Л—П–≤–Є–ї–Є, —З—В–Њ —Б—Г–њ–µ—А–љ–∞—В–∞–љ—В –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–ї –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –Ш–Ы-2-–Ј–∞–≤–Є—Б–Є–Љ–Њ–є –ї–Є–љ–Є–Є –Ї–ї–µ—В–Њ–Ї CTLL. –Ш–Ј —Б—Г–њ–µ—А–љ–∞—В–∞–љ—В–∞ –±—Л–ї –њ–Њ–ї—Г—З–µ–љ –±–µ–ї–Њ–Ї, –Њ—Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–љ–∞ –µ–≥–Њ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ–∞—П –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М –Є –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–∞ —Б—В—А—Г–Ї—В—Г—А–љ–∞—П –∞–љ–∞–ї–Њ–≥–Є—П —Б –Ш–Ы-2. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –∞–љ—В–Є—В–µ–ї–∞ –Ї ќ≤-—Ж–µ–њ–Є –Ш–Ы-2R (–Ш–Ы-2Rќ≤) –њ–Њ–і–∞–≤–ї—П—О—В –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–Њ–≤–Њ–≥–Њ —А–Њ—Б—В–Њ–≤–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞, –Ї–Њ—В–Њ—А—Л–є –±—Л–ї –љ–∞–Ј–≤–∞–љ –Ш–Ы-15 [11].
–Ш–љ—В–µ—А–ї–µ–є–Ї–Є–љ 15 —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г–µ—В—Б—П –Љ–Њ–љ–Њ—Ж–Є—В–∞–Љ–Є, –Љ–∞–Ї—А–Њ—Д–∞–≥–∞–Љ–Є –Є –і—А—Г–≥–Є–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є, —Г—З–∞—Б—В–≤—Г—О—Й–Є–Љ–Є –≤–Њ –≤—А–Њ–ґ–і–µ–љ–љ—Л—Е –Є –∞–і–∞–њ—В–Є–≤–љ—Л—Е –Є–Љ–Љ—Г–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є—П—Е [12вАУ14]. –Ш–Ы-15 –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ, –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–∞—П –Љ–∞—Б—Б–∞ –Ї–Њ—В–Њ—А–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –њ–Њ—А—П–і–Ї–∞ 15 –Ї–Є–ї–Њ–і–∞–ї—М—В–Њ–љ (–Ї–Ф–∞). –Ю–љ –Ї–Њ–і–Є—А—Г–µ—В—Б—П –≥–µ–љ–Њ–Љ —А–∞–Ј–Љ–µ—А–Њ–Љ –≤ 34 –Ї–± (–Ї–Є–ї–Њ–±–∞–Ј–∞ (–Ї–±)) = 1000 –њ–∞—А –љ—Г–Ї–ї–µ–Њ—В–Є–і–Њ–≤), –Ї–Њ—В–Њ—А—Л–є —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ –љ–∞ –і–ї–Є–љ–љ–Њ–Љ –њ–ї–µ—З–µ 4-–є —Е—А–Њ–Љ–Њ—Б–Њ–Љ—Л (4q31) [12вАУ14]. –У–µ–љ, –Ї–Њ–і–Є—А—Г—О—Й–Є–є –Ш–Ы-15, —Б–Њ—Б—В–Њ–Є—В –Є–Ј 9 —Н–Ї–Ј–Њ–љ–Њ–≤ –Є 8 –Є–љ—В—А–Њ–љ–Њ–≤, 4 –Є–Ј –Ї–Њ—В–Њ—А—Л—Е (—Н–Ї–Ј–Њ–љ—Л —Б 5 –њ–Њ 8) –Ї–Њ–і–Є—А—Г—О—В –±–µ–ї–Ї–Њ–≤—Г—О —З–∞—Б—В—М –і–∞–љ–љ–Њ–≥–Њ –¶–Ъ [12вАУ14].
–Ю–њ–Є—Б–∞–љ—Л –і–≤–µ –Є–Ј–Њ—Д–Њ—А–Љ—Л –Ш–Ы-15 [12вАУ14]. –Я–µ—А–≤–∞—П –Є–Ј–Њ—Д–Њ—А–Љ–∞ вАФ –Ш–Ы-15SSP, –і–ї—П –љ–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ–∞ –±–Њ–ї–µ–µ –Ї–Њ—А–Њ—В–Ї–∞—П —Ж–µ–њ—М, —Б–Њ–і–µ—А–ґ–∞—Й–∞—П 21 –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Г. –Т—В–Њ—А–∞—П –Є–Ј–Њ—Д–Њ—А–Љ–∞ –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В—Б—П –Ї–∞–Ї –Ш–Ы-15LSP, –Њ–±–ї–∞–і–∞–µ—В –±–Њ–ї–µ–µ –і–ї–Є–љ–љ–Њ–є —Ж–µ–њ—М—О, —Б–Њ—Б—В–Њ—П—Й–µ–є –Є–Ј 41 –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л. –Ш–Ы-15SSP –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –≤–Є–ї–Њ—З–Ї–Њ–≤–Њ–є –ґ–µ–ї–µ–Ј–µ –Є —П–Є—З–љ–Є–Ї–∞—Е. –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П [12вАУ14] —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –Є–Ј–Њ—Д–Њ—А–Љ –Є –Ј–µ–ї–µ–љ–Њ–≥–Њ —Д–ї—Г–Њ—А–µ—Б—Ж–µ–љ—В–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ –Ш–Ы-15SSP –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–µ –Є —П–і—А–µ –Ї–ї–µ—В–Ї–Є –Є –њ—А–Є–љ–Є–Љ–∞–µ—В —Г—З–∞—Б—В–Є–µ –≤ —В—А–∞–љ—Б–Ї—А–Є–њ—Ж–Є–Њ–љ–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є –±–µ–ї–Ї–Њ–≤. –Ш–Ы-15LSP —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ –У–Њ–ї—М–і–ґ–Є, —А–∞–љ–љ–Є—Е —Н–љ–і–Њ—Б–Њ–Љ–∞—Е –Є —Н–љ–і–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ —А–µ—В–Є–Ї—Г–ї—Г–Љ–µ, –≥–і–µ —А–µ–≥—Г–ї–Є—А—Г–µ—В —В—А–∞–љ—Б–ї—П—Ж–Є—О –±–µ–ї–Ї–Њ–≤ –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А—Г–µ—В –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–≥–Њ —Б–Є–≥–љ–∞–ї—М–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞.
–Ш–љ—В–µ—А–ї–µ–є–Ї–Є–љ 2 –Є –Ш–Ы-15 —Б–≤—П–Ј—Л–≤–∞—О—В—Б—П —Б –Њ–±—Й–Є–Љ –≥–µ—В–µ—А–Њ–і–Є–Љ–µ—А–љ—Л–Љ —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ, —Б–Њ—Б—В–Њ—П—Й–Є–Љ –Є–Ј ќ≤-—Б—Г–±—К–µ–і–Є–љ–Є—Ж—Л –Ш–Ы-2/15Rќ≤ (CD122) –Є ќ≥-—Б—Г–±—К–µ–і–Є–љ–Є—Ж—Л (ќ≥c –Є–ї–Є CD132). –°–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ–±–Њ–Є—Е –¶–Ъ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—О—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ —Ж–µ–њ–Є ќ±-—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ вАФ –Ш–Ы-2Rќ± (CD25) –Є –Ш–Ы-15Rќ± (CD215). –Ш–Ы-15Rќ± —Б–≤—П–Ј—Л–≤–∞–µ—В –Ш–Ы-15 —Б –≤—Л—Б–Њ–Ї–Є–Љ —Б—А–Њ–і—Б—В–≤–Њ–Љ, —В–Њ–≥–і–∞ –Ї–∞–Ї –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ—Л–є –Ш–Ы-2Rќ± —П–≤–ї—П–µ—В—Б—П –љ–Є–Ј–Ї–Њ–∞—Д—Д–Є–љ–љ—Л–Љ —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ –і–ї—П –Ш–Ы-2 [15].
–Ш–љ—В–µ—А–ї–µ–є–Ї–Є–љ 15 –Є –Ш–Ы-2 –њ–Њ—Е–Њ–ґ–Є –њ–Њ —В—А–µ—Е–Љ–µ—А–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ (—Б–Љ. —А–Є—Б—Г–љ–Њ–Ї) [16]. –Ш–Ы-15Rќ± —Б–Њ–і–µ—А–ґ–Є—В 173 –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л —Н–Ї—Б—В—А–∞—Ж–µ–ї–ї—О–ї—П—А–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞, 21 –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Г —В—А–∞–љ—Б–Љ–µ–Љ–±—А–∞–љ–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –Є 37 –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ [13, 14]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–љ—В—А–Њ–љ-—Н–Ї–Ј–Њ–љ–љ–∞—П –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є—П –≥–µ–љ–∞ –Ш–Ы-15Rќ± –∞–љ–∞–ї–Њ–≥–Є—З–љ–∞ –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –Ш–Ы-2Rќ± [13, 14]. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —Н—В–Њ —Б—Е–Њ–і—Б—В–≤–Њ, –Ш–Ы-15Rќ± –Є–Љ–µ–µ—В –љ–µ–±–Њ–ї—М—И—Г—О –≥–Њ–Љ–Њ–ї–Њ–≥–Є—О –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є —Б –Ш–Ы-2Rќ± [17]. –Ш–Ы-15Rќ± —И–Є—А–Њ–Ї–Њ —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г–µ—В—Б—П —Г –ї—О–і–µ–є –Є –Љ—Л—И–µ–є –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Ж–µ–њ–Є –Ш–Ы-2R/–Ш–Ы-15Rќ≤-ќ≥. –Ш–Ы-15, —Б–≤—П–Ј–∞–љ–љ—Л–є —Б –Ш–Ы-15Rќ±, —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В —Ж–Є—А–Ї—Г–ї–Є—А–Њ–≤–∞—В—М —З–µ—А–µ–Ј —Н–љ–і–Њ—Б–Њ–Љ–∞–ї—М–љ—Л–µ –≤–µ–Ј–Є–Ї—Г–ї—Л –≤ —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е –і–љ–µ–є (—Н–љ–і–Њ—Б–Њ–Љ–∞–ї—М–љ–∞—П —А–µ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—П), —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—В–Њ–є–Ї–Њ—Б—В–Є —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б –Љ–µ–Љ–±—А–∞–љ–Њ–є –Ш–Ы-15 [13, 14]. –Я–Њ–≤—Л—И–µ–љ–Є–µ —А–µ–≥—Г–ї—П—Ж–Є–Є –Ш–Ы-15 –Є –Ш–Ы-15Rќ± –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П –≤–Њ –≤—А–µ–Љ—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є [18, 19].
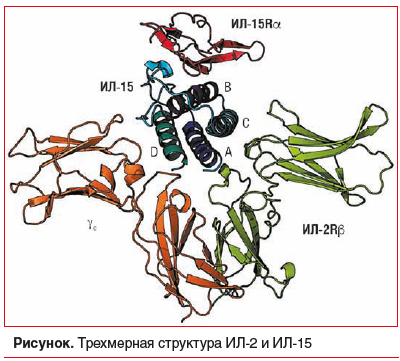
–≠–Ї—Б–њ—А–µ—Б—Б–Є—П –Ш–Ы-15 –Є –Ш–Ы-15Rќ± –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –≤–Њ –Љ–љ–Њ–≥–Є—Е —В–Є–њ–∞—Е –Ї–ї–µ—В–Њ–Ї (—Б–Љ. —В–∞–±–ї–Є—Ж—Г) [13, 14, 20вАУ25].
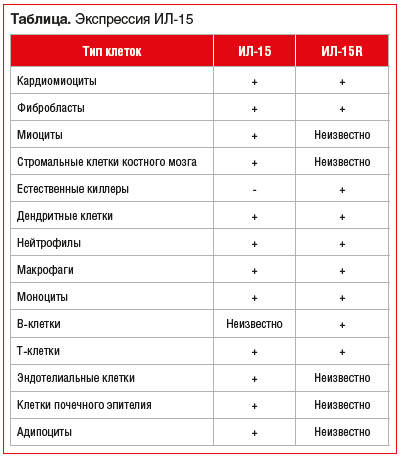
T. Dinh et al. [26] –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Ш–Ы-2, –Ї–Њ—В–Њ—А—Л–є –≤–Ї–ї—О—З–∞–µ—В –Ш–Ы-2 –Є –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ–Њ–µ –∞–љ—В–Є—В–µ–ї–Њ (mAb), —Г—Б–Є–ї–Є–≤–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —А–µ–≥—Г–ї—П—В–Њ—А–љ—Л—Е –Ґ-–ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤, —Г–Љ–µ–љ—М—И–∞–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ —Г –Љ—Л—И–µ–є —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –∞–њ–Њ–ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–∞ E (–Р–њ–Њ–Х), —Г–Љ–µ–љ—М—И–∞–µ—В —А–∞–Ј–Љ–µ—А –Ј–Њ–љ—Л –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ш–Ь) –Є —Г–ї—Г—З—И–∞–µ—В —Д—Г–љ–Ї—Ж–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–Ы–Ц). K. Webster et al. [27] –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є, —З—В–Њ –Ш–Ы-2 —Г–Љ–µ–љ—М—И–∞–µ—В –∞–њ–Њ–њ—В–Њ–Ј –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В–Њ–≤ —Г –Љ—Л—И–µ–є —Б –Ш–Ь. Z. Zeng et al. [28] –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Ш–Ы-2 –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ј–∞—Й–Є—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –љ–∞–њ—А—П–Љ—Г—О –Є–љ–≥–Є–±–Є—А—Г—П –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є—О –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤ –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—П –њ–Њ–ї—П—А–Є–Ј–∞—Ж–Є–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤ M2, —З—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, —Г–Љ–µ–љ—М—И–∞–µ—В –∞–њ–Њ–њ—В–Њ–Ј –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В–Њ–≤ –Є –Њ—Б–ї–∞–±–ї—П–µ—В –ї–Њ–Ї–∞–ї—М–љ—Л–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є.
–¶–µ–ї—М—О –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П M. Bouchentouf et al. [29] –±—Л–ї–∞ –њ—А–Њ–≤–µ—А–Ї–∞ –≥–Є–њ–Њ—В–µ–Ј—Л –Њ —В–Њ–Љ, —З—В–Њ –≤–≤–µ–і–µ–љ–Є–µ —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ–Њ–≥–Њ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Ш–Ы-2 (rh–Ш–Ы-2) —Г–ї—Г—З—И–∞–µ—В –∞–љ–≥–Є–Њ–≥–µ–љ–µ–Ј –Є —Б–Њ—Е—А–∞–љ—П–µ—В —Д—Г–љ–Ї—Ж–Є—О —Б–µ—А–і—Ж–∞ –њ–Њ—Б–ї–µ –Ш–Ь. –Ю–і–љ–Њ–Ї—А–∞—В–љ–∞—П –≤–љ—Г—В—А–Є–≤–µ–љ–љ–∞—П –Є–љ—К–µ–Ї—Ж–Є—П rh–Ш–Ы-2 —З–µ—А–µ–Ј 2 –і–љ—П –њ–Њ—Б–ї–µ –Ш–Ь —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞ –љ–∞ 27,7% —Д—А–∞–Ї—Ж–Є–Њ–љ–љ–Њ–µ —Г–Ї–Њ—А–Њ—З–µ–љ–Є–µ –Ы–Ц —Г –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ–µ—В–µ–љ—В–љ—Л—Е (C57Bl6) –Љ—Л—И–µ–є, –љ–Њ –љ–µ –≤–ї–Є—П–ї–∞ –љ–∞ —Б–µ—А–і–µ—З–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О —Г –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В–љ—Л—Е (NOD-SCID –Ш–Ы-2Rќ≥null) –Љ—Л—И–µ–є. –Ш–Љ–Љ—Г–љ–Њ–≥–Є—Б—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –њ–Њ–њ–µ—А–µ—З–љ—Л—Е —Б—А–µ–Ј–Њ–≤ —Б–µ—А–і–µ—Ж C57Bl6 –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –Њ—В–ї–Њ–ґ–µ–љ–Є–µ –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М –љ–∞ 23,1%, –∞ –њ–ї–Њ—В–љ–Њ—Б—В—М –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ —Г–≤–µ–ї–Є—З–Є–ї–∞—Б—М –≤ –Њ–±–ї–∞—Б—В–Є —А—Г–±—Ж–∞ –Є –≤ –њ–Њ–≥—А–∞–љ–Є—З–љ–Њ–є –Ј–Њ–љ–µ –Ш–Ь —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –љ–∞ 22,4% –Є 33,6% –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є rh–Ш–Ы-2. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, rh–Ш–Ы-2 —Г–≤–µ–ї–Є—З–Є–ї –≤ 1,6 —А–∞–Ј–∞ –Є–љ–і–µ–Ї—Б –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї in vivo –Є –≤ 1,8 —А–∞–Ј–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л—Е –Ї–Є–ї–ї–µ—А–Њ–≤, –Є–љ—Д–Є–ї—М—В—А–Є—А—Г—О—Й–Є—Е –Є–љ—Д–∞—А–Ї—В–љ—Л–µ —Б–µ—А–і—Ж–∞. Rh–Ш–Ы-2 –љ–µ –≤–ї–Є—П–ї –љ–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б–µ—А–і–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї CD4 –Є CD8. In vitro –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л–µ rh–Ш–Ы-2 NK-–Ї–ї–µ—В–Ї–Є —Г—Б–Є–ї–Є–≤–∞–ї–Є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Б–µ—А–і—Ж–∞ –љ–∞ 17,2%.
–Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –і–≤–µ —Б—Г–±—К–µ–і–Є–љ–Є—Ж—Л —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ш–Ы-15 –Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ш–Ы-2 —Б—Е–Њ–ґ–Є, –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ш–Ы-15 –Љ–Њ–ґ–µ—В —З–∞—Б—В–Є—З–љ–Њ —Б–Њ–≤–њ–∞–і–∞—В—М —Б –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Ш–Ы-2 [13].
–†–Њ–ї—М –Ш–Ы-15 –њ—А–Є –Љ–Є–Њ–Ї–∞—А–і–Є—В–µ –Є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–Љ —Б—В—А–µ—Б—Б–µ
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –¶–Ъ –Є–≥—А–∞—О—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –Є —В–µ—З–µ–љ–Є–Є –≤–Є—А—Г—Б–љ–Њ–≥–Њ –Љ–Є–Њ–Ї–∞—А–і–Є—В–∞ (–Т–Ь).
B. Bigalke et al. [30] –Є–Ј—Г—З–∞–ї–Є –≤–ї–Є—П–љ–Є–µ –Ш–Ы-15 –љ–∞ —В–µ—З–µ–љ–Є–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–≥–Њ –Љ–Є–Њ–Ї–∞—А–і–Є—В–∞ —Г –Љ—Л—И–µ–є, –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤–Є—А—Г—Б–Њ–Љ –Ъ–Њ–Ї—Б–∞–Ї–Є B3 (CVB3). –Я—А–Њ–≤–Њ–і–Є–ї–Є –∞–љ–∞–ї–Є–Ј —Б–µ—А–і–µ—Ж CVB3-–Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ—Л—И–µ–є (n=14), –ї–Њ–ґ–љ–Њ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ—Л—И–µ–є (n=14) –Є CVB3-–Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ—Л—И–µ–є –ї–Є–љ–Є–Є Balb/c (–Є–љ–±—А–µ–і–љ—Л—Е), –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ш–Ы-15 (n=6) –Є–ї–Є —Б–ї–Є—В—Л–є –±–µ–ї–Њ–Ї –Ш–Ы-15 (n=6). –Р–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї—Г—О —Д—Г–љ–Ї—Ж–Є—О, –Ї–ї–µ—В–Њ—З–љ—Л–µ –Є–љ—Д–Є–ї—М—В—А–∞—В—Л –Є —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ. –Ш–љ–і—Г–Ї—Ж–Є—П –Т–Ь –±—Л–ї–∞ —Б–≤—П–Ј–∞–љ–∞ —Б–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –њ–Њ—В–µ—А–µ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є –Љ–∞—Б—Б—Л —Б–µ—А–і—Ж–∞, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Д—Г–љ–Ї—Ж–Є–Є –Ы–Ц, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ –Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Є–љ—Д–Є–ї—М—В—А–∞—В–Њ–≤ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ. –Ы–µ—З–µ–љ–Є–µ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е –Ш–Ы-15 –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є –Љ–∞—Б—Б—Л —Б–µ—А–і—Ж–∞, –∞ —В–∞–Ї–ґ–µ –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є —Д—Г–љ–Ї—Ж–Є–є –Ы–Ц. –Ю—В–Љ–µ—З–µ–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ї–Њ–ї–ї–∞–≥–µ–љ–∞, –∞ —В–∞–Ї–ґ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–ї–µ—В–Њ—З–љ–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–Є –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ –Є –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ. –Ш–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –Ш–Ы-15 –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –Њ–±–Њ—Б—В—А–µ–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –ї–µ—З–µ–љ–Є–µ –Ш–Ы-15 –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ CVB3-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є –Љ–Є–Њ–Ї–∞—А–і–Є—В —Г –Љ—Л—И–µ–є –Є, –њ–Њ-–≤–Є–і–Є–Љ–Њ–Љ—Г, —П–≤–ї—П–µ—В—Б—П –Љ–љ–Њ–≥–Њ–Њ–±–µ—Й–∞—О—Й–Є–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ –Ї –Є–Ј–Љ–µ–љ–µ–љ–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П, –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –Є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Т–Ь.
Y. Yeghizarians et al. [31] –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Ш–Ы-15 –Є –µ–≥–Њ —А–µ—Ж–µ–њ—В–Њ—А—Л –њ—А–Є—Б—Г—В—Б—В–≤—Г—О—В –≤ –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В–∞—Е. –Т–≤–µ–і–µ–љ–Є–µ –Ш–Ы-15 —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Њ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В–Њ–≤ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —Д–Њ—Б—Д–Њ—А–Є–ї–Є—А–Њ–≤–∞–љ–Є—П —Б–Є–≥–љ–∞–ї—М–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ –Є –∞–Ї—В–Є–≤–∞—В–Њ—А–∞ —В—А–∞–љ—Б–Ї—А–Є–њ—Ж–Є–Є (signal transducer and activator of transcription 3, STAT3). –Ґ–∞–Ї–ґ–µ –Ш–Ы-15 –Ј–∞—Й–Є—Й–∞–ї –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В—Л –Њ—В –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ PI3K / ERK1 (—Б–Є–≥–љ–∞–ї—М–љ—Л–є –њ—Г—В—М, —Ж–µ–љ—В—А–∞–ї—М–љ—Л–Љ–Є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П—О—В—Б—П —Д–µ—А–Љ–µ–љ—В—Л —Д–Њ—Б—Д–Њ–Є–љ–Њ–Ј–Є—В–Є–і-3-–Ї–Є–љ–∞–Ј–∞ (PI3K)) / –љ–µ–Ї–ї–µ—В–Њ—З–љ–∞—П –Ї–Є–љ–∞–Ј–∞ 1, —А–µ–≥—Г–ї–Є—А—Г–µ–Љ–∞—П —Б–Є–≥–љ–∞–ї–Њ–Љ (extracellular signal-regulated kinase (ERK)).
P. Carai et al. [32] –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–ї–Є 5 –Ш–Ы (3, 4, 9, 13 –Є 15) –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –њ—А–Є CVB3-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–Є—В–µ —Г –Љ—Л—И–µ–є.
–Ш–Ы-15 –њ—А–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–µ –Є —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –љ–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –≤ –Ї–∞—З–µ—Б—В–≤–µ –≥–ї–∞–≤–љ–Њ–≥–Њ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–∞–Ј–≤–Є—В–Є—П –Љ–љ–Њ–≥–Є—Е –°–°–Ч –≤—Л—Б—В—Г–њ–∞–µ—В –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј [33вАУ35]. –Р—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б, –њ—А–Њ—П–≤–ї—П—О—Й–Є–є—Б—П –Њ—Б—В—А—Л–Љ–Є —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ї–∞—В–∞—Б—В—А–Њ—Д–∞–Љ–Є, —В–∞–Ї–Є–Љ–Є –Ї–∞–Ї –Ш–Ь –Є –Є–љ—Д–∞—А–Ї—В –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Њ—Б—В–Њ—П–љ–Є—П–Љ–Є, —В–∞–Ї–Є–Љ–Є –Ї–∞–Ї –Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞ (–Ш–С–°) –Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–∞—П –±–Њ–ї–µ–Ј–љ—М, —П–≤–ї—П–µ—В—Б—П –њ–Њ —Б—Г—В–Є —Б–Є—Б—В–µ–Љ–љ—Л–Љ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –њ—А–Њ—Ж–µ—Б—Б–Њ–Љ [36].
D. Wuttge et al. [37] –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є, —З—В–Њ –Ш–Ы-15 –∞–Ї—В–Є–≤–Є—А—Г–µ—В—Б—П –њ—А–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е –Ї–∞–Ї —Г —З–µ–ї–Њ–≤–µ–Ї–∞, —В–∞–Ї –Є —Г –ґ–Є–≤–Њ—В–љ—Л—Е –Є –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —А–µ–Ї—А—Г—В–Є—А–Њ–≤–∞–љ–Є—О –Є –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Ґ-–Ї–ї–µ—В–Њ–Ї –≤–Њ –≤—А–µ–Љ—П –∞—В–µ—А–Њ–≥–µ–љ–µ–Ј–∞.
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, CD4+CD28null (CD28null) –Ґ-–Ї–ї–µ—В–Ї–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Г—О –њ–Њ–і–≥—А—Г–њ–њ—Г –Ґ-–ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤, –њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –¶–Ъ –Є —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л. J. Bullenkamp et al. [38] –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є —А–Њ–ї—М –¶–Ъ –≤ —Н–Ї—Б–њ–∞–љ—Б–Є–Є CD28null –Ґ-–Ї–ї–µ—В–Њ–Ї –њ—А–Є –Њ—Б—В—А–Њ–Љ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ (–Ю–Ъ–°). –Ю—В—Б–Њ—А—В–Є—А–Њ–≤–∞–љ–љ—Л–µ CD4+ –Ґ-–Ї–ї–µ—В–Ї–Є –≤—Л—Б–Њ–Ї–Њ–є —З–Є—Б—В–Њ—В—Л –Њ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Ъ–° –Њ–±—А–∞–±–∞—В—Л–≤–∞–ї–Є –¶–Ъ (—Д–∞–Ї—В–Њ—А–Њ–Љ –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є ќ± (TNF-ќ±), –Ш–Ы-1ќ≤, 6, 7 –Є 15). –Ш–Ы-7 –Є -15 –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–ї–Є —Н–Ї—Б–њ–∞–љ—Б–Є—О CD28null –Ґ-–Ї–ї–µ—В–Њ–Ї —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Ъ–°, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї TNF-ќ±, –Ш–Ы-1ќ≤ –Є -6 –љ–µ –Њ–±–ї–∞–і–∞–ї–Є –і–∞–љ–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ. –Ь–µ—Е–∞–љ–Є–Ј–Љ—Л, –ї–µ–ґ–∞—Й–Є–µ –≤ –Њ—Б–љ–Њ–≤–µ —Н–Ї—Б–њ–∞–љ—Б–Є–Є CD28null T-–Ї–ї–µ—В–Њ–Ї –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Ш–Ы-7/–Ш–Ы-15, –Ј–∞–Ї–ї—О—З–∞–ї–Є—Б—М –≤ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є CD28null T-–Ї–ї–µ—В–Њ–Ї. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ш–Ы-7/–Ш–Ы-15 –Ј–∞–Љ–µ—В–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї—Г—О —Д—Г–љ–Ї—Ж–Є—О CD28null T-–Ї–ї–µ—В–Њ–Ї –Є –њ—А–Њ–і—Г–Ї—Ж–Є—О –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞ ќ≥ (IFNќ≥). –Ф–∞–ї—М–љ–µ–є—И–Є–є –∞–љ–∞–ї–Є–Ј –≤—Л—П–≤–Є–ї —А–∞–Ј–ї–Є—З–Є—П –≤ –Є—Б—Е–Њ–і–љ–Њ–є —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–љ—Л—Е —Ж–µ–њ–µ–є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ш–Ы-7/–Ш–Ы-15 (CD127 –Є CD122), –њ–Њ–≤—Л—И–µ–љ–љ–Њ–Љ –Є—Б—Е–Њ–і–љ–Њ–Љ —Г—А–Њ–≤–љ–µ —Д–Њ—Б—Д–Њ—А–Є–ї–Є—А–Њ–≤–∞–љ–Є—П STAT5 –≤ CD28null T-–Ї–ї–µ—В–Ї–∞—Е —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Ъ–° –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є —Б—Г–±–њ–Њ–њ—Г–ї—П—Ж–Є–µ–є CD28+ T-–Ї–ї–µ—В–Њ–Ї. –С—Л–ї–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ, —З—В–Њ —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є–µ CD28null –Ґ-–Ї–ї–µ—В–Њ–Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Є–љ–≥–Є–±–Є—А—Г–µ—В—Б—П —В–Њ—Д–∞—Ж–Є—В–Є–љ–Є–±–Њ–Љ (—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –Є–Љ–Љ—Г–љ–Њ–і–µ–њ—А–µ—Б—Б–∞–љ—В; –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –Љ–Њ—Й–љ—Л–є —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –Є–љ–≥–Є–±–Є—В–Њ—А —Б–µ–Љ–µ–є—Б—В–≤–∞ —П–љ—Г—Б-–Ї–Є–љ–∞–Ј, –Њ–±–ї–∞–і–∞—О—Й–Є–є –≤—Л—Б–Њ–Ї–Њ–є –Є–Ј–±–Є—А–∞—В–µ–ї—М–љ–Њ—Б—В—М—О –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–Њ—З–Є—Е –Ї–Є–љ–∞–Ј –≥–µ–љ–Њ–Љ–∞ —З–µ–ї–Њ–≤–µ–Ї–∞). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Ш–Ы-7 –Є –Ш–Ы-15 —Б—В–Є–Љ—Г–ї–Є—А—Г—О—В —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є–µ CD28null –Ґ-–Ї–ї–µ—В–Њ–Ї —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Ъ–°. –≠—В–Њ –≥–Њ–≤–Њ—А–Є—В –≤ –њ–Њ–ї—М–Ј—Г —В–Њ–≥–Њ, —З—В–Њ –±–ї–Њ–Ї–∞–і–∞ –Ш–Ы-7/–Ш–Ы-15 –Љ–Њ–ґ–µ—В –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є–µ —Н—В–Є—Е –Ї–ї–µ—В–Њ–Ї –Є —Г–ї—Г—З—И–Є—В—М —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–£—З–µ–љ—Л–µ –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ G. Tarantino [39] –Њ–±—Б–ї–µ–і–Њ–≤–∞–ї–Є 80 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Є –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є –ґ–Є—А–Њ–≤–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –њ–µ—З–µ–љ–Є. –Ґ–∞–Ї–ґ–µ –∞–≤—В–Њ—А—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —В–Њ–ї—Й–Є–љ–Њ–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Є–љ—В–Є–Љ–∞-–Љ–µ–і–Є–∞ —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є–є (–Ґ–Ъ–Ш–Ь –°–Р) –Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П–Љ–Є –Ш–Ы-15 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є. –£—А–Њ–≤–љ–Є –Ш–Ы-15 —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –±—Л–ї–Є –њ–Њ–≤—Л—И–µ–љ—Л –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤—Л–Љ–Є —Г 44 –Љ–Њ–ї–Њ–і—Л—Е –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є (2,77 (1,21вАУ4,8) –њ–≥/–Љ–ї –њ—А–Њ—В–Є–≤ 1,55 (1вАУ2,4) –њ–≥/–Љ–ї (—А=0,002)). –Т –Њ–і–љ–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ —Г—А–Њ–≤–љ–Є –Ш–Ы-15 –±—Л–ї–Є —Б–≤—П–Ј–∞–љ—Л —Б –Є–љ–і–µ–Ї—Б–Њ–Љ –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–Ш–Ь–Ґ) –Є —Г—А–Њ–≤–љ—П–Љ–Є –Љ–Њ–љ–Њ—Ж–Є—В–∞—А–љ–Њ–≥–Њ —Е–µ–Љ–Њ—В–∞–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –±–µ–ї–Ї–∞ 1 (MCP-1), —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Њ—Б—В–∞ —Д–Є–±—А–Њ–±–ї–∞—Б—В–Њ–≤ (FGF) –Є –≥—А–∞–љ—Г–ї–Њ—Ж–Є—В–∞—А–љ–Њ-–Љ–∞–Ї—А–Њ—Д–∞–≥–∞–ї—М–љ—Л–Љ –Ї–Њ–ї–Њ–љ–Є–µ—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –Љ–љ–Њ–≥–Њ–Љ–µ—А–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ —В–Њ–ї—М–Ї–Њ –≤–Њ–Ј—А–∞—Б—В –Є –Ш–Ы-15 –Њ—Б—В–∞–≤–∞–ї–Є—Б—М –њ—А–µ–і–Є–Ї—В–Њ—А–∞–Љ–Є –Ґ–Ъ–Ш–Ь (ќ≤=0,60, p=0,0001 –Є ќ≤=0,25, p=0,024 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Э–µ –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —Б–≤—П–Ј–Є –Ш–Ы-15 —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–Љ–Є –њ–∞—А–∞–Љ–µ—В—А–∞–Љ–Є, –∞ —В–∞–Ї–ґ–µ —Б —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ –ґ–Є—А–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Є —В—П–ґ–µ—Б—В—М—О —Б—В–µ–∞—В–Њ–≥–µ–њ–∞—В–Є—В–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ–Њ—Б–ї–µ –њ–Њ–њ—А–∞–≤–Ї–Є –љ–∞ –≤–Њ–Ј—А–∞—Б—В.
–¶–µ–ї—М—О –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П Es. van Thomas et al. [40] —П–≤–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ —А–Њ–ї–Є –Ш–Ы-15 –≤ —А–∞–Ј–≤–Є—В–Є–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. –Р–≤—В–Њ—А—Л –Є–Ј—Г—З–∞–ї–Є –≤–ї–Є—П–љ–Є–µ –Ш–Ы-15 –љ–∞ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–µ —Б –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ –Ї–ї–µ—В–Ї–Є in vitro –Є in vivo –њ—Г—В–µ–Љ –µ–≥–Њ –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ф–Э–Ъ-–≤–∞–Ї—Ж–Є–љ—Л (–≤–∞–Ї—Ж–Є–љ–∞ –љ–∞ –Њ—Б–љ–Њ–≤–µ –љ—Г–Ї–ї–µ–Є–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В). –Я—А–Є –Ї–Њ—А–Љ–ї–µ–љ–Є–Є –Љ—Л—И–µ–є —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ —А–µ—Ж–µ–њ—В–Њ—А–∞ –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –љ–Є–Ј–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є (LDLr (-/-)) –њ—А–Њ–і—Г–Ї—В–∞–Љ–Є, —В–Є–њ–Є—З–љ—Л–Љ–Є –і–ї—П ¬Ђ–Ј–∞–њ–∞–і–љ–Њ–є –і–Є–µ—В—Л¬ї, –≤ —Б–µ–ї–µ–Ј–µ–љ–Ї–µ –Њ—В–Љ–µ—З–µ–љ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М –Ш–Ы-15 –Є –Ї–ї–µ—В–Њ–Ї, –µ–≥–Њ —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г—О—Й–Є—Е. –Ф–Њ–±–∞–≤–ї–µ–љ–Є–µ –Ш–Ы-15 –Ї –Љ–∞–Ї—А–Њ—Д–∞–≥–∞–Љ –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–ї–Њ —Н–Ї—Б–њ—А–µ—Б—Б–Є—О TNF-ќ± –Є MCP-1. –Я–Њ—Б–ї–µ –≤–∞–Ї—Ж–Є–љ–∞—Ж–Є–Є –Љ—Л—И–µ–є –њ—А–Њ—В–Є–≤ –Ш–Ы-15 –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–∞ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –±–ї—П—И–µ–Ї –љ–∞ 75%. –Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤ –≤ –±–ї—П—И–Ї–µ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –≤ 2 —А–∞–Ј–∞ –≤—Л—И–µ —Г –≤–∞–Ї—Ж–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ—Л—И–µ–є, —З–µ–Љ —Г –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л—Е –Љ—Л—И–µ–є. –Т–∞–Ї—Ж–Є–љ–∞—Ж–Є—П –њ—А–Є–≤–Њ–і–Є–ї–∞ –Ї –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–≤–µ—А—Е—Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г—О—Й–Є—Е –Ш–Ы-15 –Ї–ї–µ—В–Њ–Ї-–Љ–Є—И–µ–љ–µ–є, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ —Б–љ–Є–ґ–µ–љ–Є—О —З–Є—Б–ї–∞ —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г—О—Й–Є—Е –Ш–Ы-15 –Ї–ї–µ—В–Њ–Ї –Є –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤ –≤ –Ї—А–Њ–≤–Є –Є —Б–µ–ї–µ–Ј–µ–љ–Ї–µ, –∞ —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–µ–љ–Є—О –Њ—В–љ–Њ—И–µ–љ–Є—П CD4/CD8.
E. Fisman et al. [41] –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ –≤–∞–Ї—Ж–Є–љ–∞—Ж–Є—П –њ—А–Њ—В–Є–≤ –Ш–Ы-15 —Г–Љ–µ–љ—М—И–Є–ї–∞ —А–∞–Ј–Љ–µ—А —Г—З–∞—Б—В–Ї–Њ–≤ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ —Г LDLr-/- –Љ—Л—И–µ–є.
S. Bulfone-Paus [42] –і–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Ш–Ы-15 —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –≤—Л–ґ–Є–≤–∞–љ–Є—О –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л—Е –Ґ-–Ї–Є–ї–ї–µ—А–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —Г—З–∞—Б—В–≤—Г—О—В –≤–Њ –≤—А–Њ–ґ–і–µ–љ–љ—Л—Е –Є –∞–і–∞–њ—В–Є–≤–љ—Л—Е –Є–Љ–Љ—Г–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є—П—Е –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞.
C. Gokkusu et al. [43] –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є 5 –Њ–і–љ–Њ–љ—Г–Ї–ї–µ–Њ—В–Є–і–љ—Л—Е –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ–Њ–≤ (SNP) –≤ –≥–µ–љ–µ –Ш–Ы-15 –Є —Г—А–Њ–≤–љ–Є –Ш–Ы-15 —Г 102 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Ъ–°, 102 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б—В–∞–±–Є–ї—М–љ–Њ–є –Ш–С–° –Є 162 –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤. –Ш–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Њ –њ—П—В—М SNP –≤ –≥–µ–љ–µ –Ш–Ы-15: G367A, C267T, A14035T, C13687A –Є A10504G. –£—А–Њ–≤–љ–Є –Ш–Ы-15 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –±—Л–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤—Л—И–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–∞–Ї —Б –Ю–Ъ–°, —В–∞–Ї –Є —Б–Њ —Б—В–∞–±–Є–ї—М–љ—Л–Љ —В–µ—З–µ–љ–Є–µ–Љ –Ш–С–° –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ї–Є—Ж–∞–Љ–Є –Є–Ј –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –≤–∞—А–Є–∞–љ—В—Л –≥–µ–љ–∞ –Ш–Ы-15 –Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ш–Ы-15 –±—Л–ї–Є –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ—Л —Б –Ш–С–°. –Р–≤—В–Њ—А—Л —Б–і–µ–ї–∞–ї–Є –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ, —З—В–Њ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–∞—П –Є–Ј–Љ–µ–љ—З–Є–≤–Њ—Б—В—М –≥–µ–љ–∞ –Ш–Ы-15 –Є —Г—А–Њ–≤–µ–љ—М –Ш–Ы-15 –≤–ї–Є—П—О—В –љ–∞ —А–Є—Б–Ї –Ш–С–°.
–У—А—Г–њ–њ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ K. Ameri [44] –њ–Њ–Ї–∞–Ј–∞–ї–∞, —З—В–Њ –≤–≤–µ–і–µ–љ–Є–µ –Ш–Ы-15 –Љ–Њ–ґ–µ—В —Г–ї—Г—З—И–∞—В—М —Д—Г–љ–Ї—Ж–Є—О —Б–µ—А–і—Ж–∞ —Г –Љ—Л—И–µ–є –њ–Њ—Б–ї–µ –Ш–Ь –Ј–∞ —Б—З–µ—В —Б–љ–Є–ґ–µ–љ–Є—П –≥–Є–±–µ–ї–Є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В–Њ–≤, —Г–Љ–µ–љ—М—И–µ–љ–Є—П —А–∞–Ј–Љ–µ—А–∞ —А—Г–±—Ж–∞ –Є —Г–ї—Г—З—И–µ–љ–Є—П –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є. –≠—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –≤ –њ–Њ–ї—М–Ј—Г —В–Њ–≥–Њ, —З—В–Њ –Ш–Ы-15 –Є–≥—А–∞–µ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О —А–Њ–ї—М –њ—А–Є –Ш–Ь.
E. Dozio et al. [45] –Њ–њ—А–µ–і–µ–ї—П–ї–Є –Ш–Ы-15 –Є –Ш–Ы-15Rќ± —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–С–° –Є —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —В–Є–њ–∞–Љ–Є –Њ–ґ–Є—А–µ–љ–Є—П. –С–µ–ї–Ї–Є –Ш–Ы-15 –Є –Ш–Ы-15Rќ± –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ –Њ–њ—А–µ–і–µ–ї—П–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О —В–≤–µ—А–і–Њ—Д–∞–Ј–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞. –≠–Ї—Б–њ—А–µ—Б—Б–Є—О –≥–µ–љ–Њ–≤ –Ш–Ы-15 –Є –Ш–Ы-15Rќ± –≤ —Н–њ–Є–Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є (–≠–Ц–Ґ) –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О —Ж–≤–µ—В–љ—Л—Е –Љ–Є–Ї—А–Њ—З–Є–њ–Њ–≤. –Ґ–Њ–ї—Й–Є–љ—Г –≠–Ц–Ґ –Є–Ј–Љ–µ—А—П–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О —Н—Е–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є–Є (–≠—Е–Њ–Ъ–У). –£—А–Њ–≤–љ–Є –Ш–Ы-15 –Є –Ш–Ы-15Rќ± –≤ –Ї—А–Њ–≤–Є –±—Л–ї–Є –≤—Л—И–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–С–°, —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Ш–С–°. –£—А–Њ–≤–µ–љ—М –Ш–Ы-15 –±—Л–ї –≤—Л—И–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–С–° –Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–Љ –Њ–ґ–Є—А–µ–љ–Є–µ–Љ (–Р–Ю). –Я–Њ–≤—Л—И–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ш–Ы-15Rќ± –љ–∞–±–ї—О–і–∞–ї—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–С–° –Ї–∞–Ї —Б –Р–Ю, —В–∞–Ї –Є –±–µ–Ј –Р–Ю. –°–Њ–≥–ї–∞—Б–љ–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –≠–Ц–Ґ —П–≤–Є–ї–∞—Б—М –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –Ш–Ы-15 –Є –Ш–Ы-15Rќ±, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є—Е —Н–Ї—Б–њ—А–µ—Б—Б–Є—П –±—Л–ї–∞ –≤—Л—И–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–С–° –Є —Г–≤–µ–ї–Є—З–µ–љ–љ–Њ–є —В–Њ–ї—Й–Є–љ–Њ–є –≠–Ц–Ґ.
–°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ M. Kaibe et al. [46] –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Њ–і–љ–Њ–Љ–µ—А–љ–Њ–≥–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ —Г—А–Њ–≤–љ–Є –Ш–Ы-15, –≤—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ –°-—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ (hs-CRP), –∞–Ј–Њ—В–∞ –Љ–Њ—З–µ–≤–Є–љ—Л, –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞, —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Є —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є, –∞ —В–∞–Ї–ґ–µ –Ш–Ь–Ґ —Б–≤—П–Ј–∞–љ—Л —Б –Ш–С–°. –Я—А–Є –Љ–љ–Њ–≥–Њ–Љ–µ—А–љ–Њ–Љ –ї–Њ–≥–Є—Б—В–Є—З–µ—Б–Ї–Њ–Љ —А–µ–≥—А–µ—Б—Б–Є–Њ–љ–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ —В–Њ–ї—М–Ї–Њ —Г—А–Њ–≤–љ–Є –Ш–Ы-15 –Є hs-CRP –±—Л–ї–Є —Б–≤—П–Ј–∞–љ—Л —Б –Ш–С–°.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [47] —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —А–Є—Б–Ї –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –°–°–Ч —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ –≤ 2 —А–∞–Ј–∞ —Г –ї–Є—Ж —Б –≤–Є—А—Г—Б–Њ–Љ –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ (–Т–Ш–І-–Є–љ—Д–µ–Ї—Ж–Є–µ–є). –Ґ–∞–Ї, S. Panigrahi et al. [48] –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є —А–Њ–ї—М –Ґ-–Ї–ї–µ—В–Њ–Ї CD8 –њ—А–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–µ –≤ –Љ–Њ–і–µ–ї–Є –Т–Ш–І-–Є–љ—Д–µ–Ї—Ж–Є–Є –љ–∞ –њ—А–Є–Љ–∞—В–∞—Е –Є —Г –љ–µ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Т–Ш–І –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є. –Ґ–∞–Ї–ґ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є —Б—В—А–µ–Љ–Є–ї–Є—Б—М –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М —Д–∞–Ї—В–Њ—А—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є, —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—О –Є —А–µ–Ї—А—Г—В–Є—А–Њ–≤–∞–љ–Є—О –Ґ-–Ї–ї–µ—В–Њ–Ї CX3CR1+ CD8. –С—Л–ї–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Н–Ї—Б–њ—А–µ—Б—Б–Є—П CX3CL1 –Є –Ш–Ы-15 –Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ґ-–Ї–ї–µ—В–Њ–Ї CD8 –≤ –∞–Њ—А—В–∞—Е –Љ–∞–Ї–∞–Ї. –Ґ–∞–Ї–ґ–µ –∞–≤—В–Њ—А—Л –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—Г–і–∞—Е –Т–Ш–І-–љ–µ–Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –ї—О–і–µ–є. –С—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ—Л–є TNF —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –њ—А–Њ–і—Г–Ї—Ж–Є—О –Є –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ CX3CL1 –Є –±–Є–Њ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Ш–Ы-15 –Є–Ј —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –∞–Њ—А—В—Л. –Ш–Ы-15, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–є —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є CX3CR1 –Є —Б–Є–љ—В–µ–Ј—Г TNF CD8 T-–Ї–ї–µ—В–Ї–∞–Љ–Є, –∞ –Њ–±—А–∞–±–Њ—В–∞–љ–љ—Л–µ –Ш–Ы-15 CD8 T-–Ї–ї–µ—В–Ї–Є –њ—А–Њ—П–≤–ї—П—О—В —Г—Б–Є–ї–µ–љ–љ—Г—О CX3CL1-–Ј–∞–≤–Є—Б–Є–Љ—Г—О —Е–µ–Љ–Њ–∞—В—В—А–∞–Ї—Ж–Є—О –Ї —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л–Љ –Ї–ї–µ—В–Ї–∞–Љ in vitro.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —А–Њ–ї—М –Ш–Ы-15 –њ—А–Є –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є–Є –Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–µ —П–≤–ї—П–µ—В—Б—П –і–Њ –Ї–Њ–љ—Ж–∞ –љ–µ —П—Б–љ–Њ–є –Є –љ—Г–ґ–і–∞–µ—В—Б—П –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –Є–Ј—Г—З–µ–љ–Є–Є.
–†–Њ–ї—М –Ш–Ы-15 –≤ –≥–ї–Є–Ї–Њ–Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–µ
–Ш–љ—В–µ—А–ї–µ–є–Ї–Є–љ 15 —П–≤–ї—П–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –¶–Ъ, –љ–Њ –Є –Љ–Є–Њ–Ї–Є–љ–Њ–Љ. –Ь–Є–Њ–Ї–Є–љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В—М –¶–Ъ, —Б–µ–Ї—А–µ—В–Є—А—Г–µ–Љ–Њ–≥–Њ —Б–Ї–µ–ї–µ—В–љ—Л–Љ–Є –Љ—Л—И—Ж–∞–Љ–Є. –Я–Њ–Љ–Є–Љ–Њ –Ш–Ы-15, —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ –Љ–Є–Њ–Ї–Є–љ–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї –Ш–Ы-6, –Є—А–Є–Ј–Є–љ –Є –і–µ–Ї–Њ—А–Є–љ [49]. –°–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Ї–µ–ї–µ—В–љ—Л—Е –Љ—Л—И—Ж —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –њ—А–Њ–і—Г–Ї—Ж–Є—О –Љ–Є–Њ–Ї–Є–љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є —Б—В–Є–Љ—Г–ї–Є—А—Г—О—В —В—А–∞–љ—Б–њ–Њ—А—В –≥–ї—О–Ї–Њ–Ј—Л [50].
–Ґ–∞–Ї, H. Yang et al. [51] –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –і–Є–µ—В–∞ —Б –≤—Л—Б–Њ–Ї–Є–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ –ґ–Є—А–Њ–≤ –≤—Л–Ј—Л–≤–∞–µ—В —Б–љ–Є–ґ–µ–љ–Є–µ —А–µ–≥—Г–ї—П—Ж–Є–Є –Ш–Ы-15 –≤ –Љ—Л—И—Ж–∞—Е –Є –Ш–Ы-15R –≤ –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є. –§–Є–Ј–Є—З–µ—Б–Ї–Є–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П –Љ–Њ–≥—Г—В —Г–Љ–µ–љ—М—И–Є—В—М –Њ–ґ–Є—А–µ–љ–Є–µ –Є –і–∞–љ–љ—Г—О –љ–µ–≥–∞—В–Є–≤–љ—Г—О —А–µ–≥—Г–ї—П—Ж–Є—О. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ M. Yargic et al. [52] —Г—А–Њ–≤–µ–љ—М –Ш–Ы-15 –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –њ–Њ–≤—Л—И–∞–ї—Б—П –њ–Њ—Б–ї–µ –Є–љ—В–µ–љ—Б–Є–≤–љ—Л—Е —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е —Г–њ—А–∞–ґ–љ–µ–љ–Є–є.
–£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ [53], —З—В–Њ –Ш–Ы-15 –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –∞–љ–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —Б–Ї–µ–ї–µ—В–љ—Л–µ –Љ—Л—И—Ж—Л, —Б–љ–Є–ґ–∞—П —Б–Ї–Њ—А–Њ—Б—В—М –њ—А–Њ—В–µ–Њ–ї–Є–Ј–∞ –љ–∞ –Ї–ї–µ—В–Њ—З–љ–Њ–Љ —Г—А–Њ–≤–љ–µ. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –Њ–љ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –њ–Њ–≥–ї–Њ—Й–µ–љ–Є–µ –≥–ї—О–Ї–Њ–Ј—Л —Б–Ї–µ–ї–µ—В–љ—Л–Љ–Є –Љ—Л—И—Ж–∞–Љ–Є –Є –љ–∞ –Ї–ї–µ—В–Њ—З–љ–Њ–Љ —Г—А–Њ–≤–љ–µ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –±—Г–і—Г—Й–µ–Љ –Ш–Ы-15 –Љ–Њ–ґ–µ—В —Б—В–∞—В—М –∞–љ—В–Є–і–Є–∞–±–µ—В–Њ–≥–µ–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ.
–Э–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞ T. Fujimoto et al. [54], L. Nadeau et al. [55] –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є, —З—В–Њ —Б–≤–µ—А—Е—Н–Ї—Б–њ—А–µ—Б—Б–Є—П –Ш–Ы-15 –≤ —Б–Ї–µ–ї–µ—В–љ—Л—Е –Љ—Л—И—Ж–∞—Е –Љ—Л—И–µ–є –Љ–Њ–ґ–µ—В —Г–ї—Г—З—И–∞—В—М –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –≥–ї—О–Ї–Њ–Ј—Л —З–µ—А–µ–Ј –њ—Г—В—М –Р–Ь–§-–∞–Ї—В–Є–≤–Є—А—Г–µ–Љ–Њ–є –њ—А–Њ—В–µ–Є–љ–Ї–Є–љ–∞–Ј—Л. –Т —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї J. Krolopp et al. [56] –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ –Є–Љ–µ–љ–љ–Њ –њ—Г—В—М –ѓ–љ—Г—Б-–Ї–Є–љ–∞–Ј–∞ 3/STAT3 —А–µ–≥—Г–ї–Є—А—Г–µ—В –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –≥–ї—О–Ї–Њ–Ј—Л. –Р L. Quinn et al. [57] –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є, —З—В–Њ —Б–≤–µ—А—Е—Н–Ї—Б–њ—А–µ—Б—Б–Є—П –Ш–Ы-15 —Г–Љ–µ–љ—М—И–∞–µ—В –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М.
Y. Duan et al. [58] –Њ–њ–Є—Б–∞–ї–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Ш–Ы-15: —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–Њ—В–µ—А–Є –ґ–Є—А–Њ–≤–Њ–є –Љ–∞—Б—Б—Л –Є –Њ–±—Й–µ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞, —Г–ї—Г—З—И–µ–љ–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –ї–Є–њ–Є–і–Њ–≤ –Є –≥–ї—О–Ї–Њ–Ј—Л, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ –±–µ–ї–Њ–є –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Љ–Є—В–Њ—Е–Њ–љ–і—А–Є–∞–ї—М–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –њ—А–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ. –Т—Б–ї–µ–і—Б—В–≤–Є–µ —Н—В–Њ–≥–Њ –Ш–Ы-15 –і–∞–µ—В –±–Њ–ї—М—И–Є–µ –љ–∞–і–µ–ґ–і—Л –≤ –∞—Б–њ–µ–Ї—В–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є, –ї–µ—З–µ–љ–Є—П –Њ–ґ–Є—А–µ–љ–Є—П –Є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ 2 —В–Є–њ–∞.
–Ш–Ы-15 –Є —Д–Є–±—А–Є–ї–ї—П—Ж–Є—П –њ—А–µ–і—Б–µ—А–і–Є–є
–Т–Њ—Б–њ–∞–ї–µ–љ–Є–µ –Є–≥—А–∞–µ—В –Ј–љ–∞—З–Є–Љ—Г—О —А–Њ–ї—М –≤ –Є–љ–Є—Ж–Є–∞—Ж–Є–Є, –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–Є –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–Є —Д–Є–±—А–Є–ї–ї—П—Ж–Є–Є –њ—А–µ–і—Б–µ—А–і–Є–є (–§–Я). –Т –і–Њ—Б—В—Г–њ–љ–Њ–є –љ–∞–Љ –ї–Є—В–µ—А–∞—В—Г—А–µ –љ–∞–є–і–µ–љ–Њ –ї–Є—И—М –Њ–і–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –њ–Њ—Б–≤—П—Й–µ–љ–љ–Њ–µ –Є–Ј—Г—З–µ–љ–Є—О —А–Њ–ї–Є –Ш–Ы-15 –њ—А–Є –§–Я. A. Borowiec et al. [59] –њ—А–Њ–≤–µ–ї–Є –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Г—О –Њ—Ж–µ–љ–Ї—Г –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Д–Њ—А–Љ–∞–Љ–Є –§–Я. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 158 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ–Њ–є/–њ–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–µ–є –§–Я (–Є–Ј –љ–Є—Е 87 (55,1%) –Љ—Г–ґ—З–Є–љ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 65,8¬±9,6 –≥–Њ–і–∞) –±–µ–Ј —Б—В—А—Г–Ї—В—Г—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Б–µ—А–і—Ж–∞. –Я–∞—А–∞–Љ–µ—В—А—Л –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П: –ї–µ–є–Ї–Њ—Ж–Є—В—Л, —Б–Ї–Њ—А–Њ—Б—В—М –Њ—Б–µ–і–∞–љ–Є—П —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ (–°–Ю–≠), hs-CRP, –Ш–Ы-6, –Ш–Ы-15 –Є TNF-ќ± –Є–Ј–Љ–µ—А—П–ї–Є –Є—Б—Е–Њ–і–љ–Њ –Є —З–µ—А–µ–Ј 1 –≥–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —З–∞—Б—В—Л–µ —Н–њ–Є–Ј–Њ–і—Л –§–Я, —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤, –°–Ю–≠ –Є hs-CRP –Є—Б—Е–Њ–і–љ–Њ –Є –њ–Њ—Б–ї–µ –љ–∞–±–ї—О–і–µ–љ–Є—П –±—Л–ї–Є –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–Њ—А–Љ—Л. –°—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤, –°–Ю–≠ –Є hs-CRP –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —В–Є–њ–Њ–≤ –§–Я –љ–µ –±—Л–ї–Њ. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е —А–∞–Ј–≤–Є–ї–∞—Б—М –њ–Њ—Б—В–Њ—П–љ–љ–∞—П —Д–Њ—А–Љ–∞ –§–Я (n=14), –Є—Б—Е–Њ–і–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є hs-CRP –±—Л–ї–Є –≤—Л—И–µ. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ–Њ—Б–ї–µ 1 –≥–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П —Н—В–Є —А–∞–Ј–ї–Є—З–Є—П –љ–µ –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є. –°—А–µ–і–Є –≤—Б–µ—Е –Є–Ј—Г—З–µ–љ–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ —В–Њ–ї—М–Ї–Њ –Ш–Ы-15 –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Ї–Њ—А—А–µ–ї–Є—А–Њ–≤–∞–ї —Б –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ —Н–њ–Є–Ј–Њ–і–Њ–≤ –§–Я. –Р–≤—В–Њ—А—Л —А–µ–Ј—О–Љ–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–∞—П —А–Њ–ї—М –Ш–Ы-15 –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–∞—А–Ї–µ—А–∞ –§–Я –Ј–∞—Б–ї—Г–ґ–Є–≤–∞–µ—В –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є–Ј—Г—З–µ–љ–Є—П.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Т —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –Љ–Є—А–µ –Њ—Б—В–∞–µ—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ –њ–Њ–Є—Б–Ї –Є –Є–Ј—Г—З–µ–љ–Є–µ –љ–Њ–≤—Л—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Љ–∞—А–Ї–µ—А–Њ–≤, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –њ–Њ–Љ–Њ–≥–∞—В—М —А–∞–љ–љ–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –°–°–Ч, —Б–ї—Г–ґ–Є—В—М –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–Љ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–Њ–Љ –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є, —П–≤–ї—П—В—М—Б—П –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Е–Њ–і–Њ–≤ –Є –Ј–љ–∞—З–Є–Љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ —Б—В—А–∞—В–Є—Д–Є–Ї–∞—Ж–Є–Є —А–Є—Б–Ї–∞. –Я–Њ—П–≤–ї—П–µ—В—Б—П –≤—Б–µ –±–Њ–ї—М—И–µ –і–∞–љ–љ—Л—Е, –њ–Њ–і—З–µ—А–Ї–Є–≤–∞—О—Й–Є—Е —Ж–µ–љ–љ–Њ—Б—В—М –Ш–Ы-15 –≤ –Ї–∞—З–µ—Б—В–≤–µ –љ–Њ–≤–Њ–≥–Њ –±–Є–Њ–Љ–∞—А–Ї–µ—А–∞ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –Њ—Ж–µ–љ–Ї–Є –њ—А–Њ–≥–љ–Њ–Ј–∞ —Г –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –†–Њ–ї—М –Ш–Ы-15 –њ—А–Є –°–°–Ч –≤–µ—Б—М–Љ–∞ –Є–љ—В–µ—А–µ—Б–љ–∞ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –µ–≥–Њ –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ю–і–љ–∞–Ї–Њ –љ–µ –≤—Б–µ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –Љ–Њ–Љ–µ–љ—В—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–∞—О—В –Њ–і–љ–Њ–Ј–љ–∞—З–љ—Г—О –Њ—Ж–µ–љ–Ї—Г —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ш–Ы-15 –Ї–∞–Ї –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–∞—А–Ї–µ—А–∞ –°–°–Ч. –Ю–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є, –њ—А–µ–і–Є–Ї—В–Є–≤–љ–Њ–є –Є, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —А–Њ–ї–Є –і–∞–љ–љ–Њ–≥–Њ –Љ–∞—А–Ї–µ—А–∞ –±—Г–і–µ—В –њ–Њ–ї—Г—З–µ–љ–Њ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –±—Г–і—Г—Й–Є—Е –Ї—А—Г–њ–љ–Њ–Љ–∞—Б—И—В–∞–±–љ—Л—Е –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є.












