–í–≤–Ķ–ī–Ķ–Ĺ–ł–Ķ
–Ę—É–Ī–Ķ—Ä–ļ—É–Ľ–Ķ–∑ –Ľ–Ķ–≥–ļ–ł—Ö (–Ę–Ď) —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —Ā–ĺ—Ü–ł–į–Ľ—Ć–Ĺ–ĺ –∑–Ĺ–į—á–ł–ľ–ĺ–Ļ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ķ–Ļ, –ļ–ĺ—ā–ĺ—Ä–į—Ź –Ņ–Ķ—Ä–Ķ–ī–į–Ķ—ā—Ā—Ź –≤–ĺ–∑–ī—É—ą–Ĺ–ĺ-–ļ–į–Ņ–Ķ–Ľ—Ć–Ĺ—č–ľ –Ņ—É—ā–Ķ–ľ. –ó–į—Ä–į–∂–Ķ–Ĺ–ł—é –Ę–Ď –Ņ–ĺ–ī–≤–Ķ—Ä–∂–Ķ–Ĺ—č —Ā–ĺ—Ü–ł–į–Ľ—Ć–Ĺ–ĺ –Ĺ–Ķ–∑–į—Č–ł—Č–Ķ–Ĺ–Ĺ—č–Ķ —Ā–Ľ–ĺ–ł –Ĺ–į—Ā–Ķ–Ľ–Ķ–Ĺ–ł—Ź, –Ņ—Ä–ł –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–ł –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ł–Ľ–ł –Ņ–ĺ–∑–ī–Ĺ–ĺ –Ĺ–į—á–į—ā–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł —ć—ā–ĺ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ķ –≤–Ķ–ī–Ķ—ā –ļ –ł–Ĺ–≤–į–Ľ–ł–ī–ł–∑–į—Ü–ł–ł –ł –Ņ—Ä–Ķ–∂–ī–Ķ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ–Ļ —Ā–ľ–Ķ—Ä—ā–Ĺ–ĺ—Ā—ā–ł [1‚Äď3].
–Ě–Ķ—Ā–ľ–ĺ—ā—Ä—Ź –Ĺ–į –≤—č—Ā–ĺ–ļ—É—é –∑–Ĺ–į—á–ł–ľ–ĺ—Ā—ā—Ć —ć—ā–ĺ–Ļ –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–ł, –Ĺ–Ķ–Ľ—Ć–∑—Ź –Ņ—Ä–ł—É–ľ–Ķ–Ĺ—Ć—ą–į—ā—Ć —Ä–ĺ–Ľ—Ć –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –ł –Ņ–ĺ–Ľ–ł–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ, –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ —É—Ö—É–ī—ą–į—é—Č–ł—Ö –ł –Ī–Ķ–∑ —ā–ĺ–≥–ĺ –Ĺ–Ķ–Ī–Ľ–į–≥–ĺ–Ņ—Ä–ł—Ź—ā–Ĺ—č–Ļ –Ņ—Ä–ĺ–≥–Ĺ–ĺ–∑. –ö–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ—Ā—ā—Ć, —Ā–ĺ–≥–Ľ–į—Ā–Ĺ–ĺ –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł—é –ź.–†. –§–į–Ļ–Ĺ—ą—ā–Ķ–Ļ–Ĺ–į, –Ķ—Ā—ā—Ć –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ –ī–ĺ–Ņ–ĺ–Ľ–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł—Ź, –ļ–ĺ—ā–ĺ—Ä–ĺ–Ķ —Ā—É—Č–Ķ—Ā—ā–≤—É–Ķ—ā –ł–Ľ–ł –≤–ĺ–∑–Ĺ–ł–ļ–į–Ķ—ā –Ĺ–į —Ą–ĺ–Ĺ–Ķ —ā–Ķ–ļ—É—Č–Ķ–≥–ĺ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź [4]. –°–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–į—Ź –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł—Ź —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ę–Ď –≤—Ā—ā—Ä–Ķ—á–į–Ķ—ā—Ā—Ź –Ņ—Ä–ł–ľ–Ķ—Ä–Ĺ–ĺ –≤ 51% —Ā–Ľ—É—á–į–Ķ–≤. –ė–∑ –Ĺ–ł—Ö —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ķ –≥–Ķ–Ņ–į—ā–ł—ā—č —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź—é—ā 38,9%, —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–į—Ź–ĺ–Ī—Ā—ā—Ä—É–ļ—ā–ł–≤–Ĺ–į—Ź –Ī–ĺ–Ľ–Ķ–∑–Ĺ—Ć –Ľ–Ķ–≥–ļ–ł—Ö (–•–ě–Ď–õ) ‚ÄĒ 37,8%, —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ-—Ā–ĺ—Ā—É–ī–ł—Ā—ā—č–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź (–°–°–ó) ‚ÄĒ 17,8%, —Ā–į—Ö–į—Ä–Ĺ—č–Ļ –ī–ł–į–Ī–Ķ—ā ‚ÄĒ 15,6%, –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –Ė–ö–Ę ‚ÄĒ 15,6% [5, 6]. –ö–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ—Ā—ā—Ć —Ā –•–ě–Ď–õ –ł –°–°–ó –∑–į–Ĺ–ł–ľ–į–Ķ—ā –≤—ā–ĺ—Ä–ĺ–Ķ –ł —ā—Ä–Ķ—ā—Ć–Ķ –ľ–Ķ—Ā—ā–ĺ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ —Ā—Ä–Ķ–ī–ł –≤—Ā–Ķ—Ö —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–ł—Ö –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–Ļ –Ņ—Ä–ł –Ę–Ď, –Ņ—Ä–ł—á–Ķ–ľ –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–į—Ź –Ī–ĺ–Ľ–Ķ–∑–Ĺ—Ć —Ā–Ķ—Ä–ī—Ü–į (–ė–Ď–°) —Ā—Ä–Ķ–ī–ł –°–°–ó —Ā—ā–ĺ–ł—ā –Ĺ–į –≤—ā–ĺ—Ä–ĺ–ľ –ľ–Ķ—Ā—ā–Ķ (12%) –Ņ–ĺ—Ā–Ľ–Ķ –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ –≥–ł–Ņ–Ķ—Ä—ā–Ķ–Ĺ–∑–ł–ł. –ö–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ–Ķ —Ā–ĺ—á–Ķ—ā–į–Ĺ–ł–Ķ –Ę–Ď —Ā –•–ě–Ď–õ –ł –ė–Ď–° —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź, –Ņ–ĺ —Ā—É—ā–ł, –ł–Ĺ–≤–į–Ľ–ł–ī–ł–∑–ł—Ä—É—é—Č–ł–ľ, –į –≤ –Ĺ–Ķ–ļ–ĺ—ā–ĺ—Ä—č—Ö —Ā–Ľ—É—á–į—Ź—Ö ‚ÄĒ –ł —Ā–ľ–Ķ—Ä—ā–Ķ–Ľ—Ć–Ĺ—č–ľ.
–ü–ĺ –Ľ–ł—ā–Ķ—Ä–į—ā—É—Ä–Ĺ—č–ľ –ī–į–Ĺ–Ĺ—č–ľ, –ĺ—ā 30% –ī–ĺ 45% –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ę–Ď –ł–ľ–Ķ—é—ā –•–ě–Ď–õ [7, 8]. –ü—Ä–ł –Ĺ–į–Ľ–ł—á–ł–ł –•–ě–Ď–õ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į —Ä–ł—Ā–ļ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –Ę–Ď —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ķ—ā—Ā—Ź –≤ 14,4 —Ä–į–∑–į [7]. –í —Ä—Ź–ī–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ļ –Ņ–ĺ–ļ–į–∑–į–Ĺ–ĺ, —á—ā–ĺ –Ņ—Ä–ł –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ—Ā—ā–ł –Ę–Ď –ł –•–ě–Ď–õ —Ā–ľ–Ķ—Ä—ā–Ĺ–ĺ—Ā—ā—Ć –Ņ–ĺ–≤—č—ą–į–Ľ–į—Ā—Ć –≤ 5 —Ä–į–∑ [8, 9], –Ņ—Ä–ł—á–Ķ–ľ –≤ –Ņ–ĺ–Ľ–ĺ–≤–ł–Ĺ–Ķ —Ā–Ľ—É—á–į–Ķ–≤ –ł–ľ–Ķ–Ľ–ł—Ā—Ć –Ķ—Č–Ķ –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č–Ķ –°–°–ó. –ü—Ä–ĺ–Ī–Ľ–Ķ–ľ–į –ł–∑–Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ę–Ď —É –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ĺ—Ā–ĺ–Ī–Ķ–Ĺ–Ĺ–ĺ –į–ļ—ā—É–į–Ľ—Ć–Ĺ–ĺ–Ļ –≤ —ć–Ņ–ł–ī–Ķ–ľ–ł–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł –Ĺ–Ķ–Ī–Ľ–į–≥–ĺ–Ņ—Ä–ł—Ź—ā–Ĺ—č—Ö –Ņ–ĺ –Ę–Ď —Ä–Ķ–≥–ł–ĺ–Ĺ–į—Ö, –ļ –ļ–ĺ—ā–ĺ—Ä—č–ľ –ĺ—ā–Ĺ–ĺ—Ā–ł—ā—Ā—Ź –°–ł–Ī–ł—Ä—Ā–ļ–ł–Ļ —Ą–Ķ–ī–Ķ—Ä–į–Ľ—Ć–Ĺ—č–Ļ –ĺ–ļ—Ä—É–≥, –ł —ā—Ä–Ķ–Ī—É–Ķ—ā –ī–į–Ľ—Ć–Ĺ–Ķ–Ļ—ą–Ķ–≥–ĺ –ł–∑—É—á–Ķ–Ĺ–ł—Ź.
–Ę–Ď, –•–ě–Ď–õ –ł –ė–Ď–°, –≤—Ā—ā—Ä–Ķ—á–į—Ź—Ā—Ć —É –ĺ–ī–Ĺ–ĺ–≥–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į, —Ź–≤–Ľ—Ź—é—ā—Ā—Ź –≤–∑–į–ł–ľ–Ĺ–ĺ –ĺ—ā—Ź–≥—á–į—é—Č–ł–ľ–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź–ľ–ł, –ļ–į–∂–ī–ĺ–Ķ –ł–∑ –ļ–ĺ—ā–ĺ—Ä—č—Ö –≤ —Ä–į–≤–Ĺ–ĺ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł –ľ–ĺ–∂–Ķ—ā –ĺ—ā—Ä–ł—Ü–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ –≤–Ľ–ł—Ź—ā—Ć –Ĺ–į —ā–Ķ—á–Ķ–Ĺ–ł–Ķ –ī—Ä—É–≥–ĺ–≥–ĺ [3, 10].
–ě–ī–Ĺ–į –ł–∑ —ā–Ķ–ĺ—Ä–ł–Ļ –≤–∑–į–ł–ľ–Ĺ–ĺ–≥–ĺ –ĺ—ā—Ź–≥–ĺ—Č–Ķ–Ĺ–ł—Ź ‚ÄĒ —ć—ā–ĺ —ā–Ķ–ĺ—Ä–ł—Ź —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ –ī–ł—Ā—Ą—É–Ĺ–ļ—Ü–ł–ł [11]. –Ę–ĺ–ļ—Ā–ł–ļ–ĺ-–į–Ľ–Ľ–Ķ—Ä–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –Ņ—Ä–ł –Ę–Ď —Ö–į—Ä–į–ļ—ā–Ķ—Ä–ł–∑—É—é—ā—Ā—Ź –Ņ–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ–ľ —Ā–ĺ—Ā—É–ī–ł—Ā—ā—č—Ö –ľ–ł–ļ—Ä–ĺ—Ü–ł—Ä–ļ—É–Ľ—Ź—ā–ĺ—Ä–Ĺ—č—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ —Ā –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–ľ –Ņ—Ä–Ķ–ĺ–Ī–Ľ–į–ī–į–Ĺ–ł–Ķ–ľ —ć–ļ—Ā—Ā—É–ī–į—ā–ł–≤–Ĺ–ĺ–Ļ —ā–ļ–į–Ĺ–Ķ–≤–ĺ–Ļ —Ä–Ķ–į–ļ—Ü–ł–ł –ł, –ļ–į–ļ —Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–Ķ, —Ä–į–∑–≤–ł—ā–ł–Ķ–ľ –ī–ł—Ā—ā—Ä–ĺ—Ą–ł—á–Ķ—Ā–ļ–ł—Ö –ł –Ĺ–Ķ–ļ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ł—Ö –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–ĺ–≤ –≤ —Ā–ĺ—Ā—É–ī–į—Ö. –°–ĺ—Ā—É–ī–ł—Ā—ā—č–Ļ —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł–Ļ –Ľ–Ķ–≥–ļ–ł—Ö –≤ –Ĺ–ĺ—Ä–ľ–Ķ –Ņ—Ä–ĺ–ī—É—Ü–ł—Ä—É—é—ā –ľ–ĺ—Č–Ĺ—č–Ķ –≤–į–∑–ĺ–ī–ł–Ľ–į—ā–į—ā–ĺ—Ä—č, —Ä–Ķ–≥—É–Ľ–ł—Ä—É—é—Č–ł–Ķ —Ä–į–Ī–ĺ—ā—É —Ā–ĺ–ļ—Ä–į—ā–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –≥–Ľ–į–ī–ļ–ĺ–ľ—č—ą–Ķ—á–Ĺ—č—Ö –ļ–Ľ–Ķ—ā–ĺ–ļ. –ü—Ä–ł –į–Ľ—Ć–≤–Ķ–ĺ–Ľ—Ź—Ä–Ĺ–ĺ–Ļ –≥–ł–Ņ–ĺ–ļ—Ā–ł–ł –ł –Ņ–į–ī–Ķ–Ĺ–ł–ł –Ņ–į—Ä—Ü–ł–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ĺ–į–Ņ—Ä—Ź–∂–Ķ–Ĺ–ł—Ź –ļ–ł—Ā–Ľ–ĺ—Ä–ĺ–ī–į –≤ –ļ—Ä–ĺ–≤–ł –Ĺ–į—Ā—ā—É–Ņ–į–Ķ—ā —É—Ö—É–ī—ą–Ķ–Ĺ–ł–Ķ –ĺ—Ā–≤–ĺ–Ī–ĺ–∂–ī–Ķ–Ĺ–ł—Ź —Ä–Ķ–Ľ–į–ļ—Ā–ł—Ä—É—é—Č–Ķ–≥–ĺ —Ą–į–ļ—ā–ĺ—Ä–į, —á—ā–ĺ –ĺ–ļ–į–∑—č–≤–į–Ķ—ā –ĺ—ā—Ä–ł—Ü–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ —Ä–Ķ–≥—É–Ľ–ł—Ä—É—é—Č–Ķ–Ķ –≤–Ľ–ł—Ź–Ĺ–ł–Ķ –Ĺ–į —Ā–ĺ—Ā—É–ī—č [11].
–°–ĺ–≥–Ľ–į—Ā–Ĺ–ĺ –ī—Ä—É–≥–ĺ–Ļ —ā–Ķ–ĺ—Ä–ł–ł –≤—č–ī–Ķ–Ľ—Ź—é—ā –ł–Ĺ—č–Ķ –Ņ–į—ā–ĺ—Ą–ł–∑–ł–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ —Ą–į–ļ—ā–ĺ—Ä—č, –Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–ĺ–ľ –ļ–ĺ—ā–ĺ—Ä—č—Ö —ā—É–Ī–Ķ—Ä–ļ—É–Ľ–Ķ–∑–Ĺ–į—Ź –ł–Ĺ—Ą–Ķ–ļ—Ü–ł—Ź –ļ–į–ļ —Ā–ł—Ā—ā–Ķ–ľ–Ĺ—č–Ļ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā –ľ–ĺ–∂–Ķ—ā –Ņ—Ä–ł–≤–Ķ—Ā—ā–ł –ļ –°–°–ó [12]. –ě–Ĺ–ł –≤–ļ–Ľ—é—á–į—é—ā –≤ —Ā–Ķ–Ī—Ź —Ā–ł—Ā—ā–Ķ–ľ–Ĺ–ĺ–Ķ –≤–ĺ—Ā–Ņ–į–Ľ–Ķ–Ĺ–ł–Ķ, –ļ–ĺ—ā–ĺ—Ä–ĺ–Ķ –Ņ—Ä–ł —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–ľ —ā–Ķ—á–Ķ–Ĺ–ł–ł —Ā–ĺ –≤—Ä–Ķ–ľ–Ķ–Ĺ–Ķ–ľ –Ņ—Ä–ł–≤–ĺ–ī–ł—ā –ļ –ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł—é –į—ā–Ķ—Ä–ĺ—Ā–ļ–Ľ–Ķ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ł—Ö –Ī–Ľ—Ź—ą–Ķ–ļ –ł –ł—Ö —Ä–į–∑—Ä—č–≤—É [12]. –í —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł, –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č —É—Ā–ł–Ľ–ł–≤–į—é—ā —Ā–Ķ–ļ—Ä–Ķ—Ü–ł—é —Ä–į—Ā—ā–≤–ĺ—Ä–ł–ľ—č—Ö –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ –į–ī–≥–Ķ–∑–ł–ł –Ľ–Ķ–Ļ–ļ–ĺ—Ü–ł—ā–ĺ–≤, –ļ–ĺ—ā–ĺ—Ä—č–Ķ —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É—é—ā –Ņ—Ä–ł–ļ—Ä–Ķ–Ņ–Ľ–Ķ–Ĺ–ł—é –ľ–ĺ–Ĺ–ĺ—Ü–ł—ā–ĺ–≤ –ļ —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł–į–Ľ—Ć–Ĺ—č–ľ –ļ–Ľ–Ķ—ā–ļ–į–ľ [13]. –°—á–ł—ā–į–Ķ—ā—Ā—Ź, —á—ā–ĺ –Ņ–ĺ—Ā–Ľ–Ķ–ī—É—é—Č–į—Ź —ā—Ä–į–Ĺ—Ā—Ą–ĺ—Ä–ľ–į—Ü–ł—Ź –ľ–ĺ–Ĺ–ĺ—Ü–ł—ā–ĺ–≤ –≤ –ľ–į–ļ—Ä–ĺ—Ą–į–≥–ł –≤ —Ā–ĺ—á–Ķ—ā–į–Ĺ–ł–ł —Ā –Ņ–ĺ–≥–Ľ–ĺ—Č–Ķ–Ĺ–ł–Ķ–ľ —Ö–ĺ–Ľ–Ķ—Ā—ā–Ķ—Ä–ł–Ĺ–ĺ–≤—č—Ö –Ľ–ł–Ņ–ĺ–Ņ—Ä–ĺ—ā–Ķ–ł–Ĺ–ĺ–≤ –ĺ–ī–Ĺ–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ –ł–Ĺ–ł—Ü–ł–ł—Ä—É–Ķ—ā –ł —É—Ā–ļ–ĺ—Ä—Ź–Ķ—ā —Ä–ĺ—Ā—ā –į—ā–Ķ—Ä–ĺ—Ā–ļ–Ľ–Ķ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –∂–ł—Ä–ĺ–≤–ĺ–Ļ –Ī–Ľ—Ź—ą–ļ–ł. –ü–ĺ –ľ–Ķ—Ä–Ķ –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –į—ā–Ķ—Ä–ĺ—Ā–ļ–Ľ–Ķ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ł—Ö –Ī–Ľ—Ź—ą–Ķ–ļ –ĺ–Ĺ–ł —Ā—ā–į–Ĺ–ĺ–≤—Ź—ā—Ā—Ź –Ņ–ĺ–ļ—Ä—č—ā—č–ľ–ł ¬ę—ą–į–Ņ–ļ–ĺ–Ļ¬Ľ –≥–Ľ–į–ī–ļ–ĺ–ľ—č—ą–Ķ—á–Ĺ—č—Ö –ļ–Ľ–Ķ—ā–ĺ–ļ –ł –Ī–ĺ–≥–į—ā–ĺ–Ļ –ļ–ĺ–Ľ–Ľ–į–≥–Ķ–Ĺ–ĺ–ľ –ľ–į—ā—Ä–ł—Ü—č, –ļ–ĺ—ā–ĺ—Ä–į—Ź –ľ–ĺ–∂–Ķ—ā —Ä–į–∑—Ä—č–≤–į—ā—Ć—Ā—Ź –Ņ—Ä–ł —Ā—Ä–į–Ī–į—ā—č–≤–į–Ĺ–ł–ł —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ā—ā—Ä–Ķ—Ā—Ā–ĺ—Ä–ĺ–≤. –í —Ā–Ľ—É—á–į–Ķ –Ę–Ď –Ľ–ł—Ü–į —Ā –į–ļ—ā–ł–≤–Ĺ—č–ľ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ķ–ľ –ł–ľ–Ķ—é—ā –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–Ĺ—č–Ļ —É—Ä–ĺ–≤–Ķ–Ĺ—Ć –Ņ—Ä–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ü–ł—ā–ĺ–ļ–ł–Ĺ–ĺ–≤, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –į—Ā—Ā–ĺ—Ü–ł–ł—Ä–ĺ–≤–į–Ĺ—č —Ā –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–Ĺ—č–ľ —Ä–ł—Ā–ļ–ĺ–ľ —Ä–į–∑–≤–ł—ā–ł—Ź –°–°–ó [14]. –í —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł, –ł–Ĺ—ā–Ķ—Ä–Ľ–Ķ–Ļ–ļ–ł–Ĺ-6 –į—Ā—Ā–ĺ—Ü–ł–ł—Ä–ĺ–≤–į–Ĺ —Ā –ł–Ĺ—Ā—É–Ľ–ł–Ĺ–ĺ—Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā—Ć—é, –ī–ł—Ā–Ľ–ł–Ņ–ł–ī–Ķ–ľ–ł–Ķ–Ļ –ł —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ –ī–ł—Ā—Ą—É–Ĺ–ļ—Ü–ł–Ķ–Ļ, –į —ā–į–ļ–∂–Ķ –ł–Ĺ–≥–ł–Ī–ł—Ä—É–Ķ—ā –Ľ–ł–Ņ–į–∑—É –Ľ–ł–Ņ–ĺ–Ņ—Ä–ĺ—ā–Ķ–ł–ī–ĺ–≤ –ł —Ā—ā–ł–ľ—É–Ľ–ł—Ä—É–Ķ—ā –Ľ–ł–Ņ–ĺ–Ľ–ł–∑, —ć–ļ—Ā–Ņ—Ä–Ķ—Ā—Ā–ł—Ä—É–Ķ—ā—Ā—Ź –≤ –∂–ł—Ä–ĺ–≤—č—Ö –ĺ—ā–Ľ–ĺ–∂–Ķ–Ĺ–ł—Ź—Ö –ł –į—ā–Ķ—Ä–ĺ–ľ–į—ā–ĺ–∑–Ĺ–ĺ–Ļ ¬ę—ą–į–Ņ–ĺ—á–ļ–Ķ¬Ľ, —á—ā–ĺ –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ķ—ā –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–ĺ–∂–ł—ā—Ć —Ä–ĺ–Ľ—Ć —ć—ā–ĺ–≥–ĺ –Ņ—Ä–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ —Ü–ł—ā–ĺ–ļ–ł–Ĺ–į –≤ –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł–ł –į—ā–Ķ—Ä–ĺ—Ā–ļ–Ľ–Ķ—Ä–ĺ–∑–į [14].
–í —Ā–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ—č—Ö —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł—Ź—Ö –ł–ľ–Ķ–Ķ—ā—Ā—Ź –ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ –ī–į–Ĺ–Ĺ—č—Ö —Ā –≤—č—Ā–ĺ–ļ–ĺ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć—é –ī–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā–ł –Ņ–ĺ –≤–ĺ–Ņ—Ä–ĺ—Ā–į–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ĺ—ā–ī–Ķ–Ľ—Ć–Ĺ—č—Ö –Ĺ–ĺ–∑–ĺ–Ľ–ĺ–≥–ł–Ļ (–•–ě–Ď–õ, –ė–Ď–°, –Ę–Ď), –ļ–ĺ—ā–ĺ—Ä—č–Ķ –ĺ–Ī—Ź–∑–į—ā–Ķ–Ľ—Ć–Ĺ—č –ļ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—é –Ņ—Ä–ł –≤–Ķ–ī–Ķ–Ĺ–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —ć—ā–ł–ľ–ł –Ĺ–ĺ–∑–ĺ–Ľ–ĺ–≥–ł—Ź–ľ–ł. –ü—Ä–ĺ–Ī–Ľ–Ķ–ľ–į –∂–Ķ –≤–Ķ–ī–Ķ–Ĺ–ł—Ź –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ–Ļ –ļ–į—ā–Ķ–≥–ĺ—Ä–ł–ł –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ –ł–∑—É—á–Ķ–Ĺ–į –ł –į—Ä–≥—É–ľ–Ķ–Ĺ—ā–ł—Ä–ĺ–≤–į–Ĺ–į –≤ –≤—č–Ī–ĺ—Ä–Ķ —Ā—Ä–Ķ–ī—Ā—ā–≤, –Ĺ—É–∂–ī–į–Ķ—ā—Ā—Ź –≤ –ī–Ķ—ā–į–Ľ–ł–∑–į—Ü–ł–ł –ł –ī–ĺ–Ņ–ĺ–Ľ–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ —Ä–į–∑—Ä–į–Ī–ĺ—ā–ļ–Ķ. –≠—ā–ĺ –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ–ĺ —ā–į–ļ–∂–Ķ —ā–Ķ–ľ, —á—ā–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ę–Ď —ā—Ä–Ķ–Ī—É–Ķ—ā –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ, –Ĺ–Ķ–Ņ—Ä–Ķ—Ä—č–≤–Ĺ–ĺ–≥–ĺ –ł –ĺ–ī–Ĺ–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ł–Ķ–ľ–į –Ĺ–Ķ—Ā–ļ–ĺ–Ľ—Ć–ļ–ł—Ö –į–Ĺ—ā–ł–Ī–į–ļ—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ—č—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤, –ļ–ĺ—ā–ĺ—Ä—č–Ķ, –Ņ–ĺ–ľ–ł–ľ–ĺ —ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —ć—Ą—Ą–Ķ–ļ—ā–į, –Ĺ–Ķ—Ä–Ķ–ī–ļ–ĺ –ĺ–ļ–į–∑—č–≤–į—é—ā –Ņ–ĺ–≤—Ä–Ķ–∂–ī–į—é—Č–Ķ–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –Ĺ–į –ľ–ł–ĺ–ļ–į—Ä–ī, —É—Ö—É–ī—ą–į—Ź –≥–Ķ–ľ–ĺ–ī–ł–Ĺ–į–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ–į—Ä–į–ľ–Ķ—ā—Ä—č [15], —É—Ā—É–≥—É–Ī–Ľ—Ź—Ź –ł—ą–Ķ–ľ–ł—é –ľ–ł–ĺ–ļ–į—Ä–ī–į. –Ē–ĺ –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–≥–ĺ –≤—Ä–Ķ–ľ–Ķ–Ĺ–ł –ĺ—Ā—ā–į—é—ā—Ā—Ź –ľ–į–Ľ–ĺ–ł–∑—É—á–Ķ–Ĺ–Ĺ—č–ľ–ł –≤–į—Ä–ł–į–Ĺ—ā—č —ā–Ķ—Ä–į–Ņ–ł–ł –ė–Ď–°, –Ķ–Ķ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –ł –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć –Ĺ–į —Ą–ĺ–Ĺ–Ķ –ĺ–ī–Ĺ–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –≤–Ņ–Ķ—Ä–≤—č–Ķ –≤—č—Ź–≤–Ľ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –Ę–Ď –ł –•–ě–Ď–õ. –¶–Ķ–Ľ—Ć –ī–į–Ĺ–Ĺ–ĺ–≥–ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź ‚ÄĒ –ĺ–Ņ—ā–ł–ľ–ł–∑–į—Ü–ł—Ź —ā–Ķ—Ä–į–Ņ–ł–ł –ė–Ď–° —É –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ę–Ď, –ė–Ď–° –ł –•–ě–Ď–õ.
–ú–į—ā–Ķ—Ä–ł–į–Ľ –ł –ľ–Ķ—ā–ĺ–ī—č
–Ě–į–ľ–ł –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ĺ –Ņ—Ä–ĺ—Ā—ā–ĺ–Ķ —Ā—Ä–į–≤–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –Ņ—Ä–ĺ—Ā–Ņ–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ĺ–į –Ī–į–∑–Ķ –Ď–£–ó–ě–ě ¬ę–ö–ü–Ę–Ē¬Ľ. –ü—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć –Ņ–Ķ—Ä–ł–ĺ–ī–į –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–į 3 –ľ–Ķ—Ā. –ė—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ī—č–Ľ–ĺ –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ–ĺ –≤ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–ł–ł —Ā–ĺ —Ā—ā–į–Ĺ–ī–į—Ä—ā–į–ľ–ł –Ě–į–ī–Ľ–Ķ–∂–į—Č–Ķ–Ļ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ņ—Ä–į–ļ—ā–ł–ļ–ł (Good Clinical Practice) –ł –Ņ—Ä–ł–Ĺ—Ü–ł–Ņ–į–ľ–ł –•–Ķ–Ľ—Ć—Ā–ł–Ĺ–ļ—Ā–ļ–ĺ–Ļ –ī–Ķ–ļ–Ľ–į—Ä–į—Ü–ł–ł. –ü—Ä–ĺ—ā–ĺ–ļ–ĺ–Ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ī—č–Ľ –ĺ–ī–ĺ–Ī—Ä–Ķ–Ĺ —ć—ā–ł—á–Ķ—Ā–ļ–ł–ľ –ļ–ĺ–ľ–ł—ā–Ķ—ā–ĺ–ľ –§–ď–Ď–ě–£ –í–ě –ě–ľ–ď–ú–£ –ú–ł–Ŭ≠–∑–ī—Ä–į–≤–į –†–ĺ—Ā—Ā–ł–ł.
–ö—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ–ł –≤–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź —Ź–≤–Ľ—Ź–Ľ–ł—Ā—Ć –Ĺ–į–Ľ–ł—á–ł–Ķ –≤–Ņ–Ķ—Ä–≤—č–Ķ –≤—č—Ź–≤–Ľ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –Ę–Ď, –Ĺ–į–Ľ–ł—á–ł–Ķ –•–ě–Ď–õ —Ā—Ä–Ķ–ī–Ĺ–Ķ–Ļ –ł —ā—Ź–∂–Ķ–Ľ–ĺ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł, –Ĺ–į–Ľ–ł—á–ł–Ķ —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —Ą–ĺ—Ä–ľ—č –ė–Ď–° –≤ –≤–ł–ī–Ķ —Ā—ā–į–Ī–ł–Ľ—Ć–Ĺ–ĺ–Ļ —Ā—ā–Ķ–Ĺ–ĺ–ļ–į—Ä–ī–ł–ł II –ł–Ľ–ł III —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–Ľ–į—Ā—Ā–į (–§–ö) –Ņ–ĺ –ö–į–Ĺ–į–ī—Ā–ļ–ĺ–Ļ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–ł, –Ņ–ĺ–ī–Ņ–ł—Ā–į–Ĺ–Ĺ–ĺ–Ķ –ł–Ĺ—Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ķ —Ā–ĺ–≥–Ľ–į—Ā–ł–Ķ –Ĺ–į —É—á–į—Ā—ā–ł–Ķ –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł.
–ö—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ–ł –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź –Ī—č–Ľ–ł –≤–Ĺ–Ķ–Ľ–Ķ–≥–ĺ—á–Ĺ—č–Ļ –Ę–Ď, –Ĺ–į–Ľ–ł—á–ł–Ķ –í–ė–ß, –≥–Ķ–Ņ–į—ā–ł—ā–į, –Ĺ–į–Ľ–ł—á–ł–Ķ —ć–Ĺ–ī–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ–ĺ–≥–ĺ —Ā—ā–Ķ–Ĺ—ā–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź —Ā–ĺ—Ā—É–ī–ĺ–≤ –≤ –į–Ĺ–į–ľ–Ĺ–Ķ–∑–Ķ, –Ĺ–į–Ľ–ł—á–ł–Ķ –ĺ—Ā—ā—Ä–ĺ–≥–ĺ –ł–Ĺ—Ą–į—Ä–ļ—ā–į –ľ–ł–ĺ–ļ–į—Ä–ī–į –≤ –į–Ĺ–į–ľ–Ĺ–Ķ–∑–Ķ, –Ĺ–į–Ľ–ł—á–ł–Ķ –ī—Ä—É–≥–ł—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ, –Ņ—Ä–ĺ—Ź–≤–Ľ—Ź—é—Č–ł—Ö—Ā—Ź —Ā—ā–Ķ–Ĺ–ĺ–ļ–į—Ä–ī–ł–Ķ–Ļ (–Ņ–ĺ—Ä–ĺ–ļ–ł —Ā–Ķ—Ä–ī—Ü–į, –ļ–į—Ä–ī–ł–ĺ–ľ–ł–ĺ–Ņ–į—ā–ł–ł, —Ā–ł—Ā—ā–Ķ–ľ–Ĺ—č–Ķ –≤–į—Ā–ļ—É–Ľ–ł—ā—č, –į–Ĺ–Ķ–ľ–ł—Ź), –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–į—Ź —Ä–į–Ĺ–Ķ–Ķ –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–į—Ź –≥–ł–Ņ–Ķ—Ä—ā–Ķ–Ĺ–∑–ł—Ź, –Ĺ–Ķ–∂–Ķ–Ľ–į–Ĺ–ł–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —É—á–į—Ā—ā–≤–ĺ–≤–į—ā—Ć –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł.
–í –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ī—č–Ľ–ł –≤–ļ–Ľ—é—á–Ķ–Ĺ—č 68 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ (48 [70,5%] –ľ—É–∂—á–ł–Ĺ, 20 [29,5%] –∂–Ķ–Ĺ—Č–ł–Ĺ) —Ā –Ę–Ď, –•–ě–Ď–õ –ł –ė–Ď–°. –°—Ä–Ķ–ī–Ĺ–ł–Ļ –≤–ĺ–∑—Ä–į—Ā—ā –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā–ĺ—Ā—ā–į–≤–ł–Ľ 65,35¬Ī9,9 –≥–ĺ–ī–į. –Ē–ł–į–≥–Ĺ–ĺ–∑ –•–ě–Ď–õ –ł –ė–Ď–° –Ī—č–Ľ –≤—č—Ā—ā–į–≤–Ľ–Ķ–Ĺ —Ä–į–Ĺ–Ķ–Ķ, –Ĺ–į –Ņ—Ä–Ķ–ī—ą–Ķ—Ā—ā–≤—É—é—Č–ł—Ö —ć—ā–į–Ņ–į—Ö. –Ě–į—ą–Ķ–Ļ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–Ļ –∑–į–ī–į—á–Ķ–Ļ –Ī—č–Ľ–ĺ –≤ –Ņ–Ķ—Ä–ł–ĺ–ī –≥–ĺ—Ā–Ņ–ł—ā–į–Ľ–ł–∑–į—Ü–ł–ł –≤ –Ņ—Ä–ĺ—ā–ł–≤–ĺ—ā—É–Ī–Ķ—Ä–ļ—É–Ľ–Ķ–∑–Ĺ—č–Ļ –ī–ł—Ā–Ņ–į–Ĺ—Ā–Ķ—Ä (–ü–Ę–Ē) –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ņ–Ķ—Ä–≤–ł—á–Ĺ—č–ľ –Ę–Ď –Ņ–ĺ–ī–ĺ–Ī—Ä–į—ā—Ć –ł –Ņ—Ä–ĺ–≤–Ķ—Ā—ā–ł –į–ī–Ķ–ļ–≤–į—ā–Ĺ—É—é —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ—É—é –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ—É—é —ā–Ķ—Ä–į–Ņ–ł—é —Ā –ľ–ł–Ĺ–ł–ľ–ł–∑–į—Ü–ł–Ķ–Ļ –Ņ–ĺ–Ī–ĺ—á–Ĺ—č—Ö —ć—Ą—Ą–Ķ–ļ—ā–ĺ–≤ —ā–į–ļ, —á—ā–ĺ–Ī—č —Ā –ĺ–ī–Ĺ–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ–ĺ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–ľ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–Ķ–Ļ –•–ě–Ď–õ –ł –Ę–Ď –Ī—č–Ľ–ĺ –ī–ĺ—Ā—ā–ł–≥–Ĺ—É—ā–ĺ —Ā–ĺ–ļ—Ä–į—Č–Ķ–Ĺ–ł–Ķ —Ā—Ä–ĺ–ļ–ĺ–≤ –Ī–į–ļ—ā–Ķ—Ä–ł–ĺ–≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź. –ė–Ĺ—Ą–ł–Ľ—Ć—ā—Ä–į—ā–ł–≤–Ĺ—č–Ļ –Ę–Ď –Ī—č–Ľ —É 60 –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö (88,2¬Ī3,9%), –ĺ—á–į–≥–ĺ–≤—č–Ļ –Ę–Ď ‚ÄĒ —É 6 –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö (8,8¬Ī3,4%), –ī–ł—Ā—Ā–Ķ–ľ–ł–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ļ –Ę–Ď ‚ÄĒ —É 1 –Ī–ĺ–Ľ—Ć–Ĺ–ĺ–≥–ĺ (1,5¬Ī1,5%), —Ą–ł–Ī—Ä–ĺ–∑–Ĺ–ĺ-–ļ–į–≤–Ķ—Ä–Ĺ–ĺ–∑–Ĺ—č–Ļ –Ę–Ď ‚ÄĒ —É 1 –Ī–ĺ–Ľ—Ć–Ĺ–ĺ–≥–ĺ (1,5¬Ī1,5%). –ü–į—Ü–ł–Ķ–Ĺ—ā—č –Ņ–ĺ–Ľ—É—á–į–Ľ–ł –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –≤ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–ł–ł —Ā I –ł III —Ä–Ķ–∂–ł–ľ–į–ľ–ł —Ö–ł–ľ–ł–ĺ—ā–Ķ—Ä–į–Ņ–ł–ł. –•–ě–Ď–õ —Ā—Ä–Ķ–ī–Ĺ–Ķ–Ļ —ā—Ź–∂–Ķ—Ā—ā–ł –ļ–ĺ–Ĺ—Ā—ā–į—ā–ł—Ä–ĺ–≤–į–Ĺ–į —É 55 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, —ā—Ź–∂–Ķ–Ľ–ĺ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł ‚ÄĒ —É 13 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤. –í—Ā–Ķ –ĺ–Ĺ–ł –Ņ–ĺ–Ľ—É—á–į–Ľ–ł –į–Ĺ—ā–ł—Ö–ĺ–Ľ–ł–Ĺ–Ķ—Ä–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź. –ü–į—Ü–ł–Ķ–Ĺ—ā—č —Ā–ĺ —Ā—Ä–Ķ–ī–Ĺ–Ķ—ā—Ź–∂–Ķ–Ľ–ĺ–Ļ –•–ě–Ď–õ –Ņ–ĺ–Ľ—É—á–į–Ľ–ł –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ī–Ķ–Ļ—Ā—ā–≤—É—é—Č–ł–Ķ –į–Ĺ—ā–ł—Ö–ĺ–Ľ–ł–Ĺ–Ķ—Ä–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č (—ā–ł–ĺ—ā—Ä–ĺ–Ņ–ł—Ź –Ī—Ä–ĺ–ľ–ł–ī 18 –ľ–ļ–≥, –Ņ–ĺ 1 –ī–ĺ–∑–Ķ 1 —Ä/—Ā—É—ā). –ü–į—Ü–ł–Ķ–Ĺ—ā—č —Ā —ā—Ź–∂–Ķ–Ľ–ĺ–Ļ –•–ě–Ď–õ –Ņ–ĺ–Ľ—É—á–į–Ľ–ł –ļ–ĺ–ľ–Ī–ł–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ķ –Ī—Ä–ĺ–Ĺ—Ö–ĺ–Ľ–ł—ā–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č: –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ī–Ķ–Ļ—Ā—ā–≤—É—é—Č–ł–Ķ ő≤2-–į–≥–ĺ–Ĺ–ł—Ā—ā –ł –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ī–Ķ–Ļ—Ā—ā–≤—É—é—Č–ł–Ķ –į–Ĺ—ā–ł—Ö–ĺ–Ľ–ł–Ĺ–Ķ—Ä–≥–ł–ļ ‚ÄĒ –ĺ–Ľ–ĺ–ī–į—ā–Ķ—Ä–ĺ–Ľ + —ā–ł–ĺ—ā—Ä–ĺ–Ņ–ł—Ź –Ī—Ä–ĺ–ľ–ł–ī 2,5 + 2,5 –ľ–≥, –Ņ–ĺ 2 –ī–ĺ–∑—č 1 —Ä/—Ā—É—ā.
–í –∑–į–≤–ł—Ā–ł–ľ–ĺ—Ā—ā–ł –ĺ—ā —Ö–į—Ä–į–ļ—ā–Ķ—Ä–į –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ–Ĺ–ĺ–Ļ –ł–Ĺ–ī–ł–≤–ł–ī—É–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č –Ī—č–Ľ–ł —Ä–į–∑–ī–Ķ–Ľ–Ķ–Ĺ—č –Ĺ–į 4 –≥—Ä—É–Ņ–Ņ—č (n=17 –≤ –ļ–į–∂–ī–ĺ–Ļ), –≤ –ļ–ĺ—ā–ĺ—Ä—č–Ķ –≤ —Ä–į–≤–Ĺ—č—Ö –ī–ĺ–Ľ—Ź—Ö –Ņ–ĺ–Ņ–į–Ľ–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā —ā—Ź–∂–Ķ–Ľ–ĺ–Ļ –ł —Ā—Ä–Ķ–ī–Ĺ–Ķ—ā—Ź–∂–Ķ–Ľ–ĺ–Ļ –•–ě–Ď–õ. –í—Ā–Ķ 4 –≥—Ä—É–Ņ–Ņ—č –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ī—č–Ľ–ł —Ā–ĺ–Ņ–ĺ—Ā—ā–į–≤–ł–ľ—č –Ņ–ĺ –≤–ĺ–∑—Ä–į—Ā—ā—É, –Ņ–ĺ–Ľ—É –ł —ā—Ź–∂–Ķ—Ā—ā–ł —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–Ķ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–ł.
–ü–ĺ–ī–Ī–ĺ—Ä —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł —Ā–ĺ–≥–Ľ–į—Ā–Ĺ–ĺ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–ľ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł—Ź–ľ –Ņ–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—é –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā–ĺ —Ā—ā–į–Ī–ł–Ľ—Ć–Ĺ–ĺ–Ļ –ė–Ď–° [16]. –Ē–Ľ—Ź —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā–ĺ —Ā—ā–į–Ī–ł–Ľ—Ć–Ĺ–ĺ–Ļ –ė–Ď–° –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź–Ľ–ł—Ā—Ć –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ķ —Ā—Ä–Ķ–ī—Ā—ā–≤–į, –ł–ľ–Ķ—é—Č–ł–Ķ—Ā—Ź –≤ –Ĺ–į–Ľ–ł—á–ł–ł –≤ –ü–Ę–Ē: –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ, –į–ľ–Ľ–ĺ–ī–ł–Ņ–ł–Ĺ, –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ, –Ĺ–ł—ā—Ä–ĺ—Ā–ĺ—Ä–Ī–ł–ī, —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ. –í–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ī—Ä—É–≥–ł—Ö –≥—Ä—É–Ņ–Ņ, –≤ —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä–ĺ–≤ If-–ļ–į–Ĺ–į–Ľ–ĺ–≤ –ł–Ľ–ł –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–į –Ņ—Ä–ĺ–Ľ–ĺ–Ĺ–≥–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–≥–ĺ –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź, –Ī—č–Ľ–ł –ĺ–≥—Ä–į–Ĺ–ł—á–Ķ–Ĺ—č —Ā–Ņ–ł—Ā–ļ–ĺ–ľ —Ā—Ä–Ķ–ī—Ā—ā–≤, –∑–į–ļ—É–Ņ–į–Ķ–ľ—č—Ö –≤ –ü–Ę–Ē.
–Ď–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ –ł –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –Ĺ–į–∑–Ĺ–į—á–į–Ľ–ł—Ā—Ć –ľ–Ķ—ā–ĺ–ī–ĺ–ľ —ā–ł—ā—Ä–ĺ–≤–į–Ĺ–ł—Ź –ī–ĺ –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —ć—Ą—Ą–Ķ–ļ—ā–į (–Ņ–Ķ—Ä–Ķ—Ö–ĺ–ī —Ā—ā–Ķ–Ĺ–ĺ–ļ–į—Ä–ī–ł–ł –Ĺ–į–Ņ—Ä—Ź–∂–Ķ–Ĺ–ł—Ź –§–ö II‚ÄďIII –≤ –§–ö I) –ł/–ł–Ľ–ł –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź –Ņ–ĺ–Ī–ĺ—á–Ĺ—č—Ö —ć—Ą—Ą–Ķ–ļ—ā–ĺ–≤, –Ņ—Ä–ł–≤–ĺ–ī—Ź—Č–ł—Ö –ļ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—é –ī–ĺ–∑—č –ł–Ľ–ł –ĺ—ā–ľ–Ķ–Ĺ–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į. –Ď–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ –Ĺ–į–∑–Ĺ–į—á–į–Ľ–ł –≤ —Ā—ā–į—Ä—ā–ĺ–≤–ĺ–Ļ –ī–ĺ–∑–Ķ 5 –ľ–≥/—Ā—É—ā, –Ņ—Ä–ł —Ö–ĺ—Ä–ĺ—ą–Ķ–Ļ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā–ł –ī–ĺ–∑—É —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ľ–ł —á–Ķ—Ä–Ķ–∑ 1‚Äď2 –Ĺ–Ķ–ī. –Ĺ–į 2,5 –ľ–≥, –ī–ĺ—Ö–ĺ–ī—Ź —á–Ķ—Ä–Ķ–∑ 2‚Äď3 –Ĺ–Ķ–ī. –ī–ĺ –ī–ĺ–∑—č 10 –ľ–≥/—Ā—É—ā. –ö–į–∂–ī—É—é –Ĺ–Ķ–ī–Ķ–Ľ—é –Ņ–ĺ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–ľ –ī–į–Ĺ–Ĺ—č–ľ –Ņ—Ä–ł–Ĺ–ł–ľ–į–Ľ–ĺ—Ā—Ć —Ä–Ķ—ą–Ķ–Ĺ–ł–Ķ –ĺ –ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ—Ā—ā–ł –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —ć—Ą—Ą–Ķ–ļ—ā–į –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į –≤ –ī–ĺ—Ā—ā–ł–≥–Ĺ—É—ā–ĺ–Ļ –ī–ĺ–∑–Ķ. –ü—Ä–ł –Ņ–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–ł –Ņ–ĺ–Ī–ĺ—á–Ĺ—č—Ö —ć—Ą—Ą–Ķ–ļ—ā–ĺ–≤ –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į –≤ –≤–ł–ī–Ķ —É—Ā–ł–Ľ–Ķ–Ĺ–ł—Ź (–Ņ–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź) –ļ–į—ą–Ľ—Ź –ł–Ľ–ł –ĺ–ī—č—ą–ļ–ł –ī–ĺ–∑–į —É–ľ–Ķ–Ĺ—Ć—ą–į–Ľ–į—Ā—Ć –ī–ĺ –Ņ—Ä–Ķ–ī—č–ī—É—Č–Ķ–Ļ. –í —Ā–Ľ—É—á–į–Ķ —Ā–ĺ—Ö—Ä–į–Ĺ–Ķ–Ĺ–ł—Ź —Ā—ā–Ķ–Ĺ–ĺ–ļ–į—Ä–ī–ł–ł –§–ö II‚ÄďIII –ł/–ł–Ľ–ł —Ā–ĺ—Ö—Ä–į–Ĺ–Ķ–Ĺ–ł—Ź –Ņ–ĺ–Ī–ĺ—á–Ĺ—č—Ö —ć—Ą—Ą–Ķ–ļ—ā–ĺ–≤ –Ņ—Ä–ł–Ĺ–ł–ľ–į–Ľ–ł —Ä–Ķ—ą–Ķ–Ĺ–ł–Ķ –ĺ –∑–į–ľ–Ķ–Ĺ–Ķ –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į –Ĺ–į –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –≤ —Ā—ā–į—Ä—ā–ĺ–≤–ĺ–Ļ –ī–ĺ–∑–Ķ 40 –ľ–≥ 3 —Ä/—Ā—É—ā.
–Ę–ł—ā—Ä–į—Ü–ł—Ź –ī–ĺ–∑—č –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–į –Ĺ–į—á–ł–Ĺ–į–Ľ–į—Ā—Ć —Ā 40 –ľ–≥ 3 —Ä/—Ā—É—ā. –ē–∂–Ķ–Ĺ–Ķ–ī–Ķ–Ľ—Ć–Ĺ–ĺ –ī–ĺ–∑—É —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ľ–ł –Ĺ–į 40 –ľ–≥ —É—ā—Ä–ĺ–ľ, –Ĺ–į —Ā–Ľ–Ķ–ī—É—é—Č–Ķ–Ļ –Ĺ–Ķ–ī–Ķ–Ľ–Ķ ‚ÄĒ 40 –ľ–≥ –≤ –ĺ–Ī–Ķ–ī –ł –Ĺ–į 4-–Ļ –Ĺ–Ķ–ī–Ķ–Ľ–Ķ ‚ÄĒ 40 –ľ–≥ –≤–Ķ—á–Ķ—Ä–ĺ–ľ, —ā–į–ļ —á—ā–ĺ —á–Ķ—Ä–Ķ–∑ 4 –Ĺ–Ķ–ī. –ī–ĺ—Ā—ā–ł–≥–į–Ľ–ł –ī–ĺ–∑—č 80 –ľ–≥ 3 —Ä/—Ā—É—ā. –ü—Ä–ł —ā–ł—ā—Ä–į—Ü–ł–ł –ī–ĺ–∑—č –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į –ł –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–į –Ķ–∂–Ķ–ī–Ĺ–Ķ–≤–Ĺ–ĺ –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä–ĺ–≤–į–Ľ–ł —É—Ä–ĺ–≤–Ķ–Ĺ—Ć –ź–Ē, –Ķ–∂–Ķ–Ĺ–Ķ–ī–Ķ–Ľ—Ć–Ĺ–ĺ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł –≠–ö–ď –≤ –Ņ–ĺ–ļ–ĺ–Ķ –ī–Ľ—Ź –ĺ—Ü–Ķ–Ĺ–ļ–ł —á–į—Ā—ā–ĺ—ā—č —Ä–ł—ā–ľ–į, –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā–ł –į—ā—Ä–ł–ĺ–≤–Ķ–Ĺ—ā—Ä–ł–ļ—É–Ľ—Ź—Ä–Ĺ–ĺ–Ļ –ł –∂–Ķ–Ľ—É–ī–ĺ—á–ļ–ĺ–≤–ĺ–Ļ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–ľ–ĺ—Ā—ā–ł.
–ü–į—Ü–ł–Ķ–Ĺ—ā—č –ł–∑ 1-–Ļ –≥—Ä—É–Ņ–Ņ—č –Ņ–ĺ–Ľ—É—á–į–Ľ–ł –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ –ł –į–ľ–Ľ–ĺ–ī–ł–Ņ–ł–Ĺ (10 –ľ–≥/—Ā—É—ā) –ĺ–ī–Ĺ–ĺ–ļ—Ä–į—ā–Ĺ–ĺ (–Ď+–ź), –ł–∑ 2-–Ļ –≥—Ä—É–Ņ–Ņ—č ‚ÄĒ –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ –ł –Ĺ–ł—ā—Ä–ĺ—Ā–ĺ—Ä–Ī–ł–ī (10 –ľ–≥ –∑–į 30 –ľ–ł–Ĺ –ī–ĺ –ĺ–∂–ł–ī–į–Ķ–ľ–ĺ–Ļ –Ĺ–į–≥—Ä—É–∑–ļ–ł 2‚Äď3 —Ä/—Ā—É—ā —Ā –Ķ–∂–Ķ–Ĺ–Ķ–ī–Ķ–Ľ—Ć–Ĺ—č–ľ–ł –Ņ–Ķ—Ä–Ķ—Ä—č–≤–į–ľ–ł –≤ 2 –ī–Ĺ—Ź) (–Ď+–Ě), –ł–∑ 3-–Ļ –≥—Ä—É–Ņ–Ņ—č ‚ÄĒ –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ –ł —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ (80 –ľ–≥/—Ā—É—ā –ĺ–ī–Ĺ–ĺ–ļ—Ä–į—ā–Ĺ–ĺ) (–Ď+–Ę), –ł–∑ 4-–Ļ –≥—Ä—É–Ņ–Ņ—č ‚ÄĒ –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –ł —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ (80 –ľ–≥/—Ā—É—ā –ĺ–ī–Ĺ–ĺ–ļ—Ä–į—ā–Ĺ–ĺ) (–í+–Ę).
–õ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ĺ—Ö–ĺ–ī–ł–Ľ–ĺ –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö —Ā—ā–į—Ü–ł–ĺ–Ĺ–į—Ä–į, –≤—Ā–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č –≤—č–ī–į–≤–į–Ľ–ł—Ā—Ć –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ —Ā—Ä–Ķ–ī–Ĺ–ł–ľ –ľ–Ķ–ī–ł—Ü–ł–Ĺ—Ā–ļ–ł–ľ –Ņ–Ķ—Ä—Ā–ĺ–Ĺ–į–Ľ–ĺ–ľ –ł –Ņ—Ä–ł–Ĺ–ł–ľ–į–Ľ–ł—Ā—Ć –≤ –Ņ—Ä–ł—Ā—É—ā—Ā—ā–≤–ł–ł –ľ–Ķ–ī—Ä–į–Ī–ĺ—ā–Ĺ–ł–ļ–į. –í—Ā—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź –Ī—č–Ľ–į –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É–Ķ–ľ–ĺ–Ļ, –≤–ļ–Ľ—é—á–į—Ź –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ—É—é, –Ņ—Ä–ĺ—ā–ł–≤–ĺ—ā—É–Ī–Ķ—Ä–ļ—É–Ľ–Ķ–∑–Ĺ—É—é –ł —ā–Ķ—Ä–į–Ņ–ł—é –•–ě–Ď–õ.
–Ē–Ľ—Ź –ĺ—Ü–Ķ–Ĺ–ļ–ł –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö –≤–į—Ä–ł–į–Ĺ—ā–ĺ–≤ –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ—č —Ā–Ľ–Ķ–ī—É—é—Č–ł–Ķ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł, –ĺ—ā—Ä–į–∂–į—é—Č–ł–Ķ —É—Ä–ĺ–≤–Ķ–Ĺ—Ć —Ą–ł–∑–ł—á–Ķ—Ā–ļ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ł —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć –Ĺ–į—Ā—č—Č–Ķ–Ĺ–ł—Ź –ļ–ł—Ā–Ľ–ĺ—Ä–ĺ–ī–ĺ–ľ –ļ—Ä–ĺ–≤–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į —Ā –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ–Ļ –Ī—Ä–ĺ–Ĺ—Ö–ĺ–Ľ–Ķ–≥–ĺ—á–Ĺ–ĺ–Ļ –ł —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ-—Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–Ķ–Ļ:
–ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ —ā–į–Ī–Ľ–Ķ—ā–ĺ–ļ –Ĺ–ł—ā—Ä–ĺ–≥–Ľ–ł—Ü–Ķ—Ä–ł–Ĺ–į –≤ –Ĺ–Ķ–ī–Ķ–Ľ—é –ļ–į–ļ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–į –Ņ—Ä–ł—Ā—ā—É–Ņ–ĺ–≤ –∑–į–≥—Ä—É–ī–ł–Ĺ–Ĺ—č—Ö –Ī–ĺ–Ľ–Ķ–Ļ –≤ –Ĺ–Ķ–ī–Ķ–Ľ—é;
—Ä–į—Ā—Ā—ā–ĺ—Ź–Ĺ–ł–Ķ, –ļ–ĺ—ā–ĺ—Ä–ĺ–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā –Ņ—Ä–Ķ–ĺ–ī–ĺ–Ľ–Ķ–≤–į–Ķ—ā –ī–ĺ –≤–ĺ–∑–Ĺ–ł–ļ–Ĺ–ĺ–≤–Ķ–Ĺ–ł—Ź –Ņ—Ä–ł—Ā—ā—É–Ņ–į –∑–į–≥—Ä—É–ī–ł–Ĺ–Ĺ—č—Ö –Ī–ĺ–Ľ–Ķ–Ļ (—Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É–Ķ—ā —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–ľ—É –ļ–Ľ–į—Ā—Ā—É —Ā—ā–Ķ–Ĺ–ĺ–ļ–į—Ä–ī–ł–ł);
—Ā–į—ā—É—Ä–į—Ü–ł—Ź –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ –ļ—Ä–ĺ–≤–ł, –ł–∑–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–į—Ź –ľ–Ķ—ā–ĺ–ī–ĺ–ľ –Ņ—É–Ľ—Ć—Ā–ĺ–ļ—Ā–ł–ľ–Ķ—ā—Ä–ł–ł (SpO2).
–í—Ā–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č, –≤–ļ–Ľ—é—á–Ķ–Ĺ–Ĺ—č–Ķ –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ —Ā –≤–Ņ–Ķ—Ä–≤—č–Ķ –≤—č—Ź–≤–Ľ–Ķ–Ĺ–Ĺ—č–ľ –Ę–Ď, —Ź–≤–Ľ—Ź–Ľ–ł—Ā—Ć –Ī–į–ļ—ā–Ķ—Ä–ł–ĺ–≤—č–ī–Ķ–Ľ–ł—ā–Ķ–Ľ—Ź–ľ–ł, –≤ —Ā–≤—Ź–∑–ł —Ā —á–Ķ–ľ –ľ—č –Ī—č–Ľ–ł –ĺ–≥—Ä–į–Ĺ–ł—á–Ķ–Ĺ—č –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł—á–Ķ—Ā–ļ–ł–ľ–ł –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā—Ź–ľ–ł –ĺ—ā–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł–ļ–ł –ü–Ę–Ē. –í—Ā–Ķ–ľ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ĺ—Ā—Ć —Ā—É—ā–ĺ—á–Ĺ–ĺ–Ķ –ľ–ĺ–Ĺ–ł—ā–ĺ—Ä–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –≠–ö–ď –Ņ–ĺ –•–ĺ–Ľ—ā–Ķ—Ä—É –≤ –Ĺ–į—á–į–Ľ–Ķ —ā–Ķ—Ä–į–Ņ–ł–ł –ł —á–Ķ—Ä–Ķ–∑ 3 –ľ–Ķ—Ā. —Ä–Ķ–≥—É–Ľ—Ź—Ä–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ł–Ķ–ľ–į –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ī–Ľ—Ź —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—Ź –Ņ–ĺ –≥—Ä—É–Ņ–Ņ–į–ľ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź. –Ē–Ľ—Ź –į–Ĺ–į–Ľ–ł–∑–į –Ī—č–Ľ–ł –≤–∑—Ź—ā—č –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł –ľ–ł–Ĺ–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–Ļ, –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–Ļ –ł —Ā—Ä–Ķ–ī–Ĺ–Ķ–Ļ –ß–°–°, –≤–į—Ä–ł–į–Ī–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć —Ä–ł—ā–ľ–į (—Ü–ł—Ä–ļ–į–ī–Ĺ—č–Ļ –ł–Ĺ–ī–Ķ–ļ—Ā), –ī–ł–Ĺ–į–ľ–ł–ļ–į —Ā–Ķ–≥–ľ–Ķ–Ĺ—ā–į ST (–ī–Ľ—Ź –į–Ĺ–į–Ľ–ł–∑–į –Ī—č–Ľ–į –≤—č–Ī—Ä–į–Ĺ–į —ā–ĺ–Ľ—Ć–ļ–ĺ –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ–į—Ź –ī–Ķ–Ņ—Ä–Ķ—Ā—Ā–ł—Ź ST –Ī–ĺ–Ľ–Ķ–Ķ 2 –ľ–ľ) –ļ–į–ļ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć, –ļ–ĺ—ā–ĺ—Ä—č–Ļ –Ī—č—Ā—ā—Ä–Ķ–Ķ –ī—Ä—É–≥–ł—Ö –ľ–ĺ–∂–Ķ—ā –ł–∑–ľ–Ķ–Ĺ—Ź—ā—Ć—Ā—Ź –Ņ—Ä–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł. –Ē–į–Ĺ–Ĺ—č–Ļ –ľ–Ķ—ā–ĺ–ī –Ī—č–Ľ –≤—č–Ī—Ä–į–Ĺ –ļ–į–ļ –ł–Ĺ—Ą–ĺ—Ä–ľ–į—ā–ł–≤–Ĺ—č–Ļ, –ī–ĺ—Ā—ā—É–Ņ–Ĺ—č–Ļ –ł –≤–ĺ—Ā–Ņ—Ä–ĺ–ł–∑–≤–ĺ–ī–ł–ľ—č–Ļ –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –Ď–£–ó–ě–ě ¬ę–ö–ü–Ę–Ē¬Ľ. –í —Ā–≤—Ź–∑–ł —Ā –Ĺ–į–Ľ–ł—á–ł–Ķ–ľ –Ī–į–ļ—ā–Ķ—Ä–ł–ĺ–≤—č–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ü–Ę–Ē –Ĺ–Ķ –Ī—č–Ľ–ĺ –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–ł—ā—Ć –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č–Ļ –ľ–Ķ—ā–ĺ–ī –ł–∑—É—á–Ķ–Ĺ–ł—Ź –ł—ą–Ķ–ľ–ł–ł –ľ–ł–ĺ–ļ–į—Ä–ī–į ‚ÄĒ –Ņ—Ä–ĺ–Ī—É —Ā —Ą–ł–∑–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ĺ–į–≥—Ä—É–∑–ļ–ĺ–Ļ –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ü–Ķ–Ĺ—ā—Ä–į –ł –ī—Ä—É–≥–ł—Ö —Ā–Ņ–Ķ—Ü–ł–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –ļ–Ľ–ł–Ĺ–ł–ļ.
–°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ—É—é –ĺ–Ī—Ä–į–Ī–ĺ—ā–ļ—É –ī–į–Ĺ–Ĺ—č—Ö –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é –Ņ—Ä–ĺ–≥—Ä–į–ľ–ľ–Ĺ–ĺ–≥–ĺ –Ņ–į–ļ–Ķ—ā–į Statistica 8.0 (StatSoft, Inc., USA). –†–Ķ–∑—É–Ľ—Ć—ā–į—ā –∑–į–Ņ–ł—Ā—č–≤–į–Ľ–ł –≤ –į–Ī—Ā–ĺ–Ľ—é—ā–Ĺ—č—Ö —Ü–ł—Ą—Ä–į—Ö, —É—á–ł—ā—č–≤–į—Ź, —á—ā–ĺ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ 4 –≥—Ä—É–Ņ–Ņ–į—Ö –ĺ–ī–ł–Ĺ–į–ļ–ĺ–≤–ĺ–Ķ (n=17). –ó–į–Ņ–ł—Ā—Ć —Ā—Ä–Ķ–ī–Ĺ–ł—Ö –∑–Ĺ–į—á–Ķ–Ĺ–ł–Ļ –Ņ—Ä–ĺ–ł–∑–≤–ĺ–ī–ł–Ľ–į—Ā—Ć –ļ–į–ļ –ú–Ķ; 25,0‚Äď75,0, –≥–ī–Ķ –ú–Ķ ‚ÄĒ –ľ–Ķ–ī–ł–į–Ĺ–į, 25,0 ‚ÄĒ –Ĺ–ł–∂–Ĺ–ł–Ļ% –ļ–≤–į—Ä—ā–ł–Ľ—Ć; 75,0 ‚ÄĒ –≤–Ķ—Ä—Ö–Ĺ–ł–Ļ% –ļ–≤–į—Ä—ā–ł–Ľ—Ć. –Ē–Ľ—Ź –ĺ—Ü–Ķ–Ĺ–ļ–ł –ī–ĺ—Ā—ā–ĺ–≤–Ķ—Ä–Ĺ–ĺ—Ā—ā–ł —Ä–į–∑–Ľ–ł—á–ł–Ļ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ –ľ–Ķ–∂–ī—É –≥—Ä—É–Ņ–Ņ–į–ľ–ł –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ–ł –Ĺ–Ķ–Ņ–į—Ä–į–ľ–Ķ—ā—Ä–ł—á–Ķ—Ā–ļ–ł–Ķ –ļ—Ä–ł—ā–Ķ—Ä–ł–ł Z-Test Wald-Wolfowitz, Ōá2 —Ā –Ņ–ĺ–Ņ—Ä–į–≤–ļ–ĺ–Ļ –ô–Ķ—ā—Ā–į (—É—á–ł—ā—č–≤–į—Ź –ľ–į–Ľ–ĺ–Ķ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≥—Ä—É–Ņ–Ņ–į—Ö). –ü—Ä–ł —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł –Ņ–į—Ä–į–ľ–Ķ—ā—Ä–ĺ–≤ –≤–Ĺ—É—ā—Ä–ł –ĺ–ī–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ—č –ī–ĺ –ł –Ņ–ĺ—Ā–Ľ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ—Ā—Ź Z-–ļ—Ä–ł—ā–Ķ—Ä–ł–Ļ (Wilcoxon). –£—Ä–ĺ–≤–Ķ–Ĺ—Ć —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –∑–Ĺ–į—á–ł–ľ–ĺ—Ā—ā–ł –Ņ—Ä–ł –Ņ—Ä–ĺ–≤–Ķ—Ä–ļ–Ķ –Ĺ—É–Ľ–Ķ–≤–ĺ–Ļ –≥–ł–Ņ–ĺ—ā–Ķ–∑—č –Ņ—Ä–ł–Ĺ–ł–ľ–į–Ľ–ł —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É—é—Č–ł–ľ —Ä<0,05.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –ł –ĺ–Ī—Ā—É–∂–ī–Ķ–Ĺ–ł–Ķ
–Ě–į –ľ–ĺ–ľ–Ķ–Ĺ—ā –≤–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –ī–ĺ—Ā—ā–ĺ–≤–Ķ—Ä–Ĺ—č—Ö —Ä–į–∑–Ľ–ł—á–ł–Ļ –Ņ—Ä–ł –Ņ–ĺ–Ņ–į—Ä–Ĺ–ĺ–ľ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł –≥—Ä—É–Ņ–Ņ –Ņ–ĺ –§–ö —Ā—ā–Ķ–Ĺ–ĺ–ļ–į—Ä–ī–ł–ł, –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤—É –Ņ—Ä–ł—Ā—ā—É–Ņ–ĺ–≤ –≤ –Ĺ–Ķ–ī–Ķ–Ľ—é, —É—Ä–ĺ–≤–Ĺ—é —Ą–ł–∑–ł—á–Ķ—Ā–ļ–ĺ–Ļ –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ł –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź–ľ –ľ–ĺ–Ĺ–ł—ā–ĺ—Ä–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –≠–ö–ď –Ņ–ĺ –•–ĺ–Ľ—ā–Ķ—Ä—É –Ĺ–Ķ –Ī—č–Ľ–ĺ (—ā–į–Ī–Ľ. 1). –°—Ä–į–≤–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –į–Ĺ–į–Ľ–ł–∑ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ –≤ —ā–į–Ī–Ľ–ł—Ü–į—Ö 1, 2 –ł 3.


–Ě–į —Ą–ĺ–Ĺ–Ķ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–ľ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –ł–ľ–Ķ–Ľ–į—Ā—Ć –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–į—Ź –ī–ł–Ĺ–į–ľ–ł–ļ–į –Ņ–ĺ –ľ–ł–Ĺ–ł–ľ–ł–∑–į—Ü–ł–ł –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–į –Ņ—Ä–ł—Ā—ā—É–Ņ–ĺ–≤ –∑–į–≥—Ä—É–ī–ł–Ĺ–Ĺ—č—Ö –Ī–ĺ–Ľ–Ķ–Ļ –≤ –Ĺ–Ķ–ī–Ķ–Ľ—é –Ņ—Ä–ł —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–ł —Ä–į—Ā—Ā—ā–ĺ—Ź–Ĺ–ł—Ź, –ļ–ĺ—ā–ĺ—Ä–ĺ–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā –ľ–ĺ–∂–Ķ—ā –Ņ—Ä–Ķ–ĺ–ī–ĺ–Ľ–Ķ—ā—Ć –ī–ĺ –≤–ĺ–∑–Ĺ–ł–ļ–Ĺ–ĺ–≤–Ķ–Ĺ–ł—Ź –Ņ—Ä–ł—Ā—ā—É–Ņ–į (—Ā–ľ. —ā–į–Ī–Ľ. 1). –ė–ľ–Ķ–Ĺ–Ĺ–ĺ —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ –Ņ–ĺ–ļ–į–∑–į–Ľ –Ĺ–į–ł–Ľ—É—á—ą—É—é –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć –ł –ĺ–ļ–į–∑—č–≤–į–Ľ –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –≤–Ľ–ł—Ź–Ĺ–ł–Ķ –Ĺ–į —Ą–ł–∑–ł—á–Ķ—Ā–ļ—É—é –į–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –≥–ł–Ņ–ĺ–ļ—Ā–ł–ł. –í–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ, –ĺ–Ĺ —ā–į–ļ–∂–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ĺ–≤–į–Ľ –ļ–į–ļ —Ā–Ķ—Ä–ī–Ķ—á–Ĺ—č–Ļ —Ü–ł—ā–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ĺ—Ä –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö —Ö–ł–ľ–ł–ĺ—ā–Ķ—Ä–į–Ņ–ł–ł –Ņ—Ä–ĺ—ā–ł–≤–ĺ—ā—É–Ī–Ķ—Ä–ļ—É–Ľ–Ķ–∑–Ĺ—č–ľ–ł —Ā—Ä–Ķ–ī—Ā—ā–≤–į–ľ–ł, –ł–ľ–Ķ—é—Č–ł–ľ–ł –ļ–į—Ä–ī–ł–ĺ–ī–Ķ–Ņ—Ä–Ķ—Ā—Ā–ł–≤–Ĺ—č–Ļ —ć—Ą—Ą–Ķ–ļ—ā [15]. –£ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ł–∑ –≥—Ä—É–Ņ–Ņ 1 –ł 2 (–Ď+–ź –ł –Ď+–Ě —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ) –ĺ—ā–ľ–Ķ—á–į–Ľ–ł—Ā—Ć —ć–Ņ–ł–∑–ĺ–ī—č –≥–ł–Ņ–ĺ—ā–ĺ–Ĺ–ł–ł, —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č–Ķ, –Ņ–ĺ-–≤–ł–ī–ł–ľ–ĺ–ľ—É, —Ā –ĺ–ī–Ĺ–ĺ–Ĺ–į–Ņ—Ä–į–≤–Ľ–Ķ–Ĺ–Ĺ—č–ľ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –≤ –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–ł –ź–Ē.
–Ē–Ľ—Ź –ĺ—Ü–Ķ–Ĺ–ļ–ł –ß–°–° –ļ–į–ļ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–≥–ĺ —Ü–Ķ–Ľ–Ķ–≤–ĺ–≥–ĺ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź –Ĺ–į —Ą–ĺ–Ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź ő≤-–Ī–Ľ–ĺ–ļ–į—ā–ĺ—Ä–ĺ–ľ –Ī—č–Ľ–ł –Ņ—Ä–ĺ–į–Ĺ–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ—č –ī–į–Ĺ–Ĺ—č–Ķ –≠–ö–ď-–ľ–ĺ–Ĺ–ł—ā–ĺ—Ä–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ņ–ĺ –•–ĺ–Ľ—ā–Ķ—Ä—É –ī–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ł —Ā–Ņ—É—Ā—ā—Ź 3 –ľ–Ķ—Ā. (—ā–į–Ī–Ľ. 2).
–Ě–į –ľ–ĺ–ľ–Ķ–Ĺ—ā –≤–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ—č—Ö —Ä–į–∑–Ľ–ł—á–ł–Ļ –Ņ—Ä–ł –Ņ–ĺ–Ņ–į—Ä–Ĺ–ĺ–ľ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł –≥—Ä—É–Ņ–Ņ –Ņ–ĺ —É—Ä–ĺ–≤–Ĺ—é –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ –ß–°–° –Ĺ–Ķ –Ī—č–Ľ–ĺ. –ß–Ķ—Ä–Ķ–∑ 3 –ľ–Ķ—Ā. —ā–Ķ—Ä–į–Ņ–ł–ł –≤–ĺ –≤—Ā–Ķ—Ö –≥—Ä—É–Ņ–Ņ–į—Ö –Ī—č–Ľ–į –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ–į –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–į—Ź –ī–ł–Ĺ–į–ľ–ł–ļ–į —Ā —Ä–į–∑–Ľ–ł—á–Ĺ–ĺ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć—é —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—Ź –ß–°–° –≤ –≥—Ä—É–Ņ–Ņ–į—Ö —Ā –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł–Ķ–ľ —Ü–Ķ–Ľ–Ķ–≤—č—Ö –∑–Ĺ–į—á–Ķ–Ĺ–ł–Ļ (—Ā–ľ. —ā–į–Ī–Ľ. 2). –°–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –ß–°–° –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī–ł–Ľ–ĺ –ļ–į–ļ –≤ –Ņ–ĺ–ļ–ĺ–Ķ, —ā–į–ļ –ł –Ņ—Ä–ł —Ą–ł–∑–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ĺ–į–≥—Ä—É–∑–ļ–Ķ, —á—ā–ĺ –ĺ—ā—Ä–į–∂–į–Ľ–ł –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł –ľ–ł–Ĺ–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–Ļ, —Ā—Ä–Ķ–ī–Ĺ–Ķ–Ļ –ł –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–Ļ –ß–°–°. –°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ–ĺ–Ķ —É—Ä–Ķ–∂–Ķ–Ĺ–ł–Ķ –ß–°–° –ĺ—ā–ľ–Ķ—ā–ł–Ľ–ł —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ł–∑ 3-–Ļ (–Ď+–Ę) –ł 4-–Ļ –≥—Ä—É–Ņ–Ņ (–í+–Ę) —ā–Ķ—Ä–į–Ņ–ł–ł (—Ā–ľ. —ā–į–Ī–Ľ. 2). –Ē–į–Ĺ–Ĺ—č–Ķ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –ľ–ĺ–∂–Ĺ–ĺ –ĺ–Ī—ä—Ź—Ā–Ĺ–ł—ā—Ć —Ą–į—Ä–ľ–į–ļ–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–ľ —ć—Ą—Ą–Ķ–ļ—ā–ĺ–ľ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑—É–Ķ–ľ—č—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤: –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ –ł –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ —É—Ä–Ķ–∂–į—é—ā –ß–°–°, –į –Ĺ–ł—ā—Ä–ĺ—Ā–ĺ—Ä–Ī–ł–ī –≤—č–∑—č–≤–į–Ķ—ā —É—á–į—Č–Ķ–Ĺ–ł–Ķ –ß–°–°, –į–ľ–Ľ–ĺ–ī–ł–Ņ–ł–Ĺ –ł —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ –Ĺ–Ķ –≤–Ľ–ł—Ź—é—ā –Ĺ–į –ß–°–°.
–í –≥—Ä—É–Ņ–Ņ–į—Ö, –Ņ–ĺ–Ľ—É—á–į—é—Č–ł—Ö –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ –≤ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —Ā –į–ľ–Ľ–ĺ–ī–ł–Ņ–ł–Ĺ–ĺ–ľ –ł–Ľ–ł –Ĺ–ł—ā—Ä–ĺ—Ā–ĺ—Ä–Ī–ł–ī–ĺ–ľ, –ĺ—ā—Ā—É—ā—Ā—ā–≤–ĺ–≤–į–Ľ–ł —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ—č–Ķ —Ä–į–∑–Ľ–ł—á–ł—Ź –≤ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–ł –ß–°–° –∑–į 3 –ľ–Ķ—Ā. —ā–Ķ—Ä–į–Ņ–ł–ł. –ü–ĺ-–≤–ł–ī–ł–ľ–ĺ–ľ—É, –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ –ł –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –ł–ľ–Ķ—é—ā –Ņ—Ä–ł–ľ–Ķ—Ä–Ĺ–ĺ –ĺ–ī–ł–Ĺ–į–ļ–ĺ–≤—č–Ļ —ć—Ą—Ą–Ķ–ļ—ā –≤ –ĺ—ā–Ĺ–ĺ—ą–Ķ–Ĺ–ł–ł –ß–°–° —É –ī–į–Ĺ–Ĺ–ĺ–Ļ –ļ–į—ā–Ķ–≥–ĺ—Ä–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, —á—ā–ĺ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É–Ķ—ā –Ľ–ł—ā–Ķ—Ä–į—ā—É—Ä–Ĺ—č–ľ –ī–į–Ĺ–Ĺ—č–ľ [17, 18], –ĺ–ī–Ĺ–į–ļ–ĺ –Ľ—É—á—ą–į—Ź –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–į –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ķ—ā –ī–ĺ—Ā—ā–ł—á—Ć –Ī–ĺ–Ľ—Ć—ą–ł—Ö –ī–ĺ–∑–ł—Ä–ĺ–≤–ĺ–ļ –ł –Ī–ĺ–Ľ–Ķ–Ķ –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—Ź –ß–°–° —É –ī–į–Ĺ–Ĺ–ĺ–Ļ –ļ–į—ā–Ķ–≥–ĺ—Ä–ł–ł –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤.
–Ě–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ –ĺ—ā–ľ–Ķ—ā–ł—ā—Ć, —á—ā–ĺ —É 16 –ł–∑ 51 (31,4%) –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į, –Ņ–ĺ–Ľ—É—á–į–≤—ą–Ķ–≥–ĺ –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ, –Ĺ–į —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö —ć—ā–į–Ņ–į—Ö –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł –ļ–ĺ—Ä—Ä–Ķ–ļ—Ü–ł—é —ā–Ķ—Ä–į–Ņ–ł–ł. –ü–ĺ—Ā–Ľ–Ķ –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź –ī–ĺ–∑—č 7,5‚Äď10 –ľ–≥/—Ā—É—ā –ĺ—Ā—ā–į–Ĺ–ĺ–≤–ļ–į —ā–ł—ā—Ä–į—Ü–ł–ł –ł —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –ī–ĺ–∑—č –ī–ĺ 5‚Äď7,5 –ľ–≥/—Ā—É—ā –≤ —Ā–≤—Ź–∑–ł —Ā –Ņ–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ–ľ –ł–Ľ–ł —É—Ā–ł–Ľ–Ķ–Ĺ–ł–Ķ–ľ –ļ–į—ą–Ľ—Ź –ł/–ł–Ľ–ł –ĺ–ī—č—ą–ļ–ł (–Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ļ –Ī—Ä–ĺ–Ĺ—Ö–ĺ–ĺ–Ī—Ā—ā—Ä—É–ļ—Ü–ł–ł) –ł–ľ–Ķ–Ľ–ł –ľ–Ķ—Ā—ā–ĺ —É 16 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ņ—Ä–ł—á–Ķ–ľ –≤—Ā–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā—ā—Ä–į–ī–į–Ľ–ł —ā—Ź–∂–Ķ–Ľ–ĺ–Ļ –•–ě–Ď–õ –ł —Ä–į–∑–Ĺ—č–ľ–ł —Ą–ĺ—Ä–ľ–į–ľ–ł –Ę–Ď. –í —Ā—ā–į—Ü–ł–ĺ–Ĺ–į—Ä–Ķ —ā–į–ļ–į—Ź –ļ–ĺ—Ä—Ä–Ķ–ļ—Ü–ł—Ź –Ī—č–Ľ–į –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ–Ļ, –Ņ–ĺ—Ā–ļ–ĺ–Ľ—Ć–ļ—É –ĺ—Ā–ľ–ĺ—ā—Ä –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł –Ķ–∂–Ķ–ī–Ĺ–Ķ–≤–Ĺ–ĺ. –ü–ĺ—ā—Ä–Ķ–Ī–ĺ–≤–į–Ľ–į—Ā—Ć –ĺ—ā–ľ–Ķ–Ĺ–į –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į —É 6 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ (–Ņ–ĺ 2 –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –ł–∑ 1-–Ļ, 2-–Ļ –ł 3-–Ļ –≥—Ä—É–Ņ–Ņ; 6/51 [11,8%]) —Ā –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ–Ļ –Ī—Ä–ĺ–Ĺ—Ö–ĺ–Ľ–Ķ–≥–ĺ—á–Ĺ–ĺ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–Ķ–Ļ –≤ —Ā–≤—Ź–∑–ł —Ā —É—Ā—É–≥—É–Ī–Ľ–Ķ–Ĺ–ł–Ķ–ľ –Ī—Ä–ĺ–Ĺ—Ö–ĺ–ĺ–Ī—Ā—ā—Ä—É–ļ—Ü–ł–ł –≤ –≤–ł–ī–Ķ —É—Ā–ł–Ľ–Ķ–Ĺ–ł—Ź –ļ–į—ą–Ľ—Ź –ł/–ł–Ľ–ł –ĺ–ī—č—ą–ļ–ł. –ė–∑ –Ĺ–ł—Ö 4 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ –Ī—č–Ľ–į –ĺ—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–į —ā–ł—ā—Ä–į—Ü–ł—Ź –Ĺ–į –ī–ĺ–∑–į—Ö 5 –ľ–≥/—Ā—É—ā –ł–Ľ–ł 7,5 –ľ–≥/—Ā—É—ā –Ī–Ķ–∑ –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —ć—Ą—Ą–Ķ–ļ—ā–į; —ć—ā–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č –Ī—č–Ľ–ł –Ņ–Ķ—Ä–Ķ–≤–Ķ–ī–Ķ–Ĺ—č –Ĺ–į —ā–Ķ—Ä–į–Ņ–ł—é –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–ĺ–ľ. –ē—Č–Ķ 2 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ –Ņ—Ä–ł—ą–Ľ–ĺ—Ā—Ć —Ā–Ĺ–ł–∑–ł—ā—Ć –ī–ĺ–∑—É –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į —Ā 10 –ľ–≥ –ī–ĺ 5 –ľ–≥, –į –∑–į—ā–Ķ–ľ –ĺ—ā–ľ–Ķ–Ĺ–ł—ā—Ć –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā –ł–∑-–∑–į —Ā–ĺ—Ö—Ä–į–Ĺ–Ķ–Ĺ–ł—Ź –ļ–į—ą–Ľ—Ź –ł —ā–į–ļ–∂–Ķ –Ņ–Ķ—Ä–Ķ–Ļ¬≠—ā–ł –Ĺ–į —ā–Ķ—Ä–į–Ņ–ł—é –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–ĺ–ľ. –ė—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–į 3 —Ä/—Ā—É—ā –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö —Ā—ā–į—Ü–ł–ĺ–Ĺ–į—Ä–į –ü–Ę–Ē –Ņ–ĺ–ļ–į–∑–į–Ľ–ĺ –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤–į –≤ –Ņ–Ľ–į–Ĺ–Ķ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā–ł —ā–Ķ—Ä–į–Ņ–ł–ł –ł –Ķ–Ķ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł ‚ÄĒ —É–ī–ĺ–≤–Ľ–Ķ—ā–≤–ĺ—Ä–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ļ –ł —Ä–ł—ā–ľ-—É—Ä–Ķ–∂–į—é—Č–ł–Ļ —ć—Ą—Ą–Ķ–ļ—ā –≤ —ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ī–ĺ–∑–Ķ 180‚Äď240 –ľ–≥/—Ā—É—ā. –°–Ľ—É—á–į–Ķ–≤ –ĺ—ā–ľ–Ķ–Ĺ—č –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–į –ł–∑-–∑–į –Ņ–ĺ–Ī–ĺ—á–Ĺ—č—Ö —ć—Ą—Ą–Ķ–ļ—ā–ĺ–≤ (—Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –ź–Ē –ł–Ľ–ł —É–ī–Ľ–ł–Ĺ–Ķ–Ĺ–ł–Ķ –į—ā—Ä–ł–ĺ–≤–Ķ–Ĺ—ā—Ä–ł–ļ—É–Ľ—Ź—Ä–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–ľ–ĺ—Ā—ā–ł) –Ĺ–Ķ –Ī—č–Ľ–ĺ. –ú–ĺ–∂–Ĺ–ĺ –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–ĺ–∂–ł—ā—Ć, —á—ā–ĺ —ā–į–ļ–ĺ–Ļ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–į –Ņ—Ä–ł 3-–ļ—Ä–į—ā–Ĺ–ĺ–ľ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–ł –≤ —Ā—É—ā–ļ–ł —É–ī–į–Ľ–ĺ—Ā—Ć –ī–ĺ–Ī–ł—ā—Ć—Ā—Ź –Ī–Ľ–į–≥–ĺ–ī–į—Ä—Ź —ā–ĺ–ľ—É, —á—ā–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č –Ņ–ĺ–Ľ—É—á–į–Ľ–ł –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö —Ā—ā–į—Ü–ł–ĺ–Ĺ–į—Ä–į –ł –Ņ—Ä–ł–Ĺ–ł–ľ–į–Ľ–ł –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č –≤ –Ņ—Ä–ł—Ā—É—ā—Ā—ā–≤–ł–ł –ľ–Ķ–ī–ł—Ü–ł–Ĺ—Ā–ļ–ł—Ö —Ä–į–Ī–ĺ—ā–Ĺ–ł–ļ–ĺ–≤. –í –į–ľ–Ī—É–Ľ–į—ā–ĺ—Ä–Ĺ—č—Ö —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ—Ā—ā—Ć –Ņ—Ä–ł–Ĺ–ł–ľ–į—ā—Ć –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā 3 —Ä/—Ā—É—ā –ľ–ĺ–∂–Ķ—ā —Ā–Ĺ–ł–∑–ł—ā—Ć —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć —ā–Ķ—Ä–į–Ņ–ł–ł –ł–∑-–∑–į –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ–Ļ –ļ–ĺ–ľ–Ņ–Ľ–į–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł. –í –į–ľ–Ī—É–Ľ–į—ā–ĺ—Ä–Ĺ—č—Ö —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –ľ–ĺ–∂–Ķ—ā –Ī—č—ā—Ć —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–ĺ–≤–į–Ĺ–ĺ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–į –≤ –Ľ–Ķ–ļ–į—Ä—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–Ļ —Ą–ĺ—Ä–ľ–Ķ ¬ę—ā–į–Ī–Ľ–Ķ—ā–ļ–ł –Ņ—Ä–ĺ–Ľ–ĺ–Ĺ–≥–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–≥–ĺ –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź¬Ľ.
–ē—Č–Ķ –ĺ–ī–Ĺ–ł–ľ —Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ—Ā–ļ–ł–ľ –Ņ—Ä–ł–∑–Ĺ–į–ļ–ĺ–ľ –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź –ł—ą–Ķ–ľ–ł–ł —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ė–Ď–° —Ź–≤–Ľ—Ź–Ľ–į—Ā—Ć –≥–ĺ—Ä–ł–∑–ĺ–Ĺ—ā–į–Ľ—Ć–Ĺ–į—Ź –ł–Ľ–ł –ļ–ĺ—Ā–ĺ–Ĺ–ł—Ā—Ö–ĺ–ī—Ź—Č–į—Ź –ī–Ķ–Ņ—Ä–Ķ—Ā—Ā–ł—Ź —Ā–Ķ–≥–ľ–Ķ–Ĺ—ā–į ST –≥–Ľ—É–Ī–ł–Ĺ–ĺ–Ļ –Ĺ–Ķ –ľ–Ķ–Ĺ–Ķ–Ķ 0,1 –ľ–í, –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć—é –Ĺ–Ķ –ľ–Ķ–Ĺ–Ķ–Ķ 0,06‚Äď0,08 —Ā –ĺ—ā —ā–ĺ—á–ļ–ł J –≤ –ĺ–ī–Ĺ–ĺ–ľ –ł –Ī–ĺ–Ľ–Ķ–Ķ –≠–ö–ď-–ĺ—ā–≤–Ķ–ī–Ķ–Ĺ–ł–Ļ. –Ē–Ľ—Ź –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–ł–∑–į—Ü–ł–ł –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ –Ĺ–į–ľ–ł –Ņ—Ä–ĺ–į–Ĺ–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–į —á–į—Ā—ā–ĺ—ā–į –≤—Ā—ā—Ä–Ķ—á–į–Ķ–ľ–ĺ—Ā—ā–ł —ć–Ņ–ł–∑–ĺ–ī–ĺ–≤ –ī–Ķ–Ņ—Ä–Ķ—Ā—Ā–ł–ł ST (2 –ł –Ī–ĺ–Ľ–Ķ–Ķ –ľ–ľ) –Ņ—Ä–ł —Ö–ĺ–Ľ—ā–Ķ—Ä–ĺ–≤—Ā–ļ–ĺ–ľ –ľ–ĺ–Ĺ–ł—ā–ĺ—Ä–ł—Ä–ĺ–≤–į–Ĺ–ł–ł –≠–ö–ď.
–Ě–į —Ā–Ľ–Ķ–ī—É—é—Č–Ķ–ľ —ć—ā–į–Ņ–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ľ—č –Ņ—Ä–ĺ–≤–Ķ–Ľ–ł —Ā—Ä–į–≤–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –į–Ĺ–į–Ľ–ł–∑ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –≤ –≥—Ä—É–Ņ–Ņ–į—Ö —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—Ź –Ņ–ĺ –≤–Ľ–ł—Ź–Ĺ–ł—é —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö —Ā–ĺ—á–Ķ—ā–į–Ĺ–ł–Ļ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –Ĺ–į —á–į—Ā—ā–ĺ—ā—É —ć–Ņ–ł–∑–ĺ–ī–ĺ–≤ –ł—ą–Ķ–ľ–ł–ł –Ņ–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ –ľ–ĺ–Ĺ–ł—ā–ĺ—Ä–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –≠–ö–ď –Ņ–ĺ –•–ĺ–Ľ—ā–Ķ—Ä—É (—ā–į–Ī–Ľ. 4).
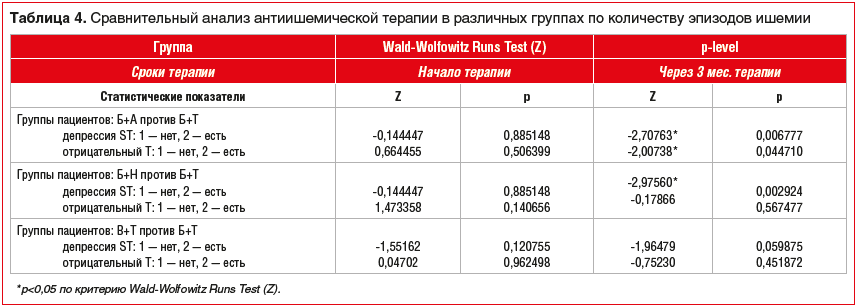
–°—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ—č–Ķ —Ä–į–∑–Ľ–ł—á–ł—Ź –≤ –Ņ–ĺ–Ľ—Ć–∑—É —É—Ä–Ķ–∂–Ķ–Ĺ–ł—Ź —ć–Ņ–ł–∑–ĺ–ī–ĺ–≤ –ł—ą–Ķ–ľ–ł–ł –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ—č –Ņ—Ä–ł –Ņ–ĺ–Ņ–į—Ä–Ĺ–ĺ–ľ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł –≤ –Ņ–ĺ–Ľ—Ć–∑—É –≥—Ä—É–Ņ–Ņ—č –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł—Ö –Ď+–Ę, –≤ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł —Ā –≥—Ä—É–Ņ–Ņ–į–ľ–ł, –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł–ľ–ł –Ď+–ź –ł –Ď+H. –Ę–į–ļ–∂–Ķ —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –∑–Ĺ–į—á–ł–ľ—č–Ķ —Ä–į–∑–Ľ–ł—á–ł—Ź –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ—č –≤ –Ņ–ĺ–Ľ—Ć–∑—É –í+–Ę –Ņ—Ä–ĺ—ā–ł–≤ –Ď+–Ę.
–ė—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–į –≤ —Ā–ĺ—á–Ķ—ā–į–Ĺ–ł–ł —Ā ő≤-–į–ī—Ä–Ķ–Ĺ–ĺ–Ī–Ľ–ĺ–ļ–į—ā–ĺ—Ä–į–ľ–ł (–Ď–ź–Ď) –ł–Ľ–ł –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–ĺ–ľ –ī–Ľ—Ź –ī–į–Ĺ–Ĺ–ĺ–Ļ –ļ–į—ā–Ķ–≥–ĺ—Ä–ł–ł –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ĺ–Ņ—ā–ł–ľ–į–Ľ—Ć–Ĺ—č–ľ —Ā —ā–ĺ—á–ļ–ł –∑—Ä–Ķ–Ĺ–ł—Ź —É—Ä–Ķ–∂–Ķ–Ĺ–ł—Ź —Ä–ł—ā–ľ–į –ł –ľ–ł–Ĺ–ł–ľ–ł–∑–į—Ü–ł–ł —ć–Ņ–ł–∑–ĺ–ī–ĺ–≤ –ī–Ķ–Ņ—Ä–Ķ—Ā—Ā–ł–ł —Ā–Ķ–≥–ľ–Ķ–Ĺ—ā–į ST –Ņ–ĺ –≠–ö–ď –ļ–į–ļ –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź –ł—ą–Ķ–ľ–ł–ł –ľ–ł–ĺ¬≠–ļ–į—Ä–ī–į. –í–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –≤ –ī–ĺ–∑–į—Ö 180‚Äď240 –ľ–≥/—Ā—É—ā –≤ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —Ā —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–ĺ–ľ 80 –ľ–≥/—Ā—É—ā (–í+–Ę) –ł–ľ–Ķ–Ľ–ł –ĺ–ī–ł–Ĺ–į–ļ–ĺ–≤—č–Ļ –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł–Ļ —ć—Ą—Ą–Ķ–ļ—ā —Ā —ā–Ķ—Ä–į–Ņ–ł–Ķ–Ļ –Ď+–Ę –Ņ—Ä–ł —É—Ā–Ľ–ĺ–≤–ł–ł –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź –ī–ĺ–∑—č –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į 7,5 –ľ–≥/—Ā—É—ā –ł –Ī–ĺ–Ľ–Ķ–Ķ –≤ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —Ā —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–ĺ–ľ 80 –ľ–≥/—Ā—É—ā. –í —ā–ĺ –∂–Ķ –≤—Ä–Ķ–ľ—Ź –Ņ—Ä–ł –Ĺ–į—Ä–į—Ā—ā–į–Ĺ–ł–ł –Ī—Ä–ĺ–Ĺ—Ö–ĺ–Ľ–Ķ–≥–ĺ—á–Ĺ—č—Ö —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤, —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č—Ö —Ā —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ –ī–ĺ–∑—č –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į, –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –ł–ľ–Ķ–Ľ —Ź–≤–Ĺ—č–Ķ –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤–į. –°—Ö–Ķ–ľ–į –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –í+–Ę –ł–ľ–Ķ–Ľ–į –Ĺ–į–ł–Ľ—É—á—ą—É—é –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć —É –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ (–•–ě–Ď–õ + –Ę–Ď) –Ņ—Ä–ł –ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ—č—Ö —Ä–ł—ā–ľ—É—Ä–Ķ–∂–į—é—Č–Ķ–ľ –ł –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ–ľ/–į–Ĺ—ā–ł¬≠–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–ľ —ć—Ą—Ą–Ķ–ļ—ā–į—Ö.
–Ę—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ, –≤ –ĺ—ā–Ľ–ł—á–ł–Ķ –ĺ—ā –Ĺ–ł—ā—Ä–į—ā–ĺ–≤ –ł –ī—Ä—É–≥–ł—Ö –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ—č—Ö —Ā—Ä–Ķ–ī—Ā—ā–≤, –Ĺ–Ķ –≤–Ľ–ł—Ź–Ķ—ā –Ĺ–į –≥–Ķ–ľ–ĺ–ī–ł–Ĺ–į–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ–į—Ä–į–ľ–Ķ—ā—Ä—č (–ź–Ē –ł –ß–°–°), —á—ā–ĺ —É–Ľ—É—á—ą–į–Ķ—ā –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć —ā–Ķ—Ä–į–Ņ–ł–ł –ł –Ņ–ĺ–≤—č—ą–į–Ķ—ā –Ņ—Ä–ł–≤–Ķ—Ä–∂–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ľ–Ķ—á–Ķ–Ĺ–ł—é. –ó–į—Č–ł—ā–Ĺ–ĺ–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ, –ļ–ĺ—ā–ĺ—Ä–ĺ–Ķ –ĺ–ļ–į–∑—č–≤–į–Ķ—ā —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ –Ĺ–į –ļ–į—Ä–ī–ł–ĺ–ľ–ł–ĺ—Ü–ł—ā—č –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –ł—ą–Ķ–ľ–ł–ł, –Ĺ–ĺ—Ā–ł—ā –ļ–ĺ–ľ–Ņ–Ľ–Ķ–ļ—Ā–Ĺ—č–Ļ —Ö–į—Ä–į–ļ—ā–Ķ—Ä. –Ę—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ —á–į—Ā—ā–ł—á–Ĺ–ĺ –Ņ–Ķ—Ä–Ķ–ļ–Ľ—é—á–į–Ķ—ā —ć–Ĺ–Ķ—Ä–≥–Ķ—ā–ł—á–Ķ—Ā–ļ–ł–Ļ –ĺ–Ī–ľ–Ķ–Ĺ —Ā –ĺ–ļ–ł—Ā–Ľ–Ķ–Ĺ–ł—Ź –ī–Ľ–ł–Ĺ–Ĺ–ĺ—Ü–Ķ–Ņ–ĺ—á–Ķ—á–Ĺ—č—Ö –∂–ł—Ä–Ĺ—č—Ö –ļ–ł—Ā–Ľ–ĺ—ā –Ĺ–į –ĺ–ļ–ł—Ā–Ľ–Ķ–Ĺ–ł–Ķ –≥–Ľ—é–ļ–ĺ–∑—č, —á—ā–ĺ –ĺ–Ņ—ā–ł–ľ–ł–∑–ł—Ä—É–Ķ—ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ –ļ–ł—Ā–Ľ–ĺ—Ä–ĺ–ī–į –ł —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ķ—ā —Ā–ł–Ĺ—ā–Ķ–∑ –ź–Ę–§ –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –ł—ą–Ķ–ľ–ł–ł, –į —ā–į–ļ–∂–Ķ —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É–Ķ—ā –Ī—č—Ā—ā—Ä–ĺ–Ļ –Ĺ–ĺ—Ä–ľ–į–Ľ–ł–∑–į—Ü–ł–ł –ļ–ł—Ā–Ľ–ĺ—ā–Ĺ–ĺ-—Č–Ķ–Ľ–ĺ—á–Ĺ–ĺ–≥–ĺ —Ä–į–≤–Ĺ–ĺ–≤–Ķ—Ā–ł—Ź –ł –∑–į–Ņ–į—Ā–ĺ–≤ –ļ—Ä–Ķ–į—ā–ł–Ĺ—Ą–ĺ—Ā—Ą–į—ā–į –Ņ—Ä–ł –≤–ĺ—Ā—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ł–ł –ļ—Ä–ĺ–≤–ĺ—ā–ĺ–ļ–į –≤ –ļ–ĺ—Ä–ĺ–Ĺ–į—Ä–Ĺ—č—Ö —Ā–ĺ—Ā—É–ī–į—Ö [19].
–í–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –≤ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł —Ā –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–ĺ–ľ —ā–į–ļ–∂–Ķ –ĺ–Ī–Ľ–į–ī–į–Ķ—ā —Ä—Ź–ī–ĺ–ľ –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ–Ļ –Ī—Ä–ĺ–Ĺ—Ö–ĺ–Ľ–Ķ–≥–ĺ—á–Ĺ–ĺ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–Ķ–Ļ, —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É—Ź —É—Ä–Ķ–∂–Ķ–Ĺ–ł—é –ß–°–°, –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ–ľ—É –ł –ļ–į—Ä–ī–ł–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–ľ—É —ć—Ą—Ą–Ķ–ļ—ā–į–ľ –Ī–Ķ–∑ —É—Ā—É–≥—É–Ī–Ľ–Ķ–Ĺ–ł—Ź –Ī—Ä–ĺ–Ĺ—Ö–ĺ–ĺ–Ī—Ā—ā—Ä—É–ļ—ā–ł–≤–Ĺ–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į. –ü–ĺ –Ľ–ł—ā–Ķ—Ä–į—ā—É—Ä–Ĺ—č–ľ –ī–į–Ĺ–Ĺ—č–ľ, —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č–Ķ ő≤1-–į–ī—Ä–Ķ–Ĺ–ĺ–Ī–Ľ–ĺ–ļ–į—ā–ĺ—Ä—č –ł –Ĺ–Ķ–ī–ł–≥–ł–ī—Ä–ĺ–Ņ–ł—Ä–ł–ī–ł–Ĺ–ĺ–≤—č–Ķ –į–Ĺ—ā–į–≥–ĺ–Ĺ–ł—Ā—ā—č –ļ–į–Ľ—Ć—Ü–ł—Ź –ĺ–Ī–Ľ–į–ī–į—é—ā —Ā–ĺ–Ņ–ĺ—Ā—ā–į–≤–ł–ľ—č–ľ –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ—č–ľ –ł –į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł–ľ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ –Ī–Ķ–∑ –ĺ—ā—Ä–ł—Ü–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–≥–ĺ –≤–Ľ–ł—Ź–Ĺ–ł—Ź –Ĺ–į –Ī—Ä–ĺ–Ĺ—Ö–ł–į–Ľ—Ć–Ĺ—É—é –Ņ—Ä–ĺ—Ö–ĺ–ī–ł–ľ–ĺ—Ā—ā—Ć [16‚Äď18]. –ö—Ä–ĺ–ľ–Ķ —ā–ĺ–≥–ĺ, –ĺ—ā–ľ–Ķ—á–į–Ķ—ā—Ā—Ź, —á—ā–ĺ –Ņ—Ä–ł –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–ľ –Ņ—Ä–ł–Ķ–ľ–Ķ –Ď–ź–Ď –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ –ł—Ö –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –≤–Ľ–ł—Ź–Ĺ–ł–Ķ –Ĺ–į –≤–ĺ—Ā—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ł–Ķ —Ą—É–Ĺ–ļ—Ü–ł–ł —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź –ļ–į–ļ –Ņ—Ä–ĺ–≥–Ĺ–ĺ—Ā—ā–ł—á–Ķ—Ā–ļ–ł –Ī–Ľ–į–≥–ĺ–Ņ—Ä–ł—Ź—ā–Ĺ–ĺ–≥–ĺ –ļ–ĺ–ľ–Ņ–ĺ–Ĺ–Ķ–Ĺ—ā–į. –°–Ľ–Ķ–ī–ĺ–≤–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ, –ī–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ —Ā–Ķ–Ľ–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö ő≤1-–į–ī—Ä–Ķ–Ĺ–ĺ–Ī–Ľ–ĺ–ļ–į—ā–ĺ—Ä–ĺ–≤ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ–ĺ–Ļ –Ī—Ä–ĺ–Ĺ—Ö–ĺ–Ľ–Ķ–≥–ĺ—á–Ĺ–ĺ–Ļ –ł —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ-—Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–Ķ–Ļ –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ –Ņ—Ä–ł —É–ī–ĺ–≤–Ľ–Ķ—ā–≤–ĺ—Ä–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā–ł —Ā –ĺ–∂–ł–ī–į–Ķ–ľ—č–ľ –Ņ—Ä–ĺ–≥–Ĺ–ĺ—Ā—ā–ł—á–Ķ—Ā–ļ–ł –Ī–Ľ–į–≥–ĺ–Ņ—Ä–ł—Ź—ā–Ĺ—č–ľ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ–ľ –Ĺ–į —Ą—É–Ĺ–ļ—Ü–ł–ł —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź.
–Ē–Ľ—Ź –ī–ł–≥–ł–ī—Ä–ĺ–Ņ–ł—Ä–ł–ī–ł–Ĺ–ĺ–≤—č—Ö –į–Ĺ—ā–į–≥–ĺ–Ĺ–ł—Ā—ā–ĺ–≤ –ļ–į–Ľ—Ć—Ü–ł—Ź (–į–ľ–Ľ–ĺ–ī–ł–Ņ–ł–Ĺ) –ł–∑–≤–Ķ—Ā—ā–Ķ–Ĺ —ć—Ą—Ą–Ķ–ļ—ā –Ī—Ä–ĺ–Ĺ—Ö–ĺ–ī–ł–Ľ–į—ā–į—Ü–ł–ł –ł —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—Ź –ī–į–≤–Ľ–Ķ–Ĺ–ł—Ź –≤ –ľ–į–Ľ–ĺ–ľ –ļ—Ä—É–≥–Ķ –ļ—Ä–ĺ–≤–ĺ–ĺ–Ī—Ä–į—Č–Ķ–Ĺ–ł—Ź, —á—ā–ĺ –ł–ľ–Ķ–Ķ—ā –ĺ—Ā–ĺ–Ī–Ķ–Ĺ–Ĺ—č–Ķ –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤–į –≤ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –ī–į–Ĺ–Ĺ–ĺ–Ļ –ļ–į—ā–Ķ–≥–ĺ—Ä–ł–ł –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤. –ě–ī–Ĺ–į–ļ–ĺ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł—Ź –į–ľ–Ľ–ĺ–ī–ł–Ņ–ł–Ĺ–į —Ā –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–ĺ–ľ –≤ –Ĺ–į—ą–Ķ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł —É –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ę–Ď, –•–ě–Ď–õ –ł –ė–Ď–° –Ĺ–Ķ –Ņ–ĺ–ļ–į–∑–į–Ľ–į –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤, –Ņ–ĺ-–≤–ł–ī–ł–ľ–ĺ–ľ—É, –≤—Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–Ķ –Ĺ–ł–≤–Ķ–Ľ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–ĺ–ľ —É–ļ–į–∑–į–Ĺ–Ĺ—č—Ö —ć—Ą—Ą–Ķ–ļ—ā–ĺ–≤ –į–ľ–Ľ–ĺ–ī–ł–Ņ–ł–Ĺ–į. –ö–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł—Ź –Ď+–ź —É—Ā–ł–Ľ–ł–≤–į–Ľ–į –≥–Ķ–ľ–ĺ–ī–ł–Ĺ–į–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ–ĺ–Ī–ĺ—á–Ĺ—č–Ķ —ć—Ą—Ą–Ķ–ļ—ā—č —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—Ź –ź–Ē, —á—ā–ĺ –≤ –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ –≥–ł–Ņ–Ķ—Ä—ā–Ķ–Ĺ–∑–ł–ł —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ņ—Ä–ł–≤–ĺ–ī–ł–Ľ–ĺ –ļ —ć–Ņ–ł–∑–ĺ–ī–į–ľ –≥–ł–Ņ–ĺ—ā–ĺ–Ĺ–ł–ł –ł —ā–į—Ö–ł–ļ–į—Ä–ī–ł–ł, –Ĺ–Ķ —ā—Ä–Ķ–Ī—É—é—Č–ł–ľ –ĺ—ā–ľ–Ķ–Ĺ—č –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤.
–ü—Ä–ł –ĺ—Ü–Ķ–Ĺ–ļ–Ķ –≤–Ľ–ł—Ź–Ĺ–ł—Ź –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ/–į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –Ĺ–į —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć —Ö–ł–ľ–ł–ĺ—ā–Ķ—Ä–į–Ņ–ł–ł –Ę–Ď —É –ļ–ĺ–ľ–ĺ—Ä–Ī–ł–ī–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ę–Ď, –•–ě–Ď–õ –ł –ė–Ď–° –Ī—č–Ľ–ł –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ—č —Ā–Ľ–Ķ–ī—É—é—Č–ł–Ķ –ī–į–Ĺ–Ĺ—č–Ķ. –ü–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ 3 –ľ–Ķ—Ā. —ā–Ķ—Ä–į–Ņ–ł–ł –Ĺ–Ķ–≥–į—ā–ł–≤–į—Ü–ł—Ź –ľ–į–∑–ļ–į –ī–ĺ—Ā—ā–ł–≥–Ĺ—É—ā–į —É 7 (41,2%) –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ď+–ź, 8 (47,1%) –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ď+–Ě, 11 (64,7%) –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≥—Ä—É–Ņ–Ņ–Ķ –Ď+–Ę –ł 10 (58,8%) –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≥—Ä—É–Ņ–Ņ–Ķ –í+–Ę. –ě—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ, —á—ā–ĺ –Ņ—Ä–ł –į–ī–Ķ–ļ–≤–į—ā–Ĺ–ĺ–Ļ –ł —Ö–ĺ—Ä–ĺ—ą–ĺ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ–Ļ –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł (–í+–Ę –ł –Ď+–Ę) –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–į—Ź –ī–ł–Ĺ–į–ľ–ł–ļ–į –≤ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –Ę–Ď –ĺ—ā–ľ–Ķ—á–į–Ľ–į—Ā—Ć –Ī—č—Ā—ā—Ä–Ķ–Ķ, –≤—Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–Ķ —á–Ķ–≥–ĺ —É –Ī–ĺ–Ľ–Ķ–Ķ —á–Ķ–ľ 50% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ (58,8‚Äď64,7%) –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–į –Ĺ–Ķ–≥–į—ā–ł–≤–į—Ü–ł—Ź –ľ–į–∑–ļ–į —á–Ķ—Ä–Ķ–∑ 3 –ľ–Ķ—Ā. —ā–Ķ—Ä–į–Ņ–ł–ł: —ć—ā–ĺ –Ņ—Ä–ĺ–ł–∑–ĺ—ą–Ľ–ĺ –≤ –≥—Ä—É–Ņ–Ņ–į—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł—Ö —ā–Ķ—Ä–į–Ņ–ł—é –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–Ķ —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–į –≤ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —Ā –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–ĺ–ľ –ł–Ľ–ł –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–ĺ–ľ (–í+–Ę –ł–Ľ–ł –Ď+–Ę).
–ó–į–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ
–ě–Ņ—ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –ė–Ď–° –Ĺ–į —Ā–Ķ–≥–ĺ–ī–Ĺ—Ź—ą–Ĺ–ł–Ļ –ī–Ķ–Ĺ—Ć –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ—Ź–Ķ—ā—Ā—Ź –ļ–į–ļ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ, –ļ–ĺ—ā–ĺ—Ä–ĺ–Ķ –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É–Ķ—ā —Ā–ł–ľ–Ņ—ā–ĺ–ľ—č –ł –Ņ—Ä–Ķ–ī–ĺ—ā–≤—Ä–į—Č–į–Ķ—ā —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č–Ķ —Ā –ė–Ď–° –ļ–į—Ä–ī–ł–į–Ľ—Ć–Ĺ—č–Ķ —Ā–ĺ–Ī—č—ā–ł—Ź –Ņ—Ä–ł –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–Ļ –Ņ—Ä–ł–≤–Ķ—Ä–∂–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į –Ľ–Ķ—á–Ķ–Ĺ–ł—é –ł –ľ–ł–Ĺ–ł–ľ–į–Ľ—Ć–Ĺ—č—Ö –Ņ–ĺ–Ī–ĺ—á–Ĺ—č—Ö —ć—Ą—Ą–Ķ–ļ—ā–į—Ö. –ö—Ä–ĺ–ľ–Ķ —ā–ĺ–≥–ĺ, –≤–į–∂–Ĺ–Ķ–Ļ—ą–ł–ľ –į—Ā–Ņ–Ķ–ļ—ā–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ę–Ď, –ė–Ď–° –ł –•–ě–Ď–õ —Ź–≤–Ľ—Ź–Ľ–ĺ—Ā—Ć –≤—č–∑–ī–ĺ—Ä–ĺ–≤–Ľ–Ķ–Ĺ–ł–Ķ –ĺ—ā –Ę–Ď. –Ě–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ —ā–į–ļ–∂–Ķ —É—á–ł—ā—č–≤–į—ā—Ć, —á—ā–ĺ —Ā–į–ľ–į —Ö–ł–ľ–ł–ĺ—ā–Ķ—Ä–į–Ņ–ł—Ź –Ę–Ď —ā–ĺ–ļ—Ā–ł—á–Ķ—Ā–ļ–ł –ī–Ķ–Ļ—Ā—ā–≤—É–Ķ—ā –Ĺ–į —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ-—Ā–ĺ—Ā—É–ī–ł—Ā—ā—É—é —Ā–ł—Ā—ā–Ķ–ľ—É, —É—Ö—É–ī—ą–į—Ź –≥–Ķ–ľ–ĺ–ī–ł–Ĺ–į–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ–į—Ä–į–ľ–Ķ—ā—Ä—č –ł —É—Ā–ł–Ľ–ł–≤–į—Ź –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź [15].
–ü–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ —ć—Ą—Ą–Ķ–ļ—ā –Ī—č–Ľ –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ –≤–ĺ –≤—Ā–Ķ—Ö 4 –≥—Ä—É–Ņ–Ņ–į—Ö –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź: –Ď+–ź, –Ď+–Ě, –Ď+–Ę, –í+–Ę. –≠—ā–ĺ —Ā–≤—Ź–∑–į–Ĺ–ĺ —Ā –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ–ł–Ķ–ľ –į–ī–Ķ–ļ–≤–į—ā–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł —Ā–ĺ–≥–Ľ–į—Ā–Ĺ–ĺ –ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–ľ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł—Ź–ľ –Ņ–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—é —Ā—ā–į–Ī–ł–Ľ—Ć–Ĺ–ĺ–Ļ –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ī–ĺ–Ľ–Ķ–∑–Ĺ–ł —Ā–Ķ—Ä–ī—Ü–į 2019 –≥. [16]. –Ē—Ä—É–≥–ł–ľ –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ –į—Ā–Ņ–Ķ–ļ—ā–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö —Ā—ā–į—Ü–ł–ĺ–Ĺ–į—Ä–į —Ź–≤–Ľ—Ź–Ľ–į—Ā—Ć –Ķ–≥–ĺ –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É–Ķ–ľ–ĺ—Ā—ā—Ć –ľ–Ķ–ī–ł—Ü–ł–Ĺ—Ā–ļ–ł–ľ –Ņ–Ķ—Ä—Ā–ĺ–Ĺ–į–Ľ–ĺ–ľ, —á—ā–ĺ –ĺ–Ī–Ķ—Ā–Ņ–Ķ—á–ł–≤–į–Ľ–ĺ —Ä–Ķ–≥—É–Ľ—Ź—Ä–Ĺ—č–Ļ –Ņ—Ä–ł–Ķ–ľ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –Ī–ĺ–Ľ—Ć–Ĺ—č–ľ–ł. –í–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –≤ –ī–ĺ–∑–Ķ 180‚Äď240 –ľ–≥/—Ā—É—ā –≤ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —Ā —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–ĺ–ľ 80 –ľ–≥/—Ā—É—ā (–í+–Ę) –ł–ľ–Ķ–Ľ–ł –Ņ—Ä–ł–ľ–Ķ—Ä–Ĺ–ĺ –ĺ–ī–ł–Ĺ–į–ļ–ĺ–≤—č–Ļ –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ—č–Ļ/–į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł–Ļ —ć—Ą—Ą–Ķ–ļ—ā –≤ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł —Ā —Ä–Ķ–∂–ł–ľ–ĺ–ľ —ā–Ķ—Ä–į–Ņ–ł–ł –Ď+–Ę –Ņ—Ä–ł —É—Ā–Ľ–ĺ–≤–ł–ł –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł—Ź –ī–ĺ–∑—č –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į 7,5 –ľ–≥/—Ā—É—ā –ł –Ī–ĺ–Ľ–Ķ–Ķ –≤ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —Ā —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–ĺ–ľ 80 –ľ–≥/—Ā—É—ā. –í —ā–ĺ –∂–Ķ –≤—Ä–Ķ–ľ—Ź –Ņ—Ä–ł –Ĺ–į—Ä–į—Ā—ā–į–Ĺ–ł–ł –Ī—Ä–ĺ–Ĺ—Ö–ĺ–Ľ–Ķ–≥–ĺ—á–Ĺ—č—Ö —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤, —Ā–≤—Ź–∑–į–Ĺ–Ĺ—č—Ö —Ā —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ –ī–ĺ–∑—č –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–į, –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ –ł–ľ–Ķ–Ķ—ā —Ź–≤–Ĺ—č–Ķ –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤–į. –Ę–Ķ—Ä–į–Ņ–ł—Ź –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–ĺ–ľ —Ā —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–ĺ–ľ –ł–ľ–Ķ–Ľ–į –Ĺ–į–ł–Ľ—É—á—ą—É—é –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ę–Ď, –ė–Ď–° –ł –•–ě–Ď–õ –Ņ—Ä–ł –ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ—č—Ö —Ä–ł—ā–ľ—É—Ä–Ķ–∂–į—é—Č–Ķ–ľ –ł –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ–ľ/–į–Ĺ—ā–ł–ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–ľ —ć—Ą—Ą–Ķ–ļ—ā–į—Ö. –í–Ķ—Ä–ĺ—Ź—ā–Ĺ–Ķ–Ķ –≤—Ā–Ķ–≥–ĺ, —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ī—Ä–ĺ–Ĺ—Ö–ĺ–Ľ–Ķ–≥–ĺ—á–Ĺ–ĺ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–Ķ–Ļ, –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł—Ö –Ņ—Ä–ĺ—ā–ł–≤–ĺ—ā—É–Ī–Ķ—Ä–ļ—É–Ľ–Ķ–∑–Ĺ—č–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č, –ļ–ĺ—ā–ĺ—Ä—č–Ķ —Ā–į–ľ–ł –Ņ–ĺ —Ā–Ķ–Ī–Ķ –ľ–ĺ–≥—É—ā –Ĺ–į—Ä—É—ą–į—ā—Ć —Ä–į–Ī–ĺ—ā—É —Ā–Ķ—Ä–ī—Ü–į –ł –ĺ–ļ–į–∑—č–≤–į—ā—Ć –ī–ĺ–Ņ–ĺ–Ľ–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –Ņ–ĺ–≤—Ä–Ķ–∂–ī–į—é—Č–Ķ–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ –Ĺ–į —Ā–ĺ—Ā—É–ī–ł—Ā—ā—É—é —Ā—ā–Ķ–Ĺ–ļ—É, –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ–ł–Ķ —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–į –ĺ–ļ–į–∑—č–≤–į–Ľ–ĺ —Ü–ł—ā–ĺ–Ņ—Ä–ĺ—ā–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ –Ĺ–į –ľ–ł–ĺ–ļ–į—Ä–ī –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –≥–ł–Ņ–ĺ–ļ—Ā–ł–ł. –ö –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ —Ā–≤–ĺ–Ļ—Ā—ā–≤–į–ľ —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–į –ľ–ĺ–∂–Ĺ–ĺ –ĺ—ā–Ĺ–Ķ—Ā—ā–ł –ł –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ –ī–ĺ–Ņ–ĺ–Ľ–Ĺ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –≥–Ķ–ľ–ĺ–ī–ł–Ĺ–į–ľ–ł—á–Ķ—Ā–ļ–ł—Ö —ć—Ą—Ą–Ķ–ļ—ā–ĺ–≤, –Ņ—Ä–ł–≤–ĺ–ī—Ź—Č–ł—Ö –ļ –≥–ł–Ņ–ĺ—ā–ĺ–Ĺ–ł–ł –ł —ā–į—Ö–ł–ļ–į—Ä–ī–ł–ł, –ļ–į–ļ –≤ —Ā–Ľ—É—á–į–Ķ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–Ļ –Ď+–ź –ł –Ď+–Ě. –≠—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į —Ā–ĺ —Ā—ā–Ķ–Ĺ–ĺ–ļ–į—Ä–ī–ł–Ķ–Ļ –≤—č—Ā–ĺ–ļ–ĺ–≥–ĺ –§–ö —Ā —É—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–ł–Ķ–ľ –Ņ–ĺ–≤—Ā–Ķ–ī–Ĺ–Ķ–≤–Ĺ—č—Ö —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤ –ł—ą–Ķ–ľ–ł–ł –ľ–ł–ĺ–ļ–į—Ä–ī–į –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–Ķ —ā—Ä–ł–ľ–Ķ—ā–į–∑–ł–ī–ł–Ĺ–į –≤ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —Ā –≤–Ķ—Ä–į–Ņ–į–ľ–ł–Ľ–ĺ–ľ –ł–Ľ–ł –Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ–ĺ–ľ –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ľ–ĺ –Ĺ–Ķ —ā–ĺ–Ľ—Ć–ļ–ĺ —É–Ľ—É—á—ą–ł—ā—Ć —Ā—É–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ–ĺ–Ķ —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ĺ–ĺ –ł –Ĺ–į–Ņ—Ä—Ź–ľ—É—é —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤–ĺ–≤–į–Ľ–ĺ –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–ł—é –ļ–ĺ–ľ–Ņ–Ľ–į–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –≤ —ā. —á. –≤ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –Ę–Ď, —Ā –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł–Ķ–ľ –Ĺ–Ķ–≥–į—ā–ł–≤–į—Ü–ł–ł –ľ–į–∑–ļ–į –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 3 –ľ–Ķ—Ā. –Ī–ĺ–Ľ–Ķ–Ķ —á–Ķ–ľ —É –Ņ–ĺ–Ľ–ĺ–≤–ł–Ĺ—č –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö (58,8‚Äď64,7%). –Ę–į–ļ–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ, –ľ–ĺ–∂–Ĺ–ĺ –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–ĺ–∂–ł—ā—Ć, —á—ā–ĺ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–į—Ź –į–Ĺ—ā–ł–į–Ĺ–≥–ł–Ĺ–į–Ľ—Ć–Ĺ–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤–ĺ–≤–į–Ľ–į –≤ –ł—ā–ĺ–≥–Ķ –Ī–ĺ–Ľ–Ķ–Ķ –Ī—č—Ā—ā—Ä–ĺ–ľ—É –į–Ī–į—Ü–ł–Ľ–Ľ–ł—Ä–ĺ–≤–į–Ĺ–ł—é –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤.












