–Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є—В–Є—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –•–Ю–С–Ы
–Р—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П (–Р–У) —П–≤–ї—П–µ—В—Б—П —Б–∞–Љ–Њ–є —З–∞—Б—В–Њ–є –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –ї–µ–≥–Ї–Є—Е (–•–Ю–С–Ы) [1вАУ3]. –І–∞—Б—В–∞—П –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В—М –Р–У –Є –•–Ю–С–Ы –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –љ–∞–ї–Є—З–Є–µ–Љ —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є —Н—В–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ъ –і–∞–љ–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ –Љ–Њ–ґ–љ–Њ –Њ—В–љ–µ—Б—В–Є: —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є, –∞—А—В–µ—А–Є–∞–ї—М–љ—Г—О –≥–Є–њ–Њ–Ї—Б–µ–Љ–Є—О –Є –≥–Є–њ–µ—А–Ї–∞–њ–љ–Є—О, –Є–Ј–Љ–µ–љ–µ–љ–љ—Г—О –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї—Г –≤ –Љ–∞–ї–Њ–Љ –Ї—А—Г–≥–µ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ–Ї—А–µ—Ж–Є–Є –∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–∞, –Є–Ј–±—Л—В–Њ—З–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —А–µ–љ–Є–љ-–∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ-–∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л (–†–Р–Р–°) –Є —Б–Є–Љ–њ–∞—В–Њ–∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Ї–Њ–ї–µ–±–∞–љ–Є–µ –≤–љ—Г—В—А–Є–≥—А—Г–і–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –њ—А–Є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є –Є –і—А. [3]. –Я—А–Є –•–Ю–С–Ы –ї–µ–≥–Њ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Є–Љ–µ–µ—В —Б–Љ–µ—И–∞–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –Ј–∞ —Б—З–µ—В —В–Ї–∞–љ–µ–≤–Њ–≥–Њ, —Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ –Є –≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Є —З–µ—А–µ–Ј –љ–∞—А—Г—И–µ–љ–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї –±–Њ–ї–µ–µ —В—П–ґ–µ–ї–Њ–Љ—Г —В–µ—З–µ–љ–Є—О –Р–У [1вАУ3]. –Т—Б–ї–µ–і—Б—В–≤–Є–µ —Б–љ–Є–ґ–µ–љ–Є—П —Г—А–Њ–≤–љ—П –њ–∞—А—Ж–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –≤ –Ї—А–Њ–≤–Є –љ–∞ —Д–Њ–љ–µ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є —Е–µ–Љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ —Б–Њ—Б—Г–і–∞—Е —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є—П, –∞ —В–∞–Ї–ґ–µ –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Б–µ–Ї—А–µ—Ж–Є—П –∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –і–µ–є—Б—В–≤–Є—П –∞–і—А–µ–љ–Њ–Ї–Њ—А—В–Є–Ї–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О –љ–∞–і–њ–Њ—З–µ—З–љ–Є–Ї–Њ–≤. –Я—А–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–Љ —Б–њ–∞–Ј–Љ–µ, –Ї–Њ—В–Њ—А—Л–є –њ—А–Є–≤–Њ–і–Є—В –Ї –Є—И–µ–Љ–Є–Є –њ–∞—А–µ–љ—Е–Є–Љ—Л –њ–Њ—З–µ–Ї, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Б–µ–Ї—А–µ—Ж–Є—П —О–Ї—Б—В–∞–≥–ї–Њ–Љ–µ—А—Г–ї—П—А–љ—Л–Љ –∞–њ–њ–∞—А–∞—В–Њ–Љ —А–µ–љ–Є–љ–∞ –∞–Ї—В–Є–≤–Є—А—Г–µ—В –†–Р–Р–°, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б—В–Њ–є–Ї–Њ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О —Г—А–Њ–≤–љ—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–Р–Ф) [2]. –Ш–Ј–±—Л—В–Њ—З–љ–∞—П –њ–Њ—Б—В–Њ—П–љ–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –†–Р–Р–° –њ—А–Є–≤–Њ–і–Є—В –Ї —В–Њ–Љ—Г, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –≥–Є–њ–Њ–Ї—Б–Є–Є —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –≤—Л—А–∞–±–Њ—В–Ї–∞ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ–Њ–≤—Л—И–µ–љ–Є—О –Р–Ф, –∞ —В–∞–Ї–ґ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–∞, —З—В–Њ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї –≥–Є–њ–Њ–Ї–∞–ї–Є–µ–Љ–Є–Є –Є —Б–љ–Є–ґ–µ–љ–Є—О —Б–Є–ї—Л –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –Љ—Л—И—Ж, –∞ –≤ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є вАФ –Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –і—Л—Е–∞—В–µ–ї—М–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є [1вАУ3]. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –†–Р–Р–° –љ–∞ —Д–Њ–љ–µ –≥–Є–њ–Њ–Ї—Б–Є–Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ–Њ–ї–Є—Ж–Є—В–µ–Љ–Є—П, –Ї–Њ—В–Њ—А–∞—П —Г –±–Њ–ї—М–љ—Л—Е —Б –•–Ю–С–Ы –Ј–∞ —Б—З–µ—В –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–∞ —Д—Г–љ–Ї—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є—П —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є–Є –Є –њ–Њ–≤—Л—И–µ–љ–Є—О –Р–Ф. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –љ–∞—А—Г—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –±–Њ–ї—М—И–Њ–Љ, –љ–Њ –Є –≤ –Љ–∞–ї–Њ–Љ –Ї—А—Г–≥—Г –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –њ—А–Є–≤–Њ–і—П –Ї —А–∞–Ј–≤–Є—В–Є—О –ї–µ–≥–Њ—З–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є.
–Э–∞ —Д–Њ–љ–µ —А–∞–Ј–≤–Є–≤–∞—О—Й–µ–є—Б—П —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤–Њ–Ј–љ–Є–Ї–∞—О—В —Б—В—А—Г–Ї—В—Г—А–љ–Њ-—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –≤ –≤–Є–і–µ –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –Є –њ–Њ–≤—Л—И–µ–љ–Є—П –µ–µ –ґ–µ—Б—В–Ї–Њ—Б—В–Є [4]. –Т–Њ–Ј–љ–Є–Ї–∞—О—Й–∞—П —А–Є–≥–Є–і–љ–Њ—Б—В—М –∞—А—В–µ—А–Є–є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ —З–∞—Б—В–Њ—В—Г –і—Л—Е–∞–љ–Є—П, —Б—В–µ–њ–µ–љ—М –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є, —З–∞—Б—В–Њ—В—Г —Б–µ—А–і–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є, –∞ —В–∞–Ї–ґ–µ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –њ–Њ–≤—Л—И–µ–љ–Є–µ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –њ—Г–ї—М—Б–Њ–≤–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П [5вАУ12].
–Ш–Ј–±—Л—В–Њ—З–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –†–Р–Р–° —Г –±–Њ–ї—М–љ—Л—Е –Р–У –Є –•–Ю–С–Ы –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —Б —Г—З–µ—В–Њ–Љ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ —Н—В—Г —Б–Є—Б—В–µ–Љ—Г. –Ґ–∞–Ї–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –Њ–±–ї–∞–і–∞—О—В –Є–љ–≥–Є–±–Є—В–Њ—А—Л –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (–Є–Р–Я–§) [4]. –£–љ–Є–Ї–∞–ї—М–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Є–Р–Я–§ –њ—А–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Б–Њ—Б—В–Њ–Є—В –≤ —В–Њ–Љ, —З—В–Њ –Њ–љ–Є –і–∞—О—В –і–≤–Њ–є–љ–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В: –Њ—Б–ї–∞–±–ї—П—О—В –∞–≥—А–µ—Б—Б–Є—О –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II (–њ—А–µ—Б—Б–Њ—А–љ–Њ–µ –Ј–≤–µ–љ–Њ) –Є —В–µ–Љ —Б–∞–Љ—Л–Љ –Њ–Ї–∞–Ј—Л–≤–∞—О—В —В–∞–Ї–Є–µ –≤–∞–ґ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, –Ї–∞–Ї —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –і–∞–≤–ї–µ–љ–Є—П –≤ –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є, –Ї–∞—А–і–Є–Њ- –Є –≤–∞–Ј–Њ–њ—А–Њ—В–µ–Ї—Ж–Є—П, –±—А–Њ–љ—Е–Њ–і–Є–ї–∞—В–∞—Ж–Є—П [2, 3], –Є —Г—Б–Є–ї–Є–≤–∞—О—В –Ј–∞—Й–Є—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞ (–і–µ–њ—А–µ—Б—Б–Њ—А–љ–Њ–µ –Ј–≤–µ–љ–Њ). –Ш–Љ–µ–љ–љ–Њ –±—А–∞–і–Є–Ї–Є–љ–Є–љ–Њ–≤—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Є–Р–Я–§, –Є–≥—А–∞—О—Й–Є–є –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є–Є —Б–µ—А–і—Ж–∞ –Є —Б–Њ—Б—Г–і–Њ–≤, –ї–µ–ґ–Є—В –≤ –Њ—Б–љ–Њ–≤–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ї–∞—И–ї—П, –Ї–Њ—В–Њ—А—Л–є, –Њ–і–љ–∞–Ї–Њ, –≤—Б—В—А–µ—З–∞–µ—В—Б—П –Ї—А–∞–є–љ–µ —А–µ–і–Ї–Њ, —Б–Њ—Б—В–∞–≤–ї—П—П –≤ —Б—А–µ–і–љ–µ–Љ –љ–µ –±–Њ–ї–µ–µ 5% [4].
–Ч–љ–∞—З–µ–љ–Є–µ –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П
–Ф–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –љ–µ —В–Њ–ї—М–Ї–Њ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М, –љ–Њ –Є –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –Р–Ф (–Т–Р–Ф), —В. –µ. –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П –Р–Ф –Њ—В —Б—А–µ–і–љ–µ–≥–Њ —Г—А–Њ–≤–љ—П –Ј–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –њ—А–Њ–Љ–µ–ґ—Г—В–Њ–Ї –≤—А–µ–Љ–µ–љ–Є, –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Њ—А–≥–∞–љ–Њ–≤-–Љ–Є—И–µ–љ–µ–є [5вАУ8] –Є –њ—А–Є–Ј–љ–∞–µ—В—Б—П —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [6, 7]. –Т–Р–Ф –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ —Ж–µ–ї—Л–Љ —А—П–і–Њ–Љ –њ—А–Є—З–Є–љ: –љ–µ–є—А–Њ—А–µ—Д–ї–µ–Ї—В–Њ—А–љ—Л—Е, –≥—Г–Љ–Њ—А–∞–ї—М–љ—Л—Е, –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є—Е –Є –і—А. [4].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –µ–і–Є–љ–Њ–є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –Т–Р–Ф –љ–µ—В. –Т—Б–µ —А–Є—В–Љ–Є—З–µ—Б–Ї–Є–µ –Ї–Њ–ї–µ–±–∞–љ–Є—П –Р–Ф (beat-to-beat variability) –і–µ–ї—П—В—Б—П –љ–∞ –Ї—А–∞—В–Ї–Њ—Б—А–Њ—З–љ—Г—О –Т–Р–Ф (short-term blood pressure variability), –≤–Ї–ї—О—З–∞—О—Й—Г—О –≤–љ—Г—В—А–Є–≤–Є–Ј–Є—В–љ—Г—О –Є —Б—Г—В–Њ—З–љ—Г—О; —Б—А–µ–і–љ–µ—Б—А–Њ—З–љ—Г—О –Т–Р–Ф, –Є–ї–Є –Т–Р–Ф –≤ —А–∞–Ј–љ—Л–µ –і–љ–Є (day-to-day blood pressure variability); –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ—Г—О –Т–Р–Ф (long term blood pressure variability), –∞ –Є–Љ–µ–љ–љ–Њ –Љ–µ–ґ–≤–Є–Ј–Є—В–љ—Г—О –Є —Б–µ–Ј–Њ–љ–љ—Г—О [4, 5].
–І—В–Њ–±—Л –Њ—Ж–µ–љ–Є—В—М –Т–Р–Ф, –њ—А–Є–Љ–µ–љ—П—О—В —А–∞–Ј–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є. –І–∞—Й–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ (standard deviation, SD) –Є–ї–Є –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –≤–∞—А–Є–∞—Ж–Є–є (—Бoefficient of variations), —А–∞–≤–љ—Л–є SD/M, –≥–і–µ M вАФ —Б—А–µ–і–љ–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Р–Ф [4]. –°—Г—В–Њ—З–љ—Г—О –Т–Р–Ф —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В —А–∞—Б—Б—З–Є—В—Л–≤–∞—В—М —Б –њ–Њ–њ—А–∞–≤–Ї–Њ–є –љ–∞ –њ–µ—А–Є–Њ–і—Л —Д–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–љ—П –Є –љ–Њ—З–Є (SDdn) [4]. –Ґ–∞–Ї–ґ–µ –≤–∞–ґ–љ–Њ —А–∞—Б—Б—З–Є—В—Л–≤–∞—В—М —А–∞–Ј–љ–Є—Ж—Г –Љ–µ–ґ–і—Г –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–Љ –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Ј–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –њ–µ—А–Є–Њ–і –≤—А–µ–Љ–µ–љ–Є –њ—А–Є —Б–∞–Љ–Њ–Ї–Њ–љ—В—А–Њ–ї–µ –±–Њ–ї—М–љ—Л–Љ —Г—А–Њ–≤–љ—П –Р–Ф [7, 13].
–Т 2010 –≥. –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ–µ—А–≤–Њ–µ –Ї—А—Г–њ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤–Ї–ї—О—З–∞–≤—И–µ–µ –Є–Ј—Г—З–µ–љ–Є–µ –Т–Р–Ф (Anglo-Scandinavian Cardiac Outcomes Trial, ASCOT) [14].
–Я–Њ–Ј–і–љ–µ–µ (2015) –њ–Њ—П–≤–Є–ї–Є—Б—М –і–∞–љ–љ—Л–µ —Б—Г–±–∞–љ–∞–ї–Є–Ј–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П ALLHAT (Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial), –≤ –Ї–Њ—В–Њ—А–Њ–Љ –Є–Ј—Г—З–∞–ї–∞—Б—М –Љ–µ–ґ–≤–Є–Ј–Є—В–љ–∞—П –Т–Р–Ф —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф (–°–Р–Ф) –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф (–Ф–Р–Ф) —Б —Ж–µ–ї—М—О –Є–Ј—Г—З–µ–љ–Є—П –Є—Е –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є [15].
–Я–Њ –і–∞–љ–љ—Л–Љ –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є (K.M. Diaz et al., 2014), –∞–љ–∞–ї–Є–Ј –Љ–µ–ґ–≤–Є–Ј–Є—В–љ–Њ–є –Т–Р–Ф –і–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В–Є –°–Р–Ф –љ–∞ –Ї–∞–ґ–і—Л–µ 5 –Љ–Љ —А—В. —Б—В. –њ–Њ–≤—Л—И–∞–µ—В—Б—П —А–Є—Б–Ї –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є —Б–µ—А–і—Ж–∞ –љ–∞ 27%, –Є–љ—Б—Г–ї—М—В–∞ вАФ –љ–∞ 17%, –Њ–±—Й–µ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є вАФ –љ–∞ 22% [16].
–Ш–Ј—Г—З–∞–ї–Њ—Б—М —В–∞–Ї–ґ–µ –≤–ї–Є—П–љ–Є–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ –Т–Р–Ф. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, —Б—Г—Й–µ—Б—В–≤—Г—О—В –Њ—В–і–µ–ї—М–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ –Ї–Њ—В–Њ—А—Л—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М —А–µ–Ј—Г–ї—М—В–∞—В—Л –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є —А–∞–Ј–љ—Л–Љ–Є –Ї–ї–∞—Б—Б–∞–Љ–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ—Г—О –Т–Р–Ф –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ [17].
–Т–ї–Є—П–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§
–љ–∞ –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П
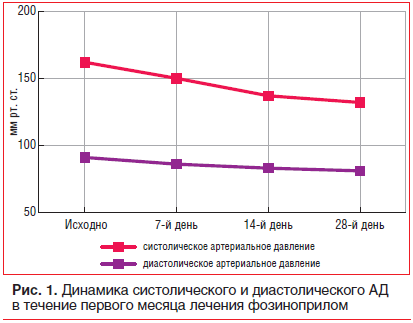
–Ф–ї–Є—В–µ–ї—М–љ—Л–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –Њ–њ—Л—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Є–Р–Я–§ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е –Р–У –Є –•–Ю–С–Ы –њ–Њ–Ј–≤–Њ–ї–Є–ї –љ–∞–Љ –Њ–њ—А–µ–і–µ–ї–Є—В—М —Н—В–Њ—В –њ—А–µ–њ–∞—А–∞—В –Ї–∞–Ї —Б—В—А–∞—В–µ–≥–Є—З–µ—Б–Ї–Є –≤–∞–ґ–љ—Л–є –≤ –ї–µ—З–µ–љ–Є–Є –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —В. –Ї. –Њ–љ –Њ–±–ї–∞–і–∞–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ (—А–Є—Б. 1, 2), –љ–Њ –Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є –њ–ї–µ–є–Њ—В—А–Њ–њ–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є, –∞ —В–∞–Ї–ґ–µ –њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ —В–µ—З–µ–љ–Є–µ –•–Ю–С–Ы [18].
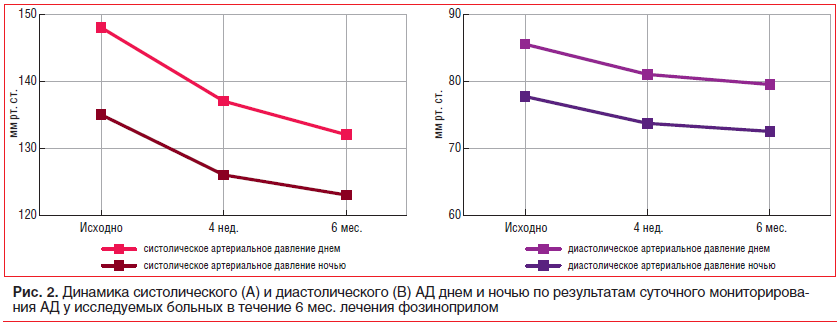
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–∞–Љ–Є –Є–Ј—Г—З–µ–љ–Њ –≤–ї–Є—П–љ–Є–µ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е –Р–У –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –•–Ю–С–Ы –љ–∞ –Ї—А–∞—В–Ї–Њ—Б—А–Њ—З–љ—Г—О, —Б—Г—В–Њ—З–љ—Г—О –Є –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ—Г—О –Т–Р–Ф [18]. –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –Р–Ф –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–∞–Ї –і–љ–µ–≤–љ–Њ–є, —В–∞–Ї –Є –љ–Њ—З–љ–Њ–є –Т–Р–Ф. –Т–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –°–Р–Ф –і–љ–µ–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –±—Л–ї–∞ –Є—Б—Е–Њ–і–љ–Њ 16,3¬±4,3 –Љ–Љ —А—В. —Б—В. –Є –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —З–µ—А–µ–Ј 6 –Љ–µ—Б. –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–Ј–Є–ї–∞—Б—М –і–Њ 13,5¬±2,9 –Љ–Љ —А—В. —Б—В. (—А<0,001). –Т–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –°–Р–Ф –≤ –љ–Њ—З–љ–Њ–µ –≤—А–µ–Љ—П –Є—Б—Е–Њ–і–љ–Њ –±—Л–ї–∞ 17,0¬±10,7 –Љ–Љ —А—В. —Б—В. –Є —З–µ—А–µ–Ј 6 –Љ–µ—Б. —Б–Њ—Б—В–∞–≤–Є–ї–∞ 15,0¬±8,7 –Љ–Љ —А—В. —Б—В. (—А<0,001). –Т–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –Ф–Р–Ф –і–љ–µ–Љ –Є—Б—Е–Њ–і–љ–Њ –±—Л–ї–∞ 12,6¬±4,3 –Љ–Љ —А—В. —Б—В. –Є —Б–љ–Є–Ј–Є–ї–∞—Б—М –і–Њ 9,9¬±1,6 –Љ–Љ —А—В. —Б—В. —З–µ—А–µ–Ј 6 –Љ–µ—Б. –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (—А<0,001). –Т–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –Ф–Р–Ф –≤ –љ–Њ—З–љ–Њ–µ –≤—А–µ–Љ—П –Є—Б—Е–Њ–і–љ–Њ –±—Л–ї–∞ 11,7¬±6,7 –Љ–Љ —А—В. —Б—В. –Є —Б–љ–Є–Ј–Є–ї–∞—Б—М –і–Њ 10,9¬±7,9 –Љ–Љ —А—В. —Б—В. —З–µ—А–µ–Ј 6 –Љ–µ—Б. –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (—А=0,2).
–Я—А–Є –Є–Ј—Г—З–µ–љ–Є–Є –Ї—А–∞—В–Ї–Њ—Б—А–Њ—З–љ–Њ–є –Т–Р–Ф –љ–∞ 28-–є –і–µ–љ—М –ї–µ—З–µ–љ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –≤–љ—Г—В—А–Є–≤–Є–Ј–Є—В–љ–∞—П –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –Ф–Р–Ф –Љ–µ–ґ–і—Г –≤—В–Њ—А—Л–Љ –Є —В—А–µ—В—М–Є–Љ –Є–Ј–Љ–µ—А–µ–љ–Є—П–Љ–Є —Б—В–∞–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–Є–ґ–µ (—А=0,04).
–Ґ–∞–Ї–ґ–µ –љ–∞–Љ–Є –±—Л–ї –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ —В–∞–Ї–Њ–є –≤–∞—А–Є–∞–љ—В –Т–Р–Ф, –Ї–∞–Ї —А–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–Љ –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ –Ј–љ–∞—З–µ–љ–Є–µ–Љ –°–Р–Ф (MMD). –Ф–∞–љ–љ–∞—П –Т–Р–Ф —А–∞—Б—Б—З–Є—В—Л–≤–∞–ї–∞—Б—М —З–µ—А–µ–Ј 2 –љ–µ–і. –Є —З–µ—А–µ–Ј 4 –љ–µ–і. –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –°—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П MMD —З–µ—А–µ–Ј 2 –љ–µ–і. —Б–Њ—Б—В–∞–≤–Є–ї–Є 50,0 [45,0; 58,0] –Љ–Љ —А—В. —Б—В. –Є —З–µ—А–µ–Ј 4 –љ–µ–і. вАФ 40,0 [38,0; 46,0] –Љ–Љ —А—В. —Б—В. (—А<0,001), —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г–ґ–µ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤–Њ–≥–Њ –Љ–µ—Б—П—Ж–∞ –ї–µ—З–µ–љ–Є—П.
–Я–ї–µ–є–Њ—В—А–Њ–њ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§
–Ф–∞–≤–ї–µ–љ–Є–µ –≤ –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є вАФ –≤–∞–ґ–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –њ–µ—А–µ–≥—А—Г–Ј–Ї–Є –Ї–∞–Ї –њ—А–∞–≤—Л—Е, —В–∞–Ї –Є –ї–µ–≤—Л—Е –Њ—В–і–µ–ї–Њ–≤ —Б–µ—А–і—Ж–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Њ—З–µ—В–∞–љ–Є–µ–Љ –Р–У –Є –•–Ю–С–Ы, –Ї–Њ—В–Њ—А—Л–є –Љ–Њ–ґ–µ—В –Љ–µ–љ—П—В—М—Б—П –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–∞–≤–Є–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –љ–∞–Љ–Є –Њ—Ж–µ–љ–µ–љ–∞ –і–Є–љ–∞–Љ–Є–Ї–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Н—В–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П. –Ш—Б—Е–Њ–і–љ–Њ —Г –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –љ–∞–Љ–Є –±–Њ–ї—М–љ—Л—Е —Б—А–µ–і–љ–µ–µ –і–∞–≤–ї–µ–љ–Є–µ –≤ –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ—А–µ–≤—Л—И–∞–ї–Њ –љ–Њ—А–Љ—Г –Є —Б–Њ—Б—В–∞–≤–ї—П–ї–Њ 19,5¬±3,6 –Љ–Љ —А—В. —Б—В. –І–µ—А–µ–Ј 6 –Љ–µ—Б. –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–∞–≤–ї–µ–љ–Є–µ –≤ –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–Є —Б–љ–Є–Ј–Є–ї–Њ—Б—М —Г 20 (67%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–Њ —Г—А–Њ–≤–љ—П 18,4¬±2,6 –Љ–Љ —А—В. —Б—В. (—А<0,001).
–Ф–Є—Б—Д—Г–љ–Ї—Ж–Є—П —Н–љ–і–Њ—В–µ–ї–Є—П вАФ –µ—Й–µ –Њ–і–Є–љ –≤–∞–ґ–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ, –Ј–∞–њ—Г—Б–Ї–∞—О—Й–Є–є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ї–Њ–љ—В–Є–љ—Г—Г–Љ–∞. –°–Є—Б—В–µ–Љ–љ–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –љ–∞–±–ї—О–і–∞–µ–Љ–Њ–µ –њ—А–Є –•–Ю–С–Ы, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ –і–µ—В–µ—А–Љ–Є–љ–∞–љ—В–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –ї–µ–≥–Њ—З–љ–Њ–є –Є —Б–Є—Б—В–µ–Љ–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П, —Е–Њ—В—П —В–Њ—З–љ—Л–µ –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —Н—В–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –і–Њ —Б–Є—Е –њ–Њ—А –љ–µ–Є–Ј–≤–µ—Б—В–љ—Л [18]. –Э–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, —З—В–Њ –Ј–љ–∞—З–Є–Љ–∞—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П —Н–љ–і–Њ—В–µ–ї–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б –•–Ю–С–Ы —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ–Њ–Љ—Г –њ—А–Њ—В–µ–Ї–∞–љ–Є—О –Ї–∞–Ї —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ, —В–∞–Ї –Є –ї–µ–≥–Њ—З–љ–Њ–≥–Њ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П —Б –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є –і–Є–ї–∞—В–∞—Ж–Є–µ–є –≤—Б–µ—Е –Ї–∞–Љ–µ—А —Б–µ—А–і—Ж–∞ –Є —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ–≥–Њ—З–љ–Њ–≥–Њ —Б–µ—А–і—Ж–∞ [12, 18]. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –њ–Њ–Є—Б–Ї –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Љ–Є–Љ–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Њ–Ї–∞–Ј—Л–≤–∞–ї–Є –±—Л –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є—П, —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ–Њ–є –Ј–∞–і–∞—З–µ–є.
–Т –љ–∞—И–Є—Е —А–∞–±–Њ—В–∞—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є –њ—А–Њ–±—Л —Б —Н–љ–і–Њ—В–µ–ї–Є–є-–Ј–∞–≤–Є—Б–Є–Љ–Њ–є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–µ–є –Є—Б—Е–Њ–і–љ–Њ –і–Є–ї–∞—В–∞—Ж–Є–Њ–љ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –њ–ї–µ—З–µ–≤–Њ–є –∞—А—В–µ—А–Є–Є –±—Л–ї–∞ —Б–љ–Є–ґ–µ–љ–∞ —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –Р–У –Є –•–Ю–С–Ы, –Њ–і–љ–∞–Ї–Њ –њ—А–Њ–Є–Ј–Њ—И–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —З–µ—А–µ–Ј 6 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ (—А–Є—Б. 3).

–У–Є–њ–Њ–Ї—Б–Є—П –њ—А–Є –•–Ю–С–Ы –Ј–∞–њ—Г—Б–Ї–∞–µ—В –∞–Ї—В–Є–≤–∞—Ж–Є—О –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —Б–≤–Њ–±–Њ–і–љ–Њ—А–∞–і–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Є –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј–≤–Є—В–Є—О –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞, —З—В–Њ –љ–∞—А—П–і—Г —Б –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є —Н–љ–і–Њ—В–µ–ї–Є—П —Б–ї—Г–ґ–Є—В —Б–≤—П–Ј—Г—О—Й–Є–Љ –Ј–≤–µ–љ–Њ–Љ –Љ–µ–ґ–і—Г –•–Ю–С–Ы –Є –Р–У. –Ш–љ—В–µ–љ—Б–Є—Д–Є–Ї–∞—Ж–Є—П –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤ (–Я–Ю–Ы) —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—О –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ. –Ю–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л–є —Б—В—А–µ—Б—Б —П–≤–ї—П–µ—В—Б—П –њ—Г—Б–Ї–Њ–≤—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –≤ –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є–Є –•–Ю–С–Ы, –њ—А–Є–≤–Њ–і—П –Ї–∞–Ї –Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Є –ї–µ–≥–Њ—З–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, —В–∞–Ї –Є –Ї —Б–Є—Б—В–µ–Љ–љ—Л–Љ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ. –Э–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –Ї–Њ–љ–µ—З–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –Я–Ю–Ы —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є–µ–є –∞—А—В–µ—А–Є–Њ–ї –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Њ–±—Й–µ–≥–Њ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, —З—В–Њ –≤–љ–Њ—Б–Є—В –≤–Ї–ї–∞–і –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Р–У —Г –±–Њ–ї—М–љ—Л—Е –•–Ю–С–Ы [12, 19, 20]. –Я–Ю–Ы —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ—Л—Е –Ј–≤–µ–љ—М–µ–≤, –Ј–∞–њ—Г—Б–Ї–∞—О—Й–Є—Е –Ї–∞—Б–Ї–∞–і –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –Ї–∞–Ї –њ—А–Є –•–Ю–С–Ы, —В–∞–Ї –Є –њ—А–Є –Р–У [20]. –Я–Њ –љ–∞—И–Є–Љ –і–∞–љ–љ—Л–Љ, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–У –Є –•–Ю–С–Ы —З–µ—А–µ–Ј 6 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Я–Ю–Ы.
–Я–µ—А–≤–Є—З–љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л –Я–Ю–Ы –Ј–∞–њ—Г—Б–Ї–∞—О—В —Б–Є—Б—В–µ–Љ–љ—Г—О –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Г—О —А–µ–∞–Ї—Ж–Є—О, –≤ —Е–Њ–і–µ –Ї–Њ—В–Њ—А–Њ–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Г—Б–Є–ї–µ–љ–Є–µ –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є –∞–і–≥–µ–Ј–Є–Є –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤ –Ї —Н–љ–і–Њ—В–µ–ї–Є—О, –љ–∞—А—Г—И–µ–љ–Є–µ —Н–љ–і–Њ—В–µ–ї–Є–є-–Ј–∞–≤–Є—Б–Є–Љ–Њ–є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–Є –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ (–њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞, –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞) –Є –≤—Б–µ—Е –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–Њ–≤ [20].
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –љ–∞–Љ–Є –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е –њ—А–Њ—В–µ–Ї–∞—О—В –Њ–і–љ–Є –Є —В–µ –ґ–µ —Б–≤–Њ–±–Њ–і–љ–Њ—А–∞–і–Є–Ї–∞–ї—М–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л —Б–Њ —Б–Љ–µ—Й–µ–љ–Є–µ–Љ –≤ —Б—В–Њ—А–Њ–љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Њ–Ї—Б–Є–і–∞–љ—В–Њ–≤. –≠—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л—Б–Ї–∞–Ј–∞—В—М –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, —З—В–Њ —Б —А–∞–љ–љ–Є—Е —Н—В–∞–њ–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є–Љ–µ–µ—В –Љ–µ—Б—В–Њ –µ–і–Є–љ—Л–є –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –≤ —А–∞–Ј–≤–Є—В–Є–Є –Р–У –Є –•–Ю–С–Ы. –Т–∞–ґ–µ–љ —Д–∞–Ї—В —В–Њ–≥–Њ, —З—В–Њ —З–µ—А–µ–Ј 6 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –њ–ї–µ–є–Њ—В—А–Њ–њ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞.
–Р–љ–∞–ї–Є–Ј –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–Є—Е —Б–Є—Б—В–µ–Љ–љ–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л–є —Б—В—А–µ—Б—Б –Є —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Г—О –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О, –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –•–Ю–С–Ы –љ–∞ –љ–∞—З–∞–ї—М–љ—Л–µ –Ј–≤–µ–љ—М—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ї–Њ–љ—В–Є–љ—Г—Г–Љ–∞ –Є –≥–Њ–≤–Њ—А–Є—В –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —А–∞–љ–љ–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Р–У –Є –•–Ю–С–Ы –Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Р–У –љ–∞ —Д–Њ–љ–µ –•–Ю–С–Ы. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ —Г —Г–Ї–∞–Ј–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–ї–Њ –µ–≥–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–µ —В–Њ–ї—М–Ї–Њ –љ–∞ —Г—А–Њ–≤–µ–љ—М –Р–Ф, –љ–Њ –Є –љ–∞ —В–µ—З–µ–љ–Є–µ –•–Ю–С–Ы.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є –±–Њ–ї—М–љ–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П вАФ —Н—В–Њ –±–Њ–ї—М–љ–Њ–є —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В—М—О, —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–µ –Љ–µ—Б—В–Њ –≤ –Ї–Њ—В–Њ—А–Њ–є –Ј–∞–љ–Є–Љ–∞–µ—В –Р–У. –Э–∞–ї–Є—З–Є–µ –Њ–±—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —Б –•–Ю–С–Ы, –∞ —В–∞–Ї–ґ–µ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –њ–µ—А–µ—Б–µ—З–µ–љ–Є—П –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –Р–У –Є –•–Ю–С–Ы –Ї–∞–Ї –Ї–Њ–Љ–Њ—А–±–Є–і–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є—В–Є—П –Р–У –њ—А–Є –•–Ю–С–Ы –Ј–∞—Б—В–∞–≤–ї—П—О—В, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Є—Б–Ї–∞—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–µ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞, –і–µ–є—Б—В–≤—Г—О—Й–Є–µ –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –Ј–≤–µ–љ—М—П –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞, –∞ —Б –і—А—Г–≥–Њ–є вАФ –Њ—Ж–µ–љ–Є–≤–∞—В—М –Є—Е –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –≤ –њ–ї–∞–љ–µ –њ–Њ–±–Њ—З–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –љ–∞ –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ—Г—О —Б–Є—Б—В–µ–Љ—Г. –С–µ—Б—Б–њ–Њ—А–љ—Л–Љ–Є –ї–Є–і–µ—А–∞–Љ–Є –≤ —Н—В–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є —П–≤–ї—П—О—В—Б—П –±–ї–Њ–Ї–∞—В–Њ—А—Л –†–Р–Р–°. –°–Њ–±—Б—В–≤–µ–љ–љ—Л–є –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї–∞ –і–Њ–Ї–∞–Ј–∞–ї —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–ї–µ–є–Њ—В—А–Њ–њ–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е –Р–У –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –•–Ю–С–Ы.












