В последнее время в лечении артериальной гипертонии (АГ) для эффективного контроля артериального давления (АД) все более широко используется комбинированная терапия. Как указано в российских и европейских рекомендациях по лечению АГ, комбинированная терапия должна быть назначена на старте лечения всем пациентам с высоким и очень высоким риском сердечно-сосудистых осложнений (ССО) [1–3]. Преимущества использования комбинированной терапии в первую очередь связаны с тем, что в большинстве случаев к развитию АГ приводит несколько патофизиологических факторов, а комбинированная терапия позволяет воздействовать на каждый из них. В метаанализе 42 исследований по лечению АГ было продемонстрировано, что сочетание антигипертензивных препаратов (АГП) 2 классов снижает АД примерно в 5 раз более эффективно, чем удвоение дозы стартового препарата [4].
При комбинированной терапии АГ предпочтительнее использование фиксированных комбинаций. Первые фиксированные комбинации АГП появились еще в начале 1960-х гг. Они были представлены следующими составами: резерпин + гидралазин + гидрохлортиазид; a-метилдопа + гидрохлортиазид; гидрохлортиазид + калийсберегающий диуретик. В 1970–1980-е гг. в терапии АГ ведущее место заняли комбинации с использованием диуретика, как правило, в высокой дозе, с β-адреноблокаторами или препаратами центрального действия. С появлением новых классов препаратов частота использования комбинированной терапии несколько уменьшилась. В середине 1980-х гг. доминировала тактика дифференцированного выбора препаратов и применения их в режиме монотерапии. Комбинированная терапия рекомендовалась лишь на поздних этапах лечения. При лечении АГ с использованием монотерапии в максимальных дозах зачастую сталкивались с активацией контррегуляторных или компенсаторных механизмов. Так, применение высоких доз диуретиков приводило к активации симпато-адреналовой и ренин-ангиотензиновой систем.
Использование фиксированных комбинаций рекомендовано у пациентов с высоким и очень высоким риском ССО, т. е. с наличием у них поражений органов-мишеней, метаболического синдрома (МС), сахарного диабета (СД), ассоциированных клинических состояний, 3 и более дополнительных факторов риска [1–3]. К преимуществам фиксированных комбинаций относятся простота использования и процесса титрования дозы, что повышает приверженность пациентов лечению; потенцирование антигипертензивного эффекта препаратов, входящих в комбинацию; уменьшение частоты побочных эффектов за счет умеренных доз препаратов и их взаимной нейтрализации; фармакоэкономическая составляющая, заключающаяся в уменьшении стоимости лечения. Выделяют рациональные и нерациональные комбинации АГП. Рациональными считаются те, в которых препарат одной группы, усиливая антигипертензивный эффект, не увеличивает, а, возможно, даже уменьшает побочное действие препарата другой группы.
К рациональным комбинациям относят в том числе и комбинацию блокаторов рецепторов ангиотензина (АТ) II (БРА) с диуретиками [1]. Этой комбинации может быть отдано предпочтение у пациентов с АГ в сочетании с хронической сердечной недостаточностью, диабетической и недиабетической нефропатией, микроальбуминурией, гипертрофией левого желудочка, СД, МС.Также применение БРА с диуретиком показано пожилым пациентам с АГ, пациентам с изолированной систолической АГ и кашлем при приеме ингибиторов ангиотензин-превращающего фермента (иАПФ) [1].
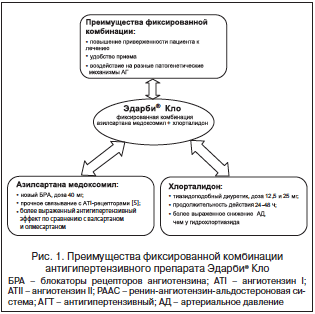
В настоящее время в России зарегистрирована новая фиксированная комбинация АГП БРА и диуретика – Эдарби® Кло (компания «Такеда»), в состав которой входят азилсартана медоксомил (40 мг) и хлорталидон (12,5 или 25 мг) (рис. 1).
Входящий в состав этого препарата азилсартана медоксомил (Эдарби®, компания «Такеда») – восьмой БРА, появившийся на фармацевтическом мировом рынке. В 2011 г. Эдарби® был одобрен FDA для лечения АГ у взрослых, а в начале 2012 г. препарат появился на фармацевтическом рынке Европы. В России Эдарби® одобрен Министерством здравоохранения РФ в феврале 2014 г. Рекомендованная начальная доза препарата составляет 40 мг/сут, максимальная доза – 80 мг/сут. Азилсартана медоксомил – это пролекарство с активным метаболитом. После приема внутрь посредством эфирного гидролиза в желудочно-кишечном тракте (ЖКТ) и печени азилсартана медоксомил превращается в активную форму – азилсартан, высокоселективный антагонист рецепторов ангиотензина.
Биодоступность препарата составляет 60%, он достигает максимальной концентрации в крови за 1,5–3 ч. 55% препарата выводится из организма через ЖКТ, 42% – почками. Важно, что фармакокинетика азилсартана не зависит от приема пищи. Азилсартана медоксомил обладает высокой липофильностью. Основным ферментом, обеспечивающим его метаболизм, служит изофермент CYP2C9.
Азилсартана медоксомил структурно подобен кандесартану, за исключением наличия в его молекуле оксадиазольного кольца вместо тетразольного кольца. Именно с его структурной особенностью связаны отличия в фармакокинетике по сравнению с другими БРА, которые выражаются в более прочном связывании с АТ1-рецепторами и в более медленной диссоциации этой связи [5]. Известно, что при применении БРА уровень АТ II может компенсаторно увеличиваться, в связи с чем происходит конкуренция с БРА за места связывания с АТ1-рецепторами. Структурные и фармакологические особенности азилсартана медоксомила не позволяют избытку АТ II вытеснять его из связи с АТ1-рецепторами. В экспериментальных исследованиях было установлено, что потенциал ингибирования специфического соединения AТ II с АТ1-рецепторами человека при концентрации IC50 (концентрация, которая ингибирует соединение 50% радиоактивно меченного 125I(Sar1-IIe8) АТ II с мембраной клеток, содержащих АТ1-рецепторы человека) у азилсартана наивысший и составляет 2,6 нМ, что приблизительно в 2 раза выше, чем у олмесартана (6,7 нМ) и телмисартана (5,1 нМ), а также в 5–20 раз выше, чем у ирбесартана (15,8 нМ) и валсартана (44,9 нМ). С другой стороны, медленная диссоциация азилсартана медоксомила из связи с рецепторами способствует его накоплению и повторному связыванию с АТ1-рецепторами. Также данные экспериментальных исследований демонстрируют присутствие у азилсартана медоксомила (как у кандесартана и олмесартана) свойств обратного агониста АТ1-рецепторов, что определяет его органопротективные эффекты [5]. Азилсартана медоксомил обеспечивает необратимую блокаду АТ1-рецепторов и полный антагонизм эндогенного АТ II даже через 24 ч после приема. Фармакологические особенности азилсартана медоксомила объясняют его более выраженный по силе и продолжительности антигипертензивный эффект по сравнению с эффектом других БРА [6].
Вторым препаратом, входящим в состав Эдарби® Кло, является диуретик хлорталидон. В отличие от азилсартана хлорталидон используется для лечения АГ еще с 1960-х гг. , но в России его применение ограничено. Хлорталидон – тиазидоподобный диуретик I поколения, механизм его действия заключается в подавлении активной реабсорбции ионов натрия, главным образом в периферических почечных канальцах (кортикальный сегмент петли Генле), увеличении выведения ионов натрия, ионов хлора и воды. Выведение ионов калия и ионов магния через почки увеличивается, в то время как выведение ионов кальция – уменьшается. В отличие от других тиазидоподобных диуретиков хлорталидон характеризуется более длительным периодом полувыведения, который составляет около 40 ч, с чем связана большая продолжительность его действия – 24–48 ч. Эффективность и безопасность хлорталидона в качестве антигипертензивной терапии были продемонстрированы в таких классических исследованиях, как MRFIT, SHEP и ALLHAT [7–9]. Во всех исследованиях было выявлено снижение риска ССО у пациентов с АГ при терапии хлорталидоном, он не уступал более новым АГП по влиянию на частоту развития первичной конечной точки. По результатам метаанализа было показано, что антигипертензивный эффект хлорталидона примерно в 1,5–2 раза превышает эффект соответствующих дозировок гидрохлоротиазида [10].
К настоящему моменту опубликован ряд исследований, изучавших безопасность и эффективность использования комбинированной терапии азилсартана медоксомила с хлорталидоном. В двойном слепом рандомизированном исследовании осуществлялся подбор дозировок препарата продолжительностью 8 нед. среди 1714 больных АГ 2-й степени. Средний возраст включенных в исследование больных составил 57 лет, мужчин было 47%. После «отмывочного» периода в 7–14 дней и пилотного периода с плацебо в течение 14 дней пациенты были рандомизированы на 11 групп: хлорталидона 12,5 и 25 мг, азилсартана медоксомила 20, 40 и 80 мг в различных комбинациях. Первичной конечной точкой было изменение систолического артериального давления (САД) через 22–24 ч по данным суточного мониторирования АД (СМАД) через 8 нед. по сравнению с исходным уровнем. В результате было продемонстрировано, что комбинация азилсартана медоксомила и хлорталидона в каждой из 6 дозировок более выраженно снизила САД по данным СМАД через 8 нед. в сравнении с плацебо, чем монотерапия любым из компонентов (p<0,001). Целевое АД (САД < 140 и ДАД < 90 мм рт. ст.) через 8 нед. терапии было достигнуто у достоверно большей доли пациентов. Также было показано, что антигипертензивная эффективность не различалась у лиц разного пола, возраста, с различным индексом массы тела, наличием или отсутствием СД, в зависимости от почечной функции [12].
Также были выполнены исследования сравнительной эффективности фиксированной комбинации азилсартана медоксомила с хлорталидоном с другими фиксированными комбинациями. В одной из таких работ проводилось сравнение азилсартана медоксомила + хлорталидон с олмесартаном + гидрохлортиазид у больных АГ (САД 135–160 мм рт. ст. на стабильных дозах 2–3 АГП) и хронической болезнью почек (ХБП) III стадии. За 2 дня до рандомизации антигипертензивную терапию отменяли, и далее пациенты были разделены на группу азилсартана медоксомила + хлорталидон 20/12,5 мг (n=77) и олмесартана + гидрохлортиазид 20/12,5 мг (n=76). При необходимости допускалось назначение дополнительных АГП. Исходные характеристики пациентов не различались в 2 группах. К 52-й нед. лечения было продемонстрировано снижение САД и ДАД, которое было сходным в обеих группах. Однако в группе олмесартана + гидрохлортиазид большее число больных получало максимальную дозу препаратов (48,7%) по сравнению с группой азилсартана медоксомила + хлорталидон (29,9%), и большее число пациентов принимали дополнительные АГП (26,3 и 16,9% соответственно) [13]. В другом рандомизированном исследовании, в которое был включен 1071 больной с систолической АГ (средний возраст пациентов составил 57 лет, 59% из них были мужчины), после «отмывочного» периода 7–14 дней, периода плацебо в течение 7 дней пациентов рандомизировали на 3 группы: азилсартана медоксомил + хлорталидон 20/12,5 мг, азилсартана медоксомил + хлорталидон 40/12,5 мг, олмесартан + гидрохлортиазид 20/12,5 мг. Через 4 нед. дозу исследуемых сартанов удваивали, еще через 4 нед. – удваивали дозу диуретиков. В обеих группах азилсартана медоксомила + хлорталидон снижение клинического САД и среднесуточного САД на 12-й нед. было статистически достоверно более выражено (p<0,05) в группах азилсартана медоксомила + хлорталидон, чем в группе олмесартана + гидрохлортиазид. В финале исследования процент достижения целевого АД менее 140/90 мм рт. ст. (81,4; 83,9 и 74,6%) или менее 130/80 мм рт. ст. (56,1; 60,6 и 41,0%) был достоверно больше в обеих группах азилсартана медоксомила + хлорталидон по сравнению с группой олмесартана + гидрохлортиазид [14].
При сравнении азилсартана медоксомила + хлорталидон с монотерапией хлорталидоном также было продемонстрировано преимущество данной фиксированной комбинации. В рандомизированном двойном слепом многоцентровом 6-недельном исследовании сравнивали эффективность комбинации азилсартана медоксомила в 2 разных дозах (40 или 80 мг) с 25 мг хлорталидона с эффективностью монотерапии хлорталидоном в дозе 25 мг. В исследование включали больных АГ 2–3-й степени. В результате было продемонстрировано, что на фоне комбинированной терапии отмечалось достоверно большее (р<0,001) снижение среднесуточного САД (азилсaртана медоксомил + хлорталидон 40/25 мг – -31,72 мм рт. ст. и азилсартана медоксомил + хлорталидон 80/25 мг – –31,3 мм рт. ст.), чем при монотерапии хлорталидоном (–15,85 мм рт. ст.). Сходные результаты были получены и в отношении среднесуточного ДАД, среднедневного и средненочного САД [15]. Схожее исследование было выполнено для сравнения эффективности комбинации азилсартана медоксомил + хлорталидон c эффективностью монотерапии азилсартана медоксомилом. В это исследование также включали больных АГ 2–3-й степени. Все пациенты получали монотерапию азилсартаном медоксомилом в дозе 40 мг в течение 4 нед. Через 4 нед. менее чем у 10% пациентов САД достигло уровня менее 140 мм рт. ст., таких пациентов исключили из исследования, остальные были рандомизированы на 3 группы: азилсартана медоксомил + хлорталидон 40/12,5; 40/25; монотерапия азилсартана медоксомилом 40 мг. Продолжительность данной двойной слепой фазы составила 8 нед. Через 8 нед. целевое САД и ДАД было отмечено у 35,3 и 60,2% больных в группе монотерапии, у 67,2 и 81% пациентов, принимавших азилсартана медоксомил + хлорталидон 40/12,5 мг, и у 77,8 и 85,9% больных, принимавших азилсартана медоксомил + хлорталидон 40/25 мг (р≤0,001) [16].
В другой работе проводилось сравнение 2 комбинаций азилсартана медоксомила с хлорталидоном и гидрохлортиазидом. В данном рандомизированном двойном слепом исследовании участвовали 609 пациентов с систолической АГ, получавшие азилсартана медоксомил 40 мг в течение 2 нед. Затем пациенты были рандомизированы на группы с приемом азилсартана медоксомил + хлорталидон или азилсартана медоксомил + гидрохлортиазид. Оба диуретика вначале назначали в дозе 12,5 мг. Если на 6-й нед. целевое АД не было достигнуто, дозу диуретиков увеличивали до 25 мг. В результате на 6-й нед. в группе азилсартана медоксомила + хлорталидон было отмечено достоверно большее снижение клинического САД (-35,1 мм рт. ст.), чем в группе азилсартана медоксомила + гидрохлортиазид (-29,5 мм рт. ст.). В конце 10-й нед. различие по клиническому АД продолжало оставаться больше в пользу группы азилсартана медоксомила + хлорталидон (разница средних значений АД: -5,0/-2,7 мм рт. ст.); р<0,001. Сходные результаты были получены и по результатам СМАД. Так, разница значений по среднесуточному САД составила 5,8 мм рт. ст. (95% доверительный интервал -8,4 – -3,2; р<0,001) в пользу комбинации азилсартана медоксомил + хлорталидон. Частота побочных эффектов не различалась между группами, также в одинаковом проценте случаев в обеих группах отмечено повышение уровня сывороточного креатинина – выше верхней границы нормы. На основании полученных данных авторы сделали вывод о том, что комбинация азилсартана медоксомила с хлорталидоном имеет большую антигипертензивную эффективность при сходной безопасности, чем комбинация с гидрохлортиазидом [17].
Таким образом, новая фиксированная комбинация азилсартана медоксомила и хлорталидона – Эдарби® Кло продемонстрировала выраженный антигипертензивный эффект и удовлетворительный контроль АД, а также удобство для применения в повседневной клинической практике.
Проблема контроля АД у пациентов с АГ по-прежнему остается актуальной, поэтому новые фиксированные комбинации АГП продолжают представлять большой интерес для врачей [18].












