–Р–Ї—В–Њ–≤–µ–≥–Є–љ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –і–ї—П —И–Є—А–Њ–Ї–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤ —Б–∞–Љ—Л—Е —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ–±–ї–∞—Б—В—П—Е –Љ–µ–і–Є—Ж–Є–љ—Л. –Т –Њ—В–і–µ–ї–µ–љ–Є—П—Е –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ –≤ –і–Њ–Ј–µ 800–1200 –Љ–≥ –і–Њ 2,0–4,0 –≥/—Б—Г—В. –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–Є–љ–і—А–Њ–Љ–∞ —А–µ–њ–µ—А—Д—Г–Ј–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ—Б—В—А—Л–Љ–Є –Є–љ—Д–∞—А–Ї—В–∞–Љ–Є –Љ–Є–Њ–Ї–∞—А–і–∞, –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В—А–Њ–Љ–±–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Є –±–∞–ї–ї–Њ–љ–љ–Њ–є –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї–Є, –њ—А–Є –ї–µ—З–µ–љ–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Є–і–Њ–≤ —И–Њ–Ї–Њ–≤, –њ–Њ—Б–ї–µ –Њ—Б—В–∞–љ–Њ–≤–Ї–Є –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є –∞—Б—Д–Є–Ї—Б–Є–Є, –њ—А–Є —В—П–ґ–µ–ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є [3]. –†–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –њ–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–Є—Е –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е –Љ–Њ–Ј–≥–Њ–≤–Њ–є –≥–Є–њ–Њ–Ї—Б–Є–µ–є [22]. –Ш—Б—Е–Њ–і—П—В –њ—А–Є —Н—В–Њ–Љ –Є–Ј –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –Њ —В–Њ–Љ, —З—В–Њ –≤–µ–і—Г—Й–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —Б–Њ—Е—А–∞–љ–µ–љ–Є—П –љ–µ–є—А–Њ–≥–ї–Є–∞–ї—М–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А –≤ —Г—Б–ї–Њ–≤–Є—П—Е –≥–Є–њ–Њ–Ї—Б–Є–Є –Є –Є—И–µ–Љ–Є–Є —П–≤–ї—П–µ—В—Б—П –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ —Б—В–∞–±–Є–ї—М–љ–Њ–≥–Њ —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –Њ–Ї—Б–Є–≥–µ–љ–∞—Ж–Є–Є –Є —Б–Њ–Ј–і–∞–љ–Є–µ —Г—Б–ї–Њ–≤–Є–є –∞–Ї—В–Є–≤–∞—Ж–Є–Є —Г—В–Є–ї–Є–Ј–∞—Ж–Є–Є –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –Є –≥–ї—О–Ї–Њ–Ј—Л —Б —Ж–µ–ї—М—О –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П —Ж–Є–Ї–ї–∞ –Ъ—А–µ–±—Б–∞, —З—В–Њ –≤ –њ–Њ–ї–љ–Њ–є –Љ–µ—А–µ –Љ–Њ–ґ–µ—В –Њ–±–µ—Б–њ–µ—З–Є—В—М –Р–Ї—В–Њ–≤–µ–≥–Є–љ.
–Р–Ї—В–Њ–≤–µ–≥–Є–љ —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –і–ї—П –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —А–∞–Ј–ї–Є—З–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є [10]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤–ї–Є—П–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –љ–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є —Г –ї–Є—Ж –њ–Њ–ґ–Є–ї–Њ–≥–Њ –Є —Б—В–∞—А—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ —Г–ґ–µ —З–µ—А–µ–Ј 2 –љ–µ–і–µ–ї–Є –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е —Д—Г–љ–Ї—Ж–Є–є, –≤–љ–Є–Љ–∞–љ–Є—П –Є –Љ—Л—И–ї–µ–љ–Є—П. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є, –њ–Њ –і–∞–љ–љ—Л–Љ –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є—П, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–µ–є —Н–ї–µ–Ї—В—А–Њ—Н–љ—Ж–µ—Д–∞–ї–Њ–≥—А–∞–Љ–Љ—Л –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –∞–Љ–њ–ї–Є—В—Г–і—Л –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ –†300, –њ—А–Є—З–µ–Љ –і–∞–ґ–µ —А–∞–Ј–Њ–≤–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Г–ї—Г—З—И–µ–љ–Є—О —Н–ї–µ–Ї—В—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–є —Д—Г–љ–Ї—Ж–Є–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [4,5]. –Т –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е (–і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е) –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–Њ–≤–µ—А—П–ї–Њ—Б—М –і–µ–є—Б—В–≤–Є–µ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –≤ –≤–Є–і–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –Є–ї–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–Є –ї–µ–≥–Ї–Њ–є –Є–ї–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ—Б–ї–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –≤ –і–Њ–Ј–µ 2 —В–∞–±–ї–µ—В–Ї–Є 3 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 8 –љ–µ–і–µ–ї—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤–Њ–Ј—А–∞—Б—В–∞–ї–∞ —Б–Ї–Њ—А–Њ—Б—В—М –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ [6]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–∞ 120 –њ–∞—Ж–Є–µ–љ—В–∞—Е —Б —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ –і–µ—Д–Є—Ж–Є—В–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ —Б–ї–µ–і—Г–µ—В –Њ—В–і–∞—В—М –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ—Г –њ—А–Є–µ–Љ—Г –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ [7]. –Я—А–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ —Г —Н—В–Њ–є –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ–∞–Љ—П—В–Є –Є –≤–љ–Є–Љ–∞–љ–Є—П, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Є —Г–ї—Г—З—И–µ–љ–Є–µ —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –∞–і–∞–њ—В–∞—Ж–Є–Є. –Ю—Б–Њ–±–Њ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –≤–Њ–Ј—А–∞—Б—В–∞–ї–∞ –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –≤—А–µ–Љ–µ–љ–Є –Ї—Г—А—Б–∞ –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –њ—А–Є—З–µ–Љ –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є, –љ–Њ –Є –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ [8,9]. –Ъ—Г—А—Б –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –њ—А–Є–≤–Њ–і–Є—В –Ї –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г –Є –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ –љ–∞—Б—В—Г–њ–∞—О—Й–µ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О —Б–Њ—Б—В–Њ—П–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –њ–Њ—Н—В–Њ–Љ—Г —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞—З–Є–љ–∞—В—М –ї–µ—З–µ–љ–Є–µ —Б –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л –њ—А–µ–њ–∞—А–∞—В–∞, –∞ –Ј–∞—В–µ–Љ –њ–µ—А–µ—Е–Њ–і–Є—В—М –љ–∞ –њ—А–Є–µ–Љ —В–∞–±–ї–µ—В–Њ–Ї [11]. –Я—А–µ–і—Б—В–∞–≤–ї—П–µ—В –±–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞, —Г—З–Є—В—Л–≤–∞—П –µ–≥–Њ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Г—В–Є–ї–Є–Ј–∞—Ж–Є—О –≥–ї—О–Ї–Њ–Ј—Л, —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є –і–ї—П –ї–µ—З–µ–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 60 –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ (–°–Ф) 2 —В–Є–њ–∞, –Є–Љ–µ—О—Й–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —А–∞–Ј–ї–Є—З–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є, –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –≤ –і–Њ–Ј–µ 400 –Љ–≥ –≤ —В–µ—З–µ–љ–Є–µ 3 –љ–µ–і–µ–ї—М –њ—А–Є–≤–µ–ї–Њ –Ї —Г–ї—Г—З—И–µ–љ–Є—О —Б—Г–Љ–Љ—Л –±–∞–ї–ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ MMSE (25,50±2,52 –±–∞–ї–ї–∞ –і–Њ –ї–µ—З–µ–љ–Є—П –Є 26,47±2,50 –±–∞–ї–ї–Њ–≤ –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П, p<0,05), –њ—А–Є—З–µ–Љ –≤ –љ–∞–Є–±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Г–ї—Г—З—И–∞–ї–∞—Б—М –њ–∞–Љ—П—В—М [13]. –£–ї—Г—З—И–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –і–µ–њ—А–µ—Б—Б–Є–Є –Є —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В–Є, –∞ —В–∞–Ї–ґ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –њ–Њ –і–∞–љ–љ—Л–Љ –і—Г–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—В—М, —З—В–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ —Б –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞.
–Т –њ–Є–ї–Њ—В–љ–Њ–є —А–∞–±–Њ—В–µ, –≤—Л–њ–Њ–ї–љ–µ–љ–љ–Њ–є –љ–∞ 10 –±–Њ–ї—М–љ—Л—Е —Б —В—П–ґ–µ–ї–Њ–є —З–µ—А–µ–њ–љ–Њ––Љ–Њ–Ј–≥–Њ–≤–Њ–є —В—А–∞–≤–Љ–Њ–є, –њ–Њ–ї—Г—З–µ–љ—Л –і–∞–љ–љ—Л–µ –Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–µ –Њ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ —Г –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е, –Њ–і–љ–∞–Ї–Њ —Б —Г—З–µ—В–Њ–Љ –Љ–∞–ї–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –µ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –≤ —А–∞–Љ–Ї–∞—Е –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [12].
–У–Њ—А–∞–Ј–і–Њ –Љ–µ–љ—М—И–µ –і–∞–љ–љ—Л—Е –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, —Б–Њ—Б—Г–і–Є—Б—В—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –њ—А–Є –Љ–љ–Њ–≥–Є—Е –Љ–Њ–љ–Њ–љ–µ–≤—А–Њ–њ–∞—В–Є—П—Е, –≤–Ї–ї—О—З–∞—П —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є, –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л—Е –Љ–Њ–љ–Њ–љ–µ–≤—А–Њ–њ–∞—В–Є—П—Е –Є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є—П—Е. –Я—А–µ–і–њ—А–Є–љ–Є–Љ–∞–ї–∞—Б—М –њ–Њ–њ—Л—В–Ї–∞ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –ї–Њ—А–љ–Њ–Ї—Б–Є–Ї–∞–Љ–Њ–Љ –Є –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ–Њ–Љ –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –і–Є—Б–Ї–Њ–≥–µ–љ–љ—Л–Љ–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П–Љ–Є, –Є–Љ–µ—О—Й–Є—Е –Є–љ—В–µ–љ—Б–Є–≤–љ—Л–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ. –Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞—Б—В—Г–њ–∞–ї –±–Њ–ї–µ–µ –±—Л—Б—В—А—Л–є —А–µ–≥—А–µ—Б—Б –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –≥—А—Г–њ–њ–∞–Љ–Є –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В–Њ–ї—М–Ї–Њ –ї–Њ—А–љ–Њ–Ї—Б–Є–Ї–∞–Љ –Є–ї–Є –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ [14]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ї–∞–Ї –њ–Њ–Ї–∞–Ј–∞–ї–Њ –Ї–∞—В–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Г—О —В–µ—А–∞–њ–Є—О —Б –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ, –љ–∞ 43% —А–µ–ґ–µ –≤–Њ–Ј–љ–Є–Ї–∞–ї–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –њ–Њ–≤—В–Њ—А–љ–Њ–є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –≤ —Б–≤—П–Ј–Є —Б —А–µ—Ж–Є–і–Є–≤–Њ–Љ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Т—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ –±—Л–ї–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–Є–ґ–µ –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Р–Ї—В–Њ–≤–µ–≥–Є–љ, —З–µ–Љ –≤ –і—А—Г–≥–Є—Е –≥—А—Г–њ–њ–∞—Е. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –ї–µ—З–Є–≤—И–Є—Е—Б—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ, –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П, –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є —Б–љ–∞. –°–і–µ–ї–∞–љ –≤—Л–≤–Њ–і –Њ —В–Њ–Љ, —З—В–Њ –≤–Ї–ї—О—З–µ–љ–Є–µ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б —В–µ—А–∞–њ–Є–Є –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є—Б–Ї–Њ–≥–µ–љ–љ–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–µ–є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –±—Л—Б—В—А–µ–µ –Ї—Г–њ–Є—А–Њ–≤–∞—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ, —Г—Б–Ї–Њ—А–Є—В—М —А–µ–≥—А–µ—Б—Б –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –Є —Г–ї—Г—З—И–Є—В—М —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є–µ –±–Њ–ї—М–љ—Л—Е.
–°—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –±–Њ–ї—М—И–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ—А–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ – –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—В–∞–ї—М–љ–Њ–є —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ–є —Б–µ–љ—Б–Њ—А–љ–Њ––Љ–Њ—В–Њ—А–љ–Њ–є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є (–Ф–Я–Э) [15,16,17], —З—В–Њ –њ—А–µ–і–Њ–њ—А–µ–і–µ–ї–µ–љ–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞. –°–љ–Є–ґ–µ–љ–Є–µ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–∞—Е, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–µ –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–µ–є, –ї–µ–ґ–Є—В –≤ –Њ—Б–љ–Њ–≤–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Ф–Я–Э. –Ь–Њ–ґ–љ–Њ —Б–Њ–≥–ї–∞—Б–Є—В—М—Б—П —Б —В–Њ—З–Ї–Њ–є –Ј—А–µ–љ–Є—П –Њ —В–Њ–Љ, —З—В–Њ «–љ–∞—З–Є–љ–∞–µ—В—Б—П –і–Є–∞–±–µ—В –Ї–∞–Ї –±–Њ–ї–µ–Ј–љ—М –Њ–±–Љ–µ–љ–∞, –∞ –Ј–∞–Ї–∞–љ—З–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї —Б–Њ—Б—Г–і–Є—Б—В–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П» [20]. –Я–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є —В–Њ—З–Ї–µ –Ј—А–µ–љ–Є—П, —А–∞–Ј–≤–Є—В–Є–µ –Ф–Я–Э —Б–≤—П–Ј–∞–љ–Њ —Б –Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ —Б—В—А–µ—Б—Б–Њ–Љ, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–Љ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –љ–∞—А—Г—И–µ–љ–Є–є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –≥–ї—О–Ї–Њ–Ј—Л, –∞ —В–∞–Ї–ґ–µ —Б–ї–∞–±–Њ—Б—В—М—О —Б–Њ–±—Б—В–≤–µ–љ–љ—Л—Е –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л—Е —Б–Є—Б—В–µ–Љ [21]. –Ь–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П, –≤—Л–Ј—Л–≤–∞—П –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –≤ —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–µ –Ї–ї–µ—В–Њ–Ї —Д–Њ—Б—Д–∞—В–љ—Л—Е —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є—Е —Б—Г–±—Б—В—А–∞—В–Њ–≤, –њ—А–Є–≤–Њ–і—П—В –Ї —А–∞–Ј–≤–Є—В–Є—О —Д–µ–љ–Њ–Љ–µ–љ–∞ «–њ—Б–µ–≤–і–Њ–≥–Є–њ–Њ–Ї—Б–Є–Є». –£—В–Њ–ї—Й–µ–љ–Є–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –Є –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Ї—А–Њ–≤–Є –њ—А–Є –°–Ф –њ—А–Є–≤–Њ–і—П—В –Ї —А–∞–Ј–≤–Є—В–Є—О –Є—Б—В–Є–љ–љ–Њ–є –≥–Є–њ–Њ–Ї—Б–Є–Є. –Ґ–∞–Ї–Њ–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–µ –Њ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е, –ї–µ–ґ–∞—Й–Є—Е –≤ –Њ—Б–љ–Њ–≤–µ —А–∞–Ј–≤–Є—В–Є—П –Ф–Я–Э, –і–µ–ї–∞–µ—В —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞, –Њ–±–ї–∞–і–∞—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ –њ—А–Њ—Ж–µ—Б—Б—Л –≥–Є–њ–Њ–Ї—Б–Є–Є –Є –Њ–±–Љ–µ–љ –≥–ї—О–Ї–Њ–Ј—Л, –і–ї—П –ї–µ—З–µ–љ–Є—П –Ф–Я–Э.
W. Jansen –Є E. Beck –Є–Ј—Г—З–Є–ї–Є –і–µ–є—Б—В–≤–Є–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –љ–∞ –±–Њ–ї—М–љ—Л—Е —Б –Ф–Я–Э –≤ —А–∞–Љ–Ї–∞—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ–і–љ–∞ –≥—А—Г–њ–њ–∞ –Є–Ј 35 –±–Њ–ї—М–љ—Л—Е –њ–Њ–ї—Г—З–∞–ї–∞ –њ–ї–∞—Ж–µ–±–Њ, –і—А—Г–≥–∞—П –≥—А—Г–њ–њ–∞ –Є–Ј 35 –±–Њ–ї—М–љ—Л—Е – —В–∞–±–ї–µ—В–Ї–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ (–њ–Њ 600 –Љ–≥ 3 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є) –≤ —В–µ—З–µ–љ–Є–µ 24 –љ–µ–і–µ–ї—М [16]. –Ъ—А–Є—В–µ—А–Є—П–Љ–Є –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ —Б–ї—Г–ґ–Є–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є (—Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л–µ —А–µ—Д–ї–µ–Ї—Б—Л, –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–∞—П –Є –≥–ї—Г–±–Њ–Ї–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М, –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞) –Є –≠–Ь–У––њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ (—Б–Ї–Њ—А–Њ—Б—В—М —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –≤–Њ–Ј–±—Г–ґ–і–µ–љ–Є—П (–°–†–Т), –∞ —В–∞–Ї–ґ–µ —А–∞—Б—Б—В–Њ—П–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ –±–Њ–ї—М–љ—Л–µ –Љ–Њ–≥–ї–Є –њ—А–Њ–є—В–Є –±–µ–Ј –±–Њ–ї–Є. –£–ї—Г—З—И–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –Њ—В–Љ–µ—З–µ–љ–Њ —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —З–µ—А–µ–Ј 8 –љ–µ–і–µ–ї—М –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П, –∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –і–Њ—Б—В–Є–≥–∞–ї—Б—П —З–µ—А–µ–Ј 16 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П. –Я–Њ–Ї–∞–Ј–∞–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –њ–ї–∞—Ж–µ–±–Њ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є: —А–∞—Б—Б—В–Њ—П–љ–Є—П —Е–Њ–і—М–±—Л –±–µ–Ј –±–Њ–ї–Є, —Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤, –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–є –Є –≥–ї—Г–±–Њ–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є (—А<0,01). –°–†–Т –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ (p<0,001) —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞—Б—М –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –њ–ї–∞—Ж–µ–±–Њ. –Я–∞—Ж–Є–µ–љ—В—Л –≥—А—Г–њ–њ—Л –ї–µ—З–µ–љ–Є—П —З—Г–≤—Б—В–≤–Њ–≤–∞–ї–Є —Б–µ–±—П –ї—Г—З—И–µ –Є –њ—А–µ–і—К—П–≤–ї—П–ї–Є –Љ–µ–љ—М—И–µ –ґ–∞–ї–Њ–± –љ–∞ –љ–∞—А—Г—И–µ–љ–Є–µ –њ—Б–Є—Е–Њ—Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П, —З—В–Њ –Ї–Њ—А—А–µ–ї–Є—А–Њ–≤–∞–ї–Њ —Б —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Є—Е —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П.
–Т —А–∞–±–Њ—В–µ –ѓ–≤–Њ—А—Б–Ї–Њ–є –Т.–Р. —Б —Б–Њ–∞–≤—В. [17] –≤ —А–∞–Љ–Ї–∞—Е –Њ—В–Ї—А—Л—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ –њ—А–Є–Љ–µ–љ—П–ї–Є –і–ї—П –ї–µ—З–µ–љ–Є—П –Ф–Я–Э —Г 24 –±–Њ–ї—М–љ—Л—Е —Б –°–Ф 1 –Є 2 —В–Є–њ–Њ–≤ –≤ –≤–Є–і–µ –µ–ґ–µ–і–љ–µ–≤–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –≤ —В–µ—З–µ–љ–Є–µ 20 –і–љ–µ–є. –Ъ—А–Є—В–µ—А–Є—П–Љ–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–ї—Г–ґ–Є–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є, –і–∞–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –≠–Ь–У––Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Ю—В–Љ–µ—З–µ–љ–Њ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –±–Њ–ї—М–љ—Л—Е –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, —Г–ї—Г—З—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤, —Г–≤–µ–ї–Є—З–µ–љ–Є—П —Б–Є–ї—Л –Љ—Л—И—Ж. –†–µ–Њ–≤–∞–Ј–Њ–≥—А–∞—Д–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–∞ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ –љ–Њ–≥–∞—Е, –∞ –≠–Ь–У––Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ – —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –Ь––Њ—В–≤–µ—В–∞ –Є –°–†–Т –њ—А–Є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –љ–µ—А–≤–Њ–≤ –љ–Њ–≥.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є 33 –±–Њ–ї—М–љ—Л—Е —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л —А–∞–Ј–ї–Є—З–љ–Њ–є —В—П–ґ–µ—Б—В–Є –њ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –Т–∞–≥–љ–µ—А–∞ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –њ–Њ–і–Ї–ї—О—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –Ї —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ –±—Л—Б—В—А–Њ–Љ—Г –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—О –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є —Г—Б–Ї–Њ—А–µ–љ–Є—О –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≥—А–∞–љ—Г–ї—П—Ж–Є–Є –Є —Н–њ–Є—В–µ–ї–Є–Ј–∞—Ж–Є–Є —П–Ј–≤–µ–љ–љ—Л—Е –і–µ—Д–µ–Ї—В–Њ–≤ —Б –Є—Е –Ј–∞–ґ–Є–≤–ї–µ–љ–Є–µ–Љ [19].
–Т –љ–∞–Є–±–Њ–ї–µ–µ —В—Й–∞—В–µ–ї—М–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —А–∞–±–Њ—В–µ –Ь–Њ—А–≥–Њ–µ–≤–Њ–є –§.–≠. —Б —Б–Њ–∞–≤—В. –Є–Ј—Г—З–µ–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –±–Њ–ї—М–љ—Л—Е —Б –°–Ф 2 —В–Є–њ–∞ [15]. –Т –≥—А—Г–њ–њ—Г –Є–Ј 30 –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Р–Ї—В–Њ–≤–µ–≥–Є–љ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –Ї–∞–њ–µ–ї—М–љ–Њ –≤ –і–Њ–Ј–µ 400 –Љ–≥, —А–∞–Ј–≤–µ–і–µ–љ–љ–Њ–Љ –≤ 200,0 –Љ–ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞, –≤ —В–µ—З–µ–љ–Є–µ 3 –љ–µ–і–µ–ї—М (15 –Є–љ—Д—Г–Ј–Є–є), –≤–Њ—И–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л —Б –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –°–Ф –љ–µ –Љ–µ–љ–µ–µ 10 –ї–µ—В –≤ –≤–Њ–Ј—А–∞—Б—В–µ 58,94±1,29 –ї–µ—В (9 –Љ—Г–ґ—З–Є–љ –Є 21 –ґ–µ–љ—Й–Є–љ–∞). –Э–∞–ї–Є—З–Є–µ –Ф–Я–Э —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–ї–Њ—Б—М –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—Б–Љ–Њ—В—А–∞, —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –≠–Ь–У, –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–µ–љ—Б–Њ—А–љ–Њ–≥–Њ –Є –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–≥–Њ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є—П. –Т –≥—А—Г–њ–њ—Г –≤–Ї–ї—О—З–∞–ї–Є—Б—М –±–Њ–ї—М–љ—Л–µ, –Є–Љ–µ–≤—И–Є–µ 2–∞ –Є 2b —Б—В–∞–і–Є–Є –Ф–Я–Э –њ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є P.J. Dyck –Є —Г—А–Њ–≤–µ–љ—М HbA1C –љ–µ –±–Њ–ї–µ–µ 10%. –Ю—Ж–µ–љ–Ї–∞ –њ–Њ–Ј–Є—В–Є–≤–љ–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О —И–Ї–∞–ї—Л TSS (Total Symptom Score – –Њ–±—Й–Є–є —Б—З–µ—В —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–µ–≤—А–Њ–њ–∞—В–Є–Є) —Б –∞–љ–∞–ї–Є–Ј–Њ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–Є, –ґ–ґ–µ–љ–Є—П, –Њ–љ–µ–Љ–µ–љ–Є—П –Є –њ–∞—А–µ—Б—В–µ–Ј–Є–є. –Э–µ–≥–∞—В–Є–≤–љ–∞—П –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ (–љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –і–µ—Д–Є—Ж–Є—В) –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ —И–Ї–∞–ї–µ NISLL (Neuropathy Impairment Score – —Б—З–µ—В –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –і–ї—П –љ–Њ–≥) —Б —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Б–Є–ї—Л –Љ—Л—И—Ж, —Б–Њ—Б—В–Њ—П–љ–Є—П —А–µ—Д–ї–µ–Ї—Б–Њ–≤ –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ–Њ–є –Љ–Њ–і–∞–ї—М–љ–Њ—Б—В–Є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ –љ–Њ–≥ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Љ–µ—В–Њ–і–Њ–Љ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–є –≠–Ь–У —Б —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ–Љ –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ (n. peroneus) –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ (n. suralis) –љ–µ—А–≤–Њ–≤. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Г—О –Њ—Ж–µ–љ–Ї—Г –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–є –Є –≥–ї—Г–±–Њ–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є, –∞ —В–∞–Ї–ґ–µ –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –Ї–∞—А–і–Є–Њ–Є–љ–љ–µ—А–≤–∞—Ж–Є–Є –њ—А–Њ–≤–Њ–і–Є–ї–Є –љ–∞ –њ—А–Є–±–Њ—А–µ CASE–IV (Medical Electronics, –°–®–Р) —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ —Е–Њ–ї–Њ–і–Њ–≤–Њ–≥–Њ, –±–Њ–ї–µ–≤–Њ–≥–Њ –Є –≤–Є–±—А–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–Њ—А–Њ–≥–Њ–≤. –Ю–± —Г—А–Њ–≤–љ–µ –Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ —Б—Г–і–Є–ї–Є –њ–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є—О –Љ–∞–ї–Њ–љ–Њ–≤–Њ–≥–Њ –і–Є–∞–ї—М–і–µ–≥–Є–і–∞ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Є –≥–µ–Љ–Њ–ї–Є–Ј–∞—В–µ —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤. –°–Њ—Б—В–Њ—П–љ–Є–µ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Є–Ј—Г—З–∞–ї–Є –≤ –љ–Њ–≥—В–µ–≤–Њ–Љ –ї–Њ–ґ–µ 2 –њ–∞–ї—М—Ж–∞ –Ї–Є—Б—В–Є –љ–∞ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–Љ –Ї–∞–њ–Є–ї–ї—П—А–Њ—Б–Ї–Њ–њ–µ GY–0,04 —Д–Є—А–Љ—Л «–¶–µ–љ—В—А –∞–љ–∞–ї–Є–Ј–∞ –≤–µ—Й–µ—Б—В–≤» (–†–Њ—Б—Б–Є—П). –¶–Є—Д—А–Њ–≤–Њ–є –∞–љ–∞–ї–Є–Ј –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–ї –Њ–њ—А–µ–і–µ–ї–Є—В—М —Б–Ї–Њ—А–Њ—Б—В—М –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ «—Б–ї–∞–і–ґ–—Д–µ–љ–Њ–Љ–µ–љ–Њ–≤», –≤–µ–ї–Є—З–Є–љ—Г –њ–µ—А–Є–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞. –Ю–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –і–Њ –Є –њ–Њ—Б–ї–µ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П.
–Ф–Њ –ї–µ—З–µ–љ–Є—П –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –°–Ф —Б –Ф–Я–Э –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –њ–µ—А–Є–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤ –≤ –њ–ї–∞–Ј–Љ–µ –Є –Љ–µ–Љ–±—А–∞–љ–∞—Е —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –Є–Ј 15 –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ —В–Њ–≥–Њ –ґ–µ –≤–Њ–Ј—А–∞—Б—В–∞, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞. –Ы–µ—З–µ–љ–Є–µ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –њ—А–Є–≤–µ–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Г—А–Њ–≤–љ—П –Љ–∞–ї–Њ–љ–Њ–≤–Њ–≥–Њ –і–Є–∞–ї—М–і–µ–≥–Є–і–∞ (–Ь–Ф–Р) –≤ –њ–ї–∞–Ј–Љ–µ –Є –Љ–µ–Љ–±—А–∞–љ–∞—Е —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ —Б –µ–≥–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–µ–є (—В–∞–±–ї. 1). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Р–Ї—В–Њ–≤–µ–≥–Є–љ –Њ–Ї–∞–Ј—Л–≤–∞–ї –љ–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–є —Н—Д—Д–µ–Ї—В, –і–µ–є—Б—В–≤—Г—П –љ–∞ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —А–∞–Ј–≤–Є—В–Є—П –Ф–Я–Э.
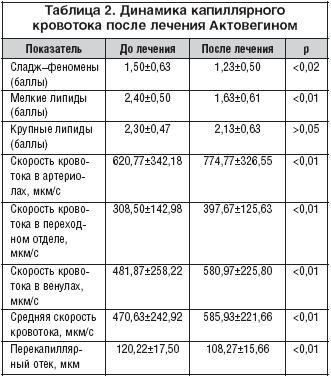
–°–Њ—Б—В–Њ—П–љ–Є–µ —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Ї—А–Њ–≤–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –Љ–µ—В–Њ–і–Њ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –Ї–∞–њ–Є–ї–ї—П—А–Њ—Б–Ї–Њ–њ–Є–Є –і–Њ –Є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ (—В–∞–±–ї. 2). –Я–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Њ—Б–љ–Њ–≤–љ—Л—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –Ї–∞–њ–Є–ї–ї—П—А–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –њ—А–Є—З–µ–Љ –љ–µ —В–Њ–ї—М–Ї–Њ –Њ—В—А–∞–ґ–∞—О—Й–Є—Е —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї—А–Њ–≤–Є, –љ–Њ –Є —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є —Б—В–µ–љ–Ї–Є –Ї–∞–њ–Є–ї–ї—П—А–∞.
–Ф–Њ –ї–µ—З–µ–љ–Є—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –њ–Њ–Ј–Є—В–Є–≤–љ–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –њ–Њ —И–Ї–∞–ї–µ TSS –±—Л–ї–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є (7,79 –±–∞–ї–ї–∞). –Я–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–∞–Ї —Б—Г–Љ–Љ—Л –±–∞–ї–ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ TSS, —В–∞–Ї –Є –±–∞–ї–ї–Њ–≤ –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј —Б–µ–љ—Б–Њ—А–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –≤ –Њ—В–і–µ–ї—М–љ–Њ—Б—В–Є (p<0,001). –Я—А–Є –Њ—Ж–µ–љ–Ї–µ –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –љ–µ–≥–∞—В–Є–≤–љ–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –±—Л–ї–∞ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є (—Б—Г–Љ–Љ–∞ –±–∞–ї–ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ NISLL – 2,27 –±–∞–ї–ї–∞), –њ—А–Є—З–µ–Љ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –≤—Л—П–≤–ї—П–ї–Є—Б—М –љ–∞—А—Г—И–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —А–µ—Д–ї–µ–Ї—Б–Њ–≤. –Я–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ (p<0,05), –љ–Њ –љ–µ –Њ—В–і–µ–ї—М–љ—Л—Е –≥—А—Г–њ–њ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ (—Б–Є–ї–∞ –Љ—Л—И—Ж, —А–µ—Д–ї–µ–Ї—Б—Л, —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М).
–Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Њ—Б–љ–Њ–≤–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ. –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л —Б–µ–љ—Б–Њ—А–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ (3,87±2,43 –Љ–Ї–Т –і–Њ –ї–µ—З–µ–љ–Є—П –Є 6,19±3,16 –Љ–Ї–Т –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П, p<0,05) –њ—А–Є –љ–µ–Є–Ј–Љ–µ–љ–љ–Њ—Б—В–Є –°–†–Т. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ—А–Њ–≥–Њ–≤ —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–є –Є –±–Њ–ї–µ–≤–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ—А–Њ–≥–Њ–≤ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б —Б–Њ—Б—В–Њ—П–љ–Є–µ–Љ —В–Њ–љ–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ (—А<0,05). –Э–µ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–≥–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –њ–Њ—А–Њ–≥–∞ –≤–Є–±—А–∞—Ж–Є–Њ–љ–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є (—В–Њ–ї—Б—В—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞), —Е–Њ—В—П –њ—А–Є –≠–Ь–У –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–Њ–ї—Г—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л —Б–µ–љ—Б–Њ—А–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞. –Т–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М —Б–µ—А–і–µ—З–љ–Њ–≥–Њ —А–Є—В–Љ–∞, –њ–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П R–R –Є–љ—В–µ—А–≤–∞–ї–Њ–≤ –≤ –њ–Њ–Ї–Њ–µ –Є –њ—А–Є –њ—А–Њ–±–µ —Б –≥–ї—Г–±–Њ–Ї–Є–Љ –і—Л—Е–∞–љ–Є–µ–Љ, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–∞—Б—М –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ, —Е–Њ—В—П –Њ—В–Љ–µ—З–µ–љ–∞ —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –µ–µ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –ї–µ—З–µ–љ–Є–µ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ, —Г–Љ–µ–љ—М—И–∞—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ –Є —Г–ї—Г—З—И–∞—П —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–Є—Б—В–µ–Љ—Л –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є, –њ—А–Є–≤–Њ–і–Є—В —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ф–Я–Э (–њ–Њ–Ј–Є—В–Є–≤–љ–Њ–є –Є –љ–µ–≥–∞—В–Є–≤–љ–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є), —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ (–≠–Ь–У –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–µ–љ—Б–Њ—А–љ–Њ–µ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ). –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –≤—Б–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –њ—А–Є –Ф–Я–Э –њ–Њ–Ї–∞–Ј–∞–ї–Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П, –Є–Љ–µ–µ—В—Б—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Љ–∞—Б—И—В–∞–±–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б –±–Њ–ї—М—И–Є–Љ —З–Є—Б–ї–Њ–Љ –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П –Є –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ–Њ–і –њ–∞—В—А–Њ–љ–∞–ґ–µ–Љ –Ї–Њ–Љ–њ–∞–љ–Є—П «–Э–Є–Ї–Њ–Љ–µ–і» –њ—А–Њ–≤–Њ–і–Є—В—Б—П –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –і–≤–Њ–є–љ–Њ–µ —Б–ї–µ–њ–Њ–µ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б –±–Њ–ї—М—И–Є–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е, —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–Њ—В–Њ—А–Њ–≥–Њ –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ —А–µ—И–∞—В –≤–Њ–њ—А–Њ—Б –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ф–Я–Э.
–° –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Љ–љ–µ–љ–Є—П, —З—В–Њ –Њ–±–ї–∞–і–∞—О—Й–Є–є –∞–љ—В–Є–≥–Є–њ–Њ–Ї—Б–∞–љ—В–љ—Л–Љ –Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Р–Ї—В–Њ–≤–µ–≥–Є–љ –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –њ—А–Є —И–Є—А–Њ–Ї–Њ–Љ –Ї—А—Г–≥–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Ї–Њ—В–Њ—А—Л—Е –Є–≥—А–∞–µ—В —А–Њ–ї—М –≥–Є–њ–Њ–Ї—Б–Є—П, –Є—И–µ–Љ–Є—П –Є –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ—Л–є —Б—В—А–µ—Б—Б. –Я—А–µ–њ–∞—А–∞—В –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –њ—А–Є –≤—Б–µ—Е —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ—А–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Є–ї–Є —Б–Љ–µ—И–∞–љ–љ—Л–Љ–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ––і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –љ–∞–њ—А–Є–Љ–µ—А –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ –љ–µ–≤—А–Њ–њ–∞—В–Є–Є, —В–Њ–љ–љ–µ–ї—М–љ—Л–µ –Є —А–∞–і–Є–Ї—Г–ї—П—А–љ—Л–µ —Б–Є–љ–і—А–Њ–Љ—Л, –≤ –≥–µ–љ–µ–Ј–µ –Ї–Њ—В–Њ—А—Л—Е —Б–Њ—Б—Г–і–Є—Б—В—Л–є —Д–∞–Ї—В–Њ—А –Љ–Њ–ґ–µ—В –Є–≥—А–∞—В—М –≤–∞–ґ–љ—Г—О —А–Њ–ї—М, —В–∞–Ї–ґ–µ —П–≤–ї—П—О—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є —Ж–µ–ї—М—О –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –†—Г–Љ—П–љ—Ж–µ–≤–∞ –°.–Р. –§–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –Є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –∞–Ї—В–Њ–≤–µ–≥–Є–љ–∞ // –Т —Б–±. «–Р–Ї—В–Њ–≤–µ–≥–Є–љ. –Э–Њ–≤—Л–µ –∞—Б–њ–µ–Ї—В—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П» – –Ь. – 2002 – —Б—В—А. 3–9.
2. –Э–Њ—А–і–≤–Є–Ї –С. –Ь–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –∞–Ї—В–Њ–≤–µ–≥–Є–љ // –Т —Б–±. «–Р–Ї—В–Њ–≤–µ–≥–Є–љ. –Э–Њ–≤—Л–µ –∞—Б–њ–µ–Ї—В—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П» – –Ь. – 2002 – —Б—В—А. 18–24.
3. –®–Є–ї–Њ–≤ –Р.–Ь. –Р–љ—В–Є–≥–Є–њ–Њ–Ї—Б–∞–љ—В—Л –Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В—Л –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ // –†—Г—Б—Б. –Љ–µ–і. –ґ—Г—А–љ.– 2004 – вДЦ2 – —Б—В—А.112–114.
4. Saletu B., Grunberger J., Linzmayer L. et al. EEG brain mapping and psychometry in age–associated memory impairment after acute and 2–week infusions with the hemoderivative Actovegin: double–blind, placebo–controlled trials // Neurophychobiol. – 1990/1991 – Vol.24 – P.135–148.
5. Semlitsch H.V., Anderer P., Saletu B. et al. Topographic mapping of cognitive event–related potentials in a double–blind, placebo–controlled study with the hemoderivative Actovegin in age–associated memory impairment // Neurophychobiol. – 1990/1991 – Vol.24 – P.49–56.
6. Oswald W.D., Steger W., Oswald B. et al. Die Verbesserung fluider kognitiver Leistungen als Indikator fur die klinische Wirksamkeit einer nootropen Substanz.Eine placebokontrollierte Doppelblind–Studie mit Actovegin // Z. Gerontopsychol.–psychiatrie. – 1991 – Vol.4 – P.209–220.
7. –ѓ–љ—Б–µ–љ –Т., –С—А—Г–Ї–љ–µ—А –У.–Т. –Ы–µ—З–µ–љ–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –і—А–∞–ґ–µ –Р–Ї—В–Њ–≤–µ–≥–Є–љ —Д–Њ—А—В–µ (–і–≤–Њ–є–љ–Њ–µ —Б–ї–µ–њ–Њ–µ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ) // –†—Г—Б—Б. –Љ–µ–і.–ґ—Г—А–љ. – 2002 – вДЦ12–13 – —Б—В—А.543–546.
8. –Ъ–∞–Љ–Љ–µ—А–µ—А –°. –†–∞–љ–љ–µ–µ –љ–∞—З–∞–ї–Њ —В–µ—А–∞–њ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–µ–Љ–µ–љ—Ж–Є–µ–є // –†—Г—Б—Б.–Љ–µ–і.–ґ—Г—А–љ. – 2003 – вДЦ10 – —Б—В—А.583–585.
9. Kinzler E., Lehmann E., Groth J. et al. Actovegin in der Behandlung geriatrischer Patienten mit hirnorganischem psychosyndrom // Munch Med Wochenschr – 1988 – Vol. 130 – P.644–646.
10. –®–Љ—Л—А–µ–≤ –Т.–Ш., –Ю—Б—В—А–Њ—Г–Љ–Њ–≤–∞ –Ю.–Ф., –С–Њ–±—А–Њ–≤–∞ –Ґ.–Р. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Р–Ї—В–Њ–≤–µ–≥–Є–љ –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є–Є –і–µ–Љ–µ–љ—Ж–Є–Є // –†—Г—Б—Б.–Љ–µ–і.–ґ—Г—А–љ. – 2003 – вДЦ4 – —Б—В—А.216–220.
11. –Ъ—Г–љ—Ж –У., –®—Г–Љ–∞–љ –У. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –∞–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –њ—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є: —А–µ–Ј—Г–ї—М—В–∞—В—Л –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –і–≤–Њ–є–љ–Њ–≥–Њ —Б–ї–µ–њ–Њ–≥–Њ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П // –Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї – 2004 – вДЦ1 – —Б—В—А.40–44.
12. –Ь–Є—Е–∞–ї–Њ–≤–Є—З –Э., –•–∞–Ї –Ф–ґ. –Р–љ—В–Є–≥–Є–њ–Њ–Ї—Б–∞–љ—В—Л –≤ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —З–µ—А–µ–њ–љ–Њ––Љ–Њ–Ј–≥–Њ–≤—Л—Е —В—А–∞–≤–Љ // –†—Г—Б—Б. –Љ–µ–і. –ґ—Г—А–љ. – 2004 – вДЦ10 – —Б—В—А.621–625.
13. –°—В—А–Њ–Ї–Њ–≤ –Ш.–Р., –Ь–Њ—А–≥–Њ–µ–≤–∞ –§.–≠., –°—В—А–Њ–Ї–Њ–≤ –Ъ.–Ш. –Є –і—А. –Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є –Є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ // –†—Г—Б—Б. –Љ–µ–і.–ґ—Г—А–љ. – 2006 – вДЦ9 – —Б—В—А.698–703.
14. –®–Љ—Л—А–µ–≤ –Т.–Ш., –С–Њ–±—А–Њ–≤–∞ –Ґ.–Р. –Р–Ї—В–Њ–≤–µ–≥–Є–љ –Є –Ї—Б–µ—Д–Њ–Ї–∞–Љ –≤ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–µ—А—В–µ–±—А–Њ–≥–µ–љ–љ—Л—Е –±–Њ–ї–µ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ —Г –њ–Њ–ґ–Є–ї—Л—Е // –Ы–µ—З–µ–љ–Є–µ –љ–µ—А–≤–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є – 2002 – вДЦ1 – —Б—В—А.37–39.
15. –Ь–Њ—А–≥–Њ–µ–≤–∞ –§.–≠., –Р–Љ–µ—В–Њ–≤ –Р., –°—В—А–Њ–Ї–Њ–≤ –Ш.–Р. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П –Є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є—П: —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ // –†—Г—Б—Б. –Љ–µ–і.–ґ—Г—А–љ. – 2005 – вДЦ 6 – —Б—В—А.302–304.
16. Jansen W., Beck E. –Ы–µ—З–µ–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є. –Ъ–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –і–≤–Њ–є–љ–Њ–µ —Б–ї–µ–њ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ // –Т —Б–±. «–Ю–њ—Л—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –≤ —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є» – –Ь., 2005 – —Б—В—А.11–20.
17. –ѓ–≤–Њ—А—Б–Ї–∞—П –Т.–Р., –Х–≥–Њ—А–Ї–Є–љ–∞ –Ю.–Т., –Ь–∞—И–Ї–Є–љ –Ю.–Э. –Є –і—А. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –њ—А–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є // –Т —Б–±. «–Ю–њ—Л—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –≤ —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є» – –Ь. – 2005 – —Б—В—А.27–30.
18. –†—Г–Љ—П–љ—Ж–µ–≤–∞ –°.–Р., –С–µ–љ–µ–≤–Њ–ї–µ–љ—Б–Ї–∞—П –Э.–У., –Х–≤—Б–µ–µ–≤ –Т.–Э. –Р–љ—В–Є–≥–Є–њ–Њ–Ї—Б–∞–љ—В—Л –≤ —А–µ–∞–љ–Є–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є // –†—Г—Б—Б. –Љ–µ–і.–ґ—Г—А–љ. – 2004 – вДЦ22 – —Б—В—А.302–304.
19. –Ю–±–Њ–ї–µ–љ—Б–Ї–Є–є –Т.–Э. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л // –Т —Б–±. «–Ю–њ—Л—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –≤ —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є» – –Ь., 2005 – —Б—В—А.39–46.
20.–Х—Д–Є–Љ–Њ–≤ –Р.–°. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є–µ –∞–љ–≥–Є–Њ–њ–∞—В–Є–Є // –Ь. «–Ь–µ–і–Є—Ж–Є–љ–∞» – 1989.
21. Brownly M. Biochemistry and molecular cell biology of diabetic complications // Nature – 2001 – Vol.414 – P.813–820.












