Введение
Синдром боли в спине остается одной из самых частых причин обращения к врачу как в нашей стране, так и за рубежом [1, 2]. Согласно последним эпидемиологическим исследованиям, в течение жизни боль в спине возникает у 70–90% населения, преимущественно у людей трудоспособного возраста, а у 20–25% регистрируется ежегодно [3]. Глобальное исследование заболеваемости населения (Global Burden of Disease Study) признало боль в спине главной причиной нетрудоспособности в мире [4]. Боль в нижней части спины (БНС) является одной из самых частых причин обращения к врачам самых разных специальностей. Европейское многоцентровое исследование продемонстрировало, что хронической болью страдает более 20% жителей Европы, при этом большинство пациентов испытывало боль именно в нижней части спины [5].При этом на терапевтическое звено оказания медицинской помощи падает наибольшая нагрузка по работе с данной категорией пациентов. Согласно опросу, проведенному Всероссийским центром изучения общественного мнения (ВЦИОМ) в ноябре 2017 г., охватившему более 700 жителей РФ трудоспособного возраста (от 22 до 45 лет), испытывавших боли в спине в настоящее время или в течение последнего года, выявлено, что более 1/3 из них обращались именно к терапевту с жалобами на боли в спине (рис. 1).

Диагностический поиск при БНС
Очевидно, что боль как патологический феномен является целой цепью изменений на разных уровнях организма [2]. Поначалу защитный механизм, сигнализирующий о проблеме, позднее становится серьезным и, подчас, самостоятельным страданием. Как писал еще Авиценна: «Боль помогает врачу распознать заболевание, нередко указывая правильный путь лечения. Такая боль приносит пользу, подобно огню, когда он согревает, а не сжигает; подобно воде, когда она орошает, а не затопляет, подобно ветру, когда он освежает, а не разрушает».Поэтому задачи терапевтической службы — не столько постановка точного топического диагноза, сколько скрининг и анализ основных жалоб и симптомов, исключение серьезной патологии (так называемых «красных флагов»), назначение противоболевой терапии, которая сама по себе может дать подсказки о причине развития болевого синдрома, и при необходимости направление пациента к узкому специалисту для уточнения диагноза [1, 3].
БНС характеризуют как боль, мышечное напряжение и/или скованность, локализующиеся между нижней парой ребер и ягодичными складками с иррадиацией в нижние конечности или без таковой. Доброкачественная скелетно-мышечная боль в спине не считается нозологической единицей. Высокая распространенность и частое отсутствие конкретной объективно визуализируемой анатомической причины заставили выделить синдром БНС в МКБ-10 в качестве регистрационной, а не нозологической категории М 54.5. Для этой формы БНС не выявлено связи между тяжестью морфологических изменений позвоночника (по данным компьютерной и магнитно-резонансной томографии) и выраженностью боли в спине. Так, явная патология межпозвонковых дисков зачастую обнаруживается у практически здоровых людей, при этом выявление патологических изменений в межпозвонковых дисках не приводит к развитию боли в спине в дальнейшем [2, 3, 5].
С практической точки зрения удобно выделять 3 основные причины болей в спине.
Неспецифическая боль в спине (частота встречаемости — 85–90%). Этот термин означает, что не удалось выявить серьезную патологию (заболевание), явившуюся причиной боли: инфекцию, травму, воспаление, опухоль, остеопороз, ревматоидный артрит, анкилозирующий спондилит, заболевание соединительной ткани и др. Помимо этого, должны отсутствовать специфические признаки вовлечения в процесс корешков спинномозговых нервов (радикулопатия — 1–5%, синдром конского хвоста — до 2%) и стеноза спинномозгового канала.
Специфические причины (частота встречаемости 4–7%):
перелом позвоночника;
первичные и метастатические опухоли позвоночника;
миеломная болезнь;
спондилоартрит;
остеомиелит;
эпидурит;
сирингомиелия;
опухоли спинного мозга и спинномозговых корешков;
заболевания внутренних органов.
Боль, вызванная компрессионной радикулопатией, стенозом поясничного канала (частота встречаемости — 7%).
С учетом того, что большинство заболеваний внутренних органов находятся в сфере ответственности терапевта, становится ясно, что именно этому врачу чаще всего приходится решать проблему болей в спине.
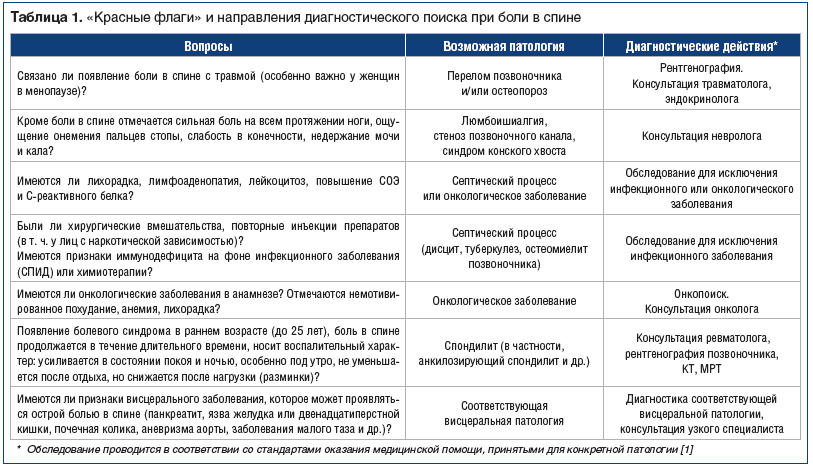
В помощь терапевтам разработаны относительно простые диагностические алгоритмы и опросники [3, 6]. Не требующий специальных инструментов, простой, но скрупулезный диагностический поиск позволяет уже на амбулаторном терапевтическом приеме не только верифицировать самые распространенные причины болевого синдрома, но и заподозрить серьезные заболевания, требующие неотложных мер, диагностических процедур, направления к узким специалистам (табл. 1).
Минимальный лабораторный диагностический набор состоит из анализа крови и мочи, оценки скорости клубочковой фильтрации, концентраций глюкозы и — при возможности — высокоточной оценки С-реактивного белка.
Минимальный инструментально-диагностический набор состоит из измерения артериального давления, ЭКГ, рент-
геновского исследования органов грудной клетки и УЗИ
органов брюшной полости и забрюшинного пространства.
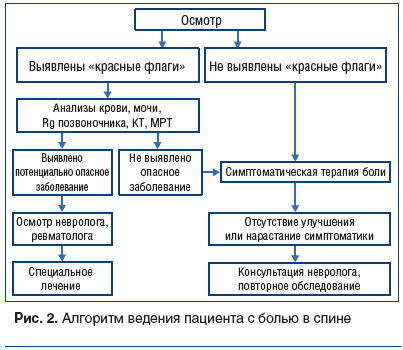
Алгоритм действий врача-терапевта представлен на рисунке 2.
Терапия боли в спине
Сложности в достижении адекватного обезболивания в рутинной практике определяются упомянутой выше коморбидностью, неизбежной полипрагмазией и необходимостью долгосрочной терапии болевого синдрома [7, 8]. У коморбидных пациентов с целой палитрой соматических заболеваний предпочтительным критерием выбора становится безопасность лекарственного препарата и безопасность лекарственного взаимодействия.Проведенные эпидемиологические исследования показывают, что не более чем у 20% пациентов удается обеспечить адекватное обезболивание. Это связано с использованием недостаточно эффективных либо устаревших лекарств, необоснованных схем применения, рефрактерностью у пациентов, часто использующих анальгетики, нежелательными побочными реакциями и др. [8].
У большинства пациентов проводимая терапия эффективно купирует боли в течение 4 нед. Однако почти у 73% больных в течение первого года наблюдения развивается как минимум одно обострение [7]. Также отмечено, что 20–25% больных продолжают испытывать боль в спине, т. е. страдание становится хроническим, что приводит к существенному возрастанию нагрузки и на органы здравоохранения, и на бюджет в целом: на эту когорту больных тратится до 80% средств здравоохранения [7].
Самым частым средством купирования как острых, так и хронических болевых синдромов в отечественной и мировой практике являются нестероидные противовоспалительные препараты (НПВП). Это корреспондирует и с Рекомендациями по ведению хронической боли [9]. Ключевыми препаратами они остаются и при лечении болей в спине [10]. Выбор НПВП должен быть обдуманным и взвешенным, с оценкой соотношения риска и пользы конкретного препарата.
Чем в основном определяется сегодня безопасность терапии НПВП? Ответ, очевидно, лежит в области коморбидности пациентов, отмечаемой в последнее время не только у пожилых, но и у относительно молодых больных. Так, риск повреждения слизистой оболочки органов желудочно-кишечного тракта (в т. ч. НПВП-гастропатии) есть у большинства пациентов отделений кардиологии, терапии, гастроэнтерологии. Причем кровотечения, связанные с собственно язвенной болезнью, составляют лишь небольшую часть всех желудочно-кишечных кровотечений (ЖКК) в структуре смертельных осложнений, явившихся причиной летального исхода [11]. При безальтернативности применения НПВП при болевых синдромах одной из основных задач менеджмента боли остается выбор правильного препарата и его лекарственной формы [10, 11].
Понимание различной роли изоформ циклооксигеназы (ЦОГ) в механизмах воспаления и генезе побочных эффектов препаратов НПВП привело к разработке и внедрению в широкую клиническую практику наряду с «классическими» и относительно селективных и высокоселективных ЦОГ-2 ингибиторов. Эти препараты имеют лучший профиль гастроэнтерологической безопасности. Однако практика их применения сопровождается сообщениями о кардиоваскулярных рисках высокоселективных ЦОГ-2 ингибиторов. Результаты клинического исследования VIGOR, в котором проводилось сопоставление эффективности и безопасности напроксена и рофекоксиба в симптоматической терапии ревматоидного артрита, показали, что при более низкой частоте желудочно-кишечных побочных эффектов у пациентов, получавших рофекоксиб, частота инфаркта миокарда в этой группе составила 0,4% в сравнении с 0,1% у пациентов группы напроксена [12]. Существенное увеличение риска кардиоваскулярных катастроф при использовании рофекоксиба было получено и в исследовании APPROVe [13]. Поэтому интерес исследователей и клиницистов при применении НПВП при острой и хронической боли смещается к препаратам со сбалансированной активностью в отношении ЦОГ [14]. Особенно это важно для коморбидных пациентов, т. к. сердечно-
сосудистые заболевания и поражения ЖКТ относятся к самым частым вариантам коморбидности.
Представителем НПВП, обладающим благоприятным профилем ингибирования активности ЦОГ, является ибупрофен, считающийся и одним из наиболее изученных анальгетиков в группе НПВП. При лечении сильных болевых синдромов, требующих быстрого купирования, перспективной оказалась комбинация ибупрофена с парацетамолом, обеспечивающая потенцирование действия обоих компонентов, возможность снижения дозировок с минимизацией риска побочных эффектов [15]. Оценка рисков развития желудочно-кишечных осложнений при терапии различными НПВП проведена в исследованиях J. Castellsague et al., А.Е. Каратеева и др., результаты приведены на рисунке 3 [16, 17].

Риски сердечно-сосудистых осложнений при терапии различными НПВП оценены в исследовании С. Varas-Lorenzo et al. (2013), результаты приведены на рисунке 4 [18].

Собственная анальгетическая эффективность предлагаемой комбинации (ибупрофен 200 мг + парацетамол 500 мг, например, препарат Нурофен Лонг) превосходит эффективность монокомпонентных НПВП и даже комбинированных препаратов, содержащих кодеин (рис. 5, 6) [19]. Эта комбинация и в одинарной, и в двойной дозе (ибупрофен 400 мг + парацетамол 1000 мг) имеет самый низкий коэффициент NNT, превосходя по эффективности диклофенак и декскетопрофен [20].

![Рис. 6. Сравнительная эффективность комбинированных анальгетиков [19] Рис. 6. Сравнительная эффективность комбинированных анальгетиков [19]](/upload/medialibrary/9da/13-7.png)
Двойное слепое плацебо-контролируемое рандомизированное исследование S.E. Daniels et al. (n=600) показало, что комбинация ибупрофен 200 мг + парацетамол 500 мг, содержащаяся в препарате Нурофен Лонг, обеспечивает сопоставимое и даже более эффективное обезболивание, чем комбинированные кодеинсодержащие препараты [19].
Современная технология Synchro-Tech™ позволяет быстро высвобождать компоненты препарата, при этом эффективный обезболивающий эффект развивается уже к 15-й мин, достигает максимума к 40 мин и продолжается до 8 ч. Клинически важным оказывается и наличие противовоспалительного эффекта препарата Нурофен Лонг, реализуемого за счет нескольких механизмов: ингибирования ЦОГ, снижения выработки простагландинов на центральном уровне регуляции, уменьшения выработки провоспалительных медиаторов на локальном уровне, ингибирования миграции лейкоцитов в очаг воспаления.
Терапия болевого синдрома в спине может требовать дополнительного назначения и препаратов, содержащих витамины группы В, миорелаксантов, применения аппаратных методов лечения, физиотерапии, когнитивно-поведенческой терапии, которую ряд исследователей относит к первостепенным подходам. При всей обоснованности этих рекомендаций именно успешность (скорость и мощность) обезболивания определяет впечатление пациента от назначений врача, формирует уровень доверия и повышает комплаентность, что в конечном итоге служит залогом эффективности терапии.












