Ретинокохлеоцеребральная васкулопатия была описана в 1979 г. группой авторов под руководством Джона Сусака [1] у лиц молодого возраста с классической клинической триадой: подострой энцефалопатией, окклюзией ветвей артерии сетчатки и нейросенсорной тугоухостью. Как следствие четко очерченной клинической составляющей, в зарубежных статьях можно встретить соответствующие ей аббревиатуры: SICRET (Small Infarcts of Cochlear, Retina and Encephalic Tissue — мелкие инфаркты слухового нерва, сетчатки и ткани мозга) и RED-M (Retinopathy, Encephalopathy, Deafness microangiopathy — ретинопатия, энцефалопатия, глухота, обусловленные микроангиопатией) [2, 3].
Первое популяционное исследование по распространенности синдрома Сусака было проведено в Австрии. Дебют заболевания описан с 9 до 72 лет, чаще у женщин в возрасте 20–40 лет [4]. При этом с учетом выявленной распространенности синдрома в соотношении 0,15 на 100 тыс. населения на сегодняшний день описано чуть более 300 случаев.
Этиология синдрома Сусака
Этиология синдрома до конца не установлена, однако, как и у большинства других аутоиммунных заболеваний, отмечается его появление после беременности, перенесенной вирусной инфекции, применения заместительной гормональной терапии.Согласно современным представлениям, в основе болезни лежит микроангиопатия головного мозга, сетчатки, внутреннего уха. Предполагается, что у таких пациентов развивается иммунообусловленная эндотелиопатия в микроваскулярном русле. При этом в отдельных сосудах паренхимы отмечаются утолщение и гиалиноз, эндотелиальные клетки гипертрофированы, что в итоге и ведет к окклюзии артериол. В результате этого возникает периваскулярное воспаление с последующей ишемией тканей головного мозга, сетчатки. Действительно, в сыворотке крови пациентов с синдромом Сусака выявлены антитела к эндотелию сосудов, которые могут вызывать развитие микроангиопатии [5], определяющей размер характерных для
синдрома очагов (в среднем около 5 мм). В результате возникает дегенерация нейроглиального комплекса. При этом иммуногистохимические исследования показывают воспаление с превалированием CD8-клеток. Как известно, CD8 являются поверхностными маркерами субпопуляции цитотоксических Т-лимфоцитов и Т-супрессоров. Экспрессия этого гликопротеина у человека происходит в основном на Т-киллерах, а также на части натуральных киллеров (NK). Это, в свою очередь, определяет аутоиммунную составляющую синдрома, дает возможность диагностировать его с помощью иммуногистохимических исследований, а также назначать таргетную терапию.
Клиническая картина синдрома Сусака
Установлено, что для синдрома Сусака характерно полиорганное поражение с развитием ретикулокохлеоцеребральных расстройств. Такие пациенты, как правило, госпитализируются в офтальмологические, отоларингологические и неврологические отделения стационаров. Однако в дебюте заболевания классическая триада возникает в полном объеме довольно редко (не более 20% случаев). Почти всегда синдром дебютирует с нарушения зрительной функции. Так, пациенты вне церебрального синдрома могут предъявлять жалобы на преходящее или стойкое нарушение зрения в виде появления пелены перед глазами, диплопии, фотопсий или парацентральных скотом. В половине случаев отмечается одно- или двустороннее снижение слуха, зачастую сопровождающееся шумом в ушах и головокружением. Иногда наблюдается нарастающая головная боль с тошнотой. При этом некоторые авторы особо подчеркивают, что при развитии головной боли у иммуноскомпрометированных лиц молодого возраста уже необходимо задуматься о синдроме Сусака. Также отмечаются сонливость, нарушение сознания, расстройства речи, концентрации внимания, памяти или ходьбы. Клинические проявления синдрома могут включать амнезию, агрессию, депрессию, в редких случаях — судороги [6–13].
Диагностика синдрома Сусака
Для синдрома Сусака нехарактерно изменение параметров крови. Имеются данные об умеренном повышении уровня белка в ликворе и незначительном лимфоцитарном плеоцитозе. Ультразвуковая диагностика с допплеровским картированием при данном синдроме не выявляет специфических маркеров.Офтальмологическое исследование (электроокулография, электроретинография, офтальмоскопия, зрительные вызванные потенциалы) выявляет картину ретинального васкулита: расширение артериол сетчатки, телеангиэктазии, микроаневризмы. По данным ангиографии с флуоресцеином определяются множественные периферические инфаркты сетчатки с обеих сторон [5, 14, 15]. Оптическая когерентная томография сетчатки выявляет выраженное пятнистое истончение слоя нервных волокон, тогда как при рассеянном склерозе это истончение имеет диффузный характер.
В диагностике нарушений слуха эффективно применение слуховых вызванных потенциалов, отоакустической эмиссии.
В дифференциальной диагностике синдрома Сусака важное значение придается нейрорадиологическим исследованиям [16]. Патогномоничным считается выявление с помощью магнитно-резонансной томографии (МРТ) головного мозга множественных гиперинтенсивных сигналов в центральной части мозолистого тела. При введении парамагнетика происходит обогащение патологических очагов, выявляемых на Т2-взвешенных изображениях. Помимо типичных изменений в виде маленьких или больших «снежных шаров» или линейных дефектов в центральной части мозолистого тела (рис. 1а, б) [17] у 70% больных имеется поражение серого вещества, а у 33% — оболочек мозга [18]. По данным МРТ (диффузионно-взвешенный режим) в этой области выявляются очаги высокой интенсивности. Режим 3D-FLAIR также выявляет вовлечение в патологический процесс мягкой мозговой оболочки [19]. Необходимо помнить, что, в отличие от рассеянного склероза, для синдрома Сусака образование патологических очагов в спинном мозге нехарактерно. МРТ головного мозга позволяет проводить раннюю диагностику синдрома Сусака и, соответственно, своевременную патогенетическую терапию [5, 11, 20].
![Рис. 1. a. «Снежные шары» в центральной части мозолистого тела по данным Т2-режима МРТ (стрелки); б. Перивентрикулярные очаги на аксиальном срезе головного мозга (стрелки) (по Vishnevskia-Dai V. et. al., 2016 [17]) Рис. 1. a. «Снежные шары» в центральной части мозолистого тела по данным Т2-режима МРТ (стрелки); б. Перивентрикулярные очаги на аксиальном срезе головного мозга (стрелки) (по Vishnevskia-Dai V. et. al., 2016 [17])](/upload/medialibrary/477/10-1.png)
Дифференциальная диагностика синдрома Сусака
Дифференциальную диагностику синдрома Сусака проводят с аутоиммунными демиелинизирующими заболеваниями (рассеянным склерозом и острым рассеянным энцефаломиелитом), инфекционными энцефалитами, первичными и вторичными васкулитами центральной нервной системы (ЦНС), болезнью Меньера, токсической лейкоэнцефалопатией, редким осложнением злоупотребления кокаином [21]. Также синдром следует дифференцировать с паранеопластическими синдромами, характерными для группы пациентов, находящихся на терапии иммуносупрессорами и таргетными противоопухолевыми препаратами.Сложность выявления синдрома Сусака состоит в том, что клиническая триада, характерная для данного заболевания, может развиваться в течение нескольких лет. Показано, что из 10 пациентов с установленным позднее диагнозом синдрома Сусака только у 2 в дебюте выявлялись подострая энцефалопатия, окклюзия ветвей артерии сетчатки и нейросенсорная тугоухость [17]. У остальных больных триада патогномоничных для синдрома Сусака проявлений развивалась в течение последующих 3 лет. В этой связи было предложено различать варианты: случаи, подозрительные на синдром Сусака, полный и неполный синдромы Сусака. Согласно диагностическим критериям, разработанным группой европейских экспертов, следует выделять возможный и определенный синдромы Сусака [11]. Исследователи рассмотрели, как они отмечают, 32 несомненных случая синдрома и на основании этого выделили критерии его диагностики. Думается, что создание классификации, необходимой для клинической практики, требует дальнейшего накопления материала.
Клинические наблюдения
Тем не менее при существующем интересе к синдрому Сусака на сегодняшний день официально зарегистрировано лишь два продолжающихся исследования по его изучению, направленных на определение характерных для него биомаркеров (NCT01273792, Германия) и выявление эпидемиологической составляющей, клинических и этиологических факторов (NCT01481662, Франция). При этом если результаты первого исследования ожидаются в декабре 2018 г., то отчет второго исследования (с учетом заявленной группы из 100 пациентов с выполнением диффузионно-тензорной МРТ), начатого в 2011 г., ожидается лишь в середине 2021 г.Причины развития синдрома Сусака окончательно неясны. К примеру, обсуждается сходство его иммунопатогенеза с ювенильным дерматомиозитом, при этом отмечен положительный эффект проведения терапии, используемой при тяжелых формах этого заболевания у подростков [18, 22, 23].
Углубленное обследование 9 пациентов (женщин — 7, мужчин — 2) и анализ 92 прежде сообщенных случаев синдрома Сусака (средний возраст — 30,4 года; срок наблюдения — 6,4 года) показало, что дебют заболевания чаще отмечался весной или осенью у 68% пациентов [24]. Полная триада симптомов в начале болезни выявлялась только у 1 из 9 больных. У всех обследованных имелись головная боль и клинические проявления энцефалопатии. При исследовании ликвора у 5 пациентов выявлены плеоцитоз и повышение уровня белка. Вовлечение внутреннего уха в патологический процесс в дебюте болезни отмечалось только у 2 больных, у других это расстройство появилось в течение последующих 11 мес. (в 3 случаях сначала одностороннее, в дальнейшем у всех обследованных — двустороннее); улучшение слуха на фоне лечения не отмечено. Поражение зрения в начале болезни отмечалось у 8 больных, спустя 3 года — еще у 1 пациента. У всех обследованных выявлялась множественная билатеральная окклюзия ветвей ретинальных артерий и/или обнаруживалась краска с гиперфлюоресценцией на артериальной стенке при ангиографии с флуоресцеином. В дальнейшем у 3 больных эти показатели нормализовались.
В период наблюдения за пациентами у 3 женщин были выявлены 4 беременности: в 2 случаях состояние пациенток потребовало прерывания беременности, 1 беременность протекала без особенностей, у 1 женщины после родов отмечалось обострение синдрома Сусака с проявлениями энцефалопатии, достаточно эффективно подвергавшейся коррекции на фоне применения кортикостероидов и антикоагулянтов.
Особый интерес в литературе вызывают описания синдрома Сусака у детей и подростков. У 14-летней девочки дебют заболевания характеризовался головной болью, развитием слабости в левых конечностях, недержанием мочи и когнитивным дефицитом. МРТ головного мозга выявила множественные очаги с высокоинтенсивным сигналом на Т2-взвешенном изображении в белом и сером веществе [15]. Сходная клиническая картина и изменения белого вещества ткани мозга могут быть при развитии рассеянного склероза или острого рассеянного энцефаломиелита в детском или подростковом возрасте. На глазном дне у пациентов с этими демиелинизирующими заболеваниями обычно находят побледнение височных дисков зрительных нервов, иногда выявляется картина ретробульбарного синдрома. Однако офтальмологическое обследование у данной больной обнаружило двустороннюю окклюзию артерий сетчатки. Через 12 мес. у девочки развилась утрата слуха.
При этом обследование на инфекции было отрицательным, иммунологические тесты не отличались от нормальных показателей. При синдроме Сусака лабораторные данные свидетельствуют о наличии микроангиопатии прекапиллярных артериол мозга, сетчатки, внутреннего уха. При ангиографии с флуоресцеином патогномоничным считаются окрашивание артериол сетчатки, проксимальных по отношению к окклюзированным, и окрашивание неокклюзированных артериол.
Болезнь часто протекает с повторными атаками, возможно развитие спонтанных ремиссий, что сходно с течением рецидивирующе-ремиттирующего типа течения рассеянного склероза. Однако при синдроме Сусака часто остаются последствия в виде утраты слуха и неврологических расстройств. Это не характерно для детей и подростков с рассеянным склерозом, у которых быстро наступает ремиелинизация очагов поражения, а динамика клинических и нейровизуализационных признаков часто является положительной [14].
Нарушение слуха может быть ранним симптомом при синдроме Сусака. При обследовании 23 таких пациентов у 43,5% больных отмечались эпизоды снижения слуха, у 61% — шум в ушах, у 56,5% — головокружение, поэтому госпитализация проводилась в отделения ЛОР-патологии [25]. У 52% пациентов клинические проявления носили односторонний характер, у 48% — двусторонний. Только у 26,5% обследованных больных выявлялось 100% распознавание слов. Одному из пациентов с синдромом Сусака авторами исследования проведена двусторонняя кохлеарная имплантация с хорошим результатом.
Лечение и прогноз при синдроме Сусака
Относительно прогноза синдрома Сусака мнения исследователей расходятся. Существует возможность спонтанного разрешения симптоматики без активных лечебных мероприятий. В литературе описано монофазное и полициклическое течение с рецидивом спустя 23 года [26]. При наблюдении за 9 больными с синдромом Сусака под влиянием кортикостероидной терапии в течение 6,4 года было отмечено улучшение неврологического статуса, однако корреляции между клиническими проявлениями и уменьшением числа патологических очагов, обнаруживаемых по данным МРТ головного мозга, выявлено не было [24]. При этом гормональная терапия не снижала выраженность расстройств слуха и зрения. У больного, в свое время описанного М.Л. Чухловиной [27], была выявлена выделенная Сусаком триада симптомов: подострая энцефалопатия, окклюзия артерий сетчатки и нейросенсорная тугоухость в сочетании с наличием линейных дефектов в мозолистом теле и лакунарных кист в стволе мозга и таламуса по данным МРТ. Пульс-терапия преднизолоном привела к улучшению состояния: несколько снизился мышечный тонус, увеличилась сила в нижних конечностях, уменьшились проявления атаксии в руках. От лечения цитостатиками пациент отказался.Изолированное применение пульс-терапии метил-преднизолоном, как правило, оказывается неэффективным. В 2008 г. группой специалистов во главе с R.M. Rennebohm [18] высказано предположение о необходимости назначения таким пациентам агрессивной иммуносупрессивной терапии, включающей, наряду с введением кортикостероидов, применение цитостатиков и внутривенных иммуноглобулинов, как это проводится при дерматомиозите. С учетом этиопатогенеза существует мнение о необходимости подключения к основной схеме лечения непрямых антикоагулянтов и блокатора кальциевых каналов (нимодипин).
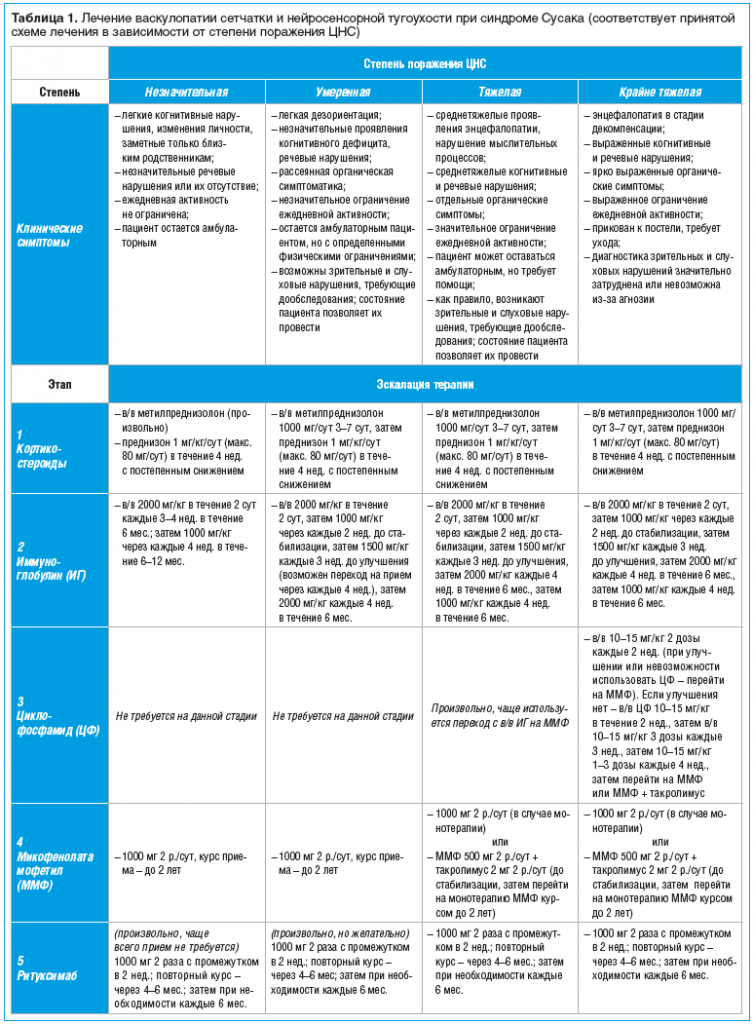
В настоящее время на базе клинического опыта зарубежных специалистов может использоваться схема терапии в зависимости от степени вовлеченности ЦНС в патологический процесс (табл. 1) [адаптировано из 28].