По данным литературы, эффективность дренажной хирургии глаукомы значительно варьирует – от 65 до 85% [5–8]. Основными недостатками при использовании дренажей в отдаленном послеоперационном периоде являются: облитерация просвета дренажа, формирование соединительнотканной капсулы вокруг наружного его конца, кистозное перерождение фильтрационной подушечки, девиация глазного яблока, регматогенные отслойки сетчатки, развитие эпителиально-эндотелиальной дистрофии роговицы, что приводит к необходимости удалять дренаж [9–15]. Вопрос о том, какие дренажи лучше и безопаснее для глаза – постоянные или биодеградируемые, – по-прежнему остается дискутабельным [16, 17].
В связи с этим актуальным является использование для дренирования в хирургии глаукомы новых полимерных материалов, сочетающих в себе высокую биосовместимость, эластичность, устойчивость и влагопроницаемость. Неоспоримым достоинством биодеградируемого материала является его способность к полному рассасыванию, что сводит к минимуму патологические реакции [18, 19]. Одной из патогенетически обоснованных является целенаправленная интраоперационная методика с использованием дренажа Глаутекс для стабильного функционирования созданных путей оттока.
Цель: оценить непосредственные и отдаленные результаты применения дренажа Глаутекс в хирургическом лечении различных видов глаукомы.
Материал и методы
Анализ результатов хирургического лечения пациентов с глаукомой проводился на базе II микрохирургического отделения ГБУ «Уфимский НИИ глазных болезней АН РБ» за 4 года (2012–2015 гг.). Всего прооперировано 243 пациента с рефрактерной глаукомой, из них 104 человека не посетили контрольные осмотры в течение срока наблюдения, в связи с чем исключены из исследования. Контрольный осмотр пациентов осуществлялся с 1 по 8 сут после операции, а также через 1, 3, 6, 12, 24 и 36 мес. Было обследовано 139 пациентов (148 глаз), в 9 случаях дренаж имплантирован на оба глаза. Клинические характеристики пациентов представлены в таблице 1.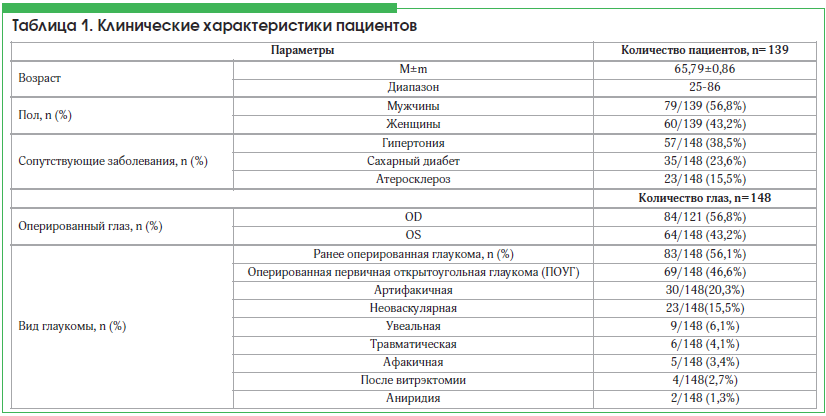
В анамнезе антиглаукомные операции выполнены в 56,1% случаев, преимущественно у пациентов с первичной открытоугольной (ПОУГ) и закрытоугольной глаукомой. Внутриглазное давление (ВГД) у всех пациентов, в т. ч. находящихся на максимальном медикаментозном режиме, превышало 32 мм рт. ст. и составляло в среднем 39,8±0,79 мм рт. ст., отмечались прогрессирование экскавации диска зрительного нерва (ДЗН) и сужение полей зрения.
Перед операцией всем пациентам провели офтальмологическое обследование, включавшее в себя определение остроты зрения по таблицам Сивцева – Головина, измерение ВГД бесконтактным пневмотонометром Topcon (Япония), биомикроскопию переднего отрезка глаза и глазного дна. Визометрия, биомикроскопия, тонометрия выполнялись до операции и при каждой последующей явке пациента на осмотр.
Техника синустрабекулэктомии с имплантацией дренажа Глаутекс была традиционной. Статистическую обработку полученных данных проводили с использованием лицензированного пакета программ Statistica 6.0. Числовые данные представлены в виде «среднее значение ± стандартная ошибка». Оценка достоверности различий между выделенными категориями объектов по какому-либо параметру проводилась при помощи методов непараметрической статистики внутри группы в динамике по критериям Вилкоксона и Фридмана. За вероятность статистически значимых различий принимались значения, начиная с p<0,05.
Результаты и обсуждение
Анализ показателей ВГД у пациентов после антиглаукомной операции с дренажом Глаутекс показал достоверное снижение изучаемого показателя на 70,3% по сравнению с исходными данными (χ2=390,4576, рФ=0,00000) (табл. 2).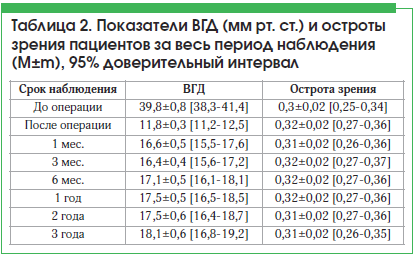
Абсолютный и относительный гипотензивный эффект составил соответственно 74,3% (110/148) и 83,1% (123/148) через 1 год после операции; 70,2% (104/148) и 79,7% (118/148) – спустя 2 года; 68,2% (101/148) и 76,3% (113/148) – после 3 лет наблюдения. При повышении ВГД были назначены гипотензивные препараты: бета-блокаторы, ингибиторы карбоангидразы, аналоги простагландина, а также их комбинации.
Отсутствие гипотензивного эффекта после антиглаукомной операции с дренажом Глаутекс при использовании гипотензивной терапии к концу наблюдаемого срока отмечено в 23,6% (35/148) случаев, из них в течение 1 мес. после операции – в 2% (3/148), через 3 мес. – в 6,1% (9/148), спустя 6 мес. – в 4,7% (7/148), 1 год – в 4,1% (6/148), 2 года – в 3,4% (5/148), 3 года – в 3,4% (5/148) случаев. Повторное хирургическое вмешательство с использованием других имплантатов выполнено в 10,8% (16/148) случаев, нидлинг – в 8,1% (12/148), при этом компенсация ВГД достигнута в 2% (3/148) случаев. Повторная синустрабекулэктомия с применением цитостатиков проведена в 6,1% (9/148) случаев. В 2,7% (4/148) случаев у пациентов с отсутствием зрительных функций и выраженным болевым синдромом выполнена криопексия. Лишь в 2% (3/148) случаев ВГД оставалось умеренно повышенным (до 28 мм рт. ст.) на фоне местной гипотензивной терапии. С учетом отсутствия ухудшения зрительных функций у этих пациентов повторное хирургическое вмешательство не проводилось.
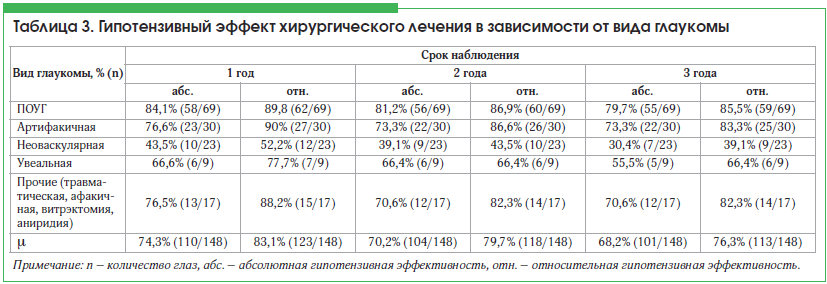
Проведенный анализ в зависимости от вида глаукомы показал, что наибольшая эффективность антиглаукомной операции с дренажом Глаутекс установлена у пациентов с ПОУГ и артифакией (табл. 3). При неоваскулярной и увеальной глаукоме количество успешных исходов значительно меньше, чем при ПОУГ и артифакии. Кроме того, дренаж Глаутекс был неэффективен у пациентов с аниридией в 50% случаев (1/2), после витрэктомии – в 25% (1/4), после травмы – в 16,7% (1/6).
Динамика показателей остроты зрения представлена в таблице 2, отмечена статистическая достоверность анализируемых данных относительно дооперационных значений (χ2=36,48117, рФ=0,00001). После антиглаукомной операции с дренажом Глаутекс повышение остроты зрения отмечено в 9,5% (14/148) случаев. Снижение остроты зрения, связанное с прогрессированием катаракты, отмечено в 5,4% (8/148) случаев. Всем пациентам с осложненной катарактой выполнена факоэмульсификация с имплантацией ИОЛ, что позволило улучшить остроту зрения к 3-му мес. наблюдения. В сроки от 6 мес. до 3-х лет наблюдения отмечалось медленное снижение зрения на фоне прогрессирования глаукомной оптической нейропатии, пролиферативной диабетической ангиоретинопатии и возрастной макулярной дегенерации.
В раннем послеоперационном периоде гифема развилась в 10,8% (16/148) случаев, преимущественно у больных, ранее оперированных по поводу глаукомы, и со вторичной неоваскулярной формой. Воспалительных реакций не было ни в одном случае.
В сроки наблюдения до 1 мес. после антиглаукомной операции с дренажом Глаутекс отслойка сосудистой оболочки отмечена в 18,2% (27/148) случаев. Выпускание супрахориоидальной жидкости в нижневнутреннем или нижненаружном квадрантах глазного яблока выполнено в 12,8% (19/148) случаев. В 5,4% (8/148) случаев отслойка сосудистой оболочки при сохранной передней камере самостоятельно прилегла на фоне медикаментозного лечения.
При биомикроскопии переднего отрезка глаза дренаж просматривался в виде прямоугольника. Полное его рассасывание происходило к 5–6 мес. после операции, однако в 2,7% (4/148) случаев при быстром рубцевании и облитерации зоны оперативного вмешательства отмечалась его визуализация в сроки более 9 мес. после хирургического вмешательства (рис. 1а). Возможно, скорость биодеградации Глаутекса зависит от циркуляции внутриглазной жидкости вокруг дренажа.
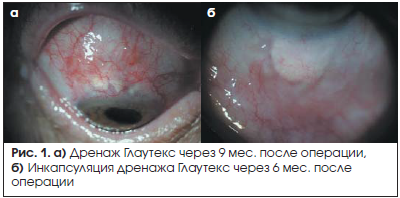
Инкапсуляция дренажа Глаутекс соединительной тканью отмечена в 3,4% (5/148) случаев. При биомикроскопии зона инкапсуляции дренажа определялась в виде приподнятого участка ткани без видимой фильтрации над ним (рис. 1б). При ревизии зоны инкапсуляции спустя 9 мес. после операции Глаутекс внутри капсулы определялся в виде бесформенной зернистой массы.
Вывод
Фистулизирующие операции с дренажом Глаутекс при рефрактерной глаукоме обеспечивают достаточно высокий гипотензивный эффект за счет предотвращения склеро-склерального и склеро-конъюнктивального избыточного послеоперационного рубцевания, обеспечивая нормализацию ВГД в 76,4% случаев при сроках наблюдения за пациентами до 3-х лет.Гипотензивный эффект фистулизирующих операций с дренажом Глаутекс зависит от исходного вида глаукомы: при ПОУГ – 85,5%, артифакии – 83,3%, неоваскулярной глаукоме – 39,1%, увеальной глаукоме – 66,4% в сроки наблюдения до 3-х лет.












