Однако факторы внешней среды также способны влиять на развитие возрастных изменений центральных отделов сетчатки. Так, курение увеличивает частоту возникновения поздних стадий ВМД в 2,5–4 раза, причем неблагоприятное воздействие этой пагубной привычки обладает выраженным дозозависимым эффектом [2]. При наличии генетических факторов риска CFH вероятность развития ВМД среди некурящих людей возрастает в 12,5 раза, тогда как при наличии тех же факторов риска курение увеличивает риск в 35 раз [1].
Таким образом, подтверждено, что модификация неблагоприятных факторов внешней среды (рациональное питание, отказ от курения, использование солнцезащитных очков), в т. ч. и адекватное консервативное лечение, способны уменьшить вероятность развития ВМД.
Однако следует признать, что консервативная терапия при «сухой» (неэкссудативной) форме ВМД – один из наиболее противоречивых разделов современной офтальмологии. С одной стороны, отечественными офтальмологами накоплен большой опыт успешного применения патогенетически ориентированной так называемой «дедистрофической» терапии с помощью различного рода препаратов (пептидные биорегуляторы, мельдония дигидрат, метилэтилпиридинол, этамзилат и др.) в виде инстилляций (глазных капель), инъекций субконъюнктивально, в парабульбарную клетчатку глазного яблока, внутрь в виде таблеток, внутримышечно и внутривенно. Подобная терапия получила широчайшее распространение во многих лечебных учреждениях страны. С другой стороны, подавляющее большинство исследований о пользе подобного рода терапии не соответствует требованиям доказательной медицины (отсутствие плацебо-контроля, малый объем выборки). Таким образом, клиническая эффективность «дедистрофической» терапии не подтверждена, поэтому в клиниках Америки и Европы такая терапия не применяется.
Под практикой доказательной медицины понимают использование данных, полученных из клинических исследований, в повседневной клинической работе врача. В современной медицинской науке принято выделять следующие категории убедительности доказательности исследований [3]:
I – основанные на тщательно спланированных, рандомизированных контролируемых исследованиях, метаанализах или систематизированных обозрениях (наиболее высокий уровень доказательности);
II – основанные на когортном исследовании или исследованиях по типу «случай – контроль»;
III – неконтролируемые исследования или соглашения экспертов.
Категории убедительности доказательств являются хорошим подспорьем практическому врачу в оценке терапевтических возможностей традиционных и новых методов лечения, поэтому дальнейшее рассмотрение материала будет основываться на исследованиях I и II уровня убедительности доказательств.
Минералы и антиоксиданты
В течение многих лет антиоксиданты назначались при ВМД исходя из теоретических представлений о том, что под воздействием фотохимически активного синего цвета в сетчатке накапливаются свободные радикалы и возникает оксидативный стресс, оказывающий разрушительное действие на структуры глазного дна. В соответствии с этим предполагалось, что назначение антиоксидантов (витамины С и Е, бета-каротин, минералы цинк, селен и марганец) может оказывать защитное действие на сетчатку. Позднее был опубликован ряд сообщений о том, что диета, богатая антиоксидантами, предупреждает развитие признаков ранней ВМД, однако роль пищевых антиоксидантов в первичной профилактике возрастных изменений сетчатки длительное время оставалась неясной.В начале 1990-х гг. плацебо-контролируемые исследования Eye Disease Case-Control Study (1993)1 и Baltimore Longitudinal Study (1994)2 подтвердили защитное действие высоких уровней витаминов А, С и Е, бета-каротина, цинка и селена в плазме крови на прогрессирование ВМД [4, 5]. В 1998 г. Beaver Dam Eye Study3 (1700 пациентов, срок наблюдения – 5 лет) продемонстрировало уменьшение риска возникновения крупных друз при употреблении высоких доз витамина Е, высокое содержание цинка в пище приводило к уменьшению частоты возникновения аномалий пигментного эпителия [6].
Исследование Age Related Eye Disease Study (AREDS, 1992–2001)4 – одно из наиболее крупных исследований возможностей профилактического лечения ВМД и катаракты, которое заслуживает более детального рассмотрения. В исследование были вовлечены 11 клинических центров США, 4757 пациентов в возрасте 55–88 лет (в среднем 69 лет), срок наблюдения составил 5 лет. Участники исследования были разделены на 4 группы: получавшие антиоксиданты, минералы, антиоксиданты + минералы и плацебо (табл. 1) [7].

Применительно к ВМД целью исследования AREDS5 явилось изучение влияния высоких доз антиоксидантов и минералов на остроту зрения и течение ВМД. Полученные результаты подтвердили защитное действие высоких доз антиоксидантов и минералов при 3 и 4 уровнях тяжести ВМД по классификации AREDS (рис. 1, 2). При отсутствии или начальной стадии ВМД профилактический эффект лечения был признан недостоверным.
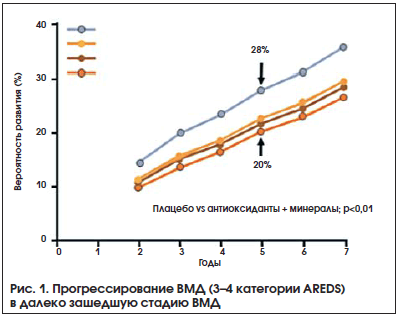
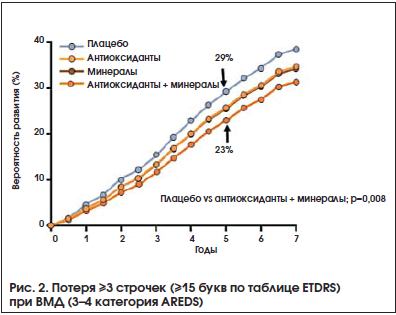
В течение 5-летнего срока наблюдения отмечено уменьшение риска развития далеко зашедшей ВМД: на 17% – в группе антиоксидантов, на 21% – в группе минералов и на 25% – в группе антиоксидантов и минералов по сравнению с плацебо-контролем. Применение комбинированной терапии на 19% сократило количество случаев утраты 3 строчек (15 букв) по таблице ETDRS. На основании результатов исследования формула AREDS (3-я группа сравнения) была рекомендована к широкому клиническому применению при промежуточной стадии ВМД или любой стадии заболевания на лучшем глазу при наличии далеко зашедшей ВМД на парном глазу.
Несколько позднее Rotterdam Study (2005)6, популяционное исследование 4170 человек с крупными друзами в макуле, также подтвердило эффективность формулы AREDS в предупреждении прогрессирования ВМД, уменьшение риска развития поздней стадии заболевания составило 35% [8].
В протоколе AREDS № 13 [9] проанализированы побочные эффекты лечения. Отмечено, что среди лиц с ВМД риск смертности выше, причем он возрастает при более тяжелых формах ВМД. Тем не менее зарегистрировано уменьшение смертности на 12% по сравнению с контролем среди лиц, получавших высокие дозы цинка в сочетании с антиоксидантами или без них. Хотя уровни смертности в группах контроля и лечения существенно не отличались, и пациенты показали хорошую переносимость исследуемых препаратов, был зарегистрирован ряд нежелательных явлений применения высоких доз антиоксидантов и минералов. Назначение бета-каротина увеличивало риск развития рака легких у курильщиков, в связи с чем формула AREDS была не рекомендована данной категории больных. Кроме того, существуют данные, что назначение высоких доз бета-каротина не только не уменьшает, но даже увеличивает риск развития неоваскулярной ВМД. Причем данная зависимость прослеживается не только у курильщиков, но и у никогда не куривших людей [10]. Также потребление высоких доз цинка (80 мг) приводило к росту случаев госпитализации у пациентов с болезнями мочеполовой системы [9].
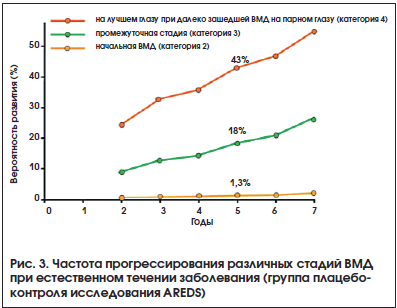
Вследствие низкой вероятности прогрессирования изменений сетчатки (рис. 3) и потенциального риска возникновения побочных эффектов исследователи AREDS не рекомендовали применение лекарственной терапии (15 мг бета-каротина и 80 мг цинка) при начальной ВМД или отсутствии возрастных изменений сетчатки [7].
Каротиноиды – природные органические пигменты, синтезируемые бактериями, грибами, водорослями, кораллами и высшими растениями. Эти вещества придают окраску большинству оранжевых или красных овощей и фруктов. В природе обнаружено более 600 каротиноидов, 34 из них выделены в сыворотке крови человека и оказывают ряд благоприятных эффектов на его организм. Только два из них – лютеин и зеаксантин определяются в сетчатке. Эти желтые пигменты макулы выполняют функции «солнцезащитных очков» сетчатки, предотвращают окисление триглицеридов и холестерина и являются протекторами перекисного окисления липидов клеточных мембран. Зеаксантин может образовываться в сетчатке из лютеина, но лютеин не синтезируется в организме человека, оба вещества поступают в него с пищей, в основном при употреблении овощей и фруктов.
К настоящему времени накоплено большое количество данных, свидетельствующих об увеличении частоты развития ВМД при снижении содержания лютеина и зеаксантина в плазме крови человека. Например, исследование Eye Disease Control Study (1993)7 подтвердило высокодостоверную (p=0,0001) обратную взаимосвязь между развитием неоваскулярной формы ВМД и уровнем лютеина и зеаксантина в плазме крови – при их низких концентрациях риск развития неоваскулярных поражений был на 70% выше [4]. Та же исследовательская группа показала, что риск возникновения ВМД достоверно снижается на 43% у лиц, в диету которых входит большое количество овощей и фруктов, содержащих каротиноиды (6 мг лютеина и зеаксантина в день) [11]. Крупное популяционное исследование POLA study (2006)8, выполненное на 899 испытуемых, выявило высокодостоверную взаимосвязь между высоким содержанием лютеина и зеаксантина в плазме крови и снижением частоты ВМД [12]. Аналогичные данные (женщины моложе 75 лет, промежуточная стадия ВМД) были получены в исследовании CAREDS (2006)9. Высокое содержание лютеина и зеаксантина в пище (3–6 мг/сут) по сравнению с группой низкого потребления каротиноидов (0,5–0,8 мг/сут) снижало риск развития ВМД на 43–57% [11, 13].
В работе P. Bernstein et al. (2002) по результатам рамановской спектроскопии зарегистрировано уменьшение средней концентрации лютеина и зеаксантина в макулярной области у лиц с проявлениями ВМД на 32% по сравнению с контролем (пожилые люди, потребляющие мало овощей и фруктов). Назначение пациентам с проявлениями ВМД и снижением концентрации макулярного пигмента пищевых добавок с лютеином (>4 мг/сут) позволило нормализовать содержание лютеина в макуле [14]. Возможность увеличения оптической плотности макулярного пигмента после приема высоких доз лютеина (6 мг) и зеаксантина (0,3 мг) подтверждена в 3-летнем рандомизированном плацебо-контролируемом исследовании с двойным слепым контролем CARMA (2006)10 (рис. 4) [15].

Аналогичные результаты представила исследовательская группа LUNA (2007)11 [16]. Помимо постепенного увеличения оптической плотности макулярных пигментов на фоне приема 12 мг лютеина и 1 мг зеаксантина сохранялась положительная динамика в ближайшие сроки после прекращения приема каротиноидов (рис. 5).
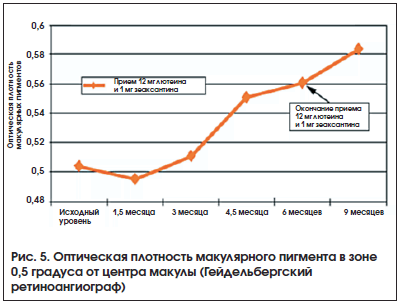
Длительный прием каротиноидов (10,8 мг лютеина, 0,3 мг зеаксантина) приводит к увеличению плотности макулярного пигмента: через 4 нед. приема – на 25% и на 50% через 14 нед. [17].
Наиболее крупное исследование терапевтического потенциала каротиноидов при «сухой» форме ВМД – недавно завершенное рандомизированное клиническое исследование AREDS-2 (2006–2012), основанное на 5-летнем наблюдении 4203 пациентов с «сухой» формой ВМД (билатеральные крупные друзы в макуле или крупные друзы на исследуемом глазу в сочетании с поздней ВМД на парном глазу). В отличие от других, ранее выполненных рандомизированных исследований, AREDS-2 подтвердило эффективность лютеина (10 мг) и зеаксантина (2 мг) в профилактике прогрессирования ВМД, а также допустимость замещения каротиноидами небезопасного для курильщиков бета-каротина в стандартной рецептуре AREDS. При этом риск развития поздних стадий ВМД снизился с 34% до 30% (p=0,02). Предполагается, что 25 мг цинка в сутки – максимально возможный уровень абсорбции минерала, поэтому AREDS-2 изучило возможность сокращения дозы цинка с 80 до 25 мг/сут. Это не привело к увеличению частоты возникновения поздних стадий ВМД и позволило уменьшить риски появления побочных эффектов лечения [18].
Полиненасыщенные жирные кислоты
Известно, что атеросклероз и сердечно-сосудистые заболевания в значительной степени связаны с избыточным потреблением жирной пищи, богатой насыщенными жирными кислотами животного происхождения. Наличие ВМД у пациента сопряжено с повышенным риском развития инфаркта миокарда. Коль скоро ВМД и сердечно-сосудистые заболевания имеют сходный патогенез развития, есть основания предполагать, что рациональное питание может предупреждать развитие возрастных изменений сетчатки.Полиненасыщенные омега-3 жирные кислоты (омега-3 ПЖК) – альфа-линоевая кислота (короткоцепочечные омега-3 жирные кислоты), а также докозагексаеновая и эйкозапентаеновая жирные кислоты (длинноцепочечные омега-3 ПЖК). Эти питательные вещества обнаруживаются в наружных сегментах палочек и колбочек, обладают противовоспалительными свойствами, препятствуют апоптозу клеток и патологическому ангиогенезу, участвуют в конформационных изменениях родопсина, уменьшают накопление липофусцина в пигментном эпителии сетчатки и липидных депозитов в мембране Бруха. Ряд эпидемиологических исследований подтвердил, что высокое потребление жиров животного происхождения сопряжено с риском развития далеко зашедших стадий ВМД. В свою очередь потребление различных сортов рыб 1–2 раза в неделю приводит к сокращению риска развития неоваскулярной ВМД и развития географической атрофии [19, 20].
Рандомизированное клиническое исследование AREDS-2 (2006–2012) продемонстрировало отсутствие профилактического эффекта при ВМД пищевых добавок, содержащих омега-3 жирные кислоты [18]. Возможным объяснением данного результата может быть как действительное отсутствие терапевтического эффекта, так и неучтенное исследователями влияние прочих факторов (особенности диеты, соотношение насыщенных и ненасыщенных жирных кислот в рационе, биологическая доступность пищевых добавок и т. д.). Тем не менее считается полезным пациентам старшей возрастной группы дополнить недельный пищевой рацион 1–2-кратным приемом рыбы.
Перспективы лечения «сухой» формы ВМД
Перспективы консервативного лечения «сухой» формы ВМД не исчерпываются применением минералов и антиоксидантов, клиническая эффективность которого подтверждена многоцентровыми исследованиями. Наблюдательные эпидемиологические исследования, сообщения отдельных авторов и групп исследователей свидетельствуют о большом потенциале самых разных биологических добавок в профилактике возрастных изменений сетчатки.Эпидемиологические данные подтверждают дефицит витамина D в плазме крови среди пациентов с неоваскулярной ВМД. Результаты лабораторных исследований подтверждают возможность снижения уровней провоспалительного цитокина TNF-альфа, восстановление нормальной структуры фоторецепторов глаз мышей на фоне приема повышенных доз витамина D. В нормальном функционировании сетчатки велика роль ряда других витаминов (А, B6 и В12), поиск оптимальных концентраций и терапевтические возможности которых продолжают изучаться. Выраженные антиоксидантные свойства присущи антоцианозидам и биофлавоноидам, которые уменьшают ломкость капилляров и улучшают состояние соединительной ткани. Большие надежды связываются с применением при ВМД системной энзимотерапии и пептидных биорегуляторов, однако налицо дефицит плацебо-контролируемых клинических исследований терапевтического потенциала подобных препаратов. Также противоречивы сообщения о профилактическом действии аспирина в профилактике ВМД.
На конгрессе EURETINA (2013) были представлены положительные результаты многоцентрового плацебо-контролируемого исследования II фазы MAHALO Study (2013)12 по ежемесячному применению интравитреальных инъекций лампализумаба (моноклональное антитело – ингибитор фактора Д комплемента) производства фирмы Genentech (США) при «сухой» форме ВМД. Препарат зарекомендовал себя безопасным. Лечебный эффект лампализумаба определялся начиная с 6 мес., к 18 мес. уменьшение частоты прогрессирования географической атрофии составило 20,4% (p<0,005). С 2014 г. проводится III фаза исследования препарата [21].
Заключение
В настоящее время аптечная сеть России насыщена витаминно-минеральными комплексами различных фармацевтических фирм. Внимания клинического врача заслуживают комплексы, соответствующие компонентам формулы многоцентрового исследования AREDS-2. Наиболее близким этому составу является Ретинорм, который в суточной норме потребления содержит 500 мг витамина С, 150 мг витамина Е, 10 мг лютеина, 2 мг зеаксантина, 25 мг цинка и 2 мг меди. С учетом Единых санитарно-эпидемиологических и гигиенических требований содержание витамина Е в Ретинорме было уменьшено с 268 до 150 мг. В то же время для компенсации уменьшения дозировки витамина Е формула AREDS-2 в Ретинорме была усилена селеном. Селен обладает выраженными антиоксидантными свойствами, предохраняет от повреждений нуклеиновые кислоты и обладает синергизмом с витаминами Е и С, предупреждая процессы клеточного окисления. Входящие в состав комплекса лютеин, зеаксантин, витамины С, Е и микроэлементы способствуют нормализации обменных процессов в тканях глаза, снижают риск развития возрастных изменений в сетчатке.1 Eye Disease Case-Control Study – глазные заболевания, исследование по типу «случай – контроль» (США).
2 Baltimore Longitudinal Study – продольное исследование (Baltimore, Maryland, США).
3 Beaver Dam Eye Study – исследование глаза (Beaver Dam, Wisconsin, США).
4 Age Related Eye Disease Study (AREDS) – исследование возрастного заболевания глаза.
5 Категории тяжести ВМД по AREDS: 1-я категория – отсутствие ВМД (единичные мелкие друзы диаметром < 63 мкм или отсутствие признаков ВМД); 2-я категория – начальная ВМД (множественные мелкие друзы, небольшое число друз среднего размера (∅ 63–124 мкм) или изменения ПЭ); 3-я категория – промежуточная стадия ВМД (множество друз среднего размера, по крайней мере, одна большая друза (∅ ≥125 мкм) или географическая атрофия, не затрагивающая центральной ямки); 4-я категория – отсутствие далеко зашедшей ВМД на исследуемом глазу (географическая атрофия в центральной ямке или хориоидальная неоваскуляризация) и наличие далеко зашедшей ВМД на парном глазу.
6 Rotterdam Study – исследование Rotterdam (Нидерланды).
7 Eye Disease Control Study – контрольное исследование заболеваний глаза (США).
8 Pathologies Oculaires Liées á l'Age (POLA) – исследование патологии глаз, связанной с возрастом (Франция).
9 Carotenoids in Age-Related Eye Disease Study (CAREDS) – каротиноиды в исследовании глазного заболевания, связанного с возрастом (США).
10 Carotenoids and co-antioxidants in Age-Related Maculopathy (CARMA) – каротиноиды и коантиоксиданты при связанной с возрастом макулопатии (Ирландия).
11 LUtein Nutrition effects measured by Auto-fluorescence (LUNA) – эффект добавления в питание лютеина, измеряемый аутофлюоресценцией (Германия).
12 MAHALO Study – исследование II фазы эффективности лампализумаба при «сухой» форме ВМД.












