Введение
Лазерная коагуляция аваскулярных зон сетчатки в настоящее время продолжает оставаться безопасным и высокоэффективным методом лечения активных стадий ретинопатии недоношенных (РН) [1–12]. Однако, несмотря на доступность и широкую распространенность, технология проведения лазерного лечения при РН постоянно оптимизируется. До сих продолжаются споры между хирургами в отношении оптимальных энергетических параметров и режимов лазерной коагуляции сетчатки (ЛКС).
Учитывая необходимость одновременного нанесения большого количества лазерных аппликатов на аваскулярную сетчатку, с 2009 г. в лечении активных стадий РН стали активно использовать сканирующую паттерновую коагуляцию сетчатки. Методика, получившая наименование по названию лазерной установки Pascal (Optimedica, США), основана на генерации ультракоротких лазерных импульсов в определенной последовательности в соответствии с заданными «шаблонами», или паттернами. Данная технология зарекомендовала себя как оптимально дозированная и безопасная, что подтверждается отдаленными результатами лечения. Было доказано, что своевременная паттерновая ЛКС при 2-й стадии классического течения заболевания приводит к регрессу РН в 100% наблюдений, а при 3-й стадии заболевания — в 96,4% [2, 11].
При проведении паттерновой ЛКС используются регулярные квадратные матричные решетки различных размеров — от 2×2 (суммарно 4 спота в паттерне) до 5×5 (суммарно 25 спотов в паттерне). Выбор размера паттерна и энергетических параметров зависит от тяжести течения, формы и стадии заболевания, а также от степени сосудистой активности и локализации патологического процесса (с учетом площади аваскулярной сетчатки) [1].
При большой площади аваскулярной сетчатки паттерновую ЛКС, как правило, начинают с применения квадратных паттернов большого размера (суммарно 25 или 16 спотов), постепенно уменьшая размер паттерна при работе на периферии (суммарно 9 или 4 спота), и переходят в режим одиночного импульса в конце операции при работе с оставшимися участками аваскулярной сетчатки, на которых лазерное воздействие еще не было проведено. Как показывает наш опыт, особенностью паттерновой ЛКС является сложность позиционирования паттернов квадратной формы на сферичную поверхность сетчатки и вблизи вала экстраретинальной пролиферации (ЭРП). Это объясняет необходимость использования во время операции большого количества одиночных коагулятов, что увеличивает время лечения и, соответственно, время нахождения недоношенного младенца в наркозе. А отсутствие оптимальной стыковки соседних квадратных паттернов друг с другом при повороте головы или глаза ребенка и/или изменении положения линзы приводит к неравномерной коагуляции.
Появление современного оборудования открыло для офтальмохирургов новые перспективы. Среди возможностей новых приборов особого внимания заслуживает функция свободной ротации паттернов и выбора их разнообразной геометрической формы [13, 14]. Анализ доступной литературы показал, что выбор конфигурации и размера паттерна зависит только от индивидуальных предпочтений хирурга. Также нет статей, в которых описывается работа с паттерном гексагональной формы (сотовидным), который относится к регулярным треугольным паттернам и состоит из 7 аппликатов. При работе с сотовидным паттерном, в отличие от квадратного, происходит оптимальный докинг соседних паттернов между собой. В результате за счет равноудаленного, доказанного математически, расположения спотов внутри гексагонального паттерна хирург получает равномерное распределение лазерных коагулятов на сферичной поверхности сетчатки глаза недоношенного ребенка [16].
Цель исследования: оценить эффективность транспупиллярной гексагональной паттерновой ЛКС в лечении активных стадий РН.
Материал и методы
За период с 2017 по 2020 г. транспупиллярная ЛКС была проведена 161 младенцу со 2-й и 3-й активными стадиями РН, с неблагоприятным типом течения (по классификации А.В. Терещенко и соавт., 2008) [15]. Постконцептуальный возраст (ПКВ) на момент лазеркоагуляции составил 34–37 нед. при 2-й стадии заболевания и 36–38 нед. при 3-й стадии. Диагноз с определением стадии и типа течения активной РН ставился на основе данных комплексного офтальмологического обследования. Комплексное диагностическое обследование и последующее лазерное лечение по показаниям проводились после получения добровольного информированного согласия родителей или законных представителей пациентов.
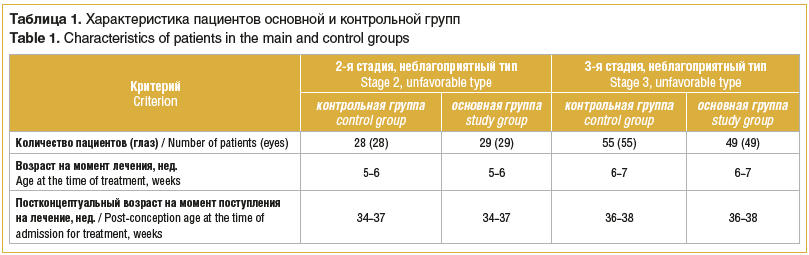
Всем детям проводили бинокулярную офтальмоскопию с использованием бинокулярного налобного офтальмоскопа (HEINE Omega 500, Германия), цифровую ретиноскопию на широкопольной цифровой ретинальной педиатрической видеосистеме RetCam-3 (Massie Research Laboratories Inc, США) и оптическую когерентную томографию (ОКТ) на приборе RTVue XR Avanti Angiovue (Optovue, США). У 57 детей (57 глаз) был выявлен неблагоприятный тип течения 2-й стадии РН, а у 104 младенцев (104 глаза) — неблагоприятный тип течения 3-й стадии РН (табл. 1).
Лазерное лечение всем младенцам проводилось под аппаратно-масочным наркозом (кислородно-воздушной смесью с севофлураном) на системе Integrе Pro Scan 561 нм (Ellex, Австралия) с использованием контактной роговичной линзы Quad Pediatric Fundus Lens (Volk, США). За 2–3 мин до начала лазерного лечения выполнялась эпибульбарная анестезия (раствор проксиметакаина 0,5% однократно). Случайным образом все пациенты были распределены в две группы: основную и контрольную. В основной группе (n=78) проводилась сотовидная ЛКС (использовался паттерн гексагональной формы из 7 равноудаленных друг от друга аппликатов), в контрольной группе (n=83) ЛКС проводилась с выбором матричных паттернов квадратной формы 3×3 (всего 9 аппликатов в паттерне). На оставшиеся необработанными участки аваскулярной сетчатки лазерные аппликаты наносили в режиме одиночного импульса. Весь объем лазерного лечения у всех младенцев выполнялся за один сеанс. Единственным отличием в параметрах коагуляции основной и контрольной групп являлся интервал между лазерными аппликатами: в основной группе межспотовое расстояние было на 0,25 диаметра коагулята больше, чем в контрольной.
Эффективность лечения оценивали через 3–4 нед. после ЛКС на основании динамики клинических признаков (уплощение, уменьшение и исчезновение вала ЭРП и демаркационного вала) и морфометрических показателей (снижение толщины сетчатки в макулярной области), что и характеризовало устойчивый регресс заболевания.
Результаты исследования
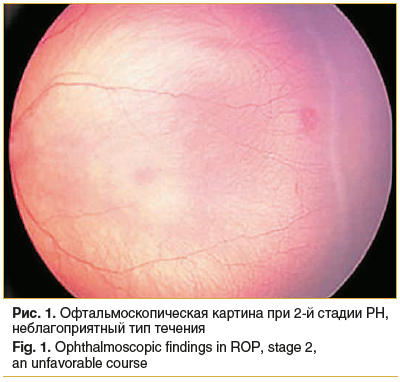
При проведении непрямой бинокулярной офтальмоскопии до лазерного лечения у 47 (83%) пациентов со 2-й стадией РН и у 45 (43%) пациентов с 3-й стадией заболевания макулярные рефлексы были сохранены; у всех остальных младенцев макулярные рефлексы отсутствовали. У младенцев со 2-й стадией с неблагоприятным типом течения, по данным цифровой ретиноскопии, выявлялся демаркационный вал, распространяющийся на 6–12 часовых меридианов и возвышающийся над поверхностью сетчатки; выявлялись извитые сосудистые коллатерали и артериовенозные шунты, определялась их штопорообразная извитость (рис. 1).
У младенцев с 3-й стадией РН непрерывный вал фиброваскулярной новообразованной ткани занимал по протяженности не менее 6 последовательных часовых меридианов и определялся на границе между первой и второй зоной или во второй зоне глазного дна (рис. 2). Было зафиксировано резкое расширение и штопорообразная извитость сосудистых шунтов и коллатералей, определялись интра- и преретинальные кровоизлияния перед валом ЭРП.

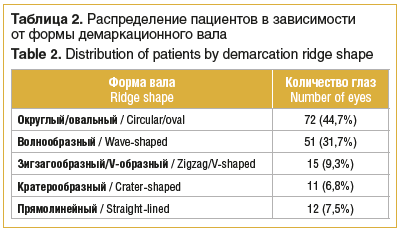
В данной работе границе васкуляризированной и аваскулярной сетчатки, а также непосредственно форме демаркационного вала было уделено особое внимание. В нашей многолетней клинической практике мы встретились с многообразием и причудливостью форм демаркационного вала. На основании собственного опыта мы условно выделили следующие его формы: округлый/овальный, волнообразный, зигзагообразный/V-образный, кратерообразный, прямолинейный.
В настоящем исследовании чаще всего встречались округлая/овальная и волнообразная формы вала (табл. 2), поэтому гексагональная форма паттерна была предпочтительна при работе на границе аваскулярной и васкуляризированной сетчатки. При работе с гексагональным паттерном удается достичь оптимального повторения конфигурации демаркационного вала и дозированно провести коагуляцию вдоль него. За счет равноудаленного расположения аппликатов внутри гексагонального паттерна и оптимального сопоставления соседних паттернов друг с другом даже при повороте линзы или глаза пациента удается сохранить регулярность матричной структуры и получить равномерную коагуляцию всей аваскулярной сетчатки.
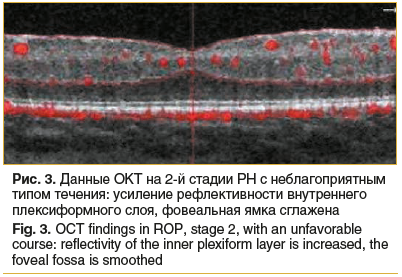
При проведении ОКТ в пределах перифовеальной области у детей с неблагоприятным типом течения 2-й стадии РН определялись участки дистрофии ретинального пигментного эпителия и слоя наружных сегментов фоторецепторов. Было зафиксировано усиление рефлективности внутреннего плексиформного слоя по всей зоне сканирования (рис. 3). У 10 (17%) младенцев определялись кистозные изменения сетчатки в пределах парафовеальной области на уровне внутреннего ядерного слоя; фовеальная ямка у них была сглажена или отсутствовала, отмечалось увеличение толщины сетчатки в области фовеа до 266±11,82 мкм. Толщина хориоидеи в макулярной области составляла 279±16,98 мкм.
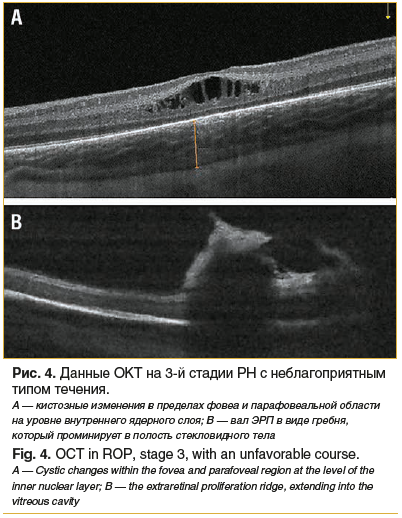
У пациентов с 3-й стадией активной РН с неблагоприятным типом течения, по данным ОКТ, толщина сетчатки в фовеа составляла 254±11,96 мкм. У 45 (43%) младенцев область фовеа была сформирована, однако имела сглаженный профиль. Выявлялись зоны локального уплотнения внутренней пограничной мембраны. У 59 (57%) детей на уровне внутреннего ядерного слоя определялись кистозные полости различной формы и размера (рис. 4А). Толщина хориоидеи в макулярной области составляла 281±11,19 мкм. Вал с участками плоскостной эпиретинальной неоваскуляризации перед ним и на его вершине визуализировался во 2-й зоне глазного дна (рис. 4В). Участки локальной эпиретинальной неоваскуляризации перед валом определялись в виде гиперрефлективных зон грибовидной формы с проминенцией в стекловидное тело.
При неблагоприятном типе течения 2-й стадии РН выполнялась коагуляция 2-й степени интенсивности (по классификации L’Esperance) всей аваскулярной зоны сетчатки пятном диаметром 200 мкм. При проведении ЛКС использовалась экспозиция 20 мс. Параметры коагуляции отличались только расстоянием между аппликатами в паттерне — в основной группе плотность коагуляции была на 0,25 диаметра коагулята меньше, чем в контрольной. Так, при квадратной ЛКС межспотовое расстояние составило 0,5 диаметра коагулята, а при гексагональной — 0,75 диаметра коагулята. Мощность лазерного излучения в обеих группах варьировала от 90 до 180 МВт. Общее время лечения в основной группе составило 9,6±0,9 мин, в контрольной — 11,2±0,7 мин (в зависимости от площади аваскулярной сетчатки и локализации патологического процесса). Общее количество коагулятов в основной группе было в 1,3 раза меньше, чем в контрольной группе, и составило 876±74,6 и 1149±88 соответственно. Среднее количество одиночных импульсов у детей со 2-й стадией РН при использовании гексагонального паттерна составило 30±1,4, при использовании квадратного паттерна — 112±6,6. Суммарная энергетическая нагрузка в основной группе была равна 1296±79 Дж/см2, в контрольной — 1700±89 Дж/см2, т. е. в основной группе в 1,3 раза меньше, чем в контрольной.
При неблагоприятном типе течения 3-й стадии РН выполнялась коагуляция 3-й степени интенсивности (по классификации L’Esperance) всей аваскулярной зоны сетчатки лазерными спотами диаметром 300 мкм с экспозицией 30 мс. При матричной ЛКС межспотовое расстояние было равно 0,25 диаметра коагулята, при гексагональной ЛКС — 0,5 диаметра коагулята. Мощность лазерного излучения в обеих группах варьировала от 100 до 200 МВт. Общее время лечения в основной и контрольной группах составило 11,3±0,8 и 14±0,6 мин соответственно. Общее количество коагулятов в основной группе было в 1,3 раза меньше, чем в контрольной группе (1047±59,2 и 1406±112 соответственно). У детей с 3-й стадией РН при использовании гексагонального паттерна среднее количество одиночных импульсов составило 41±1,8, при использовании квадратного паттерна — 165±4,9, что подтверждает идеально равномерное позиционирование гексагональных паттернов на сферичной поверхности сетчатки. Суммарная энергетическая нагрузка в основной группе была равна 1717±97 Дж/см2, в контрольной — 2305±101 Дж/см2, т. е. в основной группе в 1,3 раза меньше, чем в контрольной.
На обеих стадиях РН и во всех группах у младенцев в раннем послеоперационном периоде (до 3 сут) наблюдалась реактивная сосудистая реакция, которая выражалась во временном увеличении кровенаполнения центральных и периферических ретинальных сосудов и артериовенозных шунтов [17]. На границе васкуляризированной и аваскулярной сетчатки в обеих группах отмечалось усиление кровенаполнения и проминенции демаркационного вала в стекловидное тело. В отдельных случаях у младенцев с 3-й стадией заболевания определялись умеренно выраженный отек сетчатки в области сосудистых аркад и интраретинальные петехиальные кровоизлияния. После проведенного сеанса лечения и в основной, и в контрольной группе визуализировались множественные светло-серые лазерные коагуляты с умеренно выраженным перифокальным отеком, которые покрывали всю аваскулярную сетчатку.
В раннем послеоперационном периоде при проведении ОКТ отмечалось реактивное увеличение толщины сетчатки в области фовеа до 282±10,84 мкм при 2-й стадии заболевания (рис. 5) и до 273±4,88 мкм при 3-й стадии заболевания. Следует особо отметить, что показатели увеличения толщины сетчатки в области фовеа зависели от степени выраженности дооперационного кистозного отека. Толщина сетчатки до и после лечения не менялась, признаков отека сетчатки не отмечалось у 47 (83%) младенцев со 2-й стадией заболевания и у 45 (43%) младенцев с 3-й стадией заболевания. Толщина хориоидеи в заднем полюсе глаза в 1-е сутки после лечения при 2-й и 3-й стадиях РН по сравнению с исходными значениями увеличивалась на 44±11,63 мкм в контрольной группе и на 38±12,62 мкм в основной группе. На 5-е сутки после лазерного лечения в основной группе было зафиксировано уменьшение толщины хориоидеи в заднем полюсе глаза и возвращение ее к исходным значениям, в то время как в контрольной группе отек хориоидеи сохранялся. К 7-м суткам после проведенной ЛКС показатели толщины хориоидеи у младенцев контрольной группы возвращались к нормальным значениям.

У всех младенцев через 2 нед. было зафиксировано уплощение демаркационного вала. У детей с 3-й стадией заболевания отмечалось уменьшение объема и высоты вала ЭРП и постепенное уменьшение количества интраретинальных геморрагий. Во всех группах в зоне лазерной коагуляции визуализировалась начальная пигментация. Уже через 3 нед. у 100 (96%) младенцев с 3-й стадией РН вала ЭРП зафиксировано не было. В отдельных сегментах определялись лишь очаги пролиферации.
Через 3 нед. при проведении ОКТ у всех детей со 2-й стадией заболевания и у 101 (97%) младенца с 3-й стадией заболевания отмечались резорбция отека и уменьшение толщины сетчатки в области фовеа. Только у 3 младенцев с 3-й стадией заболевания оставались единичные интраретинальные кисты.
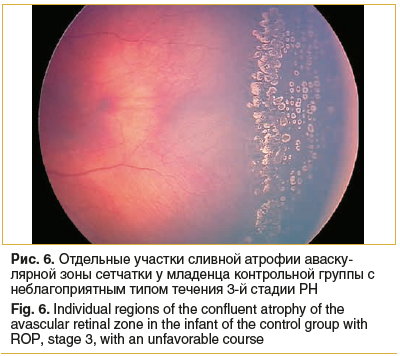
Через 1 мес. после проведенного лазерного лечения в исследуемых группах у детей с 3-й стадией РН вал ЭРП не определялся. Отмечалось формирование зоны хориоретинальной атрофии с неодинаковой пигментацией в местах нанесения лазерных аппликатов. Соответственно расположению в паттерновой матричной решетке офтальмоскопировались участки посткоагуляционной атрофии с сохранением межретинальных «мостиков» между коагулятами. У 19 (16%) младенцев контрольной группы отмечали эффект гиперкоагуляции возле вала ЭРП и формирование в аваскулярной зоне сетчатки отдельных участков «сливной» атрофии (рис. 6), которых не было зафиксировано в основной группе. Между лазерными коагулятами по направлению к зубчатой линии определялось прорастание ретинальных сосудов в аваскулярную зону сетчатки.
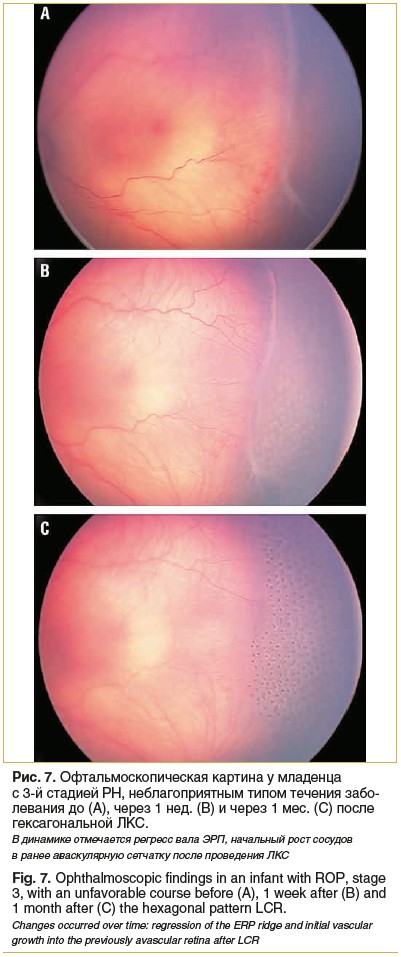
В ходе дальнейшего наблюдения — через 3 и 6 мес. после лазерного лечения у пациентов обеих групп был отмечен продолженный рост ретинальных сосудов в зону коагуляции (ранее аваскулярную зону) (рис. 7).
На 2-й стадии заболевания и в основной, и в контрольной группе (57 глаз) паттерновая ЛКС обеспечила регресс заболевания в 100% случаев. На 3-й стадии заболевания в обеих группах регресс был достигнут в 96% случаев (53 глаза в основной группе и 47 глаз в контрольной группе).
Обсуждение
АнтиVEGF-терапия рассматривается как перспективный метод лечения тяжелых форм РН, для которого, однако, остаются нерешенными вопросы об оптимальной дозе и риске развития общесоматических осложнений [18, 19].
В настоящее время патогенетически обоснованным, доказанным и безопасным методом лечения РН в активном периоде заболевания по-прежнему остается транспупиллярная ЛКС. Методика постоянно совершенствуется, и с 2009 г. в клинической практике успешно используется сканирующая паттерновая ЛКС [2, 11].
В данной работе была применена и оценена технология сотовидной паттерновой лазерной коагуляции в лечении активных стадий РН [16]. Анализ полученных результатов показал, что эффективность обеих описанных паттерновых методик сопоставима: 100% при 2-й стадии заболевания и 96% при 3-й стадии.
Коагуляция сетчатки с использованием квадратных лазерных паттернов идеальна для больших областей с относительно ровными границами при отсутствии искажений. Однако при работе на сферической поверхности аваскулярной сетчатки невозможно точно сопоставить квадратные паттерны по отношению друг к другу, что ведет к нарушению регулярности матричной структуры (рис. 8). На оставшиеся необработанными участки аваскулярной сетчатки приходится наносить лазерные коагуляты в режиме одиночного импульса, что увеличивает общее время лечения и, соответственно, время нахождения в наркозе недоношенного младенца.

Гексагональная, шестигранная, форма паттерна удобна при работе вблизи вала ЭРП, который у каждого недоношенного младенца имеет индивидуально неповторимую, а порой и причудливую форму. Методика оптимальна для работы на сферичной поверхности сетчатки глаза недоношенного ребенка и обеспечивает точный и интуитивно понятный докинг каждого последующего паттерна к предыдущему. При работе с гексагональным паттерном нами было использовано в 4 раза меньше коагулятов в режиме одиночного импульса по сравнению с коагуляцией квадратными паттернами, что позволяет уменьшить общее время лечения и является одним из основных преимуществ метода. Использование паттерна гексагональной формы позволяет унифицировать методику, получая дозированную и равномерную коагуляцию всей аваскулярной сетчатки, независимо от квалификации и опыта хирурга.
Заключение
В лечении активных стадий РН гексагональная сканирующая паттерновая транспупиллярная ЛКС показала себя как высокоэффективная и безопасная методика. Она является тканесберегающей, дозированной, позволяет достичь прогнозируемого клинического ответа с минимальной суммарной энергетической нагрузкой на сетчатку глаза недоношенного младенца.
Сведения об авторах:
Терещенко Александр Владимирович — д.м.н., директор Калужского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 248007, Россия, г. Калуга, ул. Святослава Федорова, д. 5; профессор кафедры хирургии медицинского института КГУ им. К.Э. Циолковского; 248023, Россия, г. Калуга, ул. Степана Разина, д. 26; ORCID iD 0000-0002-0840-2675.
Трифаненкова Ирина Георгиевна — д.м.н., заместитель директора по научной работе Калужского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 248007, Россия, г. Калуга, ул. Святослава Федорова, д. 5; профессор кафедры хирургии медицинского института КГУ им. К.Э. Циолковского; 248023, Россия, г. Калуга, ул. Степана Разина, д. 26; ORCID iD 0000-0001-9202-5181.
Сидорова Юлия Александровна — к.м.н., заведующая лазерным отделением донной патологии Калужского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 248007, Россия, г. Калуга, ул. Святослава Федорова, д. 5; ORCID iD 0000-0001-8396-4013.
Фирсова Виктория Владимировна — врач-офтальмолог лазерного отделения донной патологии Калужского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 248007, Россия, г. Калуга, ул. Святослава Федорова, д. 5; ORCID iD 0000-0002-8333-2785.
Контактная информация: Трифаненкова Ирина Георгиевна, e-mail: nauka@mntk.kaluga.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 26.08.2022.
Поступила после рецензирования 20.09.2022.
Принята в печать 13.10.2022.
About the authors:
Aleksandr V. Tereshchenko — Dr. Sc. (Med.), Director of Kaluga Branch of the S.N. Fedorov Eye Microsurgery Federal State Institution; 5, Svyatoslav Fedorov str., Kaluga, 248007, Russian Federation; Professor of the Department of Surgery of the Medical Institute, K.E. Tsiolkovsky Kaluga State University; 26, Stepan Razin str., Kaluga, 248023, Russian Federation; ORCID iD 0000-0002-0840-2675.
Irina G. Trifanenkova — Dr. Sc. (Med.), Deputy Director for Research of Kaluga Branch of the S.N. Fedorov Eye Microsurgery Federal State Institution; 5, Svyatoslav Fedorov str., Kaluga, 248007, Russian Federation; Professor of the Department of Surgery of the Medical Institute, K.E. Tsiolkovsky Kaluga State University; 26, Stepan Razin str., Kaluga, 248023, Russian Federation; ORCID iD 0000-0001-9202-5181.
Yuliya A. Sidorova — C. Sc. (Med.), Head of the Department of Laser Treatment of Eye Fundus Disorders, Kaluga Branch of the S.N. Fedorov Eye Microsurgery Federal State Institution; 5, Svyatoslav Fedorov str., Kaluga, 248007, Russian Federation; ORCID iD 0000-0001-8396-4013.
Victoria V. Firsova — ophthalmologist of the Department of Laser Treatment of Eye Fundus Disorders, Kaluga Branch of the S.N. Fedorov Eye Microsurgery Federal State Institution; 5, Svyatoslav Fedorov str., Kaluga, 248007, Russian Federation; ORCID iD 0000-0002-8333-2785.
Contact information: Irina G. Trifanenkova, e-mail: nauka@mntk.kaluga.ru.
Financial Disclosure: no autors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 26.08.2022.
Revised 20.09.2022.
Accepted 13.10.2022.












