Введение
Роговая оболочка – это высокоорганизованная структура, выполняющая ряд важнейших функций для поддержания полноценной работы глаза как органа, и, вместе с тем, главная преломляющая среда в оптической системе глаза. Традиционно в роговице принято выделять пять слоев: передний эпителий роговицы, переднюю пограничную пластинку (боуменову мембрану), собственное вещество роговицы (строму), заднюю пограничную пластинку (десцеметову мембрану) и задний эпителий роговицы (эндотелий). 90% толщины всей роговой оболочки составляет ее собственное вещество, состоящее из коллагеновых волокон, организованных в стромальные пластины, кератоцитов и внеклеточного матрикса. Благодаря строгой упорядоченности расположения стромальных пластин, их одинаковому диаметру и расстоянию относительно друг друга, а также равномерному распределению внеклеточного матрикса между ними роговица имеет высокую степень прозрачности. Протеогликаны и гликопротеины, представляющие собой основу внеклеточного матрикса стромы роговицы, обеспечивают равномерное распределение ее водной составляющей.Водный баланс роговицы поддерживается за счет барьерной функции переднего и заднего эпителия. Передний эпителий, являющийся плотным барьером благодаря межклеточным контактам — десмосомам, имеет низкую ионную проводимость и ограничивает поступление воды из прекорнеальной слезной пленки в переднюю строму. Задний эпителий представляет собой неполный барьер, т. е. избирательный, за счет различных типов межклеточных соединений (плотных и щелевидных). Баланс между объемом поступающей в роговицу влаги и ее возвратом обратно в переднюю камеру по градиенту осмотического давления обеспечивается функцией активного метаболического насоса (эндотелиальных помп) [1].
При глаукоме могут иметь место несколько факторов, вызывающих нарушение водного баланса роговицы. Гидростатическое давление водянистой влаги может усилить ток жидкости через неполный эндотелиальный барьер в роговицу, а также создать препятствие для осуществления нормального тока жидкости из роговицы в переднюю камеру через слой эндотелия. В результате избыточного давления на клетки эндотелиального слоя могут возникнуть структурные и функциональные нарушения эндотелиоцитов с дисфункцией метаболических помп, что приводит к набуханию стромы роговицы и возникновению ее отека [2, 3]. Является доказанным и факт снижения плотности, изменения формы клеток эндотелия на фоне глаукомного процесса [4, 5].
Как биологическая ткань роговица относится к слабо рассеивающим (прозрачным) тканям и описывается моделью малократного рассеивания упорядоченной среды с плотной упаковкой рассеивателей, содержащих поглощающие центры [6]. Оптические свойства роговицы определяются строгой ориентацией и упорядоченностью ее структур, расстояние
между которыми не превышает 200 нм (менее половины длины волны), что позволяет световым лучам проходить сквозь все слои роговой оболочки, не отклоняясь, и практически исключает их рассеивание. Степень светорассеяния роговицы в норме очень мала и составляет всего 1%.
Любые изменения морфологии роговичной ткани, в т. ч. нарушение водного баланса, снижают ее анизотропные оптические свойства и приводят к повышению эффекта светорассеяния и снижению прозрачности [6, 7].
При отеке роговицы расстояние между коллагеновыми волокнами увеличивается вследствие накопления воды в строме. Результатом хронического отека являются потеря протеогликанов и агрегация коллагеновых фибрилл. Данные нарушения приводят к появлению оптических неоднородностей, размер которых превосходит половину длины волны света, к дифракции света, увеличению светорассеяния [7].
Компенсация ВГД при глаукоме в большинстве случаев предполагает длительное использование медикаментозных средств, содержащих консерванты. Бензалконий хлорид (БХ), наиболее часто используемый из них, оказывает разрушающее действие на слезную пленку. Токсическое воздействие консерванта не ограничивается эпителиальным слоем глазной поверхности. БХ накапливается в строме роговицы, что может приводить к структурным изменениям при его длительном использовании [8, 9]. С целью защиты глазной поверхности от действия консерванта и снижения его токсического воздействия возможно использование средств слезозаместительной терапии [10–12].
Оценить состояние роговицы и, в определенной степени, возникающие морфологические нарушения в настоящее время возможно с помощью конфокальной микроскопии. Данный метод позволяет также определить уровень светорассеяния роговицы, который зависит от изменений оптической плотности и однородности ее различных слоев [13, 14]. Определение уровня интенсивности светорассеяния может служить дополнительным критерием для регистрации степени морфологических нарушений роговицы и оценки лечебного эффекта от назначаемых медикаментозных средств.
Цель работы: оценить морфологические изменения и уровень светорассеяния роговицы при глаукоме: а) при некомпенсированном ВГД без использования гипотензивных препаратов, б) при компенсированном ВГД на фоне длительного применения антиглаукомных препаратов, в) при использовании средств слезозаместительной терапии в комбинации с гипотензивными антиглаукомными препаратами.
Материал и методы
Всего было обследовано 66 пациентов (132 глаза), из них 46 (92 глаза) больных с глаукомой, возраст – от 40 до 80 лет. Работа была проведена в 2 этапа.Первый этап работы заключался в обследовании 3 групп пациентов.
1-я группа пациентов была обследована для определения уровня светорассеяния в норме. Данная группа состояла из 20 пациентов (40 глаз) в возрасте от 40 до 70 лет, без признаков глаукомы и каких-либо заболеваний роговицы в анамнезе. 2-я группа включала 22 первичных больных (44 глаза) с некомпенсированным ВГД, у которых диагноз был установлен впервые, и пациенты не использовали антиглаукомные препараты. 3-ю группу обследуемых составили 24 пациента (48 глаз) с различным стажем (от 2 мес. до 17 лет) использования антиглаукомных препаратов, содержащих в качестве консерванта БХ. Обследование в данной группе проводили на фоне компенсированного ВГД.
На втором этапе были обследованы 24 пациента (48 глаз), которым в дополнение к медикаментозному режиму был назначен слезозаменитель Стиллавит (натрия гиалуронат 0,16%, хондроитина сульфат натрия 0,05%, D-пантенол 1%, консервант – тетраборат натрия 0,05%). Инстилляции данного слезозаменителя были рекомендованы за 3–5 мин до закапывания гипотензивных средств. Все пациенты применяли данную комбинацию не менее 3–6 мес. Выбор слезозаменителя был обусловлен его трехкомпонентным составом и комплексным воздействием на ткани глаза. Натрия гиалуронат восстанавливает смачиваемость эпителия роговицы и обеспечивает механическую защиту тканей глаза. D-пантенол (провитамин В5) превращается в живых клетках в пантотеновую кислоту, которая в составе коэнзима А участвует во многих клеточных реакциях, в результате чего ускоряется деление клеток, и эпителизация проходит в более ранние сроки. Хондроитина сульфат натрия снижает активность воспалительного процесса, стимулирует выработку собственных гликозаминогликанов роговицы, которые регулируют процесс заживления и предотвращают излишнее рубцевание и помутнение роговицы.
Конфокальная микроскопия была выполнена на микроскопе Confoscan-4 фирмы Nidek. Уровень интенсивности светорассеяния оценивали во всех слоях роговицы в режиме Z-сканирования на основе анализа денситометрической кривой. Регистрировали минимальные и максимальные значения интенсивности светорассеяния во всех слоях роговицы. Оценивали также величину диапазона между максимальным и минимальным уровнями светорассеяния как косвенный критерий оптической однородности исследуемой зоны роговичной ткани.
Статистическая обработка результатов проводилась с помощью пакета программ SPSS Statistica 17.0 с определением значимости различий по критерию Уилкоксона при связанных выборках и по критерию Манна – Уитни при несвязанных выборках.
Результаты и обсуждение
Исследования с помощью конфокальной микроскопии выявили определенные закономерности морфологических изменений в слоях роговицы при первичном обследовании пациентов на фоне повышенного ВГД и при длительном использовании гипотензивной терапии. Результаты подробно описаны в предыдущей публикации [15].На первом этапе работы при обследовании пациентов с первично выявленной глаукомой (без медикаментозного режима) основные изменения, определяемые при конфокальной микроскопии, локализовались в средних и задних слоях стромы, что является результатом нарушения водного баланса роговицы. Наиболее характерными были признаки отека с диффузным снижением прозрачности межклеточного матрикса. В задней строме в зоне, прилежащей к десцеметовой мембране, наблюдали появление характерного свечения как следствие эффекта отражения света от слоя эндотелия.
На фоне длительного медикаментозного режима при компенсированном ВГД максимальные изменения морфологической картины были отмечены в слоях эпителия и передних отделах стромы роговицы. Эпителиопатия была выражена в различной степени. В передних отделах стромы наблюдали резкое снижение прозрачности вещества роговицы с тенденцией к уменьшению количества визуализированных ядер кератоцитов. Регистрируемые патологические изменения, по-видимому, связаны с токсическим действием консервантов, являющихся составляющей частью медикаментозных средств, используемых при глаукоме.
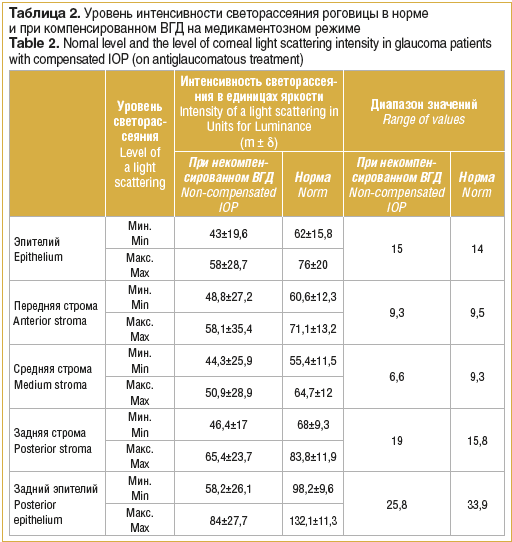
Таким образом, на основании результатов конфокальной микроскопии выявлены определенные закономерности морфологических изменений при глаукоме, что дает возможность предположить наличие характерных изменений интенсивности светорассеяния в различных слоях роговицы. Результаты исследования интенсивности светорассеяния при глаукоме на фоне повышенного ВГД и при условии его компенсации на фоне длительного медикаментозного режима (в сравнении с нормой) представлены в таблицах 1, 2.
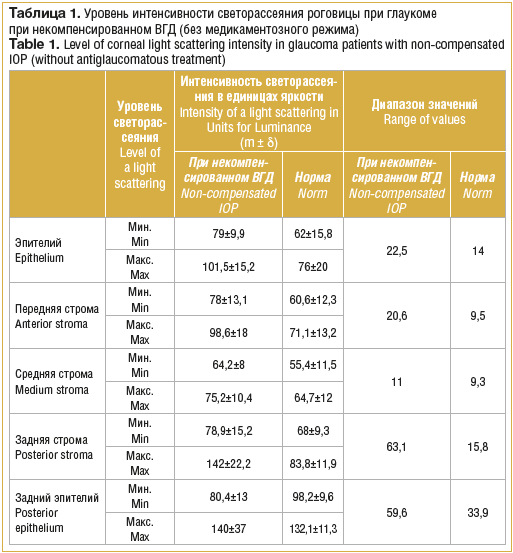
Полученные результаты свидетельствуют о повышении интенсивности светорассеяния при некомпенсированном ВГД во всех слоях роговицы (как минимальных, так и максимальных его значений) по сравнению с нормальными величинами (р<0,05). Незначительное снижение минимального уровня в слое заднего эпителия роговицы было статистически незначимым.
Наибольшие отклонения от нормы максимальной интенсивности светорассеяния наблюдали в задних слоях стромы роговицы, превышение составило 69,5%. Также значительно был превышен данный показатель в слое эпителия (33,5%) и передней строме (38,7%). Зарегистрировано также увеличение диапазона значений между максимальным и минимальным уровнем светорассеяния в задних слоях стромы в 4 раза, в эпителии – в 1,6 раза, в передней строме – в 2,2 раза.
Повышение интенсивности светорассеяния при прохождении света через слои роговицы при высоком ВГД обусловлено нарушением ее водного баланса, что приводит к хроническому отеку, нарушению оптической однородности среды. Причем по результатам конфокальной микроскопии изменения наиболее выражены в задних слоях стромы, что согласуется с полученными данными.
При компенсированном ВГД (на длительном медикаментозном режиме) выявлено некоторое снижение интенсивности светорассеяния по сравнению с нормальными величинами. В передних и средних слоях роговицы значения данного показателя сопоставимы, снижение составило от 19,5 до 21,2%. В слое эпителия минимальная интенсивность светорассеяния снизилась на 30,7%, максимальная – на 24%, в слоях задней стромы, соответственно, на 32% и 22%.
Наибольшие изменения зафиксированы в слое заднего эпителия роговицы. Снижение минимального уровня светорассеяния составило 61%, максимального уровня – 36,4% от нормы с уменьшением диапазона между данными показателями в 1,3 раза.
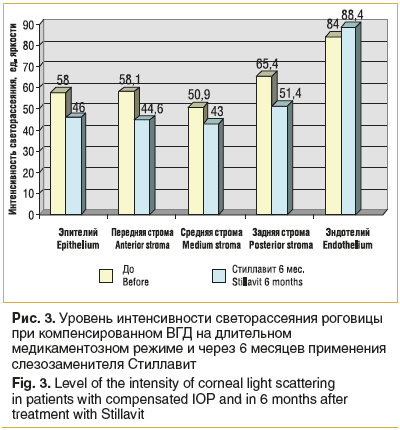
Зависимость интенсивности светорассеяния в различных слоях роговицы от компенсации ВГД при глаукоме продемонстрирована на рисунке 1.

Снижение интенсивности светорассеяния при компенсированном ВГД свидетельствует о восстановлении водного баланса роговицы. Более низкие показатели относительно нормальных величин могут быть следствием уменьшения количества и снижения контрастности ядер кератоцитов, визуализируемых при исследовании. Ядра кератоцитов обладают высокой рефлективностью, являются наиболее яркими наблюдаемыми объектами при конфокальной микроскопии и представляют собой основные центры светорассеяния. При определенной сопоставимости степени снижения интенсивности светорассеяния в слоях стромы все-таки наибольшая тенденция к снижению была отмечена в ее задних слоях, что являлось ожидаемым при компенсации ВГД. Достаточно значимое снижение светорассеяния в эпителиальном слое свидетельствует об увеличении его прозрачности и равномерности. Рассеяние света от слоя заднего эпителия роговицы резко снизилось, что может быть связано с уменьшением светорассеяния в предлежащих слоях стромы, которое, суммируясь, может приводить к увеличению светоотражения и светорассеяния в слое эндотелия.
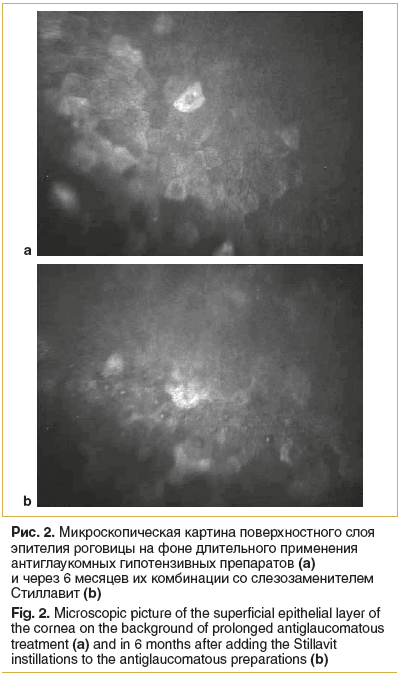
На втором этапе данной работы при анализе результатов конфокальной микроскопии была выявлена положительная динамика при использовании слезозаменителя Стиллавит. В большинстве случаев удалось зафиксировать улучшение состояния поверхностных слоев эпителия роговицы. Рисунок 2 иллюстрирует один из вариантов эпителиопатии, в данном случае поверхностный слой эпителия представлен клетками, ядра которых не визуализируются, что свидетельствует об их недостаточной дифференцировке (рис. 2а). Через 6 мес. использования слезозаместительной терапии эпителиальный слой представлен достаточно дифференцированными клетками с четко контурируемыми ядрами (рис. 2б).
Улучшение состояния стромы роговицы не всегда было достаточно демонстративным, однако в ряде случаев можно было отметить повышение прозрачности межклеточного матрикса, яркости и контрастности ядер кератоцитов.
Оценка интенсивности светорассеяния показала статистически значимое снижение как максимального, так и минимального уровня интенсивности светорассеяния в эпителиальных слоях и строме роговицы. Изменения в слое эндотелия не были статистически достоверны (рис. 3). Наибольшее снижение максимальной интенсивности светорассеяния выявлено в слое эпителия (на 21%) и передней строме (на 23,2%) с уменьшением диапазона между максимальным и минимальным уровнем, соответственно, в 2 и 1,6 раза.
Полученный результат данного исследования демонстрирует восстановление структуры эпителиального слоя, повышение прозрачности и оптической однородности передних слоев стромы.
Заключение
Результаты проведенных исследований позволяют утверждать, что высокий уровень ВГД при глаукоме приводит к нарушению водного баланса роговицы с максимальным нарушением морфологии в средних и задних слоях стромы.Компенсация ВГД способствует снижению хронического отека роговицы, что ведет к восстановлению ее структуры в задних слоях стромы. Однако длительное использование гипотензивных препаратов, содержащих консерванты, может быть причиной морфологических нарушений в эпителии и передних слоях стромы.
Закономерно, что данные структурные изменения ведут к колебаниям флюктуаций показателей преломления компонентов роговичной ткани и изменению интенсивности светорассеяния. Причем изменения показателя интенсивности светорассеяния можно зафиксировать в тех случаях, когда визуализированная картина исследуемой зоны не является четко демонстративной, позволяющей с уверенностью судить о положительной или отрицательной динамике.
Результаты конфокальной микроскопии свидетельствуют о благоприятном эффекте использования слезозаменителя Стиллавит в комбинации с гипотензивными препаратами при глаукоме, что подтверждается данными интенсивности светорассеяния.
Таким образом, величина интенсивности светорассеяния может быть использована в качестве дополнительного критерия для оценки морфологических изменений роговицы при воздействии различных неблагоприятных, повреждающих факторов, а также для оценки эффективности использования медикаментозных средств.












