Введение
Почечно-клеточная карцинома является не часто встречаемым видом рака, составляющим около 1% среди всех известных злокачественных новообразований. В то же время она представляет собой наиболее распространенную злокачественную опухоль почек [1]. Тенденция почечно-клеточной карциномы к метастазированию в головной мозг оценивается в 4–17% [2‒4]. Метастазирование в головной мозг, как правило, имеет метахронный характер и происходит гематогенным путем. В большинстве случаев, по данным магнитно-резонансной томографии (МРТ) с контрастным усилением, выявляется множественное метастатическое поражение головного мозга. Метастазы почечно-клеточной карциномы в головном мозге, даже небольшого размера, часто сопровождаются выраженным перифокальным отеком, что проявляется развитием общемозговой и очаговой симптоматики и быстро ухудшает состояние пациента [3, 5].Основными методами лечения метастазов рака в головной мозг являются хирургическое удаление и лучевое лечение в режиме стандартного фракционирования или стереотаксического высокодозного облучения (гипофракционирование и радиохирургия). Согласно клиническим наблюдениям прошлых лет, при отсутствии лечения средняя продолжительность жизни таких пациентов составляет всего несколько недель [6]. Проведение лучевой терапии на весь объем головного мозга существенно не увеличивает продолжительность жизни, т. к. почечно-клеточная карцинома относится к радиорезистентным опухолям [7, 8]. По данным рандомизированных исследований, локальные рецидивы после проведенного облучение всего объема головного мозга (WBRT) составляют 52% [9, 10]. Хирургическое удаление внутричерепных метастазов почечно-клеточной карциномы увеличивает продолжительность жизни пациентов до одного года, но возможно оно только при ограниченном количестве очагов, расположенных в доступных для хирургического вмешательства областях мозга [11, 12]. После хирургической резекции одиночных метастазов частота рецидивов составляет 46%, в сочетании с последующим проведением WBRT – 20% [9]. Радиохирургическое лечение заключается в однократном подведении высокой дозы радиации к точно локализованным метастатическим очагам и позволяет достичь высокого уровня локального контроля роста метастатических очагов и увеличить продолжительность жизни пациентов до 12–14 мес. [11, 13, 14]. Однако исследования о результатах радиохирургического лечения метастазов почечно-клеточного рака в головной мозг немногочисленны, и вопрос о целесообразности применения этого метода в лечении данной группы пациентов остается актуальным.
Цель данного исследования: оценить эффективность радиохирургического лечения и продолжительность жизни большой группы пациентов с метастазами почечно-клеточного рака в головной мозг.
Материал и методы
В исследовании проанализированы данные пациентов с метастазами почечно-клеточной карциномы в головной мозг, которым проводилось радиохирургическое лечение на аппарате «Гамма-нож» в Клинике радиохирургии, стереотаксической радиотерапии и общей онкологии МИБС.В период с января 2009 г. по ноябрь 2016 г. проведено радиохирургическое лечение 101 пациента с поражением головного мозга метастазами почечно-клеточной карциномы. Характеристика пациентов представлена в таблице 1. Средний возраст пациентов составил 59 лет (от 30 до 79 лет), в большинстве случаев это были больные старше 50 лет. Мужчин – 70, женщин – 31.
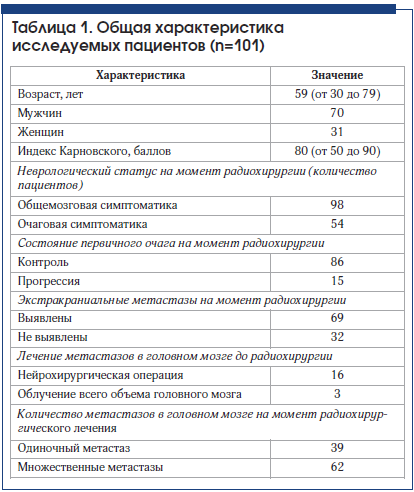
В 91 случае, до выявления внутримозговых метастазов, пациентам была выполнена нефрэктомия с последующим лечением: адъювантной лучевой терапией на область операции – у 2-х больных, химиотерапией – у 32, иммунотерапией ‒ у 32.
Гистологическая природа первичного очага верифицирована у 69 пациентов с почечно-клеточным раком. В 65 случаях это был светлоклеточный рак почки, в 3-х случаях – хромофильный (папиллярный) рак почки, в 1 случае ‒ хромофобный рак почки. У 32 больных гистологическая верификация не проводилась или сведения о ней отсутствовали.
По классификации AJCC (American Joint Committee in Cancer) пациенты распределились следующим образом: I стадия – 8 (7,9%) пациентов, II стадия – 14 (13,9%), III стадия – 17 (16,8%), IV стадия – 48 (47,5%) пациентов. У 14 (13,9%) пациентов стадия заболевания по AJCC осталась неизвестна.
Период от постановки онкологического диагноза до выявления метастатического поражения головного мозга в среднем составил 36 мес. (от 0 до 433,5). У 10 пациентов изначально было обнаружено поражение головного мозга, а затем в процессе дообследования выявлено злокачественное образование почки.
На момент проведения радиохирургического лечения большинство пациентов (77,2%) оценивались по шкале Карновского в 70 и более баллов.
Стереотаксическая радиохирургия была первым методом лечения метастазов в головной мозг у 85 больных. В 16 случаях ей предшествовало открытое нейрохирургическое удаление одиночного внутричерепного метастатического очага, в 5 случаях она была дополнена локальным облучением ложа опухоли, и в 3-х случаях проведено WBRT. Критерием отбора пациентов для сеанса радиохирургического лечения после ранее проведенных лечебных мероприятий служило наличие признаков продолженного роста или появление новых метастатических очагов по данным МРТ головного мозга с контрастным усилением.
До августа 2015 г. лечение проводилось с использованием установки для стереотаксической радиохирургии Leksell Gamma Knife 4C (производство компании Elekta Instrument AB, Швеция), с августа 2015 г. ‒ на установке Leksell Gamma Knife Perfexion (Elekta Instrument AB, Швеция).
Процедура радиохирургии начиналась с фиксации к голове пациента стереотаксической рамы (Leksell G Frame) после предварительного обезболивания точек фиксации введением местных анестетиков. Далее выполнялась стереотаксическая тонкосрезовая МРТ с фиксированным к стереотаксической раме локалайзером, обеспечивающим привязку томографических срезов к координатной системе аппарата «Гамма-нож». Полученные данные МРТ импортировались в планирующую станцию Gamma Plan, где выполнялось дозиметрическое планирование с учетом размеров метастатических очагов и их локализации по отношению к критическим структурам головного мозга. Далее проводился сеанс радиохирургии на «Гамма-ноже», который обычно не превышал 120 мин. По окончании лечения большинство пациентов отправлены на амбулаторное наблюдение в тот же день.
Всего проведено 159 сеансов лечения, причем в 37 случаях проведено 2 и более радиохирургических процедур в связи с выявлением новых метастазов или невозможностью провести лечение всех метастатических очагов за один сеанс. Радиохирургическое лечение единичных очагов проводилось у 39 пациентов; 2‒4 очагов – у 32; 5‒10 – у 22; более 10 – у 8 пациентов. Общее количество опухолей, подвергнутых стереотаксической радиохирургии на аппарате «Гамма-нож», составило 329. Средний объем метастазов составил от 0,5 до 22,9 см3, наибольшего метастаза ‒ 6,2 см3. Средний суммарный объем метастазов, подвергшихся радиохирургическому лечению, составил 5,9 см3 (от 0,5 до 28,7 см3).
Дозы облучения по краю мишени выбирались с учетом рекомендаций RTOG (Radiation Therapy Oncology Group), в большинстве случаев в диапазоне от 18 до 24 Гр (средняя доза 20,0 Гр) по изодозе от 40 до 85% (чаще ‒ 50%). В среднем максимальная доза внутри опухоли составляла около 40 Гр (от 25,9 до 50,0 Гр). Средняя лучевая нагрузка на головной мозг составляла 1,0 Гр (от 0,1 до 2,5 Гр). Параметры радиохирургического лечения суммированы в таблице 2.

Статистический анализ материала проводился в программе SPSS Statistics 17.0 (USA). Продолжительность жизни пациентов, локальный контроль и появление новых метастазов в головном мозге изучались с помощью метода анализа цензурированных данных с использованием функции вероятности Каплана ‒ Майера. Цензурирование осуществлялось на основании контрольных МРТ-исследований головного мозга, информации о состоянии и продолжительности жизни, полученной от пациента или его родственников по телефону, а также в ходе очных консультаций. Временные данные представляли в виде медианы и 95% доверительного интервала (95% ДИ), кумулятивные – в процентном отношении. Сравнение продолжительности жизни в группах проводилось с помощью непараметрического логарифмического рангового критерия. Статистически значимыми считались различия при величине p<0,05.
Результаты
Оценка результатов радиохирургического лечения проводилась на основании контрольных МР-исследований, выполненных согласно рекомендациям при выписке в срок 1‒2 мес. или ранее, если пациент проходил дополнительный сеанс радиохирургического лечения. Контрольное МР-исследование было проведено и рассмотрено при очной или заочной консультации у 84 пациентов, что составило 83% от их общего числа. Динамика изменений пролеченных очагов была детально прослежена в программе GammaPlan FollowUp, которая позволяет точно совмещать контрольные и стереотаксические МР-снимки (рис. 1). Медиана времени наблюдения после радиохирургического лечения составила 10 мес. Локальный контроль (уменьшение или стабилизация размеров метастазов) был достигнут у 80 пациентов, у 4-х пациентов выявлен продолженный рост. Время до возникновения продолженного роста варьировало от 6,5 до 20,8 мес. после лечения с медианой в 13,5 мес. Уровень локального контроля, равный 12 мес., составил 94,3% (см. рис. 1а).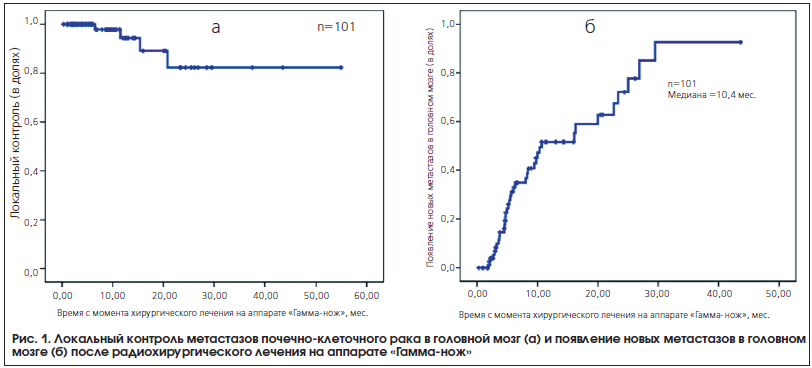
Появление новых метастатических очагов в головном мозге отмечалось у 38 (45%) из 84 пациентов. Медиана выявления новых метастазов в головном мозге от даты первого радиохирургического лечения составила 10,4 мес. (95% ДИ: 3,2–17,5). Вероятность появления новых метастазов в головном мозге через 6 мес. после радиохирургии составила 31,2%, через 12 мес. ‒ 51,6% и через 2 года – 72,1%. В случае выявления новых метастазов пациентам проводилось повторное радиохирургическое лечение (см. рис. 1б).
У всех пациентов был прослежен катамнез на основании очных консультаций, а также в ходе телефонного опроса (рис. 2). В случае смерти пациента уточнялась дата. Для выживших больных катамнез прослежен до 30 июня 2017 г.
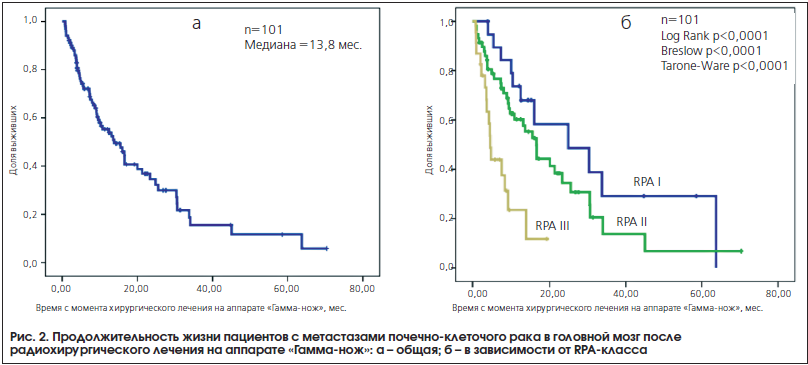
Медиана продолжительности жизни после радиохирургического лечения составила 13,8 мес. (95% ДИ: 8,2–19,5 мес.). При этом однолетняя выживаемость составила 72,1%, двухлетняя – 34,6%, трехлетняя – 15,6%. Живы по настоящее время – 22 человека (21,8% от пролеченных) (см. рис. 2а).
Для прогностической оценки все пациенты, с учетом их возраста, общего состояния по шкале Карновского, контроля первичной опухоли и наличия экстракраниальных метастазов были распределены согласно классификации RPA (Recursive Partitioning Analysis) [15].
Первый, прогностически наиболее благоприятный класс RPA I составили пациенты в возрасте не старше 65 лет с индексом Карновского 70 и более баллов и отсутствием прогрессии экстракраниального процесса (20 человек). К третьему, прогностически наименее благоприятному классу RPA III отнесены пациенты с индексом Карновского ниже 70 баллов (23 человека). Во второй класс отнесены прочие пациенты (58 человек).
В данном исследовании медиана продолжительности жизни пациентов с метастазами почечно-клеточного рака в головной мозг после радиохирургии на аппарате «Гамма-нож», относящихся к RPA I классу, превысила 2 года (95% ДИ: 4,7–45,1 мес.), при этом однолетняя выживаемость составила 73,7%, двухлетняя – 58,3%. Пациенты с RPA III классом, т. е. с индексом Карновского ниже 70 баллов на момент первого радиохирургического лечения, имели самый неблагоприятный прогноз: медиана выживаемости составила 4,7 мес. (95% ДИ: 3,9–5,4 мес.). Медиана выживаемости основной группы пациентов RPA II класса составила 16,5 мес. (95% ДИ: 12,5–20,5 мес.) (см. рис. 2б). Различия в продолжительности жизни между пациентами, составляющими разные RPA классы, являются статистически значимыми.
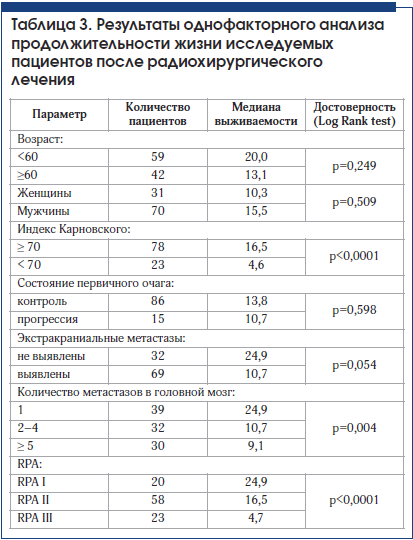
Однофакторный анализ продолжительности жизни пациентов после радиохирургического лечения позволил выявить прогностически значимые факторы, которыми оказались: индекс Карновского, количество метастатических очагов в головном мозге и состояние экстракраниального заболевания. Анализ показал, что такие факторы, как возраст и пол пациента, статистически значимо не влияют на выживаемость (табл. 3).
Обсуждение
В настоящий момент отмечается тенденция к увеличению количества пациентов с метастазами в головной мозг, связанная с возрастанием продолжительности жизни онкологических больных, что обусловлено достижениями системной терапии и большей доступностью методов нейровизуализации. В то же время пока не существует достоверно эффективной таргетной терапии метастазов в головном мозге. Поэтому данное осложнение онкологического заболевания приводит к быстрому ухудшению состояния пациента с развитием очаговой и общемозговой симптоматики. Без проведения лечения продолжительность жизни пациентов с метастазами в головной мозг ограничена 1–3-мя месяцами, несмотря на успехи в контроле экстракраниального процесса [6, 16].Для устранения метастатических очагов в головном мозге используются хирургические и лучевые методы. Нейрохирургическое вмешательство позволяет быстро купировать масс-эффект и улучшить неврологический статус пациента, однако оно возможно только при ограниченном количестве очагов, расположенных в доступных для нейрохирургического вмешательства областях мозга. Удаление метастазов из зон функциональной коры, глубинных структур мозга и стволовых отделов имеет большие риски нарастания неврологического дефицита и ухудшения качества жизни пациента. Также большую роль играет состояние системного заболевания, от которого зависит возможность применения анестезиологического пособия.
В отличие от хирургических методов, лучевое воздействие является неинвазивным и обычно не оказывает влияния на общесоматическое состояние пациента. Лучевые методы применяются в виде WBRT, стандартного фракционного облучения и высокодозного стереотаксического в режимах радиохирургии и гипофракционирования. Исторически первой методикой лучевого лечения внутричерепных метастазов является WBRT. Она позволяет увеличить продолжительность жизни пациентов с метастазами в головной мозг до 3‒6 мес. Однако существует группа радиорезистентных опухолей (к ним относится в. т. ч. почечно-клеточная карцинома), при которых применение низкодозного облучения не останавливает прогрессирования метастатических очагов. Так, исследование результатов WBRT при метастазах почечно-клеточной карциномы в головной мозг, проведенное Nieder et al., показало отсутствие полного ответа во всех случаях [17]. Стереотаксическое высокодозное облучение, заключающееся в подведении высоких доз радиации к точно определенным целевым мишеням за ограниченное количество сеансов (1–5), позволяет преодолеть радиобиологическую резистентность этих опухолей [18]. По данным публикаций разных авторов, уровень локального контроля после радиохирургического лечения составляет от 85 до 97% [11, 13, 19‒22].
Одним из исследований, обобщившим опыт лечения наибольшего количества пациентов с метастазами почечно-клеточной карциномы в головной мозг, является исследование трех радиохирургических центров Восточной Европы [23]. Авторы делают заключение о 95 % уровне локального контроля при медиане выживаемости 8 мес. Прогностически благоприятными факторами были индекс Карновского не ниже 70 баллов, контроль первичного очага и краевая доза на наибольший очаг более 20 Гр. D.J. Seastone et al. также отмечают уровень локального контроля у 90% пациентов, однако авторы заключают, что степень влияния радиохирургии на выживаемость пациентов остается неизвестной [24].
Аналогичные результаты получены еще в одном крупном исследовании, объединившем 158 пациентов с 531 метастатическим очагом в совокупности [25]. Локальный контроль достигнут в 92% случаев, медиана продолжительности жизни после радиохирургического лечения составила 8,2 мес. Молодой возраст, высокий индекс Карновского, малое количество метастазов в головном мозге и отсутствие предшествующего WBRT оказались благоприятными прогностическими факторами.
По результатам исследования, проведенного в нашей клинике, локальный контроль составил 95% при медиане продолжительности жизни 13,8 мес. Таким образом, определена более длительная медиана продолжительности жизни, что согласуется с недавно опубликованными результатами исследования радиохирургии метастазов почечно-клеточного рака в головной мозг F. Ippen et al., где медиана продолжительности жизни достигает 13,9 мес. [11]. Более высокая продолжительность жизни, полученная в исследованиях последних лет, по сравнению с отмеченной в более ранних публикациях, возможно, связана с появлением таргетных препаратов, позволяющих более эффективно контролировать экстракраниальное заболевание [26].












