–Ь–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Љ–µ—В–∞—Б—В–∞–Ј–Є—А–Њ–≤–∞–љ–Є—П
–Я—А–Њ—Ж–µ—Б—Б –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–µ—В–∞—Б—В–∞–Ј–Є—А–Њ–≤–∞–љ–Є—П –Њ—Б—В–∞–µ—В—Б—П –њ—А–µ–і–Љ–µ—В–Њ–Љ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –љ–∞—Г—З–љ–Њ–≥–Њ –њ–Њ–Є—Б–Ї–∞. –Х—Й–µ –≤ 1889 –≥. S. Paget –њ—А–µ–і–ї–Њ–ґ–Є–ї —В–µ–Њ—А–Є—О ¬Ђ—Б–µ–Љ—П–љ –Є –њ–Њ—З–≤—Л¬ї, –Ї–Њ—В–Њ—А–∞—П –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В, —З—В–Њ –і–ї—П —А–Њ—Б—В–∞ –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–є –Ї–ї–µ—В–Ї–Є (—Б–µ–Љ—П) —В—А–µ–±—Г–µ—В—Б—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–∞—П –Љ–Є–Ї—А–Њ—Б—А–µ–і–∞ (–њ–Њ—З–≤–∞). –Ъ–ї–µ—В–Ї–Є –њ–µ—А–≤–Є—З–љ–Њ–є –Њ–њ—Г—Е–Њ–ї–Є –њ—А–Њ—Е–Њ–і—П—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –±–Њ–ї—М—И–Њ–є –њ—Г—В—М –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Љ–µ—В–∞—Б—В–∞–Ј–Є—А–Њ–≤–∞–љ–Є—П. –Я—А–Њ–љ–Є–Ї–∞—П —З–µ—А–µ–Ј –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ—Л–є –Љ–∞—В—А–Є–Ї—Б –Є –Љ–µ–Љ–±—А–∞–љ—Г –∞–љ–≥–Є–Њ–ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤, –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є –њ–Њ–њ–∞–і–∞—О—В –≤ —Б–Є—Б—В–µ–Љ–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї. –Т –њ—А–Њ—Ж–µ—Б—Б–µ –Љ–µ—В–∞—Б—В–∞–Ј–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї—М—И–∞—П —З–∞—Б—В—М –Њ–њ—Г—Е–Њ–ї–µ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї –њ–Њ–≥–Є–±–∞–µ—В, —В. –Ї. –Њ–љ–Є –љ–µ —Б–њ–Њ—Б–Њ–±–љ—Л –≤—Л–ґ–Є—В—М –≤ —Н—В–Њ–є –Љ–Є–Ї—А–Њ—Б—А–µ–і–µ. –Ю—Б—В–∞–≤—И–Є–µ—Б—П –Ї–ї–µ—В–Ї–Є –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –Ј–∞—Й–Є—В–љ–Њ–Љ—Г –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є –і—А—Г–≥–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ (—А–Э, –Њ–Ї—Б–Є–≥–µ–љ–∞—Ж–Є—П). –Ы–Є—И—М –µ–і–Є–љ–Є—З–љ—Л–µ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є –њ–Њ–њ–∞–і–∞—О—В –≤ –±—Г–і—Г—Й–Є–є –Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Є–є –Њ—З–∞–≥ (–њ—А–µ–Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї—Г—О –љ–Є—И—Г). –Я—А–Є –Љ–µ—В–∞—Б—В–∞–Ј–Є—А–Њ–≤–∞–љ–Є–Є –≤ –Ї–Њ—Б—В–Є –њ–µ—А–≤–Є—З–љ–∞—П –Њ–њ—Г—Е–Њ–ї—М –∞–Ї—В–Є–≤–Є—А—Г–µ—В —А–∞–Ј–ї–Є—З–љ—Л–µ –±–µ–ї–Ї–Є –Є —Ж–Є—В–Њ–Ї–Є–љ—Л (p27, p130, HIF-1, VEGF-A, TNF-ќ±, TGF-ќ≤), –Ї–Њ—В–Њ—А—Л–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –≤—Л–±—А–Њ—Б—Г –≤ —Б–Є—Б—В–µ–Љ–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –≥–µ–Љ–Њ–њ–Њ—Н—В–Є—З–µ—Б–Ї–Є—Е –Є –Љ–µ–Ј–µ–љ—Е–Є–Љ–∞–ї—М–љ—Л—Е —Б—В–≤–Њ–ї–Њ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї. –Ш–Љ–µ–љ–љ–Њ —Н—В–Є –Ї–ї–µ—В–Ї–Є —Б–Њ–Ј–і–∞—О—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ —Г—Б–ї–Њ–≤–Є—П –і–ї—П –≤—Л–ґ–Є–≤–∞–љ–Є—П –Њ–њ—Г—Е–Њ–ї–Є –≤ –њ—А–µ–Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–Є—И–µ. –Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–Є–µ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є, –њ–Њ–њ–∞–і–∞—П —Б —В–Њ–Ї–Њ–Љ –Ї—А–Њ–≤–Є –≤ –љ–Є—И—Г –≥–µ–Љ–Њ–њ–Њ—Н—В–Є—З–µ—Б–Ї–Є—Е —Б—В–≤–Њ–ї–Њ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї, –њ–µ—А–µ—Е–Њ–і—П—В –≤ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–њ—П—З–Ї–Є –Є –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —Б–њ—Г—Б—В—П –Љ–љ–Њ–≥–Є–µ –≥–Њ–і—Л.
–§–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—Б—В–љ—Л—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Њ—Б—В–∞ –Є –Љ–Њ—А—Д–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –±–µ–ї–Ї–Њ–≤. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Є—Е —В–Є–њ–∞ —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –Њ—Б—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ –Є–ї–Є –Њ—Б—В–µ–Њ–±–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–µ –Њ—З–∞–≥–Є. –Ю—Б—В–µ–Њ–Ї–ї–∞—Б—В—Л —Б–µ–Ї—А–µ—В–Є—А—Г—О—В PTHrP (–њ–µ–њ—В–Є–і, —Б–≤—П–Ј–∞–љ–љ—Л–є —Б –≥–Њ—А–Љ–Њ–љ–Њ–Љ —Й–Є—В–Њ–≤–Є–і–љ–Њ–є –ґ–µ–ї–µ–Ј—Л), COX-2, FGF, TNF, IL-1, IL-6, IL-8, IL-11 вАФ —Д–∞–Ї—В–Њ—А—Л, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–і–∞—О—В —Б–Є–≥–љ–∞–ї –Њ—Б—В–µ–Њ–±–ї–∞—Б—В—Г –і–ї—П —Б–µ–Ї—А–µ—Ж–Є–Є RANKL (–ї–Є–≥–∞–љ–і –і–ї—П –∞–Ї—В–Є–≤–∞—В–Њ—А–∞ —А–µ—Ж–µ–њ—В–Њ—А–∞ –љ—Г–Ї–ї–µ–Њ—В–Є–і–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞-B). –Я—А–Є —Г—З–∞—Б—В–Є–Є RANKL –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–∞, –≤—Л–ґ–Є–≤–∞–љ–Є–µ –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–Њ–≤. –Я–Њ—Б–ї–µ–і–љ–Є–µ –∞–Ї—В–Є–≤–Є—А—Г—О—В —А–µ–Ј–Њ—А–±—Ж–Є—О –Ї–Њ—Б—В–Є –Є –≤—Л–±—А–Њ—Б —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Њ—Б—В–∞ IGF-I, TGF-ќ≤, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –і–∞–ї—М–љ–µ–є—И–µ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –Ї–ї–µ—В–Њ–Ї —А–∞–Ї–∞ –Љ–Њ–ї–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (–†–Ь–Ц) –Є —Б–µ–Ї—А–µ—Ж–Є–Є PTHrP. –§–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—Б—В–љ—Л—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –њ—А–Є —А–∞–Ї–µ –њ—А–µ–і—Б—В–∞—В–µ–ї—М–љ–Њ–є –ґ–µ–ї–µ–Ј—Л (–†–Я–Ц) –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ—Г—В–µ–Љ —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є –Њ—Б—В–µ–Њ¬≠–±–ї–∞—Б—В—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї —Н–љ–і–Њ—В–µ–ї–Є–љ-1, —Д–∞–Ї—В–Њ—А —А–Њ—Б—В–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –Є–љ—Б—Г–ї–Є–љ–Њ–њ–Њ–і–Њ–±–љ—Л–є —Д–∞–Ї—В–Њ—А —А–Њ—Б—В–∞, –Є –Љ–Њ—А—Д–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –±–µ–ї–Ї–Њ–≤ (—А–Є—Б. 1).
![–†–Є—Б. 1. –Ь–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Љ–µ—В–∞—Б—В–∞–Ј–Є—А–Њ–≤–∞–љ–Є—П [1] –†–Є—Б. 1. –Ь–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Љ–µ—В–∞—Б—В–∞–Ј–Є—А–Њ–≤–∞–љ–Є—П [1]](/upload/medialibrary/d8e/16-1.png)
–§–∞–Ї—В–Њ—А—Л —А–Њ—Б—В–∞, —Б–µ–Ї—А–µ—В–Є—А—Г–µ–Љ—Л–µ –Њ–њ—Г—Е–Њ–ї—М—О, –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–Є–њ–∞ –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –њ—А–Є–≤–Њ–і—П—В –Ї –њ–Њ–і–∞–≤–ї–µ–љ–Є—О –≤—Л–±—А–Њ—Б–∞ –Њ—Б—В–µ–Њ–њ—А–Њ—В–µ–≥–µ—А–Є–љ–∞ вАФ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞ RANKL, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –Ј–∞–Љ—Л–Ї–∞–µ—В—Б—П –њ–Њ—А–Њ—З–љ—Л–є –Ї—А—Г–≥ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –Њ–њ—Г—Е–Њ–ї–Є —Б –Ї–Њ—Б—В–љ—Л–Љ –Љ–Є–Ї—А–Њ–Њ–Ї—А—Г–ґ–µ–љ–Є–µ–Љ [1].
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –Љ–µ–ґ–і—Г –Ї–ї–µ—В–Ї–∞–Љ–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –Љ–Є–µ–ї–Њ–Љ—Л –Є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ—М—О
–Э–µ—Б–Ї–Њ–ї—М–Ї–Њ –Є–љ—Л–µ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –ї–µ–ґ–∞—В –≤ –Њ—Б–љ–Њ–≤–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –Љ–µ–ґ–і—Г –Ї–ї–µ—В–Ї–∞–Љ–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –Љ–Є–µ–ї–Њ–Љ—Л (–Ъ–Ь) –Є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ—М—О [2].
–Ъ–Ь —А–∞—Б—В—Г—В –≤ –Ї–Њ—Б—В–љ–Њ–Љ –Љ–Є–Ї—А–Њ–Њ–Ї—А—Г–ґ–µ–љ–Є–Є, –њ—А–Є —Н—В–Њ–Љ –Ї–ї—О—З–µ–≤—Г—О —А–Њ–ї—М –Є–≥—А–∞—О—В –Њ—Б—В–µ–Њ–±–ї–∞—Б—В—Л, –Ї–Њ—В–Њ—А—Л–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—О—В –њ—А—П–Љ–Њ–µ —А–µ–≥—Г–ї–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ—Б—В–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–Є—И–Є. –Ю—Б—В–µ–Њ¬≠–±–ї–∞—Б—В—Л —Б–µ–Ї—А–µ—В–Є—А—Г—О—В –і–µ–Ї–Њ—А–Є–љ (decorin), –Ї–Њ—В–Њ—А—Л–є –≤—Л–Ј—Л–≤–∞–µ—В –∞—А–µ—Б—В –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞ –Є –∞–њ–Њ–њ—В–Њ–Ј –Ъ–Ь (–Њ–±–Њ–Ј–љ–∞—З–µ–љ–Њ –±—Г–Ї–≤–Њ–є ¬ЂA¬ї –љ–∞ —А–Є—Б. 2). –Т –Њ—В–≤–µ—В –Ъ–Ь –њ–Њ–і–∞–≤–ї—П—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ—Б—В–µ–Њ–±–ї–∞—Б—В–Њ–≤ —З–µ—А–µ–Ј —Д–∞–Ї—В–Њ—А DKK1 (Dickkopf-1), –Ї–Њ—В–Њ—А—Л–є –±–ї–Њ–Ї–Є—А—Г–µ—В –њ—Г—В—М, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є –і–ї—П –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є. –Т —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –Њ—Б—В–µ–Њ–±–ї–∞—Б—В—Л –њ—А–Є–≤–ї–µ–Ї–∞—О—В –Є–Љ–Љ—Г–љ–љ—Л–µ –Ї–ї–µ—В–Ї–Є –≤ –Ї–Њ—Б—В–љ—Л–є –Љ–Њ–Ј–≥ (–±—Г–Ї–≤–∞ ¬Ђ–Т¬ї –љ–∞ —А–Є—Б. 2), –≥–і–µ –Њ–љ–Є –Љ–Њ–≥—Г—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М –њ—А–Њ—В–Є–≤–Њ–Њ–њ—Г—Е–Њ–ї–µ–≤—Л–є —Н—Д—Д–µ–Ї—В. –Ю–і–љ–∞–Ї–Њ –њ—А–Є–≤–ї–µ—З–µ–љ–Є–µ T-reg –Ї–ї–µ—В–Њ–Ї –Є —Б—Г–њ—А–µ—Б—Б–Њ—А–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Љ–Є–µ–ї–Њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П –Љ–Њ–ґ–µ—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М –њ–Њ—В–µ–љ—Ж–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —А–Њ—Б—В –Ъ–Ь –Ј–∞ —Б—З–µ—В –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П –њ—А–Њ—В–Є–≤–Њ–Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–≥–Њ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—Б—В–µ–Њ–±–ї–∞—Б—В–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –≤—Л–ґ–Є–≤–∞–љ–Є—О –Є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –Ъ–Ь, –љ–Њ –Ъ–Ь –∞–Ї—В–Є–≤–Є—А—Г—О—В –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В—Л (–±—Г–Ї–≤–∞ ¬Ђ–°¬ї –љ–∞ —А–Є—Б. 2). –Т–∞–ґ–љ—Л–Љ —Б—В–Є–Љ—Г–ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Ъ–Ь —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ј–Є—В–Є–≤–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –Љ–µ–Ј–µ–љ—Е–Є–Љ–∞–ї—М–љ—Л—Е —Б—В–≤–Њ–ї–Њ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї –љ–∞ –±–∞–ї–∞–љ—Б –Њ—Б—В–µ–Њ–±–ї–∞—Б—В–Њ–≤ –Є –∞–і–Є–њ–Њ—Ж–Є—В–Њ–≤ (–Ї–ї–µ—В–Њ–Ї –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є) (–±—Г–Ї–≤–∞ ¬ЂD¬ї –љ–∞ —А–Є—Б. 2). –Т–Ї–ї–∞–і –Ї–Њ—Б—В–љ–Њ–Љ–Њ–Ј–≥–Њ–≤—Л—Е –∞–і–Є–њ–Њ—Ж–Є—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і–Љ–µ—В–Њ–Љ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –љ–∞—Г—З–љ–Њ–≥–Њ –њ–Њ–Є—Б–Ї–∞. –Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Њ–љ–Є —Б–њ–Њ—Б–Њ–±–љ—Л –њ–Њ–і–∞–≤–ї—П—В—М –љ–Њ—А–Љ–∞–ї—М–љ—Л–є –≥–µ–Љ–Њ–њ–Њ—Н–Ј, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О –Ъ–Ь (–±—Г–Ї–≤–∞ ¬Ђ–Х¬ї –љ–∞ —А–Є—Б. 2). –Р–і–Є–њ–Њ—Ж–Є—В—Л –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –ґ–Є—А–Њ–≤–Њ–є —В–Ї–∞–љ–Є –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Є–Ј–±—Л—В–Њ—З–љ–Њ–≥–Њ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—П –Љ–Њ–≥—Г—В –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞—В—М —Б–Є—Б—В–µ–Љ–љ–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –Є –≤—Л–Ј—Л–≤–∞—В—М –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –∞–і–Є–њ–Њ–Ї–Є–љ–Њ–≤ –Є —Н—Б—В—А–Њ–≥–µ–љ–∞, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —А–Њ—Б—В –Є –≤—Л–ґ–Є–≤–∞–љ–Є–µ –Ъ–Ь (–±—Г–Ї–≤–∞ ¬ЂF¬ї –љ–∞ —А–Є—Б. 2).
![–†–Є—Б. 2. –Ь–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –Љ–µ–ґ–і—Г –Ї–ї–µ—В–Ї–∞–Љ–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –Љ–Є–µ–ї–Њ–Љ—Л –Є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ—М—О [2] –†–Є—Б. 2. –Ь–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –Љ–µ–ґ–і—Г –Ї–ї–µ—В–Ї–∞–Љ–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –Љ–Є–µ–ї–Њ–Љ—Л –Є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ—М—О [2]](/upload/medialibrary/393/16-2.png)
–°–Њ–±—Л—В–Є—П, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Ї–Њ—Б—В–љ–Њ–є —Б–Є—Б—В–µ–Љ–Њ–є
–Ь–µ—В–∞—Б—В–∞–Ј—Л –≤ –Ї–Њ—Б—В–Є —Б–Ї–µ–ї–µ—В–∞ –Є–Љ–µ—О—В –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Г—О –і–µ—В–µ—А–Љ–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ—Б—В—М –Є –≤—Л—Б–Њ–Ї—Г—О —З–∞—Б—В–Њ—В—Г –њ–Њ—А–∞–ґ–µ–љ–Є—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –Ї–Њ—Б—В–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л [3].
–Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Ї–Њ—Б—В–љ—Л–µ –Љ–µ—В–∞—Б—В–∞–Ј—Л –ї–Њ–Ї–∞–ї–Є–Ј—Г—О—В—Б—П –≤ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–µ, –Ї–Њ—Б—В—П—Е —В–∞–Ј–∞, —А–µ–±—А–∞—Е, –±–µ–і—А–µ–љ–љ–Њ–є –Є –њ–ї–µ—З–µ–≤–Њ–є –Ї–Њ—Б—В–Є (—А–Є—Б. 3). –Ю—З–µ–≤–Є–і–љ–Њ, –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л–є —В–Є–њ –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П, –±–Њ–≥–∞—В–∞—П –∞—А—В–µ—А–Є–Њ–≤–µ–љ–Њ–Ј–љ–∞—П —Б–µ—В—М, –Ї–Є–љ–µ—В–Є–Ї–∞ –і–≤–Є–ґ–µ–љ–Є—П —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –∞–Ї—В–Є–≤–љ–Њ–Љ—Г –Љ–µ—В–∞—Б—В–∞–Ј–Є—А–Њ–≤–∞–љ–Є—О –≤ —Н—В–Є —Г—З–∞—Б—В–Ї–Є –Ї–Њ—Б—В–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, —З—В–Њ –Є –Њ–њ—А–µ–і–µ–ї—П–µ—В –≤—Л—Б–Њ–Ї—Г—О —З–∞—Б—В–Њ—В—Г —А–∞–Ј–≤–Є—В–Є—П —Б–Ї–µ–ї–µ—В–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
![–†–Є—Б. 3. –Ь–µ—Б—В–∞ –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є 2429 –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –Ї–∞—А—Ж–Є–љ–Њ–Љ –≤ –Ї–Њ—Б—В–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ –Є–Ј 2680 —Б–ї—Г—З–∞–µ–≤ (—Ж–Є—В–Є—А—Г–µ—В—Б—П –Є–Ј Wick M.R., 2014 [3] –њ–Њ –і–∞–љ–љ—Л–Љ M. Campanacci, 1999) –†–Є—Б. 3. –Ь–µ—Б—В–∞ –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є 2429 –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –Ї–∞—А—Ж–Є–љ–Њ–Љ –≤ –Ї–Њ—Б—В–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ –Є–Ј 2680 —Б–ї—Г—З–∞–µ–≤ (—Ж–Є—В–Є—А—Г–µ—В—Б—П –Є–Ј Wick M.R., 2014 [3] –њ–Њ –і–∞–љ–љ—Л–Љ M. Campanacci, 1999)](/upload/medialibrary/654/16-3.png)
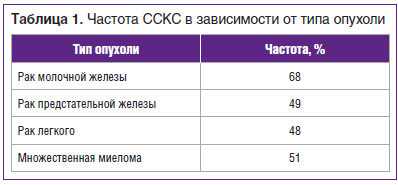
–Ф–ї—П –Њ–±–Њ–Ј–љ–∞—З–µ–љ–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –Љ–µ—В–∞—Б—В–∞–Ј–∞–Љ–Є –≤ –Ї–Њ—Б—В–Є, –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —В–µ—А–Љ–Є–љ ¬Ђ—Б–Њ–±—Л—В–Є—П, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Ї–Њ—Б—В–љ–Њ–є —Б–Є—Б—В–µ–Љ–Њ–є¬ї (–°–°–Ъ–°). –°–°–Ъ–° –Њ–±—К–µ–і–Є–љ—П—О—В: 1) –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ–µ—А–µ–ї–Њ–Љ; 2) –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –ї—Г—З–µ–≤–Њ–є —В–µ—А–∞–њ–Є–Є; 3) –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П; 4) –Ї–Њ–Љ–њ—А–µ—Б—Б–Є—О —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞; 5) –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є—О. –І–∞—Б—В–Њ—В–∞ –°–°–Ъ–° –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–Є–њ–∞ –Њ–њ—Г—Е–Њ–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 1 [1, 4].
–Ы—Г—З–µ–≤–∞—П —В–µ—А–∞–њ–Є—П –Є –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ вАФ –Љ–µ—В–Њ–і—Л, –Ї–Њ—В–Њ—А—Л–µ —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П—О—В –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Є–ї–Є —Г–≥—А–Њ–Ј–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–µ—А–µ–ї–Њ–Љ–∞, –∞ —В–∞–Ї–ґ–µ –≤ —Б–ї—Г—З–∞–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–°–°–Ъ–° –љ–µ–≥–∞—В–Є–≤–љ–Њ –≤–ї–Є—П—О—В –љ–∞ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е. –Т –Њ–і–љ–Њ–Љ –Є–Ј –±–Њ–ї—М—И–Є—Е –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є (n=36 000) –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 9 –ї–µ—В –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Њ–±—Й—Г—О –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е –†–Ь–Ц. –Ь–µ–і–Є–∞–љ–∞ –Њ–±—Й–µ–є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–µ—В–∞—Б—В–∞–Ј–∞–Љ–Є –≤ –Ї–Њ—Б—В–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 16 –Љ–µ—Б., –њ—А–Є –љ–∞–ї–Є—З–Є–Є –°–°–Ъ–° вАФ –ї–Є—И—М 7 –Љ–µ—Б. [5]. –Т –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –°–°–Ъ–° –≤—Б—В—А–µ—З–∞—О—В—Б—П —Г –Ї–∞–ґ–і–Њ–≥–Њ —З–µ—В–≤–µ—А—В–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ —А–∞–Ї–Њ–Љ –ї–µ–≥–Ї–Њ–≥–Њ —Б –Љ–µ—В–∞—Б—В–∞–Ј–∞–Љ–Є –≤ –Ї–Њ—Б—В–Є, –њ—А–Є —Н—В–Њ–Љ –Љ–µ–і–Є–∞–љ–∞ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є —Г –љ–Є—Е —Б–Њ—Б—В–∞–≤–Є–ї–∞ –Њ–Ї–Њ–ї–Њ 6 –Љ–µ—Б. [6].
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–Љ –њ—А–Њ—Ж–µ—Б—Б–Њ–Љ
–Ф–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –≤ –Ї–Њ—Б—В–Є —Б–Ї–µ–ї–µ—В–∞ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –ї—Г—З–µ–≤—Л–µ –Љ–µ—В–Њ–і—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Љ–∞—А–Ї–µ—А—Л. –Ю—Ж–µ–љ–Ї–∞ –Ї–Њ—Б—В–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Є–Љ–µ–µ—В –Њ–≥—А–Њ–Љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –і–ї—П –≤—Л–±–Њ—А–∞ –Љ–µ—В–Њ–і–∞ –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ–≥–љ–Њ–Ј–∞, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ—А–Є —А–∞–Ј–Љ–µ—А–µ –Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—З–∞–≥–∞ >1 —Б–Љ –њ–Њ—В–µ—А—П –Љ–Є–љ–µ—А–∞–ї—М–љ–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є (–Ь–Я–Ъ–Ґ) —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 50% [4]. –Ю–±—К–µ–Ї—В–Є–≤–љ—Л–Љ –ї—Г—З–µ–≤—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —П–≤–ї—П–µ—В—Б—П –Њ—Б—В–µ–Њ—Б—Ж–Є–љ—В–Є–≥—А–∞—Д–Є—П. –Я–Њ–≤—Л—И–µ–љ–љ–Њ–µ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ —А–∞–і–Є–Њ–Є–Ј–Њ—В–Њ–њ–Њ–≤ –Њ—В—А–∞–ґ–∞–µ—В –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї—Г—О —А–µ–∞–Ї—Ж–Є—О, –њ—А–Њ–Є—Б—Е–Њ–і—П—Й—Г—О –њ—А–Є –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е, —В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е. –Ь–µ—В–Њ–і –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М —Г—З–∞—Б—В–Ї–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ—Б—В–µ–є –≥–Њ—А–∞–Ј–і–Њ —А–∞–љ—М—И–µ, —З–µ–Љ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —А–µ–љ—В–≥–µ–љ–Њ–≤—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —В. –Ї. –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ—Б—В–љ—Л—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –≤–∞–ґ–љ–∞—П —А–Њ–ї—М –Њ—В–≤–Њ–і–Є—В—Б—П —Г—Б–Є–ї–µ–љ–Є—О –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≤ –Љ–µ—Б—В–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –љ–Њ–≤–Њ–≥–Њ –Њ—З–∞–≥–∞. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤—Л—П–≤–ї–µ–љ–љ—Л–µ –Њ—З–∞–≥–Є –≥–Є–њ–µ—А—Д–Є–Ї—Б–∞—Ж–Є–Є —А–∞–і–Є–Њ–Є–Ј–Њ—В–Њ–њ–Њ–≤ —Б —Ж–µ–ї—М—О –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є—П –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –≤ –Ї–Њ—Б—В–Є –Є—Б—Б–ї–µ–і—Г—О—В —Б –њ–Њ–Љ–Њ—Й—М—О —А–µ–љ—В–≥–µ–љ–∞, –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –Є–ї–Є –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є (–Ь–†–Ґ) [7].
–°–њ–Є—А–∞–ї—М–љ–∞—П –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П (–°–Ъ–Ґ) –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М—О –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–≤–Є–і–µ—В—М –Њ—З–∞–≥–Є –і–µ—Б—В—А—Г–Ї—Ж–Є–Є –Є–ї–Є —Г–њ–ї–Њ—В–љ–µ–љ–Є—П –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є, –∞ —В–∞–Ї–ґ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –љ–∞ –Љ—П–≥–Ї–Є–µ —В–Ї–∞–љ–Є –њ—А–Є –≤—Л—Е–Њ–і–µ –Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Ј–∞ –њ—А–µ–і–µ–ї—Л –Ї–Њ—Б—В–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А. –Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –°–Ъ–Ґ –і–Њ–Ї–∞–Ј–∞–љ–Њ –њ—А–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤, –ї–Њ–Ї–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–∞—Е –ї–µ—З–µ–љ–Є—П (–≤–≤–µ–і–µ–љ–Є–µ –Ї–Њ—Б—В–љ–Њ–≥–Њ —Ж–µ–Љ–µ–љ—В–∞) –Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –±–Є–Њ–њ—Б–Є–Є [4, 7].
–Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –ї—Г—З–µ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —П–≤–ї—П–µ—В—Б—П –Ь–†–Ґ, —Б–Њ—З–µ—В–∞—О—Й–∞—П –≤ —Б–µ–±–µ –≤—Л—Б–Њ–Ї—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –≤—Л—П–≤–ї—П—В—М –Љ–µ—В–∞—Б—В–∞–Ј—Л –љ–∞ —Н—В–∞–њ–µ –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–Є –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [7]. –Ь–†–Ґ —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ —Б–ї—Г—З–∞–µ –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –ї—Г—З–µ–≤–Њ–є —В–µ—А–∞–њ–Є–Є [4].
–°–Њ–≤–Љ–µ—Й–µ–љ–Є–µ –Њ–і–љ–Њ–Љ–Њ–Љ–µ–љ—В–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –њ–Њ–ї—Г—З–∞–µ–Љ—Л—Е –њ—А–Є —А–∞–і–Є–Њ–Є–Ј–Њ—В–Њ–њ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Є –Ъ–Ґ, –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г—Б—В–∞–љ–Њ–≤–Є—В—М —Е–∞—А–∞–Ї—В–µ—А –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ —Б—В—А—Г–Ї—В—Г—А–µ –Љ–µ—В–∞—Б—В–∞–Ј–∞ –Є –Њ—Ж–µ–љ–Є—В—М –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞. –Ю–і–љ–∞–Ї–Њ –≤ —А—Г—В–Є–љ–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Љ–µ—В–Њ–і –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П —А–µ–і–Ї–Њ –≤ —Б–≤—П–Ј–Є —Б –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–є –і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О [8].
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ–Њ–Ј–Є—В—А–Њ–љ–љ–Њ-—Н–Љ–Є—Б—Б–Є–Њ–љ–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є –њ—А–Є –Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Ї–Њ—Б—В–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і–Љ–µ—В–Њ–Љ –љ–∞—Г—З–љ–Њ–≥–Њ –њ–Њ–Є—Б–Ї–∞ [4].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤–Њ –Љ–љ–Њ–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –∞–Ї—В–Є–≤–љ–Њ –Є–Ј—Г—З–∞—О—В—Б—П –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Љ–∞—А–Ї–µ—А—Л –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞, –Ї–Њ—В–Њ—А—Л–µ –≤–∞–ґ–љ—Л –њ—А–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Ї–Њ—Б—В–љ—Л—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є —А–Є—Б–Ї–∞ —Б–Ї–µ–ї–µ—В–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –∞ —В–∞–Ї–ґ–µ –њ—А–Є –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥–µ –ї–µ—З–µ–љ–Є—П –Є —Б–Љ–µ—А—В–Є. –Ю—Б–љ–Њ–≤–љ—Л–µ –Љ–∞—А–Ї–µ—А—Л —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Є —А–µ–Ј–Њ—А–±—Ж–Є–Є –Ї–Њ—Б—В–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–Є–ґ–µ [9].
–Ь–∞—А–Ї–µ—А—Л –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ (—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Є —А–µ–Ј–Њ—А–±—Ж–Є–Є –Ї–Њ—Б—В–Є)
–Ь–∞—А–Ї–µ—А—Л —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ—Б—В–Є
BALP (Bone-specific alkaline phosphatase) вАФ —Б–њ–µ—Ж–Є—Д–Є—З–љ–∞—П –і–ї—П –Ї–Њ—Б—В–Є —Й–µ–ї–Њ—З–љ–∞—П —Д–Њ—Б—Д–∞—В–∞–Ј–∞;
OC (Osteocalcin) вАФ –Њ—Б—В–µ–Њ–Ї–∞–ї—М—Ж–Є–љ;
PINP (Amino-terminal propeptide of type I procollagen) вАФ –∞–Љ–Є–љ–Њ—В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л–є –њ—А–Њ–њ–µ–њ—В–Є–і –њ—А–Њ–Ї–Њ–ї–ї–∞–≥–µ–љ–∞ I —В–Є–њ–∞;
PICP (Carboxy-terminal propeptide of type I procollagen) вАФ –Ї–∞—А–±–Њ–Ї—Б–Є—В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л–є –њ—А–Њ–њ–µ–њ—В–Є–і –њ—А–Њ–Ї–Њ–ї–ї–∞–≥–µ–љ–∞ I —В–Є–њ–∞.
–Ь–∞—А–Ї–µ—А—Л —А–µ–Ј–Њ—А–±—Ж–Є–Є –Ї–Њ—Б—В–Є
–Ъ–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л–µ:
PYD (Pyridinoline) вАФ –њ–Є—А–Є–і–Є–љ–Њ–ї–Є–љ;
DPD (Deoxypyridinoline) вАФ –і–µ–Ј–Њ–Ї—Б–Є–њ–Є—А–Є–і–Є–љ–Њ–ї–Є–љ;
Hyp (Hydroxyproline) вАФ –≥–Є–і—А–Њ–Ї—Б–Є–њ—А–Њ–ї–Є–љ;
–°TX-I (ICTP) (Carboxy-terminal crosslinked telopeptide of type I collagen) вАФ –Ї–∞—А–±–Њ–Ї—Б–Є—В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л–є —В–µ–ї–Њ–њ–µ–њ—В–Є–і –њ–Њ–њ–µ—А–µ—З–љ—Л—Е —Б–≤—П–Ј–µ–є –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ I —В–Є–њ–∞;
NTX-I (Amino-terminal crosslinked telopeptide of type I collagen) вАФ –∞–Љ–Є–љ–Њ—В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л–є —В–µ–ї–Њ–њ–µ–њ—В–Є–і –њ–Њ–њ–µ—А–µ—З–љ—Л—Е —Б–≤—П–Ј–µ–є –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ I —В–Є–њ–∞;
HELP (Collagen I ќ± 1 helicoidal peptide) вАФ –Ї–Њ–ї–ї–∞–≥–µ–љ I ќ± 1 –≥–µ–ї–Є–Ї–Њ–Є–і–љ—Л–є –њ–µ–њ—В–Є–і.
–Э–µ–Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л–µ:
BSP (Bone sialoprotein) вАФ –Ї–Њ—Б—В–љ—Л–є —Б–Є–∞–ї–Њ–њ—А–Њ—В–µ–Є–љ.
–§–µ—А–Љ–µ–љ—В—Л –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–Њ–≤:
TRAcP (Tartrate-resistant acid phosphatase) вАФ —В–∞—А—В—А–∞—В-—А–µ–Ј–Є—Б—В–µ–љ—В–љ–∞—П —Й–µ–ї–Њ—З–љ–∞—П —Д–Њ—Б—Д–∞—В–∞–Ј–∞;
Cathepsins вАФ –Ї–∞—В–µ–њ—Б–Є–љ—Л.
–Ґ–µ—А–∞–њ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Ї–Њ—Б—В–µ–є
–Ф–ї—П –ї–µ—З–µ–љ–Є—П –Ї–Њ—Б—В–љ—Л—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –Љ—Г–ї—М—В–Є–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ—Л–є –њ–Њ–і—Е–Њ–і, –Ї–Њ—В–Њ—А—Л–є –≤–Ї–ї—О—З–∞–µ—В —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–µ –њ—А–Њ—В–Є–≤–Њ–Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–µ –ї–µ—З–µ–љ–Є–µ: —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—О,
–≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О, –ї—Г—З–µ–≤—Г—О —В–µ—А–∞–њ–Є—О, —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –њ–Њ—Б–Њ–±–Є—П, –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є –Є –Њ—Б—В–µ–Њ–Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–Є–µ –∞–≥–µ–љ—В—Л.
–Ю—Б—В–µ–Њ–Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–Є–µ –∞–≥–µ–љ—В—Л
–С–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В—Л
–Ь–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –Њ–±–ї–∞—Б—В–Є –±–Є–Њ–ї–Њ–≥–Є–Є –Ї–Њ—Б—В–љ—Л—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Є –±–Њ–ї–µ–µ 30 –ї–µ—В –љ–∞–Ј–∞–і —Б–Њ–Ј–і–∞—В—М –Ї–ї–∞—Б—Б –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –њ–Њ–і–∞–≤–ї—П—В—М –Ї–Њ—Б—В–љ—Г—О —А–µ–Ј–Њ—А–±—Ж–Є—О, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –љ–∞–Ј–≤–∞–љ—Л –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–∞–Љ–Є. –≠—В–Њ –∞–љ–∞–ї–Њ–≥–Є —Н–љ–і–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Є—А–Њ—Д–Њ—Б—Д–∞—В–∞ –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–∞—В—А–Є–Ї—Б–∞, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –∞—В–Њ–Љ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –Ј–∞–Љ–µ—Й–µ–љ –љ–∞ –∞—В–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є –і–ї—П —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –≥–Є–і—А–Њ–Ї—Б–Є–∞–њ–∞—В–Є—В–∞. –Э–∞–ї–Є—З–Є–µ –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≤ –±–Њ–Ї–Њ–≤–Њ–є —Ж–µ–њ–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–Њ–≤ –∞—В–Њ–Љ–∞ –∞–Ј–Њ—В–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В –Є—Е –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –њ–Њ–±–Њ—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є, –∞ –≥–Є–і—А–Њ–Ї—Б–Є–ї—М–љ—Л–є –Њ—Б—В–∞—В–Њ–Ї –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Б—А–Њ–і—Б—В–≤–Њ –Ї –Ї—А–Є—Б—В–∞–ї–ї–∞–Љ –Ї–∞–ї—М—Ж–Є—П –Є –Љ–Є–љ–µ—А–∞–ї—М–љ–Њ–Љ—Г –≤–µ—Й–µ—Б—В–≤—Г –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є. –Ь–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–Њ–≤ –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –љ–∞—А—Г—И–µ–љ–Є–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –≤–∞–ґ–љ—Л—Е —Н—В–∞–њ–Њ–≤ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–Њ–≤ вАФ –њ–Њ–і–∞–≤–ї–µ–љ–Є–Є –Є—Е –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є —Б–Њ–Ј—А–µ–≤–∞–љ–Є—П, –∞ —В–∞–Ї–ґ–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –∞–њ–Њ–њ—В–Њ–Ј–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В—Л –љ–∞—А—Г—И–∞—О—В –∞–і–≥–µ–Ј–Є—О –Њ–њ—Г—Е–Њ–ї–µ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї –Ї –Ї–Њ—Б—В–љ–Њ–Љ—Г –Љ–∞—В—А–Є–Ї—Б—Г, –њ–Њ–і–∞–≤–ї—П—О—В –Є—Е –Љ–Є–≥—А–∞—Ж–Є—О, –Є–љ–≤–∞–Ј–Є—О –Є –∞–љ–≥–Є–Њ–≥–µ–љ–µ–Ј [10, 11].
–С–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В—Л –і–µ–ї—П—В—Б—П –љ–∞ 2 –Њ—Б–љ–Њ–≤–љ—Л—Е –Ї–ї–∞—Б—Б–∞: 1) –љ–µ —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –∞–Ј–Њ—В–∞ (—Н—В–Є–і—А–Њ–љ–∞—В, –Ї–ї–Њ–і—А–Њ–љ–∞—В, —В–Є–ї—Г–і—А–Њ–љ–∞—В) –Є 2) –∞–Ј–Њ—В—Б–Њ–і–µ—А–ґ–∞—Й–Є–µ (–∞–ї–µ–љ–і—А–Њ–љ–∞—В, –Є–±–∞–љ–і—А–Њ–љ–∞—В, –њ–∞–Љ–Є–і—А–Њ–љ–∞—В, –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞).
–Э–∞–Є–±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ–∞ –Є–Ј –љ–Є—Е –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є 2 –∞—В–Њ–Љ–∞ –∞–Ј–Њ—В–∞. –Я–Њ—Б–ї–µ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –±—Л—Б—В—А–Њ –њ–µ—А–µ—А–∞—Б–њ—А–µ–і–µ–ї—П–µ—В—Б—П –≤ –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є –Є, –њ–Њ–і–Њ–±–љ–Њ –і—А—Г–≥–Є–Љ –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–∞–Љ, –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –Љ–µ—Б—В–∞—Е –µ–µ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П. –У–ї–∞–≤–љ–Њ–є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –Љ–Є—И–µ–љ—М—О –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–µ —П–≤–ї—П–µ—В—Б—П —Д–µ—А–Љ–µ–љ—В —Д–∞—А–љ–µ–Ј–Є–ї–њ–Є—А–Њ—Д–Њ—Б—Д–∞—В—Б–Є–љ—В–µ—В–∞–Ј–∞ (–§–Я–°), –њ—А–Є —Н—В–Њ–Љ –љ–µ –Є—Б–Ї–ї—О—З–∞–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –і—А—Г–≥–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –і–µ–є—Б—В–≤–Є—П –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –і–µ–є—Б—В–≤–Є—П —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –≤—Л—Б–Њ–Ї–Є–Љ –∞—Д—Д–Є–љ–Є—В–µ—В–Њ–Љ –Ї –∞–Ї—В–Є–≤–љ–Њ–Љ—Г —Ж–µ–љ—В—А—Г –§–Я–° –Є –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Б—А–Њ–і—Б—В–≤–Њ–Љ –Ї –Љ–Є–љ–µ—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є [12].
–Я–Њ–Љ–Є–Љ–Њ –Є–љ–≥–Є–±–Є—А—Г—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–∞ —А–µ–Ј–Њ—А–±—Ж–Є—О –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Њ–±–ї–∞–і–∞–µ—В –њ—А–Њ—В–Є–≤–Њ–Њ–њ—Г—Е–Њ–ї–µ–≤—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–Љ–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –Љ–µ—В–∞—Б—В–∞–Ј–∞—Е –≤ –Ї–Њ—Б—В–Є.
–Ч–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ in vivo: –Є–љ–≥–Є–±–Є—А—Г–µ—В —А–µ–Ј–Њ—А–±—Ж–Є—О –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–∞–Љ–Є, –Є–Ј–Љ–µ–љ—П–µ—В –Љ–Є–Ї—А–Њ—Б—А–µ–і—Г –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–Њ—Б—В–∞ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї, –њ—А–Њ—П–≤–ї—П–µ—В –∞–љ—В–Є–∞–љ–≥–Є–Њ–≥–µ–љ–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М. –Я–Њ–і–∞–≤–ї–µ–љ–Є–µ –Ї–Њ—Б—В–љ–Њ–є —А–µ–Ј–Њ—А–±—Ж–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –±–Њ–ї–µ–≤—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є.
–Ч–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ in vitro: –Є–љ–≥–Є–±–Є—А—Г–µ—В –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –Њ—Б—В–µ–Њ–±–ї–∞—Б—В–Њ–≤, –њ—А–Њ—П–≤–ї—П–µ—В –њ—А—П–Љ—Г—О —Ж–Є—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї—Г—О –Є –њ—А–Њ–∞–њ–Њ–њ—В–Њ—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Є —Б–Є–љ–µ—А–≥–Є—З–љ—Л–є —Ж–Є—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –≤–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–Є —Б –њ—А–Њ—В–Є–≤–Њ–Њ–њ—Г—Е–Њ–ї–µ–≤—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –∞–љ—В–Є–∞–і–≥–µ–Ј–Є–≤–љ—Г—О –Є –∞–љ—В–Є–Є–љ–≤–∞–Ј–Є–≤–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М. –Ч–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –њ–Њ–і–∞–≤–ї—П—П –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –Є –Є–љ–і—Г—Ж–Є—А—Г—П –∞–њ–Њ–њ—В–Њ–Ј, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–µ –њ—А–Њ—В–Є–≤–Њ–Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ъ–Ь –Є –†–Ь–Ц, –∞ —В–∞–Ї–ґ–µ —Г–Љ–µ–љ—М—И–∞–µ—В –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Ї–ї–µ—В–Њ–Ї –†–Ь–Ц —З–µ–ї–Њ–≤–µ–Ї–∞ —З–µ—А–µ–Ј —Н–Ї—Б—В—А–∞—Ж–µ–ї–ї—О–ї—П—А–љ—Л–є –Љ–∞—В—А–Є–Ї—Б, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –љ–∞–ї–Є—З–Є–Є —Г –љ–µ–µ –∞–љ—В–Є–Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Є–љ–≥–Є–±–Є—А—Г–µ—В –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –Ї–ї–µ—В–Њ–Ї —Н–љ–і–Њ—В–µ–ї–Є—П —З–µ–ї–Њ–≤–µ–Ї–∞ –Є –ґ–Є–≤–Њ—В–љ—Л—Е –Є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –∞–љ—В–Є–∞–љ–≥–Є–Њ–≥–µ–љ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Э–∞ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–Њ–і–µ–ї—П—Е —Г—Б–Ї–Њ—А–µ–љ–љ–Њ–є –Њ—Б—В–µ–Њ—А–µ–Ј–Њ—А–±—Ж–Є–Є –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Њ–љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Є–љ–≥–Є–±–Є—А—Г–µ—В –Ї–Њ—Б—В–љ—Г—О —А–µ–Ј–Њ—А–±—Ж–Є—О –±–µ–Ј –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ, –Љ–Є–љ–µ—А–∞–ї–Є–Ј–∞—Ж–Є—О –Є –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є, –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–Њ–≤ –Є —З–∞—Б—В–Њ—В—Г –∞–Ї—В–Є–≤–∞—Ж–Є–Є –љ–Њ–≤—Л—Е –Њ—З–∞–≥–Њ–≤ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П –Ї–∞–Ї –≤ —В—А–∞–±–µ–Ї—Г–ї—П—А–љ–Њ–є (–≥—Г–±—З–∞—В–Њ–є), —В–∞–Ї –Є –≤ –Ї–Њ—А—В–Є–Ї–∞–ї—М–љ–Њ–є (–Ї–Њ–Љ–њ–∞–Ї—В–љ–Њ–є) –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є, –љ–µ –≤—Л–Ј—Л–≤–∞—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –≤–Њ–ї–Њ–Ї–љ–Є—Б—В–Њ–є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є –Є –∞–±–µ—А—А–∞–љ—В–љ–Њ–є –∞–Ї–Ї—Г–Љ—Г–ї—П—Ж–Є–Є –Њ—Б—В–µ–Њ–Є–і–∞, –∞ —В–∞–Ї–ґ–µ –і–µ—Д–µ–Ї—В–Њ–≤ –Љ–Є–љ–µ—А–∞–ї–Є–Ј–∞—Ж–Є–Є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є [12].
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –†–Ь–Ц, –†–Я–Ц –Є –і—А—Г–≥–Є–Љ–Є —Б–Њ–ї–Є–і–љ—Л–Љ–Є –Њ–њ—Г—Е–Њ–ї—П–Љ–Є —Б –Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤, –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, —Б–љ–Є–ґ–∞–µ—В –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –ї—Г—З–µ–≤–Њ–є —В–µ—А–∞–њ–Є–Є –Є –Њ–њ–µ—А–∞—В–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞—Е, —Г–Љ–µ–љ—М—И–∞–µ—В –Њ–њ—Г—Е–Њ–ї–µ–≤—Г—О –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є—О. –Я—А–µ–њ–∞—А–∞—В –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 4 –Љ–≥ —Б–њ–Њ—Б–Њ–±–µ–љ —Б–і–µ—А–ґ–Є–≤–∞—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В–µ–Њ¬≠–±–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—З–∞–≥–∞–Љ–Є –ї–µ—З–µ–±–љ—Л–є —Н—Д—Д–µ–Ї—В –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ, —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—З–∞–≥–∞–Љ–Є [12].
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –Љ–Є–µ–ї–Њ–Љ–Њ–є –Є –†–Ь–Ц –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Ї–∞–Ї –Љ–Є–љ–Є–Љ—Г–Љ –Њ–і–љ–Њ–≥–Њ –Ї–Њ—Б—В–љ–Њ–≥–Њ –Њ—З–∞–≥–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 4 –Љ–≥ —Б—А–∞–≤–љ–Є–Љ–∞ —Б —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ–∞–Љ–Є–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 90 –Љ–≥.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–є –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–µ–є –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 4 –Љ–≥ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ї–∞–ї—М—Ж–Є—П –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –Є –≤—Л–≤–µ–і–µ–љ–Є—П –Ї–∞–ї—М—Ж–Є—П –њ–Њ—З–Ї–∞–Љ–Є. –°—А–µ–і–љ–µ–µ –≤—А–µ–Љ—П –і–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ї–∞–ї—М—Ж–Є—П —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 4 –і–љ–µ–є. –Ъ 10-–Љ—Г –і–љ—О —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ї–∞–ї—М—Ж–Є—П –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В—Б—П —Г 87вАУ88% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –°—А–µ–і–љ–µ–µ –≤—А–µ–Љ—П –і–Њ —А–µ—Ж–Є–і–Є–≤–∞ (—Б–Ї–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–∞–љ–љ–Њ–µ –њ–Њ –∞–ї—М–±—Г–Љ–Є–љ—Г —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ї–∞–ї—М—Ж–Є—П —Б—Л–≤–Њ—А–Њ—В–Ї–Є –Ї—А–Њ–≤–Є –љ–µ –Љ–µ–љ–µ–µ 2,9 –Љ–Љ–Њ–ї—М/–ї) —Б–Њ—Б—В–∞–≤–ї—П–µ—В 30вАУ40 –і–љ–µ–є. –Ч–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–∞—Е 4 –Є 8 –Љ–≥ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–Є –љ–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П [12].
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ —З–∞—Б—В–Њ—В–µ –Є —В—П–ґ–µ—Б—В–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є, –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г –≤ –і–Њ–Ј–∞—Е 4 –Љ–≥, 8 –Љ–≥, –њ–∞–Љ–Є–і—А–Њ–љ–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г –≤ –і–Њ–Ј–µ 90 –Љ–≥ –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ, –Ї–∞–Ї –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –≤ –Ї–Њ—Б—В–Є, —В–∞–Ї –Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–Є.
–Я—А–Є –љ–∞—А—Г—И–µ–љ–Є–Є –Ь–Я–Ъ–Ґ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—П –Љ–µ–љ–Њ–њ–∞—Г–Ј—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –±—Л—Б—В—А–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–Њ—Б—В–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л—Е –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –і–Њ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ –і–Њ–њ—Г—Б—В–Є–Љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П (–Ї 7-–Љ—Г –і–љ—О –і–ї—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–Њ—Б—В–љ–Њ–є —А–µ–Ј–Њ—А–±—Ж–Є–Є –Є –Ї 12-–є –љ–µ–і. –і–ї—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–Њ—Б—В–љ–Њ–≥–Њ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П). –Т–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ї–Њ—Б—В–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —Б—В–∞–±–Є–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є—Б—М –≤ –њ—А–µ–і–µ–ї–∞—Е –њ—А–µ–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є, —З—В–Њ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ –≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –љ–∞ 70% –Ї –Ї–Њ–љ—Ж—Г 3-–≥–Њ –≥–Њ–і–∞ –ї–µ—З–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—О —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Њ–і–љ–Њ–≥–Њ –Є–ї–Є –±–Њ–ї–µ–µ –љ–Њ–≤—Л—Е/–њ–Њ–≤—В–Њ—А–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –Є –≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ —Б—А–µ–і–љ–µ–є/—В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є –љ–∞ 60вАУ70%. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 75 –ї–µ—В –Є —Б—В–∞—А—И–µ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ –і–Њ—Б—В–Є–≥–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –љ–∞ 61%. –Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –±–µ–і—А–µ–љ–љ–Њ–є –Ї–Њ—Б—В–Є –Ї 3-–Љ—Г –≥–Њ–і—Г —В–µ—А–∞–њ–Є–Є —Б–љ–Є–ґ–∞–ї—Б—П –љ–∞ 40%, –њ—А–Є —Н—В–Њ–Љ —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –ї—О–±—Л—Е –і—А—Г–≥–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –Є –љ–µ–≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –ї—О–±–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є (–Є—Б–Ї–ї—О—З–∞—П –њ–µ—А–µ–ї–Њ–Љ—Л —Д–∞–ї–∞–љ–≥ –њ–∞–ї—М—Ж–µ–≤ –Є –Ї–Њ—Б—В–µ–є –ї–Є—Ж–µ–≤–Њ–є —З–∞—Б—В–Є —З–µ—А–µ–њ–∞) —Б–љ–Є–ґ–∞–ї—Б—П –љ–∞ 33 –Є 25% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [12].
–Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —В–µ—З–µ–љ–Є–µ 3 –ї–µ—В —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л–Љ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ь–Я–Ъ–Ґ –њ–Њ—П—Б–љ–Є—З–љ—Л—Е –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤, –±–µ–і—А–µ–љ–љ–Њ–є –Ї–Њ—Б—В–Є –≤ —Ж–µ–ї–Њ–Љ, –Њ–±–ї–∞—Б—В–Є —И–µ–є–Ї–Є –±–µ–і—А–µ–љ–љ–Њ–є –Ї–Њ—Б—В–Є –Є –і–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –ї—Г—З–µ–≤–Њ–є –Ї–Њ—Б—В–Є –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 6,9, 6,0, 5,0 –Є 3,2% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ—Б—В–љ–Њ–≥–Њ –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–∞ —Й–µ–ї–Њ—З–љ–Њ–є —Д–Њ—Б—Д–∞—В–∞–Ј—Л, N-–Ї–Њ–љ—Ж–µ–≤–Њ–≥–Њ –њ—А–Њ–њ–µ–њ—В–Є–і–∞ –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ I —В–Є–њ–∞ (PINP) –Є ќ≤-–°-–Ї–Њ–љ—Ж–µ–≤—Л—Е —В–µ–ї–Њ–њ–µ–њ—В–Є–і–Њ–≤ –Ї—А–Њ–≤–Є –і–Њ –њ—А–µ–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П. –Я—А–Є –њ–Њ–≤—В–Њ—А–љ—Л—Е –≤–≤–µ–і–µ–љ–Є—П—Е –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —В–µ—З–µ–љ–Є–µ 3 –ї–µ—В –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –≤ –Ї—А–Њ–≤–Є —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Љ–∞—А–Ї–µ—А–Њ–≤ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ—Б—В–Є, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ –њ–Њ–≤—Л—И–µ–љ–Є—О —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –≤ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–µ —Б –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –Є –≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л–Љ–Є –њ–µ—А–µ–ї–Њ–Љ–∞–Љ–Є.
–Я—А–Є –≤–≤–µ–і–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ (–њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–µ–Љ–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ) –њ–∞—Ж–Є–µ–љ—В–∞–Љ вАФ –Љ—Г–ґ—З–Є–љ–∞–Љ –Є –ґ–µ–љ—Й–Є–љ–∞–Љ —Б –љ–µ–і–∞–≤–љ–Є–Љ–Є (–≤ —В–µ—З–µ–љ–Є–µ 90 –і–љ–µ–є) –њ–µ—А–µ–ї–Њ–Љ–∞–Љ–Є –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –±–µ–і—А–µ–љ–љ–Њ–є –Ї–Њ—Б—В–Є (–≤–Њ–Ј–љ–Є–Ї—И–Є–Љ–Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є —В—А–∞–≤–Љ—Л –Є —В—А–µ–±–Њ–≤–∞–≤—И–Є–Љ–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞) –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е –Њ—Б—В–µ–Њ–њ–Њ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ –ї—О–±–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –љ–∞ 35% (–Є–Ј –љ–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ вАФ –љ–∞ 46%, –љ–µ–≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е –њ–µ—А–µ–ї–Њ–Љ–Њ–≤ вАФ –љ–∞ 27%), –∞ —В–∞–Ї–ґ–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ –ї–µ—В–∞–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ (–љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –µ–≥–Њ –њ—А–Є—З–Є–љ—Л) –љ–∞ 28%. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–µ—А–µ–ї–Њ–Љ–∞–Љ–Є –±–µ–і—А–µ–љ–љ–Њ–є –Ї–Њ—Б—В–Є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ –≤ —В–µ—З–µ–љ–Є–µ 2 –ї–µ—В –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ь–Я–Ъ–Ґ –±–µ–і—А–µ–љ–љ–Њ–є –Ї–Њ—Б—В–Є –≤ —Ж–µ–ї–Њ–Љ –Є –≤ –Њ–±–ї–∞—Б—В–Є —И–µ–є–Ї–Є –±–µ–і—А–µ–љ–љ–Њ–є –Ї–Њ—Б—В–Є –љ–∞ 5,4 –Є 4,3% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [12].
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ, –≤—Л–Ј–≤–∞–љ–љ—Л–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤, —В–µ—А–∞–њ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ –≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞ —В–∞–Ї–ґ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞ –Ь–Я–Ъ–Ґ (–њ–Њ—П—Б–љ–Є—З–љ—Л—Е –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤, —И–µ–є–Ї–Є –±–µ–і—А–∞, –≤–µ—А—В–µ–ї–∞, –ї—Г—З–µ–≤–Њ–є –Ї–Њ—Б—В–Є), –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞—П –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —Б—В—А—Г–Ї—В—Г—А—Г –Є –Љ–Є–љ–µ—А–∞–ї–Є–Ј–∞—Ж–Є—О –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є.
–Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –Њ—Б—В–µ–Њ¬≠–њ–Њ—А–Њ–Ј–∞ 1 —А–∞–Ј –≤ 2 –≥–Њ–і–∞ —Г –ґ–µ–љ—Й–Є–љ —Б –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј—Л –Љ–µ–љ–µ–µ –Є –±–Њ–ї–µ–µ 5 –ї–µ—В –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ь–Я–Ъ–Ґ –њ–Њ—П—Б–љ–Є—З–љ—Л—Е –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤ –љ–∞ 6,3 –Є 5,4% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Я—А–Є –≤–≤–µ–і–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ 1 —А–∞–Ј –≤ 2 –≥–Њ–і–∞ –Ь–Я–Ъ–Ґ –±–µ–і—А–µ–љ–љ–Њ–є –Ї–Њ—Б—В–Є —Г–≤–µ–ї–Є—З–Є–ї–∞—Б—М –љ–∞ 4,7 –Є 3,2% —Г –ґ–µ–љ—Й–Є–љ —Б –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј—Л –Љ–µ–љ–µ–µ –Є –±–Њ–ї–µ–µ 5 –ї–µ—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [12].
–£ –ґ–µ–љ—Й–Є–љ —Б —А–∞–Ј–ї–Є—З–љ–Њ–є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј—Л –њ—А–Є –≤–≤–µ–і–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ 1 —А–∞–Ј –≤ 2 –≥–Њ–і–∞ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є ќ≤-–°-–Ї–Њ–љ—Ж–µ–≤—Л—Е —В–µ–ї–Њ–њ–µ–њ—В–Є–і–Њ–≤ –Ї—А–Њ–≤–Є –љ–∞ 44вАУ46% (–і–Њ –њ—А–µ–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П) –Є N-–Ї–Њ–љ—Ж–µ–≤–Њ–≥–Њ –њ—А–Њ–њ–µ–њ—В–Є–і–∞ –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ I —В–Є–њ–∞ (PINP) –љ–∞ 55вАУ40%.
–Я—А–Є –ї–µ—З–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–Њ—Б—В–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –Я–µ–і–ґ–µ—В–∞ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–є, –±—Л—Б—В—А—Л–є –Є –і–ї–Є—В–µ–ї—М–љ—Л–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є –Њ—В–≤–µ—В, –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Й–µ–ї–Њ—З–љ–Њ–є —Д–Њ—Б—Д–∞—В–∞–Ј—Л –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є.
–Я—А–µ–њ–∞—А–∞—В –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ —В–∞–Ї–ґ–µ –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–µ–љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —А–∞–љ–µ–µ –ї–µ—З–µ–љ–Є–µ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ–Є –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–∞–Љ–Є. –Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є –Њ—В–≤–µ—В –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –і–Њ–ї—М—И–µ, —З–µ–Љ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —А–Є–Ј–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (7,7 –≥–Њ–і–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 5,1 –≥–Њ–і–∞) [12].
–Т—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –љ–∞ 6-–Љ –Љ–µ—Б. –њ–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 5 –Љ–≥ —Б—А–∞–≤–љ–Є–Љ–Њ —Б –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ —А–Є–Ј–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 30 –Љ–≥/—Б—Г—В.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л–Љ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–Њ–Љ –Є –±–Њ–ї–µ–Ј–љ—М—О –Я–µ–і–ґ–µ—В–∞ –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –љ–µ –≤–ї–Є—П–µ—В –љ–∞ –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є, –љ–µ –љ–∞—А—Г—И–∞–µ—В –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Ї–Њ—Б—В–љ–Њ–≥–Њ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П –Є –Љ–Є–љ–µ—А–∞–ї–Є–Ј–∞—Ж–Є–Є –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–Њ—Е—А–∞–љ–µ–љ–Є—О –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –∞—А—Е–Є—В–µ–Ї—В–Њ–љ–Є–Ї–Є —В—А–∞–±–µ–Ї—Г–ї—П—А–љ–Њ–є –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є.
–Я–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В—Л —В–∞–Ї–ґ–µ –Њ—В–ї–Є—З–∞—О—В—Б—П: –і–ї—П –њ–µ—А–Њ—А–∞–ї—М–љ—Л—Е —Е–∞—А–∞–Ї—В–µ—А–љ—Л –љ–Є–Ј–Ї–∞—П –≤—Б–∞—Б—Л–≤–∞–µ–Љ–Њ—Б—В—М (0,5вАУ4%) –≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–Љ —В—А–∞–Ї—В–µ, –і–Є–∞—А–µ—П, —Н–Ј–Њ—Д–∞–≥–Є—В, —В–Њ—И–љ–Њ—В–∞. –Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –њ–Њ–±–Њ—З–љ—Л–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —П–≤–ї—П—О—В—Б—П –Њ—Б—В—А—Л–µ —А–µ–∞–Ї—Ж–Є–Є: –≥—А–Є–њ–њ–Њ–њ–Њ–і–Њ–±–љ—Л–є —Б–Є–љ–і—А–Њ–Љ, –∞—А—В—А–∞–ї–≥–Є—П, –Љ–Є–∞–ї–≥–Є—П. –Ъ –Њ—В—Б—А–Њ—З–µ–љ–љ—Л–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –≥–Є–њ–Њ–Ї–∞–ї—М—Ж–Є–µ–Љ–Є—П, –≥–Є–њ–Њ—Д–Њ—Б—Д–∞—В–µ–Љ–Є—П. –Я–Њ—З–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –Ї–Њ—В–Њ—А–∞—П –Ј–∞—З–∞—Б—В—Г—О –Ј–∞–≤–Є—Б–Є—В –Њ—В –і–Њ–Ј—Л –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞, –Љ–Њ–ґ–µ—В –±—Л—В—М –Ї–∞–Ї –Њ—Б—В—А–Њ–є, —В–∞–Ї –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є. –Ю–і–љ–Є–Љ –Є–Ј —Б–µ—А—М–µ–Ј–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –∞–Ј–Њ—В—Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Њ—Б—В–µ–Њ–љ–µ–Ї—А–Њ–Ј –љ–Є–ґ–љ–µ–є —З–µ–ї—О—Б—В–Є, —З–∞—Й–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є –Є –Ј–∞–≤–Є—Б–Є—В –Њ—В –µ–µ –Ї—Г–Љ—Г–ї—П—В–Є–≤–љ–Њ–є –і–Њ–Ј—Л.
–Ф–ї—П —Б–љ–Є–ґ–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –њ–µ—А–µ–і –љ–∞—З–∞–ї–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–њ—А–µ–і–µ–ї—П—В—М —Г—А–Њ–≤–µ–љ—М –Ї–∞–ї—М—Ж–Є—П, –≤–Є—В–∞–Љ–Є–љ–∞ D –Є –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є. –Ґ–∞–Ї–ґ–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є—П —Б—В–Њ–Љ–∞—В–Њ–ї–Њ–≥–∞ –Є —Б–∞–љ–∞—Ж–Є—П –њ–Њ–ї–Њ—Б—В–Є —А—В–∞.
–Я—А–µ–њ–∞—А–∞—В—Л –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л—Е –∞–љ—В–Є—В–µ–ї
–Ф—А—Г–≥–Є–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –Њ—В–љ–Њ—Б—П—Й–Є–Љ—Б—П –Ї –≥—А—Г–њ–њ–µ –Њ—Б—В–µ–Њ–Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–Є—Е –∞–≥–µ–љ—В–Њ–≤ (–Ю–Ь–Р), —П–≤–ї—П–µ—В—Б—П –і–µ–љ–Њ—Б—Г–Љ–∞–±. –Ю–љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –њ–Њ–ї–љ–Њ—Б—В—М—О —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–µ –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ–Њ–µ –∞–љ—В–Є—В–µ–ї–Њ, –Њ–±–ї–∞–і–∞—О—Й–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –∞—Д–Є–љ–љ–Њ—Б—В—М—О –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М—О –Ї —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–Љ—Г RANK-–ї–Є–≥–∞–љ–і—Г (RANKL). –°–≤—П–Ј—Л–≤–∞—П—Б—М —Б RANKL, –і–µ–љ–Њ—Б—Г–Љ–∞–± –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В –µ–≥–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ —Б —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ RANK –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–Њ–≤ –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –∞–Ї—В–Є–≤–∞—Ж–Є—О —П–і–µ—А–љ–Њ–≥–Њ —В—А–∞–љ—Б–Ї—А–Є–њ—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ NF-ќЇB, —З—В–Њ –њ–Њ–і–∞–≤–ї—П–µ—В –њ—А–Њ—Ж–µ—Б—Б —Б–Њ–Ј—А–µ–≤–∞–љ–Є—П, —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –Є –≤—Л–ґ–Є–≤–∞–љ–Є—П –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–Њ–≤ вАФ –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —В–Є–њ–∞ –Ї–ї–µ—В–Њ–Ї, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л—Е –Ј–∞ –Ї–Њ—Б—В–љ—Г—О —А–µ–Ј–Њ—А–±—Ж–Є—О. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –і–µ–љ–Њ—Б—Г–Љ–∞–± —Г–Љ–µ–љ—М—И–∞–µ—В —А–µ–Ј–Њ—А–±—Ж–Є—О –Є –і–µ—Б—В—А—Г–Ї—Ж–Є—О –Ї–Њ—Б—В–љ–Њ–є —В–Ї–∞–љ–Є, –і–µ–є—Б—В–≤—Г—П –∞–љ–∞–ї–Њ–≥–Є—З–љ–Њ –љ–∞—В—Г—А–∞–ї—М–љ–Њ–Љ—Г –±–µ–ї–Ї—Г –Њ—Б—В–µ–Њ–њ—А–Њ—В–µ–≥–µ—А–Є–љ—Г.
–†–∞–љ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–µ–љ–Њ—Б—Г–Љ–∞–±–∞ (I, II —Д–∞–Ј—Л) –њ–Њ–Ї–∞–Ј–∞–ї–Є –±—Л—Б—В—А—Г—О –∞–±—Б–Њ—А–±—Ж–Є—О —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј –њ—А–µ–њ–∞—А–∞—В–∞, –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П 30вАУ46 –і–љ–µ–є, –Њ—В—Б—Г—В—Б—В–≤–Є–µ –љ–µ–є—В—А–∞–ї–Є–Ј—Г—О—Й–Є—Е –∞–љ—В–Є—В–µ–ї –Ї –њ—А–µ–њ–∞—А–∞—В—Г. –Ю–њ—В–Є–Љ–∞–ї—М–љ—Л–Љ –њ—А–Є–Ј–љ–∞–љ —А–µ–ґ–Є–Љ –≤–≤–µ–і–µ–љ–Є—П –і–µ–љ–Њ—Б—Г–Љ–∞–±–∞ –њ–Њ 120 –Љ–≥ –њ–Њ–і–Ї–Њ–ґ–љ–Њ 1 —А–∞–Ј –≤ 4 –љ–µ–і. –Т–Њ II —Д–∞–Ј–µ –≤—Л—П–≤–ї–µ–љ–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –∞–Ї—В–Є–≤–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ (–Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞) –њ—А–Є –Њ—В—Б—А–Њ—З–µ–љ–љ—Л—Е –Ї–Њ—Б—В–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П—Е –Є —Б–љ–Є–ґ–µ–љ–Є–Є –Љ–∞—А–Ї–µ—А–∞ –Ї–Њ—Б—В–љ–Њ–є —А–µ–Ј–Њ—А–±—Ж–Є–Є, –∞ —В–∞–Ї–ґ–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –њ—А–Њ—Д–Є–ї—М –µ–≥–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є [13вАУ15]. –Ш–љ—В–µ–≥—А–∞–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј 3 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є III —Д–∞–Ј—Л, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –њ–Њ –Њ–і–љ–Њ–Љ—Г –і–Є–Ј–∞–є–љ—Г –Є –≤–Ї–ї—О—З–Є–≤—И–Є—Е 5726 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г—Б—В–∞–љ–Њ–≤–Є–ї, —З—В–Њ –і–µ–љ–Њ—Б—Г–Љ–∞–± –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—П –њ–µ—А–≤–Њ–≥–Њ –≤ —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –°–°–Ъ–° –љ–∞ 17% –њ—А–Є –≤—Б–µ—Е —В–Є–њ–∞—Е –Њ–њ—Г—Е–Њ–ї–µ–є (p<0,001) [15]. –Я–Њ–Ї–∞–Ј–∞–љ–Њ –µ–≥–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –њ—А–Є –†–Ь–Ц –Є –†–Я–Ц: —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –њ–µ—А–≤–Њ–≥–Њ –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е –°–°–Ъ–° —Б–љ–Є–ґ–∞–µ—В—Б—П –љ–∞ 18% (p<0,001). –Я—А–Є –ї–µ—З–µ–љ–Є–Є –і–µ–љ–Њ—Б—Г–Љ–∞–±–Њ–Љ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ (p<0,01).
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П (–Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞) –њ—А–µ–Њ–±–ї–∞–і–∞–ї–Є –Њ—Б—В—А—Л–µ —А–µ–∞–Ї—Ж–Є–Є: 20,2% –њ—А–Њ—В–Є–≤ 8,7%. –Я–Њ—З–µ—З–љ–∞—П —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М –Є –љ–µ–Ї—А–Њ–Ј –љ–Є–ґ–љ–µ–є —З–µ–ї—О—Б—В–Є –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —З–∞—Б—В–Њ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е: 11,8% –њ—А–Њ—В–Є–≤ 9,2% –Є 1,3% –њ—А–Њ—В–Є–≤ 1,8% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Ґ–∞–Ї–ґ–µ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —З–∞—Б—В–Њ –Њ—В–Љ–µ—З–µ–љ—Л —Б–µ—А—М–µ–Ј–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е: 57,1% –њ—А–Њ—В–Є–≤ 56,3% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [16]. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Є–љ—В–µ–≥—А–∞–ї—М–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –≤—А–µ–Љ—П –±–µ–Ј –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Є –Њ–±—Й–∞—П –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –≤ –≥—А—Г–њ–њ–∞—Е –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М [17]. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –і–µ—В–∞–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–µ –±–Њ–ї—М–љ—Л—Е —А–∞–Ї–Њ–Љ –ї–µ–≥–Ї–Њ–≥–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є –љ–∞ 20% (—А=0,01), –∞ –≤ –њ–Њ–і–≥—А—Г–њ–њ–µ –љ–µ–Љ–µ–ї–Ї–Њ–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ —А–∞–Ї–∞ вАФ –љ–∞ 22% (—А=0,0104) —Г –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –і–µ–љ–Њ—Б—Г–Љ–∞–±. –Я—А–Є —Н—В–Њ–Љ —А–∞–Ј–љ–Є—Ж–∞ –≤ –Њ–±—Й–µ–є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–љ–Є–ґ–µ–љ–Є–Є —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є –љ–∞ 32% –і–Њ—Б—В–Є–≥–љ—Г—В–∞ –Ј–∞ —Б—З–µ—В –±–Њ–ї—М–љ—Л—Е —Б –њ–ї–Њ—Б–Ї–Њ–Ї–ї–µ—В–Њ—З–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ь–µ–і–Є–∞–љ–∞ –Њ–±—Й–µ–є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є –љ–∞ –і–µ–љ–Њ—Б—Г–Љ–∞–±–µ –Є –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 8,6 –Љ–µ—Б. –Є 6,4 –Љ–µ—Б. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А=0,0350; –Ю–† (–Њ—В–љ–Њ—И–µ–љ–Є–µ —А–Є—Б–Ї–Њ–≤) 0,68). –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –≤ –≤–Є–і–µ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Њ–±—Й–µ–є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є –Љ–Њ–≥—Г—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ–Љ RANKL –Є –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Є–Ї—А–Њ–Њ–Ї—А—Г–ґ–µ–љ–Є—П, —Б –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л вАФ –њ—А—П–Љ—Л–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–µ –Ї–ї–µ—В–Ї–Є, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є –љ–µ–Љ–µ–ї–Ї–Њ–Ї–ї–µ—В–Њ—З–љ–Њ–Љ —А–∞–Ї–µ —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г—О—В —А–µ—Ж–µ–њ—В–Њ—А—Л RANK –Є RANKL [18].
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –Ї–Њ—Б—В–љ—Л–Љ–Є –Љ–µ—В–∞—Б—В–∞–Ј–∞–Љ–Є –Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Њ–њ—Г—Е–Њ–ї–µ–є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —А–∞—Б—И–Є—А–Є–ї–Є—Б—М —Б –≤–љ–µ–і—А–µ–љ–Є–µ–Љ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –Ю–Ь–Р. –Ч–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ (–≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л–є –∞–Ј–Њ—В—Б–Њ–і–µ—А–ґ–∞—Й–Є–є –±–Є—Б—Д–Њ—Б—Д–Њ–љ–∞—В —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П) –Є –і–µ–љ–Њ—Б—Г–Љ–∞–± —П–≤–ї—П—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Є –≤—Б–µ—Е —В–Є–њ–∞—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ (–ї–Є—В–Є—З–µ—Б–Ї–Є–µ, –±–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–µ, —Б–Љ–µ—И–∞–љ–љ—Л–µ), –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –Њ–њ—Г—Е–Њ–ї—М—О, –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–µ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –њ–Њ–і–∞–≤–ї—П—В—М –Њ–њ—Г—Е–Њ–ї–µ–≤—Л–є —А–Њ—Б—В in vitro –Є in vivo, –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞—В—М –∞–њ–Њ–њ—В–Њ–Ј, –њ–Њ–і–∞–≤–ї—П—В—М –∞–љ–≥–Є–Њ–≥–µ–љ–µ–Ј –≤ –Њ–њ—Г—Е–Њ–ї–Є.
–Ю–Ь–Р —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –Ї–Њ—Б—В–љ—Л—Е –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –Є –њ—А–Є–Љ–µ–љ—П—В—М –і–ї–Є—В–µ–ї—М–љ–Њ, –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –≤–Є–і–∞–Љ–Є –ї–µ—З–µ–љ–Є—П (—Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є—П, –≥–Њ—А–Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П, –ї—Г—З–µ–≤–∞—П —В–µ—А–∞–њ–Є—П).
–Ь–Њ–љ–Є—В–Њ—А–Є–љ–≥ –Љ–∞—А–Ї–µ—А–Њ–≤ –Ї–Њ—Б—В–љ–Њ–є —А–µ–Ј–Њ—А–±—Ж–Є–Є (NTX, –Ї–Њ—Б—В–љ–∞—П —Й–µ–ї–Њ—З–љ–∞—П —Д–Њ—Б—Д–∞—В–∞–Ј–∞), –Ї–Њ—В–Њ—А—Л–µ —Б–љ–Є–ґ–∞—О—В—Б—П –Є–ї–Є –љ–Њ—А–Љ–∞–ї–Є–Ј—Г—О—В—Б—П –њ—А–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ –і–ї—П –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–≥–Њ –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П —В–µ—А–∞–њ–Є–Є –Ю–Ь–Р, –њ—А–Њ–≥–љ–Њ–Ј–∞ –Њ—В–≤–µ—В–∞ –љ–∞ –ї–µ—З–µ–љ–Є–µ –Є –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Њ–і–Њ–ї–ґ–∞—О—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ю–Ь–Р –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –≤ –Ї–Њ—Б—В–Є —А–∞–љ–љ–µ–≥–Њ –†–Ь–Ц, –†–Я–Ц –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–∞–Ј–≤–Є—В–Є—П –Њ—Б—В–µ–Њ–њ–µ–љ–Є–Є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П (–Є–љ–≥–Є–±–Є—В–Њ—А—Л –∞—А–Њ–Љ–∞—В–∞–Ј—Л, –∞–љ–і—А–Њ–≥–µ–љ–љ–∞—П –±–ї–Њ–Ї–∞–і–∞).
–Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Ю–Ь–Р, –≤ —В. —З. –Ј–Њ–ї–µ–і—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ—Л –≤ –†–§, –°–®–Р –Є –µ–≤—А–Њ–њ–µ–є—Б–Ї–Є—Е —Б—В—А–∞–љ–∞—Е –Ї–∞–Ї –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Љ–µ—В–∞—Б—В–∞–Ј–Њ–≤ –≤ –Ї–Њ—Б—В–Є –†–Ь–Ц –Є –†–Я–Ц, —А–∞–Ї–∞ –ї–µ–≥–Ї–Њ–≥–Њ, –њ–Њ—З–Ї–Є, –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –Љ–Є–µ–ї–Њ–Љ—Л –Є –і—А—Г–≥–Є—Е —Б–Њ–ї–Є–і–љ—Л—Е –Њ–њ—Г—Е–Њ–ї–µ–є, –∞ —В–∞–Ї–ґ–µ –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Є–љ–µ—А–∞–ї—М–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —Г –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е: –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–∞ –Є –≥–Є–њ–µ—А–Ї–∞–ї—М—Ж–Є–µ–Љ–Є–Є, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б –Њ–њ—Г—Е–Њ–ї—М—О.












