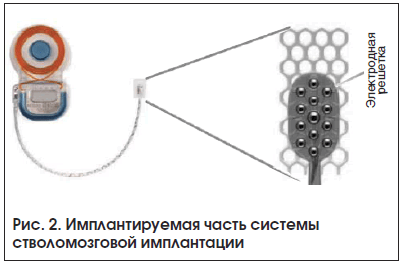
Система слуховой СМИ (ABI, auditory brainstem implant) состоит из 2-х частей и представляет собой модифицированный кохлеарный имплантат, предназначенный для электрической стимуляции кохлеарных ядер ствола мозга в обход улитки, и речевой процессор (рис. 1, 2) [6].

Показаниями для операции слуховой СМИ является сенсоневральная тугоухость IV степени, вызванная ретрокохлеарной патологией, либо прогнозируемая глухота после нейрохирургической операции [7]. Основными причинами, наиболее часто вызывающими двустороннее поражение корешков VIII нерва, является нейрофиброматоз 2-го типа, травматическое повреждение волокон слухового нерва, вызванное переломом основания черепа, хирургическими операциями и т. д., или врожденное отсутствие слуховых нервов – аплазия с двух сторон [8]. Нейрофиброматоз 2-го типа – это наследственное заболевание, представляющее собой множественные, обычно доброкачественные опухоли оболочки нервной ткани [9, 10]. В процессе развития заболевания у пациентов могут возникать двусторонние невриномы слухового нерва. Это доброкачественные опухоли, растущие из швановских оболочек слухового нерва [11, 12]. Другим показанием к слуховой СМИ является полная облитерация или аплазия улиток височных костей с двух сторон. В этом случае невозможно выполнить кохлеарную имплантацию, т. к. нет возможности установить электрод в каналы улитки.
Цель нашего исследования: оценить эффективность применения метода слуховой стволомозговой имплантации у пациентов с глухотой.
Материал и методы
Для проведения СМИ было отобрано 3 пациента с сенсоневральной тугоухостью IV степени: 2 взрослых пациента 24 и 25 лет с нейрофиброматозом 2-го типа, после хирургического удаления невриномы VIII нерва с двух сторон и 1 ребенок в возрасте 2-х лет с двухсторонней аплазией улиток. Эти пациенты прошли комплексное обследование по программе кохлеарной имплантации. По данным обследования, у всех пациентов имелись противопоказания к операции кохлеарной имплантации и определены показания к операции СМИ.Этапы операции похожи на выполнение кохлеарной имплантации. На первом этапе проводится S-образный разрез кожи в заушной области, готовится ложе для приемника и электроники слухового имплантата. После подготовки ложа начинается нейрохирургическая часть операции. Проводится трепанация. Осуществляется доступ к боковой стенке IV желудочка головного мозга. У данных пациентов использовался ретросигмовидный доступ. У всех пациентов была проведена слуховая СМИ с правой стороны. Это связано с тем, что, по данным магнитно-резонансной томографии, у них было более удобное для операции расположение правой доли мозжечка. Во время операции был использован слуховой стволовой имплантат Mi1000 CONCERTO ABI System («Медель», Австрия). В ходе операции в случае обнаружения опухоли при возможности нейрохирург ее удаляет. Так, у одного из пациентов, выбранных для проведения данного вмешательства, была интраоперационно обнаружена невринома слухового нерва и успешно удалена.
Во время операции СМИ наиболее важным для успеха является правильное расположение электродной решетки над слуховыми ядрами. В случае ошибочного расположения электрода не будет акустической стимуляции и использовать имплантат станет невозможно. Поэтому наиболее ответственный этап операции – позиционирование электрода на поверхности кохлеарных ядер IV желудочка [13–15]. Хирург обычно использует анатомические ориентиры для предварительного выбора позиции электродной решетки. Но этого недостаточно. Для подтверждения правильности выбора места установки электрода используется нейрофизиологическое тестирование. Во время операции нейрофизиолог проводит регистрацию электрических слуховых вызванных потенциалов (эСВП) с тестового электрода в зоне предположительного нахождения улиткового ядра. В случае правильного расположения тестового электрода над кохлеарными ядрами регистрируются 3, 4, 5-q пики электрических слуховых вызванных потенциалов и данная зона в стволе головного мозга используется для закрепления электродной решетки СМИ.
Во время операции СМИ нами было проведено интраоперационное тестирование на эСВП. У одного взрослого пациента с нейрофиброматозом 2-го типа эСВП были зарегистрированы (рис. 3). У второго пациента с нейрофиброматозом 2-го типа и ребенка с аплазией улитки достоверных ответов не получено.

После установки электродной решетки хирург фиксирует ее фибриновым клеем. Тело имплантата в ложе фиксируется нерассасывающимся шовным материалом. Закрывается твердая мозговая оболочка, и рана послойно зашивается. Пациент переводится в нейрохирургическую реанимацию.
После установки имплантата начинается наиболее долговременная часть слуховой СМИ – это реабилитация, очень важный и ответственный процесс, требующий большого опыта в настройке подобных систем и поддержки электрофизиологических методов диагностики. Основная опасность первой настройки связана с расположением активного электрода в стволе головного мозга, где находятся основные жизненно важные центры.
В послеоперационном периоде возможно смещение электродной решетки [16]. В этом случае электрод может попасть в ядра блуждающего нерва и другие жизненно важные центры ствола головного мозга. Это осложнение очень опасно в момент активации системы СМИ. В момент первого включения системы происходит стимуляция электродной решетки электрическими импульсами. Если электрод расположен неправильно, возможно угнетение или стимуляция сердечно-сосудистой, дыхательной систем, вестибулярные нарушения. В связи с возможностью таких осложнений первое подключение проводится в реанимации, под контролем мониторов и в присутствии анестезиолога.
Результаты и обсуждение
Подключение процессора слухового СМИ проводилось через 1,5–2,5 мес. после операции. У взрослых пациентов настройка параметров электрической стимуляции проводилась по субъективным ощущениям, а также с учетом реакций пациента на звуки и наблюдений сурдопедагога [17]. В связи с особенностью локализации электрода слухового СМИ у всех пациентов были не только слуховые, но и неслуховые ощущения. При определении порогов комфортных уровней на каждом электроде одномоментно оценивалась слуховая и неслуховая стимуляция по аналоговым шкалам интенсивности. У ребенка во время стимуляции электродов № 7 и 10 возникало ощущение покалывания в той же половине тела (side effect). При подаче импульсов с электродов № 7, 9–12 проявлялась стимуляция вестибулярных ядер – резкое головокружение во время подачи стимула (рис. 4). В процессе настройки электроды, вызывающие преимущественно неслуховую стимуляцию, были отключены (табл. 1).

У всех пациентов, во время первого подключения непрерывно оценивались ощущения при стимуляции разных электродов имплантата. В процессе ежедневных настроечных сессий были определены электроды, вызывающие слуховые ощущения, и электроды, дающие побочные эффекты. Важным этапом для взрослых пациентов было определение восприятия частоты на каждом электроде. Так как кохлеарный имплантат позволяет перераспределять электроды на разные частотные каналы СМИ, нами был определен порядок электродов, вызывающих повышение воспринимаемой частоты тонов (рис. 5).

В результате такой настройки пациенты отмечали лучшее различение звуков по частоте, т. к. низкочастотные звуки попадали в области ствола мозга, отвечающие преимущественно за низкие частоты, звуки средней частоты – в области, отвечающие за средние частоты, и звуки высокой частоты – в области, отвечающие за высокие частоты (см. табл. 1).
Как показано в таблице, ежедневно менялись комфортные уровни стимуляции на разных электродах, менялось ощущение воспринимаемой частоты стимуляции электродов. По ощущениям пациента проводились коррекции настройки речевого процессора. Электроды со стойкими неслуховыми ощущениями были в процессе настройки отключены. В результате у пациента В. были активны 9 электродов, у пациента К. – 6 электродов, и у пациента Г. – 7 электродов. У ребенка не проверялось восприятие частоты по причине возраста. За счет пластичности головного мозга у него произойдет самостоятельная адаптация ядра к данной стимуляции. У взрослых пациентов этот тест был обязательным, т.к. в ядрах ствола тонотопика очень отличается от тонотопики улитки.
Оценка результатов работы процессора слухового стволового имплантата показала, что у всех пациентов улучшилось качество жизни. Уже на первой реабилитации пациенты узнавали некоторые звуки на слух, слышали голоса людей и узнавали собственное имя, стали чувствовать себя увереннее. Порог слуха достигал 45–55 Дб.
Результаты тестирования ребенка с двусторонней аплазией улиток и слуховых нервов после слуховой СМИ представлены на рис. 6.
Видно, что за 5 мес. работы речевого процессора достигнута заметная динамика слухоречевого развития.

Выводы
1. После подключения и первых настроек речевого процессора возможно возникновение неслуховых ощущений при использовании стволомозгового имплантата. Если операция проведена успешно, эти побочные эффекты можно устранить при настройке речевого процессора.2. Для данной группы пациентов требуется более продолжительная реабилитация. Пациенты после первого подключения только на второй неделе настроек отмечали стабильные слуховые ощущения.
3. При настройке речевого процессора стволомозгового имплантата уровни максимальной комфортной громкости могут достигать больших значений, чем при настройке системы кохлеарной имплантации.
4. В ходе настройки речевого процессора стволомозгового имплантата при обнаружении неслуховой стимуляции может быть отключено большее количество электродов в 1-ю сессию настройки, чем при кохлеарной имплантации.












