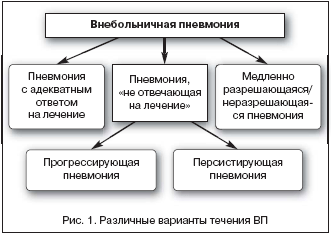
Случаи затяжного рентгенологического выздоровления ВП необходимо отличать от так называемой пневмонии, не отвечающей на лечение (для последней характерно отсутствие адекватного клинического ответа несмотря на проводимую антимикробную химиотерапию2) (рис. 1). В свою очередь, пневмония, не отвечающая на лечение, подразделяется на прогрессирующую и персистирующую. Прогрессирующая пневмония характеризуется развитием в первые 72 ч с момента поступления больного в стационар с острой дыхательной недостаточностью, требующей респираторной поддержки, и/или септического шока, которые обычно развиваются в первые 72 ч от поступления в стационар [3]. Подобный клинический «сценарий» чаще всего связывают с неэффективной терапией, развитием осложнений ВП, формированием экстраторакальных очагов инфекции. Термином же «персистирующая пневмония» описывают случаи замедленного регресса симптомов болезни, когда для достижения известных критериев клинической стабильности3 требуется, как правило, 6 и более дней [4,5].
Затяжное разрешение очагово–инфильтративных изменений в легких на фоне отчетливого обратного развития клинических симптомов заболевания обычно не рассматривается в качестве самостоятельного фактора риска неблагоприятного исхода пневмонии и в подавляющим большинстве случаев не требует повторных курсов антибактериальной терапии.
Причины медленного разрешения очагово–инфильтративных изменений в легких разнообразны и связываются с характеристиками возбудителя, особенностями клинического течения заболевания и факторами «хозяина». Здесь же следует упомянуть и многочисленный перечень заболеваний/патологических состояний, синдромосходных с пневмонией (рис. 2).
Причины медленно разрешающейся/
неразрешающейся ВП, связанные
с пациентом
Причины затяжного течения ВП, связанные с пациентом, как правило, оказывают более существенное влияние на клинико–рентгенологическую эволюцию заболевания, нежели известные характеристики возбудителя (вирулентность, лекарственная устойчивость). В числе важнейших факторов медленного рентгенологического разрешения пневмонии следует выделить пожилой/старческий возраст пациента и наличие у него сопутствующих инвалидизирующих заболеваний внутренних органов. Так, лишь у 30% больных в возрасте старше 50 лет спустя 4 недели от начала лечения наблюдается полное исчезновение пневмонической инфильтрации, в то время как у пациентов молодого/среднего возраста рентгенологическое выздоровление в эти сроки наблюдается более чем в 90% случаев [6]. У 70–80% пациентов с сопутствующими заболеваниями (ХОБЛ, застойная сердечная недостаточность, почечная недостаточность, сахарный диабет и др.) также наблюдается затяжное (более 4 недель) разрешение ВП [7–9]. В этом перечне особое место занимает застойная сердечная недостаточность – во–первых, при этом заболевании нередко ошибочно диагностируется пневмония, что «побуждает» к неоправданному назначению антибиотиков, а во–вторых, венозное полнокровие в малом круге кровообращения вследствие «застоя» сурфактанта и нарушения лимфатического дренажа обусловливает предрасположенность к бактериальной инвазии и оказывается одной из причин медленного разрешения пневмонической инфильтрации [10].
Медленное рентгенологическое выздоровление наблюдается у немалого числа (35–75%) больных хроническим алкоголизмом [11], а курение табака угнетает мукоцилиарный клиренс и является самостоятельным фактором риска инвазивной пневмококковой инфекции [12].
Отдельно необходимо выделить случаи пневмонии у лиц с иммунодефицитом, практически всегда сопровождающиеся синдромом затяжного рентгенологического разрешения. У ВИЧ–инфицированных больных обычно диагностируется пневмония, вызываемая Streptococcus pneumoniae и Haemophilus influenzae, однако при снижении числа лимфоцитов СD4+< 0,2 ×109/л чаще других развивается пневмоцистная пневмония (возбудитель – Рneumocystis jiroveci), являющаяся основной оппортунистической инфекцией при СПИДе. При этом на рентгенограмме органов грудной клетки у большинства пациентов (>85%) визуализируются ограниченные или диффузные двусторонние затенения (при компьютерной томографии наблюдается картина «матового стекла»), формируются полосные образования. Примечательно, что в 15–25% случаев несмотря на демонстративную клиническую симптоматику (лихорадка, признаки интоксикации, одышка) рентгенограмма может оставаться малоизмененной или интактной [13].
Пневмония у пациентов с иммунодефицитными заболеваниями/состояниями характеризуется, как правило, тяжелым/осложненным течением и медленным регрессом клинико–рентгенологических симптомов заболевания. Нередкими микробиологическими находками у такого рода больных наряду со S. pneumoniae, H. influenzae, Staphylococcus aureus оказываются Р. jiroveci, а также цитомегаловирусная и грибковая инфекции. Из первичных иммунодефицитов чаще других диагностируются Х–сцепленная агаммаглобулинемия и общий вариабельный иммунодефицит, требующие заместительной терапии иммуноглобулинами. Подозрение на вторичные иммунодефициты должно возникать всякий раз у истощенного больного в случаях диагностики солидных злокачественных новообразований, диффузных заболеваний соединительной ткани, гемобластозов, при приеме системных глюкокортикоидов, а также у реципиентов донорских органов [14].
Причины медленно разрешающейся/ неразрешающейся ВП, связанные
с самим заболеванием
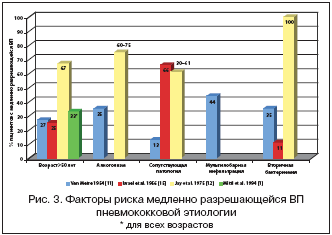
Важной причиной медленного разрешения ВП является тяжелое течение заболевания, при котором средние сроки рентгенологического выздоровления в среднем составляют около 10 недель. Мультилобарная пневмоническая инфильтрация и вторичная бактериемия также являются независимыми факторами риска затяжного течения пневмонии (рис. 3) [15].
Затяжное течение ВП закономерно часто корреспондирует с такими осложнениями заболевания, как абсцесс легкого или осложненный плеврит/эмпиема плевры, которые нередко разрешаются с образованием постпневмонического пневмо–плеврофиброза.
Еще одним из возможных факторов риска медленно разрешающейся ВП нередко оказывается неэффективная стартовая антибактериальная терапия, в свою очередь, обусловливаемая выбором антибиотика, неактивного в отношении возбудителя/возбудителей заболевания (приобретенная или природная устойчивость), нарушениями режима дозирования и др.
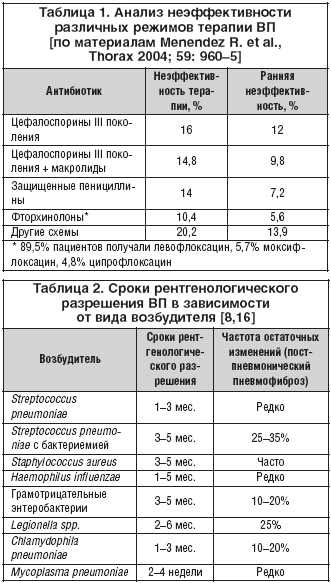
В этом отношении стоит упомянуть данные исследования, по результатам которого были обнаружены значительные различия в эффективности терапии, связанные с тем или иным антибактериальным препаратом, притом, что порядка 84% больных получали терапию, соответствовавшую требованиям рекомендаций по лечению пневмонии (табл. 1).
Показано, что применение «респираторных» фторхинолонов характеризуется наиболее низкой частотой развития ранней и общей неэффективности лечения, по-видимому, за счет своей высокой активности в отношении всех потенциальных возбудителей ВП.
Причины медленно разрешающейся/ неразрешающейся ВП, связанные
с возбудителем
На первый взгляд, парадоксальным представляется факт, что пневмококк, являющийся ведущим возбудителем ВП, обусловливает и большинство случаев затяжного течения заболевания. Еще в одном из первых исследований, посвященных изучению причин медленно разрешающейся пневмонии, показано, что рентгенологическое выздоровление пневмококковой пневмонии к исходу 4–й недели отмечалось у 91% больных с однодолевым поражением легких и в 56% случаев при мультилобарной распространенности процесса [11].
В числе известных причин затяжного течения пневмококковой пневмонии фигурируют полирезистентные S. pneumoniae и вторичная бактериемия. В последнем случае сроки полного обратного развития пневмонической инфильтрации составляют 3–5 месяцев [1].
При пневмонии, вызванной Legionella pneumophila, практически во всех случаях наблюдается длительное сохранение инфильтративных изменений в легких. Отчасти это связано с тем, что больные «не отвечают» должным образом на эмпирическую антибактериальную терапию, что сопровождается как клиническим, так и рентгенологическим ухудшением. Смена антибиотиков с назначением макролидов или «респираторных» фторхинолонов (левофлоксацин и др.) позволяет добиться выздоровления, но при этом рентгенологическое разрешение запаздывает порой до 6–12 месяцев. Впрочем, и в случаях адекватной стартовой антибактериальной терапии для «болезни легионеров» характерным является медленное обратное развитие очагово–инфильтративных изменений и высокая частота образования постпневмонического пневмофиброза. Показано, в частности, что у 65% больных с легионеллезной пневмонией рентгенографические изменения в легких сохраняются и спустя 8 недель от начала заболевания [16]. Согласно результатам целого ряда исследований рентгенологическое выздоровление наблюдается в течение первых 4 недель в среднем у 12% (от 0 до 29%) и сохраняются более 12 недель у 54% (от 42 до 70%) больных [17,18] (табл. 2).
Для микоплазменной пневмонии характерно нетяжелое течение, однако лишь в 40% случаев к исходу 4–й недели заболевания достигается рентгенологическое выздоровление, тогда как в остальных случаях для этого требуется не менее 8 недель [19].
Пневмония, вызываемая Chlamydophila pneumoniae, также протекают нетяжело и характеризуются быстрым разрешением клинико–рентгенологических симптомов, особенно у молодых пациентов. В большинстве случаев сроки разрешения пневмонической инфильтрации при этой форме ВП не превышают 4 недель, но у 20% больных могут достигать 8–9 недель. Более того, остаточные изменения в виде постпневмонического пневмофиброза сохраняются у 10–20% пациентов [8].
В отношении других возбудителей известно, что пневмония, вызываемая H. influenzae, более чем в половине случаев сопровождается длительным (в среднем 6 недель) разрешением пневмонической инфильтрации. ВП, вызываемая аэробными грамотрицательными энтеробактериями, характеризуется, как правило, более тяжелым течением и практически всегда сопровождаются длительными сроками рентгенологического выздоровления. Стафилококковая пневмония характеризуется закономерно частым формированием деструктивных изменений в легких; разрешение заболевания медленное, часто с исходом в локальный пневмофиброз.
Антибиотикорезистентность возбудителей ВП также может оказаться причиной затяжного заболевания. В этой связи важное значение приобретает знание врачом локальной эпидемиологии резистентности основных возбудителей пневмонии и учет известных факторов риска полирезистентности S. pneumoniae4 [3].
Дифференциальная диагностика
при синдроме «затяжной пневмонии»
Перечень заболеваний, протекающих под маской собственно пневмонии, чрезвычайно разнообразен (рис. 2), поэтому в случаях медленно разрешающейся/ неразрешающейся ВП поиск альтернативного заболевания приобретает порой решающее значение [20]. В целом более чем у 20% больных с синдромом «затяжной пневмонии» устанавливается альтернативный диагноз [21].
Инфильтративный туберкулез легких
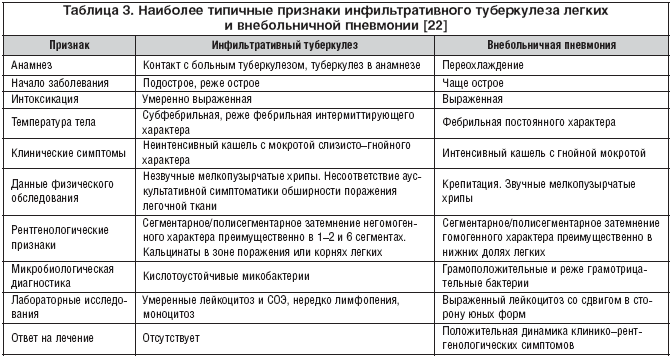
Весьма важным в процессе дифференциальной диагностики является разграничение затяжной пневмонии и инфильтративного туберкулеза легких (табл. 3). В этом контексте и сегодня весьма актуально звучат слова известного интерниста Роберта Хэгглина5: «Надо поставить за правило – каждый процесс считать туберкулезным до тех пор, пока не будет совершенно точно выявлена принадлежность его к другой группе заболеваний».
Основой диагностики туберкулеза является обнаружение кислотоустойчивых микобактерий при световой/люминесцентной микроскопии в мазках мокроты (материала, полученного при фибробронхоскопии), окрашенных по Ziehl–Neelson. При этом должно исследоваться не менее 3 проб мокроты в течение 3 последовательных дней и просматриваться не менее 100 полей зрения. Полимеразная цепная реакция позволяет выявить специфическую ДНК микобактерий, однако ввиду невысокой специфичности (высокая вероятность ложноположительных результатов) данный метод рассматривается в ряду дополнительных. Традиционная микробиологическая диагностика (посев мокроты) позволяет выделить культуру микобактерий через 21–90 дней.
Определенное значение имеет туберкулиновая диагностика – отсутствие реакции свидетельствует в пользу нетуберкулезного поражения легких. Напротив, гиперергическая реакция (размер папулы 21 мм и более) позволяет предположить инфицирование микобактериями. Положительная реакция при размере папулы от 5 до 20 мм не является диагностической, так как может быть обусловлена специфической сенсибилизацией к туберкулину как в результате инфицирования, так и вакцинации/ревакцинации БЦЖ.
В системе комплексной диагностики туберкулеза используются также методы определения антител и антигенов микобактерий (иммуноферментный анализ), однако их диагностическая ценность невысока ввиду ограниченной чувствительности и специфичности.
Новообразования
Чрезвычайно важным в период обследования больного с медленно разрешающейся/неразрешающейся ВП является исключение злокачественного новообразования. Эндобронхиальная опухоль может полностью или частично обтурировать дыхательные пути, приводя к развитию постобструктивной пневмонии. При этом рентгенологические признаки ателектаза могут отсутствовать, поскольку респираторные отделы оказываются заполненными воспалительным экссудатом.
Некоторые типы рака легкого могут манифестировать легочными инфильтратами с формированием очаговых или массивных очагово–сливных затенений на рентгенограмме. Это наиболее характерно для бронхиолоальвеолярного рака (БАР). В каждом третьем случае БАРа визуализируется лобарное уплотнение легочной ткани, причем присутствующая в части случаев воздушная бронхограмма усиливает убежденность в диагнозе пневмонии. При фибробронхоскопии эндобронхиальный рост опухолевых масс отсутствует.
Лимфома также может манифестировать преимущественно внутригрудной локализацией процесса. Так, например, поражение легочной ткани наблюдается при лимфогранулематозе примерно в 10% случаев (реже при неходжкинской лимфоме). Важно при этом подчеркнуть, что практически всегда паренхиматозный процесс «соседствует» с внутригрудной лимфаденопатией.
В редких случаях причиной медленного обратного развития очагово–инфильтративных изменений в легких могут оказаться и доброкачественные новообразования (например, аденома бронха).
В случаях медленного обратного развития пневмонии у курильщиков в возрасте старше 40 и больных из других групп риска развития рака легкого необходимо проведение фибробронхоскопии и компьютерной томографии (КТ) органов грудной клетки [23].
Тромбоэмболия легочной артерии
и инфаркт легкого
У больных с известными факторами риска глубокого венозного тромбоза (недавнее хирургическое вмешательство, травма, застойная сердечная недостаточность, ожирение, варикозная болезнь, длительный постельный режим, злокачественное новообразование, гиперглобулинемия, повторные эпизоды или семейный анамнез тромбоза/эмболии и др.) и развитием очагово–инфильтративных изменений в легких необходимо исключать тромбоэмболию легочной артерии (ТЭЛА), осложненную инфарктом легкого. В ряду характерных рентгенологических признаков ТЭЛА следует указать очаговую инфильтрацию, представленную сегментарными/полисегментарными гомогенными затенениями, прилежащими к диафрагме или костальной плевре, а вершиной обращенными к корню (признак Hampton). Данная рентгенологическая находка обнаруживается в сроки от 12 ч до нескольких дней после эмболического эпизода. Для очагово–инфильтративных изменений в случаях ТЭЛА не характерна воздушная бронхограмма с образованием полостей распада.
Вероятность ТЭЛА оказывается весьма высокой у больных с факторами риска венозного тромбоза, одышкой, тахипноэ, плевральными болями, не находящими другого объяснения.
Особое значение в диагностике ТЭЛА имеют визуализация «причинного» тромба в глубоких венах нижних конечностей (импедансная плетизмография, дуплексная ультразвуковая диагностика), перфузионная сцинтиграфия легких, КТ высокого разрешения с контрастированием и в отдельных случаях ангиопульмонография [24].
Иммунопатологические заболевания
Поражение легких характерно для васкулитов, поражающих сосуды мелкого и среднего калибра: гранулематоз Вегенера, микроскопический полиангиит, узелковый полиартериит и синдром Чардж–Стросса и др. [25]. Как правило, при васкулитах не наблюдается изолированного поражения легочной ткани, а в патологический процесс вовлекаются другие органы и системы (табл. 4).
Так, например, в ряду дебютных признаков гранулематоза Вегенера наряду с множественными (иногда транзиторными) легочными инфильтратами фигурируют поражения верхних дыхательных путей и почек. В каждом третьем случае рентгенологически визуализируются сегментарные или лобарные инфильтративные изменения. Поражения легких при гранулематозе Вегенера (чаще узловатые затенения, реже фокусная или массивная инфильтрация, плевральный выпот, ателектазы, альвеолярные геморрагии) встречаются в 70–85% случаев и могут ошибочно расцениваться, как пневмония (особенно у лихорадящих больных). Однако наличие внелегочных проявлений заболевания диктует необходимость пересмотра диагностической и лечебной тактики. В 2/3 случаев при гранулематозе Вегенера развивается гломерулонефрит. Кроме того, в патологический процесс вовлекаются верхние дыхательные пути (хронический синусит, средний отит), центральная или периферическая нервная система (20–34% случаев), кожа (40–50% случаев), суставы (60% случаев).
Реже в круг дифференциально–диагностического поиска при синдроме «затяжной пневмонии» включаются и другие системные васкулиты: синдром Чардж–Стросса (некротизирующий гранулематозный васкулит, для которого обязательно «присутствие» аллергического ринита, бронхиальной астмы, гиперэозинофилии периферической крови); микроскопический полиангиит (при котором в отличие от узелкового периартериита нередко описывается многофокусная альвеолярная инфильтрация и, напротив, практически не встречается полиневрит); синдром Гудпасчера (своеобразная комбинация легочных геморрагий и гломерулонефрита с образованием антител к базальной мембране клубочков почек и альвеол) и др.
Диагноз васкулита с установлением того или иного клинико–морфологического варианта основывается на тщательном гистологическом исследовании биоптатов пораженных органов. Очевидно, что обнаруживаемые патоморфологические изменения не являются строго специфичными, но с учетом характера клинического течения заболевания в большинстве случаев удается установить конкретный нозологический диагноз.
В числе возможных легочных и плевральных поражений при системной красной волчанке (СКВ) фигурируют плеврит с выпотом или без такового, интерстициальный пневмонит, диафрагмальная миопатия (миозит), базальные дисковидные (субсегментарные) ателектазы, острый волчаночный пневмонит (на почве легочного васкулита) и др. Объективно в круг дифференциально–диагностического поиска при синдроме «затяжной пневмонии» может быть включен волчаночный пневмонит, наблюдаемый в 1–4% случаев и манифестирующий кашлем, одышкой, болями в груди, лихорадкой. Преимущественная распространенность заболевания среди женщин (10:1), молодой возраст пациентов, прогрессирующий характер течения и полиорганность поражения (кожный, костно–мышечный, суставной, почечный, неврологический, гематологический и др. синдромы), обнаружение антинуклеарных антител и антител к ДНК позволяют правильно оценить конкретную клиническую ситуацию [27].
Идиопатическая организующаяся пневмония (облитерирующий бронхиолит с организующейся пневмонией) в типичных случаях развивается в возрасте 60–70 лет и характеризуется наблюдаемыми в течение нескольких недель кашлем, лихорадкой, одышкой, слабостью, многофокусной альвеолярной инфильтрацией. Патогенез заболевания не ясен. Нередко его развитие наблюдается на фоне переносимой «вирусной пневмонии», ревматоидного артрита, приема лекарственных препаратов (амиодарон, пенициллины, цитостатики, сульфаниламиды) и др. Диагностика организующейся пневмонии чрезвычайно важна, поскольку большинство больных хорошо «отвечают» на терапию системными глюкокортикоидами. Гистологически заболевание проявляется наличием гранулематозных «пробок» в просвете дистальных бронхов, распространяющихся внутрь альвеолярных ходов и альвеол (тельца Masson). Для постановки диагноза часто приходится прибегать к открытой или торакоскопической биопсии легкого, поскольку материал, получаемый при трансбронхиальной биопсии, часто не содержит всех элементов поражения, учет которых предполагает постановку диагноза [28,29].
В основе аллергического бронхолегочного аспергиллеза (АБЛА) лежит сенсибилизация организма к грибам рода Aspergillus с развитием патоиммунной альтерации различных структур бронхолегочной системы, что обусловливает своеобразие и полиморфизм клинического течения заболевания. Рентгенография органов дыхания – метод, с которого в большинстве случаев начинается сложный путь диагностики АБЛА. Наиболее распространены гомогенные затенения, занимающие часть или всю долю легкого, округлые уплотнения, располагающиеся перибронхиально. Среди диагностических критериев АБЛА выделяют «большие» и «малые» признаки. К «большим» признакам относят бронхоспастический синдром (синдром бронхиальной астмы), транзиторные легочные инфильтраты, центральные (проксимальные) бронхоэктазы, эозинофилию периферической крови, значительное повышение уровня общего сывороточного IgE, обнаружение преципитирующих антител к A. fumigatus, кожную гиперчувствительность немедленного типа к антигенам Aspergillus. В числе «малых» признаков фигурируют обнаружение мицелия Aspergillus в мокроте, отхождение пробок и слепков бронхов золотисто–коричневого цвета, поздняя кожная реакция с антигенами грибов (феномен Артюса) [30].
Хроническая эозинофильная пневмония (синдром Carrington) – идиопатическое заболевание, развивающееся преимущественно в среднем возрасте, в 2 раза чаще у женщин. Примерно в половине случаев у пациентов имеются признаки атопии, в т.ч. и бронхиальная астма. Симптомы заболевания (лихорадка, кашель, одышка, свистящее дыхание, ночные поты, снижение массы тела) могут наблюдаться в течение недель и месяцев, прежде чем будет установлен правильный диагноз. Эозинофилия периферической крови встречается у абсолютного большинства больных. Рентгенологическая картина представлена, как правило, билатеральной, пятнистой несегментарной альвеолярной инфильтрацией, располагающейся преимущественно в периферических и базальных отделах легких. Реже могут встречаться двусторонние или односторонние лобарные инфильтраты. КТ с большей чувствительностью обнаруживает те же признаки, а также возможную внутригрудную лимфаденопатию. Характерным для хронической эозинофильной пневмонии является быстрый «ответ» при назначении системных глюкокортикоидов: регресс клинических симптомов наступает уже через 1–2 дня, рентгенологических – через 7–10 дней [31].
Прочие заболевания
В типичных случаях диагностика саркоидоза (внутригрудная лимфаденопатия с минимальными клиническими проявлениями или отсутствием таковых) не представляет серьезных затруднений. Однако легочные проявления саркоидоза могут стимулировать широкий спектр заболеваний, включая и синдром «затяжной пневмонии». При этом особые проблемы возникают в случаях массивных тенеобразований, нередко перекрывающих корни легких, маскирующих возможное увеличение внутригрудных лимфатических узлов, что заставляет проводить дифференциальный диагноз, в т.ч. и с пневмонией (особенно у лихорадящих больных).
Основным методом диагностики саркоидоза является фибробронхоскопия с трансбронхиальной биопсией, позволяющая получить необходимый материал для последующего гистологического исследования. В тех случаях, когда результаты этого исследования оказываются недостаточно информативными (~ 20% случаев), приходится прибегать к помощи медиостиноскопии или торакоскопической/открытой биопсии легкого [32].
Оккультная аспирация кусочков пищи или других инородных тел с попаданием их в крупные бронхи – еще одна из причин медленно разрешающейся пневмонии. Чаще подобный механизм следует подозревать у пациентов с нарушенным кашлевым рефлексом или у лиц, подвергшихся интоксикации. Необходимо заметить, что далеко не все инородные тела являются рентгенопозитивными. В этой связи при малейшем подозрении на аспирацию следует незамедлительно выполнить фибробронхоскопию.
В редких случаях среди причин медленно разрешающейся пневмонии могут быть и токсические реакции на прием медикаментов. Лекарственные пневмопатии, связанные с приемом цитостатиков (блеомицин, метотрексат), обычно манифестируют диффузными интерстициальными изменениями и не создают особых проблем в дифференциальной диагностике у больных с синдромом «затяжной пневмонии». Напротив, при приеме амиодарона наряду с интерстициальными (ретикулонодулярными) изменениями могут обнаруживаться и локализованные легочные инфильтраты. Отчетливый регресс инфильтративных изменений в легких на фоне отмены препарата и назначения системных глюкокортикоидов убеждает в правильности высказанного предположения.
Тактика ведения пациентов с синдромом «затяжной пневмонии» в первую очередь предполагает учет возможных факторов риска медленного рентгенологического выздоровления:
• возраст старше 55 лет;
• алкоголизм, курение;
• наличие сопутствующих заболеваний внутренних органов (ХОБЛ, застойная сердечная недостаточность, почечная недостаточность, злокачественные новообразования, сахарный диабет и др.);
• тяжелое течение ВП;
• мультилобарная инфильтрация;
• наличие осложнений ВП (плевральный выпот, эмпиема плевры, абсцесс легкого);
• вторичная бактериемия;
• высоковирулентные возбудители (L. pneumophila, S. aureus, грамотрицательные энтеробактерии);
• лекарственноустойчивые штаммы возбудителей.
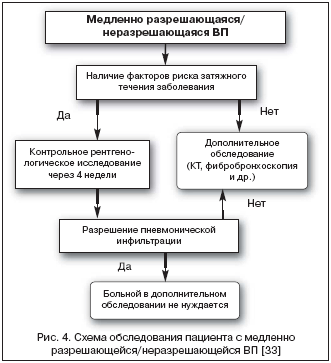
В тех случаях, когда у пациента присутствуют факторы риска медленного разрешения пневмонии, но при этом наблюдается отчетливое клиническое улучшение, целесообразна выжидательная тактика с проведением контрольного рентгенологического исследования органов грудной клетки спустя 4 недели.
Напротив, при отсутствии известных факторов затяжного течения заболевания показано дополнительное обследование – в ряду первоочередных диагностических мероприятий следует провести КТ органов грудной клетки и фибробронхоскопию с комплексом бактериологических и цитологических исследований (рис. 4).
1 Для российских врачей более привычным является тер-
мин «затяжная пневмония».
2 Речь идет о ранней терапевтической неэффективности в
ближайшие 48–72 ч с момента начала лечения.
3 Критерии клинической стабильности: температура тела
≤37,8°С; частота сердечных сокращений ≤100 в минуту; часто-
та дыхания ≤24 в минуту; систолическое артериальное давле-
ние ≥90 мм рт.ст.; сатурация артериальной крови ≥90% или pO2
≥60 мм рт.ст.; возможность приема лекарств внутрь; отсут-
ствие нарушений сознания [8,11,12].
4 Возраст <2 лет или >65 лет; применение –лактамов в
течение последних 3 месяцев; повторные курсы терапии –лак-
тамами, макролидами или фторхинолонами; ранее (в преде-
лах года) перенесенная пневмония; тяжелые сопутствующие
заболевания внутренних органов (застойная сердечная недо-
статочность, сахарный диабет, ХОБЛ и др.); хронический алко-
голизм; иммунодефицитные заболевания/со стояния (включая
терапию системными глюкокортикоидами); контакт с детьми,
посещающими детские сады
5 Р. Хэгглин. Дифференциальная диагностика внутренних
болезней. М.: Медицина, 1965


Литература
1. Mittl R.L. Jr., Schwab R.J., Duchin J.S., et al. Radiographic resolution of community–acquired pneumonia. Am J Respir Crit Care Med 1994; 149:630–5.
2. Kurtland S.H., Winterbauer R.H. Slowly resolving, chronic and recurrent pneumonia. Clin Chest Med 1991; 12: 303–18.
3. Mandell L.A., Wunderink R.G., Anzueto A., et al. Infectious Diseases Society of America/American Thoracic Society Consensus Guidelines on the Management of Community–Acquired Pneumonia in Adults. Clinical Infectious Diseases 2007; 44 (Suppl. 2): 27–72.
4. Daifuku R., Movahhed H., Fotheringham N., et al. Time to resolution of morbidity: an endpoint for assessing the clinical cure of community–acquired pneumonia. Respir Med 1996; 90:587–92.
5. Auble TE, Yealy DM, Fine MJ. Assessing prognosis and selecting an initial site of care for adults with community–acquired pneumonia. Infect Dis Clin North Am 1998; 12:741–59.
6. Fein A.M. Pneumonia in the elderly: Overview of diagnostic and therapeutic approaches. Clin Infect Dis 1999; 28:726.
7. Jay, SJ, Johnson, WG, Pierce, AK. The radiographic resolution of Streptococcus pneumoniae pneumonia. N Engl J Med 1975; 293:798.
8. Macfarlane J.T., Miller A.C., Roderick Smith W.H., et al. Comparative radiographic features of community acquired Legionnaires’disease, pneumococcal pneumonia, mycoplasma pneumonia, and psittacosis. Thorax 1984; 39:28.
9. Rodrigues J., Niederman M.S., Fein A.M. Nonresolving pneumonia in steroid treatment of patients with obstructive lung disease. Am J Med 1992; 93:29.
10. Cunha B.A. Pneumonia in the elderly. Drugs Today 2000;36:785–91.
11. Van Metre T.E. Pneumococcal pneumonia treated with antibiotics. The prognostic significance of certain clinical findigs. N Engl J Med 1954; 251: 1048–52.
12. Jay S.J., Johnson W.G., Pierce A.K. The radiographic resolution of Streptococcus pneumoniae pneumonia. N Engl J Med 1975; 293:798.
13. Каражас Н.В., Дехнич А.В. Пневмоцистная пневмония: клинические и микробиологические аспекты. Клин микробиол антимикроб химиотер 1999; 1: 12–22.
14. Sepkovitz K.A., Opportunistic infections in patients with and patients without acguired immunodeficiency syndrome. Clin Effect Dis 2002; 34: 1098–107.
15. Israel H.L., Weiss., Eisenberg G.M. et al. Delayed resolution of pneumonia. Med Clin North Am 1956; 40: 1291–303.
16. Ost D., Fein A. Feinsilver S.H. Nonresolving pneumonia. In: UpToDate, Rose, BD (Ed), UpToDate, Wellesley, MA, 2002.
17. Kuru T., Lynch J.P. Nonresolving or slowly resolving pneumonia. Clin Chest Med 1999; 20:623.
18. Coletta, FS, Fein, AM. Radiological manifestations of legionella/legionella–like organisms. Semin Respir Infect 1998; 13:109.
19. Cameron D.C., Borthwick R.N., Philip T. The radiographic patterns of acute Micoplasma pneumonias. Clin Radiol 1977; 28: 173–80. Marrie T.J. Mycoplasma pneumoniae required hospitalization with emphasis on infection in the elderly. Arch Intern Med 1993; 153:488.
20. Bulmer S.R., Lamb D., McCormack R.J., Walbaum P.R. Aetiology of unresolved pneumonia. Thorax 1978;33: 307–314.
21. Arancibia F., Ewig S, Martinez, JA, et al. Antimicrobial treatment failures in patients with community–acquired pneumonia: causes and prognostic implications. Am J Respir Crit Care Med 2000; 162:154.
22. Мишин В.Ю. Дифференциальная диагностика туберкулеза легких и пневмонии. Глава в книге «Пневмония» М.: Экономика и информатика 2002; 280–311.
23. Синопальников А.И. Медленно разрешающаяся / неразрешающаяся внебольничная пневмония. Глава в книге «Пневмония» М.: Экономика и информатика. 2002; 364–387.
24. Hartmann I.C., Hagen P.J., Melissant C.F. et al. Diagnosing Acute Pulmonary Embolism Effect of Chronic Obstructive Pulmonary Disease on the Performance of D–dimer Testing, Ventilation / Perfusion Scintigraphy, Spiral Computed Tomographic Angiography, and Conventional Angiography. Am. J. Respir. Crit. Care. Med. 2000 Vol 162: 2232–2237.
25. Чучалин А.Г. Первичные системные и легочные васкулиты. Русский мед. журнал 2001; № 21(9): 912–918.
26. Авдеев С.Н. Остро протекающие диффузные паренхиматозные заболевания легких. Consilium medicum 2008; №3 (10): 5–11.
27. Semple D., Keogh J., Forni L., Venn R. Clinical review: Vasculitis on the intesive care unit part 1: diagnosis. Critical Care 2005; 9:92–7.
28. Паттерсон Р., Греммер Л., Гринберген П. Аллергические болезни: диагностика и лечение. М.: Гэотар Медицина, 2000;768 с.
29. Cordier J.F. Criptogenic organising pneumonia. Eur Respir J. 2006; 28: 422–46.
30. Гембицкий Е.В., Синопальников А.И., Алексеев В.Г. Аллергический бронхолегочный аспергиллез. Тер архив 1987; 3: 78–83.
31. Ebara H., Ikezoe J., Johkok T., et al. Chronic eosinophilic pneumonia: evolution of chest radiograms and CT features. J Comput Assist Tomogr 1994; 18:737.
32. ATS/ERS/WASOG statement on sarcoidosis. Sarcoidosis Statement Committee. American Thoracic Society. European Respiratory Society. World Association for Sarcoidosis and Other Granulomatous Disorders. Eur. Respir. J. 1999; 4(14): 735–737.
33. Cassiere H.A., Niederman M.S. Community–acquired pneumonia. In: Parsons P.E., Heffner J.E., editors. Pulmonary/ respiratory therapy secrets. 2nd ed. Philadelphia: Hanley&Belfus, Inc.: 2002. p.144–51.












