Нестероидные противовоспалительные препараты (НПВП) при РА являются надежным инструментом, позволяющим уменьшить выраженность основных субъективных проявлений заболевания и улучшить качество жизни пациентов; значение этой группы лекарственных препаратов в дебюте РА трудно переоценить [1]. В первую очередь их применение позволяет обеспечить больному комфортный период ожидания до наступления клинического эффекта БПВП (который может растянуться на несколько месяцев). В дальнейшем НПВП играют роль действенного вспомогательного средства при сохранении артралгий и скованности. Следует так– же отметить, что применение НПВП в эффективных противовоспалительных дозах в ряде случаев позволяет избежать системного назначения ГК.
Однако согласно общепринятому мнению применение НПВП предполагает достижение лишь симптоматического эффекта. В то же время, процесс синтеза провоспалительных простагландинов может выступать не только в роли важного звена в патогенезе острого синовита при РА, но и иметь существенное значение для хронизации воспаления. Так, в развитии хронического синовита и формировании паннуса при РА в ряде работ обсуждается роль неоангиогенеза – патологического процесса, развитие которого несомненно зависит от экспрессии ЦОГ–2 [2–4]. Исходя из этого можно предположить, что использование НПВП в высоких противовоспалительных дозах в дебюте артрита позволит добиться не только симптоматического, но и определенного патогенетического эффекта.
Серьезной проблемой, которая может возникнуть при использовании высоких доз НПВП, являются нежелательные эффекты, прежде всего со стороны желудочно–кишечного тракта (ЖКТ) [5]. Поэтому рациональный выбор НПВП у больных с дебютом РА должен включать оценку безопасности лекарственного препарата. Вероятно, наиболее приемлемым в этой ситуации является использование селективных ЦОГ–2 ингибиторов (с–НПВП), существенно реже по сравнению с традиционными НПВП (неселективными ЦОГ–2 ингибиторами, н–НПВП), вызывающими осложнения со стороны ЖКТ. Однако у ряда российских врачей до настоящего времени сохраняется малообоснованное мнение о менее высокой эффективности с–НПВП по сравнению с н–НПВП [6].
Одним из наиболее широко используемых в зарубежной и российской медицинской практики с–НПВП является нимесулид. Этот препарат, помимо основного фармакологического действия (блокада ЦОГ–2), обладает рядом благоприятных эффектов, таких как блокада фосфодиэcтеразы 4, снижающая активность нейтрофилов и макрофагов в очагах воспаления, подавление синтеза провоспалительных цитокинов (интерлейкина–6 и фактора некроза опухоли–a) и др., которые могут определить его высокую эффективность именно при остром воспалении, в т.ч. в дебюте РА [7]. Однако четких данных о лечебном действии и безопасности среднетерапевтических и высоких доз нимесулида при раннем артрите до настоящего времени не имелось. Актуальным вопросом является также сравнение эффективности этого препарата при раннем артрите с диклофенаком, наиболее широко используемым в нашей стране н–НПВП.
Целью настоящего исследования явилось изучение сравнительной эффективности и переносимости высоких и среднетерапевтических доз нимесулида и диклофенака при раннем РА.
Материал и методы
В исследование были включены 268 больных с ранним артритом, соответствующих следующим критериям:
1. Наличие одного из следующих симптомов (модифицированные критерии клинического подозрения на РА, Emery P. и сотр., 2002) [8]: артрит мелких или крупных суставов, утренняя скованность более 30 минут, симметричные полиартралгии, положительный симптом сжатия кистей или стоп.
2. Наличие болевого синдрома, требующего медикаментозной коррекции (40 мм и более по ВАШ).
3. Возраст старше 18 лет.
4. Первичное обращение к ревматологу при длительности суставного синдрома не более 12 недель.
Критериями исключения была высокая воспалительная активность, являющаяся показанием для системного назначения ГК; достоверные признаки иного ревматического заболевания, наличие активной язвы или 5 и более эрозий слизистой желудка или двенадцатиперстной кишки, тяжелая сопутствующая патология; прием ГК и базисных противоревматических препаратов.
В течение 4 недель больные получали монотерапию НПВП. В настоящей работе мы использовали генерические препараты диклофенака (выбор конкретного генерика оставался на усмотрение лечащего врача) и генерический препарат нимесулида Найз® (Doctor Reddy’s). В период проведения исследования базисные препараты не назначались, использование ГК (системно или в виде внутрисуставных инъекций) не допускалось.
Больные последовательно включались в 4 исследуемые группы: больным группы 1 назначался нимесулид 200 мг 2 раза в сутки, группы 2 – нимесулид 100 мг 2 раза в сутки, группы 3 – диклофенак 100 мг 2 раза в сутки, группы 4 – диклофенак 50 мг 2 раза в сутки.
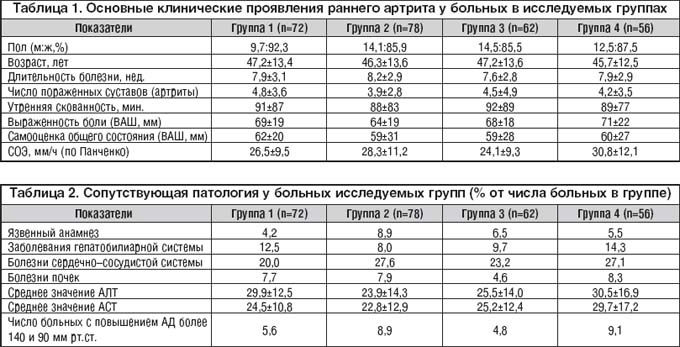
Характеристика исследуемых групп представлена на таблице 1. Явное различие в размерах исследуемых групп определялось системой набора пациентов, предусматривавшей их последовательное включение в группы. С учетом небольшого числа больных, набранных разными центрами, число пациентов оказалось закономерно больше в двух первых группах. Так, если отдельным центром было набрано 8 больных, то по распределение по группам выглядело как 2 : 2 : 2 : 2. а если только 6 – то 2 : 2 : 1 : 1.
Исследуемые группы статистически значимо не отличались по демографическим параметрам и проявлениям основного заболевания. Большинство больных – лица женского пола молодого и среднего возраста. Средняя длительность заболевания составляла около 2 месяцев. Обращает на себя внимание достаточно выраженный суставной синдром – у многих пациентов отмечалось наличие полиартрита, с выраженными болями (у подавляющего большинства – ВАШ > 50 мм). У многих больных отмечалась выраженная утренняя скованность (более 1 часа). По данным самооценки общего состояния можно говорить, что суставной синдром оказывал существенное влияние на самочувствие больных и вызывал у них серьезное беспокойство.
Многие больные имели сопутствующую патологию, способную оказать существенное влияние на переносимость НПВП (табл. 2). Наиболее часто отмечалось наличие патологии сердечно–сосудистой системы, прежде всего артериальная гипертензия. Следует отметить, что у некоторых пациентов, включенных в исследование, отмечалась неконтролируемая артериальная гипертензия (АД свыше 140/90 мм рт. ст.).
Статистически значимого различия между исследуемыми группами по наличию сопутствующей патологии выявлено не было. Лечение сопутствующих заболеваний проводилось по усмотрению лечащих врачей и специально не менялось во время проведения лечения. При наличии язвенного анамнеза больным, которым был назначен диклофенак, рекомендовалось использовать гастропротективную терапию (омепразол 20 мг/сут.), а при возникновении диспепсических явлений назначать антацидные препараты в режиме «по требованию».
Полученные в ходе исследования данные вносились в специальную карту. Заполненные карты отсылались исследователями в головной центр (ГУ ИР РАМН), где данные вносились в компьютерную базу данных и подвергались статистической обработке и анализу. Всего было обработано 327 карт, из которых 268 признаны информативными (59 карт были заполнены с ошибками и не включены в статистическую обработку).
Для определения статистической значимости различия непрерывных показателей использовался t–тест Стьюдента, для ранговых переменных – критерий c2 и точный тест Фишера. Значение непрерывных переменных представлены в тексте в виде М±s.
Результаты
Все пациенты завершили курс лечения НПВП, случаев прерывания терапии из–за неэффективности или развития серьезных нежелательных явлений отмечено не было.
Достигнуть максимального эффекта терапии (купировать все проявления заболевания) удалось лишь у 5 больных, у которых после 4–х недель монотерапии НПВП не отмечалось признаков артрита, артралгий (ВАШ 0 мм), отсутствовали клинические и лабораторные признаки воспалительной активности. Такое лечебное действие отмечалось у 2 больных, получавших нимесулид 400 мг/сут., у 2 больных, принимавших диклофенак 200 мг/сут., и у 1 принимавшего диклофенак 100 мг/сут.
Число воспаленных суставов существенно уменьшилось во всех группах и составило 2,7±1,9, 2,3±1,5, 2,7±1,7 и 2,2±1,4 соответственно. Отличие было достоверным по сравнению с исходным количеством пораженных суставов в каждой отдельной группе (p<0.05), однако значимого различия между различными группами выявлено не было.
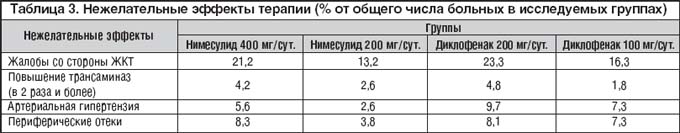
Симптоматический эффект НПВП был достаточно хорошим. Отсутствие эффекта (менее 20% уменьшение уровня боли по ВАШ) было лишь у 19,4, 27,6, 26,5 и 24,5% соответственно (различие недостоверно). Частота случаев, когда ВАШ уменьшилось на 50% и более, представлено на рисунке 1. Как видно, в трех из исследуемых групп (нимесулид 400 мг и 200 мг, диклофенак 100 мг) существенное улучшение отмечалось более чем у 40% больных, и лишь среди получавших высокие дозы диклофенака улучшение было отмечено лишь у 32.1% (достоверного отличия между группами не было).
Проводимая терапия позволила добиться существенного снижения утренней скованности, которая после курсового приема НПВП составила в среднем в исследуемых группах 37±33, 42±44, 38±31 и 46±38 минут соответственно. Отличие было достоверным по сравнению с исходной длительностью утренней скованности в каждой отдельной группе (p<0,001), однако значимых расхождений в показателях между различными группами выявлено не было.
На фоне терапии было отмечено также существенное улучшение общего самочувствия больных (по данным самооценки, ВАШ). 50% и более изменение общего самочувствия было отмечено у 34,3%, 36,9%, 33,1% и 34,7% больных (различие недостоверно).
Ни у кого из пациентов в исследуемых группах во время проведения не отмечалось развития серьезных нежелательных эффектов, потребовавших прерывания терапии.
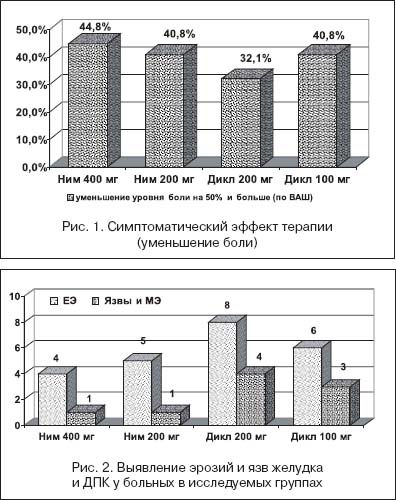
Эндоскопическое исследование верхних отделов ЖКТ (ЭГДС) не было обязательным и назначалось по усмотрению лечащих врачей при наличии показаний. ЭГДС по окончании исследования была проведена 126 больным (47,0%). На рисунке 2 представлена частота эрозий и язв желудка и 12–перстной кишки (ДПК), выявленных при ЭГДС. Эта патология реже выявлялась у пациентов, получавших нимесулид в обеих дозировках. Среди всех больных, принимавших нимесулид, единичные эрозии (ЕЭ) были выявлены у 9 (6,0%); среди всех больных, принимавших диклофенак – у 14 (11,9%); отличие недостоверно (р=0,102). Язвы и множественные эрозии (МЭ, n>10) были выявлены у 2 (1,3%) среди принимавших нимесулид, и у 7 (5,9%), принимавших диклофенак, различие достоверно (р=0,042).
Субъективные жалобы со стороны верхних отделов ЖКТ (изжога, отрыжка, гастралгии, тошнота, чувство тяжести в эпигастрии) возникли у 21,2%, 13,2%, 23,3% и 16,3% больных в исследуемых группах соответственно (различие недостоверно).
Повышение АЛТ в 2 раза и более по сравнению с исходным уровнем отмечалось у 3 (4,2%) больных, принимавших нимесулид 400 мг/сут., у 2 (2,6%) принимавших нимесулид 200 мг/сут., у 3 (4,8%) принимавших диклофенак 200 мг/сут. и у 1 (1,8%) принимавшего диклофенак 100 мг/сут. (различие недостоверно).
Артериальная гипертензия (АД 140/90 мм рт.ст. и выше) была выявлена у 4 (5,6%), 2 (2,6%), 6 (9,7%) и 4 (7,3%) больных в 4–х группах соответственно (различие недостоверно). Появление периферических отеков было отмечено у 6 (8,3%), 3 (3,8%), 5 (8,1%) и 4 (7,3%) больных соответственно (различие недостоверно).
Суммарно частота развития различных нежелательных явлений в исследуемых группах представлена в таблице 3.
Обсуждение
На основании полученных нами данных возможно утверждать, что монотерапия высокими дозами НПВП не позволяет добиться купирования суставного синдрома у подавляющего большинства больных с ранним артритом. Ремиссия на момент окончания срока наблюдения была достигнута лишь у 5 больных, при этом необходимо учесть, что данный результат был получен в ходе проведения открытого исследования. По сравнению со слепыми исследованиями в ходе проведения открытых исследований их участники зачастую определяют эффективность изучаемых препаратов более субъективно и дают им несколько завышенную оценку.
В то же время следует отметить, что исследуемая группа была в основном представлена пациентами с выраженным суставным синдромом и высокой воспалительной активностью. Очевидно, определенная часть из них имела показания для системного назначения ГК и начала активной терапии БПВП, поэтому добиться значительного клинического эффекта назначением только НПВП у этого контингента больных было невозможно.
Тем не менее эффективность терапии НПВП оказалась достаточно высокой. Более чем у 40% больных, получавших нимесулид в обеих дозировках, и диклофенак 100 мг/сут., отмечалось уменьшение интенсивности боли на 50% и более (по ВАШ). Лишь у 1/4 больных, получавших нимесулид 200 мг/сут. и диклофенак в обеих дозировках, не отмечалось значимого уменьшения интенсивности боли (несколько лучший эффект был достигнут при использовании нимесулида 400 мг/сут.).
Важно отметить, что прием НПВП оказывал не только обезболивающий, но и существенный противовоспалительный эффект, что четко видно по достоверному уменьшению числа воспаленных суставов и значительному уменьшению утренней скованности во всех исследуемых группах.
Хотя при РА использование средних и высоких терапевтических доз НПВП является общепризнанной практикой, имеется лишь ограниченное число исследований, оценивающих их эффективность при этом заболевании. Вероятно, наиболее крупным из подобных исследований является VIGOR, в ходе которого 8076 больных с достоверным диагнозом РА в течение 6 месяцев принимали высокие дозы НПВП: рофекоксиб 50 мг (n=4047) или напроксен 1000 мг/сут. (n=4029). Для субъективной оценки состояния больных использовался «Общий счет активности заболевания», который определялся самими пациентами по 5–бальной шкале (от 0 – «очень хорошо» до 4 – «очень плохо»). Исходно счет составил 1,96±0,93 в группе рофекоксиба и 1,99±0,94 в группе напроксена, а его снижение составило через 6 месяцев лечения 0,51±0,93 и 0,55±0,94 балов соответственно (т.е., более чем на 25% в каждой группе). Авторы оценили эффективность высоких доз НПВП как высокую, указывая, что прерывание исследования из–за неэффективности терапии было отмечено лишь у 6,3% и 6.5% больных. Следует отметить, что подобный эффект был достигнут у пациентов, подавляющее большинство из которых страдали РА в течение длительного времени и получали активную противоревматическую терапию (более 50% принимали ГК и метотрексат) [9].
Интересным фактом, выявленным в ходе нашего исследования, явилось отсутствие значимого отличия в эффективности различных доз НПВП (как нимесулида, так и диклофенака). Возможно предположить, что противовоспалительный и анальгетический эффект не является строго дозозависимым, хотя этот феномен требует специального изучения. Аналогичный результат был получен в работе Furst D. и сотр. [10], изучавших эффективность и безопасность различных доз мелоксикама у 894 больных с РА. Пациенты получали мелоксикам в трех различных дозах: 7,5 мг, 15 мг или 22,5 мг/сут. (контролем были диклофенак 150 мг/сут. и плацебо). Через 3 месяца наблюдения авторы не выявили существенной разницы в эффективности различных доз этого препарата. Мы можем сделать вывод, что назначение высоких доз НПВП не имеет реальных преимуществ по сравнению со среднетерапевтическими как при использовании с–НПВП, так и н–НПВП.
Полученные нами данные показали, что с–НПВП нимесулид и н–НПВП диклофенак не различаются по своему анальгетическому и противовоспалительному эффекту при раннем артрите. Это положение имеет большое значение для реальной клинической практики, поскольку использование с–НПВП дает существенные преимущества в отношении переносимости терапии. Это особенно важно в дебюте РА, когда требуется проведение агрессивной противоревматической терапии, а развитие серьезных нежелательных эффектов, требующих специального лечения, может существенно затруднить лечение основного заболевания.
Особенно важной частью нашего исследования явилась оценка безопасности терапии НПВП.
На фоне приема нимесулида в обеих дозировках достоверно реже отмечалось появление множественных эрозий и язв желудка или ДПК – патологии, потенциально угрожающей жизни пациентов (за счет повышения риска развития кровотечения и перфорации) и требующей обязательного лечения.
Более высокая по сравнению с н–НПВП гастроинтестинальная безопасность нимесулида относится к одному из основных достоинств этого препарата [11]. Большое популяционное исследование, проведенное в Северной Италии и представляющее собой анализ 10608 сообщений о побочных действиях НПВП, произошедших с 1988 по 2000 гг., показало, что частота развития серьезных гастродуоденальных осложнений на фоне приема этого препарата примерно в 2 раза ниже, чем при использовании других НПВП [12]. Особый интерес вызывает масштабное отечественное исследование, проведенное О.Н. Минушкиным и сотр., показавшее возможность относительно безопасного использования нимесулида (Найз) у больных, имевших в анамнезе патологию ЖКТ, в т.ч. язвенную болезнь [13].
В то же время, мы не выявили достоверной разницы в частоте субъективных симптомов со стороны ЖКТ у больных, получавших нимесулид и диклофенак, независимо от дозы. Возможность развития диспепсии на фоне приема с–НПВП (с частотой, близкой к частоте этого осложнения на фоне н–НПВП) является хорошо известным фактом. Так, в 3–месячном исследовании SUCCESS–1 (целекоксиб 200–400 мг/сут. vs. диклофенак 100 мг/сут. или напроксен 1000 мг/сут. при остеоартрозе (ОА), n=13194) частота развития гастралгий и диспепсии на фоне приема целекоксиба составила 9,6%, у препаратов сравнения – 12,1% [14].
Артериальная гипертензия и отечный синдром отмечались с одинаковой частотой у больных, принимавших нимесулид и диклофенак. Это также хорошо согласуется с данными мировой литературы. В упомянутом выше исследовании SUCCESS–1, на фоне приема целекоксиба артериальная гипертензия отмечалась у 5,2%, а отеки у 7,14% больных (6,1% и 6,99% в контроле).
Появление лабораторных признаков НПВП–гепатопатии (существенное повышение АЛТ) отмечалось с одинаковой частотой в исследуемых группах. Это соответствует литературным данным, свидетельствующим, что частота развития серьезных осложнений со стороны печени на фоне приема нимесулида не отличается от частоты развития подобных осложнений при приеме других НПВП [15].
В заключение следует отметить, что обоснование выбора конкретного препарата из группы селективных ЦОГ–2 ингибиторов для лечения раннего артрита является сложной задачей. Нет четких данных, что различные препараты из группы с–НПВП отличаются по своему анальгетическому или противовоспалительному эффекту. Тем не менее имеется небольшое двойное слепое РКИ, проведенное в Италии, где было показано, что нимесулид достоверно превосходит целекоксиб и рофекоксиб по скорости наступления и выраженности обезболивающего эффекта у пациентов с остеоартрозом [16].
Нет данных, что с–НПВП существенно отличаются по своей переносимости [17]. Так, было показано, что эрозии и язвы верхних отделов ЖКТ с одинаковой частотой выявляются у пациентов, принимавших нимесулид, мелоксикам и целекоксиб (n=810), но достоверно реже, чем у получавших диклофенак (n=2813) [18].
Таким образом, данные настоящего исследования доказывают целесообразность использования нимесулида (Найз) в качестве обезболивающего и противовоспалительного средства при раннем артрите. Его лечебный эффект не отличался от диклофенака, однако нимесулид существенно реже вызывал нежелательные эффекты со стороны ЖКТ. Необходимо отметить, что применение НПВП в качестве монотерапии (независимо от дозы) не позволяет добиться купирования суставного синдрома у подавляющего большинства больных и должно рассматриваться, как компонент комплексной терапии раннего артрита, основой которой являются БПВП.
Литература:
1. Насонов Е.Л. Нестероидные противовоспалительные препараты. М.: «Анко», 2000, 143 с.
2. Van Leeuwen M., van der Heijde D., van Rijswijk M., et al. Interrelationship of outcome measures and process variables in early rheumatoid arthritis. A comparison of radiologic damage, physical disability, joint counts, and acute phase reactants. J. Rheumatol., 1994, 21, p.425–429.
3. Walsh D.A., Haywood L. Angiogenesis: a therapeutic target in arthritis. Curr. Opin. Invest. Drugs, 2001, 2, p.1054–1063.
4. Koehne C., Dubois R. COX–2 inhibition and colorectal cancer. Semin Oncol., 2004, 31, 2–21.
5. Насонов Е.Л., Каратеев А.Е. Поражения желудка, связанные с приемом нестероидных противовоспалительных препаратов. Клин. Мед., 2000, 3, с.4–10 (Часть 1), Клин. Мед., 2000, 4, с.4–9 (Часть 2).
6. Каратеев А.Е., Коновалова Н.Н., Литовченко А.А., Ломарева Н.И., Немцов Б.Ф., Раскина Т.А., Пешехонова Л.К., Насонов Е.Л. НПВП – ассоциированная заболевание ЖКТ при ревматизме в России. Клин. Мед., 2005, 5, 33–39.
7. Camu F., Shi L., Vanlesberghe C. The role of COX–2 inhibitors in pain modulation. Drag., 2003, 63, suppl. 1, p.1–7.
8. Emery P., Breedveld F.C., Dougados M., Kalden J.R., Schiff M.H., Smolen J.S. Early referral recommendation for newly diagnosed rheumatoid arthritis: evidence based development of a clinical guide. Ann. Rheum. Dis., 2002, 61, No. 4., p.290–297
9. Bombardier C., Laine L., Reicin A., et al. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis. VIGOR Study Group. N. Engl. J. Med., 2000, 343, p.1520–1528.
10. Furst D., Kolba K., Fleischmann R. Dose response and safety study of meloxicam up to 22.5 mg daily in rheumatoid arthritis: a 12 week multicenter, double blind, dose response study versus placebo and diclofenac. J. Rheumatol., 2002, 29, p.436–446.
11. Bjarnason I., Thjodleifsson B., Gastrointestinal toxicity of non–steroidal anti–inflammatory drugs: the effect of nimesulide compared with naproxen on the human gastrointestinal tract. Rheumatol., 1999, 38, 24–32.
12. Conforti A., Leone R., Moretti U., Mozzo F., Velo G. Adverse drug reactions related to the use of NSAIDs with a focus on nimesulide: results of spontaneous reporting from a Northern Italian area. Drug Saf., 2001, 24,1081–1090.
13. Минушкин О.Н. Использование препарата “Найз” у больных, страдающих сочетанной патологией суставов и поражением верхних отделов желудочно–кишечного тракта. Науч. практ. ревм., 2003, 5, 72–76.
14. Singh G., Fort J., Goldstein J. et al. Celecoxib versus naproxen and diclofenac in osteoarthritis patients: SUCCESS–1 study. Am. J. Med., 2006, 119, 255–266.
15. Traversa G., Bianchi C., Da Cas R., et al. Cohort study of hepatotoxity associated with nimesulide and other non–steroidal anti–inflammatory drugs. BMJ, 2003, 327, 18–22
16. Bianchi M., Broggini M. A randomized, double–blind, clinical trial comparing the efficacy of nimesulide, celecoxib and rofecocxib in osteoarthritis of the knee. Drag., 2003, 63, suppl. 1, p.37–46.
17. Hawkey C. Cyclooxygenase inhibition: between the devil and deep blue see. GUT, 2002, 50, 1125–1130
18. Karateev A.E. Gastrointestinal safety of selective COX–2 inhibitors in clinical practice. Annuals European Congress EULAR, 2005, 64 (suppl. 3), SAT0117.












