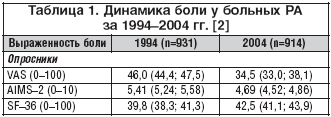
–‰–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è –≤ ―²–Α–Κ―²–Η–Κ–Β –Μ–Β―΅–Β–Ϋ–Η―è –†–ê, –Ω―Ä–Ψ–Η–Ζ–Ψ―à–Β–¥―à–Η–Β –≤ –Ω–Ψ―¹–Μ–Β–¥–Ϋ―é―é –¥–Β–Κ–Α–¥―É, –Ω–Ψ–Μ–Ψ–Ε–Η―²–Β–Μ―¨–Ϋ―΄–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ ―¹–Κ–Α–Ζ–Α–Μ–Η―¹―¨ –Ϋ–Α ―²–Β―΅–Β–Ϋ–Η–Η –Η –Η―¹―Ö–Ψ–¥–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è. Uhlig T. –Η ―¹–Ψ–Α–≤―². [2] –Ω―Ä–Ψ–≤–Β–Μ–Η –Ψ–Ω―Ä–Ψ―¹ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –†–ê, –Η―¹–Ω–Ψ–Μ―¨–Ζ―É―è 4 –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ–Α (Modified Health assessment Questionnaire, SF–36, Arthritis impact Measurement Scales 2, VAS), –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―â–Η–Β –Ψ―Ü–Β–Ϋ–Η―²―¨ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β –Α―¹–Ω–Β–Κ―²―΄ –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η. –†–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Α–Ϋ–Α–Μ–Η–Ζ–Α –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Η, ―΅―²–Ψ –Ζ–Α –¥–Β―¹―è―²–Η–Μ–Β―²–Ϋ–Η–Ι –Ω–Β―Ä–Η–Ψ–¥ (1994–2004) –Ω―Ä–Ψ–Η–Ζ–Ψ―à–Μ–Α –Ω–Ψ–Ζ–Η―²–Η–≤–Ϋ–Α―è –¥–Η–Ϋ–Α–Φ–Η–Κ–Α –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η –Ω–Ψ –≤―¹–Β–Φ –Ψ―Ü–Β–Ϋ–Η–≤–Α–Β–Φ―΄–Φ –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―è–Φ. –£ ―²–Α–±–Μ–Η―Ü–Β 1 –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ–Α –¥–Η–Ϋ–Α–Φ–Η–Κ–Α –Ψ–¥–Ϋ–Ψ–≥–Ψ –Η–Ζ –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Β–Ι –±–Ψ–Μ–Η.
–ê–Ϋ–Α–Μ–Ψ–≥–Η―΅–Ϋ―΄–Β –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è –Ω―Ä–Ψ–Η–Ζ–Ψ―à–Μ–Η –≤ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η ―³–Η–Ζ–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Η –Φ–Β–Ϋ―²–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η –±–Ψ–Μ―¨–Ϋ―΄―Ö. –û―¹–Ψ–±–Ψ –Α–≤―²–Ψ―Ä―΄ –Ψ―²–Φ–Β―΅–Α―é―² ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ ―Ä–Α–Ϋ–Ϋ–Η–Φ –†–ê, ―΅―²–Ψ, –Ω–Ψ –Η―Ö –Φ–Ϋ–Β–Ϋ–Η―é, ―¹–≤―è–Ζ–Α–Ϋ–Ψ ―¹ –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η–Β–Φ ―¹―²―Ä–Α―²–Β–≥–Η–Η –Μ–Β―΅–Β–Ϋ–Η―è, –Α –Η–Φ–Β–Ϋ–Ϋ–Ψ ―Ä–Α–Ϋ–Ϋ–Β–Ι –Α–≥―Ä–Β―¹―¹–Η–≤–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Β–Ι [2].
–û–¥–Ϋ–Η–Φ –Η–Ζ –Ω–Β―Ä–≤―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ ―¹ –¥–Ψ–Κ–Α–Ζ–Α–Ϋ–Ϋ―΄–Φ –Ω–Α―²–Ψ–≥–Β–Ϋ–Β―²–Η―΅–Β―¹–Κ–Η–Φ –¥–Β–Ι―¹―²–≤–Η–Β–Φ –Ω―Ä–Η –†–ê ―è–≤–Μ―è–Β―²―¹―è –Φ–Β―²–Ψ―²―Ä–Β–Κ―¹–Α―² (–€–Δ). –£ –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Η―Ö ―Ä–Β–Κ–Ψ–Φ–Β–Ϋ–¥–Α―Ü–Η―è―Ö –Ω–Ψ –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η―é –€–Δ –Κ–Ψ–Ϋ―¹―²–Α―²–Η―Ä―É–Β―²―¹―è, ―΅―²–Ψ –Ψ–Ϋ ―¹–Ϋ–Η–Ε–Α–Β―² –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –±–Ψ–Μ–Β–Ζ–Ϋ–Η, ―΅–Α―¹―²–Ψ―²―É ―¹–Φ–Β―Ä―²–Β–Μ―¨–Ϋ―΄―Ö –Η―¹―Ö–Ψ–¥–Ψ–≤, –≤ ―².―΅. –Ψ―² –Κ–Α―Ä–¥–Η–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Ϋ―΄―Ö –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η–Ι [3]. –î–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–Β –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β «–Ζ–Ψ–Μ–Ψ―²–Ψ–≥–Ψ ―¹―²–Α–Ϋ–¥–Α―Ä―²–Α» –≤ ―²–Β―Ä–Α–Ω–Η–Η –†–ê –Φ–Ψ–Ε–Β―² –Ω―Ä–Η–≤–Β―¹―²–Η –Κ ―Ä–Α–Ζ–≤–Η―²–Η―é –≤―²–Ψ―Ä–Η―΅–Ϋ–Ψ–Ι –Ϋ–Β―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Η–Μ–Η ―Ä–Α–Ζ–≤–Η―²–Η―é –Ω–Ψ–±–Ψ―΅–Ϋ―΄―Ö ―ç―³―³–Β–Κ―²–Ψ–≤, ―΅―²–Ψ ―²―Ä–Β–±―É–Β―² –Μ–Η–±–Ψ ―É―¹–Η–Μ–Β–Ϋ–Η―è ―²–Β―Ä–Α–Ω–Η–Η –±–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Φ–Η –Α–≥–Β–Ϋ―²–Α–Φ–Η (–≤ –Ω–Β―Ä–≤–Ψ–Φ ―¹–Μ―É―΅–Α–Β), –Μ–Η–±–Ψ –Β–≥–Ψ –Ζ–Α–Φ–Β–Ϋ―΄ –Ϋ–Α –¥―Ä―É–≥–Ψ–Ι –±–Α–Ζ–Η―¹–Ϋ―΄–Ι –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Ι –Ω―Ä–Β–Ω–Α―Ä–Α―² (–ë–ü–£–ü) (–≤–Ψ –≤―²–Ψ―Ä–Ψ–Φ).
–£ –Κ–Α―΅–Β―¹―²–≤–Β –Ϋ–Α–Η–±–Ψ–Μ–Β–Β –Ω–Α―²–Ψ–≥–Β–Ϋ–Β―²–Η―΅–Β―¹–Κ–Η––Ψ–±–Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –†–ê –Ϋ–Α―Ä―è–¥―É ―¹ –€–Δ –Η―¹–Ω–Ψ–Μ―¨–Ζ―É―é―² –Μ–Β―³–Μ―É–Ϋ–Ψ–Φ–Η–¥ (–ê―Ä–Α–≤–Α), –Ψ–±–Μ–Α–¥–Α―é―â–Η–Ι –Η–Φ–Φ―É–Ϋ–Ψ–Φ–Ψ–¥―É–Μ–Η―Ä―É―é―â–Η–Φ –Η –Α–Ϋ―²–Η–Ω―Ä–Ψ–Μ–Η―³–Β―Ä–Α―²–Η–≤–Ϋ―΄–Φ –¥–Β–Ι―¹―²–≤–Η–Β–Φ [4].
–¦–Β―³–Μ―É–Ϋ–Ψ–Φ–Η–¥ (–¦) – ―¹–Η–Ϋ―²–Β―²–Η―΅–Β―¹–Κ–Η–Ι –¥–Β―Ä–Η–≤–Α―² –Η–Ζ–Ψ–Κ―¹–Ψ–Ζ–Ψ–Μ–Α. –Δ–Β―Ä–Α–Ω–Β–≤―²–Η―΅–Β―¹–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨―é –Ψ–±–Μ–Α–¥–Α–Β―² –Β–≥–Ψ –Φ–Β―²–Α–±–Ψ–Μ–Η―² – –ê771726, ―¹―²–Α–±–Η–Μ―¨–Ϋ–Α―è –Κ–Ψ–Ϋ―Ü–Β–Ϋ―²―Ä–Α―Ü–Η―è –Κ–Ψ―²–Ψ―Ä–Ψ–≥–Ψ –≤ –Ω–Μ–Α–Ζ–Φ–Β –¥–Ψ―¹―²–Η–≥–Α–Β―²―¹―è –Ω―Ä–Η–Φ–Β―Ä–Ϋ–Ψ ―΅–Β―Ä–Β–Ζ 7 –Ϋ–Β–¥–Β–Μ―¨ –Ω―Ä–Η–Β–Φ–Α 20 –Φ–≥/―¹―É―²., –±–Ψ–Μ–Β–Β –±―΄―¹―²―Ä–Ψ–Β –¥–Ψ―¹―²–Η–Ε–Β–Ϋ–Η–Β –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ –Ω―Ä–Η –Ω―Ä–Η–Β–Φ–Β –≤ ―²–Β―΅–Β–Ϋ–Η–Β 3 –¥–Ϋ–Β–Ι –Ϋ–Α―¹―΄―â–Α―é―â–Β–Ι –¥–Ψ–Ζ―΄ 100 –Φ–≥/―¹―É―².
–€–Η–≥―Ä–Α―Ü–Η–Β–Ι –Α–Κ―²–Η–≤–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Μ–Η–Φ―³–Ψ―Ü–Η―²–Ψ–≤ –Η –Φ–Ψ–Ϋ–Ψ―Ü–Η―²–Ψ–≤ –≤ ―¹–Η–Ϋ–Ψ–≤–Η–Α–Μ―¨–Ϋ―É―é ―²–Κ–Α–Ϋ―¨ –Ω―Ä–Η –†–ê –Ψ–±―É―¹–Μ–Ψ–≤–Μ–Β–Ϋ–Α –Ϋ–Α―΅–Α–Μ―¨–Ϋ–Α―è ―¹―²–Α–¥–Η―è ―¹–Η–Ϋ–Ψ–≤–Η–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η―è, –Κ–Ψ―²–Ψ―Ä–Ψ–Β –≤–Ω–Ψ―¹–Μ–Β–¥―¹―²–≤–Η–Η –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –¥–Β–≥―Ä–Α–¥–Α―Ü–Η–Η ―¹―É―¹―²–Α–≤–Ψ–≤ [5].
–ê–Κ―²–Η–≤–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄–Β –Μ–Η–Φ―³–Ψ―Ü–Η―²―΄ ―²―Ä–Β–±―É―é―² –Ω―Ä–Η –†–ê –≤ 8 ―Ä–Α–Ζ –±–Ψ–Μ―¨―à–Β –Ω–Η―Ä–Η–Φ–Η–¥–Η–Ϋ–Α –¥–Μ―è –Ω–Β―Ä–Β―Ö–Ψ–¥–Α –Η–Ζ G1–―³–Α–Ζ―΄ –≤ S–―³–Α–Ζ―É –≤ –Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–Φ ―Ü–Η–Κ–Μ–Β. –¦ ―΅–Β―Ä–Β–Ζ –Β–≥–Ψ –Α–Κ―²–Η–≤–Ϋ―΄–Ι –Φ–Β―²–Α–±–Ψ–Μ–Η―² –ê771726 –Η–Ϋ–≥–Η–±–Η―Ä―É–Β―² ―³–Β―Ä–Φ–Β–Ϋ―² –¥–Η–≥–Η–¥―Ä–Ψ–Ψ―Ä–Ψ―²–Α―² –¥–Β–≥–Η–¥―Ä–Ψ–≥–Β–Ϋ–Α–Ζ―É (–î–ù–û–î–ù), –Ψ–≥―Ä–Α–Ϋ–Η―΅–Η–≤–Α―è ―¹–Η–Ϋ―²–Β–Ζ de novo –Ω–Η―Ä–Η–Φ–Η–¥–Η–Ϋ–Α –≤ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –Ω―É–Μ–Α―Ö –Κ–Μ–Β―²–Ψ–Κ. –‰–Ϋ–≥–Η–±–Η―Ü–Η―è –≤―²–Ψ―Ä–Ψ–≥–Ψ ―³–Β―Ä–Φ–Β–Ϋ―²–Α – ―²–Η―Ä–Ψ–Ζ–Η–Ϋ–Κ–Η–Ϋ–Α–Ζ―΄, –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Κ–Ψ―²–Ψ―Ä–Ψ–Ι –Ω–Ψ–¥–Α–≤–Μ―è–Β―²―¹―è –≤―΄―¹–Ψ–Κ–Η–Φ–Η –Κ–Ψ–Ϋ―Ü–Β–Ϋ―²―Ä–Α―Ü–Η―è–Φ–Η –¦, – –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ ―¹–Ϋ–Η–Ε–Β–Ϋ–Η―é –Ω―Ä–Ψ–¥―É–Κ―Ü–Η–Η –‰–¦–2, –Ω–Ψ–≤―΄―à–Β–Ϋ–Η―é ―É―Ä–Ψ–≤–Ϋ―è –Η–Φ–Φ―É–Ϋ–Ψ―¹―É–Ω―Ä–Β―¹―¹–Η–≤–Ϋ–Ψ–≥–Ψ ―Ü–Η―²–Ψ–Κ–Η–Ϋ–Α – ―²―Ä–Α–Ϋ―¹―³–Ψ―Ä–Φ–Η―Ä―É―é―â–Β–≥–Ψ ―³–Α–Κ―²–Ψ―Ä–Α ―Ä–Ψ―¹―²–Α β1. –ë–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Β –¥–Β–Ι―¹―²–≤–Η–Β –¦ –Ψ―¹―É―â–Β―¹―²–≤–Μ―è–Β―²―¹―è –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Η–Φ–Η –Ω―É―²―è–Φ–Η (―Ä–Η―¹. 1).
–ê–Ϋ―²–Η–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Ι ―ç―³―³–Β–Κ―² –¦ –Ω―Ä–Ψ―è–≤–Μ―è–Β―²―¹―è –Ω–Ψ–¥–Α–≤–Μ–Β–Ϋ–Η–Β–Φ –Φ–Β–Ε–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–≥–Ψ –Κ–Ψ–Ϋ―²–Α–Κ―²–Α –Δ––Μ–Η–Φ―³–Ψ―Ü–Η―²–Ψ–≤ –Η ―¹–Η–Ϋ–Ψ–≤–Η–Ψ―Ü–Η―²–Ψ–≤, ―΅―²–Ψ ―¹–Ϋ–Η–Ε–Α–Β―² –≤―΄―Ä–Α–±–Ψ―²–Κ―É –Φ–Β―²–Α–Μ–Μ–Ψ–Ω―Ä–Ψ―²–Β–Η–Ϋ–Α–Ζ (–€–€–†) –Η ―²–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ –Ζ–Α–Φ–Β–¥–Μ―è–Β―² –¥–Β―¹―²―Ä―É–Κ―²–Η–≤–Ϋ―΄–Ι –Ω―Ä–Ψ―Ü–Β―¹―¹. –ü–Ψ–Ζ–Η―²–Η–≤–Ϋ–Ψ–Β –¥–Β–Ι―¹―²–≤–Η–Β –¦ –Ϋ–Α –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Η–Ι ―Ä–Β–Α–Μ–Η–Ζ―É–Β―²―¹―è –Ζ–Α ―¹―΅–Β―² –Ω–Ψ–≤―΄―à–Β–Ϋ–Η―è –≤―΄―Ä–Α–±–Ψ―²–Κ–Η ―²–Κ–Α–Ϋ–Β–≤–Ψ–≥–Ψ –Η–Ϋ–≥–Η–±–Η―²–Ψ―Ä–Α –€–€–† (TIMP), –Α–Ϋ―²–Α–≥–Ψ–Ϋ–Η―¹―²–Α –‰–¦–1R (–‰–¦–1Ra), –Ω–Ψ–¥–Α–≤–Μ–Β–Ϋ–Η―è ―ç–Κ―¹–Ω―Ä–Β―¹―¹–Η–Η –Φ–Ψ–Μ–Β–Κ―É–Μ –Α–¥–≥–Β–Ζ–Η–Η – ICAM–1, VCAM–1 –Η RANKL.
–¦ –≤–Μ–Η―è–Β―² –Ϋ–Α ―è–¥–Β―Ä–Ϋ―΄–Ι ―³–Α–Κ―²–Ψ―Ä NFkB, ―¹–Ϋ–Η–Ε–Α―è –≥–Μ–Η–Κ–Ψ–Ζ–Η–Μ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –Φ–Ψ–Μ–Β–Κ―É–Μ –Α–¥–≥–Β–Ζ–Η–Η, –Α ―²–Α–Κ–Ε–Β –Ϋ–Α ―²―Ä–Α–Ϋ―¹―ç–Ϋ–¥–Ψ―²–Β–Μ–Η–Α–Μ―¨–Ϋ―É―é –Φ–Η–≥―Ä–Α―Ü–Η―é –Φ–Ψ–Ϋ–Ψ–Ϋ―É–Κ–Μ–Β–Α―Ä–Ψ–≤ –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Ψ–Ι –Κ―Ä–Ψ–≤–Η (PBMC) –Ζ–Α –Ω–Ψ–¥–Α–≤–Μ–Β–Ϋ–Η―è –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Φ–Ψ–Μ–Β–Κ―É–Μ –Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–Ι –Α–¥–≥–Β–Ζ–Η–Η, ―²–Α–Κ–Η―Ö –Κ–Α–Κ CD44 –Η PBMC––≥–Η–Α–Μ―É―Ä–Ψ–Ϋ–Α–Ϋ–Α, ―΅―²–Ψ –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –±–Μ–Ψ–Κ–Η―Ä–Ψ–≤–Κ–Β –Ω–Β―Ä–Β–¥–≤–Η–Ε–Β–Ϋ–Η―è –Κ–Μ–Β―²–Ψ–Κ –≤ ―¹–Η–Ϋ–Ψ–≤–Η–Α–Μ―¨–Ϋ―É―é ―²–Κ–Α–Ϋ―¨.
–£–Α–Ε–Ϋ―΄–Φ –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Ψ–Φ –¥–Β–Ι―¹―²–≤–Η―è –¦ ―è–≤–Μ―è–Β―²―¹―è ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Ω―Ä–Ψ–¥―É–Κ―Ü–Η–Η –Φ–Α–Κ―Ä–Ψ―³–Α–≥–Α–Φ–Η –Ω―Ä–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄―Ö ―Ü–Η―²–Ψ–Κ–Η–Ϋ–Ψ–≤ – –Λ–ù–û–α, –‰–¦–1β, –‰–¦–6 –Η ―³–Β―Ä–Φ–Β–Ϋ―²–Α ―Ü–Η–Κ–Μ–Ψ–Ψ–Κ―¹–Η–≥–Β–Ϋ–Α–Ζ―΄ [6].
–î–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ, ―΅―²–Ψ ―ç―Ä–Ψ–Ζ–Η–≤–Ϋ―΄–Ι –Ω―Ä–Ψ―Ü–Β―¹―¹ –≤ ―¹―É―¹―²–Α–≤–Α―Ö –Ω―Ä–Η –†–ê –≤–Ψ–Ζ–Ϋ–Η–Κ–Α–Β―² –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η –Ψ–¥–Ϋ–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ–Ψ ―¹ –Ω–Ψ―è–≤–Μ–Β–Ϋ–Η–Β–Φ –Ω–Β―Ä–≤―΄―Ö ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤ –±–Ψ–Μ–Β–Ζ–Ϋ–Η, –Ω–Ψ―ç―²–Ψ–Φ―É –Η–Φ–Β–Ϋ–Ϋ–Ψ –Α–Κ―²–Η–≤–Ϋ–Α―è ―²–Β―Ä–Α–Ω–Η―è –†–ê –Ϋ–Α ―Ä–Α–Ϋ–Ϋ–Η―Ö ―ç―²–Α–Ω–Α―Ö –Η–Φ–Β–Β―² –≤–Α–Ε–Ϋ–Ψ–Β –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β.
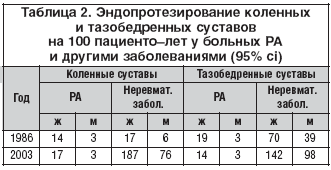
–£ ―Ä–Α–±–Ψ―²–Β Welsing P. –Η ―¹–Ψ–Α–≤―². [7] –Ω–Ψ–¥―΅–Β―Ä–Κ–Η–≤–Α–Β―²―¹―è ―Ä–Ψ–Μ―¨ –Α–≥―Ä–Β―¹―¹–Η–≤–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –ë–ü–£–ü –Ϋ–Α –Η―¹―Ö–Ψ–¥ –±–Ψ–Μ–Β–Ζ–Ϋ–Η ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö ―Ä–Α–Ϋ–Ϋ–Η–Φ –†–ê –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ –±–Ψ–Μ–Β―é―â–Η–Φ–Η. –‰–Φ–Β–Ϋ–Ϋ–Ψ ―Ä–Α–Ϋ–Ϋ–Β–Ι –¥–Η–Α–≥–Ϋ–Ψ―¹―²–Η–Κ–Ψ–Ι –†–ê –Η –Α–≥―Ä–Β―¹―¹–Η–≤–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Β–Ι Sokka T. –Η ―¹–Ψ–Α–≤―². [8] –Ψ–±―ä―è―¹–Ϋ―è―é―² ―³–Α–Κ―² –Ψ―²―¹―É―²―¹―²–≤–Η―è ―Ä–Ψ―¹―²–Α –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ―¹―²–Η ―ç–Ϋ–¥–Ψ–Ω―Ä–Ψ―²–Β–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Κ–Ψ–Μ–Β–Ϋ–Ϋ―΄―Ö –Η ―²–Α–Ζ–Ψ–±–Β–¥―Ä–Β–Ϋ–Ϋ―΄―Ö ―¹―É―¹―²–Α–≤–Ψ–≤ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö –†–ê –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Ϋ–Β―Ä–Β–≤–Φ–Α―²–Η―΅–Β―¹–Κ–Η–Φ–Η –±–Ψ–Μ―¨–Ϋ―΄–Φ–Η (―²–Α–±–Μ. 2). –≠–Ϋ–¥–Ψ–Ω―Ä–Ψ―²–Β–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –Κ–Ψ–Μ–Β–Ϋ–Ϋ―΄―Ö ―¹―É―¹―²–Α–≤–Ψ–≤ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ψ ―É 14 –Η 19 –Ϋ–Α 100 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ––Μ–Β―² ―É –Ε–Β–Ϋ―â–Η–Ϋ –Η 3 –Η 3 ―É –Φ―É–Ε―΅–Η–Ϋ, –±–Ψ–Μ–Β―é―â–Η―Ö –†–ê, –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ 17 –Η 210 ―É –Ε–Β–Ϋ―â–Η–Ϋ –Η 6 –Η 83 ―É –Φ―É–Ε―΅–Η–Ϋ – –Ϋ–Β―Ä–Β–≤–Φ–Α―²–Η―΅–Β―¹–Κ–Η―Ö –±–Ψ–Μ―¨–Ϋ―΄―Ö (―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ –≤ 1986 –Η 2003 –≥–≥.).
–£ –Μ–Η―²–Β―Ä–Α―²―É―Ä–Β –Η–Φ–Β–Β―²―¹―è –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ–Β ―΅–Η―¹–Μ–Ψ ―Ä–Α–±–Ψ―², –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Α―é―â–Η―Ö ―Ü–Β–Μ–Β―¹–Ψ–Ψ–±―Ä–Α–Ζ–Ϋ–Ψ―¹―²―¨ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η―è –¦ –Ϋ–Α ―Ä–Α–Ϋ–Ϋ–Β–Ι ―¹―²–Α–¥–Η–Η –†–ê. –‰–Ζ –±–Α–Ζ―΄ –¥–≤―É―Ö –Ω–Μ–Α―Ü–Β–±–Ψ––Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ―΄―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι MN301 –Η US301, –≤ –Κ–Ψ―²–Ψ―Ä―΄―Ö –Ψ―Ü–Β–Ϋ–Η–≤–Α–Μ–Η ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –¦ –≤ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η ―¹ ―¹―É–Μ―¨―³–Α―¹–Α–Μ–Α–Ζ–Η–Ϋ–Ψ–Φ (–Γ–Γ) –Η –Φ–Β―²–Ψ―²―Ä–Β–Κ―¹–Α―²–Ψ–Φ –Ω―Ä–Η –†–ê ―¹ –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨―é ≤2 –≥–Ψ–¥–Α, –±―΄–Μ–Ψ –≤―΄–±―Ä–Α–Ϋ–Ψ 233 –±–Ψ–Μ―¨–Ϋ―΄―Ö, ―Ä–Α–Ϋ–Β–Β –Ϋ–Β –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –ë–ü–£–ü, ―¹ –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨―é –Ψ―² 0,3 –¥–Ψ 0,8 –≥–Ψ–¥–Α. –£ –Ω–Β―Ä–≤–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Ζ–Α 6 –Φ–Β―¹. –Μ–Β―΅–Β–Ϋ–Η―è –ê–ΓR 50% –Ψ―²–≤–Β―² –±―΄–Μ –Ω–Ψ–Μ―É―΅–Β–Ϋ ―É 45,7 –Ϋ–Α –¦ –Η 38,8% –Ϋ–Α –Γ–Γ –Ω―Ä–Ψ―²–Η–≤ 22,2% –Ϋ–Α –Ω–Μ–Α―Ü–Β–±–Ψ (–ü–Μ) (―Ä=0,036 –¦––ü–Μ.). –£–Ψ –≤―²–Ψ―Ä–Ψ–Φ –Ζ–Α 12 –Φ–Β―¹. –Ω–Β―Ä–Η–Ψ–¥ –Μ–Β―΅–Β–Ϋ–Η―è –ê–ΓR 50% –Ψ―²–≤–Β―² –±―΄–Μ ―É 34,8% –Ϋ–Α –¦ –Η 23,3% –Ϋ–Α –€–Δ –Ω―Ä–Ψ―²–Η–≤ 0% –Ϋ–Α –Ω–Μ–Α―Ü–Β–±–Ψ (―Ä=0,006 –¦––ü–Μ.). –†–Β–Ϋ―²–≥–Β–Ϋ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Α―è –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―è –±―΄–Μ–Α –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –Ϋ–Η–Ε–Β ―É –Μ–Β―΅–Β–Ϋ–Ϋ―΄―Ö –¦, ―΅–Β–Φ –Ϋ–Α –ü–Μ, –Η ―¹–Ψ–Ω–Ψ―¹―²–Α–≤–Η–Φ–Α ―¹ –Μ–Β―΅–Β–Ϋ―΄–Φ–Η –Γ–Γ –Η –€–Δ [10]. –ü―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η –≤–Ψ –≤―¹–Β―Ö –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è―Ö ―É–Κ–Α–Ζ―΄–≤–Α–Β―²―¹―è, ―΅―²–Ψ ―Ä–Β–Ϋ―²–≥–Β–Ϋ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Α―è –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―è –±―΄–Μ–Α –±–Ψ–Μ―¨―à–Β –Ζ–Α –Ω–Β―Ä–Η–Ψ–¥ –Μ–Β―΅–Β–Ϋ–Η―è ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, ―É–Ε–Β –Η–Φ–Β–≤―à–Η―Ö ―ç―Ä–Ψ–Ζ–Η–≤–Ϋ―΄–Β –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è –Κ –Ϋ–Α―΅–Α–Μ―É ―²–Β―Ä–Α–Ω–Η–Η –¦, ―΅―²–Ψ –Β―â–Β ―Ä–Α–Ζ –Ω–Ψ–¥―΅–Β―Ä–Κ–Η–≤–Α–Β―² –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ―¹―²―¨ –Β–≥–Ψ ―Ä–Α–Ϋ–Ϋ–Β–≥–Ψ –≤–Κ–Μ―é―΅–Β–Ϋ–Η―è –≤ ―¹―Ö–Β–Φ―É –Μ–Β―΅–Β–Ϋ–Η―è –†–ê.
–£ ―Ä–Α–±–Ψ―²–Β Combe –£. –Η ―¹–Ψ–Α–≤―². –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ―΄ –¥–Α–Ϋ–Ϋ―΄–Β –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―ç―³―³–Β–Κ―²–Α –¦ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö –†–ê, ―Ä–Α–Ϋ–Β–Β –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö (127) –Η –Ϋ–Β –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö (272) –€–Δ [11]. –ê–ΓR 20, 50 –Η 70% –Ψ―²–≤–Β―² ―É ―Ä–Α–Ϋ–Β–Β –Μ–Β―΅–Β–Ϋ–Ϋ―΄―Ö –€–Δ –±―΄–Μ 48,9, 20,6 –Η 7,7% ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ, –≤ ―²–Ψ –≤―Ä–Β–Φ―è –Κ–Α–Κ ―É –Ϋ–Β–Μ–Β―΅–Β–Ϋ–Ϋ―΄―Ö –Ψ–Ϋ –±―΄–Μ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –≤―΄―à–Β – 62,2, 28,4 –Η 9,5% ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ.
–ê–Ϋ–Α–Μ–Η–Ζ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ II –Η III ―³–Α–Ζ―΄ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι –Ω–Ψ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –¦, –Ω–Ψ–Κ–Α–Ζ–Α–Μ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Β ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η, –Κ–Ψ―²–Ψ―Ä–Ψ–Β –Κ–Ψ―Ä―Ä–Β–Μ–Η―Ä–Ψ–≤–Α–Μ–Ψ ―¹ –ê–ΓR––Κ―Ä–Η―²–Β―Ä–Η―è–Φ–Η –Η –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö ―¹ 50% –ê–ΓR ―É–Μ―É―΅―à–Β–Ϋ–Η–Β–Φ [12].
–‰―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è, –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ―΄–Β –≤ –ù–‰–‰–† –†–ê–€–ù, –Ω–Ψ–¥―²–≤–Β―Ä–¥–Η–Μ–Η –≤―΄―¹–Ψ–Κ―É―é ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –¦ –Ω―Ä–Η ―Ä–Α–Ϋ–Ϋ–Β–Φ –†–ê [14,15].
–£ ―Ä–Β–Α–Μ–Η–Ζ–Α―Ü–Η–Η –†–Ψ―¹―¹–Η–Ι―¹–Κ–Ψ–Ι –Ω―Ä–Ψ–≥―Ä–Α–Φ–Φ―΄ –†–ê–î–‰–ö–ê–¦ –Ω–Ψ –¥–Η–Α–≥–Ϋ–Ψ―¹―²–Η–Κ–Β –Η –Μ–Β―΅–Β–Ϋ–Η―é ―Ä–Α–Ϋ–Ϋ–Β–≥–Ψ –†–ê [16] 30 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ (4 –Φ―É–Ε―΅–Η–Ϋ –Η 26 –Ε–Β–Ϋ―â–Η–Ϋ) –Ω–Ψ–Μ―É―΅–Α–Μ–Η –≤ –Κ–Α―΅–Β―¹―²–≤–Β –Ω–Β―Ä–≤–Ψ–≥–Ψ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α –¦ ―¹ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β–Φ –Ϋ–Α―¹―΄―â–Α―é―â–Β–Ι –¥–Ψ–Ζ―΄ 100 –Φ–≥ – 3 –¥–Ϋ―è, –Ζ–Α―²–Β–Φ 20 –Φ–≥/―¹―É―². –ö –Ϋ–Α―΅–Α–Μ―É ―²–Β―Ä–Α–Ω–Η–Η –¦ ―É 66,7% –Η–Φ–Β–Μ–Ψ―¹―¨ ―¹―É–Ε–Β–Ϋ–Η–Β ―¹―É―¹―²–Α–≤–Ϋ–Ψ–Ι ―â–Β–Μ–Η –Η ―É 16,7% – ―ç―Ä–Ψ–Ζ–Η–Η –≤ ―¹―É―¹―²–Α–≤–Α―Ö –Κ–Η―¹―²–Β–Ι –Η/–Η–Μ–Η ―¹―²–Ψ–Ω. DAS 28 –±―΄–Μ ―Ä–Α–≤–Β–Ϋ 6,43±0,94, ―΅―²–Ψ ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É–Β―² –≤―΄―¹–Ψ–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Ω―Ä–Ψ―Ü–Β―¹―¹–Α. 33,3% –Ω–Ψ–Μ―É―΅–Α–Μ–Η –Κ–Ψ―Ä―²–Η–Κ–Ψ―¹―²–Β―Ä–Ψ–Η–¥―΄ –≤ –¥–Ψ–Ζ–Β 10 –Φ–≥/―¹―É―². –ü–Ψ–Μ–Ϋ―΄–Ι –≥–Ψ–¥–Η―΅–Ϋ―΄–Ι –Κ―É―Ä―¹ –¦ –Ω–Ψ–Μ―É―΅–Η–Μ–Η 80% –±–Ψ–Μ―¨–Ϋ―΄―Ö. –ü–Β―Ä–≤–Η―΅–Ϋ–Α―è –Ϋ–Β―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ (–Ψ―²―¹―É―²―¹―²–≤–Η–Β 20% ―É–Μ―É―΅―à–Β–Ϋ–Η―è) –±―΄–Μ–Α ―É 3 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, ―É ―²–Α–Κ–Ψ–≥–Ψ –Ε–Β ―΅–Η―¹–Μ–Α –Ω―Ä–Β–Ω–Α―Ä–Α―² –Ψ―²–Φ–Β–Ϋ–Β–Ϋ –Η–Ζ––Ζ–Α –Ϋ–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄―Ö ―è–≤–Μ–Β–Ϋ–Η–Ι (–Ω–Ψ–≤―΄―à–Β–Ϋ–Η–Β ―²―Ä–Α–Ϋ―¹–Α–Φ–Η–Ϋ–Α–Ζ, –≤―΄–Ω–Α–¥–Β–Ϋ–Η–Β –≤–Ψ–Μ–Ψ―¹) –Ϋ–Α 8–12––Φ –Φ–Β―¹. ―²–Β―Ä–Α–Ω–Η–Η.
DAS 28 –Κ 3––Φ―É –Φ–Β―¹. ―¹–Ψ―¹―²–Α–≤–Η–Μ 4,91±0,74, –Κ 6––Φ―É –Φ–Β―¹.– 4,10±0,72, –Κ 12––Φ―É –Φ–Β―¹. – 3,07±0,54, ―΅―²–Ψ ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É–Β―² –Ϋ–Η–Ζ–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η―è. –ü–Ψ –Κ―Ä–Η―²–Β―Ä–Η―è–Φ –ê–ΓR –Ω–Ψ–Μ―É―΅–Β–Ϋ―΄ ―¹–Μ–Β–¥―É―é―â–Η–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄: 20% –ê–ΓR – ―É 1 –±–Ψ–Μ―¨–Ϋ–Ψ–≥–Ψ, 50% –ê–ΓR – ―É 5 –±–Ψ–Μ―¨–Ϋ―΄―Ö, 70% –ê–ΓR – 7 –±–Ψ–Μ―¨–Ϋ―΄―Ö. –ö–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Α―è ―Ä–Β–Φ–Η―¹―¹–Η―è –¥–Ψ―¹―²–Η–≥–Ϋ―É―²–Α ―É 13 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, ―΅―²–Ψ ―¹–≤–Η–¥–Β―²–Β–Μ―¨―¹―²–≤―É–Β―² –Ψ –≤―΄―¹–Ψ–Κ–Ψ–Ι ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –¦.
–ü–Ψ –Ϋ–Α―à–Η–Φ –¥–Α–Ϋ–Ϋ―΄–Φ [17,18], –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Α―è ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –¦ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö –†–ê ―¹ –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨―é –Φ–Β–Ϋ–Β–Β 2 –Μ–Β―² (16,0±10,1 –Φ–Β―¹.), 14 –Η–Ζ –Κ–Ψ―²–Ψ―Ä―΄―Ö –Ω–Ψ–Μ―É―΅–Α–Μ–Α –¦, 20 – –€–Δ, –Κ–Ψ―Ä―Ä–Β–Μ–Η―Ä–Ψ–≤–Α–Μ–Α ―¹–Ψ ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β–Φ ―É―Ä–Ψ–≤–Ϋ―è –€–€–†–3, ―É―Ä–Ψ–≤–Ϋ–Β–Φ –Λ–ù–û–α –Η –‰–¦–6. –™–Ψ–¥–Η―΅–Ϋ–Ψ–Β –Ϋ–Α–±–Μ―é–¥–Β–Ϋ–Η–Β –Ζ–Α –±–Ψ–Μ―¨–Ϋ―΄–Φ–Η –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Ψ, ―΅―²–Ψ –Ω―Ä–Η―Ä–Ψ―¹―² ―ç―Ä–Ψ–Ζ–Η–Ι –Κ 6––Φ―É –Φ–Β―¹. –Μ–Β―΅–Β–Ϋ–Η―è –¦ ―¹–Ψ―¹―²–Α–≤–Η–Μ 1,0±1,35, –Α –Κ 12––Φ―É –Φ–Β―¹. – 0,75±2,01, ―².–Β. ―²–Β–Φ–Ω –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Ζ–Α–Φ–Β–¥–Μ―è–Μ―¹―è –Ω–Ψ –Φ–Β―Ä–Β ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η―è ―¹―Ä–Ψ–Κ–Ψ–≤ –Ω―Ä–Η–Β–Φ–Α –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α.
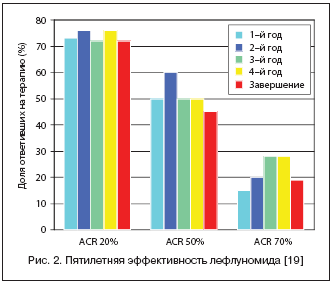
–‰–Ζ–≤–Β―¹―²–Ϋ–Ψ, ―΅―²–Ψ –Ω―Ä–Η –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Η –ë–ü–£–ü –Η―Ö ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ ―¹–Ϋ–Η–Ε–Α–Β―²―¹―è. –£ ―Ä–Α–±–Ψ―²–Β Kalden J.R. [19] –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ, ―΅―²–Ψ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Η –±–Β–Ζ–Ψ–Ω–Α―¹–Ϋ–Ψ―¹―²―¨ ―²–Β―Ä–Α–Ω–Η–Η –¦ ―¹–Ψ―Ö―Ä–Α–Ϋ―è―é―²―¹―è –Ϋ–Α –≤―΄―¹–Ψ–Κ–Ψ–Φ ―É―Ä–Ψ–≤–Ϋ–Β –Ϋ–Α –Ω―Ä–Ψ―²―è–Ε–Β–Ϋ–Η–Η 5––Μ–Β―²–Ϋ–Β–≥–Ψ –Ϋ–Α–±–Μ―é–¥–Β–Ϋ–Η―è 214 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, ―¹―²―Ä–Α–¥–Α―é―â–Η―Ö –†–ê (―Ä–Η―¹. 2).
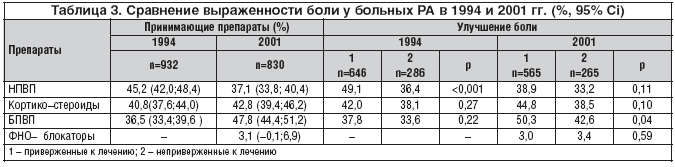
–£–Α–Ε–Ϋ―΄–Φ –Φ–Ψ–Φ–Β–Ϋ―²–Ψ–Φ –¥–Μ―è –Ω–Ψ–Μ―É―΅–Β–Ϋ–Η―è ―Ö–Ψ―Ä–Ψ―à–Β–≥–Ψ ―ç―³―³–Β–Κ―²–Α ―è–≤–Μ―è–Β―²―¹―è –Κ–Ψ–Φ–Ω–Μ–Α–Ι–Β–Ϋ―²–Ϋ–Ψ―¹―²―¨ –±–Ψ–Μ―¨–Ϋ―΄―Ö –≤ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η ―²–Β―Ä–Α–Ω–Η–Η, ―΅―²–Ψ –Ω―Ä–Ψ–¥–Β–Φ–Ψ–Ϋ―¹―²―Ä–Η―Ä–Ψ–≤–Α–Ϋ–Ψ –≤ ―Ä–Α–±–Ψ―²–Β Heiberg T. –Η ―¹–Ψ–Α–≤―². [20], –Ω―Ä–Ψ―¹–Μ–Β–¥–Η–≤―à–Η―Ö –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η–Β –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö –†–ê, –Ω―Ä–Η–≤–Β―Ä–Ε–Β–Ϋ–Ϋ―΄―Ö –Κ ―²–Β―Ä–Α–Ω–Η–Η –ë–ü–£–ü –Ζ–Α 7––Μ–Β―²–Ϋ–Η–Ι –Ω–Β―Ä–Η–Ψ–¥ (―²–Α–±–Μ. 3).
–ê–≤―²–Ψ―Ä―΄ –Ψ―²–Φ–Β―΅–Α―é―² ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β ―΅–Η―¹–Μ–Α –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ω–Ψ–Μ―É―΅–Α―é―â–Η―Ö –Κ–Α–Κ ―¹–Η–Φ–Ω―²–Ψ–Φ–Α―²–Η―΅–Β―¹–Κ–Η–Β, ―²–Α–Κ –Η –ë–ü–£–ü –≤ 2001 –≥. –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ 1994 –≥., ―΅–Β–Φ –Ψ–±―ä―è―¹–Ϋ―è―é―² –±–Ψ–Μ–Β–Β –±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ–Ψ–Β ―²–Β―΅–Β–Ϋ–Η–Β –†–ê, –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ ―É –Μ–Η―Ü, –Ω―Ä–Η–≤–Β―Ä–Ε–Β–Ϋ–Ϋ―΄―Ö –Κ –Μ–Β―΅–Β–Ϋ–Η―é.
–£ –†–Ψ―¹―¹–Η–Η –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η –Ϋ–Β –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ―΄ –≤ –Μ–Η―²–Β―Ä–Α―²―É―Ä–Β –¥–Α–Ϋ–Ϋ―΄–Β –Ω–Ψ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η―é –¦ –≤ ―Ä–Β–Α–Μ―¨–Ϋ–Ψ–Ι –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Ι –Ω―Ä–Α–Κ―²–Η–Κ–Β, –≤ ―¹–≤―è–Ζ–Η ―¹ ―΅–Β–Φ –Ψ―¹―É―â–Β―¹―²–≤–Μ―è–Β―²―¹―è –Ω―Ä–Ψ–Β–Κ―² –Ω–Ψ –Ψ―Ü–Β–Ϋ–Κ–Β ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η, –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²–Η –Η –Κ–Ψ–Φ–Ω–Μ–Α–Ι–Β–Ϋ―²–Ϋ–Ψ―¹―²–Η ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö –†–ê ―¹ –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨―é –Φ–Β–Ϋ–Β–Β 2 –Μ–Β―², –Ω–Ψ–Μ―É―΅–Α―é―â–Η―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―² –≤ –Φ–Ψ–Ϋ–Ψ―²–Β―Ä–Α–Ω–Η–Η –≤ ―Ä–Β–Α–Μ―¨–Ϋ–Ψ–Ι –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Ι –Ω―Ä–Α–Κ―²–Η–Κ–Β.
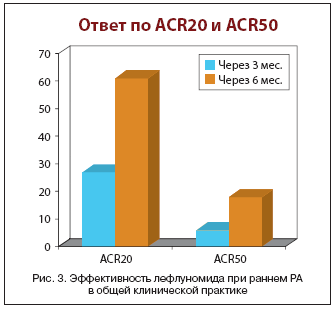
–ö –Ϋ–Α―¹―²–Ψ―è―â–Β–Φ―É –≤―Ä–Β–Φ–Β–Ϋ–Η –Ω–Ψ–Μ―É―΅–Β–Ϋ―΄ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ 6––Φ–Β―¹. ―²–Β―Ä–Α–Ω–Η–Η 51 –Ω–Α―Ü–Η–Β–Ϋ―²–Α ―¹ –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨―é –†–ê 1,5–24 –Φ–Β―¹. (12,8±7,4 –Φ–Β―¹.), ―¹―Ä–Β–¥–Ϋ–Η–Ι –≤–Ψ–Ζ―Ä–Α―¹―² –Κ–Ψ―²–Ψ―Ä―΄―Ö 48±13,1 –≥–Ψ–¥–Α. –ß–Β―Ä–Β–Ζ 3 –Φ–Β―¹. –ê–ΓR 20% –Ψ―²–≤–Β―² –Ω–Ψ–Μ―É―΅–Β–Ϋ ―É 61% –±–Ψ–Μ―¨–Ϋ―΄―Ö, ―É 18% – –ê–ΓR 50% (―Ä–Η―¹. 3).
–ù–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄–Β ―è–≤–Μ–Β–Ϋ–Η―è –Ϋ–Α–±–Μ―é–¥–Α–Μ–Η―¹―¨ –Ω–Ψ –Ψ–¥–Ϋ–Ψ–Φ―É ―¹–Μ―É―΅–Α―é: –Α–Ϋ–Β–Φ–Η―è, –Μ–Β–Ι–Κ–Ψ–Ω–Β–Ϋ–Η―è, –û–†–£–‰, –‰–ë–Γ, –Ω–Ψ–≤―΄―à–Β–Ϋ–Η–Β –ê–¦–Δ. –£―΄–±―΄–Μ–Η –Η–Ζ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è ―²―Ä–Ψ–Β: –Η–Ζ––Ζ–Α –Ϋ–Β―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η (1), –Μ–Β–Ι–Κ–Ψ–Ω–Β–Ϋ–Η–Η (1), –Ω–Ψ–≤―΄―à–Β–Ϋ–Η―è –ê–¦–Δ (1). –ü–Ψ–Μ―É–≥–Ψ–¥–Ψ–≤–Ψ–Ι –Κ―É―Ä―¹ –Μ–Β―΅–Β–Ϋ–Η―è –Ζ–Α–≤–Β―Ä―à–Η–Μ–Η 94,1% –±–Ψ–Μ―¨–Ϋ―΄―Ö, ―΅―²–Ψ ―¹–≤–Η–¥–Β―²–Β–Μ―¨―¹―²–≤―É–Β―² –Ψ–± ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η, ―Ö–Ψ―Ä–Ψ―à–Β–Ι –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²–Η –¦ –Η –Κ–Ψ–Φ–Ω–Μ–Α–Ι–Β–Ϋ―²–Ϋ–Ψ―¹―²–Η –±–Ψ–Μ―¨–Ϋ―΄―Ö –Κ ―²–Β―Ä–Α–Ω–Η–Η –≤ ―Ä–Β–Α–Μ―¨–Ϋ–Ψ–Ι –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Ι –Ω―Ä–Α–Κ―²–Η–Κ–Β [21].
–Γ –Κ–Ψ–Ϋ―Ü–Α –Ω―Ä–Ψ―à–Μ–Ψ–≥–Ψ ―¹―²–Ψ–Μ–Β―²–Η―è –Α–Κ―²–Η–≤–Ϋ–Ψ –≤–Ϋ–Β–¥―Ä―è―é―²―¹―è –≤ ―¹―Ö–Β–Φ―É –Μ–Β―΅–Β–Ϋ–Η―è –†–ê –Ϋ–Ψ–≤―΄–Β –≥–Β–Ϋ–Ϋ–Ψ––Η–Ϋ–Ε–Β–Ϋ–Β―Ä–Ϋ―΄–Β –±–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄ (–™–‰–ë–ü), –≤–Κ–Μ―é―΅–Α―è –Η–Ϋ–≥–Η–±–Η―²–Ψ―Ä―΄ –Λ–ù–û–α, –‰–¦–1 [22,23], –Κ–Ψ―²–Ψ―Ä―΄–Β –Ζ–Α–Φ–Β–¥–Μ―è―é―² ―¹―²―Ä―É–Κ―²―É―Ä–Ϋ―΄–Β –Ω–Ψ–≤―Ä–Β–Ε–¥–Β–Ϋ–Η―è ―¹―É―¹―²–Α–≤–Ψ–≤, ―΅―²–Ψ –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Β–Ϋ–Ψ –Φ–Ϋ–Ψ–≥–Ψ―΅–Η―¹–Μ–Β–Ϋ–Ϋ―΄–Φ–Η –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è–Φ–Η, –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Ϋ―΄–Φ–Η –Ϋ–Α –¥–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨–Ϋ–Ψ–Ι –Φ–Β–¥–Η―Ü–Η–Ϋ–Β. –£ –†–Ψ―¹―¹–Η–Η –Ζ–Α―Ä–Β–≥–Η―¹―²―Ä–Η―Ä–Ψ–≤–Α–Ϋ―΄ 2 –Η–Ϋ–≥–Η–±–Η―²–Ψ―Ä–Α –Λ–ù–û–α (–Η–Λ–ù–û–α) – –Η–Ϋ―³–Μ–Η–Κ―¹–Η–Φ–Α–± –Η –Α–¥–Α–Μ–Η–Φ―É–Φ–Α–±.
–£ ―Ä–Α–±–Ψ―²–Β Finc–Κh –Η ―¹–Ψ–Α–≤―². [24] –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ―΄ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ 16 –Φ–Β―¹. –Μ–Β―΅–Β–Ϋ–Η―è 1218 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –†–ê –¦ –≤ ―¹–Ψ―΅–Β―²–Α–Ϋ–Η–Η ―¹ –¥―Ä―É–≥–Η–Φ–Η –ë–ü–£–ü –Η –Η–Ϋ–≥–Η–±–Η―²–Ψ―Ä–Α–Φ–Η –Λ–ù–û–α, –Η–Ζ –Ϋ–Η―Ö 842 –Ω–Ψ–Μ―É―΅–Α–Μ–Η –Η–Λ–ù–û–α + –€–Δ, 260 – –Η–Λ–ù–û–α + –¦, 116 – –Η–Λ–ù–û–α –Η –¥―Ä―É–≥–Η–Β –ë–ü–£–ü.
–Θ–Μ―É―΅―à–Β–Ϋ–Η–Β DAS 28 –Ϋ–Α ―²–Β―Ä–Α–Ω–Η–Η –¦ + –Η–Λ–ù–û–α ―¹–Ψ―¹―²–Α–≤–Η–Μ–Ψ 0,63 –Ω―Ä–Ψ―²–Η–≤ 0,74 –Ϋ–Α –Η–Λ–ù–û–α + –€–Δ. –™–Ψ–¥–Η―΅–Ϋ–Ψ–Β ―Ä–Β–Ϋ―²–≥–Β–Ϋ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Β –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β ―¹–Ψ―¹―²–Α–≤–Η–Μ–Ψ 0,74 –Η 0,91% ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ. –½–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Β ―É–Μ―É―΅―à–Β–Ϋ–Η–Β ―³―É–Ϋ–Κ―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι ―¹–Ω–Ψ―¹–Ψ–±–Ϋ–Ψ―¹―²–Η –Ψ―²–Φ–Β―΅–Β–Ϋ–Ψ ―É –Μ–Η―Ü –Φ–Ψ–Μ–Ψ–¥–Ψ–≥–Ψ –≤–Ψ–Ζ―Ä–Α―¹―²–Α ―¹ ―Ä–Α–Ϋ–Ϋ–Η–Φ –†–ê, –±–Ψ–Μ–Β–Β –Ϋ–Η–Ζ–Κ–Ψ–Ι –Η―¹―Ö–Ψ–¥–Ϋ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨―é, –Ϋ–Β ―²―Ä–Β–±―É―é―â–Β–Ι –Ω–Ψ–¥–Κ–Μ―é―΅–Β–Ϋ–Η―è –Κ–Ψ―Ä―²–Η–Κ–Ψ―¹―²–Β―Ä–Ψ–Η–¥–Ψ–≤.
–‰―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β ReACT –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ψ –¥–Μ―è –Ψ―Ü–Β–Ϋ–Κ–Η ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Η –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²–Η –ë–ü–£–ü –≤ ―¹–Ψ―΅–Β―²–Α–Ϋ–Η–Η ―¹ –Α–¥–Α–Μ–Η–Φ―É–Φ–Α–±–Ψ–Φ (―²–Α–±–Μ. 4) [25].
–£ 2008 –≥. –Ψ–Ω―É–±–Μ–Η–Κ–Ψ–≤–Α–Ϋ―΄ ―Ä–Β–Κ–Ψ–Φ–Β–Ϋ–¥–Α―Ü–Η–Η –ê–Φ–Β―Ä–Η–Κ–Α–Ϋ―¹–Κ–Ψ–Ι –Κ–Ψ–Μ–Μ–Β–≥–Η–Η ―Ä–Β–≤–Φ–Α―²–Ψ–Μ–Ψ–≥–Ψ–≤ –Ω–Ψ –Μ–Β―΅–Β–Ϋ–Η―é –†–ê ―¹ ―É―΅–Β―²–Ψ–Φ –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²–Η, –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –Η ―³–Α–Κ―²–Ψ―Ä–Ψ–≤ –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Α [26].
–€–Ψ–Ϋ–Ψ―²–Β―Ä–Α–Ω–Η―è –€–Δ –Η–Μ–Η –¦ ―Ä–Β–Κ–Ψ–Φ–Β–Ϋ–¥―É–Β―²―¹―è –≤―¹–Β–Φ –±–Ψ–Μ―¨–Ϋ―΄–Φ –†–ê –Ϋ–Β–Ζ–Α–≤–Η―¹–Η–Φ–Ψ –Ψ―² –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²–Η –Η –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Ω―Ä–Ψ―Ü–Β―¹―¹–Α. –î–Μ―è –¦ –≤―΄―¹–Ψ–Κ–Α―è ―¹―²–Β–Ω–Β–Ϋ―¨ –¥–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨–Ϋ–Ψ―¹―²–Η (–ê) –Ω–Ψ–Μ―É―΅–Β–Ϋ–Α –¥–Μ―è –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Α –≤―΄―¹–Ψ–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Η –±–Ψ–Μ―¨―à–Ψ–Ι –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²–Η –†–ê, –¥–Μ―è –Ψ―¹―²–Α–Μ―¨–Ϋ―΄―Ö –≤–Α―Ä–Η–Α–Ϋ―²–Ψ–≤ ―¹―²–Β–Ω–Β–Ϋ―¨ –¥–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨–Ϋ–Ψ―¹―²–Η – –Γ.
–€–Δ –≤ ―¹–Ψ―΅–Β―²–Α–Ϋ–Η–Η ―¹ –¦ –Ϋ–Α–Ζ–Ϋ–Α―΅–Α―é―² –Ω―Ä–Η –≤―΄―¹–Ψ–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –†–ê –Ω―Ä–Η –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²–Η ≥6 –Φ–Β―¹. –Ϋ–Β–Ζ–Α–≤–Η―¹–Η–Φ–Ψ –Ψ―² –Ϋ–Α–Μ–Η―΅–Η―è –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄―Ö –Ω―Ä–Ψ–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Η―Ö ―³–Α–Κ―²–Ψ―Ä–Ψ–≤.
–‰–Ϋ–≥–Η–±–Η―²–Ψ―Ä―΄ –Λ–ù–û–α –Ω―Ä–Η ―Ä–Α–Ϋ–Ϋ–Β–Φ –†–ê (–¥–Ψ 6 –Φ–Β―¹.) –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ―΄ ―²–Ψ–Μ―¨–Κ–Ψ –Ω―Ä–Η –≤―΄―¹–Ψ–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –Η –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄―Ö –Ω―Ä–Ψ–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Η―Ö ―³–Α–Κ―²–Ψ―Ä–Α―Ö (–¥–Ψ–Κ. –Γ).
–½–Α–Κ–Μ―é―΅–Β–Ϋ–Η–Β. –ü–Α―²–Ψ–≥–Β–Ϋ–Β―²–Η―΅–Β―¹–Κ–Α―è ―²–Β―Ä–Α–Ω–Η―è –†–ê –Ϋ–Α–Η–±–Ψ–Μ–Β–Β ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Α –≤ ―Ä–Α–Ϋ–Ϋ–Η–Β ―¹―Ä–Ψ–Κ–Η –Ψ―² –Ϋ–Α―΅–Α–Μ–Α –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Ω―Ä–Ψ―è–≤–Μ–Β–Ϋ–Η–Ι –±–Ψ–Μ–Β–Ζ–Ϋ–Η.


–¦–Η―²–Β―Ä–Α―²―É―Ä–Α
1. Emery P, Breedveld FC, Dougados M, et al. Early referral recommendation for newly diagnosed rheumatoid arthritis: evidence based development of a clinical guide. Ann Rheum Dis. 2002;61(4):290–7
2. Uhlig T, Heiberg T, Mowinckel P. Rheumatoid arthritis is milder in the new millennium: health status in patients with rheumatoid arthritis 1994–2004. Ann Rheum Dis. 2008;67(12):1710–5.
3. Visser K, Katchamart W, Loza E. Multinational evidence–based recommendations for the use of methotrexate in rheumatic disorders with a focus on rheumatoid arthritis: integrating systematic literature research and expert opinion of a broad international panel of rheumatologists in the 3E Initiative. Ann Rheum Dis. 2009;68(7):1086–93.
4. Dayer J.M., Cutolo M. Is there a rationale to using leflunomide in early rheumatoid arthritis? Clin Exp Rheumatol. 2005;23(3):404–12.
5. Hitchon C.A., el–Gabalawy H.S. The histopathology of early synovitis. Clin Exp Rheumatol. 2003;21(5 Suppl 31):S28–36
6. Cutolo M., Capellino S., Montagna P. et al. Anti–inflammatory effects of leflunomide in combination with methotrexate on co–culture of T lymphocytes and synovial macrophages from rheumatoid arthritis patients. Ann Rheum Dis. 2006;65 (6):728–35.
7. Welsing P.M., Fransen J., van Riel PL. Is the disease course of rheumatoid arthritis becoming milder? Time trends since 1985 in an inception cohort of early rheumatoid arthritis. Arthritis Rheum. 2005;52 (9):2616–24.
8. Sokka T., Kautiainen H., Hakkinen A., Hannonen P. Radiographic progression is getting milder in patients with early rheumatoid arthritis. Results of 3 cohorts over 5 years. J Rheumatol. 2004; 31 (6):1073–82
9. Sokka T., Kautiainen H., Hannonen P. Stable occurrence of knee and hip total joint replacement in Central Finland between 1986 and 2003: an indication of improved long–term outcomes of rheumatoid arthritis. Ann Rheum Dis. 2007;66 (3):341–4.
10. Smolen J, Breedveld F, Strand S et al. Efficacy of leflunomide in DMARD–naive patients with early RA. Ann Rheum Dis, 2002; Abstract Eular, v. 61 (Suppl. 1): 166.
11. Combe B, Oed C. Higher efficacy of Leflunomide in methotrexate–naive patients. Ann Rheum Dis 2003; Abstract Eular, v. 62 (Suppl. 1): 189.
12. Scott D.L., Strand V. The effects of disease–modifying anti–rheumatic drugs on the Health Assessment Questionnaire score. Lessons from the leflunomide clinical trials database. Rheumatology (Oxford). (2002, 41, 899–909
13. –ö–Α―Ä–Α―²–Β–Β–≤ –î.–ï. –¦–Β―³–Μ―É–Ϋ–Ψ–Φ–Η–¥ –≤ ―¹–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–≥–Β–Ϋ–Β―²–Η―΅–Β―¹–Κ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η ―Ä–Α–Ϋ–Ϋ–Β–≥–Ψ ―Ä–Β–≤–Φ–Α―²–Ψ–Η–¥–Ϋ–Ψ–≥–Ψ –Α―Ä―²―Ä–Η―²–Α // –†–€–•. 2007, 15 (26), 2042–46.
14. –ë–Α–Μ–Α–±–Α–Ϋ–Ψ–≤–Α –†.–€., –ö–Α―Ä–Α―²–Β–Β–≤ –î.–ï., –ö–Α―à–Β–≤–Α―Ä–Ψ–≤ –†.–°. –¦–Β―³–Μ―É–Ϋ–Ψ–Φ–Η–¥ (–ê―Ä–Α–≤–Α) –Ω―Ä–Η ―Ä–Α–Ϋ–Ϋ–Β–Φ ―Ä–Β–≤–Φ–Α―²–Ψ–Η–¥–Ϋ–Ψ–Φ –Α―Ä―²―Ä–Η―²–Β. –ù–Α―É―΅–Ϋ–Ψ––Ω―Ä–Α–Κ―². ―Ä–Β–≤–Φ–Α―²–Ψ–Μ–Ψ–≥–Η―è, 2005, 5, 31–34
15. –ë–Α–Μ–Α–±–Α–Ϋ–Ψ–≤–Α –†.–€., –ö–Α―à–Β–≤–Α―Ä–Ψ–≤ –†.–°., –û–Μ―é–Ϋ–Η–Ϋ –°.–ê.. –Γ―Ä–Α–≤–Ϋ–Η―²–Β–Μ―¨–Ϋ–Α –Ψ―Ü–Β–Ϋ–Κ–Α leflunomide –Η –Φ–Β―²–Ψ―²―Ä–Β–Κ―¹–Α―²–Α –Ω―Ä–Η ―Ä–Α–Ϋ–Ϋ–Η―è ―Ä–Β–≤–Φ–Α―²–Ψ–Η–¥–Β–Ϋ –Α―Ä―²―Ä–Η―². –†–Β–≤–Φ–Α―²–Ψ–Μ–Ψ–≥–Η―è (–ë–Ψ–Μ–≥–Α―Ä–Η―è), 2005, 4, 42–47.
16. Karateev D.E., Luchikhina E.L., Nasonov E.L. High frequency of clinical remission in patient with early RA treated with leflunomide. Ann Rheum Dis. 2006, Abstr EULAR, 65 (Suppl. 2): 341.
17. –ë–Α–Μ–Α–±–Α–Ϋ–Ψ–≤–Α –†.–€., –ö–Α―à–Β–≤–Α―Ä–Ψ–≤ –†. –°., –û–Μ―é–Ϋ–Η–Ϋ –°.–ê. –ê–Ϋ―²–Η–¥–Β―¹―²―Ä―É–Κ―²–Η–≤–Ϋ–Ψ–Β –¥–Β–Ι―¹―²–≤–Η–Β –Μ–Β―³–Μ―É–Ϋ–Ψ–Φ–Η–¥–Α –Ω―Ä–Η ―Ä–Α–Ϋ–Ϋ–Β–Φ ―Ä–Β–≤–Φ–Α―²–Ψ–Η–¥–Ϋ–Ψ–Φ –Α―Ä―²―Ä–Η―²–Β. –Δ–Β―Ä. –ê―Ä―Ö–Η–≤, 2006, 78 (6), 6–10.
18. Kashevarov R., Balabanova R.M, Oliunin Y.A. et al. Level of matrix metalloproteinase 3 and joint destruction rate in early RA treated with leflunomide and methotrexate. Ann Rheum Dis. 2006, 65, Suppl II, 341
19. Kalden JR, Schattenkirchner M, Sorensen H, et al. The efficacy and safety of leflunomide in patients with active rheumatoid arthritis: a five–year follow–up study. Arthritis Rheum. 2003;48(6):1513–20.
20. Heiberg T., Finset A., Uhlig T., Kvien TK. Seven year changes in health status and priorities for improvement of health in patients with rheumatoid arthritis. Ann Rheum Dis. 2005;64(2):191–5.
21. –ë–Α–Μ–Α–±–Α–Ϋ–Ψ–≤–Α –†.–€., –û–Μ―é–Ϋ–Η–Ϋ –°.–ê., –ù–Α―¹–Ψ–Ϋ–Ψ–≤ –ï.–¦. –†–Β–≥–Η―¹―²―Ä –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ ―Ä–Α–Ϋ–Ϋ–Η–Φ ―Ä–Β–≤–Φ–Α―²–Ψ–Η–¥–Ϋ―΄–Φ –Α―Ä―²―Ä–Η―²–Ψ–Φ, –≤–Ω–Β―Ä–≤―΄–Β –Ω–Ψ–Μ―É―΅–Α―é―â–Η―Ö –Φ–Ψ–Ϋ–Ψ―²–Β―Ä–Α–Ω–Η―é –Μ–Β―³–Μ―É–Ϋ–Ψ–Φ–Η–¥–Ψ–Φ (–Ω―Ä–Β–¥–≤–Α―Ä–Η―²–Β–Μ―¨–Ϋ―΄–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄). IV –ù–Α―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ―΄–Ι –Κ–Ψ–Ϋ–≥―Ä–Β―¹―¹ ―²–Β―Ä–Α–Ω–Β–≤―²–Ψ–≤, M., –Δ–Β–Ζ.–¥–Ψ–Κ–Μ., 2009, ―¹. 57
22. Kalden JR, Antoni C, Alvaro–Gracia JM, et al. Use of combination of leflunomide with biological agents in treatment of rheumatoid arthritis. J Rheumatol. 2005;32(8):1620–31.
23. Perdriger A, Mariette X, Kuntz JL, et al. Safety of infliximab used in combination with leflunomide or azathioprine in daily clinical practice. J Rheumatol. 2006;33(5):865–9.
24. Finckh A, Dehler S, Gabay C; SCQM doctors. The effectiveness of leflunomide as a co–therapy of tumour necrosis factor inhibitors in rheumatoid arthritis: a population–based study. Ann Rheum Dis. 2009; 68 (1):33–9.
25. Burmester GR, Mariette X, Montecucco C, et al. Adalimumab alone and in combination with disease–modifying antirheumatic drugs for the treatment of rheumatoid arthritis in clinical practice: the Research in Active Rheumatoid Arthritis (ReAct) trial. Ann Rheum Dis. 2007; 66 (6):732–9. Epub 2007, 28.
26. Saag KG, Teng GG, Patkar NM, et al. American College of Rheumatology 2008 recommendations for the use of nonbiologic and biologic disease–modifying antirheumatic drugs in rheumatoid arthritis. Arthritis Rheum. 2008, 15;59 (6):762–84.












