
На сегодняшний день ОА входит в число наиболее распространенных заболеваний и является одной из главных причин нетрудоспособности населения. К основным факторам риска возникновения и прогрессирования ОА относятся: пожилой возраст, травмы и спортивные нагрузки в анамнезе, избыточная масса тела, наличие деформаций суставов, хронический синовит, высокие значения минеральной плотности костной ткани [2, 3].
Одним из самых важных компонентов матрикса хряща являются протеогликаны – макромолекулы, в которых стержневой белок связан с одной или несколькими цепями гликозаминогликанов (ГАГ). ГАГ разделяют на 2 группы: несульфатированные (гиалуроновая кислота, хондроитин) и сульфатированные (хондроитин сульфат и кератан сульфат). Совместно с коллагеновыми волокнами ГАГ обеспечивают устойчивость хряща к внешним воздействиям. Большое значение в лечении ОА имеют препараты медленного действия, которые представляют собой естественные компоненты хряща: гиалуроновую кислоту, глюкозамин и хондроитин сульфат. Метаанализ многочисленных исследований показал, что глюкозамина сульфат (ГС) и хондроитин сульфат (ХС) эффективны в лечении ОА [4–6]. ХС и ГС достоверно уменьшают болевой синдром, снижая тем самым потребность больного в анальгетических и противовоспалительных средствах, обладают противовоспалительными свойствами [7], улучшают функциональное состояние больных (по индексу Лекена). Лечение ГС и ХС, как правило, хорошо переносится больными.
Таким образом, в пользу перспективности применения комбинации ГС и ХС говорят экспериментальные данные о некоторых различиях в механизме действия компонентов комбинации и данные зарубежных клинических исследований, показавших уменьшение боли, припухлости и других проявлений синовита у больных с ОА [8]. Научные данные последних лет подтверждают эффективность внутримышечных инъекций препаратов замедленного действия (symptomatic slow acting drugs for osteoarthritis (SYSADOA)) в терапии первичного и посттравматического ОА коленных суставов. Экспериментальные и ex vivo исследования демонстрируют значительные противовоспалительный и анальгезирующий эффекты парентеральных форм ХС и ГС при курсовом применении.
Хондрогард (ХС натрия для внутримышечного введения, 100 мг/мл) представляет собой высокомолекулярный мукополисахарид, влияющий на обменные процессы в гиалиновом хряще. Препарат уменьшает дегенеративные изменения в хрящевой ткани суставов, ускоряет процессы ее восстановления, стимулирует синтез протеогликанов. Применение Хондрогарда при терапии ОА коленных суставов сопровождается клинически значимым симптоматическим эффектом. Хондрогард обладает высоким профилем безопасности, что было продемонстрировано в целом ряде клинических исследований [9–11].
Сустагард Артро (ГС для внутримышечного введения, 200 мг/мл) оказывает анаболическое, антикатаболическое, хондропротективное, противовоспалительное, анальгезирующее действие. ГС, активный компонент препарата Сустагард Артро, представляет собой соль натурального аминомоносахаридного глюкозамина. Глюкозамин стимулирует синтез хондроцитами протеогликанов (глюкозаминогликанов и гиалуроновой кислоты), ингибирует ферменты (коллагеназу, фосфолипазу А2 и др.), вызывающие деструкцию хрящевой ткани, препятствует образованию супероксидных радикалов, подавляет активность лизосомальных ферментов, инициирует процесс фиксации серы в синтезе хондроитинсерной кислоты и способствует нормальному отложению кальция в костной ткани, препятствует повреждающему действию кортикостероидов на хондроциты и нарушению синтеза гликозаминогликанов, индуцированному нестероидными противовоспалительными препаратами. Сульфогруппы также принимают участие в синтезе гликозаминогликанов и метаболизме хрящевой ткани, а сульфоэфиры боковых цепей в составе протеогликанов способствуют сохранению эластичности матрикса хряща. Уменьшение клинических симптомов ОА проявляется, как правило, через 2 нед. от начала лечения с сохранением клинического улучшения в течение 8 нед. и более после отмены препарата. После внутримышечного введения Сустагард Артро быстро проходит через биологические барьеры и проникает в ткани, преимущественно в суставной хрящ. Период полувыведения препарата составляет около 60 ч; препарат выводится в основном почками.
Именно ГС встраивается хондроцитами в компоненты глюкозаминосульфатных цепей непораженной хрящевой ткани [12]. Кроме того, ГС стимулирует синтез физиологических протеогликанов и снижает активность катаболических ферментов, включая металлопротеиназы [13–15].
В испытаниях, где ГС сравнивали с различными НПВП, он оказался равным по эффективности двум и превышал эффективность двух других противовоспалительных препаратов. При этом значение объединенных СРС (стандартизированная разница средних) составило 0,86 (3 испытания) и 0,32 (2 испытания) по индексу Лекена, это указывало на тенденцию к преимуществу со стороны ГС, что, по мнению авторов, является основополагающим моментом, с учетом очень высокой степени безопасности ГС. ГС оказывает благоприятный симптоматический эффект при ОА как в кратковременных, так и в долговременных испытаниях [1]. Доказано, что концентрация препарата в плазме при внутримышечном введении в 5 раз превышает таковую при пероральном применении [16].
В ряде клинических исследований, включая рандомизированные, продемонстрирована эффективность парентеральных форм ХС и ГС в сравнении с пероральными SYSADOA в терапии ОА коленных суставов [17–20].
Цель исследования – оценить эффективность и безопасность парентеральных форм ХС (Хондрогард) и ГС (Сустагард Артро) при применении по интермиттирующей схеме (через день) у пациентов с первичным и посттравматическим ОА коленных суставов.
Материал и методы
Проведено открытое рандомизированное контролируемое клиническое исследование по оценке эффективности и переносимости внутримышечных инъекций ХС (Хондрогард) и ГС (Сустагард Артро) по интермиттирующей схеме в терапии первичного и посттравматического ОА коленных суставов. В исследовании приняли участие 102 пациента с первичным и посттравматическим ОА коленных суставов I–III рентгенологической стадии по классификации Kellgren и Lowrense, рандомизированные на 2 группы.В 1-ю (основную) группу вошли 50 пациентов – 35 женщин (70 %) и 15 мужчин (30 %) в возрасте 53,16±8,35 года, получавших внутримышечные инъекции ХС (Хондрогард) по 2,0 мл (200 мг) через день № 20 и ГС (Сустагард Артро) по 3,0 мл (200 мг/2,0 мл действующего вещества и 1,0 мл растворителя) через день № 20. Препараты вводились в режиме чередования (через день): 1, 3, 5, 7 день терапии и т. д. – Хондрогард; 2, 4, 6 день терапии и т. д. – Сустагард Артро.
2-ю группу (группа сравнения) составили 52 пациента – 36 женщин (69,2%) и 16 мужчин (30,8%) в возрасте 53,23±8,44 года, ежедневно принимавшие пероральную форму комбинированных SYSADOA (ХС 1000 мг + глюкозамина гидрохлорид 1000 мг – препарат Артра, 2 табл./сут) в течение 3 мес.
В исследование были включены как амбулаторные пациенты, так и пациенты, находившиеся на стационарном лечении.
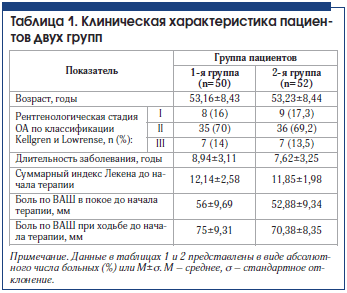
По основным демографическим и клиническим характеристикам группы пациентов были сопоставимы (табл. 1). В обеих группах преобладали пациенты со II рентгенологической стадией ОА коленных суставов.
Критерии включения в исследование:
1. Возраст пациентов – от 18 до 65 лет.2. Наличие первичного и/или посттравматического ОА коленных суставов I–III рентгенологической стадии по Kellgren и Lowrence.
3. Боль при движениях или в покое не менее 50 мм по 100 мм визуальной аналоговой шкале (ВАШ).
4. Суммарный индекс Лекена (The Lequesne Algofunctional Index) – от 4 баллов и выше.
5. Отсутствие противопоказаний к внутримышечному введению препаратов.
6. Отсутствие клинически значимых нарушений функции печени и почек.
7. Отсутствие анамнестических указаний на непереносимость применяемых в исследовании препаратов.
8. Подписанное информированное согласие на участие в исследовании.
Критерии исключения:
1. Применение симптом-модифицирующих препаратов (SYSADOA) в течение последних 3 мес.2. IV рентгенологическая стадия ОА коленных суставов.
3. Язвенная болезнь желудка или двенадцатиперстной кишки в стадии обострения.
4. Наличие у пациента помимо первичного ОА воспалительной артропатии или системного заболевания соединительной ткани.
5. Инсулинопотребный сахарный диабет (СД) и СД 2-го типа в фазе декомпенсации.
6. Внутрисуставное введение глюкокортикоидов в течение предшествующего исследованию месяца.
7. Применение антикоагулянтов прямого и непрямого действия.
За критерии эффективности терапии принимали снижение выраженности болевого синдрома по ВАШ и уменьшение значений индекса Лекена на 20,0% и более по сравнению с исходными данными.
Исследование состояло из трех этапов. Первый этап (визит 1 перед началом терапии – пациенты обеих групп) предполагал оценку исходных данных и включал: подписание пациентами информированного согласия; заполнение опросника о текущей и предшествующей лекарственной терапии; оценку боли в покое и при движениях и общего самочувствия по ВАШ; заполнение опросника оценки функциональной способности (суммарный индекс Лекена); физикальный осмотр пациента врачом; оценку результатов рентгенологического исследования коленных суставов; оценку результатов лабораторного обследования до начала терапии (биохимические показатели крови: аланинаминотрасфераза (АЛТ), аспартатаминотрансфераза (АСТ), креатинин, мочевина, сахар крови); проверку соответствия критериев включения в исследование; назначение внутримышечных инъекций ХС (Хондрогард) и ГС (Сустагард Артро) по интермиттирующей схеме (пациентам 1-й группы) и пероральной формы ХС и глюкозамина гидрохлорида (препарат Артра, 2 табл./сут) пациентам 2-й группы. На втором этапе (визит 2 – через 40 дней от момента визита 1 для пациентов 1-й группы и через 3 мес. терапии для пациентов 2-й группы) оценивались: боль по ВАШ; функциональная способность (суммарный индекс Лекена); нежелательные побочные реакции на фоне терапии SYSADOA; результаты контрольного лабораторного обследования. На третьем этапе (визит 3 – через 90 дней с момента визита 2 для пациентов обеих групп) проводились: заполнение пациентами опросника о текущей лекарственной терапии; оценка интенсивности боли в покое и при движениях по ВАШ; оценка функциональной способности (суммарный индекс Лекена); физикальный осмотр пациента врачом; оценка эффективности проведенной терапии по мнению пациента и врача.
Исследование проведено с использованием современных диагностических критериев и общепринятых в ревматологии клинических методов оценки суставного синдрома при ОА коленных суставов, стандартных методов лабораторной и инструментальной диагностики.
Статистическая обработка осуществлялась с использованием программы Statistica Base 6.0. Применялись непараметрические методы статистики: тест Манна – Уитни для независимых выборок, критерий Уилкоксона для зависимых выборок. При описании признаков использовались среднее арифметическое (M) и стандартное отклонение (σ – standard deviation). Для сравнения диапазонов значений нескольких переменных использовались диаграмма размаха, диаграмма рассеяния и коэффициент ранговой корреляции Спирмена. При сравнении зависимых групп по количественному признаку использовался Т-критерий Стьюдента. Достоверными признаны различия при уровне значимости p<0,05.
Результаты и обсуждение
На фоне проводимой терапии у пациентов в обеих группах было достигнуто статистически значимое снижение уровня альгофункциональных показателей – интенсивности боли по ВАШ и индекса Лекена (рис. 1–3; табл. 2).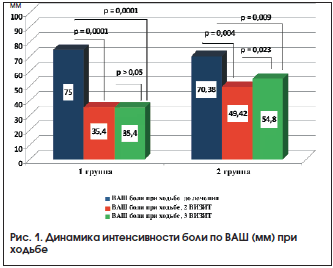
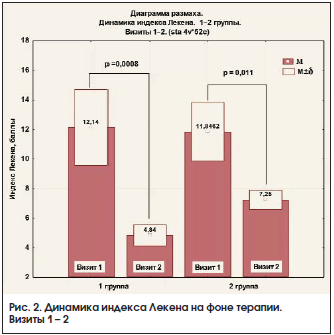

При оценке суммарного индекса Лекена на визите 2 у пациентов в обеих группах выявлено значительное улучшение функциональных показателей: уменьшилась продолжительность утренней скованности, увеличилась максимальная дистанция при ходьбе без боли, увеличилась функциональная активность, исчезли ночные боли (рис. 2, табл. 2).
Через 3 мес. после отмены терапии в обеих группах значительного нарастания интенсивности боли по ВАШ при ходьбе отмечено не было (рис. 1).
Интенсивность боли в покое по ВАШ к концу курса терапии (визит 2) снизилась до минимальных значений у пациентов в обеих группах. Через 3 мес. после окончания курса терапии (визит 3) нарастания интенсивности боли по ВАШ в покое не отмечено в обеих группах (табл. 2).
При динамическом наблюдении через 3 мес. после отмены терапии (визит 3) у пациентов 1-й группы нарастания индекса Лекена не отмечено (рис. 4, табл. 2). У пациентов 2-й группы было выявлено статистически значимое повышение индекса Лекена (рис. 4, табл. 2).

Одним из элементов терапии ОА является раннее использование медленнодействующих препаратов, в частности инъекционных форм ГС и ХС. ГС и ХС обладают симптом-модифицирующим, структурно-модифицирующим действием и высоким профилем безопасности. Результаты многочисленных исследований подтверждают, что ГС и ХС при парентеральном введении оказывают выраженный анальгетический эффект и улучшают функцию суставов при ОА по сравнению с плацебо, являются безопасными и характеризуются минимумом нежелательных реакций [20].
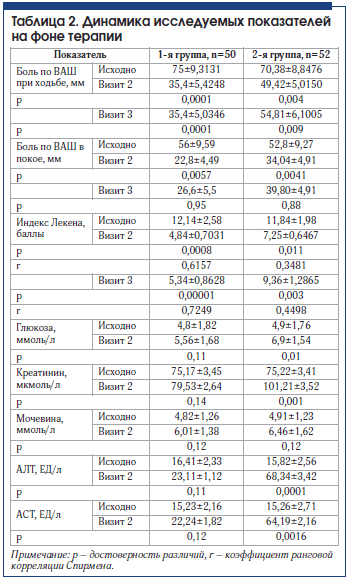
Сравнительная динамика анализируемых альгофункциональных (боль по ВАШ, индекс Лекена) и лабораторных показателей пациентов обеих групп представлена в таблице 2.
На фоне терапии у пациентов 1-й группы не было выявлено отрицательной динамики биохимических показателей. В группе сравнения в 19% случаев (у 10 пациентов) было отмечено повышение уровня креатинина, в 28% случаев (у 15 пациентов) выявлено повышение уровня трансаминаз. Также у 24 пациентов (46%) 2-й группы было отмечено незначительное повышение уровня глюкозы в сыворотке крови к концу курса терапии. В 1-й группе нарастания гликемии отмечено не было.
Переносимость парентеральных форм ХС и ГС была оценена как хорошая 5 пациентами (10%) и отличная – 45 пациентами (90%) 1-й группы. На отличную эффективность инъекционных ХС и ГС указали 48 больных (96%), на хорошую – 2 (4%), на удовлетворительную – 0, на неудовлетворительную – 0. Среди нежелательных реакций 6 пациентов 1-й группы (12%) отмечали незначительную кратковременную болезненность при внутримышечном введении Сустагарда Артро. При этом постинъекционных инфильтратов у пациентов 1-й группы не выявлено. Отмены препаратов в обеих группах пациентов не было.
Таким образом, комбинированная терапия ХС и ГС в виде внутримышечных инъекций по интермиттирующей схеме позволяет добиться снижения интенсивности боли и значительного улучшения функциональных показателей у пациентов с ОА коленных суставов в более короткие сроки по сравнению с пероральными формами SYSADOA.
Выводы
1. Переносимость комбинации парентеральных форм ХС (Хондрогард) и ГС (Сустагард Артро) по интермиттирующей схеме оценена подавляющим большинством больных как отличная и хорошая, при этом не было отмечено отрицательной динамики со стороны биохимических показателей крови, что позволяет применять данные препараты у пациентов с высокой коморбидностью.2. Обезболивающий эффект сохранялся в течение 3-х мес. после отмены терапии у пациентов, получавших инъекционные формы SYSADOA.
3. Комбинированная терапия Хондрогард + Сустагард Артро с парентеральным введением ХС и ГС по интермиттирующей схеме позволяет достичь значительного улучшения функциональных показателей, добиться более выраженного снижения интенсивности боли при ходьбе и в покое по сравнению с пероральным комбинированным хондропротектором Артра.
4. Комбинированная терапия Хондрогард + Сустагард Артро с парентеральным введением ХС и ГС по интермиттирующей схеме имеет более высокий профиль безопасности по сравнению с пероральным комбинированным хондропротектором Артра, о чем свидетельствует динамика уровня креатинина, АЛТ и АСТ, глюкозы в крови.
5. Комбинированная терапия инъекционными формами ХС (Хондрогард) и ГС (Сустагард Артро) по интермиттирующей схеме может быть рекомендована в качестве старт-терапии первичного и посттравматического ОА коленных суставов у пациентов с выраженным болевым синдромом и высоким риском коморбидности.












