
Введение
Поясничная боль (ПБ) представляет собой наиболее распространенную форму скелетно-мышечных болевых синдромов. Широкая распространенность ПБ в популяции, склонность к частым рецидивам, снижение возможности полноценного выполнения профессиональной деятельности превращают проблему ПБ из исключительно медицинской в социально-экономическую [1]. Установлено, что именно ПБ служит одной из наиболее частых причин обращения за медицинской помощью [2]. Как свидетельствуют результаты эпидемиологических исследований, проведенных в различных странах мира, ПБ — одна из наиболее частых причин увеличения количества лет, прожитых с заболеванием, а также причин временной утраты трудоспособности [3, 4]. Исключительная социально-экономическая значимость проблемы ПБ обусловлена высокими материальными затратами на лекарственное и немедикаментозное лечение, проведение реабилитационных и восстановительных мероприятий, финансовыми расходами, связанными с временной утратой трудоспособности или ограничением способности пациентов к выполнению в полном объеме трудовой деятельности, а также преждевременным выходом на пенсию или получением инвалидности [5, 6].На сегодняшний день имеются данные о росте заболеваемости, об увеличении бремени связанных с ПБ социальных последствий. Оказалось, что суммарное количество лет, прожитых с заболеванием, среди пациентов с ПБ в 1990 г. составило 58,2 млн, а в 2010 г. возросло уже до 83,0 млн [2]. Характерно увеличение числа пациентов как с первично развившейся ПБ, так и с рецидивами заболевания, наблюдается увеличение частоты случаев формирования хронического болевого синдрома [7]. Важно, что хроническая боль сама по себе является важным фактором риска дальнейшего снижения трудоспособности и дополнительных материальных расходов. Развитие ПБ связано с колоссальными материальными затратами. Так, суммарные расходы, связанные с ПБ, в 2006 г. в США составили 100 млрд долл., причем две трети этой суммы были обусловлены временной нетрудоспособностью и невозможностью выполнять привычную работу в полном объеме [8].
Серьезной проблемой, связанной с ПБ, является регистрируемое во многих странах снижение качества оказания медицинской помощи таким пациентам. В определенной степени это обусловлено недостаточно обоснованным применением дорогостоящих способов диагностики и лечения пациентов с ПБ. Так, в ряде государств наблюдается увеличение числа пациентов, госпитализированных с целью продолжения ранее начатого консервативного лечения, притом что подавляющее большинство пациентов должны получать эффективное лечение в амбулаторных условиях [3]. Обращает на себя внимание увеличение частоты необоснованного назначения и проведения инструментальных обследований, в первую очередь КТ и МРТ. Связанное с этим повышение суммарной стоимости лечебного процесса не оказывает значимого влияния на выбор терапевтической тактики и, соответственно, на его эффективность [9]. Продемонстрировано, что только в Великобритании за период с 1999 по 2013 г. число больных, госпитализированных по поводу ПБ, увеличилось с 127,09 до 216,16 на 100 тыс. населения, а количество пациентов, госпитализированных для проведения оперативного лечения, — с 24,5 до 48,8 на 100 тыс. населения [10]. Авторы указанного исследования отмечают, что связанный с этим рост затрат на лечение не связан с повышением его эффективности и улучшением его конечного результата. Более того, регистрируется увеличение числа пациентов с рецидивами острой ПБ и формированием хронического болевого синдрома.
Медикаментозная терапия ПБ
Воздействие на циклооксигеназный и липоксигеназный пути развития боли и воспаления
Лечение пациентов с ПБ направлено на купирование болевого синдрома с целью обеспечения максимально возможного уровня повседневной активности и повышения качества жизни больного. С целью устранения боли применяются ацетаминофен, метамизол и нестероидные противовоспалительные препараты (НПВП). Выбор лекарственного средства определяется не только анальгетическим эффектом того или иного препарата, но и дополнительными эффектами терапии, способствующими скорейшему восстановлению пациента, а также характером имеющегося болевого синдрома и спектром возможных побочных эффектов.Для лечения пациентов с разнообразными скелетно-мышечными болевыми синдромами, в т. ч. с ПБ, в настоящее время широко применяется препарат кетопрофен (Кетонал®) — неселективный ингибитор циклооксигеназы (ЦОГ) 1 и 2 типов, обладающий выраженным обезболивающим и противовоспалительным действием. Кетопрофен способен проникать через гематоэнцефалический барьер, благодаря чему реализуется его противоболевой эффект: как за счет воздействия непосредственно в области первичного поражения, так и вследствие влияния на системы проведения и обработки болевой импульсации в головном и спинном мозге, в т. ч. на уровне заднего рога спинного мозга [11].
Уникальной особенностью препарата является его способность подавлять фермент липоксигеназу (ЛОГ), обеспечивая таким образом комплексное действие на циклооксигеназный и липоксигеназный пути развития боли и воспаления.
Установлено, что Кетонал® обладает значительным противоболевым эффектом при ряде патологических состояний, проявляющихся болевым синдромом. Так, было продемонстрировано его обезболивающее действие для купирования боли после оперативного вмешательства в челюстно-лицевой, абдоминальной хирургии, при острой травме [12–14]. Устранение и/или предупреждение болевого синдрома, установленное в этих исследованиях, сопровождалось купированием локального воспаления и отека, притом что препарат характеризовался хорошей переносимостью. Важно, что обезболивающее действие кетопрофена оказалось достоверно более значимым, чем у препаратов, которые получали пациенты из групп сравнения [15].
Положительные результаты изучения эффективности применения кетопрофена для лечения пациентов с острыми болевыми синдромами явились основанием для изучения возможности его применения у пациентов с ПБ. Такие исследования, проведенные и в Российской Федерации, продемонстрировали его высокую эффективность при ПБ [16]. Была установлена эффективность препарата у пациентов как с изолированной ПБ, так и с болевым корешковым синдромом. Применение кетопрофена оказалось наиболее эффективным у пациентов с острым болевым синдромом, при этом авторы отметили, что у части пациентов положительный эффект был достигнут и при достаточно длительном обострении (подострый болевой синдром). Согласно инструкции препарат Кетонал® не имеет ограничений по длительности применения. Как и в проведенных ранее исследованиях, была отмечена хорошая переносимость препарата Кетонал®, а также возможность его одновременного назначения с другими лекарственными препаратами для лечения пациентов с ПБ и сопутствующими соматическими заболеваниями. Тяжелые побочные эффекты при его применении зарегистрированы не были. Высокая эффективность и хорошая переносимость кетопрофена у пациентов с мышечно-скелетными болевыми синдромами явились основанием для включения препарата в региональные и международные рекомендации по лечению больных с ПБ [17].
Несомненный практический интерес вызывает препарат Кетонал® ДУО, который выпускается в лекарственной форме «капсулы с модифицированным высвобождением». Каждая капсула содержит 2 пеллеты. Из одной пеллеты действующее вещество высвобождается сразу после поступления капсулы в желудочно-кишечный тракт (ЖКТ), вследствие чего обезболивающий эффект наступает немедленно. Химико-физические особенности других пеллет обеспечивают постепенное высвобождение кетопрофена, что позволяет поддерживать достаточно стабильную его концентрацию в крови до 24 ч. Это отличает Кетонал® ДУО от традиционно применяемых лекарственных форм, при назначении которых требуется двух- трехкратный прием в течение суток для поддержания адекватной концентрации препарата в крови. Применение препарата Кетонал® ДУО целесообразно у пациентов, получающих лечение в амбулаторных условиях, продолжающих трудовую деятельность, для которых многократный прием препарата нежелателен или неудобен.
Было проведено многоцентровое открытое исследование, посвященное изучению эффективности и безопасности применения препарата Кетонал® ДУО у пациентов с ПБ. В исследовании приняли участие 349 пациентов, получавших препарат по 150 мг/сут в течение 7 сут [18, 19]. Результаты исследования продемонстрировали достоверное снижение интенсивности ПБ как в покое, так и в движении (p<0,001); большинство пациентов и врачей (82,1% и 79,3% соответственно) сообщили о полном купировании или уменьшении интенсивности боли на 50%. Также была показана хорошая переносимость препарата Кетонал® ДУО, побочные явления развивались только у 2,8% пациентов, причем они были выражены в легкой степени. Также был отмечен высокий уровень приверженности лечению: 95,25% пациентов и 94,25% врачей посчитали однократный прием препарата Кетонал® ДУО в сутки максимально удобным для купирования острого болевого синдрома.
Кетонал® характеризуется хорошей переносимостью, в т. ч. у пациентов старших возрастных групп, с полиморбидностью, отличается низким риском лекарственных взаимодействий. Препарат обладает благоприятным профилем безопасности у пациентов с кардиологическими заболеваниями, что обеспечивает возможность его применения при стабильных формах ИБС. В масштабном исследовании, проведенном по принципу «случай — контроль», был убедительно показан низкий риск развития инфаркта миокарда на фоне применения кетопрофена [20]. Также важно, что применение кетопрофена не сопровождается значимым влиянием на системную гемодинамику. При наблюдении за группой больных с остеоартритом, которые получали кетопрофен, по результатам суточного мониторирования артериального давления не было зарегистрировано его значимого повышения [21].
Уменьшение риска гастроинтестинальных осложнений достигается одновременным назначением гастропротекторов, в частности ингибиторов протонной помпы, например омепразола. Такая комбинированная терапия обладает минимальным риском лекарственного взаимодействия и не сопровождается снижением противоболевого эффекта кетопрофена, т. к. препараты метаболизируются различными цитохромами (CYR2C9 и CYP2C19 соответственно).
Выраженность и скорость наступления терапевтического эффекта не зависели от индивидуальных генетических особенностей пациентов, в т. ч. от различных вариаций аллелей цитохромов [22]. Итоги рандомизированных клинических исследований, в ходе которых противоболевую эффективность кетопрофена сравнивали с эффективностью других НПВП, подтвердили его высокую эффективность и хорошую переносимость.
Кетопрофен помимо мультимодального, реализующегося на разных уровнях нервной системы противоболевого действия характеризуется рядом клинических эффектов. Так, клинически важным является отсутствие повреждающего действия на хрящевую ткань. Указанное свойство отличает кетопрофен от значительного числа НПВП, оказывающих разрушающее действие на хрящевую ткань, что ограничивает возможность их применения, в частности, у пациентов, которым требуются длительные или повторные курсы терапии. Вызывают интерес и требуют дальнейшего изучения сведения о том, что применение кетопрофена не только не оказывает повреждающего действия на хрящевую ткань, но, напротив, замедляет ее деструкцию, приводя к замедлению развития и прогрессирования остео-артрита. У кетопрофена практически отсутствует гепатотоксическое действие, что является его несомненным преимуществом при назначении полиморбидному пациенту, нуждающемуся в одновременном применении нескольких лекарственных препаратов.
Возможности применения селективных ингибиторов ЦОГ-2 у пациентов с ПБ
Формирование хронического болевого синдрома требует адекватной терапевтической тактики, в частности, выбора лекарственного препарата, применение которого даже в течение длительного времени не повышает существенно риска развития осложнений со стороны внутренних органов. Для лечения пациентов с длительно существующей ПБ, затянувшимся обострением, частыми рецидивами болевого синдрома обоснованным является применение селективных ингибиторов ЦОГ-2. Следует подчеркнуть, что исследования последних лет опровергли существовавшее представление о том, что селективные ингибиторы ЦОГ-2 характеризуются класс-специфическим риском кардиоваскулярных осложнений [23].Одним из представителей данного класса препаратов является эторикоксиб (Костарокс®). Помимо хорошо изученных противовоспалительного и противоболевого эффектов, обусловленных способностью ингибировать ЦОГ, препарат оказывает обезболивающее действие и на уровне ЦНС. Обладая способностью проникать через гематоэнцефалический барьер, препарат Костарокс® оказывает воздействие на ноцицептивную систему, уменьшая выраженность центральной сенситизации, предотвращая трансформацию острой боли в хроническую и/или уменьшая интенсивность хронического болевого синдрома [24]. Указанное обстоятельство имеет большое значение при лечении пациентов с неустранимым источником боли, в частности, страдающих остеоартритом суставов позвоночника. Способность препарата Костарокс® уменьшать центральную сенситизацию была показана в клиническом исследовании у пациентов с остеоартритом [25].
В клинических исследованиях, проведенных с участием пациентов, перенесших одномоментную экстракцию двух и более моляров, было показано выраженное анальгетическое действие эторикоксиба [26]. Однократное применение препарата обеспечивало достаточный контроль боли на протяжении не менее 24 ч. Проведенные впоследствии клинические исследования продемонстрировали высокую эффективность эторикоксиба при лечении пациентов с ПБ, обусловленной дегенеративным поражением позвоночника, в частности остеоартритом, в связи с чем применение данного препарата было рекомендовано Российским обществом по изучению боли для лечения больных с дорсалгиями различной локализации [27].
Отличительными чертами фармакологического профиля препарата Костарокс® являются хорошая переносимость и относительно низкий риск развития нежелательных побочных эффектов. Препарат обладает низким риском возникновения атеротромботических осложнений и стойкого повышения системного артериального давления. Важно, что препарат Костарокс® имеет благоприятный профиль безопасности в отношении нежелательных реакций со стороны ЖКТ. Согласно результатам метаанализа большого числа рандомизированных клинических исследований, относительный риск возникновения нежелательных явлений со стороны ЖКТ на фоне лечения эторикоксибом существенным образом не отличается от такового при назначении плацебо [28]. Также редко наблюдаются серьезные осложнения и со стороны других органов и систем.
Исходя из указанных особенностей спектра фармакологических эффектов препарата, вполне обоснованным и достаточно безопасным является его применение на протяжении длительного периода времени. Результаты ряда исследований показали возможность назначения эторикоксиба пациентам со скелетно-мышечными болевыми синдромами, в т. ч. обусловленными остеоартритом, на протяжении от 18 до 30 мес. [29, 30]. Даже столь длительный курс лечения характеризовался хорошей переносимостью, приемлемым числом нежелательных побочных эффектов, а также стабильностью противоболевого эффекта.
Наличие стабильных противоболевого и противовоспалительного эффектов, хороший профиль переносимости, возможность одновременного применения с другими лекарственными препаратами обусловливают важную роль препарата Костарокс® в лечении пациентов с подострой и хронической ПБ, обусловленной остеоартритом и другими дегенеративными заболеваниями позвоночника.
С целью повышения эффективности лечения больных как с острой, так и с хронической ПБ рассматривается возможность одновременного применения лекарственных препаратов, оказывающих влияние на некоторые другие механизмы формирования скелетно-мышечной боли. Задачей их применения является сокращение сроков лечения пациента с обострением ПБ, уменьшение потребности в противоболевых препаратах, возможно, предотвращение хронизации боли, увеличение продолжительности периода ремиссии. С этой целью широко применяются препараты, обладающие способностью устранять избыточное напряжение поперечно-полосатой мускулатуры, — миорелаксанты.
Роль миорелаксантов в лечении ПБ
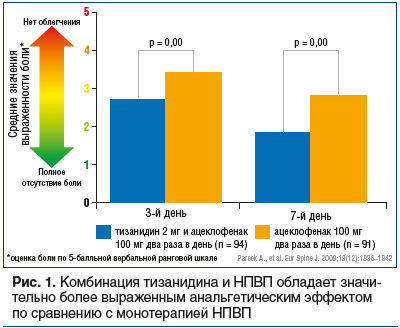
Миорелаксирующим эффектом с сохранением мышечной силы обладает тизанидин (Сирдалуд®), оказывающий, кроме того, умеренное противоболевое действие. Одним из наиболее ценных свойств препарата Сирдалуд® является его способность нивелировать гастроинтестинальные побочные эффекты НПВП. Препарат Сирдалуд® является наиболее предпочтительным среди миорелаксантов для комбинированной терапии с НПВП. Препарат потенцирует действие НПВП, сокращает сроки терапии, а также защищает слизистую ЖКТ от класс-эффекта НПВП в отношении ЖКТ.При локальных болевых синдромах он эффективен как в виде монотерапии, так и в комбинации с НПВП. Так, результаты рандомизированного двойного слепого контролируемого исследования продемонстрировали, что применение тизанидина в дозе 2 мг 2 р/сут в сочетании с ацеклофенаком оказало достоверно более выраженное противоболевое действие по сравнению с таковым при монотерапии ацеклофенаком (рис. 1) [31]. Важно, что аддитивное противоболевое действие препарата Сирдалуд®, назначавшегося в комплексе с НПВП, не зависело от типа препарата [32]. Комбинированное лечение сопровождалось более ранним (уже к 3-му дню) и полным купированием болевого синдрома, а также расширением объема движений в позвоночнике, ограниченного вследствие болевого синдрома [33].
Систематизированные обзоры исследований, посвященных оценке противоспастического действия тизанидина у больных как с поражением центрального мотонейрона, так и со скелетно-мышечными болями, убедительно продемонстрировали высокую эффективность препарата [34]. Положительные результаты клинических исследований, продемонстрировавших эффективность препарата Сирдалуд® у пациентов со скелетно-мышечными болевыми синдромами, явились основанием для его включения в клинические рекомендации, наряду с другими миорелаксантами, по лечению пациентов с ПБ в большинстве стран Евросоюза и странах Северной Америки [35, 36].
Имеются достоверные данные о том, что препарат Сирдалуд® обладает собственным умеренным гастропротективным эффектом вследствие способности уменьшать базальную и индуцированную секрецию кислоты в желудке, а также устранения дисбаланса гликопротеидов в слизистой оболочке желудка и желудочном секрете [37].
Препарат Сирдалуд® характеризуется хорошей переносимостью, редким развитием клинически значимых нежелательных побочных эффектов. Тизанидин оказывает не только миорелаксирующее, но и седативное действие.
Указанное свойство препарата можно и нужно использовать в терапевтических целях путем назначения 2 мг препарата Сирдалуд® за 30 мин до сна либо распределяя суточную дозу препарата на вторую половину дня и на ночь, что способно обеспечить достаточное качество ночного сна, нарушенного у пациента вследствие имеющегося болевого синдрома. В случае, когда седативный эффект нежелателен, его можно контролировать путем титрации дозы, начиная лечение с минимальных разовых и суточных дозировок препарата, постепенно увеличивая дозу до оптимальной. Возможный седативный эффект препарата является кратковременным и зависит от индивидуальной чувствительности.
Препарат Сирдалуд® обладает благоприятными фармакокинетическими свойствами. При приеме внутрь он быстро и практически полностью всасывается из ЖКТ.
Заключение
Таким образом, в настоящее время для лечения пациентов с ПБ существует широкий спектр лекарственных препаратов. Пациентам с острой ПБ показано применение препарата Кетонал®, наличие различных форм которого (пероральные, парентеральные, пролонгированные) обеспечивает возможность выбора наиболее подходящей для конкретного больного лекарственной формы. Повышение эффективности лечения может быть достигнуто одновременным применением препарата Сирдалуд®.RU1904991202












