–Т–≤–µ–і–µ–љ–Є–µ
–Я—Б–Њ—А–Є–∞—В–Є—З–µ—Б–Ї–Є–є –∞—А—В—А–Є—В (–Я–Р) вАФ —Б–µ—А–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–є —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –≤ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ –≤–Њ–≤–ї–µ—З–µ–љ—Л —Б—Г—Б—В–∞–≤—Л –Є —Б—Г—Е–Њ–ґ–Є–ї—М–љ–Њ-—Б–≤—П–Ј–Њ—З–љ—Л–є –∞–њ–њ–∞—А–∞—В [1]. –Т –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞—Е —А–∞–Ј–≤–Є—В–Є—П –Я–Р –±–Њ–ї—М—И—Г—О —А–Њ–ї—М –Є–≥—А–∞—О—В –∞–Ї—В–Є–≤–∞—Ж–Є—П –Ґ-–ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –Є—Е –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Њ–є –≤ –Ґh1 –Є Th17, –њ—А–Њ–і—Г–Ї—Ж–Є—П –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–Њ–≤ 1, 6, 12, 17, 23 [2]. –Я–Њ –і–∞–љ–љ—Л–Љ –Љ–Є—А–Њ–≤—Л—Е —Н–Ї—Б–њ–µ—А—В–Њ–≤, –Я–Р –≤—Б—В—А–µ—З–∞–µ—В—Б—П —Б —З–∞—Б—В–Њ—В–Њ–є –Њ–Ї–Њ–ї–Њ 6 —Б–ї—Г—З–∞–µ–≤ –љ–∞ 100 000 –љ–∞—Б–µ–ї–µ–љ–Є—П –≤ –≥–Њ–і —Б —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М—О 1вАУ2 —Б–ї—Г—З–∞—П –љ–∞ 1000 —З–µ–ї–Њ–≤–µ–Ї –≤ –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є [3]. –Я–Њ –Љ–љ–µ–љ–Є—О –≤–µ–і—Г—Й–Є—Е —А–Њ—Б—Б–Є–є—Б–Ї–Є—Е —Н–Ї—Б–њ–µ—А—В–Њ–≤, –Я–Р –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ —Б—А–µ–і–Є –Љ—Г–ґ—З–Є–љ –Є –ґ–µ–љ—Й–Є–љ [4]. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –ї–Є—В–µ—А–∞—В—Г—А—Л [5] –њ—А–Є —А–∞–љ–љ–µ–Љ –Я–Р —Г–ґ–µ —З–µ—А–µ–Ј 5 –Љ–µ—Б. –њ–Њ—Б–ї–µ –њ–Њ—П–≤–ї–µ–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Г 27% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞–±–ї—О–і–∞—О—В—Б—П —Н—А–Њ–Ј–Є–Є –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б—Г—Б—В–∞–≤–∞—Е, –∞ —З–µ—А–µ–Ј 2 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –і–µ–±—О—В–∞ –Я–Р вАФ –µ—Й–µ —Г 47%, –њ–Њ—Н—В–Њ–Љ—Г —Б–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —В–∞–Ї—В–Є–Ї–∞ –≤–µ–і–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –і–∞–љ–љ–Њ–є –∞—А—В—А–Њ–њ–∞—В–Є–µ–є, —Б–Њ–≥–ї–∞—Б–љ–Њ –Ї–Њ–љ—Ж–µ–њ—Ж–Є–Є treat to target (–ї–µ—З–µ–љ–Є–µ –і–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–Є), –њ—А–µ–і—Г—Б–Љ–∞—В—А–Є–≤–∞–µ—В –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ –±–Њ–ї–µ–µ —А–∞–љ–љ—О—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г –Є –∞–Ї—В–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –і–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Б—В–Њ–є–Ї–Њ–є –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–є —А–µ–Љ–Є—Б—Б–Є–Є –Є–ї–Є –љ–Є–Ј–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —З–µ–Љ—Г –њ—А–µ–њ—П—В—Б—В–≤—Г—О—В –њ–Њ–Ј–і–љ–µ–µ –Њ–±—А–∞—Й–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞ –Ј–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й—М—О, —В—А—Г–і–љ–Њ—Б—В—М –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Я–Р –Ї–∞–Ї –Љ—Г–ї—М—В–Є—Б–Є—Б—В–µ–Љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –њ–Њ–Ј–і–љ—П—П –Є–љ–Є—Ж–Є–∞—Ж–Є—П –±–∞–Ј–Є—Б–љ–Њ–є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–∞—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Ї –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ —Б—А–µ–і—Б—В–≤–∞–Љ, –∞ —В–∞–Ї–ґ–µ –∞–Ї—Б–Є–∞–ї—М–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П. –Т—Б–µ —Н—В–Є —Д–∞–Ї—В–Њ—А—Л –≤–Љ–µ—Б—В–µ —Б –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–Љ–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –њ–∞—Ж–Є–µ–љ—В–∞ (–≤–Њ—Б–њ—А–Є—П—В–Є–µ –±–Њ–ї–µ–Ј–љ–Є, –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л –њ–µ—А—Ж–µ–њ—Ж–Є–Є –±–Њ–ї–Є, —Б–Њ—Ж–Є–∞–ї—М–љ–Њ-–Ї—Г–ї—М—В—Г—А–љ—Л–µ —Г—Б—В–∞–љ–Њ–≤–Ї–Є) —Г—З–∞—Б—В–≤—Г—О—В –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–•–С–°) –Є –њ—А–µ–њ—П—В—Б—В–≤—Г—О—В –і–Њ—Б—В–Є–ґ–µ–љ–Є—О —А–µ–Љ–Є—Б—Б–Є–Є. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –•–С–° —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї —Б–ї–Њ–ґ–љ—Л–є –Љ–љ–Њ–≥–Њ–Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ, –Ї–Њ—В–Њ—А—Л–є —Н–≤–Њ–ї—О—Ж–Є–Њ–љ–љ–Њ –љ–µ –љ–µ—Б–µ—В –∞–і–∞–њ—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є, –∞ —П–≤–ї—П–µ—В—Б—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ вАФ –і–µ–Ј–Њ—А–≥–∞–љ–Є–Ј—Г–µ—В —А–∞–±–Њ—В—Г —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –њ—А–Є–≤–Њ–і—П –Ї —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є–Є. –°–Њ–≥–ї–∞—Б–љ–Њ –Љ–љ–µ–љ–Є—О –Љ–Є—А–Њ–≤—Л—Е –∞–≤—В–Њ—А–Њ–≤ –љ–∞–±–ї—О–і–∞–µ–Љ—Л–є –њ—А–Є —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –•–С–°, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –њ—А–Є –Я–Р, —Б–Њ—Б—В–Њ–Є—В –Є–Ј –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–≥–Њ, –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –Є –љ–µ–ЄћЖ-—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ [6]. –Э–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М (–Э–С) —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–Њ–≤ –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Љ–Њ–ґ–µ—В —Б—З–Є—В–∞—В—М—Б—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –Є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—В—М –±–Њ–ї–µ–≤—Г—О —Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–∞—Ж–Є—О —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р, –Є–Љ–Є—В–Є—А—Г—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—В–Є–≤–Њ—А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [7]. –Т—Л—Б–Ї–∞–Ј–∞–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ [8], —З—В–Њ –і–ї–Є—В–µ–ї—М–љ–∞—П –њ–µ—А—Б–Є—Б—В–µ–љ—Ж–Є—П –•–С–° —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є–Є (–¶–°), —Г—Б—Г–≥—Г–±–ї—П—О—Й–µ–є —В–µ—З–µ–љ–Є–µ –ї—О–±–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Ю —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –Э–С —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –љ–µ –Љ–љ–Њ–≥–Є–µ –Ј–∞—А—Г–±–µ–ґ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є: –≤ 2019 –≥. –Э–С —Б—А–µ–і–Є 64 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –≤—Л—П–≤–Є–ї–Є —Г 26,6%, –∞ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 2020 –≥. вАФ —Г 25% –Є–Ј 118 –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е —Б –Я–Р [9вАУ11]. –Ю—В—Б—Г—В—Б—В–≤–Є–µ –Ї—А—Г–њ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –Э–С —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –≤ –†–Њ—Б—Б–Є–Є –Є –Љ–Є—А–µ, –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Э–С —Б –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О, –Њ—В–і–µ–ї—М–љ—Л–Љ–Є –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–Љ–Є, –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Є –Ї–∞—З–µ—Б—В–≤–Њ–Љ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –±–Њ–ї—М—И–Њ–є –њ—А–Њ–±–µ–ї –≤ –њ–Њ–љ–Є–Љ–∞–љ–Є–Є –њ–Њ–ї–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –і–∞–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –і–ї—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л –≤–∞–ґ–љ–Њ, —З—В–Њ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Я–Р –Є –•–С–° —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ–Њ–ґ–µ—В —Б–љ–Є–ґ–∞—В—М—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [12] –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –≤–Њ–Ј–љ–Є–Ї–∞—О—В –љ–µ–і–Њ—Б—В–∞—В–Њ–Ї –Ї–Њ–Љ–њ–ї–∞–µ–љ—В–љ–Њ—Б—В–Є, —Г—В—А–∞—В–∞ –і–Њ–≤–µ—А–Є—П –Ї —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ–µ. –Э–∞ –њ—А–∞–Ї—В–Є–Ї–µ –і–∞–ґ–µ –њ—А–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є —Б—В–Њ–є–Ї–Њ–є –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–є —А–µ–Љ–Є—Б—Б–Є–Є –Є–ї–Є –љ–Є–Ј–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Я–Р –њ–∞—Ж–Є–µ–љ—В—Л –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –ґ–∞–ї–Њ–≤–∞—В—М—Б—П –љ–∞ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –±–Њ–ї–µ–≤—Л–µ –Њ—Й—Г—Й–µ–љ–Є—П, —З—В–Њ –Ј–∞—З–∞—Б—В—Г—О –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–Љ –Ї–∞–Ї –Њ–±–Њ—Б—В—А–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –љ–µ –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞—П –≤–Њ–≤–ї–µ—З–µ–љ–Є–µ –≤ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –Є–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А, –Њ—В–ї–Є—З–љ—Л—Е –Њ—В —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ –Є –Њ–Ї–Њ–ї–Њ—Б—Г—Б—В–∞–≤–љ—Л—Е —В–Ї–∞–љ–µ–є. –Ю—В–і–µ–ї—М–љ–Њ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ—А–Є –Я–Р —Б –•–С–° –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є [13, 14]. –Э–∞–њ—А–Є–Љ–µ—А, –≥—А—Г–њ–њ–∞ –Ї–∞–љ–∞–і—Б–Ї–Є—Е –∞–≤—В–Њ—А–Њ–≤ [15] –≤ 2021 –≥. –њ–Њ–Ї–∞–Ј–∞–ї–∞, —З—В–Њ –љ–Є–Ј–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –Љ–Њ–≥—Г—В –±—Л—В—М –њ—А–µ–і–Є–Ї—В–Њ—А–∞–Љ–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–Є –Я–Р. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Я–Р, –і–∞–ґ–µ –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –±–∞–Ј–Є—Б–љ–Њ–є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –Є –≥–µ–љ–љ–Њ-–Є–љ–ґ–µ–љ–µ—А–љ–Њ–є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–µ–Њ—В—К–µ–Љ–ї–µ–Љ–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ –•–С–° –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–∞ [16].
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ–њ—А–µ–і–µ–ї–Є—В—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р —З–∞—Б—В–Њ—В—Г –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Э–С, –љ–∞–ї–Є—З–Є–µ —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –Э–С –Є –њ–Њ–ї–Њ–Љ, –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —Б—В–∞–ґ–µ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є–µ–є (–¶–°), –Ї–∞—З–µ—Б—В–≤–Њ–Љ –ґ–Є–Ј–љ–Є.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–µ–љ–Њ 88 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –≤ –≤–Њ–Ј—А–∞—Б—В–µ —Б—В–∞—А—И–µ 18 –ї–µ—В –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –љ–∞—Е–Њ–і–Є–≤—И–Є—Е—Б—П –љ–∞ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –≤ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Њ—В–і–µ–ї–µ–љ–Є–Є –С–£–Ч –£–† ¬Ђ–†–Ъ–Ф–¶ –Ь–Ч –£–†¬ї. –Ъ—А–Є—В–µ—А–Є—П–Љ–Є –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —П–≤–ї—П–ї–Є—Б—М –і–Є–∞–≥–љ–Њ–Ј –Я–Р –њ–Њ –Ї—А–Є—В–µ—А–Є—П–Љ CASPAR 2006 –≥., –њ–Њ–і–њ–Є—Б–∞–љ–љ–Њ–µ –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ —Б–Њ–≥–ї–∞—Б–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞ –љ–∞ —Г—З–∞—Б—В–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –Ъ—А–Є—В–µ—А–Є—П–Љ–Є –љ–µ–≤–Ї–ї—О—З–µ–љ–Є—П –±—Л–ї–Є: –љ–∞–ї–Є—З–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –•–С–° –Є–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є (–Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ, —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ, –љ–∞–њ—А–Є–Љ–µ—А —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В), –љ–∞–ї–Є—З–Є–µ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–ЄћЖ, —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ —Б—В–∞–і–Є–Є –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є; –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М –Є –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤—Л–є –њ–µ—А–Є–Њ–і –Љ–µ–љ–µ–µ 6 –Љ–µ—Б. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤—Л–њ–Њ–ї–љ—П–ї–Њ—Б—М –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —Н—В–Є—З–µ—Б–Ї–Є–Љ–Є —Б—В–∞–љ–і–∞—А—В–∞–Љ–Є –•–µ–ї—М—Б–Є–љ–Ї—Б–Ї–Њ–ЄћЖ –і–µ–Ї–ї–∞—А–∞—Ж–Є–Є.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б –њ–Њ–і—Б—З–µ—В–Њ–Љ —З–Є—Б–ї–∞ –њ—А–Є–њ—Г—Е—И–Є—Е —Б—Г—Б—В–∞–≤–Њ–≤ (–І–Я–°, 0вАУ66) –Є —З–Є—Б–ї–∞ –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ (–І–С–°, 0вАУ68). –Ю—Ж–µ–љ–Ї–∞ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–Є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –≤–Є–Ј—Г–∞–ї—М–љ–Њ-–∞–љ–∞–ї–Њ–≥–Њ–≤–Њ–є —И–Ї–∞–ї—Л (–Т–Р–® –±–Њ–ї–Є, 0вАУ100 –Љ–Љ). –Ы–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–∞–ї–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –°-—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ (–°–†–С, –Љ–≥/–ї). –Р–Ї—В–Є–≤–љ–Њ—Б—В—М –Я–Р –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –њ–Њ –Є–љ–і–µ–Ї—Б—Г Disease activity in psoriatic arthritis (DAPSA): –њ—А–Є –Ј–љ–∞—З–µ–љ–Є—П—Е DAPSA 0вАУ4 –±–∞–ї–ї–∞ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М —А–µ–Љ–Є—Б—Б–Є—П, 4,1вАУ14 –±–∞–ї–ї–Њ–≤ вАФ –љ–Є–Ј–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, 14,1вАУ28 –±–∞–ї–ї–Њ–≤ вАФ —Г–Љ–µ—А–µ–љ–љ–∞—П –Є вЙ•28,1 –±–∞–ї–ї–∞ вАФ –≤—Л—Б–Њ–Ї–∞—П. –Ф–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П —Н—А–Њ–Ј–Є–≤–љ–Њ–≥–Њ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В—А–Є—В–∞ –њ—А–Њ–≤–Њ–і–Є–ї–Є —А–µ–љ—В–≥–µ–љ–Њ–≥—А–∞—Д–Є—О –Ї–Є—Б—В–µ–є –Є —Б—В–Њ–њ –≤ –њ—А—П–Љ–Њ–є –њ—А–Њ–µ–Ї—Ж–Є–Є. –Э–∞–ї–Є—З–Є–µ –Э–С –Њ–њ—А–µ–і–µ–ї—П–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О —А—Г—Б—Б–Ї–Њ—П–Ј—Л—З–љ–Њ–є –≤–µ—А—Б–Є–Є –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ PainDetect (PDQ), –Ї–Њ—В–Њ—А—Л–є –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ –њ–Њ–Ї–∞–Ј–∞–ї –љ–∞–і–µ–ґ–љ–Њ—Б—В—М –Є –≤–∞–ї–Є–і–љ–Њ—Б—В—М –≤ —А–∞–±–Њ—В–µ —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –Я–Р. –Э–С —Б—З–Є—В–∞–ї–Є –≤—Л—П–≤–ї–µ–љ–љ–Њ–є –њ—А–Є –Ј–љ–∞—З–µ–љ–Є—П—Е PDQ вЙ•19 –±–∞–ї–ї–Њ–≤, –њ—А–Є —Н—В–Њ–Љ –љ–µ–≤—А–Њ–ї–Њ–≥ –њ—А–Њ–≤–Њ–і–Є–ї –Њ—Б–Љ–Њ—В—А –і–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Є–ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –Э–С [17]. –¶–° –Њ–њ—А–µ–і–µ–ї—П–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О —А—Г—Б—Б–Ї–Њ—П–Ј—Л—З–љ–Њ–є –≤–µ—А—Б–Є–Є –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ CSI: –њ—А–Є –Ј–љ–∞—З–µ–љ–Є—П—Е вЙ•30 –±–∞–ї–ї–Њ–≤ –¶–° —Б—З–Є—В–∞–µ—В—Б—П –≤—Л—П–≤–ї–µ–љ–љ–Њ–є –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–є [18]. –Ъ–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ The Short Form-36 (SF-36) —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ (–§–Ъ –Є –Я–Ъ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) –Ј–і–Њ—А–Њ–≤—М—П. –Ф–∞–љ–љ—Л–є –Њ–њ—А–Њ—Б–љ–Є–Ї –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ –њ–Њ–Ї–∞–Ј–∞–ї –љ–∞–і–µ–ґ–љ–Њ—Б—В—М –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р [18].
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О –њ—А–Њ–≥—А–∞–Љ–Љ—Л IBM SPSS 26.0. –Я—А–Њ–≤–µ—А–Ї—Г —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –љ–∞ –љ–Њ—А–Љ–∞–ї—М–љ–Њ—Б—В—М –≤—Л–њ–Њ–ї–љ—П–ї–Є –њ–Њ –Ї—А–Є—В–µ—А–Є—О –Ъ–Њ–ї–Љ–Њ–≥–Њ—А–Њ–≤–∞ вАФ –°–Љ–Є—А–љ–Њ–≤–∞ —Б –њ–Њ—Б—В—А–Њ–µ–љ–Є–µ–Љ –Ї–≤–∞–љ—В–Є–ї—М–љ—Л—Е –і–Є–∞–≥—А–∞–Љ–Љ (Q-Q Plots). –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї—Г—О –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–Є–є –љ–Њ—А–Љ–∞–ї—М–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е –Њ–њ—А–µ–і–µ–ї—П–ї–Є –њ–Њ –Ї—А–Є—В–µ—А–Є—О –°—В—М—О–і–µ–љ—В–∞ –і–ї—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≤—Л–±–Њ—А–Њ–Ї, –љ–Њ—А–Љ–∞–ї—М–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Ј–∞–≤–Є—Б–Є–Љ—Л—Е –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е вАФ –њ–Њ –Ї—А–Є—В–µ—А–Є—О –°—В—М—О–і–µ–љ—В–∞ –і–ї—П –њ–∞—А–љ—Л—Е –≤—Л–±–Њ—А–Њ–Ї, –і–ї—П —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Њ—В–ї–Є—З–љ–Њ –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е вАФ –њ–Њ –Ї—А–Є—В–µ—А–Є—О –Ь–∞–љ–љ–∞ вАФ –£–Є—В–љ–Є –і–ї—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –Є –њ–Њ –Ї—А–Є—В–µ—А–Є—О –£–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞ вАФ –і–ї—П –Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≤—Л–±–Њ—А–Њ–Ї, –і–ї—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е вАФ –њ–Њ –Ї—А–Є—В–µ—А–Є—О ѕЗ2 –Я–Є—А—Б–Њ–љ–∞, –Ј–∞–≤–Є—Б–Є–Љ—Л—Е вАФ –њ–Њ –Ї—А–Є—В–µ—А–Є—О –Ь–∞–Ї-–Эe–Љ–∞—А–∞. –Ф–ї—П –≤—Б–µ—Е –≤–Є–і–Њ–≤ –∞–љ–∞–ї–Є–Ј–∞ –і–∞–љ–љ—Л—Е —А–∞–Ј–ї–Є—З–Є—П —Б—З–Є—В–∞–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є –њ—А–Є pвЙ§0,05. –Э–Њ—А–Љ–∞–ї—М–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Ї–∞–Ї —Б—А–µ–і–љ–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ (–Ь), —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ (–°–Ю) –Є 95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї (–Ф–Ш) (–Ь¬±–°–Ю; 95% –Ф–Ш), –і–∞–љ–љ—Л–µ, —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е –Њ—В–ї–Є—З–∞–ї–Њ—Б—М –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ, вАФ –Ї–∞–Ї –Љ–µ–і–Є–∞–љ–∞ (Me), 25-–є, 75-–є –њ—А–Њ—Ж–µ–љ—В–Є–ї–Є –Є 95% –Ф–Ш (–Ь–µ [25%; 75%]; 95% –Ф–Ш).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Њ 2 –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤: —Б –Э–С (–≥—А—Г–њ–њ–∞ –Э–С+) –Є –±–µ–Ј –Э–С (–≥—А—Г–њ–њ–∞ –Э–С-) (—Б–Љ. —В–∞–±–ї–Є—Ж—Г).
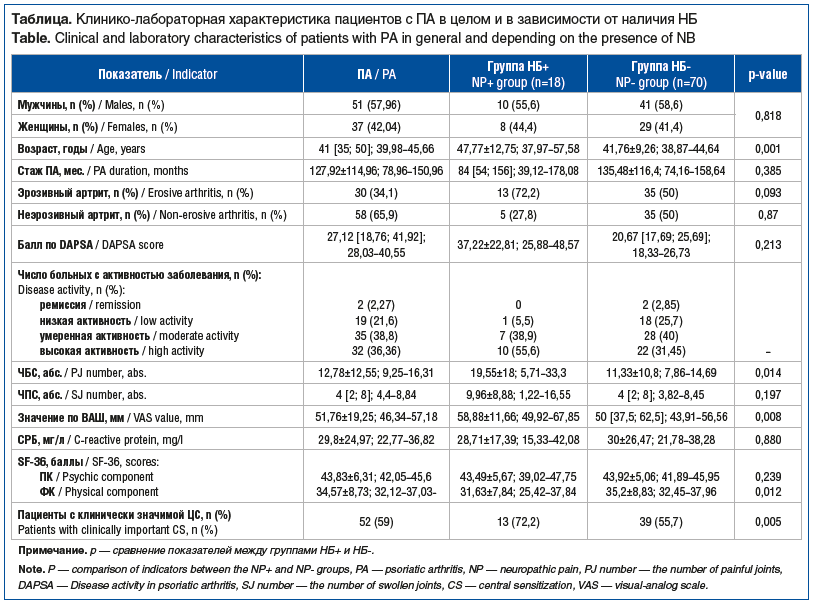
–°—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ—Л–µ –≥—А—Г–њ–њ—Л –±—Л–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л –њ–Њ –њ–Њ–ї—Г –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е. –У—А—Г–њ–њ—Г –Э–С+ —Б–Њ—Б—В–∞–≤–Є–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л –±–Њ–ї–µ–µ —Б—В–∞—А—И–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (p=0,001). –†–∞–Ј–љ–Є—Ж—Л –≤ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є —В–µ—З–µ–љ–Є—П –Я–Р –≤ –≥—А—Г–њ–њ–∞—Е –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ (—А=0,385), –Њ–і–љ–∞–Ї–Њ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –±–Њ–ї—М—И–µ–є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Э–С. –У—А—Г–њ–њ—Л –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М –њ–Њ —З–Є—Б–ї—Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Н—А–Њ–Ј–Є–≤–љ—Л–Љ –Є –љ–µ—Н—А–Њ–Ј–Є–≤–љ—Л–Љ –Я–Р. –Ь—Л –љ–µ –≤—Л—П–≤–Є–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є —Б—А–µ–і–љ–Є—Е –Ј–љ–∞—З–µ–љ–Є–є –Є–љ–і–µ–Ї—Б–∞ DAPSA (p=0,213) –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞–µ–Љ—Л–µ –±√≥–ї—М—И–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —В–∞–Ї–Њ–≤–Њ–≥–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–С. –Т –≥—А—Г–њ–њ–µ –Э–С+ –Њ–њ—А–µ–і–µ–ї–µ–љ—Л –±√≥–ї—М—И–Є–µ —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –њ–Њ –Т–Р–® –±–Њ–ї–Є, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –Э–С- (—А=0,008). –°—А–µ–і–љ–µ–µ –І–С–° —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–С –њ—А–µ–≤—Л—И–∞–ї–Њ —В–∞–Ї–Њ–≤–Њ–µ –≤ –≥—А—Г–њ–њ–µ –±–µ–Ј –Э–С (—А=0,014). –°—А–µ–і–љ–µ–µ –І–Я–° –≤ –≥—А—Г–њ–њ–∞—Е –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Њ—Б—М (—А=0,197). –†–∞–Ј–ї–Є—З–Є–є –≤ —Б—А–µ–і–љ–Є—Е –Ј–љ–∞—З–µ–љ–Є—П—Е —Г—А–Њ–≤–љ—П –°–†–С –≤ –≥—А—Г–њ–њ–∞—Е –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ (p=0,880). –£ –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є —Б–Њ–≥–ї–∞—Б–љ–Њ –Њ–њ—А–Њ—Б–љ–Є–Ї—Г SF-36, –њ—А–Є—З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л –Э–С+ –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –≥—А—Г–њ–њ–Њ–є –Э–С- –±—Л–ї–Є —Б–љ–Є–ґ–µ–љ—Л —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –§–Ъ (p=0,012), –љ–Њ –љ–µ –Я–Ъ (—А=0,239). –£ 52 (59%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –≤—Л—П–≤–ї–µ–љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П –¶–°. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤—Л—Б–Њ–Ї—Г—О —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–є –¶–° –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л –Э–С+ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П –¶–° –≤—Б—В—А–µ—З–∞–ї–∞—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —З–∞—Й–µ (—А=0,005).
–Э–∞–Љ–Є –≤—Л—П–≤–ї–µ–љ–∞ –≤—Л—Б–Њ–Ї–∞—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Э–С –Є –¶–° —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р (20,4 –Є 59% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Э–С –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–∞—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–Њ–ї–µ–µ —Б—В–∞—А—И–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –°—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–є –Э–С —Б—А–µ–і–љ–µ–µ –І–С–° –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Т–Р–® –±–Њ–ї–Є –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ, –Њ–і–љ–∞–Ї–Њ —Б—А–µ–і–љ—П—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —Б—А–µ–і–љ–µ–µ –І–Я–°, —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –Є–љ–і–µ–Ї—Б–∞ DAPSA –Є –Ј–љ–∞—З–µ–љ–Є—П –°–†–С –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—П–≤–ї–µ–љ–љ–Њ–є –Э–С –љ–µ –Њ—В–ї–Є—З–∞–ї–Є—Б—М –Њ—В —В–∞–Ї–Њ–≤—Л—Е —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Э–С. –°—Е–Њ–ґ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї—Г—З–µ–љ—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [19], –њ–Њ–Ї–∞–Ј–∞–≤—И–µ–Љ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Я–Р –Є –Э–С. –Ь—Л —Б—З–Є—В–∞–µ–Љ, —З—В–Њ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –•–С–° –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ —Б–Њ —Б—В–Њ–ї—М –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, —З—В–Њ —Н—В–Њ –Љ–Њ–ґ–µ—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ ¬Ђ–Ј–∞–≤—Л—И–∞—В—М¬ї –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Ј–∞ —Б—З–µ—В —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ—Б–њ—А–Є—П—В–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Є —В—П–ґ–µ—Б—В–Є –њ—А–Њ—П–≤–ї–µ–љ–Є–є –±–Њ–ї–µ–Ј–љ–Є –Є –Є—Б–Ї–∞–ґ–∞—В—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–µ –≤—А–∞—З–∞ –Њ–± –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є–ї–Є –±—Л—В—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ —В—П–ґ–µ–ї–Њ–≥–Њ –Є –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Ш–љ—Л–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–С –љ–µ –Є—Б–Ї–ї—О—З–∞–µ—В—Б—П –≤–Ї–ї–∞–і –љ–µ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–Ј–љ–Є. –Э–∞—И–Є –≤—Л–≤–Њ–і—Л —Б–Њ–≥–ї–∞—Б—Г—О—В—Б—П —Б –і–∞–љ–љ—Л–Љ–Є –≥—А—Г–њ–њ—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є, –њ–Њ–Ї–∞–Ј–∞–≤—И–Є–Љ–Є –њ—А–Є—Б—Г—В—Б—В–≤–Є–µ –Э–С —Г 24% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р, –Є –Є—Е –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ–Љ –Њ –≤–Ї–ї–∞–і–µ –Э–С –≤ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є–є –Т–Р–® –±–Њ–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р [19]. –Ь—Л –љ–∞–±–ї—О–і–∞–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –§–Ъ –Є –Я–Ъ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є —Б—А–µ–і–Є –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р, –њ—А–Є —Н—В–Њ–Љ —Б—А–µ–і–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –§–Ъ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–С –±—Л–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–Є–ґ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤—Л–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Э–С, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –≤ –њ–Њ–ї—М–Ј—Г –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–С. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ —Б–Њ–Њ—В–љ–Њ—Б–Є–Љ—Л —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е –∞–≤—В–Њ—А–Њ–≤, –Њ—В–Љ–µ—З–∞–≤—И–Є—Е —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–С –њ—А–Є –Я–Р [20]. –Ш–љ—В–µ—А–µ—Б–љ–Њ, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–є –Э–С –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П –¶–° –≤—Б—В—А–µ—З–∞–ї–∞—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —З–∞—Й–µ, —З—В–Њ –Љ–Њ–ґ–µ—В –≥–Њ–≤–Њ—А–Є—В—М –Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ –≤–Ї–ї–∞–і–µ –њ–Њ—Б–ї–µ–і–љ–µ–є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г –•–С–° –њ—А–Є –і–∞–љ–љ–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є. –†–µ–Ј—Г–ї—М—В–∞—В—Л –љ–∞—И–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–Њ–Њ—В–љ–Њ—Б—П—В—Б—П —Б –љ–µ–і–∞–≤–љ–Є–Љ –Ј–∞—А—Г–±–µ–ґ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ [21], –Ї–Њ—В–Њ—А–Њ–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї–Њ –¶–° —Г 42,9% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р, –∞–≤—В–Њ—А—Л —В–∞–Ї–ґ–µ —Г–Ї–∞–Ј–∞–ї–Є –љ–∞ –Є—Б–Ї–∞–ґ–µ–љ–Є–µ –Є–љ–і–µ–Ї—Б–∞ DAPSA —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –¶–°. –Э–∞—И–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–Ј–≤–Њ–ї—П—О—В –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—В—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р ¬Ђ–±–Њ–ї–µ–≤—Г—О —Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–∞—Ж–Є—О¬ї, –Ї–Њ—В–Њ—А–∞—П —В—А–µ–±—Г–µ—В –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–≥–Њ –Є –Љ–µ–ґ–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ —Б —Г—З–µ—В–Њ–Љ –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В–Є –Ї–ї–Є–љ–Є–Ї–Є –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Т—Л–≤–Њ–і—Л –љ–∞—И–µ–є —А–∞–±–Њ—В—Л —З–µ—В–Ї–Њ –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В —Г—З–∞—Б—В–Є–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –Є —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е –љ–µ–є—А–Њ–≥–µ–љ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –≤ —А–∞–Ј–≤–Є—В–Є–Є –•–С–° –њ—А–Є –Я–Р.
–°—В–Њ–Є—В —Г–Ї–∞–Ј–∞—В—М –Є –і—А—Г–≥—Г—О —В–Њ—З–Ї—Г –Ј—А–µ–љ–Є—П. –Ґ–∞–Ї, –∞–≤—В–Њ—А—Л –±–Њ–ї–µ–µ —А–∞–љ–љ–µ–є —А–∞–±–Њ—В—Л [22] —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –њ—А–Є–љ—П—В–Є—П –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ –Ї—Г–ї—М—В—Г—А–љ—Л—Е –Є —Б–Њ—Ж–Є–∞–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–µ–≥–Є–Њ–љ–∞, –Ї –Ї–Њ—В–Њ—А—Л–Љ –њ—А–Є–љ–∞–і–ї–µ–ґ–∞—В –Ї–Њ–≥–Њ—А—В—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–∞–±–ї—О–і–∞–µ–Љ–Њ–є –¶–°, –њ–Њ–і—З–µ—А–Ї–Є–≤–∞—П –Є–Љ–µ–љ–љ–Њ –Є—Е —А–µ—И–∞—О—Й—Г—О —А–Њ–ї—М, –∞ –љ–µ —Б–∞–Љ–Њ –±—А–µ–Љ—П –±–Њ–ї–µ–Ј–љ–Є.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –≤—Л—П–≤–ї–µ–љ–∞ —З–∞—Б—В–∞—П –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В—М –Э–С вАФ 20,1%, –Ї–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ ¬Ђ–Ј–∞–≤—Л—И–∞—В—М¬ї –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Ј–∞ —Б—З–µ—В —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е —Б—Г–ґ–і–µ–љ–Є–є –њ–∞—Ж–Є–µ–љ—В–∞ –Њ —В—П–ґ–µ—Б—В–Є –±–Њ–ї–µ–Ј–љ–Є, –Њ–і–љ–∞–Ї–Њ —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є —Б–љ–Є–ґ–∞–µ—В –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є. –Ґ–∞–Ї, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –Ј–љ–∞—З–µ–љ–Є—П –§–Ъ –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–Є–ґ–µ –≤ –≥—А—Г–њ–њ–µ –Э–С+, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –Э–С- (p=0,012). –С–Њ–ї–µ–µ —З–µ–Љ —Г –њ–Њ–ї–Њ–≤–Є–љ—Л (59%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Я–Р –≤—Л—П–≤–ї–µ–љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П –¶–° (–≤ –≥—А—Г–њ–њ–µ –Э–С+ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —З–∞—Й–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –Э–С- (—А=0,005)). –Ф–∞–ї—М–љ–µ–є—И–µ–µ –Є–Ј—Г—З–µ–љ–Є–µ –і–∞–љ–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–ї—П –±–Њ–ї–µ–µ —В–Њ—З–љ–Њ–є –Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Я–Р, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –±–Њ–ї–µ–≤–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞, –∞ —В–∞–Ї–ґ–µ –і–ї—П —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–µ—А—Б–Њ–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –≤ –Њ–Ї–∞–Ј–∞–љ–Є–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –Є –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —Б—В—А–∞—В–µ–≥–Є–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–є –і–ї—П –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П –і–Њ—Б—В–Њ–є–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Н—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є.
–°–≤–µ–і–µ–љ–Є—П –Њ–± –∞–≤—В–Њ—А–∞—Е:
–Р–Ї—Г–ї–Є–љ—Г—И–Ї–Є–љ–∞ –Х–Ї–∞—В–µ—А–Є–љ–∞ –Ѓ—А—М–µ–≤–љ–∞ вАФ –≤—А–∞—З-—А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥ –С–£–Ч –£–† ¬Ђ–†–Ъ–Ф–¶ –Ь–Ч –£–†¬ї; 426000, –†–Њ—Б—Б–Є—П, –≥. –Ш–ґ–µ–≤—Б–Ї, —Г–ї. –Ы–µ–љ–Є–љ–∞, –і. 87–С; ORCID iD 0000-0002-9321-431X.
–Ш–≤–∞–љ–Њ–≤–∞ –Ы–∞—А–Є—Б–∞ –Т–ї–∞–і–Є–Љ–Є—А–Њ–≤–љ–∞ вАФ –≥–ї–∞–≤–љ—Л–є –≤–љ–µ—И—В–∞—В–љ—Л–є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В –Ь–Ч –£–† –њ–Њ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ј–∞–≤–µ–і—Г—О—Й–∞—П —Б—В–∞—Ж–Є–Њ–љ–∞—А–Њ–Љ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–і–µ–ї–µ–љ–Є—П –С–£–Ч –£–† ¬Ђ–†–Ъ–Ф–¶ –Ь–Ч –£–†¬ї; 426000, –†–Њ—Б—Б–Є—П, –≥. –Ш–ґ–µ–≤—Б–Ї, —Г–ї. –Ы–µ–љ–Є–љ–∞, –і. 87–С; ORCID iD 0000-0003-0411-6118.
–ѓ–Ї—Г–њ–Њ–≤–∞ –°–≤–µ—В–ї–∞–љ–∞ –Я–µ—В—А–Њ–≤–љ–∞ вАФ –Ї.–Љ.–љ., –≥–ї–∞–≤–љ—Л–є –≤–љ–µ—И—В–∞—В–љ—Л–є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В –Ь–Ч –†–Ґ –њ–Њ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, –і–Њ—Ж–µ–љ—В –Ї–∞—Д–µ–і-—А—Л –≥–Њ—Б–њ–Є—В–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –§–У–С–Ю–£ –Т–Ю –Ъ–∞–Ј–∞–љ—Б–Ї–Є–є –У–Ь–£ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є; 420012, –†–Њ—Б—Б–Є—П, –≥. –Ъ–∞–Ј–∞–љ—М, —Г–ї. –С—Г—В–ї–µ—А–Њ–≤–∞, –і. 49; ORCID iD 0000-0002-8590-4839.
–ѓ–Ї—Г–њ–Њ–≤ –≠–і—Г–∞—А–і –Ч–∞–Ї–Є—А–Ј—П–љ–Њ–≤–Є—З вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А, –і–Є—А–µ–Ї—В–Њ—А –Ю–Ю–Ю ¬Ђ–Э–Ш–Ь–Ъ ¬Ђ–Т–∞—И–µ –Ч–і–Њ—А–Њ–≤—М–µ¬ї; 420097, –†–Њ—Б—Б–Є—П, –≥. –Ъ–∞–Ј–∞–љ—М, —Г–ї. –Ф–Њ—Б—В–Њ–µ–≤—Б–Ї–Њ–≥–Њ, –і. 52; ORCID iD 0000-0003-2965-1424.
–Ъ–Њ–љ—В–∞–Ї—В–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П: –Р–Ї—Г–ї–Є–љ—Г—И–Ї–Є–љ–∞ –Х–Ї–∞—В–µ—А–Є–љ–∞ –Ѓ—А—М–µ–≤–љ–∞, e-mail: katewenterly@gmail.com.
–Ш—Б—В–Њ—З–љ–Є–Ї —Д–Є–љ–∞–љ—Б–Є—А–Њ–≤–∞–љ–Є—П: –∞–≤—В–Њ—А—Л –љ–µ –Є–Љ–µ—О—В —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –Є–ї–Є –Љ–µ—В–Њ–і–∞—Е.
–Ъ–Њ–љ—Д–ї–Є–Ї—В –Є–љ—В–µ—А–µ—Б–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В.
–°—В–∞—В—М—П –њ–Њ—Б—В—Г–њ–Є–ї–∞ 20.01.2023.
–Я–Њ—Б—В—Г–њ–Є–ї–∞ –њ–Њ—Б–ї–µ —А–µ—Ж–µ–љ–Ј–Є—А–Њ–≤–∞–љ–Є—П 14.02.2023.
–Я—А–Є–љ—П—В–∞ –≤ –њ–µ—З–∞—В—М 14.03.2023.
About the authors:
Ekaterina Yu. Akulinushkina вАФ rheumatologist, Republican Clinical and Diagnostic Center of the Ministry of Health of the Udmurt Republic; 87B, Lenin str., Izhevsk, 426000, Russian Federation; ORCID iD 0000-0002-9321-431X.
Larisa V. Ivanova вАФ chief external specialist in rheumatology of the Ministry of Health of the Udmurt Republic, Head of the Rheumatology Department Hospital, Republican Clinical and Diagnostic Center of the Ministry of Health of the Udmurt Republic; 87B, Lenin str., Izhevsk, 426000, Russian Federation; ORCID iD 0000-0003-0411-6118.
Svetlana P. Yakupova вАФ C. Sc. (Med.), chief external specialist in rheumatology of the Ministry of Health of the Udmurt Republic, associate professor of the Department of Hospital Therapy, Kazan State Medical University; 49, Butlerov str., Kazan, 420012, Russian Federation; ORCID iD 0000-0002-8590-4839.
Eduard Z. Yakupov вАФ Dr. Sc. (Med.), Professor, Director, LLC "Research Medical Complex вАЬVashe Zdorovie"; 52, Dostoevsky str., Kazan, 420097, Russian Federation; ORCID iD 0000-0003-2965-1424.
Contact information: Ekaterina Yu. Akulinushkina, e-mail: katewenterly@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 20.01.2023.
Revised 14.02.2023.
Accepted 14.03.2023.












