Актуальность проблемы аллергического ринита
Хронический ринит представляет собой воспалительное заболевание слизистой оболочки полости носа, поражающее около 10–30% взрослых и 40% детей, и стоит на 6-м месте среди наиболее частых хронических заболеваний. За последние 30 лет распространенность данного состояния в промышленно развитых странах резко возросла, в отношении других атопических состояний (например, астмы) отмечается схожая тенденция. Ринит ложится тяжелым бременем на экономику, связанные с ним прямые и непрямые расходы ежегодно составляют от 2 до 5 млрд долл. США [1], а количество пропущенных рабочих дней равно около 3,5 млн в год [2]. Одной из форм ринита является аллергический ринит (АР). Результаты исследований последних лет свидетельствуют о росте заболеваемости АР, особенно в странах с изначально низкой распространенностью. Распространенность подтвержденного диагноза АР среди взрослого населения Европы варьирует от 17 до 28,5% [3], в России — от 12 до 24%. Симптомы АР оказывают выраженное негативное влияние на качество жизни (КЖ) пациентов, нарушая не только повседневную активность, но и качество сна, что, в свою очередь, способствует усталости в течение дня и снижению когнитивных функций [4]. Объединенная рабочая группа по аллергологической практике и ее параметрам (Joint Task Force on Allergy Practice and Parameters) упоминает, что облегчение симптомов уменьшает негативное влияние ринита на повседневную жизнь пациентов. В исследовании L. Devyani et al. изучалось восприятие клинических симптомов и влияние АР на КЖ пациентами и их врачами [5]. Результаты подтвердили, что симптомы тяжело переносятся пациентами и снижают КЖ. Причем пациенты оценивали течение своего заболевания как более тяжелое, чем это представлялось врачам [6]. КЖ отрицательно коррелировало с количеством симптомов, при этом персистирующий АР оказывал значительно большее негативное влияние на пациентов, чем интермиттирующий АР. Более 50% обследованных пациентов использовали 2 или более лекарственных препарата для лечения АР [6].За последние 4 года были разработаны новые международные руководства по диагностике и лечению АР, которые помогли существенно улучшить ведение пациентов с данной нозологией. В 2015 г. был опубликован отчет PRACTALL «Фенотипы и эндотипы ринита: диагностика и лечение» [7], в котором впервые описаны и фенотипы, и эндотипы ринита, представлены подходы к диагностике и лечению ринита с учетом фенотипа и эндотипа, выработана концепция лечения, основанная на контроле клинической картины и охватывающая все подтипы ринита. Предложенная классификация, основывающаяся на фенотипе и эндотипе, способствует переходу к стратифицированной и персонализированной медицине в сфере лечения ринита. В 2016 г. основной документ, являющийся руководством по лечению АР, ARIA (Allergic Rhinitis and its Impacton Asthma — Аллергический ринит и его влияние на астму), подвергся пересмотру [8]. Рекомендации разрабатывались в соответствии с методикой оценки достоверности доказательств и силы рекомендаций в области здравоохранения [9]. Рекомендации ARIA не являются обязательным стандартом терапии, они обеспечивают основу для рациональных решений клиницистов, дают рекомендации для типичных случаев, без учета уникальных индивидуальных обстоятельств, возникающих в реальной клинической практике. Важное замечание: рекомендации ARIA (2016) касаются прежде всего пациентов со среднетяжелым и тяжелым АР, ибо именно эти пациенты, как правило, включаются в клинические исследования, в то время как пациенты с легким АР часто не обращаются за медицинской помощью и сами справляются с симптомами, применяя безрецептурные препараты. Особое внимание эксперты уделили применению пероральных H1-антигистаминных и интраназальных H1-антигистаминных препаратов (АГП), интраназальных кортикостероидов (ИнКС) и антагонистов лейкотриеновых рецепторов и их комбинаций. В 2017 г. Европейская академия аллергологии и иммунологии опубликовала позиционный документ по неаллергическим ринитам (Non-Allergic Rhinitis: Position paper of the European Academy of Allergology and Clinical Immunology), в котором также были рассмотрены фенотипы и эндотипы ринитов [10]. В 2018 г. были обновлены Российские клинические рекомендации по АР, основанные на современных международных руководствах [11].
Современная классификация хронических ринитов и АР
В соответствии с современными представлениями хронический ринит подразделяется на три основных клинических фенотипа: АР, инфекционный ринит и неаллергический, неинфекционный ринит, который, в свою очередь, представлен несколькими подтипами. Фенотипы и эндотипы не имеют четких границ, динамичны и перекрывают друг друга, к тому же способны переходить один в другой, что затрудняет четкое их разграничение (рис. 1).
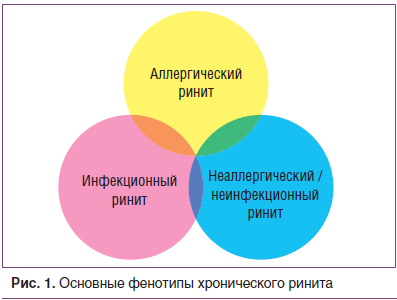
Классификация на основе эндотипов (эндотип — патобиологический механизм, лежащий в основе формирования болезни) на сегодняшний момент условна и требует более четких характеристик и обновленных научных данных. Возможно, в будущем данная классификация в какой-то мере поможет объяснить наблюдаемую вариабельность клинических проявлений и ответа на проводимое лечение [12].
Классификация на основе фенотипов учитывает различные клинические критерии (возраст на момент начала заболевания, тяжесть, внешние проявления заболевания, провоцирующие факторы и пр.). Разрабатываются также все усложняющиеся кластерные подходы, однако в отличие от концепции фенотипирования бронхиальной астмы (БА) применительно к риниту многое требует доработки [13, 14]. Необходимость проведения и оптимизации именно кластерного анализа обусловлена растущим разнообразием выявляемых признаков и симптомов ринита, а также тем соображением, что каждая отдельная группа пациентов, видимо, по-разному реагирует на разные варианты лечения, и будущие перспективные виды лечения не станут исключением. Фенотипы учитывают тяжесть заболевания (легкое течение, умеренное, тяжелое, тяжелое сочетанное заболевание верхних дыхательных путей) [15], длительность течения (острое или хроническое, интермиттирующее или персистирующее) [16], временной паттерн (сезонное или длящееся круглый год), преобладающий симптом (ринорея или заложенность носа) [17], возможность контроля заболевания (поддается контролю или не поддается) [18], пусковой фактор, если он известен (аллерген, инфекционный агент, лекарственный препарат и пр.) [19–21], а также ответ на специфическое лечение (к примеру, ИнКС) [22]. Дополнительно учитывается коморбидная патология, имеющаяся у пациента (респираторная аллергия, риноконъюнктивит). Диагноз АР часто основывается на клинических симптомах и эмпирической эффективности АГП и ИнКС, однако верифицированный диагноз АР можно поставить, только проведя специфическое аллергологическое обследование, которое служит дифференциально-диагностическим приемом и в отношении неаллергического ринита. Следует помнить, что существует много различных видов неаллергических и неинфекционных ринитов: гормональный, медикаментозный, неаллергический эозинофильный, индуцированный пищей, ирритантный, атрофический, эмоциональный и идиопатический (вазомоторный) [12].
Экспертами был выделен особый фенотип АР — локальный аллергический ринит (ЛАР). Как показали результаты исследований последних лет, данный фенотип имеют свыше 47% (47,0–62,5%) больных с симптомами ринита, ранее диагностированного как неаллергический или идиопатический [23]. ЛАР является формой АР с типичными клиническими симптомами и данными анамнеза, но отрицательными результатами кожных проб и отсутствием специфических иммуноглобулинов класса E (IgE) в сыворотке крови. Такие клинические симптомы, как ринорея, чихание, зуд в носу и заложенность носа, типичны для ЛАР. Эти симптомы могут носить круглогодичный или сезонный характер. Диагностика ЛАР проводится с помощью назальных провокационных тестов с предполагаемыми причинно-значимыми аллергенами [24].
На сегодняшний день осталась неизменной классификация АР, в основе которой лежат длительность и тяжесть симптомов, она была предложена консорциумом ARIA, международными сообществами — Европейской академией аллергологии и клинической иммунологии (European Academy of Allergy and Clinical Immunology, EAACI), Всемирной организацией по аллергии (World Allergy Organization) (EAACI/WAO, ARIA 2008 и 2010 гг.). Кроме того, выделяют сезонный и круглогодичный аллергический ринит.
Современные принципы терапии АР
Новая концепция лечения АР на основе контроля симптомов соответствует лечению БА. Для оценки результатов лечения и упрощения мониторинга заболевания используют практический контроль ринита (табл. 1). Следует помнить, что эти критерии относятся к последним 4 нед. до проведения консультации. Необходимо оценить наличие сопутствующих заболеваний (астма, синусит, синдром ночного апноэ), поскольку их обострение может повлиять на эффективность контроля ринита. Потребность в повышенном использовании симптоматических лекарственных препаратов указывает на отсутствие контроля, а любое отклонение от этих критериев указывает на отсутствие контроля и на необходимость перехода к следующему этапу алгоритма лечения. Клиническая оценка должна учитывать длительность отсутствия симптоматики с возможностью возвращения лечения на предыдущий этап алгоритма.
Хотя понятие «контроль ринита» означает главным образом отсутствие симптоматики, в настоящее время единое точное определение этого понятия отсутствует, поскольку выявление симптомов зависит от используемых методов (например, CARAT, RCAT, VAS для полной оценки назальных симптомов и пр.) [25–28]. Тем не менее подход с использованием понятия «контроль» весьма перспективен для рутинного лечения ринита и, в отличие от концепта «тяжесть», может применяться к пациентам, уже получающим лечение [29]. Введен термин «препарат скорой помощи», такими препаратами являются назальные деконгестанты. Следует отметить, что увеличение используемых деконгестантов для купирования симптомов тоже свидетельствует об отсутствии контроля. Наконец, наличие сопутствующих заболеваний при рините также может препятствовать контролю ринита, поскольку от 10 до 40% больных ринитом страдают одновременно и астмой, а некоторые из них — одновременно синдромом ночного апноэ. Тяжесть и контроль всех этих заболеваний, очевидно, связаны с тяжестью и контролем ринита. Подход, включающий оценку контроля, должен стать практическим руководством в клинических условиях для всех пациентов с ринитом, независимо от фенотипа и эндотипа, и дополнить уже валидизированные сегодня инструменты оценки контроля ринита [30].
Для достижения контроля назальных симптомов предлагается терапия, состоящая из четырех ступеней [7, 11]. Каждая из них включает различные варианты фармакологической терапии в зависимости от выраженности симптомов АР. Принцип ступенчатого подхода к лечению АР, равно как и БА, заключается в увеличении объема терапии и переходе на ступень вверх (step-up) при отсутствии контроля симптомов АР и, напротив, снижении объема терапии и переходе на ступень вниз (step-down) в случае контролируемого уменьшения симптомов АР. При назначении терапии рекомендуется разработать индивидуальный план лечения пациента на основе принципов персонифицированной медицины с учетом:
доминирующего или самого неприятного клинического симптома (симптомов) АР, имеющегося у пациента;
эндотипа воспаления (воспаление типа Th2, смешанное воспаление);
сопутствующих заболеваний (конъюнктивит, астма);
предпочтения пациента.
Согласительные документы рекомендуют, учитывая доказанную эффективность ряда лекарственных средств для лечения АР, а также различные пути введения препаратов и различные цели лечения, предоставить пациенту право активного участия в выработке одной из следующих стратегий первой линии для лечения АР (предварительно предоставив пациенту информацию об особенностях того или иного вида лечения). Пациент может выбрать по своему усмотрению пероральный или интраназальный способ введения лекарственных препаратов; вариант лечения с применением или без применения ИнКС; фармакологическое лечение и/или аллерген-специфическую иммунотерапию (АСИТ).
Терапия АР в реальной клинической практике
Несмотря на наличие современных международных и российских согласительных документов по лечению пациентов с АР, в реальной клинической практике, к сожалению, терапия зачастую подбирается эмпирически, без учета клинических рекомендаций, тяжести клинических проявлений и предпочтений пациента. Мы сталкиваемся с тем, что изначально неправильно назначенная терапия АР, без учета тяжести клинической симптоматики, приводит к затягиванию лечебного процесса и усугублению тяжести заболевания, что неизбежно вызывает у пациента недоверие к лечению.Примером может служить анализ 779 амбулаторных карт пациентов с хроническим ринитом, проведенный в нескольких поликлиниках Москвы в 2017 г. При формулировке диагноза лишь однократно был указан интермиттирующий АР, а степень тяжести ринита была упомянута только дважды. Из 216 человек комплексное исследование выполнено у 6,5%, у 52,7% диагноз установлен эмпирическим путем. АГП назначались только 27,3% пациентов, причем 14% — в виде монотерапии. АСИТ проводилась крайне редко, у 1,9% пациентов. Антагонисты лейкотриеновых рецепторов получили 9,7% пациентов (совместно либо с АГП, либо с ИнКС). Лидирующие позиции занимали топические ГКС — 77,8% случаев, причем в 64% — в виде монотерапии. При неаллергическом рините (563 человека) ИнКС получали 77,4%, АГП — 7,5%, монтелукаст — 3,7%, хирургическое лечение — 4,8%. Отмечаются оригинальные методы терапии в виде местных антибиотиков, гомеопатических препаратов, бактериальных лизатов. У пациентов с АР выявлено нарушение схемы ступенчатой терапии [31].
Роль антигистаминных препаратов в терапии АР
Среди препаратов для лечения АР наиболее широко используются пероральные АГП 2-го поколения (АГП 2). Заметим, что ни в одном согласительном документе для лечения АР не рекомендованы АГП 1-го поколения. АГП 2 не только блокируют Н1-гистаминовые рецепторы, но и подавляют продукцию гистамина и других медиаторов поздней фазы аллергического ответа, с чем связано их противовоспалительное действие. Благодаря этим и другим фармакокинетическим преимуществам современных (высокая степень сродства к Н1-рецепторам, быстро наступающий и длительный эффект, отсутствие тахифилаксии, высокий профиль безопасности) АГП 2 предпочтительны при лечении АР. АГП 2 относятся к лекарственным средствам первой ступени, назначаются при первых проявлениях заболевания и применяются в виде монотерапии или в комбинации с другими медикаментозными средствами, такими как топические ГКС [32]. На сегодняшний момент на фармацевтическом рынке представлено большое количество препаратов данной группы, как оригинальных, так и дженериков. Чем руководствуются врачи при назначении терапии? Исследование P. Demoly et al. [33] было предпринято с целью выявления основных критериев, определяющих выбор конкретного АГП 2 аллергологами в лечебных учреждениях Франции. В исследование включали пациентов, страдающих АР или риноконъюнктивитом, за которыми наблюдали в течение 30 дней после назначения монотерапии АГП 2. Участвовали лишь те пациенты, которые, по мнению врача, могли получить пользу от терапии АГП 2.Основное внимание уделялось выявлению критериев, основываясь на которых врач делал выбор в пользу назначения того или иного перорального АГП. Врача просили выбрать и ранжировать по важности три основных критерия из следующего списка: эффективность, быстрота наступления эффекта, длительность эффекта, общая переносимость, отсутствие кардиотоксических эффектов, отсутствие седативного действия, отсутствие усталости, отсутствие сухости во рту, фармакокинетические характеристики, безопасность для пациентов группы риска, удобство лекарственной формы. Врач указывал также основную причину отказа от прежнего лечения (не подходит для пациентов группы риска, неудобная лекарственная форма, недостаточная эффективность, несочетаемость лекарственных препаратов, плохая переносимость). Второстепенными целями явились оценка эффективности и переносимости вновь назначенного АГП 2 и характеристика профиля пациентов, лучше всего реагирующих на это лечение.
Пациентам предлагали самостоятельно заполнять опросник в начале исследования: ежедневно в течение первых 10 дней нового лечения и в конце периода наблюдения. Регистрировали и анализировали данные об эффективности, переносимости, безопасности и характере реакции на лечение, а также удовлетворенность пациента лечением.
237 аллергологов включили в исследование 1080 пациентов с АР от умеренной степени до тяжелой (82,0%). Чаще всего в качестве основания при выборе конкретного АГП 2 указывалась его ожидаемая эффективность (85,3%) (рис. 2). Среднее время до излечения от носовых или глазных симптомов составляло 6 дней, и у 78,2% пациентов в течение этого срока проявлялся значимый эффект. Наличие конъюнктивита оказалось достоверно связано с более быстрым ответом на терапию. В конце периода наблюдения удовлетворение результатом лечения было выше у пациентов, перешедших на эту терапию с прежней (87,5%), чем у пациентов, которым терапия была назначена впервые (78,8%).
![Рис. 2. Критерии назначения АГП 2 для лечения АР в реальной клинической практике, указанные врачами-аллергологами (адаптировано из [33]) Рис. 2. Критерии назначения АГП 2 для лечения АР в реальной клинической практике, указанные врачами-аллергологами (адаптировано из [33])](/upload/medialibrary/213/45-3.png)
Таким образом, основной причиной в пользу выбора нового лечения была его ожидаемая эффективность, а основной причиной прекращения ранее назначенного лечения — отсутствие эффекта.
Один из критериев включения в исследование состоял в том, что пациенту по решению врача назначалась монотерапия пероральным АГП 2. В соответствии с рекомендациями ARIA лишь пациенты с легкими симптомами АР могли соответствовать этому критерию. Однако большинство пациентов в данном исследовании имели АР умеренной или тяжелой степени тяжести. Это наблюдение согласуется с результатами срезового опросного исследования, проведенного во Франции [34], и подтверждает тот факт, что в реальной клинической практике врачи назначают АГП как лечение первой линии, не учитывая тяжесть симптоматики АР. В целом 8–9 пациентов из 10 заявили, что они удовлетворены лечением пероральным АГП 2 и отметили достоверное улучшение КЖ во время лечения.
Итак, опыт применения АГП 2 при АР показал основные характеристики этой группы фармакологических средств, которые соответствуют предъявляемым требованиям: высокая клиническая эффективность в отношении симптомов интермиттирующего и персистирующего АР; способность подавлять глазные симптомы; эффективность у детей и пожилых лиц; отсутствие тахифилаксии при длительном применении; отсутствие нежелательных побочных эффектов; улучшение КЖ больных.
Одним из препаратов, наиболее полно удовлетворяющих этим требованиям, является цетиризин (например, оригинальный препарат Зиртек®). Препарат был создан в 1987 г. и стал первым оригинальным высокоизбирательным блокатором Н1-рецепторов на основе фармакологически активного метаболита ранее известного АГП 1-го поколения — гидроксизина. До настоящего времени цетиризин остается эталоном противогистаминного и противоаллергического действия, используется для сравнения при разработке новейших антигистаминных и противоаллергических средств. Препарат является селективным АГП 2, обладает высокой аффинностью к Н1-гистаминовым рецепторам. Цетиризин предупреждает развитие и облегчает течение аллергических реакций, оказывает противозудное и противовоспалительное действие, уменьшает заложенность носа. Важнейшей целью фармакотерапии АР является 24-часовой контроль симптомов заболевания при однократном суточном приеме. Цетиризин соответствует этому требованию: эффект продолжается более суток [35].
Применять цетиризин можно длительно, при необходимости в течение нескольких месяцев [36, 37]. Цетиризин обладает всеми положительными свойствами АГП 2, а кроме того, характеризуется некоторыми особенностями. По сравнению с некоторыми другими известными АГП 2 цетиризин имеет низкий объем распределения (0,5 л/кг), обеспечивая, таким образом, больший охват Н1-рецепторов и высокое противогистаминное действие [38]. Выраженная противогистаминная активность цетиризина также связана с его высоким сродством к Н1-рецепторам, которое значительно выше, чем у лоратадина и эбастина [39, 40].
В двойном слепом плацебо-контролируемом исследовании, проведенном в параллельных группах, цетиризин сравнивали с лоратадином и плацебо у больных с симптомами сезонного АР, которые были подвергнуты контролируемому воздействию аллергена — пыльцы полыннолистной амброзии в концентрации, встречающейся в природных условиях (средний уровень пыльцы амброзии 3480±350 частиц/м3). Исследование включало 2 периода воздействия (от 5,5 до 6,5 ч и более 2 дней), предпринятых до появления вызванных применением пыльцы симптомов АР (до 6 экспозиций). Пациенты получали 1 р./день 10 мг цетиризина (n=67), 10 мг лоратадина (n=67) или плацебо (n=68). Эффективность терапии оценивалась по шкалам общего комплекса симптомов (total symptom complex, TSC) и основного комплекса симптомов (major symptom complex, MSC). Симптомы оценивали каждые полчаса на протяжении всего исследования. В группе цетиризина было отмечено среднее снижение показателя TSC в целом на 36,7% в сравнении с 15,4% в группе лоратадина и 12,0% в группе плацебо (р<0,01). В группе цетиризина также зарегистрировано снижение показателя MSC в целом на 37,4% (на 14,7% в группе лоратадина и на 6,7% в группе плацебо, р<0,01). Начало действия препаратов регистрировалось по снижению показателей TSC и MSC в течение 1 ч для цетиризина (р<0,02) и в течение 3 ч для лоратадина (р<0,03). Побочные эффекты были схожи во всех группах, самым частым побочным эффектом явилась головная боль.
Таким образом, в исследовании продемонстрировано, что при контролируемом воздействии аллергена цетиризин высокоэффективен в контроле симптомов сезонного АР, обеспечивая более высокую клиническую эффективность, чем плацебо и лоратадин, и при этом хорошо переносится пациентами [41].
Интересным является метаанализ 13 различных исследований, целью которого являлась оценка сомнолентного эффекта цетиризина 10 мг/сут по сравнению с плацебо у пациентов в возрасте 6 лет и старше. Был проведен поиск в базах данных рандомизированных контролируемых исследований цетиризина, опубликованных до 2015 г. Метаанализ показал, что цетиризин в дозе 10 мг/день не оказывает сомнолентного эффекта по сравнению с плацебо [42].
Следуя алгоритму терапии АР в зависимости от тяжести симптомов, предложенному нами (рис. 3) [30], АГП 2 в качестве стартовой терапии следует назначать всем пациентам с легкими симптомами АР, а также тем пациентам со среднетяжелыми и тяжелыми симптомами, у которых заложенность носа не является ведущим симптомом.
![Рис. 3. Алгоритм терапии АР в зависимости от тяжести симптомов [30] Рис. 3. Алгоритм терапии АР в зависимости от тяжести симптомов [30]](/upload/medialibrary/bfe/45-4.png)












