–í–≤–Ķ–ī–Ķ–Ĺ–ł–Ķ
–ě–ī–Ĺ–ĺ–Ļ –ł–∑ —Ā–į–ľ—č—Ö —á–į—Ā—ā–ĺ –≤—Ā—ā—Ä–Ķ—á–į–Ķ–ľ—č—Ö —Ā–Ķ—Ä–ī–Ķ—á–Ĺ–ĺ-—Ā–ĺ—Ā—É–ī–ł—Ā—ā—č—Ö –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–Ļ –≤ –Ņ–ĺ–Ņ—É–Ľ—Ź—Ü–ł–ł —Ź–≤–Ľ—Ź—é—ā—Ā—Ź —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ķ –ĺ–Ī–Ľ–ł—ā–Ķ—Ä–ł—Ä—É—é—Č–ł–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –į—Ä—ā–Ķ—Ä–ł–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ, –≤—č–∑—č–≤–į—é—Č–ł–Ķ —Ä–į–∑–≤–ł—ā–ł–Ķ —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ł—ą–Ķ–ľ–ł–ł.–ó–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –Ņ–Ķ—Ä–ł—Ą–Ķ—Ä–ł—á–Ķ—Ā–ļ–ł—Ö –į—Ä—ā–Ķ—Ä–ł–Ļ —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź—é—ā 3‚Äď4% –ĺ—ā —á–ł—Ā–Ľ–į –≤—Ā–Ķ—Ö —Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ł—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ. –†–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć –Ņ–Ķ—Ä–Ķ–ľ–Ķ–∂–į—é—Č–Ķ–Ļ—Ā—Ź —Ö—Ä–ĺ–ľ–ĺ—ā—č –≤ –∑–į–≤–ł—Ā–ł–ľ–ĺ—Ā—ā–ł –ĺ—ā –≤–ĺ–∑—Ä–į—Ā—ā–į –≤–į—Ä—Ć–ł—Ä—É–Ķ—ā—Ā—Ź –ĺ—ā 0,9 –ī–ĺ 7,0% —Ā —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ–ľ –≤ —Ā—ā–į—Ä—ą–ł—Ö –≤–ĺ–∑—Ä–į—Ā—ā–Ĺ—č—Ö –≥—Ä—É–Ņ–Ņ–į—Ö (1‚Äď5% —É –Ľ–ł—Ü –ľ–ĺ–Ľ–ĺ–∂–Ķ 50 –Ľ–Ķ—ā, 10‚Äď14% ‚ÄĒ —Ā—Ä–Ķ–ī–ł –Ľ—é–ī–Ķ–Ļ 50‚Äď70 –Ľ–Ķ—ā) [1]. –•–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –ľ–Ķ—ā–ĺ–ī—č –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –ĺ–Ī–Ľ–ł—ā–Ķ—Ä–ł—Ä—É—é—Č–ł—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ –į—Ä—ā–Ķ—Ä–ł–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–į—é—ā —Ā—ā—Ä–Ķ–ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ —Ä–į–∑–≤–ł–≤–į—ā—Ć—Ā—Ź, –Ņ–ĺ—Ā—ā–ĺ—Ź–Ĺ–Ĺ–ĺ —É–≤–Ķ–Ľ–ł—á–ł–≤–į–Ķ—ā—Ā—Ź –ī–ĺ–Ľ—Ź —Ä–Ķ–Ĺ—ā–≥–Ķ–Ĺ—ć–Ĺ–ī–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č—Ö –≤–ľ–Ķ—ą–į—ā–Ķ–Ľ—Ć—Ā—ā–≤. –ď–ĺ–≤–ĺ—Ä—Ź –∂–Ķ –ĺ –ļ–ĺ–Ĺ—Ā–Ķ—Ä–≤–į—ā–ł–≤–Ĺ–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł, –ī–ĺ—Ā—ā–ĺ–≤–Ķ—Ä–Ĺ—č—Ö –≤—č–≤–ĺ–ī–ĺ–≤ –ĺ –Ņ–ĺ–Ľ—Ć–∑–Ķ —ā–Ķ—Ö –ł–Ľ–ł –ł–Ĺ—č—Ö —Ą–į—Ä–ľ–į–ļ–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł—Ö –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ —Ā–ī–Ķ–Ľ–į—ā—Ć –Ĺ–Ķ–Ľ—Ć–∑—Ź. –ě—á–Ķ–≤–ł–ī–Ĺ—č–ľ–ł —Ā—ā–ĺ–Ľ–Ņ–į–ľ–ł –ļ–ĺ–Ĺ—Ā–Ķ—Ä–≤–į—ā–ł–≤–Ĺ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ĺ—Ā—ā–į—é—ā—Ā—Ź –Ľ–Ķ—á–Ķ–Ī–Ĺ–į—Ź —Ą–ł–∑–ł—á–Ķ—Ā–ļ–į—Ź –ļ—É–Ľ—Ć—ā—É—Ä–į –ł –ļ–ĺ—Ä—Ä–Ķ–ļ—ā–ł—Ä–ĺ–≤–ļ–į —Ą–į–ļ—ā–ĺ—Ä–ĺ–≤ —Ä–ł—Ā–ļ–į, –Ĺ–ĺ —á—ā–ĺ –ļ–į—Ā–į–Ķ—ā—Ā—Ź –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤, —á—Ć–Ķ –ī–Ķ–Ļ—Ā—ā–≤–ł–Ķ –Ĺ–į–Ņ—Ä–į–≤–Ľ–Ķ–Ĺ–ĺ –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –Ĺ–į –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ņ–Ķ—Ä–Ķ–ľ–Ķ–∂–į—é—Č–Ķ–Ļ—Ā—Ź —Ö—Ä–ĺ–ľ–ĺ—ā—č, —ā–ĺ –ł–ľ–Ķ—é—Č–ł–Ķ—Ā—Ź –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ĺ–Ķ —Ā–≤–ł–ī–Ķ—ā–Ķ–Ľ—Ć—Ā—ā–≤—É—é—ā –ĺ –Ņ–ĺ–Ľ—Ć–∑–Ķ –ļ–į–ļ–ĺ–≥–ĺ-–Ľ–ł–Ī–ĺ –ł–∑ –Ĺ–ł—Ö [2]. –ď–Ľ–į–≤–Ĺ–į—Ź –Ņ—Ä–ł—á–ł–Ĺ–į —ć—ā–ĺ–≥–ĺ ‚ÄĒ –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ļ—Ä–ł—ā–Ķ—Ä–ł–Ķ–≤, –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–ł –ļ–ĺ—ā–ĺ—Ä—č—Ö –ľ–ĺ–∂–Ĺ–ĺ –Ī—č–Ľ–ĺ –Ī—č —Ā—Ä–į–≤–Ĺ–ł–≤–į—ā—Ć —Ā—É—Č–Ķ—Ā—ā–≤—É—é—Č–ł–Ķ —Ā—Ö–Ķ–ľ—č –ļ–ĺ–Ĺ—Ā–Ķ—Ä–≤–į—ā–ł–≤–Ĺ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź. –ü—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ł—Ā—Ć –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł –ľ–ĺ—Ä—Ą–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –≤ —Ā—ā—Ä—É–ļ—ā—É—Ä–Ķ –ľ—č—ą—Ü –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł, –ĺ–ī–Ĺ–į–ļ–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ä–į–∑–Ľ–ł—á–ł–Ļ –ľ–Ķ–∂–ī—É –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–ĺ–Ļ –ł –≥—Ä—É–Ņ–Ņ–ĺ–Ļ –ļ–ĺ–Ĺ—Ā–Ķ—Ä–≤–į—ā–ł–≤–Ĺ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ–ĺ –Ĺ–Ķ –Ī—č–Ľ–ĺ [3]. –Ę–į–ļ–∂–Ķ —Ā—É—Č–Ķ—Ā—ā–≤—É—é—ā –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł —Ą—É–Ĺ–ļ—Ü–ł–ł –Ĺ–Ķ—Ä–≤–ĺ–≤ [4], –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –≤ –ľ–Ķ—ā–į–Ī–ĺ–Ľ–ł–∑–ľ–Ķ –ź–Ē–§, —Ą–ĺ—Ā—Ą–ĺ–ļ—Ä–Ķ–į—ā–ł–Ĺ–ł–Ĺ–į [5] –≤ –Ī–ł–ĺ–Ņ—ā–į—ā–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł, –Ĺ–ĺ –ł –Ņ—Ä–ł –ĺ—Ü–Ķ–Ĺ–ļ–Ķ —ć—ā–ł—Ö —Ą–į–ļ—ā–ĺ—Ä–ĺ–≤ –Ĺ–Ķ –Ī—č–Ľ–ĺ –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ–ĺ –ļ–į–ļ–ł—Ö-–Ľ–ł–Ī–ĺ –∑–Ĺ–į—á–ł–ľ—č—Ö —Ä–į–∑–Ľ–ł—á–ł–Ļ –ľ–Ķ–∂–ī—É –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –ł –ł—Ā—Ā–Ľ–Ķ–ī—É–Ķ–ľ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–į–ľ–ł.
–Ē–Ķ–Ļ—Ā—ā–≤–ł–Ķ –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–į –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ī–Ľ—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ņ–Ķ—Ä–Ķ–ľ–Ķ–∂–į—é—Č–Ķ–Ļ—Ā—Ź —Ö—Ä–ĺ–ľ–ĺ—ā—č, –ł—Ā–Ņ–ĺ–Ľ—Ć–∑—É–Ķ–ľ—č—Ö –≤ –į–ļ—ā—É–į–Ľ—Ć–Ĺ—č—Ö —Ā—Ö–Ķ–ľ–į—Ö, –Ĺ–į–Ņ—Ä–į–≤–Ľ–Ķ–Ĺ–ĺ –Ĺ–į –ļ–ĺ—Ä—Ä–Ķ–ļ—ā–ł—Ä–ĺ–≤–ļ—É —Ā–ł–ľ–Ņ—ā–ĺ–ľ–ĺ–≤, –Ĺ–Ķ –Ĺ–į —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł—é –ł –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ķ–∑ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź. –ě–ī–Ĺ–ł–ľ –ł–∑ –Ĺ–Ķ–ľ–Ĺ–ĺ–≥–ł—Ö –ľ–Ķ—ā–ĺ–ī–ĺ–≤, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –ĺ–ļ–į–∑—č–≤–į—é—ā –≤–Ľ–ł—Ź–Ĺ–ł–Ķ –Ĺ–į –Ņ–į—ā–ĺ–≥–Ķ–Ĺ–Ķ–∑ —Ä–į–∑–≤–ł—ā–ł—Ź —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ł—ą–Ķ–ľ–ł–ł –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ, —Ź–≤–Ľ—Ź—é—ā—Ā—Ź –≥–Ķ–Ĺ–Ĺ–ĺ-—ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ł–Ķ —ā–Ķ—Ö–Ĺ–ĺ–Ľ–ĺ–≥–ł–ł. –°—ā–ł–ľ—É–Ľ—Ź—Ü–ł—é –į–Ĺ–≥–ł–ĺ–≥–Ķ–Ĺ–Ķ–∑–į –Ĺ–į –≥–Ķ–Ĺ–Ķ—ā–ł—á–Ķ—Ā–ļ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ –ľ–ĺ–∂–Ĺ–ĺ —Ā—á–ł—ā–į—ā—Ć –Ņ–Ķ—Ä—Ā–Ņ–Ķ–ļ—ā–ł–≤–Ĺ—č–ľ –Ĺ–į–Ņ—Ä–į–≤–Ľ–Ķ–Ĺ–ł–Ķ–ľ —Ä–į–∑–≤–ł—ā–ł—Ź —ā–Ķ—Ä–į–Ņ–ł–ł –Ĺ–Ķ–ļ–ĺ—ā–ĺ—Ä—č—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ, –≤ —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł –Ņ–Ķ—Ä–Ķ–ľ–Ķ–∂–į—é—Č–Ķ–Ļ—Ā—Ź —Ö—Ä–ĺ–ľ–ĺ—ā—č. –ö –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–ľ—É –ľ–ĺ–ľ–Ķ–Ĺ—ā—É —Ā—É—Č–Ķ—Ā—ā–≤—É—é—ā –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł—Ź —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö —Ą–į–ļ—ā–ĺ—Ä–ĺ–≤ —Ä–ĺ—Ā—ā–į –ī–Ľ—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź:
—Ą–į–ļ—ā–ĺ—Ä —Ä–ĺ—Ā—ā–į —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź (VEGF, –ł–∑–ĺ—Ą–ĺ—Ä–ľ—č: VEGF-A –ī–ĺ -E) [6, 7];
—Ą–į–ļ—ā–ĺ—Ä—č —Ä–ĺ—Ā—ā–į –Ņ–Ľ–į—Ü–Ķ–Ĺ—ā—č (PLGF, –ł–∑–ĺ—Ą–ĺ—Ä–ľ—č: PLGF-1 –ł -2);
—Ą–į–ļ—ā–ĺ—Ä—č —Ä–ĺ—Ā—ā–į —Ą–ł–Ī—Ä–ĺ–Ī–Ľ–į—Ā—ā–ĺ–≤ (FGF, –ł–∑–ĺ—Ą–ĺ—Ä–ľ—č:
23 –ĺ—ā FGF-1 –ī–ĺ FGF-23) [8];
—Ą–į–ļ—ā–ĺ—Ä—č —Ä–ĺ—Ā—ā–į –≥–Ķ–Ņ–į—ā–ĺ—Ü–ł—ā–ĺ–≤ (HGF, –ł–∑–ĺ—Ą–ĺ—Ä–ľ—č HGF/NK1 –ł HGF/NK2) [9];
—Ą–į–ļ—ā–ĺ—Ä—č —Ä–ĺ—Ā—ā–į, –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ–Ĺ—č–Ķ –ł–∑ —ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–ĺ–≤ (PDGF, –ł–∑–ĺ—Ą–ĺ—Ä–ľ—č: PDGF-AA, -AB, -BB, -CC –ł -DD);
–į–Ĺ–≥–ł–ĺ–Ņ—Ä–ĺ—ā–Ķ–ł–Ĺ (Ang, –ł–∑–ĺ—Ą–ĺ—Ä–ľ—č: Ang-1, -2, -3, –ł -4);
—ć—Ä–ł—ā—Ä–ĺ–Ņ–ĺ—ć—ā–ł–Ĺ (EPO).
–ü—Ä–ł –ł—ą–Ķ–ľ–ł–ł –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–Ķ –≥–Ķ–Ĺ–į VEGF 165 –Ľ–ł–ī–ł—Ä—É—é—ā –ļ–į–ļ –Ņ–ĺ –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā–ł, —ā–į–ļ –ł –Ņ–ĺ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł, –Ņ–ĺ—Ā–ļ–ĺ–Ľ—Ć–ļ—É —ć—ā–į –ł–∑–ĺ—Ą–ĺ—Ä–ľ–į VEGF-–ź, —Ā–ĺ—Ā—ā–ĺ—Ź—Č–į—Ź –ł–∑ 165 –į–ľ–ł–Ĺ–ĺ–ļ–ł—Ā–Ľ–ĺ—ā, –ĺ–Ī–Ľ–į–ī–į–Ķ—ā –Ĺ–į–ł–Ī–ĺ–Ľ—Ć—ą–ł–ľ –ľ–ł—ā–ĺ—ā–ł—á–Ķ—Ā–ļ–ł–ľ —ć—Ą—Ą–Ķ–ļ—ā–ĺ–ľ –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é —Ā –ĺ—Ā—ā–į–Ľ—Ć–Ĺ—č–ľ–ł –ł–∑–ĺ—Ą–ĺ—Ä–ľ–į–ľ–ł. –Ě–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ–Ļ —Ā—ā—Ä–į—ā–Ķ–≥–ł–Ķ–Ļ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–į –Ĺ—É–∂–Ĺ–ĺ–≥–ĺ –≥–Ķ–Ĺ–į –≤ –ļ–Ľ–Ķ—ā–ļ–ł-–ľ–ł—ą–Ķ–Ĺ–ł —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ –Ĺ–Ķ–≤–ł—Ä—É—Ā–Ĺ—č—Ö —Ā–ł—Ā—ā–Ķ–ľ, –≤ —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł –Ņ–Ľ–į–∑–ľ–ł–ī. –ü–Ľ–į–∑–ľ–ł–ī—č ‚ÄĒ —ć–ļ—Ā—ā—Ä–į—Ö—Ä–ĺ–ľ–ĺ—Ā–ĺ–ľ–Ĺ—č–Ķ –ļ–ĺ–Ľ—Ć—Ü–Ķ–≤—č–Ķ –ī–≤—É—Ü–Ķ–Ņ–ĺ—á–Ķ—á–Ĺ—č–Ķ –ľ–ĺ–Ľ–Ķ–ļ—É–Ľ—č –Ē–Ě–ö, –ĺ–Ī–Ĺ–į—Ä—É–∂–ł–≤–į–Ķ–ľ—č–Ķ –≤ –ļ–Ľ–Ķ—ā–ļ–į—Ö –Ī–į–ļ—ā–Ķ—Ä–ł–Ļ –ł –ī–į–≤–Ĺ–ĺ —Ā—ā–į–≤—ą–ł–Ķ –ĺ–ī–Ĺ–ł–ľ –ł–∑ —Ā–į–ľ—č—Ö —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ—č—Ö –ł–Ĺ—Ā—ā—Ä—É–ľ–Ķ–Ĺ—ā–ĺ–≤ –≥–Ķ–Ĺ–Ĺ–ĺ–Ļ –ł–Ĺ–∂–Ķ–Ĺ–Ķ—Ä–ł–ł. –ü—Ä–ł –Ľ—é–Ī–ĺ–ľ —Ā–Ņ–ĺ—Ā–ĺ–Ī–Ķ –≤–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –ĺ—ā–ľ–Ķ—á–į–Ķ—ā—Ā—Ź —ć–ļ—Ā–Ņ—Ä–Ķ—Ā—Ā–ł—Ź —ā—Ä–į–Ĺ—Ā–≥–Ķ–Ĺ–į –≤ –ľ—č—ą–Ķ—á–Ĺ—č—Ö –≤–ĺ–Ľ–ĺ–ļ–Ĺ–į—Ö –ł—ą–Ķ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ —ā–ļ–į–Ĺ–ł, –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–Ķ –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–ł–Ķ –ļ–ĺ–Ĺ—Ü–Ķ–Ĺ—ā—Ä–į—Ü–ł–ł –Ņ—Ä–ĺ–ī—É—Ü–ł—Ä—É–Ķ–ľ–ĺ–≥–ĺ –Ī–Ķ–Ľ–ļ–į, –≤ —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł VEGF, –ł —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ –Ņ–Ķ—Ä—Ą—É–∑–ł–ł —ā–ļ–į–Ĺ–Ķ–Ļ –∑–į —Ā—á–Ķ—ā —Ä–į–∑–≤–ł—ā–ł—Ź –Ĺ–ĺ–≤—č—Ö –ļ–į–Ņ–ł–Ľ–Ľ—Ź—Ä–ĺ–≤.
–ü–Ķ—Ä–≤—č–ľ –∑–į—Ä–Ķ–≥–ł—Ā—ā—Ä–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–ľ –≤ –†–§ –≥–Ķ–Ĺ–Ĺ–ĺ-—ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ł–ľ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–ľ –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–Ķ –Ņ–Ľ–į–∑–ľ–ł–ī—č —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ě–Ķ–ĺ–≤–į—Ā–ļ—É–Ľ–≥–Ķ–Ĺ (–†–£ ‚ĄĖ –õ–ü-000671 –ĺ—ā 28.09.2011). –ě–Ĺ –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ—Ź–Ķ—ā —Ā–ĺ–Ī–ĺ–Ļ –≤—č—Ā–ĺ–ļ–ĺ–ĺ—á–ł—Č–Ķ–Ĺ–Ĺ—É—é —Ā–≤–Ķ—Ä—Ö—Ā–ļ—Ä—É—á–Ķ–Ĺ–Ĺ—É—é —Ą–ĺ—Ä–ľ—É –Ņ–Ľ–į–∑–ľ–ł–ī—č pCMV‚ÄďVEGF165, –ļ–ĺ–ī–ł—Ä—É—é—Č—É—é —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł–į–Ľ—Ć–Ĺ—č–Ļ —Ą–į–ļ—ā–ĺ—Ä —Ä–ĺ—Ā—ā–į —Ā–ĺ—Ā—É–ī–ĺ–≤ (VEGF ‚ÄĒ vascular endothelial growth factor) –Ņ–ĺ–ī –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–Ķ–ľ –Ņ—Ä–ĺ–ľ–ĺ—ā–ĺ—Ä–į (—É–Ņ—Ä–į–≤–Ľ—Ź—é—Č–Ķ–≥–ĺ —É—á–į—Ā—ā–ļ–į –Ē–Ě–ö). –ü—Ä–Ķ–Ņ–į—Ä–į—ā —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī—É–Ķ—ā—Ā—Ź –≤–≤–ĺ–ī–ł—ā—Ć –≤–Ĺ—É—ā—Ä–ł–ľ—č—ą–Ķ—á–Ĺ–ĺ –≤ —Ā—Ä–Ķ–ī–Ĺ—é—é –ł–Ľ–ł –Ĺ–ł–∂–Ĺ—é—é —ā—Ä–Ķ—ā—Ć –∑–į–ī–Ĺ–Ķ–Ļ –Ņ–ĺ–≤–Ķ—Ä—Ö–Ĺ–ĺ—Ā—ā–ł –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č [6]. –ė–ľ–Ķ—é—ā—Ā—Ź –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –≥–ĺ–≤–ĺ—Ä—Ź—ā –ĺ –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–ľ –≤–Ľ–ł—Ź–Ĺ–ł–ł –ī–į–Ĺ–Ĺ–ĺ–≥–ĺ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –Ĺ–į —Ā—É–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č–Ķ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł –ĺ—Ü–Ķ–Ĺ–ļ–ł, —ā–į–ļ–ł–Ķ –ļ–į–ļ –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ –Ņ—Ä–ĺ—Ö–ĺ–ī–ł–ľ–į—Ź –ī–ł—Ā—ā–į–Ĺ—Ü–ł—Ź [6] –≤ –Ī–Ľ–ł–∂–į–Ļ—ą–Ķ–ľ (3 –ľ–Ķ—Ā.) –ł –ĺ—ā–ī–į–Ľ–Ķ–Ĺ–Ĺ–ĺ–ľ –Ņ–Ķ—Ä–ł–ĺ–ī–Ķ (–ī–ĺ 5 –Ľ–Ķ—ā) [10].
–¶–Ķ–Ľ—Ć—é –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–Ļ —Ä–į–Ī–ĺ—ā—č —Ź–≤–ł–Ľ–į—Ā—Ć –ĺ—Ü–Ķ–Ĺ–ļ–į —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ļ–ĺ–Ĺ—Ā–Ķ—Ä–≤–į—ā–ł–≤–Ĺ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ł—ą–Ķ–ľ–ł–Ķ–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ (–•–ė–Ě–ö) —Ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ–ľ –≥–Ķ–Ĺ–Ĺ–ĺ-–ł–Ĺ–∂–Ķ–Ĺ–Ķ—Ä–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł (–Ņ—Ä–Ķ–Ņ–į—Ä–į—ā –Ě–Ķ–ĺ–≤–į—Ā–ļ—É–Ľ–≥–Ķ–Ĺ) –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–ł –ļ–ĺ–ľ–Ņ–Ľ–Ķ–ļ—Ā–į –ļ–į–ļ —Ā—É–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö, —ā–į–ļ –ł –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ļ—Ä–ł—ā–Ķ—Ä–ł–Ķ–≤. –ė–∑ –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö –ļ—Ä–ł—ā–Ķ—Ä–ł–Ķ–≤ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ–ł—Ā—Ć –≥–ł—Ā—ā–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ (–ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ BNIP3 ‚ÄĒ BCL2/adenovirus E1B 19 kDa protein-interacting protein 3, –Ņ—Ä–ĺ–į–Ņ–ĺ–Ņ—ā–ĺ–∑–Ĺ—č–Ļ –Ī–Ķ–Ľ–ĺ–ļ —Ā–Ķ–ľ–Ķ–Ļ—Ā—ā–≤–į B-–ļ–Ľ–Ķ—ā–ĺ—á–Ĺ—č—Ö –Ľ–ł–ľ—Ą–ĺ–ľ 2 (BCL2) –≤ –Ī–ł–ĺ–Ņ—ā–į—ā–Ķ –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł) –ł –Ī–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ (–ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ —Ą–į–ļ—ā–ĺ—Ä–į —Ä–ĺ—Ā—ā–į —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź (VEGF-–ź) –≤ –Ņ–Ķ—Ä–ł—Ą–Ķ—Ä–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ļ—Ä–ĺ–≤–ł, –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –ĺ—ā—ā–Ķ–ļ–į—é—Č–Ķ–Ļ –ĺ—ā –ł—ą–Ķ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –ľ—č—ą—Ü).
–§–į–ļ—ā–ĺ—Ä —Ä–ĺ—Ā—ā–į —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź VEGF-–ź –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ—Ź–Ķ—ā —Ā–ĺ–Ī–ĺ–Ļ —Ā–ł–≥–Ĺ–į–Ľ—Ć–Ĺ—č–Ļ –Ī–Ķ–Ľ–ĺ–ļ, –≤—č—Ä–į–Ī–į—ā—č–≤–į–Ķ–ľ—č–Ļ –ļ–Ľ–Ķ—ā–ļ–į–ľ–ł –ī–Ľ—Ź —Ā—ā–ł–ľ—É–Ľ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –≤–į—Ā–ļ—É–Ľ–ĺ–≥–Ķ–Ĺ–Ķ–∑–į (–ĺ–Ī—Ä–į–∑–ĺ–≤–į–Ĺ–ł–Ķ —ć–ľ–Ī—Ä–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ —Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č) –ł –į–Ĺ–≥–ł–ĺ–≥–Ķ–Ĺ–Ķ–∑–į (—Ä–ĺ—Ā—ā –Ĺ–ĺ–≤—č—Ö —Ā–ĺ—Ā—É–ī–ĺ–≤ –≤ —É–∂–Ķ —Ā—É—Č–Ķ—Ā—ā–≤—É—é—Č–Ķ–Ļ —Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ–Ķ).
–ě–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ –ľ–į—Ä–ļ–Ķ—Ä–ĺ–≤ –į–Ņ–ĺ–Ņ—ā–ĺ–∑–į (BNIP3) –≤ –Ī–ł–ĺ–Ņ—ā–į—ā–Ķ –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ķ—ā –ĺ—Ü–Ķ–Ĺ–ł—ā—Ć –ľ–ĺ—Ä—Ą–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –ł –≥–ł—Ā—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –≤ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł. –í—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć –į–Ņ–ĺ–Ņ—ā–ĺ–∑–į –ł—Ā–Ņ–ĺ–Ľ—Ć–∑—É—é—ā –ī–Ľ—Ź –ĺ—Ü–Ķ–Ĺ–ļ–ł —É—Ä–ĺ–≤–Ĺ—Ź –ł—ą–Ķ–ľ–ł–ł –ĺ—Ä–≥–į–Ĺ–ĺ–≤: —ā–į–ļ, –Ĺ–į–Ņ—Ä–ł–ľ–Ķ—Ä, —Ā—É—Č–Ķ—Ā—ā–≤—É—é—ā –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź, —á–Ķ—ā–ļ–ĺ —É–ļ–į–∑—č–≤–į—é—Č–ł–Ķ, —á—ā–ĺ –į–Ņ–ĺ–Ņ—ā–ĺ–∑ –ļ–į—Ä–ī–ł–ĺ–ľ–ł–ĺ—Ü–ł—ā–ĺ–≤ –ł–≥—Ä–į–Ķ—ā –Ĺ–į–ł–≤–į–∂–Ĺ–Ķ–Ļ—ą—É—é —Ä–ĺ–Ľ—Ć –≤ –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł–ł –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ī–ĺ–Ľ–Ķ–∑–Ĺ–ł —Ā–Ķ—Ä–ī—Ü–į –ł –ĺ—Ā—ā—Ä–ĺ–≥–ĺ –ł–Ĺ—Ą–į—Ä–ļ—ā–į –ľ–ł–ĺ–ļ–į—Ä–ī–į [11].
–í –Ĺ–į—ą–Ķ–Ļ —Ä–į–Ĺ–Ķ–Ķ –ĺ–Ņ—É–Ī–Ľ–ł–ļ–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ —Ä–į–Ī–ĺ—ā–Ķ –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ—č –ī–į–Ĺ–Ĺ—č–Ķ, —É–ļ–į–∑—č–≤–į—é—Č–ł–Ķ –Ĺ–į –Ņ—Ä—Ź–ľ—É—é –∑–į–≤–ł—Ā–ł–ľ–ĺ—Ā—ā—Ć –ľ–Ķ–∂–ī—É —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć—é –ł—ą–Ķ–ľ–ł–ł –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł –ł —ć–ļ—Ā–Ņ—Ä–Ķ—Ā—Ā–ł–Ķ–Ļ BNIP3 —Ā –ī–ĺ—Ā—ā–ł–∂–Ķ–Ĺ–ł–Ķ–ľ –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ—č—Ö –∑–Ĺ–į—á–Ķ–Ĺ–ł–Ļ –Ĺ–į II–Ď —Ā—ā–į–ī–ł–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –Ņ–ĺ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–ł –ü–ĺ–ļ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ ‚ÄĒ –§–ĺ–Ĺ—ā–Ķ–Ļ–Ĺ–į, –ļ–ĺ–≥–ī–į –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ –į–ļ—ā–ł–≤–ł–∑–ł—Ä—É–Ķ—ā—Ā—Ź –Ņ—Ä–ĺ–≥—Ä–į–ľ–ľ–ł—Ä—É–Ķ–ľ–į—Ź —Ā–ľ–Ķ—Ä—ā—Ć –ļ–Ľ–Ķ—ā–ļ–ł [12].
–ú–į—ā–Ķ—Ä–ł–į–Ľ –ł –ľ–Ķ—ā–ĺ–ī—č
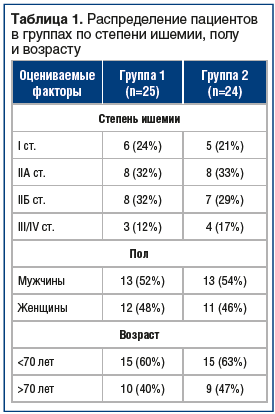
–í –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ī—č–Ľ–ł –≤–ļ–Ľ—é—á–Ķ–Ĺ—č 49 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —Ä–į–∑–Ľ–ł—á–Ĺ—č–ľ–ł —Ā—ā–į–ī–ł—Ź–ľ–ł –•–ė–Ě–ö –≤ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–ł–ł —Ā –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–Ķ–Ļ –ü–ĺ–ļ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ ‚ÄĒ –§–ĺ–Ĺ—ā–Ķ–Ļ–Ĺ–į. –ü–į—Ü–ł–Ķ–Ĺ—ā—č –Ī—č–Ľ–ł —Ä–į–∑–ī–Ķ–Ľ–Ķ–Ĺ—č –Ĺ–į 2 –≥—Ä—É–Ņ–Ņ—č, –≤ –ļ–į–∂–ī–ĺ–Ļ –ł–∑ –≥—Ä—É–Ņ–Ņ –Ī—č–Ľ–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā I, II, III –ł IV —Ā—ā–į–ī–ł—Ź–ľ–ł –ł—ą–Ķ–ľ–ł–ł (—ā–į–Ī–Ľ. 1). –Ě–Ķ—Ā–ľ–ĺ—ā—Ä—Ź –Ĺ–į —ā–ĺ, —á—ā–ĺ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–Ļ —Ü–Ķ–Ľ–Ķ–≤–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–ĺ–Ļ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –≥–Ķ–Ĺ–Ĺ–ĺ-—ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ł–ľ–ł –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į–ľ–ł —Ź–≤–Ľ—Ź—é—ā—Ā—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā –Ņ–Ķ—Ä–Ķ–ľ–Ķ–∂–į—é—Č–Ķ–Ļ—Ā—Ź —Ö—Ä–ĺ–ľ–ĺ—ā–ĺ–Ļ, —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É—é—Č–Ķ–Ļ II —Ā—ā–į–ī–ł–ł –ł—ą–Ķ–ľ–ł–ł –Ņ–ĺ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–ł –ü–ĺ–ļ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ ‚ÄĒ –§–ĺ–Ĺ—ā–Ķ–Ļ–Ĺ–į, –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ —ā–į–ļ–∂–Ķ –≤–ļ–Ľ—é—á–į–Ľ–ł—Ā—Ć –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā –Ĺ–į—á–į–Ľ—Ć–Ĺ—č–ľ–ł –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź–ľ–ł –ł —Ā –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ł—ą–Ķ–ľ–ł–Ķ–Ļ. –ü–į—Ü–ł–Ķ–Ĺ—ā—č —Ā I —Ā—ā–į–ī–ł–Ķ–Ļ –ł—ą–Ķ–ľ–ł–ł –Ĺ–Ķ —ā—Ä–Ķ–Ī—É—é—ā —Ā–Ņ–Ķ—Ü–ł—Ą–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ—Ā—ā–ł, –Ĺ–ĺ –ł—Ö –≤–ļ–Ľ—é—á–Ķ–Ĺ–ł–Ķ –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ī—č–Ľ–ĺ –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ –ī–Ľ—Ź –ĺ—Ü–Ķ–Ĺ–ļ–ł —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–ł –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ, –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī—Ź—Č–ł—Ö –≤ –ł—ą–Ķ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö —ā–ļ–į–Ĺ—Ź—Ö –Ĺ–į –≥–ł—Ā—ā–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ –Ĺ–į –ļ–į–∂–ī–ĺ–ľ –ł–∑ —ć—ā–į–Ņ–ĺ–≤ —Ä–į–∑–≤–ł—ā–ł—Ź –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–≥–ĺ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź. –ü–ĺ —ć—ā–ĺ–Ļ –∂–Ķ –Ņ—Ä–ł—á–ł–Ĺ–Ķ –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł –Ņ—Ä–ł–Ĺ–ł–ľ–į–Ľ–ł —É—á–į—Ā—ā–ł–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā –ł—ą–Ķ–ľ–ł–Ķ–Ļ, —É–≥—Ä–ĺ–∂–į—é—Č–Ķ–Ļ –∂–ł–∑–Ĺ–Ķ—Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā–ł –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł, —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É—é—Č–Ķ–Ļ III –ł IV —Ā—ā–į–ī–ł—Ź–ľ–ł –ł—ą–Ķ–ľ–ł–ł –Ņ–ĺ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–ł –ü–ĺ–ļ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ ‚ÄĒ –§–ĺ–Ĺ—ā–Ķ–Ļ–Ĺ–į. –ď—Ä—É–Ņ–Ņ–į 1 –Ņ–ĺ–Ľ—É—á–į–Ľ–į —ā–Ķ—Ä–į–Ņ–ł—é –≤ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–ł–ł —Ā –Ě–į—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–ľ–ł —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł—Ź–ľ–ł –Ņ–ĺ –≤–Ķ–ī–Ķ–Ĺ–ł—é –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź–ľ–ł –į—Ä—ā–Ķ—Ä–ł–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ, –ļ–ĺ—ā–ĺ—Ä–į—Ź –≤–ļ–Ľ—é—á–į–Ľ–į: –į–Ĺ—ā–ł—ā—Ä–ĺ–ľ–Ī–ĺ—Ü–ł—ā–į—Ä–Ĺ—É—é (–į—Ü–Ķ—ā–ł–Ľ—Ā–į–Ľ–ł—Ü–ł–Ľ–ĺ–≤–į—Ź –ļ–ł—Ā–Ľ–ĺ—ā–į 100 –ľ–≥), –Ľ–ł–Ņ–ł–ī–ĺ—Ā–Ĺ–ł–∂–į—é—Č—É—é (–į—ā–ĺ—Ä–≤–į—Ā—ā–į—ā–ł–Ĺ 10 –ľ–≥), –≥–ł–Ņ–ĺ—ā–Ķ–Ĺ–∑–ł–≤–Ĺ—É—é (–Ī–ł—Ā–ĺ–Ņ—Ä–ĺ–Ľ–ĺ–Ľ 2,5 –ľ–≥) —ā–Ķ—Ä–į–Ņ–ł—é. –Ę–Ķ—Ä–į–Ņ–ł—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≥—Ä—É–Ņ–Ņ—č 2 –Ī—č–Ľ–į –ī–ĺ–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ–į –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–ľ –Ě–Ķ–ĺ–≤–į—Ā–ļ—É–Ľ–≥–Ķ–Ĺ, –ļ–ĺ—ā–ĺ—Ä—č–Ļ –≤–≤–ĺ–ī–ł–Ľ—Ā—Ź –≤–Ĺ—É—ā—Ä–ł–ľ—č—ą–Ķ—á–Ĺ–ĺ –≤ –ł—ą–Ķ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—É—é –∑–ĺ–Ĺ—É –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č –ī–≤—É–ļ—Ä–į—ā–Ĺ–ĺ –Ņ–ĺ 1,2 –ľ–≥ —Ā –ł–Ĺ—ā–Ķ—Ä–≤–į–Ľ–ĺ–ľ –≤ 14 –ī–Ĺ–Ķ–Ļ. –ď—Ä—É–Ņ–Ņ—č –Ī—č–Ľ–ł —Ā–ĺ–Ņ–ĺ—Ā—ā–į–≤–ł–ľ—č –Ņ–ĺ –Ņ–ĺ–Ľ—É, –≤–ĺ–∑—Ä–į—Ā—ā—É, —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–Ķ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–ł –ł —É—Ä–ĺ–≤–Ĺ—é –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł—Ź —Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–≥–ĺ —Ä—É—Ā–Ľ–į (—Ā–ľ. —ā–į–Ī–Ľ. 1).
–ü–Ķ—Ä–ł–ĺ–ī –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź –∑–į –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ–ł —Ā–ĺ—Ā—ā–į–≤–ł–Ľ 6 –ľ–Ķ—Ā. –ü–Ķ—Ä–Ķ–ī –Ĺ–į—á–į–Ľ–ĺ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ –≤—č–Ņ–ĺ–Ľ–Ĺ—Ź–Ľ–ł—Ā—Ć –ļ–į–ļ –Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č–Ķ (–ĺ–Ī—Č–ł–Ļ –į–Ĺ–į–Ľ–ł–∑ –ļ—Ä–ĺ–≤–ł, –Ī–ł–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ł–Ļ –į–Ĺ–į–Ľ–ł–∑ –ļ—Ä–ĺ–≤–ł, –ļ–ĺ–į–≥—É–Ľ–ĺ–≥—Ä–į–ľ–ľ–į, –ĺ–Ī—Č–ł–Ļ –į–Ĺ–į–Ľ–ł–∑ –ľ–ĺ—á–ł), —ā–į–ļ –ł –ł–Ĺ—Ā—ā—Ä—É–ľ–Ķ–Ĺ—ā–į–Ľ—Ć–Ĺ—č–Ķ (—Ü–≤–Ķ—ā–Ĺ–ĺ–Ķ –ī—É–Ņ–Ľ–Ķ–ļ—Ā–Ĺ–ĺ–Ķ —Ā–ļ–į–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ (–¶–Ē–°) –į—Ä—ā–Ķ—Ä–ł–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ, –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ –Ľ–ĺ–ī—č–∂–Ķ—á–Ĺ–ĺ-–Ņ–Ľ–Ķ—á–Ķ–≤–ĺ–≥–ĺ –ł–Ĺ–ī–Ķ–ļ—Ā–į (–õ–ü–ė)) –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź. –Ē–Ľ—Ź –ĺ—Ü–Ķ–Ĺ–ļ–ł —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ĺ–≤–ĺ–ī–ł–ľ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ–ł—Ā—Ć –ļ–į–ļ —Ā—É–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č–Ķ (–ĺ—Ü–Ķ–Ĺ–ļ–į –ī–ł—Ā—ā–į–Ĺ—Ü–ł–ł –Ī–Ķ–∑–Ī–ĺ–Ľ–Ķ–≤–ĺ–Ļ —Ö–ĺ–ī—Ć–Ī—č (–Ē–Ď–•)), —ā–į–ļ –ł –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č–Ķ –ļ—Ä–ł—ā–Ķ—Ä–ł–ł –ĺ—Ü–Ķ–Ĺ–ļ–ł (–ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ —Ą–į–ļ—ā–ĺ—Ä–į —Ä–ĺ—Ā—ā–į —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź (VEGF-–ź) –≤ –Ņ–Ķ—Ä–ł—Ą–Ķ—Ä–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ļ—Ä–ĺ–≤–ł, –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –ĺ—ā—ā–Ķ–ļ–į—é—Č–Ķ–Ļ –ĺ—ā –ł—ą–Ķ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –ľ—č—ą—Ü, –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ BNIP3 –≤ –Ī–ł–ĺ–Ņ—ā–į—ā–Ķ –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł). –Ē–Ď–• –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–į—Ā—Ć –Ņ–ĺ –ī–į–Ĺ–Ĺ—č–ľ —ā—Ä–Ķ–ī–ľ–ł–Ľ-—ā–Ķ—Ā—ā–į (—Ā–ļ–ĺ—Ä–ĺ—Ā—ā—Ć –Ī–Ķ–≥–ĺ–≤–ĺ–Ļ –ī–ĺ—Ä–ĺ–∂–ļ–ł 3 –ļ–ľ/—á, —É–≥–ĺ–Ľ –Ĺ–į–ļ–Ľ–ĺ–Ĺ–į 10%). –§–į–ļ—ā–ĺ—Ä —Ä–ĺ—Ā—ā–į —ć–Ĺ–ī–ĺ—ā–Ķ–Ľ–ł—Ź –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ—Ź–Ľ—Ā—Ź –≤ –≤–Ķ–Ĺ–ĺ–∑–Ĺ–ĺ–Ļ –ļ—Ä–ĺ–≤–ł, –≤–∑—Ź—ā–ĺ–Ļ –ł–∑ v. marginalis lateralis –Ĺ–į —Ā—ā–ĺ–Ņ–Ķ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł. –ö—Ä–ĺ–≤—Ć –ī–Ľ—Ź –ĺ—Ü–Ķ–Ĺ–ļ–ł –ľ–Ķ—Ā—ā–Ĺ—č—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ –≤ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ –∑–į–Ī–ł—Ä–į—ā—Ć –ł–ľ–Ķ–Ĺ–Ĺ–ĺ –ł–∑ –≤–Ķ–Ĺ –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł –≤ –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–Ļ –Ī–Ľ–ł–∑–ĺ—Ā—ā–ł –ĺ—ā –ł—ą–Ķ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö —ā–ļ–į–Ĺ–Ķ–Ļ, —ā. –ļ. –≤–Ķ–Ĺ–ĺ–∑–Ĺ–į—Ź –ļ—Ä–ĺ–≤—Ć –≤ —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö —É—á–į—Ā—ā–ļ–į—Ö –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į —Ā—É—Č–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ —Ä–į–∑–Ľ–ł—á–į–Ķ—ā—Ā—Ź –Ņ–ĺ –ĺ–Ī—Č–ł–ľ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź–ľ (—ā–į–ļ–ł–ľ –ļ–į–ļ –Ņ–į—Ä—Ü–ł–į–Ľ—Ć–Ĺ–ĺ–Ķ –ī–į–≤–Ľ–Ķ–Ĺ–ł–Ķ –ļ–ł—Ā–Ľ–ĺ—Ä–ĺ–ī–į –ł —É–≥–Ľ–Ķ–ļ–ł—Ā–Ľ–ĺ–≥–ĺ –≥–į–∑–į), –ł–∑ —á–Ķ–≥–ĺ –ľ–ĺ–∂–Ĺ–ĺ —Ā–ī–Ķ–Ľ–į—ā—Ć –≤—č–≤–ĺ–ī, —á—ā–ĺ –ł –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł –į–Ĺ–≥–ł–ĺ–≥–Ķ–Ĺ–Ķ–∑–į –≤ —Ä–į–∑–Ĺ—č—Ö –∑–ĺ–Ĺ–į—Ö —ā–į–ļ–∂–Ķ –ĺ—ā–Ľ–ł—á–į—é—ā—Ā—Ź. –Ď–ł–ĺ–Ņ—ā–į—ā –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č –Ī—č–Ľ –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ –Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–ĺ–ľ –Ņ–ł—Ā—ā–ĺ–Ľ–Ķ—ā–Ĺ–ĺ–Ļ –į–≤—ā–ĺ–ľ–į—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ī–ł–ĺ–Ņ—Ā–ł–ł (–ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ—Ā—Ź –Ņ–ł—Ā—ā–ĺ–Ľ–Ķ—ā Sterylab Colt) –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č –Ĺ–į –≥—Ä–į–Ĺ–ł—Ü–Ķ –≤–Ķ—Ä—Ö–Ĺ–Ķ–Ļ –ł —Ā—Ä–Ķ–ī–Ĺ–Ķ–Ļ —ā—Ä–Ķ—ā–ł –≥–ĺ–Ľ–Ķ–Ĺ–ł –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł [13]. –ó–į–Ī–ĺ—Ä –ľ–į—ā–Ķ—Ä–ł–į–Ľ–į –ī–Ľ—Ź –Ī–ł–ĺ–Ņ—Ā–ł–ł –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ –ł–ľ–Ķ–Ĺ–Ĺ–ĺ –Ĺ–į —ć—ā–ĺ–ľ —É—Ä–ĺ–≤–Ĺ–Ķ, —ā. –ļ. –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č –≤ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł —Ā—ā—Ä–į–ī–į–Ľ–ł ¬ę–Ĺ–ł–∑–ļ–ĺ–Ļ¬Ľ –Ņ–Ķ—Ä–Ķ–ľ–Ķ–∂–į—é—ą–Ķ–Ļ—Ā—Ź —Ö—Ä–ĺ–ľ–ĺ—ā–ĺ–Ļ, –Ņ—Ä–ĺ—Ź–≤–Ľ—Ź–≤—ą–Ķ–Ļ—Ā—Ź –Ī–ĺ–Ľ—Ź–ľ–ł –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –≤ –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ—č—Ö –ľ—č—ą—Ü–į—Ö. –£—Ä–ĺ–≤–Ķ–Ĺ—Ć VEGF-–ź –≤ —Ā—č–≤–ĺ—Ä–ĺ—ā–ļ–Ķ –ļ—Ä–ĺ–≤–ł –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ—Ā—Ź —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é –ł–ľ–ľ—É–Ĺ–ĺ—Ą–Ķ—Ä–ľ–Ķ–Ĺ—ā–Ĺ–ĺ–≥–ĺ –į–Ĺ–į–Ľ–ł–∑–į —Ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ–ľ —Ä–Ķ–į–ļ—ā–ł–≤–ĺ–≤ RandD (–°–®–ź).
–Ď–ł–ĺ–Ņ—Ā–ł—Ź –≤—č–Ņ–ĺ–Ľ–Ĺ—Ź–Ľ–į—Ā—Ć –≤ 1-–Ļ –ī–Ķ–Ĺ—Ć –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł —á–Ķ—Ä–Ķ–∑ 6 –ľ–Ķ—Ā. –Ņ–ĺ—Ā–Ľ–Ķ –Ĺ–į—á–į–Ľ–į. –ú–į—ā–Ķ—Ä–ł–į–Ľ —Ą–ł–ļ—Ā–ł—Ä–ĺ–≤–į–Ľ—Ā—Ź –≤ –ī–≤—É—Ö —Ä–į–∑–Ľ–ł—á–Ĺ—č—Ö —Ā—Ä–Ķ–ī–į—Ö: –Ņ–Ķ—Ä–≤–į—Ź —á–į—Ā—ā—Ć ‚ÄĒ –≤ 10% —Ä–į—Ā—ā–≤–ĺ—Ä–Ķ —Ą–ĺ—Ä–ľ–į–Ľ–ł–Ĺ–į, –≤—ā–ĺ—Ä–į—Ź —á–į—Ā—ā—Ć ‚ÄĒ –≤ —Ą–ĺ—Ā—Ą–į—ā–Ĺ–ĺ–ľ –Ī—É—Ą–Ķ—Ä–Ķ —Ā –ī–ĺ–Ī–į–≤–Ľ–Ķ–Ĺ–ł–Ķ–ľ 2,5% —Ä–į—Ā—ā–≤–ĺ—Ä–į –≥–Ľ—É—ā–į—Ä–ĺ–≤–ĺ–≥–ĺ –į–Ľ—Ć–ī–Ķ–≥–ł–ī–į. –°–≤–Ķ—ā–ĺ–≤–į—Ź –ľ–ł–ļ—Ä–ĺ—Ā–ļ–ĺ–Ņ–ł—Ź –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–į—Ā—Ć —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é –ľ–ł–ļ—Ä–ĺ—Ā–ļ–ĺ–Ņ–į LeicaDM 2500. –ě–ļ—Ä–į—Ā–ļ–į –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–į—Ā—Ć –≥–Ķ–ľ–į—ā–ĺ–ļ—Ā–ł–Ľ–ł–Ĺ–ĺ–ľ –ł —ć–ĺ–∑–ł–Ĺ–ĺ–ľ. –Ē–Ľ—Ź –ł–ľ–ľ—É–Ĺ–ĺ–≥–ł—Ā—ā–ĺ—Ö–ł–ľ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ–ł—Ā—Ć —ā–ļ–į–Ĺ–ł, —Ą–ł–ļ—Ā–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ķ –≤ —Ä–į—Ā—ā–≤–ĺ—Ä–Ķ —Ą–ĺ—Ä–ľ–į–Ľ–ł–Ĺ–į. –ė—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ĺ—Ā—Ć –Ĺ–į —Ā—Ä–Ķ–∑–į—Ö —ā–ĺ–Ľ—Č–ł–Ĺ–ĺ–Ļ 4‚Äď5 –ľ–ļ–ľ –Ĺ–į –Ņ–ĺ–ļ—Ä—č—ā—č—Ö –Ņ–ĺ–Ľ–ł-L-–Ľ–ł–∑–ł–Ĺ–ĺ–ľ –Ņ—Ä–Ķ–ī–ľ–Ķ—ā–Ĺ—č—Ö —Ā—ā–Ķ–ļ–Ľ–į—Ö. –ė—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ–ł –Ņ–Ķ—Ä–≤–ł—á–Ĺ—č–Ķ –Ņ–ĺ–Ľ–ł–ļ–Ľ–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–Ķ –į–Ĺ—ā–ł—ā–Ķ–Ľ–į –ļ BNIP3 —Ą–ł—Ä–ľ—č Santa Kruz Biotechnology (–°–®–ź) –ł –Ĺ–į–Ī–ĺ—Ä —Ä–Ķ–į–ļ—ā–ł–≤–ĺ–≤ –ī–Ľ—Ź –Ņ–Ķ—Ä–ĺ–ļ—Ā–ł–ī–į–∑–Ĺ–ĺ–Ļ —Ä–Ķ–į–ļ—Ü–ł–ł UniversalLSAB2 DAKO (–°–®–ź). –†–Ķ–∑—É–Ľ—Ć—ā–į—ā –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ—Ā—Ź —Ā–Ľ–Ķ–ī—É—é—Č–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ: 0 ‚ÄĒ —Ä–Ķ–į–ļ—Ü–ł—Ź –ĺ—ā—Ā—É—ā—Ā—ā–≤—É–Ķ—ā, 1 ‚ÄĒ –ľ–į–Ľ–ĺ–Ķ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ –≤—Ā—ā—É–Ņ–ł–≤—ą–ł—Ö –≤ —Ä–Ķ–į–ļ—Ü–ł—é –ļ–Ľ–Ķ—ā–ĺ–ļ, 2 ‚ÄĒ —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–ĺ–Ķ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ, 3 ‚ÄĒ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–ĺ.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź
–ě—Ā–Ĺ–ĺ–≤–Ĺ—č–ľ–ł –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ–ł –ĺ—Ü–Ķ–Ĺ–ļ–ł —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ĺ–≤–ĺ–ī–ł–ľ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ī—č–Ľ–ł –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł –Ē–Ď–•, –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ VEGF-A –≤ –Ņ–Ķ—Ä–ł—Ą–Ķ—Ä–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ļ—Ä–ĺ–≤–ł, –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –ĺ—ā—ā–Ķ–ļ–į—é—Č–Ķ–Ļ –ĺ—ā –ł—ą–Ķ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –ľ—č—ą—Ü, –ł –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–Ķ BNIP3 –≤ –Ī–ł–ĺ–Ņ—ā–į—ā–Ķ –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł –Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–ĺ–ľ —ć–Ľ–Ķ–ļ—ā—Ä–ĺ–Ĺ–Ĺ–ĺ–Ļ –ľ–ł–ļ—Ä–ĺ—Ā–ļ–ĺ–Ņ–ł–ł. –í –≥—Ä—É–Ņ–Ņ–Ķ 1 –Ī—č–Ľ–ł –∑–į—Ą–ł–ļ—Ā–ł—Ä–ĺ–≤–į–Ĺ—č –Ĺ–Ķ—É–ī–ĺ–≤–Ľ–Ķ—ā–≤–ĺ—Ä–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č ‚ÄĒ –ļ–į–ļ–ĺ–≥–ĺ-–Ľ–ł–Ī–ĺ –∑–Ĺ–į—á–ł–ľ–ĺ–≥–ĺ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –≤—č—ą–Ķ—É–ļ–į–∑–į–Ĺ–Ĺ—č—Ö –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ –Ĺ–Ķ –Ī—č–Ľ–ĺ.–í –≥—Ä—É–Ņ–Ņ–Ķ 2 –Ī—č–Ľ–į –∑–į—Ą–ł–ļ—Ā–ł—Ä–ĺ–≤–į–Ĺ–į –ī–ł–Ĺ–į–ľ–ł–ļ–į –Ņ–ĺ –≤—Ā–Ķ–ľ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź–ľ: –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–Ķ –Ē–Ď–•, –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–ł–Ķ VEGF-A, –į —ā–į–ļ–∂–Ķ –ī–ĺ—Ā—ā–ĺ–≤–Ķ—Ä–Ĺ–ĺ–Ķ —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ —É—Ä–ĺ–≤–Ĺ—Ź BNIP3 (—ā–į–Ī–Ľ. 2, 3).
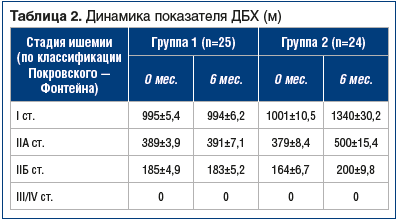
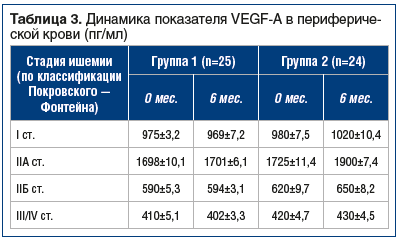
–ě–Ī—Ä–į—Č–į–Ķ—ā –Ĺ–į —Ā–Ķ–Ī—Ź –≤–Ĺ–ł–ľ–į–Ĺ–ł–Ķ –≤—č—Ā–ĺ–ļ–ł–Ļ –ļ–į–ļ –Ĺ–į—á–į–Ľ—Ć–Ĺ—č–Ļ, —ā–į–ļ –ł —á–Ķ—Ä–Ķ–∑ 6 –ľ–Ķ—Ā. —É—Ä–ĺ–≤–Ķ–Ĺ—Ć VEGF —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā–ĺ II–ź —Ā—ā–į–ī–ł–Ķ–Ļ –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é —Ā —ā–į–ļ–ĺ–≤—č–ľ –≤–ĺ –≤—Ā–Ķ—Ö –ī—Ä—É–≥–ł—Ö –≥—Ä—É–Ņ–Ņ–į—Ö. –≠—ā–ĺ –ĺ–Ī—ä—Ź—Ā–Ĺ—Ź–Ķ—ā—Ā—Ź —ā–Ķ–ľ, —á—ā–ĺ II–ź —Ā—ā–į–ī–ł—Ź —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —Ā–≤–ĺ–Ķ–≥–ĺ —Ä–ĺ–ī–į –Ņ–ĺ–≥—Ä–į–Ĺ–ł—á–Ĺ–ĺ–Ļ –Ľ–ł–Ĺ–ł–Ķ–Ļ, –ļ–ĺ–≥–ī–į –ļ–ĺ–ľ–Ņ–Ķ–Ĺ—Ā–į—ā–ĺ—Ä–Ĺ—č–Ķ –ľ–Ķ—Ö–į–Ĺ–ł–∑–ľ—č –∑–į–ī–Ķ–Ļ—Ā—ā–≤–ĺ–≤–į–Ĺ—č –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ, –≤ –ī–į–Ľ—Ć–Ĺ–Ķ–Ļ—ą–Ķ–ľ –Ņ—Ä–ł –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź —Ā–ĺ–Ņ—Ä–ĺ—ā–ł–≤–Ľ–Ķ–Ĺ–ł–Ķ –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—é —Ā–Ĺ–ł–∂–į–Ķ—ā—Ā—Ź [13].
–Ě–į–ł–Ľ—É—á—ą–ł–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ī—č–Ľ–ł –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ—č —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ĺ–į—á–į–Ľ—Ć–Ĺ—č–ľ–ł —Ā—ā–į–ī–ł—Ź–ľ–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź (—Ā—ā–į–ī–ł–ł I –ł II –Ņ–ĺ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–ł –ü–ĺ–ļ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ ‚ÄĒ –§–ĺ–Ĺ—ā–Ķ–Ļ–Ĺ–į).
–ě–Ī—Ā—É–∂–ī–Ķ–Ĺ–ł–Ķ
–í –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–Ķ —á–Ķ–Ľ–ĺ–≤–Ķ–ļ–į, –ļ–į–ļ –∑–ī–ĺ—Ä–ĺ–≤–ĺ–≥–ĺ, —ā–į–ļ –ł –Ī–ĺ–Ľ—Ć–Ĺ–ĺ–≥–ĺ, –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č –į–Ĺ–≥–ł–ĺ–≥–Ķ–Ĺ–Ķ–∑–į –ł –į–Ņ–ĺ–Ņ—ā–ĺ–∑–į –ł–ī—É—ā –Ņ–ĺ—Ā—ā–ĺ—Ź–Ĺ–Ĺ–ĺ, –Ĺ–ĺ –Ņ—Ä–ł –Ņ–ĺ—Ä–į–∂–Ķ–Ĺ–ł–ł –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —Ä—É—Ā–Ľ–į –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł —Ā —Ä–į–∑–≤–ł—ā–ł–Ķ–ľ —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ—Ā—ā–ł –≤ –ī–į–Ľ—Ć–Ĺ–Ķ–Ļ—ą–Ķ–ľ —ć—ā–ł –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā—č –ľ–Ķ–Ĺ—Ź—é—ā —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć —Ā–≤–ĺ–Ķ–Ļ –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł. –ü–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ –Ĺ–į—ą–Ķ–≥–ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –≤–ł–ī–Ĺ–ĺ, —á—ā–ĺ II–ź —Ā—ā–į–ī–ł—Ź —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ņ–ĺ–≥—Ä–į–Ĺ–ł—á–Ĺ–ĺ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć—é –ł—ą–Ķ–ľ–ł–ł, –ļ–ĺ–≥–ī–į –ľ–ĺ—Ä—Ą–ĺ—Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–Ķ –Ĺ–į—Ä—É—ą–Ķ–Ĺ–ł—Ź –Ķ—Č–Ķ –Ĺ–ĺ—Ā—Ź—ā –ĺ–Ī—Ä–į—ā–ł–ľ—č–Ļ —Ö–į—Ä–į–ļ—ā–Ķ—Ä, –Ņ–ĺ—ć—ā–ĺ–ľ—É –ł–ľ–Ķ–Ĺ–Ĺ–ĺ –≤ —ć—ā–ĺ –≤—Ä–Ķ–ľ—Ź —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ –≤—č—Ä–į–∂–Ķ–Ĺ –į–Ĺ–≥–ł–ĺ–≥–Ķ–Ĺ–Ķ–∑. –° –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ–ľ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –ľ–ĺ—Ä—Ą–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ –ł —Ą—É–Ĺ–ļ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–Ķ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź —Ā—ā–į–Ĺ–ĺ–≤—Ź—ā—Ā—Ź –Ņ–ĺ—Ā—ā–ĺ—Ź–Ĺ–Ĺ—č–ľ–ł, –Ņ–ĺ—ć—ā–ĺ–ľ—É –ļ–ĺ–ľ–Ņ–Ķ–Ĺ—Ā–į—ā–ĺ—Ä–Ĺ—č–Ķ –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–ł –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į —Ā–Ĺ–ł–∂–į—é—ā—Ā—Ź.–ö–į–ļ –≤ –≥—Ä—É–Ņ–Ņ–Ķ 1, —ā–į–ļ –ł –≥—Ä—É–Ņ–Ņ–Ķ 2 –Ĺ–Ķ –Ī—č–Ľ–ĺ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ –∑–Ĺ–į—á–ł–ľ—č—Ö –Ņ–ĺ–Ī–ĺ—á–Ĺ—č—Ö —Ä–Ķ–į–ļ—Ü–ł–Ļ, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –ľ–ĺ–∂–Ĺ–ĺ –Ī—č–Ľ–ĺ –Ī—č –į—Ā—Ā–ĺ—Ü–ł–ł—Ä–ĺ–≤–į—ā—Ć —Ā –Ņ—Ä–ĺ–≤–ĺ–ī–ł–ľ—č–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ–ľ. –í —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –Ī—č–Ľ–į –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–į –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–į—Ź –≤–Ĺ—É—ā—Ä–ł–≥—Ä—É–Ņ–Ņ–ĺ–≤–į—Ź –ī–ł–Ĺ–į–ľ–ł–ļ–į –ĺ—ā–Ĺ–ĺ—Ā–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ł—Ā—Ö–ĺ–ī–Ĺ—č—Ö —Ā—É–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö (–Ē–Ď–•) –ł –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č—Ö (VEGF –≤ –Ņ–Ķ—Ä–ł—Ą–Ķ—Ä–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ļ—Ä–ĺ–≤–ł –ł BNIP3 –≤ –Ī–ł–ĺ–Ņ—ā–į—ā–Ķ –ł–ļ—Ä–ĺ–Ĺ–ĺ–∂–Ĺ–ĺ–Ļ –ľ—č—ą—Ü—č) –Ņ–į—Ä–į–ľ–Ķ—ā—Ä–ĺ–≤ –ī–Ľ—Ź –≥—Ä—É–Ņ–Ņ—č, –ļ–ĺ—ā–ĺ—Ä–į—Ź –Ņ–ĺ–Ľ—É—á–į–Ľ–į –≥–Ķ–Ĺ–Ĺ–ĺ-—ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ, –Ņ—Ä–ł —ć—ā–ĺ–ľ –Ľ—É—á—ą–ł–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ī—č–Ľ–ł –Ņ–ĺ–Ľ—É—á–Ķ–Ĺ—č –ī–Ľ—Ź –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –Ĺ–į—á–į–Ľ—Ć–Ĺ—č–ľ–ł –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź–ľ–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź –ł —Ā –Ņ–Ķ—Ä–Ķ–ľ–Ķ–∂–į—é—Č–Ķ–Ļ—Ā—Ź —Ö—Ä–ĺ–ľ–ĺ—ā–ĺ–Ļ. –£ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ł—ą–Ķ–ľ–ł–Ķ–Ļ –Ĺ–Ķ–Ľ—Ć–∑—Ź –≥–ĺ–≤–ĺ—Ä–ł—ā—Ć –ĺ –∑–Ĺ–į—á–ł–ľ–ĺ–Ļ –ī–ł–Ĺ–į–ľ–ł–ļ–Ķ ‚ÄĒ –Ĺ–ł –ĺ—ā—Ä–ł—Ü–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ, –Ĺ–ł –Ņ–ĺ–Ľ–ĺ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ. –£ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≥—Ä—É–Ņ–Ņ—č 1, –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł—Ö —Ā—ā–į–Ĺ–ī–į—Ä—ā–Ĺ–ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ, –ļ–į–ļ–ĺ–Ļ-–Ľ–ł–Ī–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ –ī–ł–Ĺ–į–ľ–ł–ļ–ł –ł—Ā—Ā–Ľ–Ķ–ī—É–Ķ–ľ—č—Ö –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ –∑–į—Ą–ł–ļ—Ā–ł—Ä–ĺ–≤–į–Ĺ–ĺ –Ĺ–Ķ –Ī—č–Ľ–ĺ.
–Ě–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ņ–Ķ—Ä–Ķ–ľ–Ķ–∂–į—é—Č–Ķ–Ļ—Ā—Ź —Ö—Ä–ĺ–ľ–ĺ—ā—č (–≥–Ķ–Ĺ–Ĺ–ĺ-—ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č, –ł–Ĺ–≥–ł–Ī–ł—ā–ĺ—Ä—č —Ą–ĺ—Ā—Ą–ĺ–ī–ł—ć—Ā—ā–Ķ—Ä–į–∑—č, –į–Ĺ—ā–ł–≥–ł–Ņ–ĺ–ļ—Ā–ł—á–Ķ—Ā–ļ–ł–Ķ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā—č) –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ķ—ā –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ –Ĺ–į –Ņ—Ä–ĺ—ā—Ź–∂–Ķ–Ĺ–ł–ł –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –≤—Ä–Ķ–ľ–Ķ–Ĺ–ł –ł–∑–Ī–Ķ–≥–į—ā—Ć —Ä–į–∑–≤–ł—ā–ł—Ź –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ł—ą–Ķ–ľ–ł–ł. –Ď–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–ĺ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤ –ī–Ľ—Ź –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź —Ö—Ä–ĺ–ľ–ĺ—ā—č –Ĺ–Ķ –ĺ–ļ–į–∑—č–≤–į—é—ā –≤–Ľ–ł—Ź–Ĺ–ł—Ź –Ĺ–į —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł—é –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź. –ü–ĺ—ć—ā–ĺ–ľ—É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ —Ā –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ł—ą–Ķ–ľ–ł–Ķ–Ļ (—Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É—é—Č–Ķ–Ļ III –ł IV —Ā—ā–į–ī–ł–ł –Ņ–ĺ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–ł –ü–ĺ–ļ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ ‚ÄĒ –§–ĺ–Ĺ—ā–Ķ–Ļ–Ĺ–į) —Ā–Ľ–Ķ–ī—É–Ķ—ā —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–ĺ–≤–į—ā—Ć –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –≤ —Ā–Ņ–Ķ—Ü–ł–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –į–Ĺ–≥–ł–ĺ—Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ł—Ö —Ā—ā–į—Ü–ł–ĺ–Ĺ–į—Ä–į—Ö, –≥–ī–Ķ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ—č–ľ –ľ–Ķ—ā–ĺ–ī–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź —Ā–Ľ–Ķ–ī—É–Ķ—ā –≤—č–Ī–ł—Ä–į—ā—Ć –ĺ–Ņ–Ķ—Ä–į—ā–ł–≤–Ĺ–ĺ–Ķ (–ĺ—ā–ļ—Ä—č—ā–ĺ–Ķ –ł–Ľ–ł —Ä–Ķ–Ĺ—ā–≥–Ķ–Ĺ—ć–Ĺ–ī–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ–ĺ–Ķ). –ď–ĺ–≤–ĺ—Ä—Ź –ĺ –ļ–ĺ–Ĺ—Ā–Ķ—Ä–≤–į—ā–ł–≤–Ĺ–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –ł—ą–Ķ–ľ–ł–ł, —É–≥—Ä–ĺ–∂–į—é—Č–Ķ–Ļ –∂–ł–∑–Ĺ–Ķ—Ā–Ņ–ĺ—Ā–ĺ–Ī–Ĺ–ĺ—Ā—ā–ł –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł, —Ā–Ľ–Ķ–ī—É–Ķ—ā –ĺ—ā–ī–į–≤–į—ā—Ć –Ņ—Ä–Ķ–ī–Ņ–ĺ—á—ā–Ķ–Ĺ–ł–Ķ –ī—Ä—É–≥–ł–ľ –≥—Ä—É–Ņ–Ņ–į–ľ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–≤, –≤ —á–į—Ā—ā–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ĺ—Ā—ā–į–≥–Ľ–į–Ĺ–ī–ł–Ĺ–į–ľ.








.gif)



