к терапии
Нейропатическая боль – это болевой синдром, обусловленный поражением соматосенсорной нервной системы вследствие самых разных причин (табл. 1). Частота встречаемости в популяции составляет 6–7%, а на неврологических приемах пациенты с нейропатической болью составляют 10–12%. Клинически этот тип боли характеризуется комплексом специфических чувствительных расстройств, которые можно разделить на две группы. С одной стороны, это позитивные симптомы (спонтанная боль, аллодиния, гипералгезия, дизестезии, парестезии), с другой – негативные симптомы (гипестезия, гипалгезия). Этот тип болевого синдрома бывает трудно лечить, и не всегда удается полностью купировать болевой синдром. Нередко у таких пациентов нарушается сон, развивается депрессия и тревога, снижается качество жизни. Многие из них долго мучаются, прежде чем получают адекватную помощь. Большинство пациентов (около 80%) более года испытывают боль до своего первого обращения к специалисту. Лечение основного заболевания (что естественно является безусловным) не всегда приводит к редукции боли. Нередко мы наблюдаем диссоциацию между выраженностью боли и степенью поражения нервной системы. Увы, многие пациенты с нейропатической болью ошибочно принимают НПВП, которые при этом типе боли неэффективны. Это обусловлено тем, что при нейропатической боли главными патогенетическими механизмами являются не процессы активации периферических ноцицепторов, а нейрональные и рецепторные нарушения, периферическая и центральная сенситизация.
В терапии нейропатической боли лучше всего использовать комплексный подход. Даже в рамках амбулаторной помощи может быть начато лечение несколькими разными методами. Сегодня отсутствует достаточное количество доказательных данных о пользе применения консервативных немедикаментозных методов лечения (например, физиотерапии, физических упражнений, чрескожной электронейростимуляции). Однако, учитывая относительную безопасность этих методов, при отсутствии противопоказаний не следует исключать возможность их применения.
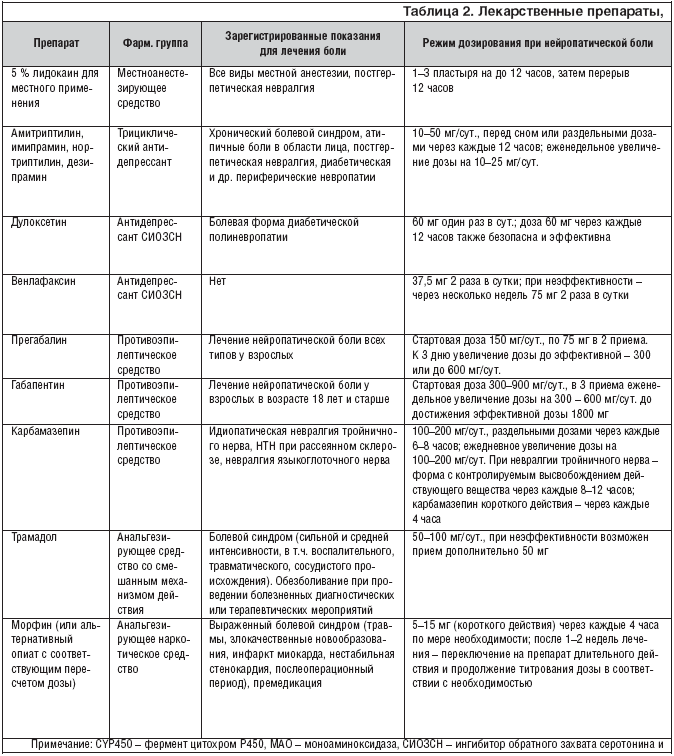
Наиболее признанной в лечении нейропатической боли на сегодняшний день является фармакотерапия. Основные препараты и их характеристики приведены в таблице 2.
При постгерпетической невралгии сначала может быть назначено местное лечение лидокаином. Считается, что действие лидокаина основано на блокировании движения натриевых ионов через клеточную мембрану нейронов. Это стабилизирует клеточную мембрану и предотвращает распространение потенциала действия и соответственно уменьшает боль. Следует иметь в виду, что уменьшение боли при местном применении обезболивающих средств не распространяется за пределы площади и продолжительности контакта с пораженной областью тела. Это может быть удобным для пациентов с небольшой зоной распространения боли. Лидокаин 5% в виде пластыря или пластин показан для снятия боли при постгерпетической невралгии (ПГН). Побочные реакции в виде жжения и эритемы могут наблюдаться в месте наклеивания при длительном применении.
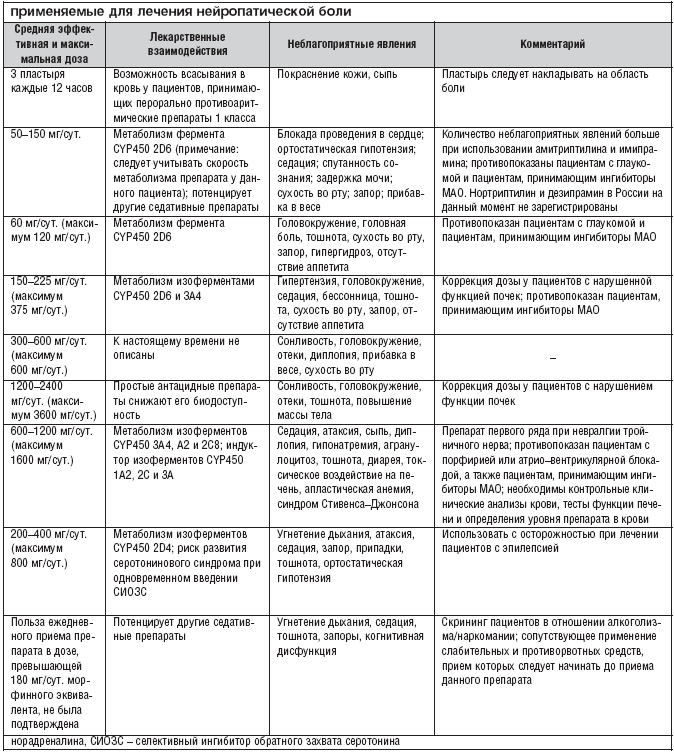
При нейропатических болях другого происхождения, а также в случае безуспешности лечения лидокаином рекомендуется начать пероральную монотерапию прегабалином или габапентином, трициклическим антидепрессантом или смешанным ингибитором обратного захвата серотонина и норадреналина. Из перечисленных препаратов наилучшей переносимостью обладают прегабалин и габапентин. Эти препараты характеризуются практически полным отсутствием лекарственных взаимодействий и невысокой частотой развития нежелательных явлений. Оба препарата показали свою эффективность в лечении различных нейропатических болей. Однако по сравнению с габапентином прегабалин, обладая линейной фармакокинетикой и значительно более высокой биодоступностью (90%), оказывает быстрый положительный дозозависимый эффект: в проведенных исследованиях достоверное снижение боли более 60% от исходного уровня было достигнуто в течение 1–3 дней лечения и сохранялось на протяжении всего курса лечения. Быстрота редукции боли напрямую коррелирует с улучшением сна и настроения у этих больных, удобный режим дозирования прегабалина повышает также комплаентность при лечении этих пациентов и способствует более быстрому улучшению качества жизни. Дозировка прегабалина от 300 до 600 мг/сут. показала себя наиболее эффективной по сравнению с плацебо, значительно уменьшая боль и нарушения сна. Препарат можно принимать до, во время или после еды. При лечении нейропатической боли стартовая доза может составлять 150 мг/сут. в 2 приема. Для получения ++оптимального терапевтического эффекта дозу прегабалина необходимо увеличить до 300 мг/сут. начиная с 4 дня терапии. При необходимости дозу повышают до максимальной (600 мг/сут.) через 7–дневный интервал. В соответствии с опытом применения препарата при необходимости прекращения приема рекомендуется постепенно снижать дозу в течение недели. Прегабалин не метаболизируется в печени и не связывается с белками плазмы, поэтому он практически не взаимодействует с другими лекарствами. Прегабалин хорошо переносится. Наиболее частыми побочными реакциями являются головокружение и сонливость.
Трициклические антидепрессанты также эффективны, но более дешевы; однако при их применении более высока вероятность развития побочных эффектов. Более того, они относительно противопоказаны при сердечно–сосудистой патологии (перед назначением трициклических антидепрессантов рекомендуется проведение ЭКГ), ортостатической гипотензии, задержке мочи и закрытоугольной глаукоме, а также их необходимо назначать с осторожностью пожилым пациентам. Из имеющихся трициклических антидепрессантов в Европе предпочтение отдают нортриптилину и дезипрамину, так как их применение сопровождается меньшим количеством побочных эффектов. Считается, что более современные смешанные ингибиторы обратного захвата серотонина и норадреналина (например, венлафаксин и дулоксетин) менее эффективны по сравнению с трициклическими антидепрессантами, но в то же время они характеризуются лучшей переносимостью.
На сегодняшний день неизвестно, является ли неэффективность одного препарата предиктором неэффективности другого или всей последующей медикаментозной терапии. В том случае, если первый назначенный препарат оказался малоэффективным или плохо переносился пациентом, следует переключаться на альтернативную монотерапию препаратом первого ряда (рис. 1). Если все препараты первого ряда оказались неэффективными или плохо переносимыми, то рекомендуется начать монотерапию трамадолом или его комбинацией с парацетамолом либо опиоидным анальгетиком. К сожалению, это не всегда возможно, так как назначение опиоидных препаратов ограничено специальными требованиями, предъявляемыми к выписке этих препаратов.
В связи с разнообразием механизмов возникновения боли, лечение каждого пациента должно быть индивидуализировано с учетом заболевания, явившегося причиной боли, а также клинических особенностей самого болевого синдрома. Кроме того, следует принимать во внимание множество факторов, таких как: общее состояние пациента, наличие сопутствующих заболеваний (например, сопутствующей депрессии или наркомании/токсикомании, заболеваний печени и почек и т.д.), безуспешность/успешность предшествующей терапии, а также доступность препаратов в аптеке или больнице. При разработке индивидуального подхода к лекарственному лечению, помимо непосредственного анальгетического эффекта, должны быть учтены другие положительные эффекты выбранного препарата (например, уменьшение тревоги, улучшение сна, настроения и качества жизни), а также такие факторы, как его переносимость и возможность развития серьезных побочных эффектов. Пациенты с нейропатической болью нуждаются в постоянной психологической поддержке. Рациональная психотерапия в этом случае может играть ключевую роль. Информация о причинах заболевания, о реальных прогнозах лечения и планируемых терапевтических мероприятиях также крайне важна для пациентов.
Лечение нейропатической боли – длительный процесс, который требует регулярного контроля состояния здоровья пациента и выполнения врачебных назначений. В начале терапии особое внимание следует обращать на правильное титрование дозы препаратов и отслеживать возможность развития лекарственных взаимодействий. В процессе лечения требуется регулярно интересоваться, как пациент соблюдает схемы лечения, решать вопрос о необходимости продолжения приема препарата и оценивать его эффективность. Учитывая долгосрочность терапии, следует мониторировать и, по возможности, предотвращать развитие отдаленных нежелательных явлений (таких, например, как гепато– и гастротоксичность, изменения со стороны системы крови и др.), возникающих на фоне приема некоторых лекарственных средств.
Перед началом терапии следует провести разъяснительную беседу с больным и его родственниками о том, что лечение может быть длительным, и уменьшение боли будет происходить постепенно. При нейропатической боли даже при правильной программе лечения редко удается достичь 100%–го обезболивания. Таким образом, врач должен определенным образом формировать адекватные ожидания пациента и его близких по поводу лечения. В специальной работе было показано, что снижение интенсивности боли на 30% от исходного уровня по ВАШ оценивается самими больными как удовлетворительный результат. Эту цифру следует иметь в виду при оценке эффективности проводимого лечения и решении вопросов о переходе на другой препарат или присоединении нового лекарства к уже принимаемому (рациональная полифармакотерапия).
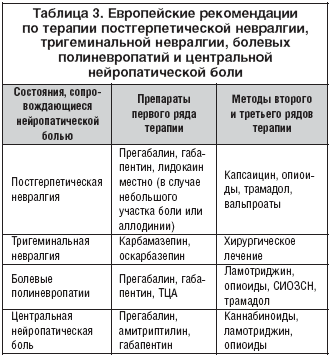
В таблице 3 приведены рекомендации Европейской федерации неврологических обществ (EFNS) по терапии некоторых состояний, сопровождающихся нейропатической болью. Эксперты этой федерации провели анализ всех клинических исследований по нейропатической боли, зарегистрированных в Кокрановской библиотеке (база данных доказательных клинических исследований), начиная с 1966 года. В результате были отобраны исследования с высоким уровнем доказательности, и на их основании построены европейские рекомендации по фармакотерапии.
Рациональная полифармакотерапия
Фармакотерапия при лечении нейропатической боли является основным методом лечения. Однако если на фоне монотерапии препаратами первого ряда не удается полностью купировать болевой синдром, то назначение комбинированной фармакотерапии позволяет повысить эффективность лечения при меньших дозировках препаратов и снизить риск развития побочных явлений. Этот принцип получил название рациональной полифармакотерапии. Многие пациенты с нейропатической болью вынуждены принимать одновременно несколько лекарственных препаратов, несмотря на отсутствие доказательных исследований, подтверждающих пользу таких сочетаний. В последнее время в литературе стали появляться сведения об эффективности различных комбинаций уже известных лекарств. В одном рандомизированном плацебо–контролируемом исследовании, было показано, что сочетание морфина и габапентина превосходит каждый из этих препаратов в отдельности по силе анальгетического эффекта. В другой работе, где участвовали 11 пациентов с нейропатической болью, рефрактерных к габапентину, было продемонстрировано превосходство сочетания габапентина и венлафаксина над монотерапией габапентином. Сегодня очевидна необходимость проведения дальнейших исследований с целью выявления оптимально эффективных сочетаний лекарственных препаратов, подбора доз и наиболее безопасных комбинаций, а также для оценки фармакоэкономических аспектов терапии.
Некоторые аспекты фармакотерапии
Перед назначением любого нового препарата по поводу лечения нейропатической боли необходим тщательный анализ препаратов, уже принимаемых пациентом, с целью исключения лекарственного взаимодействия. В случае полифармакотерапии необходимо отдавать предпочтение препаратам, не имеющим известных лекарственных взаимодействий (например, прегабалину).
В настоящее время описана потенциальная возможность взаимодействия опиоидных анальгетиков и трициклических антидепрессантов, вызывающих серьезные нежелательные явления при передозировке. В случае применения такой комбинации необходимо тщательно взвешивать пользу и риск данного назначения. Нельзя одновременно назначать препараты СИОЗС (например, флуоксетин или пароксетин) и СИОЗСН (например, дулоксетин), поскольку они метаболизируются при участии цитохрома P450, что повышает риск побочных реакций.
Большинство трициклических антидепрессантов, противосудорожных препаратов и опиоидных анальгетиков обладает угнетающим действием на центральную нервную систему. С целью уменьшения выраженности этих и других побочных эффектов в процессе достижения эффективной дозы необходимо использовать постепенное титрование, начиная с минимальной (например,1/4 таблетки амитриптилина, содержащей 25 мг) до максимальной переносимой дозы на протяжении нескольких недель. В этом случае врач и пациент должны осознавать, что облегчение боли будет постепенным. Поскольку трициклические антидепрессанты и карбамазепин у некоторых пациентов быстро метаболизируются, требуется мониторинг уровня препарата в плазме крови, прежде чем безопасно осуществлять дальнейшее повышение дозы в случае отсутствия обезболивающего эффекта на минимальной дозе.
Дифференцированная терапия
болевых синдромов
Анализ болевого синдрома с точки зрения его патофизиологических механизмов (ноцицептивная, нейропатическая, смешанная) оказался очень важным прежде всего с точки зрения лечения. Если врач оценивает боль как ноцицептивную, то наилучшими средствами для ее лечения будут простые анальгетики и НПВП. Если боль является нейропатической или имеется нейропатический компонент, то препаратами выбора являются антиконвульсанты (прегабалин), антидепрессанты, опиоидные анальгетики и лидокаин, особенности которых обсуждались выше (рис. 2). В случае смешанных болевых синдромов, возможна комбинированная терапия с выбором средств в зависимости от представленности ноцицептивного и нейропатического компонентов (рис. 3).
Таким образом, лечение нейропатической боли в настоящее время остается сложной задачей. Представленные выше принципы и алгоритмы лечения могут помочь врачу проводить наиболее эффективное и безопасное лечение пациентов с нейропатическим болевым синдромом. В будущем успех и перспективы лечения связывают с разработкой препаратов, воздействующих на конкретные патофизиологические механизмы данного синдрома.




Литература
1. Данилов А.Б., Давыдов О.С. Нейропатическая боль. Москва: «Боргес», 2007. – 198 с.
2. Attal N., Cruccu G., Haanpaa M., Hansson P., Jensen T.S., Nurmikko T., Sampaio C.,Sindrup S., Wiffen P. EFNS guidelines on pharmacological treatment of neuropathic pain. European Journal of Neurology 2006, 13:1153–1169.
3. Finnerup N.B., Otto M., McQuay H.J., Jensen T.S., Sindrup S.H. Algorithm for neuropathic pain treatment: an evidence based proposal. Pain. 2005 Dec 5;118(3):289 –305.
4. Freynhagen R., Strojek K., Griesing T., Whalen E., Balkenohl M. Efficacy of pregabalin in neuropathic pain evaluated in a 12–week, randomised, double–blind, multicentre, placebo–controlled trial of fble– and fixeddose regimens. Pain. 2005 Jun;115(3):254–63.
5. Galer B.S., Jensen M.P., Ma T., Davies P.S., Rowbotham M.C. The lidocaine patch 5% effectively treats all neuropathic pain qualities: results of a randomized, double–blind, vehicle–controlled, 3–week efficacy study with use of the neuropathic pain scale. Clin J Pain. 2002;18:297–301.
6. Gilron I., Bailey J.M., Tu D., Holden R.R., Weaver D.F., Houlden R.L. Morphine, gabapentin, or their combination for neuropathic pain. N Engl J Med. 2005 Mar 31;352(13):1324–34.
7. Goldstein D.J., Lu Y., Detke M.J., Lee T.C., Iyengar S. Duloxetine vs. placebo in patients with painful diabetic neuropathy. Pain. 2005;116:109–118.
8. Harati Y., Gooch C., Swenson M. et al. Double–blind randomized trial of tramadol for the treatment of the pain of diabetic neuropathy. Neurology. 1998 ;50:1842–1846.
9. Saarto T., Wiffen P. Antidepressants for neuropathic pain. Cochrane Database of Systemic Reviews 2005; 20:CD005454.
10. Sabatowski R., Ga’levz R., Cherry D.A. et al. Pregabalin reduces pain and improves sleep and mood disturbances in patients with post–herpetic neuralgia: Results of a randomized, placebo–controlled clinical trial. Pain 2004.
11. Siddall P.J., Cousins M.J., Otte A., Griesing T., Chambers R., Murphy T.K. Pregabalin in central neuropathic pain associated with spinal cord injury: a placebo–controlled trial. Neurology. 2006 Nov 28;67(10):1792–800.
12. Sindrup S.H., Otto M., Finnerup N.B. et al. Antidepressants in the treatment of neuropathic pain. Basic and Clinical Pharmacology and Therapy 2005; 9 6: 399 –409.
13. van Seventer R., Feister H.A., Young J.P. Jr, Stoker M., Versavel M., Rigaudy L. Efficacy and tolerability of twice–daily pregabalin for treating pain and related sleep interference in postherpetic neuralgia: a 13–week, randomized trial.Curr Med Res Opin. 2006 Feb;22(2):375–84.
14. Wiffen P., McQuay H., Edwards J. et al. Gabapentin for acute and chronic pain. Cochrane Database Systematic Reviews 2005a; 20: CD005452.
15. Wiffen P., Collins S., McQuay H. et al. Anticonvulsant drugs for acute and chronic pain. Cochrane Database Systematic Reviews 2005c; 20: CD001133.








.gif)



