–Т–≤–µ–і–µ–љ–Є–µ
–•—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –ї–µ–≥–Ї–Є—Е (–•–Ю–С–Ы) —П–≤–ї—П–µ—В—Б—П –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є–Љ –њ—А–Є–Љ–µ—А–Њ–Љ –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Т —А–∞–Ј–≤–Є—В–Є–Є –•–Ю–С–Ы –≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –Ї–∞–Ї –≤–љ–µ—И–љ–Є–µ —Б—А–µ–і–Њ–≤—Л–µ —Д–∞–Ї—В–Њ—А—Л (–Ї—Г—А–µ–љ–Є–µ, –њ—А–Њ—Д–µ—Б—Б–Є–Њ–љ–∞–ї—М–љ—Л–µ –Є –±—Л—В–Њ–≤—Л–µ –њ–Њ–ї–ї—О—В–∞–љ—В—Л), —В–∞–Ї –Є –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л [1вАУ3].–Я—А–Є —Н—В–Њ–Љ –≤–µ–і—Г—Й–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –•–Ю–С–Ы —Б—З–Є—В–∞–µ—В—Б—П –Ї—Г—А–µ–љ–Є–µ, –Њ–і–љ–∞–Ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ —Г 15вАУ20% –Ї—Г—А–Є–ї—М—Й–Є–Ї–Њ–≤.
–Ь–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ –≥–µ–љ–µ—В–Є–Ї–Њ-—Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б-
—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г—Б—В–∞–љ–Њ–≤–Є–ї–Є –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В–Є –≤ –і–µ—В–µ—А–Љ–Є–љ–∞—Ж–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Д—Г–љ–Ї—Ж–Є–Є –≤–љ–µ—И–љ–µ–≥–Њ –і—Л—Е–∞–љ–Є—П –Є –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–Є —Б–ї—Г—З–∞–µ–≤ –•–Ю–С–Ы –≤ —Б–µ–Љ—М—П—Е [4], –∞ —В–∞–Ї–ґ–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–Ј—Г—З–µ–љ–Є—П –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–∞—А–Ї–µ—А–Њ–≤ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Є—Е –≤–Ї–ї–∞–і–∞ –≤ —А–∞–Ј–≤–Є—В–Є–µ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ
–•–Ю–С–Ы [5вАУ7]. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Ї –Њ—Б–љ–Њ–≤–љ—Л–Љ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–∞–Љ, –ї–µ–ґ–∞—Й–Є–Љ –≤ –Њ—Б–љ–Њ–≤–µ —А–∞–Ј–≤–Є—В–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –•–Ю–С–Ы, –Њ—В–љ–Њ—Б—П—В—Б—П: —А–∞–Ј–ї–Є—З–љ—Л–µ –≥–µ–љ—Л –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є, –≥–µ–љ—Л, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л–µ –Ј–∞ –Є–Љ–Љ—Г–љ–љ—Л–є —Б—В–∞—В—Г—Б, –Є –≥–µ–љ—Л –Љ–µ–ґ–Ї–ї–µ—В–Њ—З–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є. –†—П–і –∞–≤—В–Њ—А–Њ–≤ –Њ—В–Љ–µ—З–∞—О—В –Њ—Б–Њ–±—Г—О –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –і–ї—П –Є–Ј—Г—З–µ–љ–Є—П —Б–Є—Б—В–µ–Љ—Л –≥–µ–љ–Њ–≤ –Ї—Б–µ–љ–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ (–≥–µ–љ–Њ–≤ ¬Ђ–≤–љ–µ—И–љ–µ–є —Б—А–µ–і—Л¬ї) –≤ —Б–≤—П–Ј–Є —Б –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–Є–Љ —Г—Е—Г–і—И–µ–љ–Є–µ–Љ —Н–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Є —В–Њ–Ї—Б–Є–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Њ–±—Б—В–∞–љ–Њ–≤–Ї–Є –Є —Г–≤–µ–ї–Є—З–Є–≤–∞—О—Й–Є–Љ—Б—П –љ–∞ —Д–Њ–љ–µ —Н—В–Њ–≥–Њ —А–Њ—Б—В–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –•–Ю–С–Ы. –Ю–і–љ–Є–Љ –Є–Ј –Ј–љ–∞—З–Є–Љ—Л—Е —П–≤–ї—П–µ—В—Б—П –≥–µ–љ N-–∞—Ж–µ—В–Є–ї-—В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л 2 (NAT2), –Ї–Њ—В–Њ—А—Л–є –Ї–Њ–і–Є—А—Г–µ—В –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Г—О –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М —Ж–Є—В–Њ–Ј–Њ–ї—М–љ–Њ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ N-–∞—Ж–µ—В–Є–ї-—В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л II —В–Є–њ–∞, —Г—З–∞—Б—В–≤—Г—О—Й–µ–≥–Њ –≤–Њ –≤—В–Њ—А–Њ–є —Д–∞–Ј–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Ї—Б–µ–љ–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ вАФ –≤ –Є—Е –і–µ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –∞—Ж–µ—В–Є–ї–Є—А–Њ–≤–∞–љ–Є—П. –Ш–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ —А–Њ–ї–Є –≥–µ–љ–∞ NAT2 –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –•–Ю–С–Ы –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞—Е–Њ–і–Є—В—Б—П –љ–∞ —Б—В–∞–і–Є–Є –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—П [8вАУ10].
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Є–Ј—Г—З–Є—В—М –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М —З–∞—Б—В–Њ—В—Л –∞–ї–ї–µ–ї–µ–є –Є –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –≥–µ–љ–∞ NAT2 —Б —Е–∞—А–∞–Ї—В–µ—А–Њ–Љ —В–µ—З–µ–љ–Є—П, —З–∞—Б—В–Њ—В–Њ–є —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Є –Њ–±–Њ—Б—В—А–µ–љ–Є–є –•–Ю–С–Ы.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т—Б–µ–≥–Њ –±—Л–ї–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Њ 120 —З–µ–ї–Њ–≤–µ–Ї, –Є–Ј –љ–Є—Е 90 вАФ —Б –•–Ю–С–Ы –Є 30 вАФ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж –≤ –Ї–∞—З–µ—Б—В–≤–µ –≥—А—Г–њ–њ—Л –Ї–Њ–љ—В—А–Њ–ї—П. –Ф–Є–∞–≥–љ–Њ–Ј –•–Ю–С–Ы —Б —Г–Ї–∞–Ј–∞–љ–Є–µ–Љ —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤—Л—Б—В–∞–≤–ї—П–ї—Б—П –њ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ ¬Ђ–У–ї–Њ–±–∞–ї—М–љ–Њ–є —Б—В—А–∞—В–µ–≥–Є–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є, –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –ї–µ–≥–Ї–Є—Е¬ї (GOLD, –њ–µ—А–µ—Б–Љ–Њ—В—А 2014 –≥.). –•–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 1.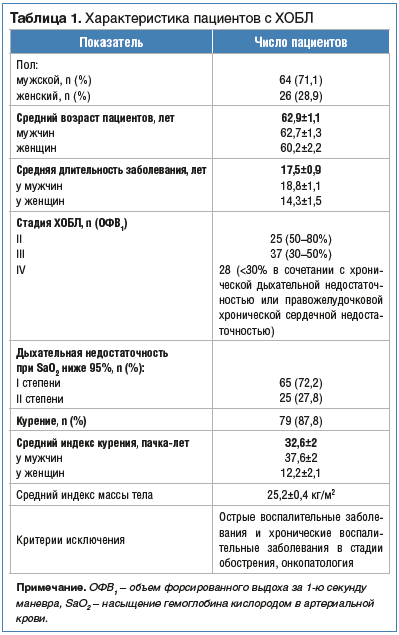
–Э–µ–Ї—Г—А—П—Й–Є–µ –ґ–µ–љ—Й–Є–љ—Л –Њ—В–Љ–µ—З–∞–ї–Є –љ–∞–ї–Є—З–Є–µ —В–∞–Ї–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞, –Ї–∞–Ї –њ–∞—Б—Б–Є–≤–љ–Њ–µ –Ї—Г—А–µ–љ–Є–µ –≤ —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е –ї–µ—В. –Ш–Ј –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы 5 —З–µ–ї–Њ–≤–µ–Ї –Њ—В–Љ–µ—В–Є–ї–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–µ–љ–љ—Л—Е –њ–Њ–ї–ї—О—В–∞–љ—В–Њ–≤ (—Ж–µ–Љ–µ–љ—В–љ–∞—П –Є —Б—В—А–Њ–Є—В–µ–ї—М–љ–∞—П –њ—Л–ї—М, –≥–∞–Ј–Њ—Н–ї–µ–Ї—В—А–Њ—Б–≤–∞—А–Њ—З–љ—Л–є –∞—Н—А–Њ–Ј–Њ–ї—М, —Б—В–µ–Ї–ї–Њ–≤–Њ–ї–Њ–Ї–љ–Њ). –Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л —Б –•–Ю–С–Ы –њ–Њ–ї—Г—З–∞–ї–Є –ї–µ—З–µ–љ–Є–µ –њ–Њ —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ —Б—Е–µ–Љ–∞–Љ, –њ—А–µ–і—Г—Б–Љ–Њ—В—А–µ–љ–љ—Л–Љ —Б—В–∞–љ–і–∞—А—В–Њ–Љ GOLD –њ–µ—А–µ—Б–Љ–Њ—В—А–∞ 2014 –≥. –Ъ–Њ–љ—В—А–Њ–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ –њ–Њ –≥–µ–љ–і–µ—А–љ–Њ–Љ—Г —Б–Њ—Б—В–∞–≤—Г –Є –≤–Њ–Ј—А–∞—Б—В—Г –±—Л–ї–∞ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–∞ —Б –≥—А—Г–њ–њ–Њ–є –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы.
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –∞–ї–ї–µ–ї—М–љ–Њ–≥–Њ –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ–∞ –≥–µ–љ–∞ NAT2 –≤—Л–њ–Њ–ї–љ—П–ї–Њ—Б—М –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –њ—А–µ–љ–∞—В–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є –Ш–љ—Б—В–Є—В—Г—В–∞ –∞–Ї—Г—И–µ—А—Б—В–≤–∞ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є –Є–Љ. –Ф.–Ю. –Ю—В—В–∞ (–°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥). –Я–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ –≥–µ–љ–∞ NAT2 –±—Л–ї –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –≤ –≤–Є–і–µ:
–Њ–і–љ–Њ–≥–Њ ¬Ђ–±—Л—Б—В—А–Њ–≥–Њ¬ї F (–љ–µ–Љ—Г—В–∞–љ—В–љ–Њ–≥–Њ) –∞–ї–ї–µ–ї—П;
—В—А–µ—Е ¬Ђ–Љ–µ–і–ї–µ–љ–љ—Л—Е –∞–ї–ї–µ–ї–µ–є¬ї: S1(C481T), S2(G590A) –Є S3(G857A).
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ –і–∞–љ–љ—Л—Е –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –њ—А–Њ–≥—А–∞–Љ–Љ—Л Statistica 12.0, Stat Soft, Inc. (–°–®–Р).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–Э–∞ –њ–µ—А–≤–Њ–Љ —Н—В–∞–њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ —З–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 —Г –≤—Б–µ—Е –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –ї–Є—Ж. –†–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –•–Ю–С–Ы –Є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л–Љ–Є –ї–Є—Ж–∞–Љ–Є –њ–Њ —З–∞—Б—В–Њ—В–µ –≥–µ–љ–Њ—В–Є–њ–Њ–≤ (S/S, S/F, F/F) –Є –∞–ї–ї–µ–ї–µ–є (S, F) –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–Ј–љ–∞—З–Є–Љ—Л. –І–∞—Й–µ –≤—Б–µ–≥–Њ —Б—А–µ–і–Є –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –ї–Є—Ж –≤—Б—В—А–µ—З–∞–ї—Б—П –≥–µ–љ–Њ—В–Є–њ S/S, —А–µ–ґ–µ вАФ –≥–µ–љ–Њ—В–Є–њ F/F (—А–Є—Б. 1).
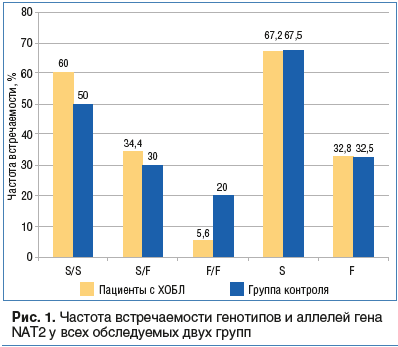
–Ф–∞–ї–µ–µ –Љ—Л –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є —З–∞—Б—В–Њ—В—Г –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы –Є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—А–≤—Л—Е.
–І–∞—Й–µ –≤—Б–µ–≥–Њ –Ї–∞–Ї —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы, —В–∞–Ї –Є —Б—А–µ–і–Є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж –≤—Б—В—А–µ—З–∞–ї–Њ—Б—М –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ –∞–ї–ї–µ–ї—П S (—А–Є—Б. 2).

–†–∞–Ј–ї–Є—З–Є—П –њ–Њ —З–∞—Б—В–Њ—В–µ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –•–Ю–С–Ы –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л–Љ–Є –ї–Є—Ж–∞–Љ–Є –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л (p<0,05). –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы II —Б—В–∞–і–Є–Є –њ—А–µ–Њ–±–ї–∞–і–∞–ї –≥–µ–љ–Њ—В–Є–њ S/F, –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ –≥–µ–љ–Њ—В–Є–њ–∞ S/S –≤—Б—В—А–µ—З–∞–ї–Њ—Б—М —А–µ–і–Ї–Њ, –∞ –≥–µ–љ–Њ—В–Є–њ F/F –љ–µ –≤—Б—В—А–µ—В–Є–ї—Б—П –љ–Є —Г –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ (—А–Є—Б. 3).
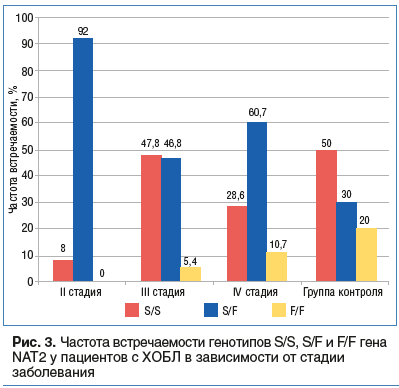
–Э–∞–Є–±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –љ–Њ—Б–Є—В–µ–ї–µ–є –≥–µ–љ–Њ—В–Є–њ–∞ S/F –±—Л–ї–Њ —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы II —Б—В–∞–і–Є–Є. –†–∞–Ј–ї–Є—З–Є—П –њ–Њ —З–∞—Б—В–Њ—В–µ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –≥–µ–љ–∞ NAT2 –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –•–Ю–С–Ы –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є –Ј–і–Њ—А–Њ–≤—Л–Љ–Є –ї–Є—Ж–∞–Љ–Є –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л (p<0,05).
–°–ї–µ–і—Г—О—Й–Є–є —Н—В–∞–њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї –њ–Њ—Б–≤—П—Й–µ–љ –≤—Л—П–≤–ї–µ–љ–Є—О —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Д–Њ—А–Љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —З–∞—Б—В–Њ—В—Л –Њ–±–Њ—Б—В—А–µ–љ–Є—П. –С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ (p<0,05) —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –љ–Њ—Б–Є—В–µ–ї–µ–є –≥–µ–љ–Њ—В–Є–њ–Њ–≤ S/F, F/F –Є –∞–ї–ї–µ–ї—П S —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е –•–Ю–С–Ы —Б –±—А–Њ–љ—Е–Є—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Н–Љ—Д–Є–Ј–µ–Љ–∞—В–Њ–Ј–љ–Њ–є —Д–Њ—А–Љ–Њ–є. –Я–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Њ—В–љ–Њ—И–µ–љ–Є—П —И–∞–љ—Б–Њ–≤, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –±—А–Њ–љ—Е–Є—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л –•–Ю–С–Ы, —Б–Њ—Б—В–∞–≤–Є–ї:
вАҐ —Г –љ–Њ—Б–Є—В–µ–ї–µ–є –≥–µ–љ–Њ—В–Є–њ–∞ S/F: 8,65, 95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї (–Ф–Ш) 1,14вАУ67,71 (ѕЗ2=4,06, df=1, p=0,041);
вАҐ —Г –љ–Њ—Б–Є—В–µ–ї–µ–є –≥–µ–љ–Њ—В–Є–њ–∞ F/F: 8,09, 95% –Ф–Ш 1,11вАУ59,65 (ѕЗ2=4,19, df=1, p=0,038).
–†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ —З–∞—Б—В–Њ—В –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 —Г –±–Њ–ї—М–љ—Л—Е –•–Ю–С–Ы —Б —А–∞–Ј–љ–Њ–є —З–∞—Б—В–Њ—В–Њ–є –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –≤ —В–∞–±–ї–Є—Ж–µ 2.

–Э–µ –≤—Л—П–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–Є –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є —Г –±–Њ–ї—М–љ—Л—Е –•–Ю–С–Ы —Б —А–∞–Ј–ї–Є—З–љ–Њ–є —З–∞—Б—В–Њ—В–Њ–є –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (—А=0,138, ѕЗ2=6,75, df=4). –Ю—В–Љ–µ—З–µ–љ–∞ –ї–Є—И—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –љ–Њ—Б–Є—В–µ–ї–µ–є –≥–µ–љ–Њ—В–Є–њ–Њ–≤ S/S –Є –≤—Л—П–≤–ї–µ–љ–Є—О –∞–ї–ї–µ–ї—П S —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы –њ—А–Є —З–∞—Б—В–Њ—В–µ –Њ–±–Њ—Б—В—А–µ–љ–Є—П 3 —А–∞–Ј–∞ –≤ –≥–Њ–і –Є –±–Њ–ї—М—И–µ. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤—Л—П–≤–ї–µ–љ—Л –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —З–∞—Б—В–Њ—В –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ (p<0,05).
–Ш –љ–∞ –њ–Њ—Б–ї–µ–і–љ–µ–Љ —Н—В–∞–њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–∞ –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–∞ —З–∞—Б—В–Њ—В–∞ –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ф–ї—П —Н—В–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В—Л —Б –•–Ю–С–Ы –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л:
вАҐ 1-—П –≥—А—Г–њ–њ–∞: 25 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Њ–±–Њ—Б—В—А–µ–љ–Є—П –•–Ю–С–Ы 7вАУ10 –і–љ–µ–є;
вАҐ 2-—П –≥—А—Г–њ–њ–∞: 23 –њ–∞—Ж–Є–µ–љ—В–∞ —Б –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Њ–±–Њ—Б—В—А–µ–љ–Є—П 15 –і–љ–µ–є –Є –±–Њ–ї–µ–µ.
–Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –њ–Њ —З–∞—Б—В–Њ—В–µ –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –њ–Њ –≥–µ–љ—Г NAT2 –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –•–Ю–С–Ы –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–є –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ (—А–Є—Б. 4).

–†–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ–± –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ, –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ–Љ, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Є —В—П–ґ–µ—Б—В—М—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –Њ–њ—А–µ–і–µ–ї—П—О—В —А–Є—Б–Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є –Є –±—А–Њ–љ—Е–Є—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Т—Л–≤–Њ–і—Л
–†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –≥–µ–љ–Њ—В–Є–њ–Њ–≤ –Є –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –•–Ю–С–Ы –Ј–∞–≤–Є—Б–Є—В –Њ—В —В—П–ґ–µ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.–Т—Л—П–≤–ї–µ–љ–∞ –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—П –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ–Њ–≤
–≥–µ–љ–∞ NAT2 —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ–Љ –•–Ю–С–Ы.
–І–∞—Б—В–Њ—В–∞ –њ–Њ–ї–Є–Љ–Њ—А—Д–љ—Л—Е –∞–ї–ї–µ–ї–µ–є –≥–µ–љ–∞ NAT2 –Є —З–∞—Б—В–Њ—В–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Є —Е–∞—А–∞–Ї—В–µ—А –Њ–±–Њ—Б—В—А–µ–љ–Є—П –•–Ю–С–Ы –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–∞–љ—Л.
–Э–Њ—Б–Є—В–µ–ї–µ–є –≥–µ–љ–Њ—В–Є–њ–Њ–≤ S/F, F/F –Є –∞–ї–ї–µ–ї—П S —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±—А–Њ–љ—Е–Є—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –•–Ю–С–Ы –±–Њ–ї—М—И–µ, —З–µ–Љ —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Н–Љ—Д–Є–Ј–µ–Љ–∞—В–Њ–Ј–љ–Њ–є —Д–Њ—А–Љ–Њ–є –•–Ю–С–Ы, –Ї –њ–Њ—Е–Њ–ґ–Є–Љ –≤—Л–≤–Њ–і–∞–Љ –њ—А–Є—И–ї–Є M.K. Kukkonen et al. –≤ 2011 –≥.
–£–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Љ–Њ–ґ–µ—В –≤–ї–Є—П—В—М –љ–∞ –њ—А–Њ—Ж–µ—Б—Б—Л –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –Є —Н–Ї–Ј–Њ–≥–µ–љ–љ—Л—Е —Б—Г–±—Б—В—А–∞-
—В–Њ–≤ –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —А–∞–Ј–≤–Є—В–Є—О –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ.








.gif)



