Достаточно редко при жизни диагностируются «стрессовые» острые повреждения слизистой оболочки желудка или ДПК у критических больных с обострением ишемической болезни сердца (ИБС).
ЖКК у больных с сердечно–сосудистыми заболеваниями (ССЗ) составляют 11–44% от всех кровотечений из верхнего отдела желудочно–кишечного тракта и сопровождаются 50–80%–ной летальностью.
В наших исследованиях (2005 г.) острые эрозии, или язвы, желудка и ДПК, приведшие к ЖКК у больных, умерших от острого инфаркта миокарда (ОИМ) или расслоения аневризмы аорты, были выявлены в 21% случаев.
ЖКК имели место у 7% умерших больных с декомпенсацией сердечной недостаточности на фоне постинфарктного кардиосклероза и у 5% больных с острым инфарктом миокарда, у которых при аутопсии был выявлен рак.
Возраст больных с ЖКК на фоне обострения ИБС оставил 76±7,7 лет, мужчин в выборке было 54%, женщин — 46%. В структуре причин летального исхода у больных терапевтического профиля стационара скорой медицинской помощи (СМП) частота ЖКК при острых заболеваниях сердца и аорты составила 8%.
Характерно, что ЖКК у больных с острыми ишемическими заболеваниями сердца и аорты составили более 2/3 всех кровотечений из верхнего отдела ЖКТ, приведших к летальному исходу больных терапевтического профиля в стационаре СМП.
Высокий риск ЖКК у пожилых пациентов со стабильной ИБС традиционно связывают с длительным приемом антиагрегантов с целью вторичной профилактики ССЗ [М. Al–Mallah, 2007] и неконтролируемым применением НПВП для лечения сопутствующего болевого синдрома. Установлено [Taylor D.W., Barnet H.J.M. et al., 1999], что частоту ЖКК в 2–3 раза увеличивает длительный прием даже «малых» (50–100 мг) доз ацетилсалициловой кислоты (АСК). По выражению B. Cryer (2002), вероятно, нет такой дозы АСК, которая бы обладала антитромботическим эффектом и не была гастротоксичной.
Таким образом, уменьшение резистентности гастродуоденальной слизистой на фоне терапии АСК потенциально угрожает любому пациенту с ИБС, однако наиболее высоким риск ЖКК является у больных с установленными в известном исследовании ARAMIS [J.T. Fries, 1997] факторами риска НПВП–гастропатии.
Основные факторы риска развития НПВП–гастропатии [ARAMIS, J.T. Fries, 1997]:
• ЯБ в анамнезе;
• возраст старше 65 лет;
• сопутствующий прием кортикостероидов.
Отдельного внимания требует более высокий риск ЖКК у больных с обострением ИБС, на амбулаторном этапе получавших варфарин.
Важнейшими причинами развития ЖКК у больных ССЗ также являются развитие острых форм или ухудшение течения хронической ИБС, приводящие к прогрессирующему падению систолической функции сердца. Возникающая при этом острая ишемия гастродуоденальной слизистой оболочки вызывает транзиторную гиперацидность, на фоне которой развиваются острые эрозивно–язвенные поражения и риск ЖКК многократно увеличивается.
По данным аутопсий, эрозивно–язвенные гастродуоденальные поражения развиваются не менее, чем у 10% больных с первичным и у 54% с повторным инфарктом миокарда [С.В. Колобов и соавт., 2003].
Таким образом, риск ЖКК у больных ИБС является кумулятивным, включающим как острые, так и хронические ишемические поражения гастродуоденальной слизистой оболочки, а также НПВП–гастропатию.
Однако в клинической практике риск ЖКК у больных с ССЗ традиционно оценивают лишь при развитии острых форм ИБС с позиций противопоказаний для назначения терапии антикоагулянтами или антиагрегантами. При этом наиболее значимым предиктором риска ЖКК у больных ИБС считают анамнестические указания на язвенную болезнь, выявление которых повсеместно приводит к отказу от антикоагулянтной или антиагрегантной терапии.
Между тем, согласно международным клиническим рекомендациям, выявление 2 и более факторов риска ЖКК должно приводить не к отмене антиагрегантной терапии, а к замене АСК на клопидогрел или одновременному назначению ингибиторов протонной помпы (ИПП).
Однако на практике этот алгоритм оценки риска и профилактики ЖКК широко не применяется: антисекреторные препараты получают не более 5–10% больных с обострением ИБС [Cook D.J. et al. 1999; Б.Р. Гельфанд и соавт., 2005].
При развитии ЖКК у больных ИБС на практике вступает в силу алгоритм хирургического лечения, приоритетом которого является поиск показаний к оперативному лечению и поддержание жизненно–важных функций вне зависимости от коморбидного фона.
Таким образом, в хирургической клинике больные с ЖКК часто не получают адекватной терапии ИБС, при том, что фармакологическая профилактика раннего рецидива кровотечения также носит эмпирический характер.
Как уже говорилось, результаты ряда исследований, в которых показана более высокая частота развития тяжелых острых поражений гастродуоденальной слизистой оболочки у пациентов с ОИМ на фоне постинфарктного кардиосклероза, сахарного диабета, плохо контролируемой артериальной гипертонии, требует создания алгоритма рассмотрения веса фоновых заболеваний и других факторов коморбидности в аспекте анализа предикторов ЖКК при обострении ИБС. Так, при ретроспективном изучении результатов аутопсий 3008 умерших от ОИМ, было установлено, что ЖКК чаще развивается у пожилых больных с повторным ОИМ, артериальной гипертензией и сахарным диабетом. Согласно данным литературы, риск кровотечения существенно увеличивается у пожилых женщин и в тех случаях, когда больной уже переносил ЖКК, а также имеет сердечную недостаточность, анемию или уремию.
Таким образом, на практике выявление симптомов ЯБ, кислой диспепсии или эрозивно–язвенного поражения желудка и ДПК в пожилом возрасте должно приводить к определенному клинико–диагностическому поиску и рассматриваться как предиктор высокого риска ЖКК.
Факторами риска является сочетанное применение НПВП и глюкокортикостероидов (ГКС). Риск развития эрозивно–язвенных поражений ЖКТ у таких больных возрастает в 10 раз. Увеличение риска развития осложнений можно объяснить системным действием ГКС: блокируя фермент фосфолипазу–А2, они тормозят высвобождение арахидоновой кислоты из фосфолипидов клеточных мембран, что ведет к уменьшению образования простагландинов (ПГ).
Наряду с основными существует ряд сопутствующих факторов риска. Например, отмечено нарастание частоты желудочных кровотечений у пациентов, принимающих НПВП в сочетании с ингибиторами обратного захвата серотонина и, вероятно, ингибиторами кальциевых каналов.
Негативное влияние «стандартных» НПВП на функцию почек и систему кровообращения также характерно для лиц пожилого и старческого возраста, особенно страдающих заболеваниями сердечно–сосудистой системы и почек. В целом эти осложнения встречаются примерно у 1–5% пациентов и нередко требуют стационарного лечения. Риск обострения застойной сердечной недостаточности (ЗСН) у лиц, принимающих НПВП, в 10 раз выше, чем у не принимающих эти препараты. Прием НПВП удваивает риск госпитализаций, связанных с обострением ЗСН. В целом риск декомпенсации кровообращения у пожилых пациентов со «скрытой» ЗСН на фоне недавнего приема НПВП примерно такой же, как и тяжелых желудочно–кишечных осложнений.
Механизм развития язвенно–эрозивного поражения слизистой оболочки ЖКТ, возникающего на фоне приема НПВП, до конца не изучен. Основной механизм развития язв желудка и ДПК связан с блокированием синтеза ПГ НПВП. Снижение синтеза ПГ приводит к уменьшению синтеза слизи и бикарбонатов, являющихся основным защитным барьером слизистой оболочки желудка от агрессивных факторов желудочного сока. При приеме НПВП снижается уровень простациклина и оксида азота, что неблагоприятно сказывается на кровообращении в подслизистой ЖКТ и создает дополнительный риск повреждения слизистой оболочки желудка и ДПК.
Препараты этой группы обладают способностью в кислой желудочной среде непосредственно проникать в клетки слизистой оболочки, нарушая слизисто–бикарбонатный барьер и вызывая обратную диффузию ионов водорода, и оказывать таким образом прямое, «контактное» повреждающее действие на клетки покровного эпителия. В этом плане особую опасность представляют так называемые кислые НПВП.
Одним из основных моментов в патогенезе контактного действия НПВП может являться блокирование ферментных систем митохондрий эпителиоцитов, вызывающее нарушение процессов окислительного фосфорилирования и приводящее к развитию каскада некробиотических процессов в клетках. Это проявляется снижением устойчивости клеток слизистой оболочки к повреждающему действию кислоты и пепсина и уменьшению их регенераторного потенциала.
Хотя НПВП могут вызывать своеобразные изменения слизистой оболочки, соответствующие гистологической картине «химического» гастрита, в большинстве случаев эта патология маскируется проявлениями гастрита, ассоциированного с H. pylori. В отличие от H. pylori–ассоциированной язвенной болезни, при которой характерным фоном язвы является хронический активный гастрит, при НПВП–гастропатии язвы могут выявляться при минимальных изменениях слизистой оболочки.
Особенности клинической картины
ЖКК при острых эрозивно–язвенных поражениях слизистой оболочки верхних отделов ЖКТ носит характер паренхиматозного, часто развивается на 2–5 сутки после госпитализации больного в отделение интенсивной терапии и начинается бессимптомно. По данным А.С. Логинова и соавт. (1998), у 52% больных с обострением ИБС кровотечение становится первым проявлением поражения ЖКТ, которое у 68% больных развивается в течение 10 дней от начала ОИМ или аорто–коронарного шунтирования.
Большинство исследователей согласно с тем, что на деле ЖКК у критических больных происходят гораздо чаще, чем выявляются. Однако поскольку в большинстве случаев они протекают субклинически, не приводят к существенным гемодинамическим нарушениям, то и не являются актуальной клинической проблемой. В этой связи значительная часть исследователей считает, что клиническое значение острого поражения гастродуоденальной слизистой (ОПГС), не стоит преувеличивать. Этому мнению оппонируют данные С.В. Колобова и соавт. (2002), согласно которым у больных с ОИМ состоявшееся ЖКК в 30% случаев приводит к острой постгеморрагической анемии, что, как известно, в 1,5 раза увеличивает риск госпитальной смерти и в 4 раза увеличивает риск повторного массивного ЖКК.
В свою очередь, ЖКК вдвое увеличивает риск летального исхода (RR = 1–4) и удлиняет сроки лечения в отделении интенсивной терапии, в среднем на 4–8 дней.
Не связанными между собой факторами наиболее высокого риска ЖКК у критических больных, вне зависимости от основного заболевания, являются дыхательная недостаточность, коагулопатия, искусственная вентиляция легких более 48 ч.
Лечение и профилактика ЖКК
при острых поражениях
гастродуоденальной слизистой
на фоне обострения ИБС
Установлено, что антисекреторная терапия, позволяющая увеличить рН содержимого желудка до 5,0–7,0 ед. в течение периода активного влияния факторов риска, снижает вероятность ЖКК у критически больных как минимум на 50% и позволяет инициировать активную эпителизацию ОПГС. Адекватная антисекреторная терапия позволяет решить как минимум три задачи:
• прекратить активное кровотечение;
• предотвратить рецидив кровотечения;
• предотвратить ЖКК в принципе.
Антисекреторная терапия влияет на объем активного кровотечения и предотвращет его рецидивы: рН содержимого желудка устойчиво сдвигается в щелочную сторону, что блокирует лизис свежих тромбов и обеспечивает полноценный сосудисто–тромбоцитарный гемостаз. Другой механизм действия представляется особенно важным для пациентов с обострением ИБС, страдающих от нарастающего снижения сократительной способности миокарда, гипотонии и длительной ишемии гастродуоденальной слизистой. Он заключается в прекращении, при условии раннего назначения антисекреторной терапии, влияния длительной пептической агрессии на слизистую желудка и ДПК.
Доказательства необходимости как можно более раннего назначения адекватной антисекреторной терапии были получены в уже упомянутом уникальном клинико–морфологическом исследовании, проведенном С.В. Колобовым и соавт. (2003). При иммуноморфологическом исследовании авторы обнаружили, что у пациентов с ОИМ имеют место тяжелые нарушения микроциркуляции и угнетение пролиферации эпителия слизистой оболочки желудка и ДПК.
При этом продукция соляной кислоты нисколько не уменьшается и приводит к стабильному уменьшению рН содержимого желудка в острейшем периоде ОИМ.
Теоретически нейтрализации содержимого желудка можно добиться введением любых антацидов или антисекреторных препаратов: гидроокисей магния и алюминия, сукральфата, антагонистов Н2–рецепторов к гистамину (АН2–Р), ингибиторов протонной помпы (ИПП).
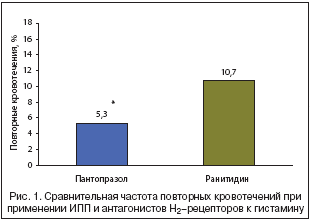
Однако на базе результатов доказательных исследований оптимальными по антисекреторной активности, быстроте развития эффекта, отсутствию толерантности, безопасности и простоте применения у больных с ЖКК были признаны ингибиторы протонной помпы (уровень доказательности А) (рис. 1).
ИПП также являются более эффективными, чем АН2–Р, при назначении для профилактики рецидива кровотечения.
Масштабное исследование Stupnicki T. и соавт. (2003) продемонстрировало преимущество пантопразола 20 мг/сут. над мизопростолом 200 мкг 2 раза/ сут. в качестве средства профилактики НПВП–ассоциированной патологии ЖКТ в ходе 6–месячного исследования (n=515): частота язв, множественных эрозий и рефлюкс–эзофагита на фоне ИПП оказалась существенно меньше, чем на фоне препарата сравнения, – 5 и 14% (р=0,005).
В отделениях интенсивной терапии и кардиореанимации только 10% больных с обострением ИБС получают антисекреторную терапию ранитидином, а ИПП чаще не назначаются.
Ингибиторы протонной помпы сегодня являются самыми мощными анти¬секреторными препаратами и при этом характеризуются безопасностью и удобством применения [Frilling B., Schiele R., Gitt A.K. et al., 2004]. Неуди¬вительно, что их высокая эффективность была продемонстрирована как в плацебоконтролируемых ис¬следованиях, так и в многоцентровых сравнительных исследованиях с мизопростолом и блокаторами Н2–гистаминовых рецепторов. По заключению международной группы экспертов, «...основой эффективности ИПН при повреждениях гастродуоденальной слизистой оболочки под действием НПВП является выраженное подавление желудочной секреции...» [Karen P. Alexander, Matthew T. Roe, Anita Y. Chen et al., 2005], т.е. чем сильнее подавлена желудочная секреция, тем выше профилактический и ле¬чебный эффект антисекреторного средства.
Целесообразность применения ИПП в комплексном лечении больных связана со следующими основными особенностями действия этих препаратов:
1) ИПП обладают высокой липофильностью, легко проникают в париетальные клетки слизистой оболочки желудка, где накапливаются и активируются при кислом значении рН;
2) ИПП ингибируют Н+–, К+–АТФазу секреторной мембраны париетальных клеток («протонный насос»), прекращая выход ионов водорода в полость желудка и блокируя заключительную стадию секреции соляной кислоты, тем самым снижая уровень базальной, но в основном стимулированной секреции соляной кислоты. После однократного приема одного из ИПП угнетение желудочной секреции отмечается в течение первого часа, достигая максимума через 2–3 ч. После лечения способность париетальных клеток слизистой оболочки желудка продуцировать выделение соляной кислоты восстанавливается через 3–4 суток после отмены препарата.
Показания к применению ИПП в комплексном лечении больных ИБС и инфарктом миокарда с профилактическими целями: для уменьшения вероятности появления кровотечений у больных, которым проводится тромболитическая терапия; для предотвращения появления язв желудка и двенадцатиперстной кишки у больных, имевших в анамнезе язвенную болезнь, а также язвы другой этиологии (например, язвы, ассоциированные с НПВП, включая АСК, и т.д.), а также для предупреждения возможных кровотечений из этих язв; для предотвращения появления в желудочно–кишечном тракте эрозий и возникновения кровотечений; для устранения клинических симптомов, рассматриваемых в качестве характерных для ГЭРБ и язвенной болезни; в комплексном лечении больных инфарктом миокарда после остановки кровотечений.
В настоящее время на отечественном фармацевтическом рынке существует как минимум пять представителей класса ингибиторов протонной помпы: омепразол, эзомепразол, лансопразол, рабепразол, пантопразол.
Эффективность всех препаратов продемонстрирована в РКИ, доказана их безопасность. Однако фармакологическая активность, связанная с особенностями фармакокинетики, а следовательно и эффективность варьирует у разных представителей этой группы лекарственных препаратов.
Выбор ингибиторов протонной помпы в клинической практике
ИПП имеют единый механизм действия, сравнимый по клиническому эффекту, но различаются по скорости и особенностям активации в зависимости от внутриклеточного рН (так называемая рН–селективность), продолжительности и выраженности кислотоснижающего эффекта, особенностям метаболизма в системе цитохрома Р450, побочным эффектам и профилю безопасности.
Наилучшие результаты по переносимости среди ИПП показывает пантопразол: при его приеме незначительные побочные эффекты зафиксированы только у 1,1% пациентов.
Пантопразол (Контролок) снижает уровень базальной и стимулированной (независимо от вида раздражителя) секреции соляной кислоты в желудке. Известно, что пантопразол, единственный из всех ИПП, вызывает необратимую блокаду протонной помпы, а не временное прерывание химической связи, при этом кислотность восстанавливается за счет синтеза новых протонных помп. Тем не менее подавление секреции соляной кислоты сохраняется примерно в течение 3 суток. Это обусловлено достижением определенного баланса между количеством вновь синтезируемых молекул протонных помп и количеством уже ингибированных молекул. Единичная доза пантопразола внутривенно обеспечивает быструю (в течение 1 ч) дозозависимую ингибицию кислотной продукции: при введении 40 мг кислотная продукция уменьшается на 86%, 60 мг – на 98%, 80 мг – на 99%, причем уменьшается не только кислотная продукция, но и объем желудочной секреции. После внутривенного введения стандартной дозы пантопразола в 80 мг через 12 ч степень снижения кислотности составляет 95%, а через 24 ч – 79%. Поэтому время для возобновления исходной кислотопродукции составляет для ланзопразола около 15 ч, для омепразола и рабепразола – около 30 ч, для пантопразола – примерно 46 ч. Т.е. пантопразол имеет дополнительное преимущество в виде наиболее продолжительного кислотоснижающего эффекта.
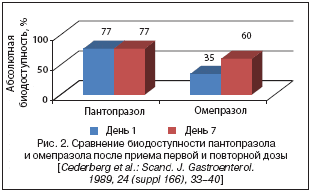
Пантопразол обладает постоянной линейной предсказуемой фармакокинетикой (рис. 2). При удвоении дозы ИПП, имеющих нелинейную фармакокинетику, их концентрация в сыворотке крови будет либо ниже, либо выше ожидаемой, т.е. она непредсказуема. Это может привести к неадекватному контролю секреции кислоты или оказать влияние на безопасность использования препарата.
Кроме того, пантопразол, в отличие от других ИПП, имеет наиболее низкую аффинность к печеночной цитохром–Р450–ферментной системе. При одновременном применении нескольких препаратов, метаболизирующихся цитохромом Р450, их эффективность может меняться. Пантопразол не влияет на активность цитохрома Р450, поэтому не дает клинически значимых перекрестных реакций с другими лекарственными средствами. Это значительно расширяет область его применения с достижением хорошего профиля безопасности.
Дополнительным преимуществом данного препарата является наличие пероральной и парентеральной формы, позволяющие обеспечить преемственность терапии.
Таким образом, при наличии высокого риска эрозивно–язвенного поражения слизистой оболочки верхних отделов ЖКТ необходимо немедленное назначение ингибиторов протонной помпы, среди которых пантопразол имеет ряд преимуществ. Высокая эффективность, линейная фармакокинетика, отсутствие взаимодействия с другими лекарствами и, в свою очередь, отсутствие реакций полипрагмазии делают пантопразол универсальным ингибитором протонной помпы в неотложной медицине.