–°–Њ–і–µ—А–ґ–Є–Љ–Њ–µ –ґ–µ–ї—Г–і–Ї–∞ —Б–Њ–і–µ—А–ґ–Є—В –Ї–Є—Б–ї–Њ—В—Г –Є –µ–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П —Б –і—А—Г–≥–Є–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є, —В–∞–Ї–Є–Љ–Є –Ї–∞–Ї –њ–µ–њ—Б–Є–љ—Л –Є –ґ–µ–ї—З—М, –Ї–Њ—В–Њ—А—Л–µ, –Ї–∞–Ї —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, –≤—Л–Ј—Л–≤–∞—О—В –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –њ–Є—Й–µ–≤–Њ–і–∞ [10]. –Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ї–Є—Б–ї–Њ—В–љ–Њ—Б—В–Є –≤ –њ–Є—Й–µ–≤–Њ–і–µ –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –≤–љ—Г—В—А–Є–њ–Є—Й–µ–≤–Њ–і–љ–Њ–≥–Њ —А–Э––Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ –њ—А–Є–µ–Љ–ї–µ–Љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —А–µ—Д–ї—О–Ї—Б–∞ [11]. –Ъ–Є—Б–ї–Њ—В–љ–∞—П —Б—А–µ–і–∞, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –Ј–љ–∞—З–µ–љ–Є–µ —А–Э –≤ –њ–Є—Й–µ–≤–Њ–і–µ <4, —Б—З–Є—В–∞–µ—В—Б—П –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є–Љ —Г—Б–ї–Њ–≤–Є–µ–Љ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ—А–Є —Н—В–Њ–Љ –ґ–µ–ї—Г–і–Њ—З–љ—Л–µ –њ—А–Њ—В–µ–∞–Ј—Л (–њ–µ–њ—Б–Є–љ—Л) —Б—В–∞–љ–Њ–≤—П—В—Б—П –±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–љ—Л–Љ–Є. –Ґ–∞–Ї–ґ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Љ–љ–µ–љ–Є–µ, —З—В–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Є–Ј –њ–µ–њ—Б–Є–љ–Њ–≤ –Љ–Њ–≥—Г—В –±—Л—В—М –∞–Ї—В–Є–≤–љ—Л –њ—А–Є —А–Э –і–Њ 6 –Є –Њ—Б—В–∞—О—В—Б—П —Б—В–∞–±–Є–ї—М–љ—Л–Љ–Є –і–Њ –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ–є –і–µ–љ–∞—В—Г—А–∞—Ж–Є–Є –њ—А–Є pH –≤—Л—И–µ 7 [12,13]. –Т –Њ—Б–љ–Њ–≤–љ–Њ–Љ –љ–Є–ґ–љ–Є–µ –Њ—В–і–µ–ї—Л –њ–Є—Й–µ–≤–Њ–і–∞ –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О —А–µ—Д–ї—О–Ї—Б–∞ –Ї–Є—Б–ї—Л–Љ —Б–Њ–і–µ—А–ґ–Є–Љ—Л–Љ –ґ–µ–ї—Г–і–Ї–∞, –њ–Њ—Н—В–Њ–Љ—Г –Њ–±—Л—З–љ–Њ pH––њ—А–Њ–±–∞ —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П –љ–∞ 5 —Б–Љ –≤—Л—И–µ –љ–Є–ґ–љ–µ–≥–Њ –њ–Є—Й–µ–≤–Њ–і–љ–Њ–≥–Њ —Б—Д–Є–љ–Ї—В–µ—А–∞ (–Э–Я–°) –Є –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—Б—П –Є–Ј–Љ–µ—А–µ–љ–Є–µ –≤–µ–ї–Є—З–Є–љ—Л –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П (–њ—А–Њ—Ж–µ–љ—В –≤—А–µ–Љ–µ–љ–Є, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є–µ —А–Э –љ–Є–ґ–µ 4 –Є–ї–Є 5).
–У–ї–∞–≤–љ–Њ–є —Ж–µ–ї—М—О –і–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–ї—П–ї–Њ—Б—М —Б—А–∞–≤–љ–µ–љ–Є–µ –і–≤—Г—Е –∞–ї—М–≥–Є–љ–∞—В–љ—Л—Е —Б—А–µ–і—Б—В–≤ –і–ї—П –њ–Њ–і–∞–≤–ї–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–∞, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–Ї—В–Є–≤–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤, –љ–Њ –≤ —А–∞–Ј–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Д–Њ—А–Љ–∞—Е (—Б—Г—Б–њ–µ–љ–Ј–Є—П –Є —В–∞–±–ї–µ—В–Ї–Є). –Ф–∞–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–∞, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ —А–µ—Д–ї—О–Ї—Б–Њ–≥–µ–љ–љ–Њ–є –њ–Є—Й–µ–є, —Г –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤. –Ю—Ж–µ–љ–Ї–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –њ—А–Є –њ–Њ–Љ–Њ—Й–Є —А–Э––Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥–∞. –Р–ї—М–≥–Є–љ–∞–љ—В–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –і–ї—П –њ–Њ–і–∞–≤–ї–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–∞ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –і–ї—П —В–µ—А–∞–њ–Є–Є –У–≠–†–С –≤–Њ—В —Г–ґ–µ –±–Њ–ї–µ–µ 30 –ї–µ—В, –љ–Њ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—В—А–∞–љ–∞—Е –≤ –њ—А–Њ–і–∞–ґ–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —А–∞–Ј–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Д–Њ—А–Љ—Л [14,15] —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П–Љ–Є –∞–ї—М–≥–Є–љ–∞—В–∞ –Є –∞–љ—В–∞—Ж–Є–і–љ—Л—Е –∞–Ї—В–Є–≤–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤. –£–і–Є–≤–Є—В–µ–ї—М–љ–Њ, –љ–Њ –і–Њ –љ–µ–і–∞–≤–љ–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є —В–∞–±–ї–µ—В–Ї–Є –Є –ґ–Є–і–Ї–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Д–Њ—А–Љ—Л –∞–ї—М–≥–Є–љ–∞—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–µ —Б–Њ–і–µ—А–ґ–∞–ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –∞–Ї—В–Є–≤–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤. –Ґ–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ—Л–µ —Д–Њ—А–Љ—Л –Њ–±—Л—З–љ–Њ –±—Л–ї–Є –Њ—Б–љ–Њ–≤–∞–љ—Л –љ–∞ –љ–µ—А–∞—Б—В–≤–Њ—А–Є–Љ–Њ–є –∞–ї—М–≥–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–µ, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ —Б–Њ—Б—В–∞–≤ –ґ–Є–і–Ї–Є—Е —Д–Њ—А–Љ –≤—Е–Њ–і–Є–ї–Є —А–∞—Б—В–≤–Њ—А–Є–Љ—Л–µ —Б–Њ–ї–Є –∞–ї—М–≥–Є–љ–∞—В–∞. –≠—В–Њ –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –∞–ї—М–≥–Є–љ–∞—В–љ—Л–є –њ–ї–Њ—В, –Ї–Њ—В–Њ—А—Л–є –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В —А–µ—Д–ї—О–Ї—Б, –Њ–±—Л—З–љ–Њ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –≤–Њ —А—В—Г –њ—А–Є —А–∞–Ј–ґ–µ–≤—Л–≤–∞–љ–Є–Є —В–∞–±–ї–µ—В–Њ–Ї, —В–Њ–≥–і–∞ –Ї–∞–Ї –≤ —Б–ї—Г—З–∞–µ –ґ–Є–і–Ї–Є—Е —Б–Њ—Б—В–∞–≤–Њ–≤ —Н—В–Њ—В –њ–ї–Њ—В —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Ї–Є—Б–ї–Њ—В—Л –≤ –ґ–µ–ї—Г–і–Ї–µ. –Ґ–µ–њ–µ—А—М —Б—Г—Й–µ—Б—В–≤—Г–µ—В –љ–Њ–≤–∞—П –∞–ї—М–≥–Є–љ–∞—В–љ–∞—П —Д–Њ—А–Љ–∞ – —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–∞—П, –≤ –Ї–Њ—В–Њ—А–Њ–є —Б–Њ–і–µ—А–ґ–∞—В—Б—П —В–µ –ґ–µ –∞–Ї—В–Є–≤–љ—Л–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л (–љ–∞—В—А–Є—П –∞–ї—М–≥–Є–љ–∞—В –Є –Ї–∞–ї–Є—П –±–Є–Ї–∞—А–±–Њ–љ–∞—В), —З—В–Њ –Є –≤ –ґ–Є–і–Ї–Њ–є —Д–Њ—А–Љ–µ – –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ («–†–µ–Ї–Є—В—В –С–µ–љ–Ї–Є–Ј–µ—А –•—Н–ї—Б–Ї–µ—А», –•–∞–ї–ї, –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є—П).
–Ф–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —П–≤–ї—П–µ—В—Б—П –њ–µ—А–≤—Л–Љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –∞–ї—М–≥–Є–љ–∞—В–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –≤ —В–≤–µ—А–і–Њ–є –Є –ґ–Є–і–Ї–Њ–є —Д–Њ—А–Љ–∞—Е. –Э–µ–і–∞–≤–љ–Њ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –ґ–Є–і–Ї–Њ–≥–Њ –∞–ї—М–≥–Є–љ–∞—В–∞, —А–∞–љ–Є—В–Є–і–Є–љ–∞ –Є –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–∞ –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –Ї–Њ–љ—В—А–Њ–ї—П —А–Э –њ–Є—Й–µ–≤–Њ–і–∞ [16], —Ж–µ–ї—М—О –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П–ї–Њ—Б—М —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–Є–є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–∞—З–∞–ї–∞ –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Є —Н–њ–Є–Ј–Њ–і–∞–Љ–Є —А–µ—Д–ї—О–Ї—Б–∞. –¶–µ–ї—М—О –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б—В–∞–ї–Њ –≤—Л—П–≤–ї–µ–љ–Є–µ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–Њ–≤–Њ–є —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є –∞–ї—М–≥–Є–љ–∞—В–љ–Њ–є —Д–Њ—А–Љ—Л –љ–∞ —Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ—Л–є —А–µ—Д–ї—О–Ї—Б –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ґ–Є–і–Ї–Њ–є —Д–Њ—А–Љ–Њ–є – –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –і–ї—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —П–≤–ї—П–µ—В—Б—П —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ, –Ї–Њ–≥–і–∞ —В—А–µ–±—Г–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞—В—М –љ–µ –Љ–µ–љ—М—И—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Б—Г—Й–µ—Б—В–≤—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–µ–є, –∞ –љ–µ –њ—А–µ–≤–Њ—Б—Е–Њ–і—Б—В–≤–Њ –Њ–і–љ–Њ–є –љ–∞–і –і—А—Г–≥–Њ–є [17]. –≠–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ—Л–є —А–µ—Д–ї—О–Ї—Б – –Њ–±—Л—З–љ–Њ–µ —П–≤–ї–µ–љ–Є–µ, —А–µ–≥—Г–ї—П—А–љ–Њ –њ—А–Њ–Є—Б—Е–Њ–і—П—Й–µ–µ —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ—Б–ї–µ –µ–і—Л [18]. –І–∞—Б—В–Њ—В–∞ –Є —В—П–ґ–µ—Б—В—М —Н–њ–Є–Ј–Њ–і–Њ–≤ –Љ–Њ–≥—Г—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –і–∞–ґ–µ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л –і–ї—П –і–µ–Љ–Њ–љ—Б—В—А–∞—Ж–Є–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –∞–ї—М–≥–Є–љ–∞—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ —Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ—Л–є —А–µ—Д–ї—О–Ї—Б –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≤–Њ–і–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л–Љ –Њ–±—А–∞–Ј—Ж–Њ–Љ –±–µ–Ј –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ—В–±–Њ—А–∞ —Б—Г–±—К–µ–Ї—В–Њ–≤ —Б –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є —Б—В–µ–њ–µ–љ—М—О –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П [19].
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–Ф–Є–Ј–∞–є–љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –Њ–і–Њ–±—А–µ–љ–Є–µ
—Н—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–Є—В–µ—В–∞
–Ф–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ – –Њ–і–љ–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ, —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ, –Њ—В–Ї—А—Л—В–Њ–µ, —В—А–µ—Е–њ–µ—А–Є–Њ–і–љ–Њ–µ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–µ, —Б —Г—З–∞—Б—В–Є–µ–Љ –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ –њ–Њ –Э–∞–і–ї–µ–ґ–∞—Й–µ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Є –•–µ–ї—М—Б–Є–љ–Ї—Б–Ї–Њ–є –і–µ–Ї–ї–∞—А–∞—Ж–Є–µ–є. –Я–µ—А–µ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –≤—Б–µ —Б—Г–±—К–µ–Ї—В—Л –њ–Њ–і–њ–Є—Б–∞–ї–Є –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ —Б–Њ–≥–ї–∞—Б–Є–µ. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ —Б —Г—З–∞—Б—В–Є–µ–Љ –†–Є—З–Љ–Њ–љ–і –§–∞—А–Љ–∞–Ї–Њ–ї–Њ–і–ґ–Є –Ы—В–і., –£–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ –°–≤.–У–µ–Њ—А–≥–Є—П, –Ы–Њ–љ–і–Њ–љ, –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є—П. –†–∞–Ј—А–µ—И–µ–љ–Є–µ –Њ —Б–Њ–±–ї—О–і–µ–љ–Є–Є —Н—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–љ—Ж–Є–њ–Њ–≤ –±—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ –Њ—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ –Э–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ —Н—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–Є—В–µ—В–∞ (–≠—В–Є—З–µ—Б–Ї–Є–є –Ї–Њ–Љ–Є—В–µ—В –≤ –†—Н–є–≤–µ–љ—Б–Ї–Њ—А—В, –≠—И—Д–Њ—А–і –У–Њ—Б–њ–Є—В–∞–ї—М, –≠—И—Д–Њ—А–і, –Ь–Є–і–ї—Б–µ–Ї—Б, –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є—П).
–Ш—Б—Б–ї–µ–і—Г–µ–Љ–∞—П –њ–Њ–њ—Г–ї—П—Ж–Є—П
–С—Л–ї–Є –Њ—В–Њ–±—А–∞–љ—Л –Ј–і–Њ—А–Њ–≤—Л–µ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л, —В.–Ї. –і–ї—П —Г—З–∞—Б—В–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–µ —В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –љ–∞–ї–Є—З–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ъ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –і–Њ–њ—Г—Б–Ї–∞–ї–Є—Б—М –ї–Є—Ж–∞ –Љ—Г–ґ—Б–Ї–Њ–≥–Њ –Є –ґ–µ–љ—Б–Ї–Њ–≥–Њ –њ–Њ–ї–∞ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 18 –і–Њ 65 –ї–µ—В, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П pH –≤ –њ–Є—Й–µ–≤–Њ–і–µ <4 –≤ —В–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–µ 2% –Њ—В 4–—З–∞—Б–Њ–≤–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –≤—А–µ–Љ–µ–љ–Є –≤ —Е–Њ–і–µ —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —А–µ—Д–ї—О–Ї—Б–∞.
–С—Л–ї–Є –Њ—В–Њ–±—А–∞–љ—Л –Ј–і–Њ—А–Њ–≤—Л–µ –њ–∞—Ж–Є–µ–љ—В—Л —Б —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–Љ–Є –і–∞–љ–љ—Л–Љ–Є –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Њ—Б–Љ–Њ—В—А–∞, –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, –±–Є–Њ—Е–Є–Љ–Є–Є –Є —Н–ї–µ–Ї—В—А–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞–Љ–Љ—Л –≤–Њ –≤—А–µ–Љ—П –љ–∞—З–∞–ї—М–љ–Њ–≥–Њ –Њ—Б–Љ–Њ—В—А–∞. –Ъ—А–Є—В–µ—А–Є–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П: –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М –Є–ї–Є –ї–∞–Ї—В–∞—Ж–Є—П; –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–µ, —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–µ, –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ, –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–µ, –њ–Њ—З–µ—З–љ–Њ–µ, –њ–µ—З–µ–љ–Њ—З–љ–Њ–µ, —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–µ, —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–µ, —Н–љ–і–Њ–Ї—А–Є–љ–љ–Њ–µ –Є–ї–Є –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ; –њ—А–Є–µ–Љ –≤–Є—В–∞–Љ–Є–љ–љ—Л—Е –і–Њ–±–∞–≤–Њ–Ї –≤ —В–µ—З–µ–љ–Є–µ –њ—А–µ–і—Л–і—Г—Й–Є—Е 48 —З–∞—Б–Њ–≤, —Б–∞–Љ–Њ–ї–µ—З–µ–љ–Є–µ –≤ —В–µ—З–µ–љ–Є–µ –њ—А–µ–і—Л–і—Г—Й–Є—Е 7 –і–љ–µ–є –Є–ї–Є –њ—А–Є–µ–Љ –њ—А–Њ–њ–Є—Б–∞–љ–љ—Л—Е –≤—А–∞—З–Њ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Ї—А–Њ–Љ–µ —Б—А–µ–і—Б—В–≤ –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є) –≤ —В–µ—З–µ–љ–Є–µ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є—Е 14 –і–љ–µ–є –њ–µ—А–µ–і –љ–∞—З–∞–ї—М–љ—Л–Љ –Њ—Б–Љ–Њ—В—А–Њ–Љ; –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є—П –≤ —В–µ—З–µ–љ–Є–µ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є—Е 3 –Љ–µ—Б—П—Ж–µ–≤ –Є–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –≤ —В–µ—З–µ–љ–Є–µ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є—Е 4 –љ–µ–і–µ–ї—М; –∞–ї–Ї–Њ–≥–Њ–ї–Є–Ј–Љ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ; –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –∞–ї—М–≥–Є–љ–∞—В–∞–Љ –Є–ї–Є –≤—Б–њ–Њ–Љ–Њ–≥–∞—В–µ–ї—М–љ—Л–Љ –≤–µ—Й–µ—Б—В–≤–∞–Љ, –≤—Е–Њ–і—П—Й–Є–Љ –≤ —Б–Њ—Б—В–∞–≤ –њ—А–µ–њ–∞—А–∞—В–∞; —Г—З–∞—Б—В–Є–µ –≤ –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ –њ—А–µ–і—Л–і—Г—Й–Є—Е 3 –Љ–µ—Б—П—Ж–µ–≤.
–Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П —В–µ—А–∞–њ–Є—П
–Є –њ—А–Њ—Ж–µ–і—Г—А–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Ф–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л –њ–Њ–ї—Г—З–∞–ї–Є –Њ–і–љ–Њ–Ї—А–∞—В–љ—Г—О –і–Њ–Ј—Г –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј —В—А–µ—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —Б–ї—Г—З–∞–є–љ–Њ–Љ –њ–Њ—А—П–і–Ї–µ, –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–Њ–Љ. –†–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є—О –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤ –≥—А—Г–њ–њ–∞—Е –Є–Ј —И–µ—Б—В–Є –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –≤—Б–µ–≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –њ–µ—А–µ—Б—В–∞–љ–Њ–≤–Њ–Ї —В—А–µ—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ґ–µ—А–∞–њ–Є—П –≤–Ї–ї—О—З–∞–ї–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ 10 –Љ–ї —Б—Г—Б–њ–µ–љ–Ј–Є–Є –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ, –і–≤—Г—Е —В–∞–±–ї–µ—В–Њ–Ї –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ –і–ї—П —А–∞–Ј–ґ–µ–≤—Л–≤–∞–љ–Є—П —Б 10 –Љ–ї –≤–Њ–і—Л –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Є –Ї–Њ–љ—В—А–Њ–ї—П – 10 –Љ–ї –≤–Њ–і—Л. –°—Г—Б–њ–µ–љ–Ј–Є–Є –Є —В–∞–±–ї–µ—В–Ї–Є –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–Ї—В–Є–≤–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Б–Њ–і–µ—А–ґ–∞–ї–Є 1000 –Љ–≥ –љ–∞—В—А–Є—П –∞–ї—М–≥–Є–љ–∞—В–∞ –Є 200 –Љ–≥ –Ї–∞–ї–Є—П –±–Є–Ї–∞—А–±–Њ–љ–∞—В–∞.
–Я–∞—Ж–Є–µ–љ—В—Л –њ–Њ—Б–µ—Й–∞–ї–Є —Ж–µ–љ—В—А –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–ї—П —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —А–µ—Д–ї—О–Ї—Б–∞ –≤ —В–µ—З–µ–љ–Є–µ 14 –і–љ–µ–є –њ–Њ—Б–ї–µ –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –Њ—Б–Љ–Њ—В—А–∞ –Є –њ—А–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А–µ—Д–ї—О–Ї—Б–∞ –≤ —В–µ—З–µ–љ–Є–µ 3–21 –і–љ–µ–є –і–Њ–ї–ґ–љ—Л –±—Л–ї–Є —П–≤–ї—П—В—М—Б—П –љ–∞ –Њ—Б–Љ–Њ—В—А –Є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —В—А–Є —А–∞–Ј–∞ –њ–µ—А–µ–љ–Њ—З–µ–≤–∞—В—М –≤ —Ж–µ–љ—В—А–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –∞–ї—М–≥–Є–љ–∞—В—Л –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –Њ—А–≥–∞–љ–Є–Ј–Љ, –±—Л–ї–Њ —А–µ—И–µ–љ–Њ, —З—В–Њ –њ–µ—А–Є–Њ–і –≤—Л–Љ—Л–≤–∞–љ–Є—П, —А–∞–≤–љ—Л–є –њ—А–Є–Љ–µ—А–љ–Њ 24 —З–∞—Б–∞–Љ, –±—Г–і–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ –і–ї—П –≥–∞—А–∞–љ—В–Є–Є –Њ—В—Б—Г—В—Б—В–≤–Є—П –њ–µ—А–µ–љ–µ—Б–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Б –Њ–і–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –љ–∞ –і—А—Г–≥–Њ–є.
–Т —Е–Њ–і–µ –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤–Њ–≥–Њ –њ–Њ—Б–µ—Й–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В—Л –њ—А–Њ—Е–Њ–і–Є–ї–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤–Ї–ї—О—З–∞–≤—И–µ–µ –њ—А–Њ—Б–Љ–Њ—В—А –Є—Б—В–Њ—А–Є–Є –±–Њ–ї–µ–Ј–љ–Є, –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї, –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–є –Њ—Б–Љ–Њ—В—А, —В–µ—Б—В –љ–∞ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М (–ґ–µ–љ—Й–Є–љ—Л), –њ—А–Њ–≤–µ—А–Ї—Г –љ–∞ —В–µ–Ї—Г—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –£ —Б—Г–±—К–µ–Ї—В–Њ–≤ –±—А–∞–ї–Є –Ї—А–Њ–≤—М –і–ї—П –∞–љ–∞–ї–Є–Ј–∞ –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Є –∞–љ–∞–ї–Є–Ј–∞ –љ–∞ –≤–Є—А—Г—Б–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –∞ —В–∞–Ї–ґ–µ –њ—А–Њ–±—Г –Љ–Њ—З–Є –і–ї—П –Њ–±—Й–µ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –Є –∞–љ–∞–ї–Є–Ј–∞ –љ–∞ –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –≤–µ—Й–µ—Б—В–≤–∞. –С—Л–ї–Є —Б–і–µ–ї–∞–љ—Л —Н–ї–µ–Ї—В—А–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞–Љ–Љ—Л –Є –≤–Ј—П—В—Л –њ—А–Њ–±—Л –љ–∞ –∞–ї–Ї–Њ–≥–Њ–ї—М –≤ –≤—Л–і—Л—Е–∞–µ–Љ–Њ–Љ –≤–Њ–Ј–і—Г—Е–µ.
–Т —Е–Њ–і–µ –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤–Њ–≥–Њ –њ–Њ—Б–µ—Й–µ–љ–Є—П –њ–Њ—Б–ї–µ –≥–Њ–ї–Њ–і–∞–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ –љ–µ –Љ–µ–љ–µ–µ 4 —З–∞—Б–Њ–≤ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є—П –Э–Я–° –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –Љ–∞–љ–Њ–Љ–µ—В—А–Є–Є –Є —А–Э––њ—А–Њ–±—Л, –≤–≤–Њ–і–Є–Љ–Њ–є —З–µ—А–µ–Ј –љ–Њ—Б –≤ –ґ–µ–ї—Г–і–Њ–Ї —Б 50 –Љ–ї –≤–Њ–і—Л –Є —А–∞—Б–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–є –љ–∞ 5 —Б–Љ –≤—Л—И–µ –Э–Я–°. –†–∞—Б—Б—В–Њ—П–љ–Є–µ –Њ—В –Ї–Њ–љ—Ж–∞ –Ј–Њ–љ–і–∞ —А–Э––Љ–µ—В—А–∞ –і–Њ –љ–Њ—Б–∞ –Ј–∞–њ–Є—Б—Л–≤–∞–ї–Є –і–ї—П –њ—А–∞–≤–Є–ї—М–љ–Њ–є –њ–Њ–≤—В–Њ—А–љ–Њ–є —Г—Б—В–∞–љ–Њ–≤–Ї–Є —А–Э––Љ–µ—В—А–∞ –≤ –і–µ–љ—М –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞. –Ч–Њ–љ–і —А–Э––Љ–µ—В—А–∞ —Б–Њ–µ–і–Є–љ—П–ї–Є —Б —Б–Є—Б—В–µ–Љ–Њ–є –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П —А–Э Flexilog 2020 (Oakfield Instruments, –£–Є—В–љ–Є, –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є—П). –Ч–∞—В–µ–Љ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л –њ–Њ—В—А–µ–±–ї—П–ї–Є —Б—В–∞–љ–і–∞—А—В–љ—Г—О –њ–Є—Й—Г –і–ї—П –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Є —А–µ—Д–ї—О–Ї—Б–∞ –Є —З–µ—А–µ–Ј 30 –Љ–Є–љ—Г—В –њ–Њ—Б–ї–µ –њ—А–Є–љ—П—В–Є—П –њ–Є—Й–Є –њ–Њ–ї—Г—З–∞–ї–Є 10 –Љ–ї –љ–µ–Њ—Е–ї–∞–ґ–і–µ–љ–љ–Њ–є –≤–Њ–і—Л. –Ч–љ–∞—З–µ–љ–Є–µ —А–Э –њ–Є—Й–µ–≤–Њ–і–∞ —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є –Ї–∞–ґ–і—Л–µ 6 —Б–µ–Ї—Г–љ–і –≤ —В–µ—З–µ–љ–Є–µ 4 —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –≤–Њ–і—Л. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –Ј–љ–∞—З–µ–љ–Є—П —А–Э –±—Л–ї–Є –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є—П –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞ —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ –Ї —Г—З–∞—Б—В–Є—О –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є (pH<4 –≤ —В–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–µ 2% –Њ—В –њ–µ—А–Є–Њ–і–∞ –Є–Ј–Љ–µ—А–µ–љ–Є—П).
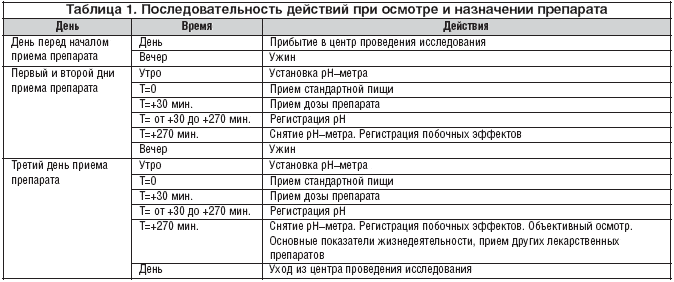
–Т–Њ –≤—А–µ–Љ—П –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ—В–Њ–±—А–∞–љ–љ—Л–µ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л –і–Њ–ї–ґ–љ—Л –±—Л–ї–Є –љ–∞—Е–Њ–і–Є—В—М—Б—П –≤ —Ж–µ–љ—В—А–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ —В—А–µ—Е –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ—Л—Е –і–љ–µ–є –Є –љ–Њ—З–µ–є. –Ф–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л —Г–ґ–Є–љ–∞–ї–Є –≤ –і–µ–љ—М –і–Њ –њ–µ—А–≤–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Є –≤ —В–µ—З–µ–љ–Є–µ —Б–ї–µ–і—Г—О—Й–Є—Е –і–≤—Г—Е –і–љ–µ–є –њ—А–Є–µ–Љ–∞, –љ–Њ –Ї–∞–ґ–і—Л–є —А–∞–Ј –≤–Њ –≤—А–µ–Љ—П –Є–Ј–Љ–µ—А–µ–љ–Є—П —А–Э –Є–Љ –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–ї–Њ—Б—М —Г–њ–Њ—В—А–µ–±–ї—П—В—М –љ–Є—З–µ–≥–Њ, –Ї—А–Њ–Љ–µ –≤—Л–і–∞–≤–∞–µ–Љ–Њ–є –њ–Є—Й–Є –Є –≤–Њ–і—Л. –Т –і–µ–љ—М –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Г—З–∞—Б—В–љ–Є–Ї–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г—В—А–Њ–Љ –≤–≤–Њ–і–Є–ї–Є –Ї–∞–ї–Є–±—А–Њ–≤–∞–љ–љ—Л–є —А–Э––Љ–µ—В—А –і–Њ —Г—А–Њ–≤–љ—П –љ–∞ 5 —Б–Љ –≤—Л—И–µ –Э–Я–°. –Ф–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л –њ–Њ—В—А–µ–±–ї—П–ї–Є —Б—В–∞–љ–і–∞—А—В–љ—Г—О –њ–Є—Й—Г –Є —З–µ—А–µ–Ј 30 –Љ–Є–љ—Г—В –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є –њ–Њ–ї—Г—З–∞–ї–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Г—О –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞ (—В–∞–±–ї–µ—В–Ї–Є –Ј–∞–њ–Є–≤–∞–ї–Є 10 –Љ–ї –љ–µ–Њ—Е–ї–∞–ґ–і–µ–љ–љ–Њ–є –≤–Њ–і—Л). –Ч–љ–∞—З–µ–љ–Є–µ —А–Э –≤ –њ–Є—Й–µ–≤–Њ–і–µ —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є –Ї–∞–ґ–і—Л–µ 6 —Б–µ–Ї—Г–љ–і –≤ —В–µ—З–µ–љ–Є–µ 4 —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –Я–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –Ј–∞–њ–Є—Б–Є –Ј–љ–∞—З–µ–љ–Є–є —А–Э––Љ–µ—В—А –≤—Л–љ–Є–Љ–∞–ї–Є –Є–Ј –њ–Є—Й–µ–≤–Њ–і–∞ –Є –Ј–∞–њ–Є—Б—Л–≤–∞–ї–Є –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, –µ—Б–ї–Є —В–∞–Ї–Њ–≤—Л–µ –љ–∞–±–ї—О–і–∞–ї–Є—Б—М. –Т –Ї–Њ–љ—Ж–µ —В—А–µ—В—М–µ–≥–Њ –і–љ—П –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Њ–≤–Њ–і–Є–ї–Є –љ–µ–±–Њ–ї—М—И–Њ–є –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–є –Њ—Б–Љ–Њ—В—А –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –і–ї—П –Њ—Ж–µ–љ–Ї–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ґ–Є–Ј–љ–µ–і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є, —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–≥–Њ –ї–µ—З–µ–љ–Є—П, –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ц–µ–љ—Й–Є–љ–∞–Љ –њ—А–Њ–≤–Њ–і–Є–ї—Б—П —В–µ—Б—В –љ–∞ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М. –Т —В–∞–±–ї–Є—Ж–µ 1 –њ–Њ–Ї–∞–Ј–∞–љ–∞ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М –Њ—Б–Љ–Њ—В—А–∞ –Ї–∞–ґ–і–Њ–≥–Њ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞ –≤–Њ –≤—А–µ–Љ—П –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞.
–Ъ–∞–ї–Є–±—А–Њ–≤–∞–љ–Є–µ —А–Э––Љ–µ—В—А–∞
–Ъ–∞–ґ–і—Л–є —А–Э––Љ–µ—В—А –Ї–∞–ї–Є–±—А–Њ–≤–∞–ї–Є –µ–ґ–µ–і–љ–µ–≤–љ–Њ –і–Њ –Є –њ–Њ—Б–ї–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤ –±—Г—Д–µ—А–љ–Њ–Љ —А–∞—Б—В–≤–Њ—А–µ —Б —А–Э 1,07 –Є 7,01 –њ—А–Є 37°C —Б–Њ–≥–ї–∞—Б–љ–Њ —Г–Ї–∞–Ј–∞–љ–Є—П–Љ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В–µ–ї—П.
–Р–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е
–Т—Б–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л —А–Э, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ —Г –Ї–∞–ґ–і–Њ–≥–Њ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞ –≤ –Ї–∞–ґ–і—Л–є –і–µ–љ—М –њ—А–Є–µ–Љ–∞, –±—Л–ї–Є –Ј–∞–≥—А—Г–ґ–µ–љ—Л –Є–Ј –Ј–∞–њ–Є—Б—Л–≤–∞—О—Й–µ–≥–Њ —Г—Б—В—А–Њ–є—Б—В–≤–∞ —А–Э––Љ–µ—В—А–∞ Flexilog 2020 –≤ —Д–∞–є–ї—Л ASCII, –Ї–Њ—В–Њ—А—Л–µ –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –њ–µ—А–µ–≤–Њ–і–Є–ї–Є –≤ –љ–∞–±–Њ—А—Л –і–∞–љ–љ—Л—Е SAS (–°–Р–° –Ш–љ—Б—В–Є—В—Г—В –Ш–љ–Ї., –Ъ—Н—А–Є, –°–µ–≤–µ—А–љ–∞—П –Ъ–∞—А–Њ–ї–Є–љ–∞, –°–®–Р), –Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –њ–Њ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–Љ—Г –њ–µ—А–Є–Њ–і—Г –≤—А–µ–Љ–µ–љ–Є –Є —З–Є—Б–ї—Г —Б–ї—Г—З–∞–µ–≤ —Б–љ–Є–ґ–µ–љ–Є—П —А–Э < 4 –Є 5 –≤ —В–µ—З–µ–љ–Є–µ 4–—З–∞—Б–Њ–≤–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –Ј–∞–њ–Є—Б–Є –і–∞–љ–љ—Л—Е –і–ї—П –∞–љ–∞–ї–Є–Ј–∞.
–Я–µ—А–≤–Є—З–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –±—Л–ї –њ—А–Њ—Ж–µ–љ—В –≤—А–µ–Љ–µ–љ–Є, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є–µ —А–Э –≤ –њ–Є—Й–µ–≤–Њ–і–µ –Њ–њ—Г—Б–Ї–∞–ї–Њ—Б—М <4. –Я–Њ—Б–ї–µ —В—А–Є–≥–Њ–љ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –і–∞–љ–љ—Л–є –њ–∞—А–∞–Љ–µ—В—А –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –і–Є—Б–њ–µ—А—Б–Є–Њ–љ–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –≤ —А–∞–Љ–Ї–∞—Е –Љ–Њ–і–µ–ї–Є –њ–Њ —Б–ї–µ–і—Г—О—Й–Є–Љ –њ–µ—А–µ–Љ–µ–љ–љ—Л–Љ: –і–Њ–±—А–Њ–≤–Њ–ї–µ—Ж, –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–µ–Љ–∞ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –Є—Б—Б–ї–µ–і—Г–µ–Љ–∞—П —В–µ—А–∞–њ–Є—П. –С—Л–ї —А–∞—Б—Б—З–Є—В–∞–љ 95%––є –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї, –≤—Л—З–Є—Б–ї–µ–љ–љ—Л–є –Љ–µ—В–Њ–і–Њ–Љ –љ–∞–Є–Љ–µ–љ—М—И–Є—Е –Ї–≤–∞–і—А–∞—В–Њ–≤ —Б—А–µ–і–љ–µ–≥–Њ —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г —Б—Г—Б–њ–µ–љ–Ј–Є–µ–є –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ 10 –Љ–ї –Є –і–≤—Г–Љ—П —В–∞–±–ї–µ—В–Ї–∞–Љ–Є –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ.
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–Ф–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤
–†–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є—О –њ—А–Њ—И–ї–Є 36 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –і–ї—П —В–Њ–≥–Њ, —З—В–Њ–±—Л –љ–µ –Љ–µ–љ–µ–µ 30 –њ—А–Њ—И–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –і–Њ –Ї–Њ–љ—Ж–∞. –Ш–Ј 115 –≤—Л–±—А–∞–љ–љ—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ 89 –њ—А–Њ—И–ї–Є –Є—Б—Е–Њ–і–љ—Л–є –Њ—Б–Љ–Њ—В—А (–њ–Њ–њ—Г–ї—П—Ж–Є—П –і–ї—П –Њ—Ж–µ–љ–Ї–Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є) –Є 86 –њ—А–Њ—И–ї–Є —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г —А–µ—Д–ї—О–Ї—Б–∞. –°–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Є –Ї—А–Є—В–µ—А–Є—П–Љ –і–ї—П –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ 46 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤, –Є–Ј –љ–Є—Е –≤—Б–µ–≥–Њ 39 –µ–≥–Њ –њ—А–Є–љ–Є–Љ–∞–ї–Є. –Ґ—А–Є–і—Ж–∞—В—М —И–µ—Б—В—М –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –±—Л–ї–Є —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ—Л. –Ґ–∞–±–ї–µ—В–Ї–Є –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ –Є –≤–Њ–і–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –њ–Њ–ї—Г—З–∞–ї–Є 36 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤. 35 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –њ–Њ–ї—Г—З–∞–ї–Є —Б—Г—Б–њ–µ–љ–Ј–Є—О –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ 10 –Љ–ї, 35 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –њ—А–Њ—И–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –і–Њ –Ї–Њ–љ—Ж–∞. –†–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ 35 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞–Љ –≤–Ї–ї—О—З–µ–љ—Л –≤ –∞–љ–∞–ї–Є–Ј —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є.
–Т—Б–µ –і–∞–љ–љ—Л–µ –Њ–і–љ–Њ–≥–Њ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞ –±—Л–ї–Є –Є—Б–Ї–ї—О—З–µ–љ—Л –Є–Ј –∞–љ–∞–ї–Є–Ј–∞ –њ–Њ—Б–ї–µ –Њ–±–Ј–Њ—А–∞ –і–∞–љ–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–є –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —А–Э––њ—А–Њ–±–∞ –±—Л–ї–∞ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–∞ —Б–ї–Є—И–Ї–Њ–Љ –±–ї–Є–Ј–Ї–Њ –Ї –Э–Я–°. –†–µ–Ј—Г–ї—М—В–∞—В—Л –µ—Й–µ –Њ–і–љ–Њ–≥–Њ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞ –њ–Њ –њ—А–Є–µ–Љ—Г —В–∞–±–ї–µ—В–Њ–Ї –±—Л–ї–Є –Є—Б–Ї–ї—О—З–µ–љ—Л –њ–Њ –њ—А–Є—З–Є–љ–µ –љ–µ—Б–Њ–±–ї—О–і–µ–љ–Є—П –і–љ–µ–є –њ—А–Є–µ–Љ–∞. –Ю–±—Й–Є–µ –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ –і–∞–љ–љ—Л–µ (–њ–Њ–њ—Г–ї—П—Ж–Є—П –і–ї—П –Њ—Ж–µ–љ–Ї–Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є –њ–Њ–њ—Г–ї—П—Ж–Є—П, –њ—А–Є–≥–Њ–і–љ–∞—П –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є) –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2.
–Я—А–Є —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ 65 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ (73%) —Б–Њ–Њ–±—Й–Є–ї–Є –∞–љ–∞–Љ–љ–µ–Ј –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –љ–Є –Њ–і–љ–Њ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –љ–µ –±—Л–ї–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ; 20 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ —Б–Њ–Њ–±—Й–Є–ї–Є –Њ–± –∞–ї–ї–µ—А–≥–Є–Є, –Є–Ј –љ–Є—Е 7 –њ—А–Њ—И–ї–Є —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є—О –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞; 18 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –њ–Њ–ї—Г—З–∞–ї–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–µ –ї–µ—З–µ–љ–Є–µ (—Б—А–µ–і—Б—В–≤–∞ –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є), –Є–Ј –љ–Є—Е 4 –њ—А–Њ—И–ї–Є —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є—О.
–Р–љ–∞–ї–Є–Ј —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є
–Ю–±—Й–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –њ—А–Є —А–∞—Б—З–µ—В–µ –њ—А–Њ—Ж–µ–љ—В–∞ –≤—А–µ–Љ–µ–љ–Є, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П —А–Э –≤ –њ–Є—Й–µ–≤–Њ–і–µ < 4, –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —В—А–µ—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е —А–µ–ґ–Є–Љ–Њ–≤, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 3. 95%––є –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї –і–ї—П –≤—Л—З–Є—Б–ї–µ–љ–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–Њ–Љ –љ–∞–Є–Љ–µ–љ—М—И–Є—Е –Ї–≤–∞–і—А–∞—В–Њ–≤ —Б—А–µ–і–љ–µ–≥–Њ —А–∞–Ј–ї–Є—З–Є—П –њ–Њ —В—А–Є–≥–Њ–љ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є –њ—А–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л–Љ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–Љ (%) –њ–µ—А–Є–Њ–і–∞–Љ –≤—А–µ–Љ–µ–љ–Є, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ–∞–і–µ–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П —А–Э –≤ –њ–Є—Й–µ–≤–Њ–і–µ < 4 (—В–∞–±–ї–µ—В–Ї–Є–—Б—Г—Б–њ–µ–љ–Ј–Є—П), —Б–Њ—Б—В–∞–≤–ї—П–ї –Њ—В –0,0121 –і–Њ 0,0501 –Є –њ–Њ—Н—В–Њ–Љ—Г —Ж–µ–ї–Є–Ї–Њ–Љ –љ–∞—Е–Њ–і–Є–ї—Б—П –љ–Є–ґ–µ –њ—А–µ–і–µ–ї—М–љ–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П 0,056. –≠—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В, —З—В–Њ —В–µ—А–∞–њ–Є—П —В–∞–±–ї–µ—В–Ї–∞–Љ–Є –љ–µ –Љ–µ–љ–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞, —З–µ–Љ —В–µ—А–∞–њ–Є—П —Б—Г—Б–њ–µ–љ–Ј–Є–µ–є. –Т —В–∞–±–ї–Є—Ж–µ 3 —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–µ—А–Є–Њ–і –≤—А–µ–Љ–µ–љ–Є, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є–µ —А–Э –Њ–њ—Г—Б–Ї–∞–ї–Њ—Б—М –љ–Є–ґ–µ 4, –Љ–µ–ґ–і—Г —В–µ—А–∞–њ–Є–µ–є –њ—А–Є –њ–Њ–Љ–Њ—Й–Є —Б—Г—Б–њ–µ–љ–Ј–Є–Є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є –±—Л–ї–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ (p<0,0001), —З—В–Њ –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Љ–µ—В–Њ–і–∞ –і–ї—П —А–∞–Ј–ї–Є—З–Є—П –∞–Ї—В–Є–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–°—Е–Њ–і–љ—Л–µ –Є—В–Њ–≥–Њ–≤—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –і–ї—П —В—А–µ—Е –≤–Є–і–Њ–≤ —В–µ—А–∞–њ–Є–Є, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Њ—Ж–µ–љ–Ї–Є –њ–µ—А–Є–Њ–і–∞ –≤—А–µ–Љ–µ–љ–Є (%), –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ–∞–і–µ–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П —А–Э –њ–Є—Й–µ–≤–Њ–і–∞ –љ–Є–ґ–µ –њ—П—В–Є, –њ–Њ–Ї–∞–Ј–∞–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 4. –Э–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г —В–µ—А–∞–њ–Є–µ–є —В–∞–±–ї–µ—В–Ї–∞–Љ–Є –Є —Б—Г—Б–њ–µ–љ–Ј–Є–µ–є (p=0,3415). –≠—В–Њ —П–≤–ї—П–µ—В—Б—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ —В–Њ–≥–Њ, —З—В–Њ —В–µ—А–∞–њ–Є—П —В–∞–±–ї–µ—В–Ї–∞–Љ–Є –љ–µ –Љ–µ–љ–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞, —З–µ–Љ —В–µ—А–∞–њ–Є—П —Б—Г—Б–њ–µ–љ–Ј–Є–µ–є.
–Ґ–∞–Ї–ґ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ —Б—В–∞—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–∞—П —А–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г —В–µ—А–∞–њ–Є–µ–є —Б—Г—Б–њ–µ–љ–Ј–Є–µ–є –Є –Ї–Њ–љ—В—А–Њ–ї–µ–Љ, –Ї–Њ–≥–і–∞ –Ј–љ–∞—З–µ–љ–Є–µ –≤–љ—Г—В—А–Є–њ–Є—Й–µ–≤–Њ–і–љ–Њ–≥–Њ —А–Э –Њ–њ—Г—Б–Ї–∞–ї–Њ—Б—М –љ–Є–ґ–µ 5 (p<0,0001), —З—В–Њ —Б–љ–Њ–≤–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Љ–µ—В–Њ–і–Є–Ї–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–∞–Ј–ї–Є—З–Є—П –∞–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є –Ї–Њ–љ—В—А–Њ–ї—П.
–Э–µ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г —В–µ—А–∞–њ–Є–µ–є —В–∞–±–ї–µ—В–Ї–∞–Љ–Є –Є —Б—Г—Б–њ–µ–љ–Ј–Є–µ–є –њ–Њ –≤—Л—З–Є—Б–ї–µ–љ–љ–Њ–Љ—Г –Љ–µ—В–Њ–і–Њ–Љ –љ–∞–Є–Љ–µ–љ—М—И–Є—Е –Ї–≤–∞–і—А–∞—В–Њ–≤ —Б—А–µ–і–љ–µ–Љ—Г –ї–Њ–≥–∞—А–Є—Д–Љ–Є—З–µ—Б–Ї–Є –њ—А–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ–Њ–Љ—Г —З–Є—Б–ї—Г —Б–ї—Г—З–∞–µ–≤, –≤ –Ї–Њ—В–Њ—А—Л—Е –Ј–љ–∞—З–µ–љ–Є–µ —А–Э –±—Л–ї–Њ –ї–Є–±–Њ <4 (p=0,1013), –ї–Є–±–Њ 5 (p=0,2321). –Ю–і–љ–∞–Ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —А–∞–Ј–ї–Є—З–Є–µ –Љ–µ–ґ–і—Г —В–µ—А–∞–њ–Є–µ–є —Б—Г—Б–њ–µ–љ–Ј–Є–µ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л–Љ –Њ–±—А–∞–Ј—Ж–Њ–Љ –њ–Њ –≤—Л—З–Є—Б–ї–µ–љ–љ–Њ–Љ—Г –Љ–µ—В–Њ–і–Њ–Љ –љ–∞–Є–Љ–µ–љ—М—И–Є—Е –Ї–≤–∞–і—А–∞—В–Њ–≤ —Б—А–µ–і–љ–µ–Љ—Г –ї–Њ–≥–∞—А–Є—Д–Љ–Є—З–µ—Б–Ї–Є –њ—А–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ–Њ–Љ—Г —З–Є—Б–ї—Г —Б–ї—Г—З–∞–µ–≤, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е –Ј–љ–∞—З–µ–љ–Є–µ —А–Э –Њ–њ—Г—Б–Ї–∞–ї–Њ—Б—М –љ–Є–ґ–µ 4 –Є 5 (p<0,0001 –≤ –Њ–±–Њ–Є—Е —Б–ї—Г—З–∞—П—Е).
–Ю—Ж–µ–љ–Ї–∞ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є
–Я–µ—А–µ–і —В–µ—А–∞–њ–Є–µ–є —Г 11 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М 13 –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є (–Э–ѓ). –Я–Њ—Б–ї–µ —В–µ—А–∞–њ–Є–Є —Г 12 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –Њ—В–Љ–µ—З–µ–љ–Њ 19 —Б–ї—Г—З–∞–µ–≤ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є, –Є–Ј –љ–Є—Е 7 – –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —В–∞–±–ї–µ—В–Њ–Ї (2 —Б–ї—Г—З–∞—П –±–Њ–ї–µ–є –≤ –ґ–Є–≤–Њ—В–µ/–≤–Ј–і—Г—В–Є—П –ґ–Є–≤–Њ—В–∞, 2 —Б–ї—Г—З–∞—П –Ј–∞–њ–Њ—А–∞, 1 —Б–ї—Г—З–∞–є —А–µ—Д–ї—О–Ї—Б–∞, 1 —Б–ї—Г—З–∞–є –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є –Є 1 —Б–ї—Г—З–∞–є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л), 4 –Э–ѓ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Б—Г—Б–њ–µ–љ–Ј–Є–Є (1 —Б–ї—Г—З–∞–є –і–Є–∞—А–µ–Є, 1 —Б–ї—Г—З–∞–є –і–Є—Б–њ–µ–њ—Б–Є–Є –Є 2 —Б–ї—Г—З–∞—П –љ–Њ—Б–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П) –Є 8 —П–≤–ї–µ–љ–Є–є –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –Ї–Њ–љ—В—А–Њ–ї—П (1 —Б–ї—Г—З–∞–є –±–Њ–ї–Є –≤ –ґ–Є–≤–Њ—В–µ, 3 —Б–ї—Г—З–∞—П —В–Њ—И–љ–Њ—В—Л, 1 —Б–ї—Г—З–∞–є –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є, 2 —Б–ї—Г—З–∞—П —А–Є–љ–Њ—А–µ–Є –Є 1 —Б–ї—Г—З–∞–є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л).
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є—Е –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞. –Т–Њ–Ј–љ–Є–Ї—И–Є–µ –≤ –њ–µ—А–Є–Њ–і –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ 16 –Э–ѓ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –±—Л–ї–Є —Б–≤—П–Ј–∞–љ—Л —Б –Є–Ј—Г—З–∞–µ–Љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ (7 —П–≤–ї–µ–љ–Є–є –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —В–∞–±–ї–µ—В–Њ–Ї, 3 –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Б—Г—Б–њ–µ–љ–Ј–Є–Є –Є 6 – –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –Ї–Њ–љ—В—А–Њ–ї—П). –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–Ј –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –±—Л–ї–Є –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є, —В–Њ–ї—М–Ї–Њ 1 –Э–ѓ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —В–∞–±–ї–µ—В–Њ–Ї (–Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞), 1 – –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Б—Г—Б–њ–µ–љ–Ј–Є–Є (–і–Є—Б–њ–µ–њ—Б–Є—П) –Є 2 – –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –Ї–Њ–љ—В—А–Њ–ї—П (–±–Њ–ї—М –ґ–Є–≤–Њ—В–µ –Є —В–Њ—И–љ–Њ—В–∞) –±—Л–ї–Є —Б—А–µ–і–љ–µ–є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є. –Ґ—П–ґ–µ–ї—Л—Е, –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е –Є–ї–Є —Б–µ—А—М–µ–Ј–љ—Л—Е —П–≤–ї–µ–љ–Є–є –љ–µ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ. –Э–Є –Њ–і–Є–љ –Є–Ј –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –љ–µ –±—Л–ї –≤—Л–≤–µ–і–µ–љ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ –њ—А–Є—З–Є–љ–∞–Љ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ–і–љ–Њ–Ї—А–∞—В–љ–∞—П –і–Њ–Ј–∞ –Њ–±–Њ–Є—Е –Є–Ј—Г—З–∞–µ–Љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–є –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –Ј–і–Њ—А–Њ–≤—Л–Љ–Є –≤–Ј—А–Њ—Б–ї—Л–Љ–Є –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞–Љ–Є, —Г—З–∞—Б—В–≤–Њ–≤–∞–≤—И–Є–Љ–Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Т–љ—Г—В—А–Є–њ–Є—Й–µ–≤–Њ–і–љ—Л–є pH––Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –і–ї—П —Б—Г–њ—А–µ—Б—Б–Є–Є —А–µ—Д–ї—О–Ї—Б–∞, –Ї–Њ—В–Њ—А—Л–є —Б–њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞–љ —А–µ—Д–ї—О–Ї—Б–Њ–≥–µ–љ–љ–Њ–є –њ–Є—Й–µ–є, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –Є —А–∞–љ–µ–µ –і–ї—П —Б—А–∞–≤–љ–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–ї—М–≥–Є–љ–∞—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –і–ї—П –њ–Њ–і–∞–≤–ї–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–∞ [19]. –Э–∞—Б—В–Њ—П—Й–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ—Л–є –Њ—В–±–Њ—А —Б—Г–±—К–µ–Ї—В–Њ–≤ —Б –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–Љ –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –Ї–Є—Б–ї–Њ—В—Л –љ–∞ –њ–Є—Й–µ–≤–Њ–і, —В–Є–њ–Є—З–љ—Л–Љ –і–ї—П –±–Њ–ї—М–љ—Л—Е —Б –У–≠–†–С (–і–Њ–±—А–Њ–≤–Њ–ї—М—Ж—Л —Б–Њ –Ј–љ–∞—З–µ–љ–Є–µ–Љ pH –≤ –њ–Є—Й–µ–≤–Њ–і–µ <4 –≤ —В–µ—З–µ–љ–Є–µ 2% –Њ—В –њ–µ—А–Є–Њ–і–∞ –≤—А–µ–Љ–µ–љ–Є –Є–Ј–Љ–µ—А–µ–љ–Є—П –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞), –≤–µ–і–µ—В –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є –Љ–µ—В–Њ–і–∞. –Т –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ —Н—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ —А–∞–Ј–ї–Є—З–Є—П–Љ (p<0,0001) –Љ–µ–ґ–і—Г –∞–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є –Є –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –њ–Њ –≤—Б–µ–Љ —З–µ—В—Л—А–µ–Љ –≤—Л–±—А–∞–љ–љ—Л–Љ –Ї—А–Є—В–µ—А–Є—П–Љ –Њ—Ж–µ–љ–Ї–Є.
–Т–љ—Г—В—А–Є–њ–Є—Й–µ–≤–Њ–і–љ—Л–є pH––Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е –ї–µ—В, –Ї–∞–Ї —Б–њ–Њ—Б–Њ–± –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б—Г—Б–њ–µ–љ–Ј–Є–Є –У–µ–≤–Є—Б–Ї–Њ–љ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–∞ –і–ї—П –њ–Њ–і–∞–≤–ї–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–∞ –Є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤, –Є —Г –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е –Њ—В —А–µ—Д–ї—О–Ї—Б–љ–Њ–≥–Њ —Н–Ј–Њ—Д–∞–≥–Є—В–∞ [16,23]. –Т–Њ –≤—Б–µ—Е —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ї–Є—Б–ї–Њ—В–љ–Њ–≥–Њ —А–µ—Д–ї—О–Ї—Б–∞ –њ–Њ—Б–ї–µ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–Њ–≥–µ–љ–љ–Њ–є –њ–Є—Й–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –њ—А–Њ—Ж–µ–љ—В –Њ—В –њ–µ—А–Є–Њ–і–∞ –≤—А–µ–Љ–µ–љ–Є –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ (—А–∞–≤–љ–Њ–≥–Њ 3 —З, –≤ –њ–Њ—Б–ї–µ–і–љ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е – 4 —З), –≤ —Е–Њ–і–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ pH –Њ–њ—Г—Б–Ї–∞–ї–Њ—Б—М <4. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Б —Г—З–∞—Б—В–Є–µ–Љ –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Т–∞—И–Є–љ–≥—В–Њ–љ–Њ–Љ —Б –Ї–Њ–ї–ї–µ–≥–∞–Љ–Є [23], –њ—А–Њ—Ж–µ–љ—В –≤—А–µ–Љ–µ–љ–Є —Б pH < 4 –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –і–Њ–Ј—Л –≤–Њ–і—Л –Ї–Њ–ї–µ–±–∞–ї—Б—П –Њ—В 9,5 –і–Њ 3,2% –Є –њ–Њ–љ–Є–Ј–Є–ї—Б—П –і–Њ –Ј–љ–∞—З–µ–љ–Є—П –Љ–µ–ґ–і—Г 1,5 –Є 0,88% –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Б—Г—Б–њ–µ–љ–Ј–Є–Є –У–µ–≤–Є—Б–Ї–Њ–љ. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б —Г—З–∞—Б—В–Є–µ–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ—Л–Љ —Б–ї–∞–±–Њ–≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Н–Ј–Њ—Д–∞–≥–Є—В–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –њ—А–Њ—Ж–µ–љ—В –≤—А–µ–Љ–µ–љ–Є, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ —А–Э –Њ–њ—Г—Б–Ї–∞–ї–Њ—Б—М <4, –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –≤–Њ–і–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П —Б–Њ—Б—В–∞–≤–Є–ї 16,4% –Є —Б–љ–Є–Ј–Є–ї—Б—П –і–Њ 5,4% –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Б—Г—Б–њ–µ–љ–Ј–Є–Є –У–µ–≤–Є—Б–Ї–Њ–љ. –Т —Е–Њ–і–µ —Б–∞–Љ–Њ–≥–Њ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П [16], –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ —Б —Г—З–∞—Б—В–Є–µ–Љ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤, –Ї–Њ—В–Њ—А—Л–µ, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Ј–∞–љ–Є–Љ–∞–ї–Є—Б—М —Б–∞–Љ–Њ–ї–µ—З–µ–љ–Є–µ–Љ, –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ —Б—А–∞–≤–љ–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –≤—Л—И–µ–љ–∞–Ј–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П —Б 6,6% –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–≥–Њ –Њ–±—А–∞–Ј—Ж–∞ –і–Њ 0,98% –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Б—Г—Б–њ–µ–љ–Ј–Є–Є –У–µ–≤–Є—Б–Ї–Њ–љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ –і–∞–љ–љ–Њ–Љ—Г –њ–∞—А–∞–Љ–µ—В—А—Г (–њ—А–Њ—Ж–µ–љ—В –≤—А–µ–Љ–µ–љ–Є, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ pH<4) —Б–ї–µ–і—Г–µ—В –Њ–ґ–Є–і–∞—В—М —И–Є—А–Њ–Ї–Њ–≥–Њ –і–Є–∞–њ–∞–Ј–Њ–љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Ї–∞–Ї –і–ї—П –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤, —В–∞–Ї –Є –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –У–≠–†–С. –†–µ–Ј—Г–ї—М—В–∞—В—Л, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї–Њ–љ—В—А–Њ–ї—П –≤ –љ–∞—Б—В–Њ—П—Й–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є (—В–∞–±–ї. 3), –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В —Н—В–Њ.
–°—А–∞–≤–љ–µ–љ–Є–µ —В–∞–±–ї–Є—Ж 3 –Є 4 –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –њ—А–Њ—Ж–µ–љ—В –≤—А–µ–Љ–µ–љ–Є —Б —А–Э<5 –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ –≤ –і–≤–∞ —А–∞–Ј–∞ –±–Њ–ї—М—И–µ –њ—А–Њ—Ж–µ–љ—В–∞ –≤—А–µ–Љ–µ–љ–Є —Б —А–Э<4 –Ї–∞–Ї –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –Ї–Њ–љ—В—А–Њ–ї—П, —В–∞–Ї –Є –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –∞–ї—М–≥–Є–љ–∞—В–∞. –≠—В–Њ –њ–Њ–ї–љ–Њ—Б—В—М—О —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —А–∞–љ–µ–µ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –і–ї—П –Њ—Ж–µ–љ–Ї–Є —А–µ—Д–ї—О–Ї—Б–∞ —В–∞–Ї–ґ–µ –±—Л–ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ –њ—А–Њ—Ж–µ–љ—В –≤—А–µ–Љ–µ–љ–Є —Б —А–Э<5 [19]. –Ф–∞–љ–љ–Њ–µ —А–∞–љ–µ–µ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —Е–Њ—В—П —Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ—Л–є —А–µ—Д–ї—О–Ї—Б (–Ї–∞–Ї –Ї–Є—Б–ї–Њ—В–љ—Л–є, —В–∞–Ї –Є –њ–Є—Й–µ–≤–Њ–є) –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї—Б—П –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —Б—Г—Б–њ–µ–љ–Ј–Є–Є –У–µ–≤–Є—Б–Ї–Њ–љ, –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –і—А—Г–≥–Њ–≥–Њ –∞–ї—М–≥–Є–љ–∞—В–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ – –ґ–Є–і–Ї–Њ–є —Д–Њ—А–Љ—Л –Р–ї—М–≥–Є–Ї–Њ–љ–∞, –њ–Њ–і–Њ–±–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М. –Р–≤—В–Њ—А—Л –Ј–∞–Ї–ї—О—З–Є–ї–Є, —З—В–Њ –Р–ї—М–≥–Є–Ї–Њ–љ –љ–µ —Б–њ–Њ—Б–Њ–±–µ–љ –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—В—М –њ–ї–Њ—В, –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—Й–Є–є —А–µ—Д–ї—О–Ї—Б, –љ–∞—Б—В–Њ–ї—М–Ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ, –Ї–∞–Ї —Б—Г—Б–њ–µ–љ–Ј–Є—П –У–µ–≤–Є—Б–Ї–Њ–љ–∞, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–љ—В–∞—Ж–Є–і–∞ –≤ —Б–Њ—Б—В–∞–≤–µ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –њ–ї–Њ—В–∞ –њ—Г—В–µ–Љ –љ–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є–Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ —Б–Њ–Ї–∞, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–≥–Њ –і–ї—П –Њ—Б–∞–ґ–і–µ–љ–Є—П –∞–ї—М–≥–Є–љ–∞—В–∞. –Т–∞—И–Є–љ–≥—В–Њ–љ –Є —Б–Њ–∞–≤—В–Њ—А—Л [24], –∞ —В–∞–Ї–ґ–µ –і—А—Г–≥–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є [25] —Г—Б—В–∞–љ–Њ–≤–Є–ї–Є, —З—В–Њ –∞–ї—М–≥–Є–љ–∞—В–љ—Л–є —Б–Њ—Б—В–∞–≤ —Б –≤—Л—Б–Њ–Ї–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–љ–µ–є—В—А–∞–ї–Є–Ј—Г—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О (—В–∞–Ї–Њ–є –Ї–∞–Ї –Р–ї—М–≥–Є–Ї–Њ–љ) –љ–µ–є—В—А–∞–ї–Є–Ј—Г–µ—В –ґ–µ–ї—Г–і–Њ—З–љ—Л–є —Б–Њ–Ї in vivo, —В–Њ–≥–і–∞ –Ї–∞–Ї —Б–Њ—Б—В–∞–≤–∞ —Б –љ–Є–Ј–Ї–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–љ–µ–є—В—А–∞–ї–Є–Ј—Г—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О (—В–∞–Ї–Њ–є –Ї–∞–Ї –У–µ–≤–Є—Б–Ї–Њ–љ) –љ–µ—В. –Э–∞—Б—В–Њ—П—Й–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –ґ–Є–і–Ї–Є—Е –Є —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –∞–ї—М–≥–Є–љ–∞—В–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –і–∞–ґ–µ —Б –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–љ–µ–є—В—А–∞–ї–Є–Ј—Г—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О, —З–µ–Љ —Г —Б—Г—Б–њ–µ–љ–Ј–Є–Є –У–µ–≤–Є—Б–Ї–Њ–љ, –µ—Й–µ —А–∞–Ј –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –і–ї—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ–ї–Њ—В–∞ –Є –њ–Њ–і–∞–≤–ї–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–∞ –љ–µ —В—А–µ–±—Г–µ—В—Б—П –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–љ—В–∞—Ж–Є–і–∞.
–Т —Е–Њ–і–µ –≤—Л—И–µ—Г–њ–Њ–Љ—П–љ—Г—В—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Т–∞—И–Є–љ–≥—В–Њ–љ–Њ–Љ –Є —Б–Њ–∞–≤—В. [19,22,23], –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–µ–њ–∞—А–∞—В—Л, –Њ–±—А–∞–Ј—Г—О—Й–Є–µ –њ—А–Њ—З–љ—Л–є –∞–ї—М–≥–Є–љ–∞—В–љ—Л–є –њ–ї–Њ—В, –±—Л–ї–Є –≤ —А–∞–≤–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–љ–Є–ґ–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–∞ –њ–Є—Й–Є –≤ –њ–Є—Й–µ–≤–Њ–і.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –∞–ї—М–≥–Є–љ–∞—В–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–µ –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–µ—Д–ї—О–Ї—Б–∞ –Є —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–љ—В–∞—Ж–Є–і–∞ (—Б—Г—Б–њ–µ–љ–Ј–Є–Є –Є —В–∞–±–ї–µ—В–Ї–Є –У–µ–≤–Є—Б–Ї–Њ–љ –§–Њ—А—В–µ), —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ–Њ–і–∞–≤–ї—П—О—В –Ї–Є—Б–ї–Њ—В–љ—Л–є —А–µ—Д–ї—О–Ї—Б, —Б–њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є —А–µ—Д–ї—О–Ї—Б–Њ–≥–µ–љ–љ–Њ–є –њ–Є—Й–µ–є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≤–Њ–і–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ. –Ґ–∞–Ї–ґ–µ –≤ —Е–Њ–і–µ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ї–∞–Ї —Б—Г—Б–њ–µ–љ–Ј–Є—П, —В–∞–Ї –Є —В–∞–±–ї–µ—В–Ї–Є –±—Л–ї–Є –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л, —З–µ–Љ –Ї–Њ–љ—В—А–Њ–ї—М, –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–Њ—Ж–µ–љ—В–∞ –≤—А–µ–Љ–µ–љ–Є –Є —З–Є—Б–ї–∞ —Б–ї—Г—З–∞–µ–≤, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е —А–Э –њ–Є—Й–µ–≤–Њ–і–∞ –Њ–њ—Г—Б–Ї–∞–ї—Б—П –љ–Є–ґ–µ 4 –Є 5. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –љ–Є –њ–Њ –Њ–і–љ–Њ–Љ—Г –Є–Ј –≤—Л—И–µ—Г–Ї–∞–Ј–∞–љ–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –љ–Є–Ї–∞–Ї–Є—Е —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г —В–µ—А–∞–њ–Є–µ–є —Б—Г—Б–њ–µ–љ–Ј–Є–µ–є –Є —В–∞–±–ї–µ—В–Ї–∞–Љ–Є –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–ї—М–≥–Є–љ–∞—В–∞, —З—В–Њ –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —Г—Б–њ–µ—И–љ–Њ–µ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –Ї–Є—Б–ї–Њ—В–љ–Њ–≥–Њ —А–µ—Д–ї—О–Ї—Б–∞ –њ—А–Є –њ—А–Є–µ–Љ–µ —А–∞–Ј–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Д–Њ—А–Љ –∞–ї—М–≥–Є–љ–∞—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Malfertheiner P, Hallerback B. Clinical manifestations and compli¬cations of gastroesophageal reflux disease (GERD). Int J Clin Pract 2005; 59: 3.
2. Achkar E. The death of the chief complaint or how GERD replaced heartburn. Am J Gastroenterol 2006; 101: 1719–20.
3. Vakil N, VanZanten SV, Kahrilas P et al. The Montreal definition and classification of gastroesophageal reflux disease: a global evidence–based consensus. Am J Gastroenterol 2006; 101: 1900–20.
4. Chevrel B. A comparative crossover study on the treatment of heartburn and epigastric pain: Liquid Gaviscon and a magnesium–aluminium antacid gel. / Int Med Res 1980; 8: 300–2.
5. Galmiche JP, Shi G, Simon B et al. On–demand treatment of gas–tro–oesophageal reflux symptoms: a comparison of ranitidine 75 mg with cimetidine 200 mg or placebo. Aliment Pharmacol Ther 1998; 12: 909–17.
6. Simon TJ, Berlin RG, Gardner AH et al. Self–directed treatment of intermittent heartburn: a randomised, multi–centre double–blind, placebo–controlled evaluation of antacid and low doses of an H2–receptor antagonist (famotidine). Am I Ther 1995; 2: 304–13.
7. Poynard T, Vernisse B, Agostini H. Randomised, multicentre com¬parison of sodium alginate and cisapride in the symptomatic treat¬ment of uncomplicated gastrooesophageal reflux. Aliment Pharmacol Ther 1998; 12: 159–65.
8. Jones RH, Hungin AP, Phillips J et al. Gastro–oesophageal reflux disease in primary care in Europe: clinical presentation and endo–scopic findings. Eur I Gen Pract 1995; 1: 149–54.
9. Ronkainen JA, Aro P, Storskrubb T et al. Prevalence of oesophagi–tis and endoscopy–negative reflux disease in a population: a report from the Kalixanda study. Gastroenterology 2002; 122 (4 Suppl. 1): A213.
10. Hopwood D, Bateson MC, Milne G et al. Effects of bile acids and hydrogen ions on the fine structure of oesophageal epithelium. Gut 1981; 22: 306–11.
11. Johnson LF, De Meester TR. Twenty–four hour pH monitoring of the distal oesophagus, a quantitative measure of gastroesophageal reflux. Am J Gastroenterol 1974; 62: 325–32.
12. Piper DW, Fenton BH. pH stability and activity curves of pepsin with special reference to their clinical importance. Gut 1965; 6: 506–8.
13. Roberts NB. Review article: human pepsins – their multiplicity, function and role in reflux disease. Aliment pharmacol Ther 2006; 24 (Suppl. 2): 2–9.
14. Mandel KG, Daggy BP, Brodie DA et al. Review article: alginate–raft formulations in the treatment of heartburn and acid reflux. Aliment Pharmacol Ther 2000; 14: 669–90.
15. Hampson F C, Farndale A, Strugala V et al. Alginate rafts and their characterisation. Int J Pharmaceut 2005; 294: 137–47.
16. Dettmar PW, Sykes J, Little SL et al. Rapid onset of effect of sodium alginate on gastro–oesophageal reflux compared with ranti–dine and omeprazole, and relationship between symptoms and reflux episodes. Int J Clin Pract 2006; 60: 275–83.
17. D’Agostino RB Sr, Massaro JM, Sullivan LM. Non–inferiority trials: design concepts and issues – the encounters of academics consul¬tants in statistics. Statist Med 2003; 22: 169–86.
18. Janssens J, Vantrappen G. Pathophysiology of reflux esophagitis. Scand J Gastroenterol 1989; 24 (Suppl. 156): 15–9.
19. Washington N, Greaves JL, Iftikhar SY. A comparison of gastro–oesophageal reflux in volunteers assessed by ambulatory pH and gamma monitoring after treatment with either Liquid Gaviscon or Algicon Suspension. Aliment Pharmacol Ther 1992; 6: 579–88.
20. Armitage P. Statistical Methods in Medical Research. Oxford: Blackwell Scientific Publications, 1971, 356.
21. Jones B, Jarvis P, Lewis JA, Ebbutt AF. Trials to assess equivalence: the importance of rigorous methods. Br Med J 1996; 313: 36–9.
22. Washington N. Investigation into the barrier action of an alginate gastric reflux suppressant, Liquid Gaviscon. Drug Investig 1990; 2: 23–30.
23. Washington N, Steele RJC, Jackson SJ et al. Patterns of food and acid reflux in patients with low–grade oesophagitis–the role of an anti–reflux agent. Aliment Pharmacol Ther 1998; 12: 53–8.
24. Washington N, Washington C, Wilson CG. Gastric distribution and residence time of two anti–reflux formulations. Int J Pharm 1987; 39: 163–71.
25. Lambert JR, Korman MG, Nicholson L et al. In vivo anti–reflux and raft properties of alginates. Aliment Pharmacol Ther 1990; 4: 615–22.
26. Tamhankar AP, Peters JH, Portale G et al. Omeprazole does not reduce gastroesophageal reflux: new insights using multichannel intraluminal impedance technology. J Gastrointest Surg 2004; 8: 888–95.
27. Vela MF, Camacho–Lobato L, Srinivasan R et al. Simultaneous in–traesophageal impedance and pH measurement of acid and non–acid gastroesophageal reflux: effect of omeprazole. Gastroenterology 2001; 120: 1599–606.
28. Zentilin P, Dulbecco P, Savarino E et al. An evaluation of the anti–reflux properties of sodium alginate by means of combined multi¬channel intraluminal impedance and pH–metry. Aliment Pharmacol Ther 2005; 21: 29–34.












