–•–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–∞—А—Г—И–µ–љ–Є–µ –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є —П–≤–ї—П–µ—В—Б—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б–∞ —Б—В–∞—А–µ–љ–Є—П. –Ф–∞–љ–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –≤–µ—Б—М–Љ–∞ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л. –Э–∞–њ—А–Є–Љ–µ—А, —Г –ґ–µ–љ—Й–Є–љ —Б—В–∞—А—И–µ 45–50 –ї–µ—В —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П «–≤–µ—Б–љ—Г—И—З–∞—В–Њ—Б—В—М» –Ї–Њ–ґ–Є –ї–Є—Ж–∞, –њ–ї–µ—З, –≤–µ—А—Е–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л –Є —В—Л–ї—М–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Є—Б—В–µ–є —А—Г–Ї. –Ч–∞—З–∞—Б—В—Г—О —Н—В–Є —Д–µ–љ–Њ–Љ–µ–љ—Л —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –њ–∞–і–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П —Н—Б—В—А–Њ–≥–µ–љ–Њ–≤. –£—Б–Є–ї–µ–љ–Є–µ –њ–Є–≥–Љ–µ–љ—В–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —Б –≤–Њ–Ј—А–∞—Б—В–Њ–Љ —Г –ґ–µ–љ—Й–Є–љ —Б–≤—П–Ј–∞–љ–Њ –љ–µ —В–Њ–ї—М–Ї–Њ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –≥–Њ—А–Љ–Њ–љ–Њ—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —П–Є—З–љ–Є–Ї–Њ–≤. –Ш —Г –ґ–µ–љ—Й–Є–љ, –Є —Г –Љ—Г–ґ—З–Є–љ —Б –≤–Њ–Ј—А–∞—Б—В–Њ–Љ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М –Ї–Њ–ґ–Є –Ї —Г–ї—М—В—А–∞—Д–Є–Њ–ї–µ—В–Њ–≤–Њ–Љ—Г –Њ–±–ї—Г—З–µ–љ–Є—О (–£–§–Ю), —Б–љ–Є–ґ–∞—О—В—Б—П –±–∞—А—М–µ—А–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є –Ї–Њ–ґ–Є, –≤—Б–ї–µ–і—Б—В–≤–Є–µ —З–µ–≥–Њ –Њ–љ–∞ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –±–Њ–ї–µ–µ —Б–Ї–ї–Њ–љ–љ–Њ–є –Ї –Љ–Є–Ї—А–Њ—В—А–∞–≤–Љ–∞—В–Є–Ј–∞—Ж–Є–Є. –≠—В–Є —Д–∞–Ї—В–Њ—А—Л —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і—П—В –Ї –њ–Њ—П–≤–ї–µ–љ–Є—О –њ–Є–≥–Љ–µ–љ—В–љ—Л—Е –њ—П—В–µ–љ (–њ—П—В–µ–љ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є).
–Ф—А—Г–≥–Њ–є –њ—А–Є–Љ–µ—А: –≤–Њ –≤—В–Њ—А–Њ–є –њ–Њ–ї–Њ–≤–Є–љ–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —Г –ґ–µ–љ—Й–Є–љ —Б –Њ—З–µ–љ—М —Б–≤–µ—В–ї–Њ–є –Ї–Њ–ґ–µ–є, –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ–Њ—П–≤–ї–µ–љ–Є–µ —Г—З–∞—Б—В–Ї–Њ–≤ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–ґ–Є –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –≥–Њ—А–Љ–Њ–љ–Њ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –Ј–Њ–љ–∞—Е (–Њ–±–ї–∞—Б—В—М –∞—А–µ–Њ–ї—Л, –≤–љ—Г—В—А–µ–љ–љ—П—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –±–µ–і–µ—А –Є –њ—А—П–Љ–∞—П –ї–Є–љ–Є—П –ґ–Є–≤–Њ—В–∞). –£ —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї (—Б–Њ —Б–≤–µ—В–ї–Њ–є –Ї–Њ–ґ–µ–є/–Є–ї–Є –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ–µ–є –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤) –Њ—В–Љ–µ—З–µ–љ–Њ –њ–Њ—П–≤–ї–µ–љ–Є–µ –њ–Є–≥–Љ–µ–љ—В–љ—Л—Е –њ—П—В–µ–љ –љ–µ–њ—А–∞–≤–Є–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л –≤ –Њ–±–ї–∞—Б—В–Є —Й–µ–Ї, —Б–Ї—Г–ї, –ї–±–∞, —И–µ–Є –Є —В.–і. –°–≤—П–Ј–∞–љ–љ—Л–µ —Б –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М—О –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Ж–≤–µ—В–∞ –Ї–Њ–ґ–Є –њ–Њ—П–≤–ї—П—О—В—Б—П –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ —Г 90% –±–µ—А–µ–Љ–µ–љ–љ—Л—Е [1].
–Ь–љ–Њ–≥–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (—В–∞–Ї–Є–µ, –Ї–∞–Ї –∞–ї–Ї–Њ–≥–Њ–ї–Є–Ј–Љ, –≥–µ–њ–∞—В–Є—В, –љ–∞—А—Г—И–µ–љ–Є–µ –≤—Л–і–µ–ї–Є—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –∞–і—А–µ–љ–∞–ї–Њ–≤—Л—Е –ґ–µ–ї–µ–Ј [2], –≥–µ–Љ–Њ—Е—А–Њ–Љ–∞—В–Њ–Ј, —А–∞–Ј–ї–Є—З–љ—Л–µ –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є –Є –і—А. [3]) –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—В —Б—В–∞—А–µ–љ–Є–µ –Ї–Њ–ґ–Є –њ–Њ —В–Є–њ—Г «—А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–є» –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є (–њ–Њ—В–µ–Љ–љ–µ–љ–Є–µ –Ї–Њ–ґ–Є). –Ъ—Г—А–µ–љ–Є–µ —Б–љ–Є–ґ–∞–µ—В –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї –Ї–Њ–ґ–Є –Є –њ—А–Є–≤–Њ–і–Є—В –Ї —Г—Б–Ї–Њ—А–µ–љ–Є—О —А–∞–Ј–≤–Є—В–Є—П –≤–Є–і–Є–Љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –µ–µ —Б—В–∞—А–µ–љ–Є—П –≤ –≤–Є–і–µ –њ–Њ—В–µ—А–Є –≤–ї–∞–≥–Є, —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є –Є –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є. –Т—Б–ї–µ–і—Б—В–≤–Є–µ –Љ–µ–љ—М—И–µ–є —В–Њ–ї—Й–Є–љ—Л –Ї–Њ–ґ–Є —Г –Ї—Г—А—П—Й–Є—Е –ґ–µ–љ—Й–Є–љ —Н—В–Њ—В —Д–µ–љ–Њ–Љ–µ–љ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –љ–∞ 10–12 –ї–µ—В –±—Л—Б—В—А–µ–µ, —З–µ–Љ —Г –Ї—Г—А—П—Й–Є—Е –Љ—Г–ґ—З–Є–љ.
–Ш–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В –њ—А–Њ—В–µ–Ї–∞–љ–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤. –Я–Њ—Б—В–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ—А–Є –Љ–љ–Њ–≥–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Ї–Њ–ґ–Є, –≤–Ї–ї—О—З–∞—П –∞–Ї–љ–µ, —Н–Ї–Ј–µ–Љ—Г, –Ї–Њ–љ—В–∞–Ї—В–љ—Л–є –і–µ—А–Љ–∞—В–Є—В, –Љ–Њ–ґ–µ—В –±—Л—В—М –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –≤–љ–Њ–≤—М –Њ–±—А–∞–Ј–Њ–≤–∞–≤—И–µ–є—Б—П –Ї–Њ–ґ–Є –љ–∞–і —А—Г–±—Ж–Њ–≤–Њ–є –Ј–Њ–љ–Њ–є —А–∞–љ [4]. –Я–µ—А–≤–∞—П –ї–Є–љ–Є—П —В–µ—А–∞–њ–Є–Є –Њ–±—Л—З–љ–Њ —Б–Њ—Б—В–Њ–Є—В –Є–Ј –і–µ–њ–Є–≥–Љ–µ–љ—В–Є—А—Г—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –≤ –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Ї –Ј–∞—Й–Є—В–µ –Ї–Њ–ґ–Є –Њ—В –Є–Ј–±—Л—В–Ї–∞ —Б–Њ–ї–љ–µ—З–љ–Њ–≥–Њ –Є–Ј–ї—Г—З–µ–љ–Є—П. –Т –Ї–∞—З–µ—Б—В–≤–µ –і–µ–њ–Є–≥–Љ–µ–љ—В–Є—А—Г—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П —В–∞–Ї–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л —В–Є—А–Њ–Ј–Є–љ–∞–Ј—Л, –Ї–∞–Ї –≥–Є–і—А–Њ—Е–Є–љ–Њ–љ, –∞–Ј–µ–ї–∞–Є–љ–Њ–≤–∞—П –Є –Ї–Њ–є–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В—Л, –∞—А–±—Г—В–Є–љ, —Н–Ї—Б—В—А–∞–Ї—В —Б–Њ–ї–Њ–і–Ї–Є, —А–µ—В–Є–љ–Њ–Є–і—Л, –∞—Б–Ї–Њ—А–±–Є–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –љ–Є–∞—Ж–Є–љ–∞–Љ–Є–і, N––∞—Ж–µ—В–Є–ї–≥–ї—О–Ї–Њ–Ј–∞–Љ–Є–љ –Є —Н–Ї—Б—В—А–∞–Ї—В—Л —Б–Њ–Є [5]. –Ы–Є–љ–Њ–ї–µ–≤–∞—П –Є α––ї–Є–љ–Њ–ї–µ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В—Л —В–Њ—А–Љ–Њ–Ј—П—В –≤—Л—А–∞–±–Њ—В–Ї—Г –Љ–µ–ї–∞–љ–Є–љ–∞ –∞–Ї—В–Є–≤–љ—Л–Љ–Є –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–∞–Љ–Є –Є —Г—Б–Є–ї–Є–≤–∞—О—В –≤—Л—И–µ–ї—Г—И–Є–≤–∞–љ–Є–µ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Н–њ–Є–і–µ—А–Љ–Є—Б–∞ [6].
–Э–∞—А—Г—И–µ–љ–Є—П –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –њ–ї–Њ—Е–Њ –њ–Њ–і–і–∞—О—В—Б—П –ї–µ—З–µ–љ–Є—О, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—Б—Е–Њ–і–љ–Њ –±–Њ–ї–µ–µ —В–µ–Љ–љ—Л–Љ —Ж–≤–µ—В–Њ–Љ –Ї–Њ–ґ–Є –ї–Є—Ж–∞. –Т –Є–і–µ–∞–ї–µ —Ж–µ–ї—М—О —В–µ—А–∞–њ–Є–Є —П–≤–ї—П–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Њ—В–і–µ–ї—М–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –±–µ–Ј —А–∞–Ј–≤–Є—В–Є—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ–є –≥–Є–њ–Њ–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Є–ї–Є —А–∞–Ј–і—А–∞–ґ–µ–љ–Є—П –≤ –Њ–Ї—А—Г–ґ–µ–љ–Є–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ –њ–Є–≥–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–ґ–Є. –Э–∞–њ—А–Є–Љ–µ—А, —Б–∞–Љ—Л–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ –ї–µ—З–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П —В–Њ–њ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–∞–Ј–µ–є –љ–∞ –Њ—Б–љ–Њ–≤–µ –≥–Є–і—А–Њ—Е–Є–љ–Њ–љ–∞ [7]. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ, —Б—Г—Й–µ—Б—В–≤—Г—О—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Њ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≥–Є–і—А–Њ—Е–Є–љ–Њ–љ–∞: —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ, –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–є –Ї–Њ–љ—В–∞–Ї—В–љ—Л–є –і–µ—А–Љ–∞—В–Є—В, –Њ–±–µ—Б—Ж–≤–µ—З–Є–≤–∞–љ–Є–µ –љ–Њ–≥—В–µ–є –Є –≥–Є–њ–Њ–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –љ–Њ—А–Љ–∞–ї—М–љ–Њ –Њ–Ї—А–∞—И–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –Ї–Њ–ґ–Є [8].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ, —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–≥–Њ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –Ї–Њ–ґ–Є —П–≤–ї—П–µ—В—Б—П –љ–∞—Б—Г—Й–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л, —В—А–µ–±—Г—О—Й–µ–є –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї –ї–µ—З–µ–љ–Є—О. –Я—А–Њ–≤–µ–і–µ–љ–љ—Л–є –љ–∞–Љ–Є —А–∞–љ–µ–µ –∞–љ–∞–ї–Є–Ј –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –Њ–±–µ—Б–њ–µ—З–µ–љ–љ–Њ—Б—В—М—О –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Љ–∞–≥–љ–Є–µ–Љ –Є —Б–Њ—Б—В–Њ—П–љ–Є–µ–Љ –Ї–Њ–ґ–Є –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ—Л–є –і–µ—Д–Є—Ж–Є—В –Љ–∞–≥–љ–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї —Г—Б–Ї–Њ—А–µ–љ–Є—О –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ —Б—В–∞—А–µ–љ–Є—П –Ї–ї–µ—В–Њ–Ї –Ї–Њ–ґ–Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П —А–µ–њ–∞—А–∞—Ж–Є–Є –Ф–Э–Ъ –Є –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –≤—Л–ґ–Є–≤–∞–љ–Є—П. –Ф–µ—Д–Є—Ж–Є—В –Љ–∞–≥–љ–Є—П —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –Ј–∞—В—А—Г–і–љ—П–µ—В –Ј–∞–ґ–Є–≤–ї–µ–љ–Є–µ —А–∞–љ –Є –њ—А–Є–≤–Њ–і–Є—В –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –≥—А—Г–±—Л—Е —А—Г–±—Ж–Њ–≤ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Ї—А–∞–є–љ–µ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –≤—Б–µ—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є (—Д–Є–±—А–Њ–±–ї–∞—Б—В–Њ–≤, –Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л—Е –Є —Н–ї–∞—Б—В–Є–љ–Њ–≤—Л—Е —Д–Є–±—А–Є–ї–ї, –≥–µ–ї–µ–Њ–±—А–∞–Ј–љ–Њ–є —Б—А–µ–і—Л), –Ї–Њ—В–Њ—А–∞—П —П–≤–ї—П–µ—В—Б—П —Б—В—А—Г–Ї—В—Г—А–љ–Њ–є –Њ—Б–љ–Њ–≤–Њ–є –Ї–Њ–ґ–Є [9].
–Т –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В–µ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ —В–µ—А–∞–њ–Є–Є –љ–∞—А—Г—И–µ–љ–Є–є –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є – –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–ї–µ–є –Љ–∞–≥–љ–Є—П. –†–∞—Б—Б–Љ–Њ—В—А–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л —Д—Г–љ–і–∞–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —Б—Д–Њ—А–Љ—Г–ї–Є—А–Њ–≤–∞–љ—Л –љ–∞–Є–±–Њ–ї–µ–µ –≤–µ—А–Њ—П—В–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Љ–∞–≥–љ–Є—П –љ–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є.
–Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –Њ—Ж–µ–љ–Ї–µ —Б—В–µ–њ–µ–љ–Є –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є
–Ф–µ—А–Љ–∞—В–Њ–ї–Њ–≥–Є –Є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В—Л –њ–Њ —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ–µ –Є–Љ–µ—О—В –і–µ–ї–Њ —Б –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Б—В—А—Г–Ї—В—Г—А—Л –Є –Њ–Ї—А–∞—Б–Ї–Є –Ї–Њ–ґ–Є –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –≤ –Њ–±–ї–∞—Б—В–Є –ї–Є—Ж–∞, —И–µ–Є –Є –Ї–Є—Б—В–µ–є —А—Г–Ї. –І–∞—Й–µ –≤—Б–µ–≥–Њ –љ–∞ –њ—А–∞–Ї—В–Є–Ї–µ –≤—А–∞—З —Б—В–∞–ї–Ї–Є–≤–∞–µ—В—Б—П —Б –њ—А–Њ–±–ї–µ–Љ–Њ–є –ї–µ—З–µ–љ–Є—П –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л—Е –Њ—З–∞–≥–Њ–≤ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є. –Т–Њ–Ј–љ–Є–Ї–∞–µ—В –≤–Њ–њ—А–Њ—Б –Њ–±—К–µ–Ї—В–Є–≤–Є–Ј–∞—Ж–Є–Є –љ–∞–±–ї—О–і–µ–љ–Є–є –≤—А–∞—З–∞ –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є —Б—В–µ–њ–µ–љ–Є –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –і–Њ –Є –њ–Њ—Б–ї–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Ш—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ –≤ —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е –ї–µ—В —Ж–≤–µ—В–Њ–≤—Л–µ —И–Ї–∞–ї—Л –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Г—Б–њ–µ—И–љ–Њ –і–Њ–њ–Њ–ї–љ—П—О—В—Б—П –љ–Њ–≤—Л–Љ–Є –∞–њ–њ–∞—А–∞—В–љ—Л–Љ–Є –Љ–µ—В–Њ–і–Є–Ї–∞–Љ–Є. –†–∞—Б—Б–Љ–Њ—В—А–Є–Љ –≤–Ї—А–∞—В—Ж–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Љ–µ—В–Њ–і—Л –Њ—Ж–µ–љ–Ї–Є –Ї–Њ–ї–Њ—А–Є—Б—В–Є–Ї–Є –Ї–Њ–ґ–Є.
–Ю–Ї—А–∞—Б–Ї–∞ –Ї–Њ–ґ–Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –Ї—А–∞—Б–Є—В–µ–ї–µ–є, –Є–ї–Є –њ–Є–≥–Љ–µ–љ—В–Њ–≤, –≤ –µ–µ —Б–ї–Њ—П—Е. –Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –њ–Є–≥–Љ–µ–љ—В–∞–Љ–Є —П–≤–ї—П—О—В—Б—П –Љ–µ–ї–∞–љ–Є–љ –Є –њ–Њ—А—Д–Є—А–Є–љ—Л (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ) [10,11]. –Т—Л—Б–Њ–Ї–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Љ–µ–ї–∞–љ–Є–љ–∞ –Є –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ —П–≤–ї—П—О—В—Б—П –Љ–∞—А–Ї–µ—А–∞–Љ–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Ї–Њ–ґ–Є –Є –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –љ–∞—А—Г—И–∞—О—В –µ–µ —А–Є—Б—Г–љ–Њ–Ї.
–Ь–µ–ї–∞–љ–Є–љ –Ј–∞–ї–µ–≥–∞–µ—В –љ–∞ —А–∞–Ј–љ—Л—Е –≥–ї—Г–±–Є–љ–∞—Е –≤ –њ—А–µ–і–µ–ї–∞—Е —Н–њ–Є–і–µ—А–Љ–Є—Б–∞. –Т –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є, –Ј–і–Њ—А–Њ–≤–Њ–є –Ї–Њ–ґ–µ —З–∞—Б—В–Є—Ж—Л –Љ–µ–ї–∞–љ–Є–љ–∞ –Њ—З–µ–љ—М –Љ–∞–ї—Л –Є —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ—Л, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –≥–ї–∞–і–Ї–Є–є, —А–Њ–≤–љ—Л–є —В–Њ–љ –Ї–Њ–ґ–Є. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ—В–ї–Њ–ґ–µ–љ–Є–є –Љ–µ–ї–∞–љ–Є–љ–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–Ј–≤–∞–љ–Њ –і–ї–Є—В–µ–ї—М–љ—Л–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –£–§–Ю –Є–ї–Є –Ї–Њ–ґ–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є (–љ–∞–њ—А–Є–Љ–µ—А, —Г–≥—А–µ–≤–Њ–є —Б—Л–њ—М—О). –Ґ–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л–µ «–£–§–Ю––њ—П—В–љ–∞» –Њ—В—А–∞–ґ–∞—О—В –Њ–±—Й–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –Ї–Њ–ґ–Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –£–§–Ю––Њ–±–ї—Г—З–µ–љ–Є—П – –Љ–µ–љ—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ, –Љ–µ–љ—М—И–∞—П –њ–ї–Њ—Й–∞–і—М –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –њ—П—В–µ–љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—В –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Ї–Њ–ґ–Є.
–Я–Њ–≤—Л—И–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ (–≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞) –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ—П–≤–ї–µ–љ–Є—О –Ї—А–∞—Б–љ—Л—Е –њ—П—В–µ–љ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є. –Я—А–Є –Љ–Є–Ї—А–Њ—В—А–∞–≤–Љ–∞—В–Є–Ј–∞—Ж–Є–Є –Ї–Њ–ґ–Є –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ –њ–µ—А–µ–Љ–µ—Й–∞–µ—В—Б—П –Є–Ј —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б—В—А—Г–Ї—В—Г—А –≤ —Б–Њ—Б–Њ—З–Ї–Њ–≤—Л–є —Б–ї–Њ–є –і–µ—А–Љ—Л. –Э–µ–Ї–Њ—В–Њ—А—Л–µ –Ї–Њ–ґ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —В–∞–Ї–Є–µ –Ї–∞–Ї –∞–Ї–љ–µ, —А–Њ–Ј–∞—Ж–µ–∞, —В–µ–ї–µ–∞–љ–≥–Є—Н–Ї—В–∞–Ј–Є–Є, –њ—А–Є–≤–Њ–і—П—В –Ї –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ –≤ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б—В—А—Г–Ї—В—Г—А–∞—Е –Є –њ–Њ–≤—Л—И–∞—О—В —Г—А–Њ–≤–µ–љ—М –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ –≤ –Ї–Њ–ґ–µ. –Я–Њ—А—Д–Є—А–Є–љ–Њ–≤—Л–µ –њ—П—В–љ–∞ —В–∞–Ї–ґ–µ –Љ–Њ–≥—Г—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П –Ї–∞–Ї –Ї–Њ—Б–≤–µ–љ–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Њ–ґ–Є (—Г—А–Њ–≤–љ–Є –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ –≤—Л—И–µ –њ—А–Є –±–Њ–ї—М—И–µ–Љ —З–Є—Б–ї–µ –±–∞–Ї—В–µ—А–Є–є), –Љ–µ–љ—М—И–µ–µ —З–Є—Б–ї–Њ –±–∞–Ї—В–µ—А–Є–є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—О –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є –Љ–Є–Ї—А–Њ—В—А–µ—Й–Є–љ –Ї–Њ–ґ–Є.
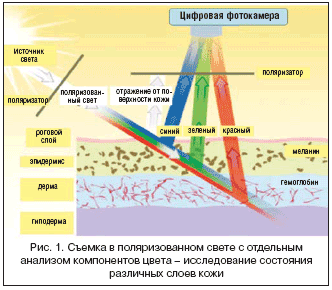
–Я–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –Ї–Њ–ґ–Є –љ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ—Ж–µ–љ–µ–љ–∞ —В–Њ–ї—М–Ї–Њ —З–µ—А–µ–Ј –µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–∞ –Њ–±—Л—З–љ—Л—Е —Д–Њ—В–Њ–≥—А–∞—Д–Є—П—Е, –і–∞–ґ–µ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–∞–Ј—А–µ—И–µ–љ–Є–µ–Љ. –Я–Њ—Н—В–Њ–Љ—Г –і–ї—П –±–Њ–ї–µ–µ –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ —Б—К–µ–Љ–Ї–∞ –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –Њ—Б–≤–µ—Й–µ–љ–Є—П [12]. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, —В–µ—Е–љ–Њ–ї–Њ–≥–Є—П VISIA – —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ –љ–Њ–≤–∞—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–∞—П –њ—А–Њ–≥—А–∞–Љ–Љ–љ–Њ––∞–њ–њ–∞—А–∞—В–љ–∞—П —Б–Є—Б—В–µ–Љ–∞, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–∞—П –і–µ–ї–∞—В—М —Ж–Є—Д—А–Њ–≤—Л–µ —Д–Њ—В–Њ–≥—А–∞—Д–Є–Є –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –Њ—Б–≤–µ—Й–µ–љ–Є—П (–њ–Њ–ї—П—А–Є–Ј–Њ–≤–∞–љ–љ—Л–є —Б–≤–µ—В, –£–§–Ю –Є –і—А.) –Є –њ—А–Њ–≤–Њ–і–Є—В—М –Є—Е –∞–љ–∞–ї–Є–Ј –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л—Е –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Л—Е –∞–ї–≥–Њ—А–Є—В–Љ–Њ–≤. –Ф–∞–љ–љ–∞—П —В–µ—Е–љ–Њ–ї–Њ–≥–Є—П (–Є–Ј–≤–µ—Б—В–љ–∞ –Ї–∞–Ї RBX, –Њ—В –∞–љ–≥–ї. Red/Brown/X, —В.–µ. –Ї—А–∞—Б–љ—Л–є/–Ї–Њ—А–Є—З–љ–µ–≤—Л–є/–•–—Б–њ–µ–Ї—В—А) –≤—Б–µ —И–Є—А–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –і–µ—А–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –Є —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ–µ –і–ї—П –Є–Ј—Г—З–µ–љ–Є—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–Ї–ї–Є–Ї–∞ –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –њ—А–Њ—Ж–µ–і—Г—А [13–15].
–Р–≤—В–Њ–Љ–∞—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —З–Є—Б–ї–∞, –њ–ї–Њ—Й–∞–і–Є –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –Љ–µ–ї–∞–љ–Є–љ–Њ–≤—Л—Е (–£–§–Ю) –Є –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤—Л—Е –њ—П—В–µ–љ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–∞—В—М –Њ–±—К–µ–Ї—В–Є–≤–љ—Г—О –Њ—Ж–µ–љ–Ї—Г —Б–Њ—Б—В–Њ—П–љ–Є—П –Ї–Њ–ґ–Є –ї–Є—Ж–∞ —Б –њ–Њ–і—А–Њ–±–љ—Л–Љ –Њ–њ–Є—Б–∞–љ–Є–µ–Љ –њ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ: –Љ–Њ—А—Й–Є–љ—Л, –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –Ї–Њ–ґ–Є, —А–∞–Ј–Љ–µ—А –њ–Њ—А, —Ж–≤–µ—В –Ї–Њ–ґ–Є, –Њ—Ж–µ–љ–Ї–∞ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –±–∞–Ї—В–µ—А–Є–є, —Б–Ї—А—Л—В–∞—П –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –Ї–Њ–ґ–Є, –≤—Л–Ј–≤–∞–љ–љ–∞—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —Б–Њ–ї–љ—Ж–∞ [16–18]. –Ш–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–Є –Љ–µ–ї–∞–љ–Є–љ–∞ –Є –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ –≤ –Ї–Њ–ґ–µ –њ–Њ–ї—Г—З–∞–µ—В—Б—П —Б –њ–Њ–Љ–Њ—Й—М—О –Љ—Г–ї—М—В–Є—Б–њ–µ–Ї—В—А–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –≤–Ї–ї—О—З–∞—О—В —А–∞–Ј–і–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј —Д—Г–љ–і–∞–Љ–µ–љ—В–∞–ї—М–љ—Л—Е —Ж–≤–µ—В–Њ–≤—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П (–Ї—А–∞—Б–љ–Њ–≥–Њ, –Ј–µ–ї–µ–љ–Њ–≥–Њ –Є —Б–Є–љ–µ–≥–Њ) [19,20] (—А–Є—Б. 1).
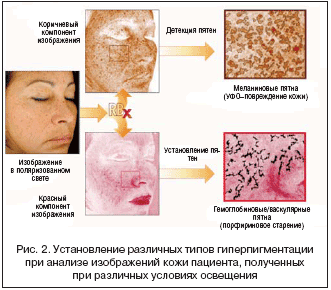
–°—К–µ–Љ–Ї–∞ –Ї–Њ–ґ–Є –њ–∞—Ж–Є–µ–љ—В–∞ –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –Њ—Б–≤–µ—Й–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ–≤–µ—Б—В–Є —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –љ–∞ –Њ—Б–љ–Њ–≤–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤ –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ —А–∞—Б–њ–Њ–Ј–љ–∞—О—В—Б—П –Љ–µ–ї–∞–љ–Є–љ–Њ–≤—Л–µ –Є –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤—Л–µ –њ—П—В–љ–∞ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є, –і–µ—Д–µ–Ї—В—Л —Б—В—А—Г–Ї—В—Г—А—Л –Ї–Њ–ґ–Є –Є –і—А. –Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –∞–љ–∞–ї–Є–Ј–∞ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –њ—А–Є—Б–≤–∞–Є–≤–∞—О—В—Б—П –±–∞–ї–ї—М–љ—Л–µ –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –Ї–Њ–ґ–Є –ї–Є—Ж–∞ –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –Љ–Њ—А—Й–Є–љ, –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є, —А–∞–Ј–Љ–µ—А—Г –њ–Њ—А, —Б–Њ–і–µ—А–ґ–∞–љ–Є—О –±–∞–Ї—В–µ—А–Є–є (–њ–Њ—А—Д–Є—А–Є–љ–Њ–≤—Л–µ –њ—П—В–љ–∞), –£–§–Ю––њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є (–Љ–µ–ї–∞–љ–Є–љ–Њ–≤—Л–µ –њ—П—В–љ–∞) –Є –і—А. (—А–Є—Б. 2).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –∞–њ–њ–∞—А–∞—В–љ–Њ––њ—А–Њ–≥—А–∞–Љ–Љ–љ—Л–µ –Љ–µ—В–Њ–і–Є–Ї–Є –њ–Њ–Ј–≤–Њ–ї—П—О—В –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ –Њ—Ж–µ–љ–Є–≤–∞—В—М —А–µ–Ј—Г–ї—М—В–∞—В—Л —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є. –Ч–∞–Љ–µ—В–Є–Љ, —З—В–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є —В—А—Г–і–љ–Њ –Њ–ґ–Є–і–∞—В—М –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б—А–µ–і—Б—В–≤ –і–ї—П —Г—Б—В—А–∞–љ–µ–љ–Є—П –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є. –Ю–њ–Є—Б–∞–љ–љ—Л–µ –≤—Л—И–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –Љ–Њ–≥—Г—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ–і—Е–Њ–і–Њ–≤ –Ї –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Љ–Є–љ–µ—А–∞–ї—М–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–∞–≥–љ–Є—П.
–£—А–Њ–≤–љ–Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Љ–∞–≥–љ–Є—П
–љ–∞ –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—О –Ї–Њ–ґ–Є
–Ф–µ—Д–Є—Ж–Є—В –Љ–∞–≥–љ–Є—П —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј–≤–Є—В–Є—О –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —Г–њ—А–∞–≤–ї–µ–љ–Є—П –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–∞–Љ–Є.
–Я—А–Њ–≤–µ–і–µ–љ–љ—Л–є –≤ –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В–µ —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј —Г—З–∞—Б—В–Є—П –Љ–∞–≥–љ–Є—П –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є —А–Њ–≤–љ–Њ–є, —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –Љ–∞–≥–љ–Є–є –Љ–Њ–ґ–µ—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—О –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ –њ–Њ —З–µ—В—Л—А–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л–Љ —Г—А–Њ–≤–љ—П–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П. –Т–Њ––њ–µ—А–≤—Л—Е, –Љ–∞–≥–љ–Є–є —А–µ–≥—Г–ї–Є—А—Г–µ—В —Б–µ–Ї—А–µ—Ж–Є—О –Љ–µ–ї–∞–љ–Є–љ–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б –≥–ї—Г—В–∞–Љ–∞—В–љ—Л–Љ–Є —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є. –Т–Њ––≤—В–Њ—А—Л—Е, –Љ–∞–≥–љ–Є–є –њ—А–Є–љ–Є–Љ–∞–µ—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–µ —Г—З–∞—Б—В–Є–µ –≤ –њ–µ—А–µ–і–∞—З–µ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ —Б–Є–≥–љ–∞–ї–∞ –Њ—В —А–µ—Ж–µ–њ—В–Њ—А–∞ –Љ–µ–ї–∞–љ–Є–љ–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ –Є –і—А—Г–≥–Є—Е –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤. –Т–—В—А–µ—В—М–Є—Е, –Љ–∞–≥–љ–Є–є –Љ–Њ–ґ–µ—В –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М —В–Є—А–Њ–Ј–Є–љ–∞–Ј—Г – —Д–µ—А–Љ–µ–љ—В —Б–Є–љ—В–µ–Ј–∞ –Љ–µ–ї–∞–љ–Є–љ–∞. –Т–—З–µ—В–≤–µ—А—В—Л—Е, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—П —Б—В—А—Г–Ї—В—Г—А—Г —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –Љ–∞–≥–љ–Є–є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –±–Њ–ї–µ–µ —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–Љ—Г —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—О –Љ–µ–ї–∞–љ–Є–љ–∞ –≤ –Ї–Њ–ґ–µ. –†–∞—Б—Б–Љ–Њ—В—А–Є–Љ —Н—В–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Љ–∞–≥–љ–Є—П –±–Њ–ї–µ–µ –њ–Њ–і—А–Њ–±–љ–Њ.
–Ь–∞–≥–љ–Є–є –Є –њ—А–Њ—Ж–µ—Б—Б—Л —Б–µ–Ї—А–µ—Ж–Є–Є –Љ–µ–ї–∞–љ–Є–љ–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞. –Ь–µ–ї–∞–љ–Њ—Ж–Є—В–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–µ –≥–Њ—А–Љ–Њ–љ—Л —Б—А–µ–і–љ–µ–є –і–Њ–ї–Є –≥–Є–њ–Њ—Д–Є–Ј–∞ —Б—В–Є–Љ—Г–ї–Є—А—Г—О—В —Б–Є–љ—В–µ–Ј –Є —Б–µ–Ї—А–µ—Ж–Є—О –Љ–µ–ї–∞–љ–Є–љ–∞ —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є––Љ–µ–ї–∞–љ–Њ—Ж–Є—В–∞–Љ–Є –Ї–Њ–ґ–Є –Є –≤–Њ–ї–Њ—Б—П–љ–Њ–є –ї—Г–Ї–Њ–≤–Є—Ж—Л. –Э–∞–Є–±–Њ–ї–µ–µ —Б–Є–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—О –Ї–Њ–ґ–Є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В α––Љ–µ–ї–∞–љ–Њ—Ж–Є—В–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–є –≥–Њ—А–Љ–Њ–љ (α–MSH).
–Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ N––Љ–µ—В–Є–ї–D––∞—Б–њ–∞—А–∞–≥–Є–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ (NMDA) –≤ –Ї—Г–ї—М—В—Г—А–µ –Ї–ї–µ—В–Њ–Ї –≥–Є–њ–Њ—В–∞–ї–∞–Љ—Г—Б–∞ —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–ї–∞ —Б–µ–Ї—А–µ—Ж–Є—О α–MSH –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Њ—Б–Њ–±–Њ–є —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В–Є NMDA–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л, –Ї–∞–Ї –Є –і—А—Г–≥–Є–µ –≤–Є–і—Л NMDA–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —Б–Њ–і–µ—А–ґ–∞–ї–Є —Б–∞–є—В –і–ї—П —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –Љ–∞–≥–љ–Є—П. –Я–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ–µ–є –Љ–∞–≥–љ–Є—П –≤ –Ї—Г–ї—М—В—Г—А–µ –і–Њ 5 –Љ–Љ–Њ–ї—М/–ї —В–Њ—А–Љ–Њ–Ј–Є–ї–Њ —Б–µ–Ї—А–µ—Ж–Є—О α–MSH, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ–Є—В–∞—В–µ–ї—М–љ–Њ–є —Б—А–µ–і—Л, –Њ–±–µ–і–љ–µ–љ–љ–Њ–є –Љ–∞–≥–љ–Є–µ–Љ, —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ —Г—Б–Є–ї–µ–љ–љ–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ –Ї–ї–µ—В–Ї–∞–Љ–Є –≥–Є–њ–Њ—В–∞–ї–∞–Љ—Г—Б–∞ [21].
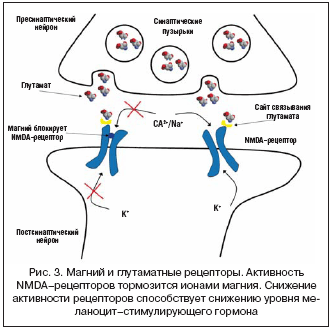
–Р–Ї—В–Є–≤–∞—Ж–Є—П NMDA–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –ї–µ–ґ–Є—В –≤ –Њ—Б–љ–Њ–≤–µ –±—Л—Б—В—А–Њ–є —Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Њ–є –њ–µ—А–µ–і–∞—З–Є —Б–Є–≥–љ–∞–ї–Њ–≤ –≤ –¶–Э–°. –Ш–Ј–Љ–µ–љ—П—П –њ–Њ—В–Њ–Ї–Є Na+/K+ —З–µ—А–µ–Ј –Љ–µ–Љ–±—А–∞–љ—Г, NMDA–—А–µ—Ж–µ–њ—В–Њ—А—Л –њ–µ—А–µ–і–∞—О—В —Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Є–є —Б–Є–≥–љ–∞–ї –Ї —Н—Д—Д–µ–Ї—В–Њ—А–љ—Л–Љ —Б–Є—Б—В–µ–Љ–∞–Љ [22]. –Т –љ–µ–∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ–µ –Ї–∞–љ–∞–ї —А–µ—Ж–µ–њ—В–Њ—А–∞ –Ј–∞–Ї—А—Л—В –Є–Њ–љ–Њ–Љ –Љ–∞–≥–љ–Є—П, –Ї–Њ—В–Њ—А—Л–є —Г–і–∞–ї—П–µ—В—Б—П –њ—А–Є –і–µ–њ–Њ–ї—П—А–Є–Ј–∞—Ж–Є–Є –њ–Њ—Б—В—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б —Н—В–Є–Љ –і–ї—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П —А–µ—Ж–µ–њ—В–Њ—А–∞ –≤ —Б–Є–љ–∞–њc –і–Њ–ї–ґ–µ–љ –њ–Њ—Б—В—Г–њ–Є—В—М –∞–≥–Њ–љ–Є—Б—В (–≥–ї—Г—В–∞–Љ–∞—В). –Т –љ–Њ—А–Љ–µ —В–∞–Ї–∞—П –∞–Ї—В–Є–≤–∞—Ж–Є—П —А–µ—Ж–µ–њ—В–Њ—А–∞ –≤—Л–Ј—Л–≤–∞–µ—В –Њ—В–Ї—А—Л—В–Є–µ –Є–Њ–љ–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, —З—В–Њ –≤–µ–і–µ—В –Ї –њ—А–Є—В–Њ–Ї—Г –≤ –Ї–ї–µ—В–Ї—Г Na+ –Є Ca2+ (—А–Є—Б. 3). –Ш–Њ–љ—Л –Ї–∞–ї—М—Ж–Є—П, –≤–Њ—И–µ–і—И–Є–µ —З–µ—А–µ–Ј –Ї–∞–љ–∞–ї NMDA–—А–µ—Ж–µ–њ—В–Њ—А–∞, –∞–Ї—В–Є–≤–Є—А—Г—О—В –°–∞––Ј–∞–≤–Є—Б–Є–Љ—Г—О –њ—А–Њ—В–µ–Є–љ–Ї–Є–љ–∞–Ј—Г II (CaMK–II), –Ї–Њ—В–Њ—А–∞—П –Є –Ј–∞–њ—Г—Б–Ї–∞–µ—В –њ—А–Њ—Ж–µ—Б—Б—Л —Б–Є–љ—В–µ–Ј–∞/—Б–µ–Ї—А–µ—Ж–Є–Є –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞.
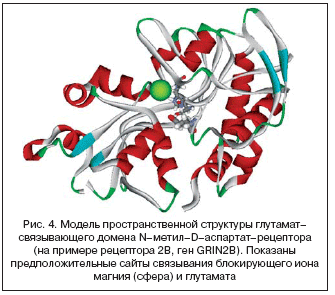
–Ь–∞–≥–љ–Є–є –±–ї–Њ–Ї–Є—А—Г–µ—В –Є–Њ–љ–љ—Л–µ –Ї–∞–љ–∞–ї—Л NMDA–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —А–∞–Ј–љ–Њ—Б—В–Є –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–≤ –љ–∞ –Ї–ї–µ—В–Њ—З–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ–µ. –Я—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞
NMDA–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (—А–Є—Б. 4) —Г—Б—В—А–Њ–µ–љ–∞ —В–∞–Ї, —З—В–Њ —А–µ—Ж–µ–њ—В–Њ—А—Л –±–ї–Њ–Ї–Є—А—Г—О—В—Б—П –Є–Њ–љ–∞–Љ–Є –Љ–∞–≥–љ–Є—П –Є –±—Г–і—Г—В —А–µ–∞–≥–Є—А–Њ–≤–∞—В—М –љ–∞ –≥–ї—Г—В–∞–Љ–∞—В —В–Њ–ї—М–Ї–Њ –њ—А–Є —Г–і–∞–ї–µ–љ–Є–Є –Љ–∞–≥–љ–Є–є––Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –±–ї–Њ–Ї–∞–і—Л [23].
–Ь–∞–≥–љ–Є–є –Є —А–µ—Ж–µ–њ—В–Њ—А—Л –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –≤ –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–∞—Е. –Я–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –Ї–Њ–ґ–љ—Л—Е –њ–Њ–Ї—А–Њ–≤–Њ–≤ —А–µ–≥—Г–ї–Є—А—Г–µ—В—Б—П —Б–ї–Њ–ґ–љ–Њ–є —Б–µ—В—М—О –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є –Љ–µ–ґ–і—Г —Ж–Є—В–Њ–Ї–Є–љ–∞–Љ–Є –Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Њ—Б—В–∞ –Ї–µ—А–∞—В–Є–љ–Њ—Ж–Є—В–Њ–≤/—Д–Є–±—А–Њ–±–ї–∞—Б—В–Њ–≤. –Я–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П –Ї–Њ–ґ–Є, –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–∞—П —Г–ї—М—В—А–∞—Д–Є–Њ–ї–µ—В–Њ–≤—Л–Љ –Є–Ј–ї—Г—З–µ–љ–Є–µ–Љ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б–µ–Ї—А–µ—Ж–Є–µ–є –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ –Ї–µ—А–∞—В–Є–љ–Њ—Ж–Є—В–∞–Љ–Є –Є —Д–Є–±—А–Њ–±–ї–∞—Б—В–∞–Љ–Є –≤ –Њ–±–ї—Г—З–µ–љ–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –Ї–Њ–ґ–Є. –Я—А–Є –±–Є–Њ–њ—Б–Є–Є –≤ —Г—З–∞—Б—В–Ї–∞—Е –Ї–Њ–ґ–Є —Б –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–µ–є —В–∞–Ї–ґ–µ –±—Л–ї–Є –љ–∞–є–і–µ–љ—Л –њ–Њ–≤—Л—И–µ–љ–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Д–∞–Ї—В–Њ—А–∞ —А–Њ—Б—В–∞ –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ (HGF), —Д–∞–Ї—В–Њ—А–∞ —А–Њ—Б—В–∞ –Ї–µ—А–∞—В–Є–љ–Њ—Ж–Є—В–Њ–≤ (KGF) –Є —Д–∞–Ї—В–Њ—А–∞ —Б—В–≤–Њ–ї–Њ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї (SCF) [24].
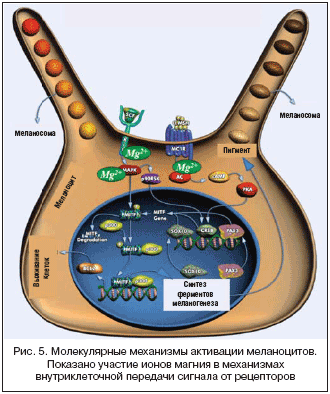
–Я—А–Њ—Ж–µ—Б—Б—Л —Б–Є–љ—В–µ–Ј–∞ –Є —Б–µ–Ї—А–µ—Ж–Є–Є –Љ–µ–ї–∞–љ–Є–љ–∞ –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Ј–∞–≤–Є—Б—П—В –Њ—В –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Љ–∞–≥–љ–Є—П –≤–љ—Г—В—А–Є –Ї–ї–µ—В–Ї–Є. –Ґ–∞–Ї, –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ —В—А–Є –Ї–ї—О—З–µ–≤—Л—Е —Д–µ—А–Љ–µ–љ—В–∞ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–≥–Њ –Ї–∞—Б–Ї–∞–і–∞ —Г–њ—А–∞–≤–ї–µ–љ–Є—П —Г—А–Њ–≤–љ–µ–Љ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Љ–µ–ї–∞–љ–Є–љ–∞ —П–≤–ї—П—О—В—Б—П –Љ–∞–≥–љ–Є–є––Ј–∞–≤–Є—Б–Є–Љ—Л–Љ–Є (—А–Є—Б. 5): —А–µ—Ж–µ–њ—В–Њ—А KIT —Д–∞–Ї—В–Њ—А–∞ —А–Њ—Б—В–∞ —Б—В–≤–Њ–ї–Њ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї (SCF), —Г–њ—А–∞–≤–ї—П—О—Й–Є–є –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–Њ–≤; —Д–µ—А–Љ–µ–љ—В –Ь–Р–†–Ъ, –њ–µ—А–µ–і–∞—О—Й–Є–є —Б–Є–≥–љ–∞–ї –Њ—В —А–µ—Ж–µ–њ—В–Њ—А–∞ KIT; —Д–µ—А–Љ–µ–љ—В –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј—Л (–Р–°), –њ–µ—А–µ–і–∞—О—Й–µ–є —Б–Є–≥–љ–∞–ї –Њ—В G––±–µ–ї–Њ–Ї––Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ —А–µ—Ж–µ–њ—В–Њ—А–∞ —Г–њ–Њ–Љ–Є–љ–∞–µ–Љ–Њ–≥–Њ —А–∞–љ–µ–µ α––Љ–µ–ї–∞–љ–Њ—Ж–Є—В–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ (α–MSH).
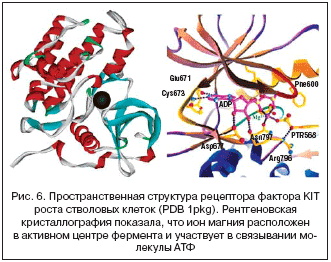
–†–µ—Ж–µ–њ—В–Њ—А–Њ–Љ —Д–∞–Ї—В–Њ—А–∞ —А–Њ—Б—В–∞ —Б—В–≤–Њ–ї–Њ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї —П–≤–ї—П–µ—В—Б—П –±–µ–ї–Њ–Ї KIT, –Ї–Њ—В–Њ—А—Л–є –Є–≥—А–∞–µ—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –Љ–µ–ї–∞–љ–Њ–≥–µ–љ–µ–Ј–µ, –љ–Њ –Є –≤ —А–µ–≥—Г–ї—П—Ж–Є–Є –≤—Л–ґ–Є–≤–∞–љ–Є—П –Ї–ї–µ—В–Њ–Ї –Є –Ї—А–Њ–≤–µ—В–≤–Њ—А–µ–љ–Є–Є. –Ф–µ—Д–µ–Ї—В—Л –≥–µ–љ–∞ KIT —П–≤–ї—П—О—В—Б—П –њ—А–Є—З–Є–љ–Њ–є –≤—А–Њ–ґ–і–µ–љ–љ–Њ–є –∞–љ–Њ–Љ–∞–ї–Є–Є —А–∞–Ј–≤–Є—В–Є—П –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є (–Ї–Њ–і –њ–Њ MIM 172800), —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–µ–є—Б—П —З–µ—А–µ–і–Њ–≤–∞–љ–Є–µ–Љ –±–µ–ї—Л—Е –Є —В–µ–Љ–љ—Л—Е –њ—П—В–µ–љ –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Њ–ґ–Є [25]. –Ф–∞–љ–љ—Л–є –±–µ–ї–Њ–Ї —Б–Њ–і–µ—А–ґ–Є—В –Є–Њ–љ –Љ–∞–≥–љ–Є—П –≤ –∞–Ї—В–Є–≤–љ–Њ–Љ —Ж–µ–љ—В—А–µ (—А–Є—Б. 6) [26]. –Э–µ–і–Њ—Б—В–∞—В–Њ–Ї –Љ–∞–≥–љ–Є—П –±—Г–і–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –њ–∞–і–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —А–µ—Ж–µ–њ—В–Њ—А–∞, –љ–∞—А—Г—И–∞—В—М —А–µ–≥—Г–ї—П—Ж–Є—О —Б–Є–љ—В–µ–Ј–∞ –Љ–µ–ї–∞–љ–Є–љ–∞ –Є –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –њ—П—В–µ–љ –Ї–∞–Ї —Б –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –Љ–µ–ї–∞–љ–Є–љ–∞, —В–∞–Ї –Є –њ—П—В–µ–љ —Б –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–µ–є. –≠—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–µ—А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–Љ—Г —В–Њ–љ—Г –Ї–Њ–ґ–Є.
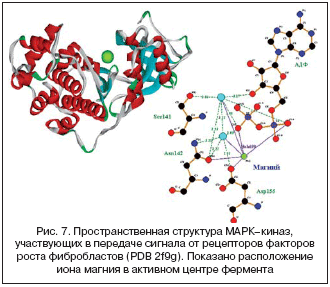
–Ь–∞–≥–љ–Є–є —П–≤–ї—П–µ—В—Б—П –Є–љ—В–µ–≥—А–∞–ї—М–љ–Њ–є —Б–Њ—Б—В–∞–≤–ї—П—О—Й–µ–є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —Ж–µ–љ—В—А–∞ –Љ–Є—В–Њ–≥–µ–љ––∞–Ї—В–Є–≤–Є—А—Г–µ–Љ—Л—Е –Ь–Р–†–Ъ––Ї–Є–љ–∞–Ј (–∞–љ–≥–ї. Mitogen–Activated Protein Kinase, —А–Є—Б. 7). –£—З–∞—Б—В–≤—Г—П –≤ –њ–µ—А–µ–і–∞—З–µ —Б–Є–≥–љ–∞–ї–∞ –Њ—В —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–Њ–≤, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —А–µ—Ж–µ–њ—В–Њ—А–∞ —Д–∞–Ї—В–Њ—А–∞ KIT —А–Њ—Б—В–∞ —Б—В–≤–Њ–ї–Њ–≤—Л—Е –Ї–ї–µ—В–Њ–Ї, –і–∞–љ–љ–∞—П –≥—А—Г–њ–њ–∞ –Ї–Є–љ–∞–Ј –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤–Њ–≤–ї–µ—З–µ–љ–∞ –≤ —А–∞–Ј–ї–Є—З–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л –ґ–Є–Ј–љ–µ–і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є —Н—В–Є—Е –Ї–ї–µ—В–Њ–Ї [27].
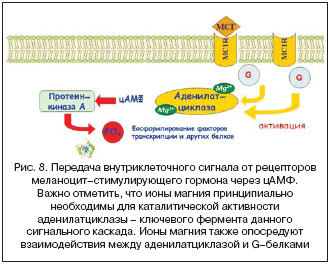
G––±–µ–ї–Њ–Ї––Ј–∞–≤–Є—Б–Є–Љ—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ –∞–Ї—В–Є–≤–Є—А—Г—О—В –Љ–∞–≥–љ–Є–є––Ј–∞–≤–Є—Б–Є–Љ—Л–µ –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј—Л, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ—В–Њ—А—Л—Е –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ –Є—В–Њ–≥–µ –≤–ї–Є—П–µ—В –љ–∞ —Г—А–Њ–≤–љ–Є —Б–µ–Ї—А–µ—Ж–Є–Є –Љ–µ–ї–∞–љ–Є–љ–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б –±–µ–ї–Ї–Њ–Љ G –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –∞–Ї—В–Є–≤–∞—Ж–Є—П —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–∞–≥–љ–Є–є––Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј—Л, –Ї–Њ—В–Њ—А—Л–є —Б–Є–љ—В–µ–Ј–Є—А—Г–µ—В —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–є –∞–і–µ–љ–Є–љ–Љ–Њ–љ–Њ—Д–Њ—Б—Д–∞—В (—Ж–Р–Ь–§) –Є –∞–Ї—В–Є–≤–Є—А—Г–µ—В —Ж–µ–њ—М –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е —Б–Њ–±—Л—В–Є–є, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї —Б–Є–љ—В–µ–Ј—Г –Љ–µ–ї–∞–љ–Є–љ–∞. –Т —Ж–µ–ї–Њ–Љ, —Ж–Р–Ь–§––Ј–∞–≤–Є—Б–Є–Љ—Л–є —Б–Є–≥–љ–∞–ї –њ–µ—А–µ–і–∞–µ—В—Б—П –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ—П—В–Є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ—Л—Е —Б—В–∞–і–Є–є: —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ –ї–Є–≥–∞–љ–і–∞ (–Ь–°–У) —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ, –∞–Ї—В–Є–≤–∞—Ж–Є—П G––±–µ–ї–Ї–∞, –∞–Ї—В–Є–≤–∞—Ж–Є—П –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј—Л –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Г—А–Њ–≤–љ–µ–є —Ж–Р–Ь–§, –∞–Ї—В–Є–≤–∞—Ж–Є—П –њ—А–Њ—В–µ–Є–љ–Ї–Є–љ–∞–Ј—Л –Р –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Д–Њ—Б—Д–Њ—А–Є–ї–Є—А–Њ–≤–∞–љ–Є—П –±–µ–ї–Ї–Њ–≤, –Ї–Њ–Њ—А–і–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –Љ–Њ–і—Г–ї—П—Ж–Є—П —В—А–∞–љ—Б–Ї—А–Є–њ—Ж–Є–Є —Б–Њ—В–µ–љ —А–∞–Ј–ї–Є—З–љ—Л—Е –≥–µ–љ–Њ–≤ (—А–Є—Б. 8).
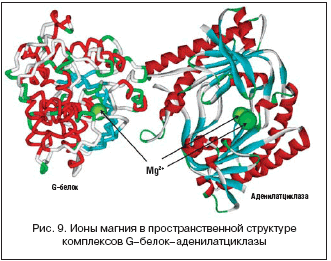
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–∞–≥–љ–Є–є––Ј–∞–≤–Є—Б–Є–Љ—Л–µ –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј—Л —П–≤–ї—П—О—В—Б—П –≤–∞–ґ–љ—Л–Љ–Є –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–Љ–Є –њ–Њ—Б—А–µ–і–љ–Є–Ї–∞–Љ–Є –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞. –Ґ–∞–Ї –Ї–∞–Ї –Є–Њ–љ—Л –Љ–∞–≥–љ–Є—П –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л –і–ї—П –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј—Л –Є –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–Є—П –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є –Љ–µ–ґ–і—Г –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј–Њ–є –Є G––±–µ–ї–Ї–∞–Љ–Є (—А–Є—Б. 9), –і–µ—Д–Є—Ж–Є—В –Љ–∞–≥–љ–Є—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –±—Г–і–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г –њ–∞–і–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј –Є –љ–∞—А—Г—И–µ–љ–Є—О —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–є –≤—Л—А–∞–±–Њ—В–Ї–Є –Љ–µ–ї–∞–љ–Є–љ–∞ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —Г—З–∞—Б—В–Ї–∞—Е –Ї–Њ–ґ–Є. –Я—А–Є —Н—В–Њ–Љ –≤ –Ї–ї–µ—В–Ї–∞—Е —Б –ї—Г—З—И–Є–Љ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ–Љ –Љ–∞–≥–љ–Є–µ–Љ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –ї—Г—З—И–µ–є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Ї–Њ–ґ–Є –≤ –і–∞–љ–љ–Њ–Љ —А–µ–≥–Є–Њ–љ–µ –±—Г–і–µ—В –њ—А–Њ–Є—Б—Е–Њ–і–Є—В—М –∞–Ї—В–Є–≤–љ–∞—П –≤—Л—А–∞–±–Њ—В–Ї–∞ –Љ–µ–ї–∞–љ–Є–љ–∞ (–≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П), –∞ –≤ –Ї–ї–µ—В–Ї–∞—Е —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –Љ–∞–≥–љ–Є—П – –Ј–∞–Љ–µ–і–ї–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –Є —Б–µ–Ї—А–µ—Ж–Є–Є –Љ–µ–ї–∞–љ–Є–љ–∞ (–љ–µ—А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–µ –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –Њ–Ї—А–∞—Б–Ї–Є –Ї–Њ–ґ–Є).
–Ь–∞–≥–љ–Є–є –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В–Є—А–Њ–Ј–Є–љ–∞–Ј—Л. –Ъ–∞–Ї –Њ—В–Љ–µ—З–µ–љ–Њ —А–∞–љ–µ–µ, —Ж–≤–µ—В –Ї–Њ–ґ–Є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —В–Є–њ–Њ–Љ –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ —Б–Є–љ—В–µ–Ј–Є—А—Г–µ–Љ–Њ–≥–Њ –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–∞–Љ–Є –Љ–µ–ї–∞–љ–Є–љ–∞ –Є —Е–∞—А–∞–Ї—В–µ—А–Њ–Љ –µ–≥–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –≤ –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е –Ї–µ—А–∞—В–Є–љ–Њ—Ж–Є—В–∞—Е. –Ь–µ–ї–∞–љ–Є–љ —Б–Є–љ—В–µ–Ј–Є—А—Г–µ—В—Б—П –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —А—П–і–∞ –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є —Б —Г—З–∞—Б—В–Є–µ–Љ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л —В–Є—А–Њ–Ј–Є–љ–∞ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Д–µ—А–Љ–µ–љ—В–∞ —В–Є—А–Њ–Ј–Є–љ–∞–Ј—Л. –Ґ–Є—А–Њ–Ј–Є–љ–∞–Ј–∞ –Ї–∞—В–∞–ї–Є–Ј–Є—А—Г–µ—В –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ –і–≤–µ —А–∞–Ј–ї–Є—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –±–Є–Њ—Б–Є–љ—В–µ–Ј–∞ –Љ–µ–ї–∞–љ–Є–љ–∞ –≤ –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–∞—Е: –≥–Є–і—А–Њ–Ї—Б–Є–ї–Є—А–Њ–≤–∞–љ–Є–µ —В–Є—А–Њ–Ј–Є–љ–∞ –≤ –Ф–Ю–§–Р –Є –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –Ф–Ю–§–Р –≤ –Ф–Ю–§–Р–—Е–Є–љ–Њ–љ [28].
–Ь–µ–і—М—Б–Њ–і–µ—А–ґ–∞—Й–Є–є —Д–µ—А–Љ–µ–љ—В —В–Є—А–Њ–Ј–Є–љ–Ї–Є–љ–∞–Ј–∞ —Г—З–∞—Б—В–≤—Г–µ—В –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є —В–∞–Ї–Є—Е –њ–Є–≥–Љ–µ–љ—В–Њ–≤, –Ї–∞–Ї –Љ–µ–ї–∞–љ–Є–љ—Л –Є –і—А—Г–≥–Є–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –њ–Њ–ї–Є—Д–µ–љ–Њ–ї–Њ–≤. –£—А–Њ–≤–љ–Є —Д–µ—А–Љ–µ–љ—В–∞ –њ–Њ–≤—Л—И–∞—О—В—Б—П –њ–Њ—Б–ї–µ –£–§–Ю –Ї–Њ–ґ–Є. –Э—Г–Ї–ї–µ–Њ—В–Є–і–љ—Л–µ –≤–∞—А–Є–∞—Ж–Є–Є –≥–µ–љ–∞ TYR –њ—А–Є–≤–Њ–і—П—В –Ї –≤–∞—А–Є–∞—Ж–Є–Є –≤ —Ж–≤–µ—В–µ –Ї–Њ–ґ–Є –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –≤–µ—Б–љ—Г—И–µ–Ї. –Ф–µ—Д–µ–Ї—В –≤ –≥–µ–љ–µ —П–≤–ї—П–µ—В—Б—П —З–∞—Б—В–Њ–є –њ—А–Є—З–Є–љ–Њ–є –∞—Г—В–Њ—Б–Њ–Љ–љ–Њ–—А–µ—Ж–µ—Б—Б–Є–≤–љ–Њ–≥–Њ –∞–ї—М–±–Є–љ–Є–Ј–Љ–∞ –≥–ї–∞–Ј.
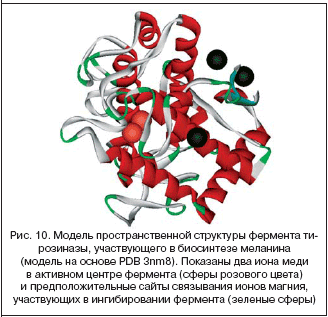
–Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ –Ї—Г–ї—М—В—Г—А—Л –Љ–µ–ї–∞–љ–Њ—Ж–Є—В–Њ–≤, –≤—Л—А–∞—Й–µ–љ–љ—Л–µ –њ—А–Є –љ–Є–Ј–Ї–Њ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–Є –Ї–∞–ї—М—Ж–Є—П –Є –Љ–∞–≥–љ–Є—П –≤ –њ–Є—В–∞—В–µ–ї—М–љ–Њ–є —Б—А–µ–і–µ, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є—Б—М —Б–Є–ї—М–љ–Њ–є –њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–µ–є –Є –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–Є—А–Њ–Ј–Є–љ–∞–Ј—Л [29]. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Є–Њ–љ—Л –Љ–∞–≥–љ–Є—П –Є –Ї–∞–ї—М—Ж–Є—П –Љ–Њ–≥—Г—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ —Г—З–∞—Б—В–≤–Њ–≤–∞—В—М –≤ –љ–µ–Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ–Њ–Љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–Є —В–Є—А–Њ–Ј–Є–љ–∞–Ј—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—П —В–∞–Ї–ґ–µ –њ–Њ–љ–Є–ґ–µ–љ–Є—О —Б—В–∞–±–Є–ї—М–љ–Њ—Б—В–Є —Д–µ—А–Љ–µ–љ—В–∞ [30] (—А–Є—Б. 10). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–∞–≥–љ–Є–є –Љ–Њ–ґ–µ—В –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М —В–Є—А–Њ–Ј–Є–љ–∞–Ј—Г –Є —Г–Љ–µ–љ—М—И–∞—В—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є–Ј–±—Л—В–Њ—З–љ–Њ —Б–Є–љ—В–µ–Ј–Є—А—Г–µ–Љ–Њ–≥–Њ –Љ–µ–ї–∞–љ–Є–љ–∞, —В–µ–Љ —Б–∞–Љ—Л–Љ —Г—Б—В—А–∞–љ—П—П –Њ–і–љ—Г –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—А–Є—З–Є–љ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є.
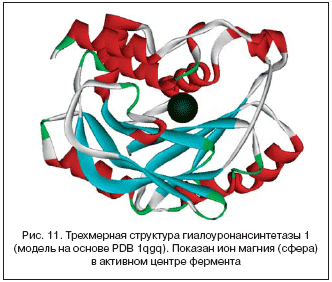
–Ь–∞–≥–љ–Є–є –Є —Б—В—А—Г–Ї—В—Г—А–∞ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є. –Ю—Б–љ–Њ–≤–љ—Л–µ –Љ–∞–Ї—А–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ —Н–ї–µ–Љ–µ–љ—В—Л –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–є –Љ–∞—В—А–Є—Ж—Л: 1) —Д–Њ—А–Љ–Є—А—Г–µ–Љ–∞—П –њ—А–Њ—В–µ–Њ–≥–ї–Є–Ї–∞–љ–∞–Љ–Є –≥–µ–ї–µ–Њ–±—А–∞–Ј–љ–∞—П —Б—А–µ–і–∞, 2) —Б—В—А—Г–Ї—В—Г—А–љ—Л–µ –Є —А–µ—В–Є–Ї—Г–ї—П—А–љ—Л–µ –Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞, 3) –≥–Є–±–Ї–Є–µ —Н–ї–∞—Б—В–Є–љ–Њ–≤—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞ –Є 4) –Ї–ї–µ—В–Ї–Є (—Д–Є–±—А–Њ–±–ї–∞—Б—В—Л). –Ь–∞–≥–љ–Є–є –њ—А–Є–љ–Є–Љ–∞–µ—В —Г—З–∞—Б—В–Є–µ –≤ –њ–Њ–і–і–µ—А–ґ–Ї–µ –≤—Б–µ—Е —Н—В–Є—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є [31]. –Э–∞–њ—А–Є–Љ–µ—А, –≥–Є–∞–ї–Њ—Г—А–Њ–љ–∞–љ—Б–Є–љ—В–µ—В–∞–Ј—Л, —Б–Є–љ—В–µ–Ј–Є—А—Г—О—Й–Є–µ –њ–Њ–ї–Є–Љ–µ—А –≥–Є–∞–ї–Њ—Г—А–Њ–љ–∞–љ, –Њ–±—А–∞–Ј—Г—О—Й–Є–є –≥–µ–ї–µ–≤—Г—О –Њ—Б–љ–Њ–≤—Г, —Б–Њ–і–µ—А–ґ–∞—В –Є–Њ–љ –Љ–∞–≥–љ–Є—П –≤ –∞–Ї—В–Є–≤–љ–Њ–Љ —Ж–µ–љ—В—А–µ (—А–Є—Б. 11). –Ф–µ—Д–Є—Ж–Є—В –Љ–∞–≥–љ–Є—П –±—Г–і–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –њ–Њ–љ–Є–ґ–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≥–Є–∞–ї–Њ—Г—А–Њ–љ–∞–љ—Б–Є–љ—В–µ—В–∞–Ј, —З—В–Њ –≤—Л–Ј–Њ–≤–µ—В —Г—Е—Г–і—И–µ–љ–Є–µ –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –љ–Є—В–µ–є –≥–Є–∞–ї–Њ—Г—А–Њ–љ–∞–љ–∞ –Є «–≤—Л—Б—Л—Е–∞–љ–Є–µ» –Њ—Б–љ–Њ–≤—Л —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є.
–Ъ–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞ —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А–љ–Њ–є –њ–Њ–і–і–µ—А–ґ–Ї–Њ–є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є. –І—А–µ–Ј–Љ–µ—А–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–µ—А–Љ–µ–љ—В–Њ–≤––Ї–Њ–ї–ї–∞–≥–µ–љ–∞–Ј, –і–µ–≥—А–∞–і–Є—А—Г—О—Й–Є—Е –Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л–µ –≤–Њ–ї–Њ–Ї–љ–∞, –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–µ—Г–њ—А–∞–≤–ї—П–µ–Љ–Њ–є —Д—А–∞–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ї–ї–∞–≥–µ–љ–∞, —З—В–Њ –і–µ–ї–∞–µ—В —В–Ї–∞–љ—М –±–Њ–ї–µ–µ –∞–Љ–Њ—А—Д–љ–Њ–є. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є Mg2+ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Г–Љ–µ–љ—М—И–∞–µ—В —Г—А–Њ–≤–љ–Є –Ї–Њ–ї–ї–∞–≥–µ–љ–∞–Ј 1 –Є 2 [32]. –≠—Д—Д–µ–Ї—В –Љ–∞–≥–љ–Є—П –љ–∞ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є MMP2 –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ –і–≤—Г–Љ—П —В–Є—А–Њ–Ј–Є–љ–Ї–Є–љ–∞–Ј–љ—Л–Љ–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є (–≥–µ–љ–Є—Б—В–µ–Є–љ, –≥–µ—А–±–Є–Љ–Є—Ж–Є–љ), –њ–Њ–Ј–≤–Њ–ї—П—П –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ—Л–є –Љ–∞–≥–љ–Є–є —Г–Љ–µ–љ—М—И–∞–µ—В —Б–µ–Ї—А–µ—Ж–Є—О –Ь–Ь–Я —З–µ—А–µ–Ј –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–є —Б–Є–≥–љ–∞–ї—М–љ—Л–є –Ї–∞—Б–Ї–∞–і, –Ї–Њ—В–Њ—А—Л–є –≤–Ї–ї—О—З–∞–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О —В–Є—А–Њ–Ј–Є–љ–Ї–Є–љ–∞–Ј—Г [33].
–У–µ–њ–∞—А–∞–љ—Б—Г–ї—М—Д–∞—В – —Ж–µ–љ—В—А–∞–ї—М–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –≥–ї–Є–Ї–Њ–Ј–∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–∞–љ–Њ–≤ –Є –њ—А–Њ—В–µ–Њ–≥–ї–Є–Ї–∞–љ–Њ–≤ –≥–µ–ї–µ–≤–Њ–є –Њ—Б–љ–Њ–≤—Л —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є. –§–µ—А–Љ–µ–љ—В –≥–µ–њ–∞—А–∞–љ–∞–Ј–∞, –і–µ–≥—А–∞–і–Є—А—Г—О—Й–Є–є –≥–µ–њ–∞—А–∞–љ—Б—Г–ї—М—Д–∞—В, –∞–Ї—В–Є–≤–Є—А—Г–µ—В—Б—П –≤ –Њ–±–ї—Г—З–µ–љ–љ–Њ–є –£–§–Ю –Ї–Њ–ґ–µ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ—В–µ—А–µ –≥–µ–њ–∞—А–∞–љ—Б—Г–ї—М—Д–∞—В–∞ –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ —А–∞–Ј—А—Г—И–µ–љ–Є—П –≥–µ–ї–µ–≤–Њ–є –Њ—Б–љ–Њ–≤—Л —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є [34]. –Ф–µ—Д–Є—Ж–Є—В –Љ–∞–≥–љ–Є—П –±—Г–і–µ—В —Г—Б—Г–≥—Г–±–ї—П—В—М —А–∞–Ј—А—Г—И–µ–љ–Є–µ —Б—В—А—Г–Ї—В—Г—А—Л —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, —В.–Ї. –Љ–∞–≥–љ–Є–є —П–≤–ї—П–µ—В—Б—П –љ–µ–Њ—В—К–µ–Љ–ї–µ–Љ—Л–Љ –Ї–Њ—Д–∞–Ї—В–Њ—А–Њ–Љ –Ї–∞–Ї —Г–њ–Њ–Љ—П–љ—Г—В—Л—Е —А–∞–љ–µ–µ, —В–∞–Ї –Є —А—П–і–∞ –і—А—Г–≥–Є—Е –±–Є–Њ—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–Є—Е —Б—В—А—Г–Ї—В—Г—А—Г —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є.
–Ь–∞–≥–љ–Є—П –∞—Б–Ї–Њ—А–±–Є–ї—Д–Њ—Б—Д–∞—В —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–≤–ї–∞–ґ–љ–µ–љ–Є—О –Є –Њ—Б–≤–µ—В–ї–µ–љ–Є—О –Ї–Њ–ґ–Є. –Т —Е–Њ–і–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Њ—Б—М —В–Њ–њ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞—Б–Ї–Њ—А–±–Є–ї—Д–Њ—Б—Д–∞—В–∞ –Љ–∞–≥–љ–Є—П –љ–∞ –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ–µ –ї–Є—Ж–∞ –Є –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є. –Ш–Ј–Љ–µ—А–µ–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Є –і–Њ –ї–µ—З–µ–љ–Є—П –Є –њ–Њ—Б–ї–µ 1, 3 –Є 6 –Љ–µ—Б. –Њ—В –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞—Б–Ї–Њ—А–±–Є–ї—Д–Њ—Б—Д–∞—В–∞ –Љ–∞–≥–љ–Є—П –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–Њ–Ї—А–∞—В–Є—В—М –Њ–±—Й—Г—О –њ–ї–Њ—Й–∞–і—М –њ—П—В–µ–љ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є (—А<0,005) —Г–ґ–µ –њ–Њ—Б–ї–µ 1 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П. –Ю–±—Й–∞—П –њ–ї–Њ—Й–∞–і—М –њ—П—В–µ–љ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є —З–µ—А–µ–Ј 6 –Љ–µ—Б. –њ–Њ—Б–ї–µ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П –ї–µ—З–µ–љ–Є—П –≤–µ—А–љ—Г–ї–∞—Б—М –Ї –Є—Б—Е–Њ–і–љ–Њ–Љ—Г —Г—А–Њ–≤–љ—О. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞—Б–Ї–Њ—А–±–Є–ї—Д–Њ—Б—Д–∞—В –Љ–∞–≥–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—Б–ї–∞–±–Є—В—М –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—О –Є —Б–Њ—Е—А–∞–љ–Є—В—М –њ—А–Є —Н—В–Њ–Љ –љ–Њ—А–Љ–∞–ї—М–љ—Л–є —Ж–≤–µ—В –Ї–Њ–ґ–Є –ї–Є—Ж–∞ [35]. –Р—Б–Ї–Њ—А–±–Є–ї—Д–Њ—Б—Д–∞—В –Љ–∞–≥–љ–Є—П, –њ–Њ –≤—Б–µ–є –≤–Є–і–Є–Љ–Њ—Б—В–Є, —В–Њ—А–Љ–Њ–Ј–Є—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Љ–µ–ї–∞–љ–Є–љ–∞ —В–Є—А–Њ–Ј–Є–љ–∞–Ј–Њ–є –Ї–∞–Ї –Ј–∞ —Б—З–µ—В –∞—Б–Ї–Њ—А–±–∞—В–∞, —В–∞–Ї –Є –Љ–∞–≥–љ–Є—П [36].
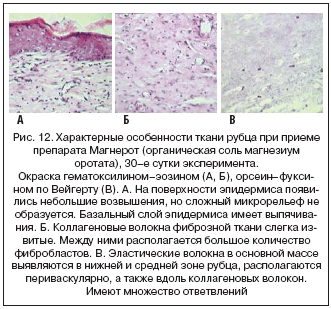
–Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –њ—А–Є–µ–Љ–∞ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–ї–µ–є –Љ–∞–≥–љ–Є—П (–њ—А–µ–њ–∞—А–∞—В –Ь–∞–≥–љ–µ—А–Њ—В) –љ–∞ —Б—В—А—Г–Ї—В—Г—А—Г —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ –Љ–Њ–і–µ–ї—П—Е —А–∞–љ –Є –Њ–ґ–Њ–≥–Њ–≤. –Я—А–Є–µ–Љ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–∞–≥–љ–Є—П –≤–љ—Г—В—А—М —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–ї –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –Є –±—Л—Б—В—А–Њ–µ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є–µ —А–∞–љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є —Б–Њ–ї–Ї–Њ—Б–µ—А–Є–ї–Њ–Љ. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –∞–љ–∞–ї–Є–Ј–Њ–≤ —В–Ї–∞–љ–µ–є —А—Г–±—Ж–∞ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –≥—А—Г–њ–њ–∞—Е –ґ–Є–≤–Њ—В–љ—Л—Е, –њ—А–Є–µ–Љ –Љ–∞–≥–љ–Є—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–ї –Є–Ј–±—Л—В–Њ—З–љ–Њ–µ —А–∞–Ј—А–∞—Б—В–∞–љ–Є–µ –Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–≤—Л—Е —Д–Є–±—А–Є–ї–ї, —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї —А–Њ—Б—В—Г —Н–ї–∞—Б—В–Є–љ–Њ–≤—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, —А–Њ—Б—В—Г —З–Є—Б–ї–∞ —Д–Є–±—А–Њ–±–ї–∞—Б—В–Њ–≤ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є –Є —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –∞–Љ–Њ—А—Д–љ–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ (–њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–љ–Њ–≥–Њ –≥–µ–ї—П), —З—В–Њ, –≤ —Ж–µ–ї–Њ–Љ, –њ—А–Є–≤–µ–ї–Њ –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞—З–µ—Б—В–≤–∞ —А—Г–±—Ж–∞ (—А–Є—Б. 12). –≠—Д—Д–µ–Ї—В –Љ–∞–≥–љ–Є—П –љ–∞ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–ї–Њ—Й–∞–і–Є —А–∞–љ—Л –±—Л–ї –Ј–∞–Љ–µ—В–µ–љ –љ–∞—З–Є–љ–∞—П —Б 1––≥–Њ –і–љ—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П; –≤ —Б–ї—Г—З–∞–µ –Њ–ґ–Њ–≥–Њ–≤ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ—А–Є –њ—А–Є–µ–Љ–µ –Љ–∞–≥–љ–Є—П –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –љ–∞—З–Є–љ–∞—П —Б–Њ 2––є –љ–µ–і. —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞ [37].
–Ь–µ—В–∞–±–Њ–ї–Є–Ј–Љ –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ –Є –Љ–∞–≥–љ–Є—П –≤ –Ї–µ—А–∞—В–Є–љ–Њ—Ж–Є—В–∞—Е
–Ъ–∞–Ї –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –≤—Л—И–µ, –њ—А–Њ—Ж–µ—Б—Б, –љ–∞–Ј—Л–≤–∞—О—Й–Є–є—Б—П «–њ–Њ—А—Д–Є—А–Є–љ–Њ–≤—Л–Љ —Б—В–∞—А–µ–љ–Є–µ–Љ» –Є –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А—Г–µ–Љ—Л–є –љ–∞ –Њ—Б–љ–Њ–≤–µ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є –Ї–Њ–ґ–Є –њ–∞—Ж–Є–µ–љ—В–∞, –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –љ–∞—А—Г—И–µ–љ–Є—П–Љ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Ї—А–Њ–≤–Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Љ–Є–Ї—А–Њ—В—А–∞–≤–Љ–∞—В–Є–Ј–∞—Ж–Є–Є –Ї–Њ–ґ–Є –Є –∞–Ї—В–Є–≤–∞—Ж–Є–Є –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ –Є–Љ–µ—О—Й–Є–µ—Б—П –і–∞–љ–љ—Л–µ —Д—Г–љ–і–∞–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ј–≤–Њ–ї—П—О—В –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –њ–Њ—А—Д–Є—А–Є–љ—Л –Є —Б–∞–Љ–Є –њ–Њ —Б–µ–±–µ –Љ–Њ–≥—Г—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ—А–Њ—Ж–µ—Б—Б—Л —Б—В–∞—А–µ–љ–Є—П –Ї–ї–µ—В–Њ–Ї –Ї–Њ–ґ–Є.
–Ф–ї—П –Є–Ј—Г—З–µ–љ–Є—П –±–Є–Њ—Б–Є–љ—В–µ–Ј–∞ –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ –≤ –Ї–µ—А–∞—В–Є–љ–Њ—Ж–Є—В–∞—Е —З–µ–ї–Њ–≤–µ–Ї–∞ –Ї–ї–µ—В–Ї–Є –≤ –Ї—Г–ї—М—В—Г—А–µ –Є–љ–Ї—Г–±–Є—А–Њ–≤–∞–ї–Є —Б –і–µ–ї—М—В–∞––∞–Љ–Є–љ–Њ–ї–µ–≤—Г–ї–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є (–Р–Ы–Ъ), –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–Њ–Љ —Б–Є–љ—В–µ–Ј–∞ –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ –Є –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї–Є —Б–њ–µ–Ї—В—А–Њ—Д–ї—Г–Њ—А–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ—А–µ–љ–Є—П –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—П –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ї–µ—А–∞—В–Є–љ–Њ—Ж–Є—В—Л —З–µ–ї–Њ–≤–µ–Ї–∞ —Б–њ–Њ—Б–Њ–±–љ—Л —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞—В—М –њ–Њ—А—Д–Є—А–Є–љ—Л. –Т–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –£–§–Ю –љ–∞ –њ–Њ—А—Д–Є—А–Є–љ–—Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –Ї–ї–µ—В–Ї–Є —Б–љ–Є–ґ–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–µ—А—А–Њ—Е–µ–ї–∞—В–∞–Ј—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—П –і–∞–ї—М–љ–µ–є—И–µ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О —Г—А–Њ–≤–љ—П –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ [38].
–Т–∞–ґ–љ–Њ—Б—В—М –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ —В–µ–Љ, —З—В–Њ –Њ—В –Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ј–∞–≤–Є—Б–Є—В –≤—Л–ґ–Є–≤–∞–љ–Є–µ –Ї–ї–µ—В–Њ–Ї –Ї–Њ–ґ–Є. –Ґ–∞–Ї, –њ—А–Њ—В–Њ–њ–Њ—А—Д–Є—А–Є–љ IX —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –∞–њ–Њ–њ—В–Њ–Ј, –Ї–Њ–≥–і–∞ –Ї–ї–µ—В–Ї–Є –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О –£–§. –°–Є–љ—В–µ–Ј –њ—А–Њ—В–Њ–њ–Њ—А—Д–Є—А–Є–љ–∞ IX –Є –µ–≥–Њ —Б–ї–Њ–ґ–љ—Л—Е —Н—Д–Є—А–Њ–≤ –Є–љ–і—Г—Ж–Є—А—Г–µ—В—Б—П –≤ –Ї–µ—А–∞—В–Є–љ–Њ—Ж–Є—В–∞—Е –Є —Д–Є–±—А–Њ–±–ї–∞—Б—В–∞—Е –Ї–Њ–ґ–Є –њ—А–Є –і–Њ–±–∞–≤–ї–µ–љ–Є–Є –Р–Ы–Ъ. –Т —А—П–і–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —З–∞—Б—В–Њ—В–∞ –≥–Є–±–µ–ї–Є –Ї–ї–µ—В–Њ–Ї –≤ –Њ—В–≤–µ—В –љ–∞ –£–§–Ю –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–Њ—В–Њ–њ–Њ—А—Д–Є—А–Є–љ–∞ IX –Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Ј–∞–≤–Є—Б–Є—В –Њ—В –і–Њ–Ј—Л –£–§–Ю [39,40].
–Я–Њ–Ј–і–љ–µ–є –Ї–Њ–ґ–љ–Њ–є –њ–Њ—А—Д–Є—А–Є–µ–є (Porphyria cutanea tarda) –љ–∞–Ј—Л–≤–∞–µ—В—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ –±–Є–Њ—Б–Є–љ—В–µ–Ј–∞ –≥–µ–Љ–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —Б–љ–Є–ґ–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–µ—А–Љ–µ–љ—В–∞ —Г—А–Њ–њ–Њ—А—Д–Є—А–Є–љ–Њ–≥–µ–љ –і–µ–Ї–∞—А–±–Њ–Ї—Б–Є–ї–∞–Ј—Л (–≥–µ–љ UROD). –Р–љ–∞–ї–Є–Ј –Љ–Є–Ї—А–Њ—Н–ї–µ–Љ–µ–љ—В–љ–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–∞ –Ї—А–Њ–≤–Є –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Н—В–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є Mg, P –Є S –≤ —Ж–µ–ї—М–љ–Њ–є –Ї—А–Њ–≤–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–љ–Є–ґ–µ–љ—Л (—А<0,05), –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Г—А–Њ–≤–љ–Є —В–Њ–Ї—Б–Є—З–љ–Њ–≥–Њ –±–∞—А–Є—П –њ–Њ–≤—Л—И–µ–љ—Л [41].
–Ш–Њ–љ—Л –Љ–∞–≥–љ–Є—П —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Б–±–Њ—А–Ї–µ –њ–Њ–ї–љ–Њ—Б—В—М—О –∞–Ї—В–Є–≤–љ–Њ–є –Љ–Њ–ї–µ–Ї—Г–ї—Л —Д–µ—А–Љ–µ–љ—В–∞ –њ–Њ—А—Д–Њ–±–Є–ї–Є–љ–Њ–≥–µ–љ —Б–Є–љ—В–∞–Ј—Л (–≥–µ–љ ALAD), –Ї–Њ—В–Њ—А—Л–є —Б–≤—П–Ј—Л–≤–∞–µ—В 2 –Љ–Њ–ї–µ–Ї—Г–ї—Л 5––∞–Љ–Є–љ–Њ–ї–µ–≤—Г–ї–Є–љ–∞—В–∞ —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ–Њ—А—Д–Њ–±–Є–ї–Є–љ–Њ–≥–µ–љ–∞. –Ф–µ—Д–µ–Ї—В—Л –≤ –≥–µ–љ–µ –њ–Њ—А—Д–Њ–±–Є–ї–Є–љ–Њ–≥–µ–љ —Б–Є–љ—В–∞–Ј—Л —П–≤–ї—П—О—В—Б—П –њ—А–Є—З–Є–љ–Њ–є –Њ—Б—В—А–Њ–є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –њ–Њ—А—Д–Є—А–Є–Є (–Ї–Њ–і –њ–Њ –ЮMIM 612740), –њ—А–Є–≤–Њ–і—П—Й–µ–є –Ї –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—О –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –њ–Њ—А—Д–Є—А–Є–љ–Њ–≤ –Є–ї–Є –Є—Е –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤ –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–µ–є—Б—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ–Њ—В–µ–Љ–љ–µ–љ–Є–µ–Љ —В–Њ–љ–∞ –Ї–Њ–ґ–Є (–Ј–µ–Љ–ї–Є—Б—В—Л–є –Є–ї–Є –ґ–µ–ї—В—Л–є —Ж–≤–µ—В –ї–Є—Ж–∞). –Ф–µ—Д–Є—Ж–Є—В –Љ–∞–≥–љ–Є—П —В–∞–Ї–ґ–µ –±—Г–і–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –њ–∞–і–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Њ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
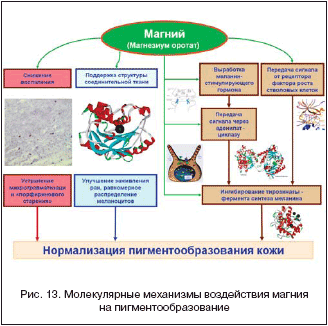
–Э–∞—Б—Г—Й–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л —П–≤–ї—П–µ—В—Б—П —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ –њ—А–Њ—Ж–µ–і—Г—А –і–ї—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —В–Њ–љ–∞ –Ї–Њ–ґ–Є –Є —Г—Б—В—А–∞–љ–µ–љ–Є—П –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –±—Л –љ–µ –Є–Љ–µ–ї–Є –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Я–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –і–∞–љ–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–µ —П–≤–ї—П—О—В—Б—П –Љ–µ—В–Њ–і—Л –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Ї–Њ–ґ–Є –Є –µ–µ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є. –Ь–∞–≥–љ–Є–є, —П–≤–ї—П—П—Б—М –Љ–љ–Њ–≥–Њ—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Ї–Њ—Д–∞–Ї—В–Њ—А–Њ–Љ, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –∞—Б–њ–µ–Ї—В—Л –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Ї–Њ–ґ–Є. –Т –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Љ–∞–≥–љ–Є—П –љ–∞ –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є–µ –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є–Є –Ї–Њ–ґ–Є. –°—Д–Њ—А–Љ—Г–ї–Є—А–Њ–≤–∞–љ—Л –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Љ–∞–≥–љ–Є—П –љ–∞ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л, –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А—Л—Е —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤–∞–ґ–љ–∞ –і–ї—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ–є –Њ–Ї—А–∞—Б–Ї–Є –Ї–Њ–ґ–Є: —Б–µ–Ї—А–µ—Ж–Є—П –Љ–µ–ї–∞–љ–Є–љ–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞, –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–∞—П –њ–µ—А–µ–і–∞—З–∞ —Б–Є–≥–љ–∞–ї–∞ –Њ—В —А–µ—Ж–µ–њ—В–Њ—А–∞ –Љ–µ–ї–∞–љ–Є–љ–—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ –Є –і—А—Г–≥–Є—Е –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ —Д–µ—А–Љ–µ–љ—В–∞ —Б–Є–љ—В–µ–Ј–∞ –Љ–µ–ї–∞–љ–Є–љ–∞ –Є –њ–Њ–і–і–µ—А–ґ–Ї–∞ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ—В–Ї–∞–љ–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –Ї–Њ–ґ–Є (—А–Є—Б. 13). –°—Г—Й–µ—Б—В–≤–Њ–≤–∞–љ–Є–µ —Н—В–Є—Е —Д—Г–љ–і–∞–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Љ–∞–≥–љ–Є—П –љ–∞ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ —Ж–≤–µ—В–∞ –Ї–Њ–ґ–љ—Л—Е –њ–Њ–Ї—А–Њ–≤–Њ–≤ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –≤–∞–ґ–љ—Л–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–∞–≥–љ–Є—П (–њ—А–µ–њ–∞—А–∞—В –Ь–∞–≥–љ–µ—А–Њ—В) –≤ —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ–µ –і–ї—П –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –њ—А–Њ–±–ї–µ–Љ –Ї–Њ–ґ–Є, —В–∞–Ї–Є—Е –Ї–∞–Ї —Г—В—А–∞—В–∞ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ—В–Ї–∞–љ–љ–Њ–≥–Њ –Ї–∞—А–Ї–∞—Б–∞ –Є –≥–Є–њ–µ—А–њ–Є–≥–Љ–µ–љ—В–∞—Ж–Є—П.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Szamkolowicz G., Mierzecki A., Zaluga E. Physiological skin changes during pregnancy // Ginekol. Pol. 2005. Vol. 76(11). P.926–930.
2. Schurer N., Zumdick M., Goerz G. Hyperpigmentation in primary adrenal cortex insufficiency: Addison disease // Hautarzt. 1993. Vol. 44(5). P.300–305.
3. Rendon M., Gaviria J. Skin Lightening Agents / Ed. Zoe Draelos. – Philadelphia: Elsevier, 2005. P.103–104.
4. Anderson R.R. Polarized light examination and photography of the skin // Arch. Dermatol. 1991.Vol. 127. P. 1000–1005.
5. Nishidate I., Aizu Y., Mishina H. Estimation of melanin and hemoglobin in skin tissue using multiple regression analysis aided by Monte Carlo simulation // J. Biomed. Optics. 2004. Vol. 9(4). P. 700–710.
6. Ando H., Ryu A., Hashimoto A. et al. Linoleic acid and alpha–linolenic acid lightens ultraviolet–induced hyperpigmentation of the skin // Arch. Dermatol. Res. 1998. Vol. 290(7). P. 375–381.
7. Halder R.M., Richards G.M. Topical agents used in the management of hyperpigmentation // Skin. Therapy Lett. 2004. Vol. 9(6). P.1–3.
8. Grimes P.E. Melasma. Etiologic and therapeutic considerations // Arch. Dermatol. 1995. Vol. 131(12). P. 1453–1457.
9. –Ґ–Њ—А—И–Є–љ –Ш.–Ѓ., –У—А–Њ–Љ–Њ–≤–∞ –Ю.–Р., –Ц–Є–і–Њ–Љ–Њ—А–Њ–≤ –Э.–Ѓ., –У—А–Є—И–Є–љ–∞ –Ґ.–†. –Ь–∞–≥–љ–Є–є –Є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л —Г—З–∞—Б—В–≤—Г—О—Й–Є–µ –≤ –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–Є —Б—В–∞—А–µ–љ–Є—П –Ї–Њ–ґ–Є: —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј // –≠—Б—В–µ—В–Є—З–µ—Б–Ї–∞—П –Љ–µ–і–Є—Ж–Є–љ–∞, 2012.
10. Brunsting L.A., Sheard C. The color of the skin as analyzed by spectrophotometric methods: II.The role of pigmentation // J. Clin. Invest. 1929. Vol. 7. P. 559–574.
11. Edwards E.A., Duntley S.Q. The pigments and color of living human skin // Am. J. Anatomy. 1939. Vol. 65. P. 1–33.
12. Stamatas G.N., Zmudzka B.Z., Kollias N., Beer J.Z. Non– invasive measurements of skin pigmentation in–situ, Review // Innovative Technology, Pigment Cell Res. 2004. Vol.17. P. 618–626.
13. Demirli R., Otto P., Viswanathan R. et al. RBX™ Technology Overview. http://www.canfieldsci.com/imaging_systems/facial_systems/VISIA_Complexion_Analysis.html
14. Pootongkam S, Asawanonda P. Purpura–free treatment of lentigines using a long–pulsed 595 nm pulsed dye laser with compression handpiece: a randomized, controlled study // J. Drugs Dermatol. 2009. Vol. 8 (11 Suppl). s.18–s24.
15. Taub A.F., Devita E.C. Successful treatment of erythematotelangiectatic rosacea with pulsed light and radiofrequency // J. Clin. Aesthet. Dermatol. 2008. Vol.1(1). P.37–40.
16. Michaels BM, Csank GA, Ryb GE, Eko FN, Rubin A. Prospective randomized comparison of onabotulinumtoxinA (Botox) and abobotulinumtoxinA (Dysport) in the treatment of forehead, glabellar, and periorbital wrinkles // Aesthet. Surg J. 2012. Vol.32(1). P. 96–102.
17. Herane M.I., Orlandi C., Zegpi E. et al. Clinical efficacy of adapalene (differin((R))) 0.3% gel in Chilean women with cutaneous photoaging // J. Dermatolog. Treat. 2012. Vol. 23(1). P.57–64 Epub 2011 Dec.
18. Arjinpathana N., Asawanonda P. Glutathione as an oral whitening agent: A randomized, double–blind, placebo–controlled study // J. Dermatolog. Treat. 2012. Vol. 23(2). P. 97–102 Epub 2010 Ju.
19. Woolery–Lloyd H., Kammer J.N. Treatment of hyperpigmentation // Semin. Cutan. Med. Surg. 2011. Vol.30(3). P. 171–175 doi.
20. Davis E.C., Callender V.D. Postinflammatory hyperpigmentation: a review of the epidemiology, clinical features, and treatment options in skin of color // J. Clin. Aesthet. Dermatol. 2010. Vol. 3(7). P.20–31.
21. Wayman C.P., Wilson J.F. Characteristics of NMDA receptors that stimulate release of hypothalamic alpha–MSH // Neuroreport. 1991. Vol. 2(8). P. 481–484.
22. Wang M., Yang Y., Dong Z. et al. NR2B–containing N–methyl–D–aspartate subtype glutamate receptors regulate the acute stress effect on hippocampal long–term potentiation/long–term depression in vivo // Neuroreport. 2006. Vol.17(12). P.1343–1346.
23. Lyden P., Wahlgren N.G. Mechanisms of action of neuroprotectants in stroke // J. Stroke Cerebrovasc. Dis. 2000. Vol. 9(6 Pt 2). P.9–14.
24. Kovacs D., Cardinali G., Aspite N. et al. Role of fibroblast–derived growth factors in regulating hyperpigmentation of solar lentigo // Br. J. Dermatol. 2010. Vol.163(5). P. 1020–1027 doi.
25. Fleischman RA. Human piebald trait resulting from a dominant negative mutant allele of the c–kit membrane receptor gene // J. Clin. Invest. 1992. Vol. 89(6). P.1713–1717.
26. Mol C.D., Lim K.B., Sridhar V. et al. Structure of a c–kit product complex reveals the basis for kinase transactivation // J. Biol. Chem. 2003. Vol. 278(34). P. 31461–4 Epub 2003 J.
27. Kato Y., Kravchenko V.V., Tapping R.I. et al. BMK1/ERK5 regulates serum–induced early gene expression through transcription factor MEF2C // EMBO J. 1997. Vol.16(23). P.7054–7066.
28. Parvez S., Kang M., Chung H.S. et al. Survey and mechanism of skin depigmenting and lightening agents // Phytother. Res. 2006. Vol. 20(11). P.921–934.
29. Boissy R.E., Halaban R. Establishment of proliferative, pure cultures of pigmented chicken melanocytes from neural tubes // J. Invest. Dermatol. 1985. Vol. 84(2). P.158–161.
30. Jimenez–Cervantes C., Solano F., Lozano J.A., Garcia–Borron J.C. Tyrosinase isoenzymes: two melanosomal tyrosinases with different kinetic properties and susceptibility to inhibition by calcium // Pigment. Cell. Res. 1994. Vol.7(5). P.291–297.
31. –Ґ–Њ—А—И–Є–љ –Ш.–Ѓ., –У—А–Њ–Љ–Њ–≤–∞ –Ю.–Р. –Ь–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Љ–∞–≥–љ–Є—П –Є –і–Є—Б–њ–ї–∞–Ј–Є–Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є // –†–Ь–Ц.. – 2008. – –°. 263–269.
32. Guo H., Lee J.D., Uzui H. et al. Effects of folic acid and magnesium on the production of homocysteine–induced extracellular matrix metalloproteinase–2 in cultured rat vascular smooth muscle cells // Circ. J. 2006. Vol.70(1). P. 141–146.
33. Yue H., Lee J.D., Shimizu H. et al. Effects of magnesium on the production of extracellular matrix metalloproteinases in cultured rat vascular smooth muscle cells // Atherosclerosis. 2003. Vol.166(2). P.271–277.
34. Iriyama S., Ono T., Aoki H., Amano S. Hyperpigmentation in human solar lentigo is promoted by heparanase–induced loss of heparan sulfate chains at the dermal–epidermal junction // J. Dermatol. Sci. 2011. Vol. 64(3). P. 223–228 Epub 2011 Sep.
35. Miyamoto K., Takiwaki H., Hillebrand G.G., Arase S. Utilization of a high–resolution digital imaging system for the objective and quantitative assessment of hyperpigmented spots on the face // Skin. Res. Technol. 2002. Vol. 8(2). P.73–77.
36. Kameyama K., Sakai C., Kondoh S. et al. Inhibitory effect of magnesium L–ascorbyl–2–phosphate (VC–PMG) on melanogenesis in vitro and in vivo // J. Am. Acad. Dermatol. 1996. Vol.34(1). P. 29–33.
37. –°—Г—А–∞–Ї–Њ–≤–∞ –Ґ.–Р., –Ц–Є–і–Њ–Љ–Њ—А–Њ–≤ –Э.–Ѓ., –У—А–Є—И–Є–љ–∞ –Ґ.–†. –Є –і—А. –Я–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Ь–∞–≥–љ–µ—А–Њ—В –≤ —Н—Б—В–µ—В–Є—З–µ—Б–Ї–Њ–є –Љ–µ–і–Є—Ж–Є–љ–µ // –≠—Б—В–µ—В–Є—З–µ—Б–Ї–∞—П –Љ–µ–і–Є—Ж–Є–љ–∞. –2011. – вДЦ 3. – –°. 525–535.
38. He D., Sassa S., Lim H.W. Effect of UVA and blue light on porphyrin biosynthesis in epidermal cells // Photochem. Photobiol. 1993. Vol.57(5). P. 825–829.
39. Lee J.B., Choi J.Y., Chun J.S. et al. Relationship of protoporphyrin IX synthesis to photodynamic effects by 5–aminolaevulinic acid and its esters on various cell lines derived from the skin // Br. J. Dermatol. 2008. Vol. 159(1). P. 61–67.
40. Kappus H., Reinhold C., Artuc M. Photodynamic toxicity of hematoporphyrin derivatives to human keratinocytes in culture // Mol. Toxicol. 1987–1988 Fall. 1987. Vol.1(4). P. 295–299.
41. Dinya M., Szekely E., Szentmihalyi K. et al. Major and trace elements in whole blood of phlebotomized patients with porphyria cutanea tarda // J. Trace Elem. Med. Biol. 2005. Vol.19(2–3). P. 217–220.












