–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л –і–µ–є—Б—В–≤–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–∞
–Р–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–є —Н—Д—Д–µ–Ї—В –Ґ–∞–љ–∞–Ї–∞–љ–∞ –±—Л–ї –Є–Ј—Г—З–µ–љ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е —А–∞–±–Њ—В–∞—Е, —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–Њ—В–Њ—А—Л—Е —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–Є —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –Є —Ж–Є—В–Њ–њ–ї–∞–Ј–Љ–µ –Ї–ї–µ—В–Њ–Ї –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ –њ–Њ–і –µ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ [12]. –Т –Њ–і–љ–Њ–є –Є–Ј —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е —А–∞–±–Њ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ґ–∞–љ–∞–Ї–∞–љ–∞, –Ї–∞–Ї «–ї–Њ–≤—Г—И–Ї–Є» –Њ—Б–љ–Њ–≤–љ—Л—Е –≤–Є–і–Њ–≤ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤: —Б—Г–њ–µ—А–Њ–Ї—Б–Є–і–∞ –Є –≥–Є–і—А–Њ–Ї—Б–Є–ї–—А–∞–і–Є–Ї–∞–ї–∞ –±—Л–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Љ–µ—В–Њ–і–∞ —Б–њ–µ–Ї—В—А–Њ–Љ–µ—В—А–Є–Є —Н–ї–µ–Ї—В—А–Њ–љ–љ–Њ–≥–Њ –њ–∞—А–∞–Љ–∞–≥–љ–Є—В–љ–Њ–≥–Њ —А–µ–Ј–Њ–љ–∞–љ—Б–∞. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ґ–∞–љ–∞–Ї–∞–љ –Њ—З–Є—Й–∞–µ—В –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л–є –Њ–њ—Л—В–љ—Л–є —А–∞—Б—В–≤–Њ—А –Њ—В –Њ–±–Њ–Є—Е –≤–Є–і–Њ–≤ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ —Б –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ (—А–Є—Б. 1) [25]. –Т—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –і–µ–є—Б—В–≤–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–∞ –љ–∞ —Б—Г–њ–µ—А–Њ–Ї—Б–Є–і –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –і–µ–є—Б—В–≤–Є–µ–Љ —В–µ—А–њ–µ–љ–Њ–≤—Л—Е –ї–∞–Ї—В–Њ–љ–Њ–≤ (–≥–Є–љ–Ї–≥–Њ–ї–Є–і–Њ–≤ –Т –Є –°) [21].
–Ґ–∞–љ–∞–Ї–∞–љ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є –Ј–∞ —А—Г–±–µ–ґ–Њ–Љ –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є —Г –ї—О–і–µ–є –њ–Њ–ґ–Є–ї–Њ–≥–Њ –Є —Б—В–∞—А—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –і–ї—П —Г–Љ–µ–љ—М—И–µ–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Љ—Г–ї—М—В–Є–Є–љ—Д–∞—А–Ї—В–љ–Њ–є –Є –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞, —Г–Љ–µ–љ—М—И–µ–љ–Є—П –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–є –Є —И—Г–Љ–∞ –≤ —Г—И–∞—Е [2]. –°–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–ї—Г—З—И–∞—В—М —Б–Њ—Б—В–Њ—П–љ–Є–µ –љ–µ–є—А–Њ–љ–Њ–≤ –Ї–Њ—А—Л –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –≥–Є–њ–њ–Њ–Ї–∞–Љ–њ–∞ —Г –Љ—Л—И–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–µ—З–µ–љ–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ, –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [24]. –Т –†–Њ—Б—Б–Є–Є –њ—А–Њ–≤–µ–і–µ–љ–Њ –Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ґ–∞–љ–∞–Ї–∞–љ–∞ –≤ —В–µ—А–∞–њ–Є–Є —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —Г 140 –±–Њ–ї—М–љ—Л—Е, –њ–Њ–Ї–∞–Ј–∞–≤—И–µ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї 3––Љ—Г –Љ–µ—Б—П—Ж—Г –ї–µ—З–µ–љ–Є—П [11].
–†–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—П –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –і–µ–є—Б—В–≤–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–∞: –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–Љ–µ–љ—М—И–∞—В—М –њ–µ—А–µ–Ї–Є—Б–љ–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –ї–Є–њ–Є–і–Њ–≤, —Г–ї—Г—З—И–∞—В—М –Ї—А–Њ–≤–Њ—В–Њ–Ї –≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–Љ —А—Г—Б–ї–µ, —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї—А–Њ–≤–Є, –∞–Ї—В–Є–≤–Є–Ј–Є—А–Њ–≤–∞—В—М —Н–љ–і–Њ—В–µ–ї–Є–є––Ј–∞–≤–Є—Б–Є–Љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є (–і–Є–ї–∞—В–∞—Ж–Є—П –Є –Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є—П), —Г–Љ–µ–љ—М—И–∞—В—М –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤–Њ–њ—А–Њ—Б –Њ –µ–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ (–°–Ф), –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Є–≥—А–∞—О—В –Њ—Б–љ–Њ–≤–љ—Г—О —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –њ–Њ–Ј–і–љ–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Ґ–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П—Е –°–Ф –њ–Њ–Ї–∞ –µ—Й–µ –Љ–∞–ї–Њ –Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Њ–љ–Є –њ–Њ—Б–≤—П—Й–µ–љ—Л –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—П–Љ —В–µ—А–∞–њ–Є–Є –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є –Є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є.
–Ґ–∞–љ–∞–Ї–∞–љ –≤ –ї–µ—З–µ–љ–Є–Є
–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є
–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є—П (–Ф–Я–Э), —Б–∞–Љ–∞—П —З–∞—Б—В–∞—П —Д–Њ—А–Љ–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є–Є, —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –љ–∞—А—Г—И–µ–љ–Є—П —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б–Њ—Б—В–Њ—П–љ–Є—П —Б—В–µ–љ–Ї–Є —Б–Њ—Б—Г–і–Њ–≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –Њ–±—А–∞—В–љ–Њ–є –Ї–Њ—А—А–µ–ї—П—Ж–Є–µ–є –Љ–µ–ґ–і—Г —В–Њ–ї—Й–Є–љ–Њ–є –±–∞–Ј–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л —Н–љ–і–Њ–љ–µ–≤—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –Є –њ–ї–Њ—В–љ–Њ—Б—В—М—О –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–Љ –љ–µ—А–≤–µ [17]. –С–Њ–ї–µ–µ 50% –±–Њ–ї—М–љ—Л—Е –°–Ф —Б—В—А–∞–і–∞—О—В –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–Љ–Є –љ–µ–≤—А–Њ–њ–∞—В–Є—П–Љ–Є, —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ—В–Њ—А–Њ–є —П–≤–ї—П—О—В—Б—П –≤—А–µ–Љ—П —В–µ—З–µ–љ–Є—П –Є —В–Є–њ –°–Ф, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–µ—А–Є–Њ–і–Њ–≤ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є, HbA1C, –љ–∞–ї–Є—З–Є–µ –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Є –Ї—Г—А–µ–љ–Є–µ [23]. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ф–Я–Э –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤—Б–µ—Е –Љ–Њ–і–∞–ї—М–љ–Њ—Б—В–µ–є, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Є–ї–Є –≤—Л–њ–∞–і–µ–љ–Є–µ–Љ –∞—Е–Є–ї–ї–Њ–≤—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —Б–Є–ї—Л –Љ—Л—И—Ж, –њ—А–Є—З–µ–Љ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –і–µ—Д–Є—Ж–Є—В –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –≤ –і–Є—Б—В–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–∞—Е –љ–Њ–≥. –Я–Њ—А–∞–ґ–µ–љ–Є–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ –њ—А–Є –Ф–Я–Э –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –≠–Ь–У –Љ–µ—В–Њ–і–∞–Љ–Є –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–Љ —Б–µ–љ—Б–Њ—А–љ—Л–Љ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ–Љ.
–Т–Њ–Ј–Љ–Њ–ґ–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ґ–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤ 80––µ –≥–Њ–і—Л XX –≤–µ–Ї–∞. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Д—А–∞–љ—Ж—Г–Ј—Б–Ї–Є—Е –≤—А–∞—З–µ–є –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ґ–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є –і–Є—Б—В–∞–ї—М–љ–Њ–є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–Є [13]. –Т –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 90–—Е –≥–Њ–і–Њ–≤ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ –≤ —В–µ—З–µ–љ–Є–Є 60 –і–љ–µ–є –±–Њ–ї—М–љ—Л—Е —Б –°–Ф –Є –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–µ–є –±—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ—Й—Г—Й–µ–љ–Є–є –Њ–љ–µ–Љ–µ–љ–Є—П –љ–Њ–≥, —Б–ї–∞–±–Њ—Б—В–Є –≤ –љ–Њ–≥–∞—Е –Є –Ї—А–∞–Љ–њ–Є —Б–Є–љ–і—А–Њ–Љ–∞ [3]. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ґ–∞–љ–∞–Ї–∞–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф –Є –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—П–Љ–Є –љ–Њ–≥ –±—Л–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –Њ—Ж–µ–љ–Ї–Њ–є —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є, –љ–Њ –Є –і–Є–љ–∞–Љ–Є–Ї–Њ–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є–Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є [1]. –£–ї—Г—З—И–µ–љ–Є–µ —Ж–µ–ї–Њ–≥–Њ —А—П–і–∞ –≥–µ–Љ–Њ—А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г –±–Њ–ї—М–љ—Л—Е —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Б–Њ—Б—Г–і–Њ–≤ –љ–Њ–≥ –Њ—В–Љ–µ—З–µ–љ–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –≤ –У–µ—А–Љ–∞–љ–Є–Є [18].
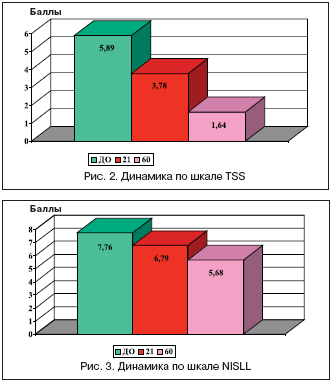
–Э–∞–Є–±–Њ–ї–µ–µ –Љ–∞—Б—И—В–∞–±–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ґ–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є –Ф–Я–Э –њ—А–Њ–≤–µ–і–µ–љ–Њ –≤ –љ–∞—З–∞–ї–µ —В–µ–Ї—Г—Й–µ–≥–Њ —Б—В–Њ–ї–µ—В–Є—П –†–Њ—Б—Б–Є–є—Б–Ї–Є–Љ–Є —Г—З–µ–љ—Л–Љ–Є [4]. –Т —А–∞–Љ–Ї–∞—Е –Њ—В–Ї—А—Л—В–Њ–≥–Њ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ–±—Б–ї–µ–і–Њ–≤–∞–ї–Є 58 –±–Њ–ї—М–љ—Л—Е 2 —В–Є–њ–Њ–Љ –°–Ф –і–Њ –Є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –њ—Г—В–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П 120 –Љ–≥ –Ґ–∞–љ–∞–Ї–∞–љ–∞ –≤ —Б—Г—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 2 –Љ–µ—Б—П—Ж–µ–≤. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–∞–ї–Є –±–Њ–ї—М–љ—Л—Е —Б –Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф (—Б—А–µ–і–љ–Є–є HbA1C – 8,56±0,18%), –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤ —В–µ—З–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б—В–∞–љ–і–∞—А—В–љ—Г—О —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й—Г—О —В–µ—А–∞–њ–Є—О. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–Ј—Г—З–∞–ї–∞—Б—М –і–Є–љ–∞–Љ–Є–Ї–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л, –≠–Ь–У–—Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є, –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—П –љ–Њ–≥—В–µ–≤–Њ–≥–Њ –ї–Њ–ґ–∞ –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –њ–µ—А–Є–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤. –Ы–µ—З–µ–љ–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ –љ–µ –Њ–Ї–∞–Ј–∞–ї–Њ –љ–Є–Ї–∞–Ї–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —Г–≥–ї–µ–≤–Њ–і–љ—Л–є –Њ–±–Љ–µ–љ. –Ф–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї—Б—П —Г—А–Њ–≤–µ–љ—М —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Є b––ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤, —З—В–Њ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –Є –≤ –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–±–ї–Є—В–µ—А–Є—А—Г—О—Й–Є–Љ —Н–љ–і–∞—А—В–µ—А–Є–Є—В–Њ–Љ [10]. –Ю –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ —Б—Г–і–Є–ї–Є –њ–Њ —Г—А–Њ–≤–љ—О –Љ–∞–ї–Њ–љ–Њ–≤–Њ–≥–Њ –і–µ–∞–ї—М–і–µ–≥–Є–і–∞, –Ї–Њ—В–Њ—А—Л–є —Б–љ–Є–ґ–∞–ї—Б—П –Ї–∞–Ї –≤ –њ–ї–∞–Ј–Љ–µ, —В–∞–Ї –Є –≤ –Љ–µ–Љ–±—А–∞–љ–∞—Е —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ. –Я–Њ–Ј–Є—В–Є–≤–љ–∞—П –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –њ–Њ —И–Ї–∞–ї–µ Total Symptom Score (TSS – –Ю–±—Й–Є–є —Б—З–µ—В —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–µ–≤—А–Њ–њ–∞—В–Є–Є) –≤ –Ї–Њ—В–Њ—А—Г—О –≤–Ї–ї—О—З–µ–љ—Л –Њ—Б–љ–Њ–≤–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –њ—А–Є –Ф–Я–Э (–±–Њ–ї—М, –ґ–ґ–µ–љ–Є–µ, –Њ–љ–µ–Љ–µ–љ–Є–µ, –њ–∞—А–µ—Б—В–µ–Ј–Є–Є). –Ъ 60 –і–љ—О –ї–µ—З–µ–љ–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–∞–ї–ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ TSS (—А–Є—Б. 2). –Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –і–µ—Д–Є—Ж–Є—В (–љ–µ–≥–∞—В–Є–≤–љ–∞—П –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞) –Њ—Ж–µ–љ–Є–≤–∞–ї—Б—П –њ–Њ —И–Ї–∞–ї–µ Neuropathy Symptom Score Low Limb (NISLL – –°—З–µ—В –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –≤ –љ–Њ–≥–∞—Е), –њ–Њ –Ї–Њ—В–Њ—А–Њ–є —В–µ—Б—В–Є—А—Г—О—В —Б–Є–ї—Г –Љ—Л—И—Ж, —А–µ—Д–ї–µ–Ї—Б—Л –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–љ—Л—Е –Љ–Њ–і–∞–ї—М–љ–Њ—Б—В–µ–є –≤ –љ–Њ–≥–∞—Е. –Э–∞ 60 –і–µ–љ—М –ї–µ—З–µ–љ–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ –Њ—В–Љ–µ—З–µ–љ–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–∞–ї–ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ NISLL (—А–Є—Б. 3). –≠–Ь–У —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–ї–Њ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–∞–Ї –≤ –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е, —В–∞–Ї –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –љ–µ—А–≤–∞—Е. –Я—А–Є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –Ї–∞–њ–Є–ї–ї—П—А–Њ—Б–Ї–Њ–њ–Є–Є –љ–Њ–≥—В–µ–≤–Њ–≥–Њ –ї–Њ–ґ–∞ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–Є—Б—В–Њ—П–љ–Є—П –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞: —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Ї–Њ—А–Њ—Б—В–Є –Ї–∞–њ–Є–ї–ї—П—А–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–µ—А–Є–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞, —З–Є—Б–ї–∞ —Б–ї–∞–і–ґ–—Д–µ–љ–Њ–Љ–µ–љ–Њ–≤ –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –ї–Є–њ–Є–і–љ—Л—Е –≤–Ї–ї—О—З–µ–љ–Є–є. –Я—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –Ґ–∞–љ–∞–Ї–∞–љ, —Г–Љ–µ–љ—М—И–∞—П –Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–є —Б—В—А–µ—Б—Б, —Г–ї—Г—З—И–∞–µ—В –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О –Є —Д—Г–љ–Ї—Ж–Є—О –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –±–Њ–ї—М–љ—Л—Е —Б –Ф–Я–Э. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, —З—В–Њ –Ґ–∞–љ–∞–Ї–∞–љ –Є–Љ–µ–µ—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –≤–ї–Є—П–љ–Є—П –љ–∞ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ –љ–µ —Б–≤—П–Ј–∞–љ–љ—Л–µ –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ —Б –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ—Л–Љ —Б—В—А–µ—Б—Б–Њ–Љ –Є —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є. –Т –њ–Њ–ї—М–Ј—Г —В–∞–Ї–Њ–≥–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є—П —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ —Ж–Є—Б–њ–ї–∞—В–Є–љ–Њ–≤–Њ–є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є [20].
–Ґ–∞–љ–∞–Ї–∞–љ –≤ –ї–µ—З–µ–љ–Є–Є
–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є
–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —А–µ—В–Є–љ–Њ–њ–∞—В–Є—П (–Ф–†) —П–≤–ї—П–µ—В—Б—П —Б–∞–Љ—Л–Љ –≥—А–Њ–Ј–љ—Л–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ–Љ –°–Ф –Є —Б–∞–Љ–Њ–є —З–∞—Б—В–Њ–є –њ—А–Є—З–Є–љ–Њ–є —Б–ї–µ–њ–Њ—В—Л —Б—А–µ–і–Є –љ–∞—Б–µ–ї–µ–љ–Є—П —А–∞–Ј–≤–Є—В—Л—Е —Б—В—А–∞–љ. –£ –±–Њ–ї—М–љ—Л—Е –°–Ф —Б–ї–µ–њ–Њ—В–∞ –љ–∞—Б—В—Г–њ–∞–µ—В –≤ 25 —А–∞–Ј —З–∞—Й–µ, —З–µ–Љ –≤ –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –љ–∞—Б–µ–ї–µ–љ–Є—П. –Ш–љ–≤–∞–ї–Є–і–љ–Њ—Б—В—М –њ–Њ –Ј—А–µ–љ–Є—О –Њ—В–Љ–µ—З–∞–µ—В—Б—П –±–Њ–ї–µ–µ —З–µ–Љ —Г 10% –±–Њ–ї—М–љ—Л—Е –°–Ф. –Ъ –Љ–Њ–Љ–µ–љ—В—Г —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞ –°–Ф 2 —В–Є–њ–∞, –Њ–Ї–Њ–ї–Њ 5% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Љ–µ—О—В –њ—А–Є–Ј–љ–∞–Ї–Є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є, —З–µ—А–µ–Ј 10 –ї–µ—В –Њ—В –љ–∞—З–∞–ї–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ–∞ –Њ—В–Љ–µ—З–∞—О—В—Б—П —Г 40–50% –±–Њ–ї—М–љ—Л—Е, –∞ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –°–Ф –±–Њ–ї–µ–µ 20 –ї–µ—В —А–∞–Ј–ї–Є—З–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Ф–† –≤—Л—П–≤–ї—П—О—В—Б—П —Г 90% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ф–ї—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –љ–∞–ї–Є—З–Є–µ –Љ–Є–Ї—А–Њ–∞–љ–µ–≤—А–Є–Ј–Љ, —В–Њ—З–µ—З–љ—Л—Е –Ї—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є–є –≤ —Б–µ—В—З–∞—В–Ї—Г, –Њ—В–µ–Ї–∞ —Б–µ—В—З–∞—В–Ї–Є, —В–≤–µ—А–і—Л—Е —Н–Ї—Б—Б—Г–і–∞—В–Њ–≤, —А–∞—Б—И–Є—А–µ–љ–Є—П –Є –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –Є–Ј –≤–µ–љ —Б–µ—В—З–∞—В–Ї–Є, –∞–љ–≥–Є–Њ—А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є, –Є–љ—Д–∞—А–Ї—В–Њ–≤ –≤ —Б–ї–Њ–µ –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ (–Љ—П–≥–Ї–Є–µ —Н–Ї—Б—Б—Г–і–∞—В—Л), –љ–∞–ї–Є—З–Є–µ –±–µ—Б—Б—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤, –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, —Д–Є–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є, —З—В–Њ –Љ–Њ–ґ–µ—В –≤—Л–Ј–≤–∞—В—М –Њ—В—Б–ї–Њ–є–Ї—Г —Б–µ—В—З–∞—В–Ї–Є [7].
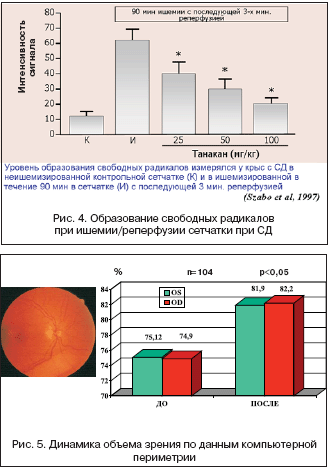
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Ґ–∞–љ–∞–Ї–∞–љ —Г–Љ–µ–љ—М—И–∞–µ—В —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ –≤ —Б–µ—В—З–∞—В–Ї–µ, –≤—Л–Ј–≤–∞–љ–љ—Л—Е –Љ–µ—В–Њ–і–Њ–Љ –Є—И–µ–Љ–Є–Є/—А–µ–њ–µ—А—Д—Г–Ј–Є–Є [22]. –Ф–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–∞ –љ–∞ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ –≤ —Б–µ—В—З–∞—В–Ї–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Ї–∞–Ї —Н—Д—Д–µ–Ї—В–Њ–Љ «–ї–Њ–≤—Г—И–Ї–Є», —В–∞–Ї –Є —Г–≥–љ–µ—В–µ–љ–Є–µ–Љ –њ—А–Њ–і—Г–Ї—Ж–Є–Є —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤, –≤–Њ –≤—Б—П–Ї–Њ–Љ —Б–ї—Г—З–∞–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –Є–љ–≥–Є–±–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–∞ –љ–∞ –Є–љ–і—Г—Ж–Є–±–Є–ї—М–љ—Г—О NO–—Б–Є–љ—В–∞–Ј—Г [16]. –Т —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є —А–µ—В–Є–љ–∞–ї—М–љ–Њ–є –∞—А—В–µ—А–Є–Є –Ґ–∞–љ–∞–Ї–∞–љ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≥–љ–µ—В–∞–ї –њ–µ—А–Є–Ї–Є—Б–љ–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –ї–Є–њ–Є–і–Њ–≤, –≤—Л–Ј–≤–∞–љ–љ–Њ–µ –Є—И–µ–Љ–Є–µ–є/—А–µ–њ–µ—А—Д—Г–Ј–Є–µ–є. –Я—А–Є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є –≤–≤–µ–і–µ–љ–Є–µ–Љ –Ї—Б–∞–љ—В–Є–љ–∞ –Є –Ї—Б–∞–љ—В–Є–љ–Њ–Ї—Б–Є–і–∞–Ј—Л –≤ —Б—В–µ–Ї–ї–Њ–≤–Є–і–љ–Њ–µ —В–µ–ї–Њ, –њ–Њ–Ї–∞–Ј–∞–љ–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –≤–ї–Є—П–љ–Є–µ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ –љ–∞ —Б–µ—В—З–∞—В–Ї—Г, —Б–≤—П–Ј—М —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ —Б –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л–Љ–Є –њ—А–Њ—Ж–µ—Б—Б–∞–Љ–Є –Є –њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–∞ [12]. –°–µ—В—З–∞—В–Ї–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ –±–Њ–≥–∞—В–∞ –њ–Њ–ї–Є–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л–Љ–Є –ґ–Є—А–љ—Л–Љ–Є –Ї–Є—Б–ї–Њ—В–∞–Љ–Є, –њ–Њ—Н—В–Њ–Љ—Г –≤—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–∞ –Ї –ї–Є–њ–Є–і–љ–Њ–є –њ–µ—А–Њ–Ї—Б–Є–і–∞—Ж–Є–Є. –Ґ–∞–љ–∞–Ї–∞–љ –њ—А–µ–і–Њ—Е—А–∞–љ—П–µ—В —Б–µ—В—З–∞—В–Ї—Г –Њ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –Є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ –Я–Ю–Ы [19]. –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Н–ї–µ–Ї—В—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–µ—В—З–∞—В–Ї–Є –Ї—А—Л—Б –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–∞ –Љ–Њ–ґ–µ—В –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М –љ–∞—А—Г—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ —Б–µ—В—З–∞—В–Ї–Є, –Ї–Њ—В–Њ—А—Л–µ –љ–∞–±–ї—О–і–∞—О—В—Б—П –њ—А–Є –°–Ф [16].–Ґ–∞–љ–∞–Ї–∞–љ –≤—Л–Ј—Л–≤–∞–µ—В –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ –≤ —Б–µ—В—З–∞—В–Ї–µ –Ї—А—Л—Б –њ—А–Є –Є—И–µ–Љ–Є–Є/—А–µ–њ–µ—А—Д—Г–Ј–Є–Є, –њ—А–Є—З–µ–Љ –µ–≥–Њ —Н—Д—Д–µ–Ї—В –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї—А–Њ–≤–Є –Є —В—П–ґ–µ—Б—В–Є –°–Ф, –Є –Ј–∞—Й–Є—Й–∞–µ—В –Њ—В —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –Ї–ї–µ—В–Ї–∞—Е —Б–µ—В—З–∞—В–Ї–Є (—А–Є—Б. 4) [22].
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ—А–Є –Ф–† –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Ґ–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є –њ—А–Є–µ–Љ–µ –≤ –і–Њ–Ј–µ 120 –Љ–≥ –≤ —Б—Г—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–Є 6 –Љ–µ—Б—П—Ж–µ–≤ –≤ –≤–Є–і–µ —Г–ї—Г—З—И–µ–љ–Є—П —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–µ—В—З–∞—В–Ї–Є –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Њ—Б—В—А–Њ—В—Л –Ј—А–µ–љ–Є—П [15]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –≤ –†–Њ—Б—Б–Є–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Њ 104 –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ –і–Њ –Є –њ–Њ—Б–ї–µ 60 –і–љ–µ–є –ї–µ—З–µ–љ–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ –≤ –і–Њ–Ј–µ 120 –Љ–≥ –≤ –і–µ–љ—М [9]. –Ю–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–∞–ї–Њ –≤–Є–Ј–Њ–Љ–µ—В—А–Є—О, –Њ—Д—В–∞–ї—М–Љ–Њ—Б–Ї–Њ–њ–Є—О, —Н–ї–µ–Ї—В—А–Њ—А–µ—В–Є–љ–Њ–≥—А–∞—Д–Є—О, –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Г—О –њ–µ—А–Є–Љ–µ—В—А–Є—О. –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ—П –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Њ—В–µ–Ї–∞ —Б–µ—В—З–∞—В–Ї–Є, —З–∞—Б—В–Є—З–љ–Њ–≥–Њ –Є–ї–Є –њ–Њ–ї–љ–Њ–≥–Њ —А–∞—Б—Б–∞—Б—Л–≤–∞–љ–Є—П –Ї—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є–є –њ–Њ —Е–Њ–і—Г —Б–Њ—Б—Г–і–Њ–≤ –Є–ї–Є –≤–Њ–Ј–ї–µ –і–Є—Б–Ї–∞ –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞. –Ъ–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П –њ–µ—А–Є–Љ–µ—В—А–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–∞, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –Ј—А–µ–љ–Є—П –Ј–∞ —Б—З–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л—Е –Є –∞–±—Б–Њ–ї—О—В–љ—Л—Е —Б–Ї–Њ—В–Њ–Љ (—А–Є—Б. 5). –°–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–µ –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е —Б –Ф–† –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–µ—З–µ–љ–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–Њ–Љ –Є –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В–µ—А–∞–њ–Є—О –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–∞–Љ–Є –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –±–Њ–ї–µ–µ 25% –±–Њ–ї—М–љ—Л—Е –≤—В–Њ—А–Њ–є –≥—А—Г–њ–њ—Л –Ј–∞ –≥–Њ–і –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –ї–∞–Ј–µ—А–љ–Њ–є –Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є —Б–µ—В—З–∞—В–Ї–Є, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П —В–∞–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї —В–Њ–ї—М–Ї–Њ –Њ–і–Є–љ –±–Њ–ї—М–љ–Њ–є [4]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Ґ–∞–љ–∞–Ї–∞–љ —Г–Љ–µ–љ—М—И–∞—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞, —Г–ї—Г—З—И–∞–µ—В –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–µ—В—З–∞—В–Ї–Є. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–Ј–≤–Њ–ї—П—О—В —Б—З–Є—В–∞—В—М –Ґ–∞–љ–∞–Ї–∞–љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є.
–Я–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –Ґ–∞–љ–∞–Ї–∞–љ–∞
–≤ –ї–µ—З–µ–љ–Є–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞
–Ю–і–љ–Є–Љ –Є–Ј —Б–∞–Љ—Л—Е –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–є –њ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –њ—А–µ–њ–∞—А–∞—В–∞ –Ґ–∞–љ–∞–Ї–∞–љ –≤ —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф —Б –љ–∞—А—Г—И–µ–љ–љ—Л–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є —Д—Г–љ–Ї—Ж–Є—П–Љ–Є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ —В–µ—З–µ–љ–Є–Є –°–Ф 2 —В–Є–њ–∞ (–±–Њ–ї–µ–µ 10 –ї–µ—В) —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –љ–µ —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –≤–Њ–Ј—А–∞—Б—В–Њ–Љ –±–Њ–ї—М–љ—Л—Е [5]. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Ґ–∞–љ–∞–Ї–∞–љ–∞ —Г–ї—Г—З—И–∞—В—М –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –њ—А–µ–і–і–µ–Љ–µ–љ—В–љ—Л–Љ–Є –Є –і–µ–Љ–µ–љ—В–љ—Л–Љ–Є —Б–Њ—Б—В–Њ—П–љ–Є—П–Љ–Є —А–∞–Ј–ї–Є—З–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [2]. –Ф–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е –°–Ф —Б –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є –њ—А–µ–і–ї–∞–≥–∞–µ—В—Б—П —В–µ—А–∞–њ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Љ–Є–ї–і—А–Њ–љ–∞—В (L––Ї–∞—А–љ–Є—В–Є–љ), –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–Њ–Ї–∞–Ј–∞–љ–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ [6]. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї—Г—З–µ–љ—Л –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, —Г–Љ–µ–љ—М—И–∞—О—Й–Є–Љ–Є –≤–ї–Є—П–љ–Є–µ –Є—И–µ–Љ–Є–Є –Є –≥–Є–њ–Њ–Ї—Б–Є–Є –љ–∞ –Љ–Њ–Ј–≥–Њ–≤—Г—О —В–Ї–∞–љ—М [5,8]. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –њ—А–Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ (–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П) –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л —В–µ–Љ, –Ї–Њ—В–Њ—А—Л–µ –љ–∞–±–ї—О–і–∞—О—В—Б—П –њ—А–Є –Ф–Я–Э. –Т —Н—В–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –Є–Љ–µ–љ–љ–Њ –Ґ–∞–љ–∞–Ї–∞–љ –≤—Л–≥–ї—П–і–Є—В –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ –њ—А–∞–≤–Є–ї–∞–Љ –љ–∞–і–ї–µ–ґ–∞—Й–µ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–Є, –Ї–Њ—В–Њ—А–Њ–µ —Б–Љ–Њ–≥–ї–Њ –±—Л –Њ—В–≤–µ—В–Є—В—М –љ–∞ –≤–Њ–њ—А–Њ—Б –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ґ–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є. –Я—А–Є —Н—В–Њ–Љ —Б–ї–µ–і—Г–µ—В –Є–Љ–µ—В—М –≤ –≤–Є–і—Г, —З—В–Њ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –°–Ф –Њ—В–≤–µ—З–∞—О—В –љ–∞ —В–µ—А–∞–њ–Є—О –∞–љ—В–Є–≥–Є–њ–Њ–Ї—Б–∞–љ—В–∞–Љ–Є, —В.–µ. —П–≤–ї—П—О—В—Б—П –Њ–±—А–∞—В–Є–Љ—Л–Љ–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е [5].
–Я–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Ґ–∞–љ–∞–Ї–∞–љ–∞
–Ю—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Ґ–∞–љ–∞–Ї–∞–љ–∞ –љ–∞–±–ї—О–і–∞—О—В—Б—П —А–µ–і–Ї–Њ –Є –Ј–∞–Ї–ї—О—З–∞—О—В—Б—П –≤ –њ–Њ—П–≤–ї–µ–љ–Є–Є –і–Є—Б–њ–µ–њ—В–Є—З–µ—Б–Ї–Є—Е —П–≤–ї–µ–љ–Є–є, —А–µ–ґ–µ –≥–Њ–ї–Њ–≤–љ—Л—Е –±–Њ–ї–µ–є –Є –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є. –Я–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–∞–±–ї—О–і–∞—О—В—Б—П –Љ–µ–љ–µ–µ —З–µ–Љ —Г 1% –±–Њ–ї—М–љ—Л—Е –Є –њ—А–Њ—Е–Њ–і—П—В —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞ [2].
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ш–Љ–µ—О—Й–Є–µ—Б—П —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ґ–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ –њ–Њ–ї—Г—З–Є–ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞–Є–±–Њ–ї–µ–µ –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є —П–≤–ї—П–µ—В—Б—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ–Њ–Ј–і–љ–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤ —А–∞–Љ–Ї–∞—Е –љ–∞–і–ї–µ–ґ–∞—Й–µ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–Є (—А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е) –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –Ф–Я–Э –Є –Ф–†, –љ–Њ –Є –њ—А–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є, —З—В–Њ –Љ–Њ–ґ–µ—В –њ–Њ–Ј–≤–Њ–ї–Є—В—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–∞—Б—И–Є—А–Є—В—М —З–Є—Б–ї–Њ –љ–Њ–Ј–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ґ–∞–љ–∞–Ї–∞–љ–∞.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Р–ї–Є–µ–≤ –Ь.–Р., –Ф–ґ–∞–Ї—Г–ї–Њ–≤ –Т.–Р., –°–µ–Ї–µ—А–±–∞–µ–≤ –Ю.–Р. –Ъ–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –∞–љ–≥–Є–Њ–њ–∞—В–Є–є // –Т —Б–±–Њ—А. «–•–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –∞–љ–≥–Є–Њ–њ–∞—В–Є–є» – –Р–ї–Љ–∞—В—Л – 1998 – —Б—В—А.29–32.
2. –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –ѓ—Е–љ–Њ –Э.–Э. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —В–∞–љ–∞–Ї–∞–љ–∞ –њ—А–Є –љ–∞—А—Г—И–µ–љ–Є–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П // –†—Г—Б—Б –Љ–µ–і –ґ—Г—А–љ – 2001 – —В.9 – —Б—В—А.3–9.
3. –Я—А–Є—Б—В—Г–њ–Њ–Ї –Р.–Ь. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ґ–∞–љ–∞–Ї–∞–љ–∞ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –Є–љ—Б—Г–ї–Є–љ–Њ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ // –Т —Б–±–Њ—А. «–Ґ–∞–љ–∞–Ї–∞–љ: –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤ —Б—В—А–∞–љ–∞—Е –°–Э–У – –Ь. – 2001 – —Б—В—А.73–74.
4. –°—В—А–Њ–Ї–Њ–≤ –Ш.–Р., –Ы–∞–≤—А–Њ–≤–∞ –Ш.–Э., –Ь–Њ—А–≥–Њ–µ–≤–∞ –§.–≠. –Р–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–∞—П —В–µ—А–∞–њ–Є—П –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є –Є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞ // –†—Г—Б—Б–Ї –Љ–µ–і –ґ—Г—А–љ – 2004 – —В.12 – —Б—В—А.585–589.
5. –°—В—А–Њ–Ї–Њ–≤ –Ш.–Р., –Ь–Њ—А–≥–Њ–µ–≤–∞ –§.–≠., –Ъ.–Ш.–°—В—А–Њ–Ї–Њ–≤ –Є –і—А. –Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є –Є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є –∞–Ї—В–Њ–≤–µ–≥–Є–љ–Њ–Љ // –†—Г—Б—Б–Ї –Љ–µ–і –ґ—Г—А–љ – 2006 – вДЦ9 – —Б—В—А.698–703.
6. –°—Г—Б–ї–Є–љ–∞ –Ч.–Р., –Ь–∞–Ї—Б–Є–Љ–Њ–≤–∞ –Ь.–Ѓ., –Ъ–Є—Б—В–µ–љ–µ–≤ –С.–Р. –Є –і—А. –Р–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–∞—П —В–µ—А–∞–њ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є, –Њ—В—П–≥–Њ—Й–µ–љ–љ–Њ–є —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ —В–Є–њ–∞ 2 // –§–∞—А–Љ–∞—В–µ–Ї–∞ – 2005 – —В.12 – —Б—В—А.66–69.
7. –Ъ–∞—Ж–љ–µ–ї—М—Б–Њ–љ –Ы.–Р., –§–Њ—А–Њ—Д–Њ–љ–Њ–≤–∞ –Ґ.–Ш., –С—Г–љ–Є–љ –Р.–ѓ. –°–Њ—Б—Г–і–Є—Б—В—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≥–ї–∞–Ј – –Ь. – 1990.
8. –Ъ–Њ—В–Њ–≤ –°.–Т., –†—Г–і–∞–Ї–Њ–≤–∞ –Ш.–У., –Ш—Б–∞–Ї–Њ–≤–∞ –Х.–Т. –≠–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ II —В–Є–њ–∞. –Ъ–ї–Є–љ–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ // –Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї – 2001 – вДЦ3 – —Б—В—А.35–37.
9. –Ь–Њ—И–µ—В–Њ–≤–∞ –Ы.–Ъ., –Р—А–ґ–Є–Љ–∞—В–Њ–≤–∞ –У.–®., –°—В—А–Њ–Ї–Њ–≤ –Ш.–Р. –Є –і—А. –°–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–∞—П —В–µ—А–∞–њ–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—П – 2006 – —В.7 – —Б—В—А. 2–3
10. –Э–∞—Г–Љ–Њ–≤ –°.–°. –Ґ–∞–љ–∞–Ї–∞–љ –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤ —Б—В—А–∞–љ–∞—Е –°–Э–У – –Ь.2001 – —Б—В—А.73–74.
11. –ѓ—Е–љ–Њ –Э.–Э., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –Ы–Њ–Ї—И–Є–љ–∞ –Р.–С. –Є –і—А. –Ґ–∞–љ–∞–Ї–∞–љ (EGb 761) –≤ —В–µ—А–∞–њ–Є–Є —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є (–Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ) – –Ц—Г—А–љ –љ–µ–≤—А–Њ–ї–Њ–≥ –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є –Є–Љ –°.–°.–Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞ – 2006 – вДЦ12 – —Б—В—А.41–46.
12. Baudouin C., Pisella P.J. Ettaiche M. et al.// Graefes Arch Clin Exp Ophthalmol – 1999 – Vol. 237 – p. 58–66.
13. Boissier P. Etude clinique du Tanakan dans les arteriopathies des members inferrieurs // La vie medicale – 1980 – Vol.6 – p.513–515.
14. Brownlee
15. Doly M., Bonhomme B., Cluzel J. et al. //Invest Opthalmol Vis Sci – 1994 – Vol.35 – p.1587.
16. Droy–Lefaix M.T., Bonhomme B., Doly M. // Drugs Exp Clin Res – 1991 – Vol.17 – p.571–575
17. Giannini C., Dyck P.J. Diabetic neuropathy // Eds P.J.Dyck, P.K.Thomas – 2–nd Ed. – Philadelphia, 1999 – p.279–295.
18. Li A–L, Shi Y–D., Landsmann B. et al. Hemorheology and walking of peripheral arterial occlusive diseases patients during treatment with Ginkgo biloba extract // Acta Pharmacol Sinica – 1998 – Vol. 19 – p.417–421.
19. Murata T., Nishida T., Eto S. et al. // Metab Pediatr Ophthalmol – 1981 – Vol.5 – p. 83–87.
20. Ozturk G., Anlar O., Erdogan E. et al. The effect of Ginkgo extract Egb761 in cisplatin–induced peripheral neuropathy in mice // Toxicol Applied Pharmacol – 2004 – Vol.196 – p.169–175
21 Scholtyssek H., Damerrau W., Wessel R. et al. //Chem Biol Interact – 1997 – Vol.106 – p.183–190.
22. Szabo M.E., Dray–Lefaix M.T., Doly M. // Ophthal Res – 1995 – Vol.27 – p. 102–109.
23. Strokov I.A., Bursa T.R., Drepa O.I. et al. // Acta Diabetol – 2003 – Vol.40 – p.375–379.
24. Watanabe C.M., Wolffram S., Ader P. et al. The in vivo neuromodulatory effects of the herbal medicine Ginkgo biloba // Proc Natl Acad Sci USA – 2001 – Vol.98 – p.6577–6580.
25. Yashikawa T., Naito Y., Kondo M. Ginkgo biloba leaf extract: Review of biological actions and clinical applications // Antioxidants and Redox Signaling – 1999 – Vol.1 – p.469–480.












