Введение
Проблема функциональных расстройств желудочно-кишечного тракта (ЖКТ) чрезвычайно актуальна в связи с высокой распространенностью. Несмотря на то, что данная патология ассоциируется с хорошим прогнозом, качество жизни больных существенно снижается. Это приводит к частым посещениям врача, дополнительным, часто необоснованным дорогостоящим обследованиям и неэффективному лечению.
Согласно Римским критериям IV [1, 2] в основе функциональных гастроинтестинальных расстройств лежат комбинированные морфологические и физиологические отклонения:
нарушение моторики ЖКТ;
снижение защитного слизистого барьера и иммунной функции;
изменение состава кишечной микробиоты;
висцеральная гиперчувствительность;
нарушение координирующей функции ЦНС.
В обновленном документе сделано несколько важных дополнений. Так, впервые официально утверждена роль микробов и некоторых пищевых продуктов в качестве этиологических факторов возникновения функциональных нарушений ЖКТ. Кроме этого, введено понятие «синдром перекреста функциональных нарушений ЖКТ» — одновременное течение нескольких функциональных расстройств или переход из одного в другое.
Функциональные заболевания органов пищеварения
Наиболее распространенными функциональными заболеваниями органов пищеварения (ФЗОП) являются функциональная диспепсия (ФД) и синдром раздраженного кишечника (СРК). Распространенность ФД в мире достигает в среднем 20–30%, заболеваемость составляет примерно 1% в год. По данным эпидемиологических исследований, число дней нетрудоспособности у больных с ФД на 2–3 нед. в год больше по сравнению с таковым у лиц, имеющих другую патологию, что подчеркивает социальную значимость и недостаточную эффективность лечения. Критериями диагностики ФД являются ощущение переполнения и раннего насыщения, боль и жжение в эпигастрии, активно беспокоящие пациента последние 3 мес. при общей продолжительности симптомов по крайней мере 6 мес. Согласно Римским критериям IV выделяют два варианта ФД [3]:
Постпрандиальный дистресс-синдром — диагностируется, если не менее 3 дней в неделю пациент прерывает прием порции пищи привычного размера по причине появляющегося гнетущего ощущения переполнения и раннего насыщения, при этом симптомы всегда возникают после приема пищи и по интенсивности должны быть достаточными для того, чтобы нарушать повседневную деятельность больного.
Синдром эпигастральной боли характеризуется наличием боли и/или жжения в эпигастрии натощак или после еды не менее 1 дня в неделю, интенсивность симптомов непременно мешает повседневной деятельности больного.
СРК страдают, по данным разных исследователей, от 10 до 20% населения. Это преимущественно лица молодого возраста (20–40 лет) с существенным преобладанием женщин (2–3:1). Россия относится к регионам мира с высокой распространенностью заболевания (до 19,9%). Критерии диагностики СРК в рекомендациях последнего пересмотра были существенно скорректированы. Так, к диагностическим критериям патологии теперь не относится понятие «абдоминальный дискомфорт», поскольку международные эксперты пришли к общему мнению, что часто больные под дискомфортом понимают разнообразные субъективные неприятные ощущения, не всегда связанные с функциональным расстройством со стороны кишечника [4]. Также в новых Римских критериях болевой абдоминальный синдром при СРК больше не ассоциируется с облегчением после отхождения стула, однако связь с актом дефекации сохранена. Обновленные диагностические критерии СРК представлены следующим образом:
рецидивирующая абдоминальная боль, беспокоящая пациента как минимум 1 раз в неделю последние 3 мес. при общем стаже заболевания не менее 6 мес.;
боль ассоциируется с 2 или более факторами:
связь с дефекацией;
изменение частоты стула;
изменение консистенции стула.
Таким образом, ФД и СРК имеют общие диагностические критерии: общая продолжительность симптомов (6 мес. и более), текущая активность симптомов (последние 3 мес.), частота возникновения симптомов (в среднем по крайней мере 1 день в неделю), отсутствие явных анатомических или физиологических патологий, выявленных при проведении диагностических обследований.
Общность клинических симптомов
Общность клинических симптомов следует из общих патогенетических механизмов всех функциональных расстройств ЖКТ и, в частности, ФД и СРК.
Висцеральная гиперчувствительность (ВГЧ). В ряде исследований у больных с сочетанием ФД и СРК выявлены более высокие показатели висцеральной чувствительности к растяжению желудка (44%) по сравнению с таковыми у пациентов, страдающих только ФД (28%) [5, 6]. У трети пациентов, страдающих СРК, выявляется гиперчувствительность к растяжению желудка и двенадцатиперстной кишки [7].
Нарушения аккомодации и моторной активности желудка, являющиеся основными патогенетическими факторами формирования симптомов ФД, выявляют не менее чем у 30% пациентов, страдающих СРК [8, 9].
Активно изучается генетическая предрасположенность к развитию функциональных нарушений одновременно на разных уровнях ЖКТ. Так, в работах последних лет установлено, что полиморфизм гена транспортера серотонина (SERT) и гена G-протеина 3 (GN3) ассоциируется с развитием одновременно ФД и СРК [10, 11].
В исследованиях показана роль инфекционных агентов и ассоциированных с ними нарушений кишечной микрофлоры в развитии ФЗОП и их перекрестов. Так, метаанализ 9 исследований показал, что перенесенные кишечные инфекции повышают риск развития СРК в 7 раз, при этом факторами риска являются женский пол, исходная депрессия, курение, прием антибактериальных препаратов. В другой работе [12] обнаружено сохранение повышенного риска развития СРК в течение 36 мес. после бактериального гастроэнтерита [13]. У пациентов с постинфекционным СРК в 62% случаев диагностируется ФД, при этом клиническими предикторами формирования перекреста являются длительная абдоминальная боль и рвота во время острого течения инфекции [14].
В свою очередь, нарушение микробиоты кишечника при СРК может являться фактором риска развития ФД: избыточное газообразование и повышенное давление в нижележащих отделах ЖКТ приводят к повышению внутрипросветного давления в тонкой кишке и, как следствие, к нарушению эвакуации из верхних отделов ЖКТ. Показано, что адъювантная терапия с использованием препаратов-пеногасителей в таких случаях эффективнее нормализует моторную функцию ЖКТ [15]. Доказана роль Helicobacter pylori в формировании диспепсии, устранение симптомов после успешной эрадикации является критерием диагностики Helicobacter pylori-ассоциированной диспепсии [3].
Синдром перекреста ФЗОП
Перекрест ФЗОП представляет собой сочетание заболеваний одного или нескольких органов ЖКТ с общими доказанными или предполагаемыми механизмами патогенеза. Статистические данные свидетельствуют о высокой частоте выявления перекрестов функциональных расстройств ЖКТ: по данным ВОЗ, у 42–87% пациентов с СРК диагностируется ФД [16], почти у половины больных с СРК (49%) имеются нарушения моторной функции билиарного тракта. Установлено, что у больных с диспепсией частота выявления СРК значительно выше, чем у лиц без ФД (37% и 7% соответственно) [17].
В одном из исследований [18] сочетание ФД с СРК выявлялось в 11–27% случаев, причем перекрест этих функциональных расстройств ассоциировался с более тяжелыми клиническими проявлениями. Исследователи назвали это явление феноменом «взаимного отягощения». Так, интенсивность постпрандиального переполнения, болезненного чувства голода и выраженности изжоги была достоверно выше у пациентов с сочетанием двух и более ФЗОП, чем у больных, страдающих только одним функциональным расстройством (p<0,001). Наличие феномена «взаимного отягощения» в значительной мере негативно влияло на качество жизни и эффективность лечения
В настоящее время при широкой распространенности перекресты ФЗОП практически не диагностируются, и часто именно это становится причиной неэффективного лечения больных. Цель выделения синдрома перекреста — совершенствование диагностики и повышение эффективности терапии. Теоретически в ряде случаев применение одного патогенетического средства в разной степени должно повлиять на течение всех сочетающихся заболеваний. В случае сочетания функциональных расстройств с различными клиническими проявлениями (например, перекрест ФД и СРК) логично назначать лекарственные препараты, рекомендованные для применения при каждой из патологий. Так, медикаментозное лечение ФД предполагает применение ингибиторов протонной помпы и прокинетиков, а также обязательную эрадикацию Helicobacter pylori [3]. При СРК препаратами первой линии являются миотропные спазмолитики в сочетании с медикаментами, нормализующими эвакуаторную функцию толстой кишки, а также пре- и пробиотики [19].
Роль ЦНС и психосоциальных факторов в развитии ФЗОП
Необходимо отметить, что еще одной важной причиной неэффективного лечения является то, что и пациенты, и врачи недооценивают значение психоэмоциональных расстройств со стороны ЦНС в виде тревожности и даже депрессии. Между тем, по мнению международных экспертов [20], в развитии функциональных заболеваний всех уровней ЖКТ определяющее значение имеют психосоциальные факторы: стрессовые ситуации, психологический статус, характерные личностные качества и восприимчивость к стрессам, преодоление трудностей (рис. 1). Так, при СРК предрасполагающим фоном для развития болезни являются субъективные, сверхзначимые для личности эмоции, которые вызывают перенапряжение вегетативной нервной системы, ведущее к нарушению их реализации в виде вербального или физического выражения переживаний. Патология формируется постепенно, при воздействии комплекса факторов в течение всей жизни, причем в детском и подростковом возрасте большое значение имеют средовые факторы и семейные привычки.
![Рис. 1. Биопсихосоциальная модель генеза функциональных заболеваний ЖКТ [1]. Рис. 1. Биопсихосоциальная модель генеза функциональных заболеваний ЖКТ [1].](/upload/medialibrary/366/24-1.png)
Еще в 2000 г. G. Engel предложил биопсихосоциальную модель развития СРК, при которой возникает расстройство регуляции между ЦНС и автономной энтеральной нервной системой, в норме регулирующей основные функции кишечника — моторику, абсорбцию и секрецию при минимальном влиянии со стороны симпатической и парасимпатической систем. При наличии сенсибилизирующего фактора любые отклонения функции кишечника вызывают активацию большого числа спинальных нейронов, приводя к синдрому спинальной гипервозбудимости, связанному с активацией большого числа молекул оксида азота, при этом корригирующий рефлекторный ответ воспринимается как болезненный [21, 22].
Генетическая предрасположенность в сочетании с воздействием сенсибилизирующего фактора у некоторых лиц могут способствовать формированию длительной следовой памяти о боли. Поэтому в дальнейшем обычные (не чрезмерные) отклонения вызывают аггравированный болевой ответ, соответствующий воздействию стрессорного сенсибилизирующего фактора. Таким образом, у больных с СРК нарушен процесс нисходящего подавления восприятия боли (центральная антиноцицептивная дисфункция) при отсутствии повреждения нейрональной передачи висцеральной
боли [21, 23, 24]. Эти процессы лежат в основе формирования синдрома висцеральной гиперчувствительности, в котором W.E. Whitehead (2002) выделил 2 типа висцеральной гипералгезии: снижение порога восприятия боли и более интенсивное ощущение боли при нормальном пороге ее восприятия.
В многочисленных работах показано, что ВГЧ, являющаяся у больных с СРК основным фактором формирования упорного интенсивного и плохо поддающегося традиционному лечению абдоминального болевого синдрома, характеризуется избирательностью в отношении механических стимулов, при этом восприятие электрических, термических и химических воздействий на стенку кишки не отличается от такового у здоровых лиц. Висцеральную гипералгезию принято считать биологическим маркером СРК, а баллонно-дилатационный тест — специфичным (95%) и чувствительным (70%) методом диагностики заболевания [4, 21–25]. Предиктором формирования ВГЧ является взаимодействие комплекса сенсибилизирующих факторов: кишечной инфекции, психосоциального стресса, физической травмы.
Комплексное взаимодействие психосоциальных, физиологических (повышенная сенситивность и др.) и средовых факторов формирует нарушения взаимодействия ЦНС c периферическим звеном нервной системы, обеспечивающего деятельность органов ЖКТ (так называемая ось «головной мозг — ЖКТ») [1]. Развившиеся функциональные расстройства, в свою очередь, поддерживают и усугубляют дисбаланс регуляции деятельности ЖКТ и, более того, приводят к выраженным нарушениям в психоэмоциональной сфере. Известно, что качество жизни больных с ФЗОП существенно снижено по сравнению с таковым в основной популяции, а неэффективное лечение традиционными препаратами еще больше утяжеляет эмоциональное состояние больного из-за фиксации на своем болезненном, «неизлечимом» состоянии. Например, при тяжелом течении СРК отмечается резистентная к лечению упорная клиническая симптоматика, при этом у всех пациентов прослеживается связь болезни с психоэмоциональными проблемами, а в ряде случаев уже имеются психоэмоциональные нарушения в форме тревоги, депрессии и т. д. В исследованиях сопутствующие функциональные вегетативные нарушения, аффективные и тревожные, депрессивные или ипохондрические расстройства выявляются у 75–80% больных с СРК [26].
Таким образом, состояние ЦНС может являться основополагающим в возникновении и прогрессировании ФЗОП. Именно поэтому один из главных акцентов в последней редакции европейских рекомендаций сделан на выраженной взаимосвязи этих расстройств с нарушениями восприятия. Более того, вместо определения «функциональное расстройство» теперь рекомендуется применять определение «нарушение церебро-интестинального взаимодействия», а определение «функциональная абдоминальная боль» рекомендовано заменить на «нарушение центрального восприятия гастроинтестинальной боли» [1, 20].
Лечение ФЗОП
Для коррекции эмоционально-психического статуса и повышения эффективности лечения в международных и национальных рекомендациях при неэффективности препаратов, оказывающих влияние на нормализацию моторики ЖКТ и ВГЧ, предлагается дополнить лечение трициклическими антидепрессантами [1, 4, 9]. Метаанализ результатов 11 рандомизированных контролируемых исследований показал эффективность антидепрессантов в лечении функциональных гастроинтестинальных заболеваний, в т. ч. СРК [27]. При этом отмечено, что лечение антидепрессантами, особенно трициклическими, ассоциировано с уменьшением выраженности боли. Однако к данной группе препаратов может возникать зависимость, лечение сопровождается побочными эффектами. В связи с этим чрезвычайно актуальным представляется применение анксиолитиков — препаратов с противотревожным действием.
Анксиолитики традиционно широко используются в неврологической практике для лечения функциональных расстройств со стороны ЦНС. Основанием для применения этой группы препаратов при ФЗОП является то, что в регуляции ответа на экзо- и эндогенные стрессорные факторы важную роль играет сбалансированная работа стресс-реализующей и стресс-лимитирующей систем (эустресс). Одним из главных медиаторов, регулирующих ответ на стрессовые состояния, является γ-аминомасляная кислота (ГАМК), дефицит которой приводит к превалированию активности стресс-реализующей системы и развитию биологически отрицательного стресса (дистресс), а в дальнейшем — к устойчивой патологии (тревожные состояния, депрессии и т. д.). Этим объясняется совокупность развивающихся при функциональных расстройствах ЖКТ симптомов (тревога, депрессия, высокая стресс-сенситивность). Для тревожных и невротических состояний, сопровождающих ФЗОП, характерны жалобы на моторные и вегетативные симптомы: чувство нервозности, дрожь, мышечное напряжение, потливость, сердцебиение, дискомфорт в эпигастральной области, раздражительность, головокружение, головные боли напряжения (ГБН) и симптомы диспепсии [28].
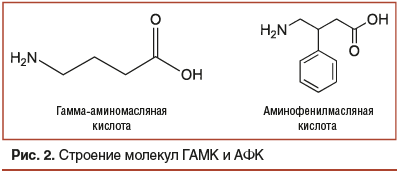
Снижение активности стресс-лимитирующих систем (в частности, ГАМКергической) при функциональных расстройствах ЖКТ делает патогенетически обоснованным назначение ГАМКергических препаратов. Оптимальным патогенетическим средством для повышения активности стресс-лимитирующих систем являются синтетические аналоги ГАМК [29]. Одним из таких препаратов является аминофенилмасляная кислота (АФК) — ноотропное и анксиолитическое (противотревожное) средство, являющееся фенильным производным γ-аминомасляной кислоты. Благодаря наличию фенильного кольца в бета-положении, которое существенно повышает липофильность молекулы, это вещество способно проникать через гематоэнцефалический барьер и доставлять ГАМК в ткань мозга (рис. 2). ГАМК воздействует на тормозные синапсы в мозге путем связывания со специфическими трансмембранными рецепторами, что сопровождается открытием ионных каналов, обеспечивающих поток отрицательно заряженных ионов хлора в клетку и обратный поток положительно заряженных ионов калия [30].
АФК хорошо изучена и широко применяется в неврологической практике у взрослых и детей. В ряде исследований показано, что ведущим в спектре действия препаратов АФК является не столько транквилизирующий, сколько активирующий компонент, что дает преимущество в отличие от бензодиазепиновых и других препаратов с исключительно седативным действием. Еще одним преимуществом АФК является то, что препарат уменьшает вазовегетативные симптомы, в т. ч. головную боль, ощущение тяжести в голове, нарушения сна, раздражительность, эмоциональную лабильность. В клинических исследованиях при курсовом приеме препарат АФК (Анвифен®) повышает физическую и умственную работоспособность (внимание, память, скорость и точность сенсорно-моторных реакций) на фоне уменьшения проявления астении без седации или возбуждения и способствует снижению чувства тревоги, напряженности и беспокойства, а также нормализует сон [29–31]. С учетом улучшения концентрации внимания, интеллектуально-мнестических способностей, исчезновения вялости и усталости, нормализации сна у больных с астеническим синдромом был сделан вывод о том, что первичным в психотропном действии этих препаратов является ноотропный эффект [32–34]. У больных наблюдали транквилизирующее действие препаратов АФК в виде редукции тревоги, страха, повышенной эмоциональной возбудимости и фобических нарушений. В ряде публикаций приведена последовательность обратной динамики отдельных психопатологических расстройств при назначении препаратов АФК. Так, уже в первые дни лечения отмечаются исчезновение тревоги, внутреннего напряжения, страха, уменьшение раздражительности, угрюмости, дисфории. Одновременно наблюдались оживление интереса, повышение активности, а у детей — побуждение к игровой деятельности и учебе, уменьшение психической и соматической астении [35–38].
Трехнедельный прием АФК при ГБН у подростков оказывает положительное влияние на стресс-индуцированные феномены, продолжение приема препарата в течение последующих 3 нед. сопровождалось дальнейшим снижением тревоги, депрессии, стресс-сенситивности, частоты и интенсивности ГБН и улучшением сна. Имеются данные о положительном эффекте препарата АФК (Анвифен®) при лечении церебрастенического синдрома у детей и так называемых невротических расстройств, которые по своей сути являются проявлениями дезадаптационного синдрома [33–37].
Важным преимуществом АФК является ее безопасность при длительном и даже неконтролируемом применении в отличие от антидепрессантов [39–41]. Одним из наиболее важных механизмов формирования зависимости является возможность повышения дозы вещества для того, чтобы преодолеть толерантность к нему, или привыкание к его эффектам. Однако попытка увеличить дозировку АФК неминуемо приводит не к увеличению активности дофаминовых нейронов, а к их торможению. По данным зарубежных исследователей, лица, использующие этот препарат даже не по медицинским показаниям, фактически не могут выйти за пределы терапевтического диапазона [39]. В свою очередь это приводит к тому, что АФК даже в условиях полного отсутствия какого-либо врачебного контроля остается безопасным препаратом. Случаи развития серьезных осложнений (гиперседация, синдром отмены) при использовании АФК не по медицинским показаниям достаточно редки, а смертельные исходы не зарегистрированы [39–43]. У людей пожилого возраста препарат не вызывает угнетения ЦНС и мышечно-расслабляющего последействия [28].
АФК улучшает когнитивные функции и стабилизирует эмоциональную активность, влияя на процессы обучаемости. По результатам двойных слепых плацебо-контролируемых исследований у больных с психоневрологическими расстройствами АФК активизирует интеллектуальную деятельность, увеличивает выносливость и переносимость физических нагрузок, снижает признаки астенизации, раздражительности, агрессии. Анксиолитическое действие данного препарата в сочетании с активизацией умственной деятельности позволяет назначать АФК при функциональных невротических расстройствах, в т. ч. при функциональных расстройствах ЖКТ и их перекрестах с целью повышения эффективности лечения.












