–Т–≤–µ–і–µ–љ–Є–µ
–У–ї–Њ–±–∞–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –∞–љ–µ–Љ–Є—П –±–µ—А–µ–Љ–µ–љ–љ—Л—Е, —З–∞—Б—В–Њ—В–∞ –Ї–Њ—В–Њ—А–Њ–є –≤ –Љ–Є—А–µ –і–Њ—Б—В–Є–≥–∞–µ—В 50% [1], –∞ –≤ —А–∞–Ј–≤–Є–≤–∞—О—Й–Є—Е—Б—П —Б—В—А–∞–љ–∞—Е вАФ 80% [2]. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Є–Ј 107 —Б—В—А–∞–љ –Љ–Є—А–∞ –Ј–∞ –њ–Њ—Б–ї–µ–і–љ–Є–µ –і–µ—Б—П—В–Є–ї–µ—В–Є—П —З–∞—Б—В–Њ—В–∞ –∞–љ–µ–Љ–Є–Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ —Б–љ–Є–ґ–∞–µ—В—Б—П. –Ґ–∞–Ї, –≤ 1995 –≥. —З–∞—Б—В–Њ—В–∞ –∞–љ–µ–Љ–Є–Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 43%, –≤ 2011 –≥. вАФ 38% [3]. –Я–Њ –Ї—А–Є—В–µ—А–Є—П–Љ –Т–Ю–Ч –і–Є–∞–≥–љ–Њ–Ј –∞–љ–µ–Љ–Є–Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ (Hb) <110 –≥/–ї –Є–ї–Є –≥–µ–Љ–∞—В–Њ–Ї—А–Є—В–∞ (Ht) <33% –≤ –ї—О–±–Њ–Љ —В—А–Є–Љ–µ—Б—В—А–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є [1], —В–Њ–≥–і–∞ –Ї–∞–Ї —Б–Њ–≥–ї–∞—Б–љ–Њ –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Є–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ CDC (Center for Disease Control and Prevention вАФ –¶–µ–љ—В—А –њ–Њ –Ї–Њ–љ—В—А–Њ–ї—О –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є) –∞–љ–µ–Љ–Є—П –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В —Г—А–Њ–≤–љ—О Hb<110 –≥/–ї –Є–ї–Є Ht<33% –≤ I –Є III —В—А–Є–Љ–µ—Б—В—А–∞—Е –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, –Є —Г—А–Њ–≤–љ—О Hb<105 –≥/–ї –Є–ї–Є Ht<32% –≤–Њ II —В—А–Є–Љ–µ—Б—В—А–µ [4]. –Я–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –Т–Ю–Ч —Г—А–Њ–≤–µ–љ—М Hb<70 –≥/–ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –∞–љ–µ–Љ–Є–Є —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є, –∞ Hb<40 –≥/–ї вАФ –Њ—З–µ–љ—М —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є [5].
–Ю—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –∞–љ–µ–Љ–Є–Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —П–≤–ї—П–µ—В—Б—П –і–µ—Д–Є—Ж–Є—В –ґ–µ–ї–µ–Ј–∞, —Д–Њ–ї–Є–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є –≤–Є—В–∞–Љ–Є–љ–∞ –Т12, —З—В–Њ —В—А–µ–±—Г–µ—В –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є —В–µ—А–∞–њ–Є–Є —Б —Ж–µ–ї—М—О –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –Љ–∞—В–µ—А–Є–љ—Б–Ї–Є—Е –Є –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ц–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ–∞—П –∞–љ–µ–Љ–Є—П (–Ц–Ф–Р) –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–∞ —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ—Л—Е —А–Њ–і–Њ–≤, –њ–ї–∞—Ж–µ–љ—В–∞—А–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, —Б–Є–љ–і—А–Њ–Љ–∞ –Ј–∞–і–µ—А–ґ–Ї–Є —А–Њ—Б—В–∞ –њ–ї–Њ–і–∞, –њ—А–µ—Н–Ї–ї–∞–Љ–њ—Б–Є–Є, –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Њ—В—Б–ї–Њ–є–Ї–Є –њ–ї–∞—Ж–µ–љ—В—Л [6, 7]. –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –і–µ—Д–Є—Ж–Є—В –ґ–µ–ї–µ–Ј–∞ —Г –Љ–∞—В–µ—А–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П –ґ–µ–ї–µ–Ј–∞ –≤ –њ—Г–њ–Њ–≤–Є–љ–љ–Њ–є –Ї—А–Њ–≤–Є [8] –Є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–ї–Є—П–љ–Є–µ –љ–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ —А–µ–±–µ–љ–Ї–∞ [9].
–Т —В–µ—З–µ–љ–Є–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є —А–∞—Б—Е–Њ–і –ґ–µ–ї–µ–Ј–∞ –љ–∞ —А–Њ—Б—В –њ–ї–Њ–і–∞ –Є –њ–ї–∞—Ж–µ–љ—В—Л —Б–Њ—Б—В–∞–≤–ї—П–µ—В 300вАУ350 –Љ–≥, –љ–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –Љ–∞—В–µ—А–Є–љ—Б–Ї–Є—Е —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ вАФ 500 –Љ–≥, –∞ –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А—П –њ—А–Є —А–Њ–і–Њ—А–∞–Ј—А–µ—И–µ–љ–Є–Є —В—А–µ–±—Г–µ—В –µ—Й–µ –Њ–Ї–Њ–ї–Њ 250 –Љ–≥ –ґ–µ–ї–µ–Ј–∞. –Я–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –ґ–µ–ї–µ–Ј–µ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –Њ—В 0,8 –Љ–≥/—Б—Г—В –≤ I —В—А–Є–Љ–µ—Б—В—А–µ –і–Њ 7,5 –Љ–≥/—Б—Г—В –≤ III —В—А–Є–Љ–µ—Б—В—А–µ, —В–Њ–≥–і–∞ –Ї–∞–Ї –њ—А–Є –Њ–±—Л—З–љ–Њ–є –і–Є–µ—В–µ –µ–ґ–µ–і–љ–µ–≤–љ–Њ–µ —Г—Б–≤–Њ–µ–љ–Є–µ –ґ–µ–ї–µ–Ј–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ—В 1 –і–Њ 5 –Љ–≥, —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –∞–ї–Є–Љ–µ–љ—В–∞—А–љ–Њ–є –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є —А–∞—Б—Е–Њ–і–∞ –ґ–µ–ї–µ–Ј–∞ –њ—А–Є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є [10].
–†–Є—Б–Ї –∞–љ–µ–Љ–Є–Є –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б –љ–Є–Ј–Ї–Є–Љ —Б–Њ—Ж–Є–∞–ї—М–љ–Њ-—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–Љ —Б—В–∞—В—Г—Б–Њ–Љ (–Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї (–Ю–†) 2,03), –Њ–і–љ–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –њ–Є—В–∞–љ–Є–µ–Љ (–Ю–†=3,18), –њ–∞—А–∞¬≠–Ј–Є—В–∞—А–љ—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є (–Ю–†=2,69), –≤—Л—Б–Њ–Ї–Є–Љ –њ–∞—А–Є—В–µ—В–Њ–Љ (–Ю–†=1,78) –≤–Њ II –Є III —В—А–Є–Љ–µ—Б—В—А–∞—Е –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є (–Ю–†=3,09 –Є 3,68 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ), –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Д–µ—А—А–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є (–Ю–†=1,72) [11]. –Ю–і–љ–Њ–Ј–љ–∞—З–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г —А—Г—В–Є–љ–љ–Њ–є —Д–µ—А—А–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В. –Ґ–∞–Ї, –њ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ CDC –њ–Њ–Ї–∞–Ј–∞–љ –µ–ґ–µ–і–љ–µ–≤–љ—Л–є –њ—А–Є–µ–Љ 30 –Љ–≥ –ґ–µ–ї–µ–Ј–∞ —Б –Љ–Њ–Љ–µ–љ—В–∞ –њ–µ—А–≤–Њ–≥–Њ –њ—А–µ–љ–∞—В–∞–ї—М–љ–Њ–≥–Њ –≤–Є–Ј–Є—В–∞ [4], –њ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –Т–Ю–Ч вАФ 60 –Љ–≥/—Б—Г—В –ґ–µ–ї–µ–Ј–∞ –≤—Б–µ–Љ –±–µ—А–µ–Љ–µ–љ–љ—Л–Љ [1], —В–Њ–≥–і–∞ –Ї–∞–Ї —Б–Њ–≥–ї–∞—Б–љ–Њ –±—А–Є—В–∞–љ—Б–Ї–Є–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—В–Њ–Ї–Њ–ї–∞–Љ —А—Г—В–Є–љ–љ–∞—П —Д–µ—А—А–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –≤ —В–µ—З–µ–љ–Є–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П [12].
–Ф–ї—П —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –ґ–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –≤—Л–і–µ–ї—П—О—В —В—А–Є —Б—В–∞–і–Є–Є –і–µ—Д–Є—Ж–Є—В–∞ –ґ–µ–ї–µ–Ј–∞: –њ—А–µ–і–ї–∞—В–µ–љ—В–љ—Л–є –і–µ—Д–Є—Ж–Є—В –ґ–µ–ї–µ–Ј–∞, –ї–∞—В–µ–љ—В–љ—Л–є –Є –Љ–∞–љ–Є—Д–µ—Б—В–љ—Л–є, –Є–ї–Є –Ц–Ф–Р [13]. –°–Ї—А–Є–љ–Є–љ–≥ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –≤ I —В—А–Є–Љ–µ—Б—В—А–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Є –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ –і–Њ–ї–ґ–µ–љ –≤–Ї–ї—О—З–∞—В—М –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ —Д–µ—А—А–Є—В–Є–љ–∞ (–°–§), —П–≤–ї—П—О—Й–µ–≥–Њ—Б—П –±–Њ–ї–µ–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ—Л–Љ –Љ–∞—А–Ї–µ—А–Њ–Љ, —З–µ–Љ —Г—А–Њ–≤–µ–љ—М —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞: —В–∞–Ї, —Г—А–Њ–≤–µ–љ—М –°–§<30 –љ–≥/–Љ–ї –Є–Љ–µ–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М 92% –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М 98% –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –і–µ—Д–Є—Ж–Є—В–∞ –ґ–µ–ї–µ–Ј–∞ [7, 10]. –§–µ—А—А–Є—В–Є–љ —Б—Л–≤–Њ—А–Њ—В–Ї–Є –њ—А–Є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Њ–±—Л—З–љ–Њ —Б–љ–Є–ґ–∞–µ—В—Б—П –і–Њ –љ–Є–ґ–љ–Є—Е –љ–Њ—А–Љ–∞—В–Є–≤–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є, –Њ–і–љ–∞–Ї–Њ –њ—А–Є –∞–љ–µ–Љ–Є–Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –љ–∞ —Д–Њ–љ–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є –∞–љ–µ–Љ–Є–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П) –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ–≤—Л—И–µ–љ [13]. –°–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –°–§ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ–± –Є—Б—В–Њ—Й–µ–љ–Є–Є –Ј–∞–њ–∞—Б–Њ–≤ –ґ–µ–ї–µ–Ј–∞, –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –њ—А–Є –Ц–Ф–Р —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ —Г—А–Њ–≤–µ–љ—М <20 –Љ–Ї–≥/–ї [13], —Б–Њ–≥–ї–∞—Б–љ–Њ –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Є–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ CDC вАФ <10вАУ15 –Љ–Ї–≥/–ї [4]. –Я—А–Є –Ц–Ф–Р —Б–љ–Є–ґ–µ–љ–∞ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞, –њ–Њ–≤—Л—И–µ–љ—Л –Њ–±—Й–∞—П –ґ–µ–ї–µ–Ј–Њ—Б–≤—П–Ј—Л–≤–∞—О—Й–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б—Л–≤–Њ—А–Њ—В–Ї–Є (–Ю–Ц–°–°) –Є –ї–∞—В–µ–љ—В–љ–∞—П –ґ–µ–ї–µ–Ј–Њ—Б–≤—П–Ј—Л–≤–∞—О—Й–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М, —Б–љ–Є–ґ–µ–љ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –љ–∞—Б—Л—Й–µ–љ–Є—П —В—А–∞–љ—Б—Д–µ—А—А–Є–љ–∞ –ґ–µ–ї–µ–Ј–Њ–Љ (<16%) [13]. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–ї—Г—З–∞–µ–≤ —Г—А–Њ–≤–µ–љ—М Hb, –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –љ–∞—Б—Л—Й–µ–љ–Є—П —В—А–∞–љ—Б—Д–µ—А—А–Є–љ–∞ –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —Д–µ—А—А–Є—В–Є–љ–∞ –њ–Њ–Ј–≤–Њ–ї—П—О—В –Њ—Ж–µ–љ–Є—В—М —Б—В–∞—В—Г—Б –ґ–µ–ї–µ–Ј–∞ —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е, –∞ —Б–Њ—З–µ—В–∞–љ–Є–µ –∞–љ–µ–Љ–Є–Є –Є —Г—А–Њ–≤–љ—П —Д–µ—А—А–Є—В–Є–љ–∞ <15вАУ30 –љ–≥/–Љ–ї –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –ґ–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –∞–љ–µ–Љ–Є–Є [1]. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –±–Є–Њ–Љ–∞—А–Ї–µ—А–Њ–Љ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞ –ґ–µ–ї–µ–Ј–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ —П–≤–ї—П–µ—В—Б—П –≥–µ–њ—Ж–Є–і–Є–љ вАФ —А–µ–≥—Г–ї—П—В–Њ—А –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є –ґ–µ–ї–µ–Ј–∞, –µ–≥–Њ —Г—А–Њ–≤–µ–љ—М –≤ —В–µ—З–µ–љ–Є–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –њ—А–Њ–≥—А–µ—Б—Б–Є–≤–љ–Њ —Б–љ–Є–ґ–∞–µ—В—Б—П [14].
–°–Њ–≥–ї–∞—Б–љ–Њ –њ—А–Є–Ї–∞–Ј—Г –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є –Њ—В 1 –љ–Њ—П–±—А—П 2012 –≥. вДЦ 572–љ ¬Ђ–Ю–± —Г—В–≤–µ—А–ґ–і–µ–љ–Є–Є –Я–Њ—А—П–і–Ї–∞ –Њ–Ї–∞–Ј–∞–љ–Є—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –њ–Њ –њ—А–Њ—Д–Є–ї—О ¬Ђ–∞–Ї—Г—И–µ—А—Б—В–≤–Њ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—П¬ї –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б –∞–љ–µ–Љ–Є–µ–є –≤–Ї–ї—О—З–∞–µ—В: –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є вАФ 1 —А./–Љ–µ—Б. —Б –ї–µ–є–Ї–Њ—Ж–Є—В–∞—А–љ–Њ–є —Д–Њ—А–Љ—Г–ї–Њ–є, –њ–Њ–і—Б—З–µ—В–Њ–Љ —А–µ—В–Є–Ї—Г–ї–Њ—Ж–Є—В–Њ–≤ –Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤; –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є (–Њ–±—Й–Є–є –±–µ–ї–Њ–Ї, —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–µ –ґ–µ–ї–µ–Ј–Њ, —Д–µ—А—А–Є—В–Є–љ, —В—А–∞–љ—Б—Д–µ—А—А–Є–љ, –±–Є–ї–Є—А—Г–±–Є–љ –Њ–±—Й–Є–є –Є –њ—А—П–Љ–Њ–є); –і—А—Г–≥–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –≤—А–∞—З–∞-—В–µ—А–∞–њ–µ–≤—В–∞; –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є—О –≤—А–∞—З–∞-—В–µ—А–∞–њ–µ–≤—В–∞ (–≤—А–∞—З–∞-–≥–µ–Љ–∞—В–Њ–ї–Њ–≥–∞) –Є –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ (1вАУ2 —А./–Љ–µ—Б.); —Н–ї–µ–Ї—В—А–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є—О –≤ –Ї–∞–ґ–і–Њ–Љ —В—А–Є–Љ–µ—Б—В—А–µ; —Г—В–Њ—З–љ–µ–љ–Є–µ –і–Є–∞–≥–љ–Њ–Ј–∞ –Є —А–µ—И–µ–љ–Є–µ –≤–Њ–њ—А–Њ—Б–∞ –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –њ—А–Є —Б—А–Њ–Ї–µ –і–Њ 10 –љ–µ–і.; –њ—Г–љ–Ї—Ж–Є—О –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ (–њ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –≤—А–∞—З–∞-–≥–µ–Љ–∞—В–Њ–ї–Њ–≥–∞); –Њ—Ж–µ–љ–Ї—Г —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–ї–Њ–і–∞ вАФ –Ї–∞—А–і–Є–Њ—В–Њ–Ї–Њ–≥—А–∞—Д–Є—О –Є –і–Њ–њ–њ–ї–µ—А–Њ–Љ–µ—В—А–Є—О –≤ –і–Є–љ–∞–Љ–Є–Ї–µ [15].
–Ь–µ—В–Њ–і–∞–Љ–Є –ї–µ—З–µ–љ–Є—П –Ц–Ф–Р —П–≤–ї—П—О—В—Б—П —Д–µ—А—А–Њ—В–µ—А–∞–њ–Є—П (–њ–µ—А¬≠–Њ—А–∞–ї—М–љ–∞—П –Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–∞—П), –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н—А–Є—В—А–Њ–њ–Њ—Н–Ј—Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Д–µ—А—А–Њ—В–µ—А–∞–њ–Є–µ–є –Є –≥–µ–Љ–Њ—В—А–∞–љ—Б—Д—Г–Ј–Є–Є [13, 16]. –Я–µ—А–Њ—А–∞–ї—М–љ–∞—П —Д–µ—А—А–Њ—В–µ—А–∞–њ–Є—П —Б–ї—Г–ґ–Є—В —В–µ—А–∞–њ–Є–µ–є –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –њ—А–Є –њ—А–µ–і–ї–∞—В–µ–љ—В–љ–Њ–Љ, –ї–∞—В–µ–љ—В–љ–Њ–Љ –Є –Љ–∞–љ–Є—Д–µ—Б—В–љ–Њ–Љ –і–µ—Д–Є—Ж–Є—В–µ –ґ–µ–ї–µ–Ј–∞; –і–Њ–Ј–∞ —Н–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞ –≤–∞—А—М–Є—А—Г–µ—В –Њ—В 60 –і–Њ 200 –Љ–≥ [4, 12]. –°–Њ–≥–ї–∞—Б–љ–Њ –§–µ–і–µ—А–∞–ї—М–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –њ—А–Є –ї–∞—В–µ–љ—В–љ–Њ–Љ –і–µ—Д–Є—Ж–Є—В–µ –ґ–µ–ї–µ–Ј–∞ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П 50вАУ100 –Љ–≥/—Б—Г—В —Н–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞, –њ—А–Є –∞–љ–µ–Љ–Є–Є –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є вАФ 100вАУ120 –Љ–≥/—Б—Г—В, —Б—А–µ–і–љ–µ–є —Б—В–µ–њ–µ–љ–Є вАФ 150 –Љ–≥/—Б—Г—В, —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є вАФ 200 –Љ–≥/—Б—Г—В [13]. –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –≤—Б–∞—Б—Л–≤–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –і–Њ 28% –ґ–µ–ї–µ–Ј–∞, –Њ–і–љ–∞–Ї–Њ –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ґ–µ–ї–µ–Ј–∞ 2вАУ3 —А./—Б—Г—В –њ—А–Є–≤–Њ–і–Є—В –Ї —А–µ–Ј–Ї–Њ–Љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—О –≥–µ–њ—Ж–Є–і–Є–љ–∞, —З—В–Њ —Б–љ–Є–ґ–∞–µ—В –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –ґ–µ–ї–µ–Ј–∞ –Є –љ–µ –і–∞–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –њ–µ—А–µ–і –Њ–і–љ–Њ–Ї—А–∞—В–љ—Л–Љ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –ґ–µ–ї–µ–Ј–∞ –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї [17]. –І—А–µ–Ј–Љ–µ—А–љ–Њ–µ –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ґ–µ–ї–µ–Ј–∞ –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —А–∞–Ј–≤–Є—В–Є—О –≥–µ—Б—В–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ –Є –≥–∞—Б—В—А–Њ–Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, –∞ –≤ –Ј—А–µ–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ вАФ –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є [18].
–Я—А–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –ґ–µ–ї–µ–Ј–∞ –Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї –∞–і–µ–Ї–≤–∞—В–љ–Њ–µ, –µ—Б–ї–Є –њ–Њ—Б–ї–µ 2 –љ–µ–і. —Д–µ—А—А–Њ—В–µ—А–∞–њ–Є–Є —Г—А–Њ–≤–µ–љ—М Hb –њ–Њ–≤—Л—И–∞–µ—В—Б—П –љ–∞ 10 –≥/–ї, –∞ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ–µ—А–µ—Е–Њ–і–Є—В—М –љ–∞ –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л [19, 20]. –Я—А–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, —В. –µ. –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –∞–љ–µ–Љ–Є–Є, –њ–µ—А–Њ—А–∞–ї—М–љ—Г—О —Д–µ—А—А–Њ—В–µ—А–∞–њ–Є—О —Б–ї–µ–і—Г–µ—В –њ—А–Њ–і–Њ–ї–ґ–∞—В—М –≤ —В–µ—З–µ–љ–Є–µ 2вАУ3 –Љ–µ—Б. –і–ї—П –≤–Њ—Б–њ–Њ–ї–љ–µ–љ–Є—П –і–µ–њ–Њ –ґ–µ–ї–µ–Ј–∞, –Ј–∞—В–µ–Љ –≤ —В–µ—З–µ–љ–Є–µ 6 –љ–µ–і. –њ–Њ—Б–ї–µ —А–Њ–і–Њ–≤ [19, 21]. –£ –Ј–і–Њ—А–Њ–≤—Л—Е –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –±–µ–Ј –∞–љ–µ–Љ–Є–Є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є –µ–ґ–µ–і–љ–µ–≤–љ–Њ–Љ—Г –њ—А–Є–µ–Љ—Г –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ґ–µ–ї–µ–Ј–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–µ—В–Њ–і–∞ —Д–µ—А—А–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –≤–Њ IIвАУIII —В—А–Є–Љ–µ—Б—В—А–∞—Е –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М –Є–љ—В–µ—А–Љ–Є—В—В–Є—А—Г—О—Й–Є–є (2вАУ3 —А./–љ–µ–і.) –Є –µ–ґ–µ–љ–µ–і–µ–ї—М–љ—Л–є —А–µ–ґ–Є–Љ—Л –њ—А–Є–µ–Љ–∞ [22, 23]. –°–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є –Њ–±–Ј–Њ—А (2017 –≥.) –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –ґ–µ–ї–µ–Ј–∞ –≤–Љ–µ—Б—В–µ —Б —Б–Є–љ–µ—А–≥–Є—Б—В–∞–Љ–Є –≤ —Б–Њ—Б—В–∞–≤–µ –≤–Є—В–∞–Љ–Є–љ–љ–Њ-–Љ–Є–љ–µ—А–∞–ї—М–љ—Л—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–≤ –і–ї—П –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –ґ–µ–ї–µ–Ј–∞ –Є–ї–Є –ґ–µ–ї–µ–Ј–∞/—Д–Њ–ї–∞—В–Њ–≤ —Б–љ–Є–ґ–∞–µ—В —З–∞—Б—В–Њ—В—Г –Ј–∞–і–µ—А–ґ–Ї–Є —А–Њ—Б—В–∞ –њ–ї–Њ–і–∞ –Є –і—А—Г–≥–Є—Е –∞–Ї—Г—И–µ—А—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —В–∞–Ї–Њ–є –њ–Њ–і—Е–Њ–і –Њ—Б–Њ–±–µ–љ–љ–Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–µ–љ –≤ –њ–Њ–њ—Г–ї—П—Ж–Є—П—Е —Б –љ–Є–Ј–Ї–Є–Љ –Є —Б—А–µ–і–љ–Є–Љ —Б–Њ—Ж–Є–∞–ї—М–љ–Њ-—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ [18].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—Г—Й–µ—Б—В–≤—Г—О—В —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –ї–µ—З–µ¬≠–љ–Є—О –Ц–Ф–Р –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –ґ–µ–ї–µ–Ј–∞ –≤ I —В—А–Є–Љ–µ—Б—В—А–µ –Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є вАФ –≤–Њ IIвАУIII —В—А–Є–Љ–µ—Б—В—А–∞—Е [10]. –Т —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ —Б—Г–ї—М—Д–∞—В–∞ –ґ–µ–ї–µ–Ј–∞ –Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞ –Ї–∞—А–±–Њ–Ї—Б–Є–Љ–∞–ї—М—В–Њ–Ј–∞—В–∞, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –≤ —Б—А–Њ–Ї–Є 16вАУ33 –љ–µ–і., –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —А–Њ—Б—В Hb –Є —З–∞—Б—В–Њ—В–∞ –Љ–∞—В–µ—А–Є–љ—Б–Ї–Є—Е –Є –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –±—Л–ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ–Є, –Њ–і–љ–∞–Ї–Њ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є–µ –Є —Б–Њ—Ж–Є–∞–ї—М–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—Л–ї–Є –≤—Л—И–µ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞ [24]. –Т –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–Љ –њ–µ—А–Є–Њ–і–µ –і–ї—П –ї–µ—З–µ–љ–Є—П –∞–љ–µ–Љ–Є–Є –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є –њ–Њ–Ї–∞–Ј–∞–љ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ, —Г–Љ–µ—А–µ–љ–љ–Њ–є –Є —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є вАФ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ь–µ—В–∞–∞–љ–∞–ї–Є–Ј 103 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —Б—А–∞–≤–љ–Є–≤–∞—О—Й–Є—Е –Ї–Њ–≥–Њ—А—В—Л –Є–Ј 10 391 –њ–∞—Ж–Є–µ–љ—В–Ї–Є —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞, 4044 –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –ї–µ—З–µ–љ–Є–µ–Љ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, 1329 вАФ –ї–µ—З–µ–љ–Є–µ–Љ –±–µ–Ј –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ґ–µ–ї–µ–Ј–∞, 3335 вАФ —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –њ–ї–∞—Ж–µ–±–Њ, –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —З–∞—Б—В–Њ—В–∞ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –Є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [25].
–Я—А–µ–њ–∞—А–∞—В—Л –ґ–µ–ї–µ–Ј–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ц–Ф–Р –њ–Њ–і—А–∞–Ј–і–µ–ї—П—О—В—Б—П –љ–∞ –Є–Њ–љ–љ—Л–µ —Б–Њ–ї–µ–≤—Л–µ, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ—А–µ–њ–∞—А–∞—В—Л –і–≤—Г—Е–≤–∞–ї–µ–љ—В–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞ (II), –Є –њ—А–µ–њ–∞—А–∞—В—Л —В—А–µ—Е–≤–∞–ї–µ–љ—В–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞ (III). –Т –Ї–ї–µ—В–Ї–∞—Е —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–≥–Њ –Ї–Є—И–µ—З–љ–Є–Ї–∞ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –ґ–µ–ї–µ–Ј–∞ (II), —В. –Ї. –∞–њ–Њ—Д–µ—А—А–Є—В–Є–љ –≤ —Н–љ—В–µ—А–Њ—Ж–Є—В–∞—Е –Љ–Њ–ґ–µ—В —Б–≤—П–Ј—Л–≤–∞—В—М—Б—П —В–Њ–ї—М–Ї–Њ —Б –Є–Њ–љ–∞–Љ–Є Fe2+. –Я—А–µ–њ–∞—А–∞—В—Л –љ–∞ –Њ—Б–љ–Њ–≤–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б–Њ–ї–µ–є –ґ–µ–ї–µ–Ј–∞ (II) (—Б—Г–ї—М—Д–∞—В–∞, —Д—Г–Љ–∞—А–∞—В–∞, –≥–ї—О–Ї–Њ–љ–∞—В–∞, —Б—Г–Ї—Ж–Є–љ–∞—В–∞, –≥–ї—Г—В–∞–Љ–∞—В–∞, –ї–∞–Ї—В–∞—В–∞ –Є —В. –њ.) –Њ–±–ї–∞–і–∞—О—В –±–Њ–ї—М—И–µ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О –Є —П–≤–ї—П—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б—В–∞—А—В–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є.
–Ц–µ–ї–µ–Ј–∞ (II) —Д—Г–Љ–∞—А–∞—В + —Д–Њ–ї–Є–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є–Є –ґ–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –њ—А–Є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є
–Ф–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –і–µ—Д–Є—Ж–Є—В–∞ –ґ–µ–ї–µ–Ј–∞ –Є –ї–µ—З–µ–љ–Є—П –Ц–Ф–Р –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ –њ—А–µ–њ–∞—А–∞—В –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. вАФ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –ґ–µ–ї–µ–Ј–∞ (II) —Д—Г–Љ–∞—А–∞—В–∞ —Б —Д–Њ–ї–Є–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є (¬Ђ–У.–Ы. –§–∞—А–Љ–∞ –У–Љ–±–•¬ї, –Р–≤—Б—В—А–Є—П). –Я—А–µ–њ–∞—А–∞—В –≤—Л–њ—Г—Б–Ї–∞–µ—В—Б—П –≤ —Д–Њ—А–Љ–µ –Ї–∞–њ—Б—Г–ї –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е 152,1 –Љ–≥ –ґ–µ–ї–µ–Ј–∞ (II) —Д—Г–Љ–∞—А–∞—В–∞ (–≤ –њ–µ—А–µ—Б—З–µ—В–µ –љ–∞ —Н–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ–µ –ґ–µ–ї–µ–Ј–Њ 50 –Љ–≥) –Є —Д–Њ–ї–Є–µ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г (500 –Љ–Ї–≥) [26]. –§—Г–Љ–∞—А–∞—В –ґ–µ–ї–µ–Ј–∞ –Є–Љ–µ–µ—В —А—П–і –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –њ–µ—А–µ–і –і—А—Г–≥–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –љ–∞ –Њ—Б–љ–Њ–≤–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б–Њ–ї–µ–є –ґ–µ–ї–µ–Ј–∞ (II): –Њ–љ –Љ–∞–ї–Њ—А–∞—Б—В–≤–Њ—А–Є–Љ –≤ –≤–Њ–і–µ, –Њ–і–љ–∞–Ї–Њ —Е–Њ—А–Њ—И–Њ —А–∞—Б—В–≤–Њ—А—П–µ—В—Б—П –≤ —А–∞–Ј–±–∞–≤–ї–µ–љ–љ—Л—Е —А–∞—Б—В–≤–Њ—А–∞—Е –Ї–Є—Б–ї–Њ—В (–ґ–µ–ї—Г–і–Њ—З–љ–Њ–Љ —Б–Њ–Ї–µ), –њ–Њ—Н—В–Њ–Љ—Г –њ–Њ—Б–ї–µ —А–∞—Б—В–≤–Њ—А–µ–љ–Є—П –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –ґ–µ–ї—Г–і–Ї–µ –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О; —Б—В–∞–±–Є–ї–µ–љ, –љ–µ –Є–Љ–µ–µ—В —Е–∞—А–∞–Ї—В–µ—А–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–љ–Њ–≥–Њ –њ—А–Є–≤–Ї—Г—Б–∞, –љ–µ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –±–µ–ї–Ї–∞–Љ–Є –≤ –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–∞—Е –Ц–Ъ–Ґ. –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. —Б–Њ–і–µ—А–ґ–Є—В –ґ–µ–ї–µ–Ј–∞ —Д—Г–Љ–∞—А–∞—В –≤ –Ї–∞–њ—Б—Г–ї–µ –≤ –≤–Є–і–µ –Љ–Є–Ї—А–Њ–≥—А–∞–љ—Г–ї –Љ–µ–і–ї–µ–љ–љ–Њ–≥–Њ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—П, –њ–Њ—Н—В–Њ–Љ—Г –∞–±—Б–Њ—А–±—Ж–Є—П –ґ–µ–ї–µ–Ј–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ –Љ–µ—Б—В–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П вАФ 12-–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–µ –Є –≤ —В–Њ—Й–µ–є –Ї–Є—И–Ї–µ –≤ —В–µ—З–µ–љ–Є–µ 4 —З, —З—В–Њ —Б–љ–Є–ґ–∞–µ—В —А–∞–Ј–і—А–∞–ґ–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –Ц–Ъ–Ґ, —Г–Љ–µ–љ—М—И–∞–µ—В –і–Є—Б–њ–µ–њ—Б–Є—З–µ—Б–Ї–Є–µ –Є –і—А—Г–≥–Є–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —П–≤–ї–µ–љ–Є—П.
–†–∞–Ј–ї–Є—З–љ–∞—П –і–Њ–Ј–Є—А–Њ–≤–Ї–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–і–±–Є—А–∞—В—М –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Г—О —Б—Е–µ–Љ—Г –ї–µ—З–µ–љ–Є—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Г—А–Њ–≤–љ—П —Д–µ—А—А–Є—В–Є–љ–∞, –ґ–µ–ї–µ–Ј–∞ –Є Hb –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е. –Ф–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –і–µ—Д–Є—Ж–Є—В–∞ –ґ–µ–ї–µ–Ј–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ 1вАУ2 –Ї–∞–њ—Б./—Б—Г—В –њ–µ—А–Њ—А–∞–ї—М–љ–Њ, –і–ї—П –ї–µ—З–µ–љ–Є—П –Ц–Ф–Р –ї–µ–≥–Ї–Њ–є –Є —Б—А–µ–і–љ–µ–є —Б—В–µ–њ–µ–љ–Є вАФ 2вАУ3 –Ї–∞–њ—Б./—Б—Г—В –і–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Г—А–Њ–≤–љ—П –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞, –њ–Њ—Б–ї–µ —З–µ–≥–Њ —Б–ї–µ–і—Г–µ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В—М –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –њ–Њ 1 –Ї–∞–њ—Б./—Б—Г—В (–њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–∞—П –і–Њ–Ј–∞) –і–ї—П –≤–Њ—Б–њ–Њ–ї–љ–µ–љ–Є—П –Ј–∞–њ–∞—Б–Њ–≤ –ґ–µ–ї–µ–Ј–∞ –љ–µ –Љ–µ–љ–µ–µ 8вАУ12 –љ–µ–і.
–Э–∞–Љ–Є –њ—А–Њ–≤–µ–і–µ–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, —Ж–µ–ї—М—О –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –ґ–µ–ї–µ–Ј–∞ —Д—Г–Љ–∞—А–∞—В–∞ —Б —Д–Њ–ї–Є–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є (–§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ.) –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є–Є –∞–љ–µ–Љ–Є–Є –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –≤–Њ IIвАУIII —В—А–Є–Љ–µ—Б—В—А–∞—Е –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П –Љ–∞—В–µ—А–Є–љ—Б–Ї–Є—Е –Є –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 90 –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –≤–Њ II —В—А–Є–Љ–µ—Б—В—А–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є (13вАУ27 (6) –љ–µ–і.): –≤ I –≥—А—Г–њ–њ—Г –≤–Њ—И–ї–Є 30 –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є —Д–µ—А—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є, –≤–Њ II –≥—А—Г–њ–њ—Г вАФ 30 –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б –ї–∞—В–µ–љ—В–љ—Л–Љ –і–µ—Д–Є—Ж–Є—В–Њ–Љ –ґ–µ–ї–µ–Ј–∞ (–Ї—А–Є—В–µ—А–Є–Є –≤–Ї–ї—О—З–µ–љ–Є—П: Hb>110 –≥/–ї, –°–§<30 –Љ–Ї–≥/–ї), –≤ III –≥—А—Г–њ–њ—Г вАФ 30 –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–љ–Њ–є –∞–љ–µ–Љ–Є–µ–є (–Ї—А–Є—В–µ—А–Є–Є –≤–Ї–ї—О—З–µ–љ–Є—П: Hb<110 –≥/–ї, Fe<12,5 –Љ–Ї–Љ–Њ–ї—М/–ї, –°–§<20 –Љ–Ї–≥/–ї). –Т–Њ–Ј—А–∞—Б—В –≤—Б–µ—Е –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –Ї–Њ–ї–µ–±–∞–ї—Б—П –Њ—В 18 –і–Њ 40 –ї–µ—В, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В —Б–Њ—Б—В–∞–≤–Є–ї 28,8¬±4,6 –≥–Њ–і–∞.
–Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–∞–ї–Њ: –∞–љ–∞–ї–Є–Ј —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –∞–Ї—Г—И–µ—А—Б–Ї–Њ-–≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–Љ–љ–µ–Ј–∞, —В–µ—З–µ–љ–Є–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, —А–Њ–і–Њ–≤ –Є –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞; –Њ–±—Й–µ–µ –Є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–µ –∞–Ї—Г—И–µ—А—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –і–Њ–њ–њ–ї–µ—А–Њ–Љ–µ—В—А–Є—О –Є –Ї–∞—А–і–Є–Њ—В–Њ–Ї–Њ–≥—А–∞—Д–Є—О (–≤ III —В—А–Є–Љ–µ—Б—В—А–µ); –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є –Є –Љ–Њ—З–Є –≤ –і–Є–љ–∞–Љ–Є–Ї–µ, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –≥—А—Г–њ–њ—Л –Ї—А–Њ–≤–Є –Є —А–µ–Ј—Г—Б-—Д–∞–Ї—В–Њ—А–∞, –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞, —Д–µ—А—А–Є—В–Є–љ–∞ –≤ –і–Є–љ–∞–Љ–Є–Ї–µ, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ (–Ї–Њ–∞–≥—Г–ї–Њ–≥—А–∞–Љ–Љ—Г) –≤ –і–Є–љ–∞–Љ–Є–Ї–µ, –∞–љ–∞–ї–Є–Ј –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –≤–ї–∞–≥–∞–ї–Є—Й–∞ –Є —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞. –Ґ–∞–Ї–ґ–µ –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј —Б–Њ—Б—В–Њ—П–љ–Є—П –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ–Њ–≥–Њ –њ—А–Є —А–Њ–ґ–і–µ–љ–Є–Є –Є —В–µ—З–µ–љ–Є—П —А–∞–љ–љ–µ–≥–Њ –љ–µ–Њ–љ–∞—В–∞–ї—М–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞.
–С–µ—А–µ–Љ–µ–љ–љ—Л–Љ I –Є II –≥—А—Г–њ–њ –љ–∞–Ј–љ–∞—З–∞–ї–Є 1 –Ї–∞–њ—Б./—Б—Г—В (50 –Љ–≥ –ґ–µ–ї–µ–Ј–∞ + 500 –Љ–Ї–≥ —Д–Њ–ї–Є–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л) –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ., III –≥—А—Г–њ–њ—Л вАФ 2 –Ї–∞–њ—Б./—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 2 –Љ–µ—Б., –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞, –љ–∞–ї–Є—З–Є–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є. –Ч–∞—В–µ–Љ –њ—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–µ–є –і–Њ–Ј–µ –і–Њ –Ї–Њ–љ—Ж–∞ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –≤–Њ –≤—Б–µ—Е –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –≥—А—Г–њ–њ–∞—Е (1 –Ї–∞–њ—Б./—Б—Г—В). –У–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є (Hb, Ht, —Н—А–Є—В—А–Њ—Ж–Є—В—Л, —А–µ—В–Є–Ї—Г–ї–Њ—Ж–Є—В—Л, MCV (mean corpuscular volume вАФ —Б—А–µ–і–љ–Є–є –Њ–±—К–µ–Љ —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤), MCH (mean cell hemoglobin вАФ —Б—А–µ–і–љ–µ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ Hb –≤ —Н—А–Є—В—А–Њ—Ж–Є—В–µ), MCHC (mean cell Hb concentration вАФ —Б—А–µ–і–љ—П—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ –≤ —Н—А–Є—В—А–Њ—Ж–Є—В–∞—Е), RDW (red cell distribution width вАФ —И–Є—А–Є–љ–∞ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –њ–Њ –Њ–±—К–µ–Љ—Г)) –Є —Д–µ—А—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л (—Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–µ –ґ–µ–ї–µ–Ј–Њ, —Д–µ—А—А–Є—В–Є–љ) –Њ–њ—А–µ–і–µ–ї—П–ї–Є –і–Њ –ї–µ—З–µ–љ–Є—П (–њ–Њ–і–≥—А—Г–њ–њ—Л Ia, IIa, IIIa) –Є —З–µ—А–µ–Ј 2 –Љ–µ—Б. –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П (–њ–Њ–і–≥—А—Г–њ–њ—Л Ib, IIb, IIIb).
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –±—Л–ї –≤—Л–њ–Њ–ї–љ–µ–љ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ—А–Њ–≥—А–∞–Љ–Љ—Л –і–ї—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞–±–Њ—В–Ї–Є Statistica 6, —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Ї–∞–Ї —Б—А–µ–і–љ–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ (M) ¬± —Б—В–∞–љ–і–∞—А—В–љ–∞—П –Њ—И–Є–±–Ї–∞ (SE), —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г —Б—А–∞–≤–љ–Є–≤–∞–µ–Љ—Л–Љ–Є –≤–µ–ї–Є—З–Є–љ–∞–Љ–Є –њ—А–Є–Ј–љ–∞–≤–∞–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є –њ—А–Є —Г—А–Њ–≤–љ–µ –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є p<0,05.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Р–љ–∞–ї–Є–Ј –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–Љ–љ–µ–Ј–∞ –љ–µ –≤—Л—П–≤–Є–ї –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –≥—А—Г–њ–њ. –Р–љ–∞–ї–Є–Ј —Б—В—А—Г–Ї—В—Г—А—Л —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≤—Л—П–≤–Є–ї –≤—Л—Б–Њ–Ї—Г—О —З–∞—Б—В–Њ—В—Г —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ –≤–Њ II –Є III –≥—А—Г–њ–њ–∞—Е: —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –ї–∞—В–µ–љ—В–љ—Л–Љ –і–µ—Д–Є—Ж–Є—В–Њ–Љ –ґ–µ–ї–µ–Ј–∞ вАФ 4 (13,3%) —Б–ї—Г—З–∞—П, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –Ц–Ф–Р вАФ 4 (13,3%) —Б–ї—Г—З–∞—П. –Р–љ–µ–Љ–Є—П –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —Г 1 (3,3%) –њ–∞—Ж–Є–µ–љ—В–Ї–Є I –≥—А—Г–њ–њ—Л, 2 (6,7%) вАФ II –≥—А—Г–њ–њ—Л –Є 7 (23,3%) вАФ III –≥—А—Г–њ–њ—Л. –Я–∞—В–Њ–ї–Њ–≥–Є—П –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–∞—Б—М –≤ III –≥—А—Г–њ–њ–µ вАФ 8 (26,7%) –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б –Ц–Ф–Р (–≤ I –Є II –≥—А—Г–њ–њ–∞—Е 3 (10,0%) –Є 4 (13,3%) –њ–∞—Ж–Є–µ–љ—В–Ї–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ).
–†–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј –±—Л–ї –Њ—В—П–≥–Њ—Й–µ–љ –љ–µ–≤—Л–љ–∞—И–Є–≤–∞–љ–Є–µ–Љ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є —Г 4 (13,3%) –±–µ—А–µ–Љ–µ–љ–љ—Л—Е I –≥—А—Г–њ–њ—Л, 4 (13,3%) вАФ II –≥—А—Г–њ–њ—Л, 6 (20,0%) вАФ III –≥—А—Г–њ–њ—Л; –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ—Л–µ —А–Њ–і—Л –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ вАФ —Г 1 (3,3%) –±–µ—А–µ–Љ–µ–љ–љ–Њ–є III –≥—А—Г–њ–њ—Л. –Т I –≥—А—Г–њ–њ–µ –њ–µ—А–≤–Њ—А–Њ–і—П—Й–Є—Е –±—Л–ї–Њ –±–Њ–ї—М—И–µ, —З–µ–Љ –≤–Њ II –Є III –≥—А—Г–њ–њ–∞—Е (23 (76,7%), 21 (70,0%) –Є 18 (60,0%) —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Ш–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є—Б–Ї–ї—О—З–µ–љ—Л —Б–ї—Г—З–∞–Є –Љ–љ–Њ–≥–Њ–њ–ї–Њ–і–љ–Њ–є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є.
–Р–љ–∞–ї–Є–Ј —В–µ—З–µ–љ–Є—П –і–∞–љ–љ–Њ–є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є —Г –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –≤—Л—П–≤–Є–ї –≤—Л—Б–Њ–Ї—Г—О —З–∞—Б—В–Њ—В—Г —Г–≥—А–Њ–Ј—Л –њ—А–µ—А—Л–≤–∞–љ–Є—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –≤–Њ –≤—Б–µ—Е –≥—А—Г–њ–њ–∞—Е: 15 (50,0%) —Б–ї—Г—З–∞–µ–≤ –≤ I –≥—А—Г–њ–њ–µ, 17 (56,7%) вАФ –≤–Њ II –≥—А—Г–њ–њ–µ, 17 (56,7%) вАФ –≤ III –≥—А—Г–њ–њ–µ. –Т –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –≥—А—Г–њ–њ–∞—Е –≤—Л—П–≤–ї–µ–љ–∞ –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ –≥–µ—Б—В–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ вАФ 1 —Б–ї—Г—З–∞–є (3,3%) –≤ I –≥—А—Г–њ–њ–µ, 4 (13,3%) вАФ –≤–Њ II –≥—А—Г–њ–њ–µ, 5 вАФ (16,7%) –≤ III –≥—А—Г–њ–њ–µ. –Ф–Є–∞–≥–љ–Њ–Ј –њ–ї–∞—Ж–µ–љ—В–∞—А–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ —Г 1 (3,3%) –±–µ—А–µ–Љ–µ–љ–љ–Њ–є I –≥—А—Г–њ–њ—Л, 2 (6,7%) вАФ II –≥—А—Г–њ–њ—Л –Є 3 (10,0%) вАФ III –≥—А—Г–њ–њ—Л. –Т III —В—А–Є–Љ–µ—Б—В—А–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є —Г —А—П–і–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –±—Л–ї–∞ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–∞ —Г–Љ–µ—А–µ–љ–љ–∞—П –њ—А–µ—Н–Ї–ї–∞–Љ–њ—Б–Є—П: —Г 1 (3,3%) –±–µ—А–µ–Љ–µ–љ–љ–Њ–є I –≥—А—Г–њ–њ—Л,
2 (6,7%) вАФ II –≥—А—Г–њ–њ—Л –Є 2 (6,7%) вАФ III –≥—А—Г–њ–њ—Л.
–£ –≤—Б–µ—Е –±–µ—А–µ–Љ–µ–љ–љ—Л—Е III –≥—А—Г–њ–њ—Л –≤–Њ II —В—А–Є–Љ–µ—Б—В—А–µ –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ –Ц–Ф–Р –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є (Hb 90вАУ110 –≥/–ї), –Њ–і–љ–∞–Ї–Њ –њ—А–Є –њ–µ—А–≤–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. —В–Њ–ї—М–Ї–Њ 7 (23,3%) –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–µ–і—К—П–≤–ї—П–ї–Є –ґ–∞–ї–Њ–±—Л –љ–∞ —Б–ї–∞–±–Њ—Б—В—М, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, –Њ–і—Л—И–Ї—Г –њ—А–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–µ. –С–µ—А–µ–Љ–µ–љ–љ—Л–µ II –≥—А—Г–њ–њ—Л —Б –ї–∞—В–µ–љ—В–љ—Л–Љ –і–µ—Д–Є—Ж–Є—В–Њ–Љ –ґ–µ–ї–µ–Ј–∞ –њ—А–Є —Б–±–Њ—А–µ –∞–љ–∞–Љ–љ–µ–Ј–∞ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –ґ–∞–ї–Њ–± –љ–µ –њ—А–µ–і—К—П–≤–ї—П–ї–Є.
–Я—А–Њ–≤–µ–і–µ–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –Є—Б—Е–Њ–і–Њ–≤ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —А–Њ–і—Л –±—Л–ї–Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ—Л–Љ–Є —Г –≤—Б–µ—Е –±–µ—А–µ–Љ–µ–љ–љ—Л—Е I –Є II –≥—А—Г–њ–њ –Є —Г 28 (93,3%) –±–µ—А–µ–Љ–µ–љ–љ—Л—Е III –≥—А—Г–њ–њ—Л (2 –±–µ—А–µ–Љ–µ–љ–љ—Л–µ –±—Л–ї–Є —А–Њ–і–Њ—А–∞–Ј—А–µ—И–µ–љ—Л –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ–Њ –≤ —Б—А–Њ–Ї–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є 36вАУ37 –љ–µ–і. –њ–Њ –∞–Ї—Г—И–µ—А—Б–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ вАФ —Г–Љ–µ—А–µ–љ–љ–∞—П –њ—А–µ—Н–Ї–ї–∞–Љ–њ—Б–Є—П, –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ–∞—П –њ–ї–∞—Ж–µ–љ—В–∞—А–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М). –†–Њ–і–Њ—А–∞–Ј—А–µ—И–µ–љ–Є–µ –њ—Г—В–µ–Љ –Њ–њ–µ—А–∞—Ж–Є–Є –Ї–µ—Б–∞—А–µ–≤–∞ —Б–µ—З–µ–љ–Є—П –њ–Њ –∞–Ї—Г—И–µ—А—Б–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ (—А—Г–±–µ—Ж –љ–∞ –Љ–∞—В–Ї–µ, —В–∞–Ј–Њ–≤–Њ–µ –њ—А–µ–і–ї–µ–ґ–∞–љ–Є–µ –њ–ї–Њ–і–∞, –∞–љ–Њ–Љ–∞–ї–Є–Є —А–Њ–і–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є, –њ—А–µ–і–ї–µ–ґ–∞–љ–Є–µ –њ–ї–∞—Ж–µ–љ—В—Л, –њ—А–µ—Н–Ї–ї–∞–Љ–њ—Б–Є—П, –≥–Є–њ–Њ–Ї—Б–Є—П –њ–ї–Њ–і–∞ –Є –і—А.) –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Њ —Г 6 (20,0%), 6 (20,0%) –Є 7 (23,3%) –±–µ—А–µ–Љ–µ–љ–љ—Л—Е I, II –Є III –≥—А—Г–њ–њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ.
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –±—Л–ї–Є –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л –Љ–∞—Б—Б–∞ –њ—А–Є —А–Њ–ґ–і–µ–љ–Є–Є, —А–Њ—Б—В, –Њ—Ж–µ–љ–Ї–∞ –њ–Њ —И–Ї–∞–ї–µ –Р–њ–≥–∞—А –љ–∞ 1-–є –Є 5-–є –Љ–Є–љ –ґ–Є–Ј–љ–Є. –Ь–∞—Б—Б–∞ –і–Њ–љ–Њ—И–µ–љ–љ—Л—Е –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –≤ I –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 3560¬±158 –≥, —А–Њ—Б—В 50,3¬±1,2 —Б–Љ; –≤–Њ II –≥—А—Г–њ–њ–µ вАФ 3450¬±138 –≥, —А–Њ—Б—В 50,3¬±1,1 —Б–Љ; –≤ III –≥—А—Г–њ–њ–µ –Љ–∞—Б—Б–∞ –і–Њ–љ–Њ—И–µ–љ–љ—Л—Е –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е —Б–Њ—Б—В–∞–≤–Є–ї–∞ 3520¬±174 –≥, —А–Њ—Б—В 50,4¬±1,2 —Б–Љ, –љ–µ–і–Њ–љ–Њ—И–µ–љ–љ—Л—Е вАФ 2430¬±166 –≥, —А–Њ—Б—В 46¬±1,0 —Б–Љ; —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ (—А<0,05). –І–∞—Б—В–Њ—В–∞ —А–Њ–ґ–і–µ–љ–Є—П –Ї—А—Г–њ–љ–Њ–≥–Њ –њ–ї–Њ–і–∞ (>4000 –≥) —Б—А–µ–і–Є –і–Њ–љ–Њ—И–µ–љ–љ—Л—Е –і–µ—В–µ–є I –≥—А—Г–њ–њ—Л —Б–Њ—Б—В–∞–≤–Є–ї–∞ 3 —Б–ї—Г—З–∞—П (10,0%), II –≥—А—Г–њ–њ—Л вАФ 2 —Б–ї—Г—З–∞—П (6,7%), III –≥—А—Г–њ–њ—Л вАФ 3 —Б–ї—Г—З–∞—П (10,0%). –Я—А–Є–Ј–љ–∞–Ї–Є —Б–Є–љ–і—А–Њ–Љ–∞ –Ј–∞–і–µ—А–ґ–Ї–Є —А–Њ—Б—В–∞ –њ–ї–Њ–і–∞ I —Б—В–µ–њ–µ–љ–Є –≤—Л—П–≤–ї–µ–љ—Л —Г 3 (10,0%) –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е III –≥—А—Г–њ–њ—Л. –Э–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л–µ –≤ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –≥—А—Г–њ–њ–∞—Е —А–Њ–і–Є–ї–Є—Б—М –≤ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є —Б –Њ—Ж–µ–љ–Ї–Њ–є –њ–Њ —И–Ї–∞–ї–µ –Р–њ–≥–∞—А –љ–∞ 1-–є –Љ–Є–љ –ґ–Є–Ј–љ–Є 7,9¬±0,3, 7,8¬±0,2, 7,5¬±0,4 –±–∞–ї–ї–∞ –≤ I, II, III –≥—А—Г–њ–њ–∞—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –љ–∞ 5-–є –Љ–Є–љ 8,9¬±0,3, 8,8¬±0,2, 8,5¬±0,3 –±–∞–ї–ї–∞ –≤ I, II, III –≥—А—Г–њ–њ–∞—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –°–ї—Г—З–∞–µ–≤ –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–µ –±—Л–ї–Њ.
–Р–љ–∞–ї–Є–Ј —В–µ—З–µ–љ–Є—П –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –Њ–љ –Њ—Б–ї–Њ–ґ–љ–Є–ї—Б—П –∞–љ–µ–Љ–Є–µ–є –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є —Г 1 (3,3%) —А–Њ–і–Є–ї—М–љ–Є—Ж—Л I –≥—А—Г–њ–њ—Л, —Г 2 (6,7%) вАФ II –≥—А—Г–њ–њ—Л –Є —Г 7 (23,3%) вАФ III –≥—А—Г–њ–њ—Л. –Т—Б–µ —А–Њ–і–Є–ї—М–љ–Є—Ж—Л –±—Л–ї–Є –≤—Л–њ–Є—Б–∞–љ—Л –і–Њ–Љ–Њ–є –≤ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –љ–∞ 3вАУ6-–µ —Б—Г—В –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞.
–Э–∞–Љ–Є –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є —Д–µ—А—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П (–њ–Њ–і–≥—А—Г–њ–њ—Л Ia, IIa, IIIa) –Є –≤ –і–Є–љ–∞–Љ–Є–Ї–µ —З–µ—А–µ–Ј 2 –Љ–µ—Б. –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П (–њ–Њ–і–≥—А—Г–њ–њ—Л Ib, IIb, IIIb), –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1.
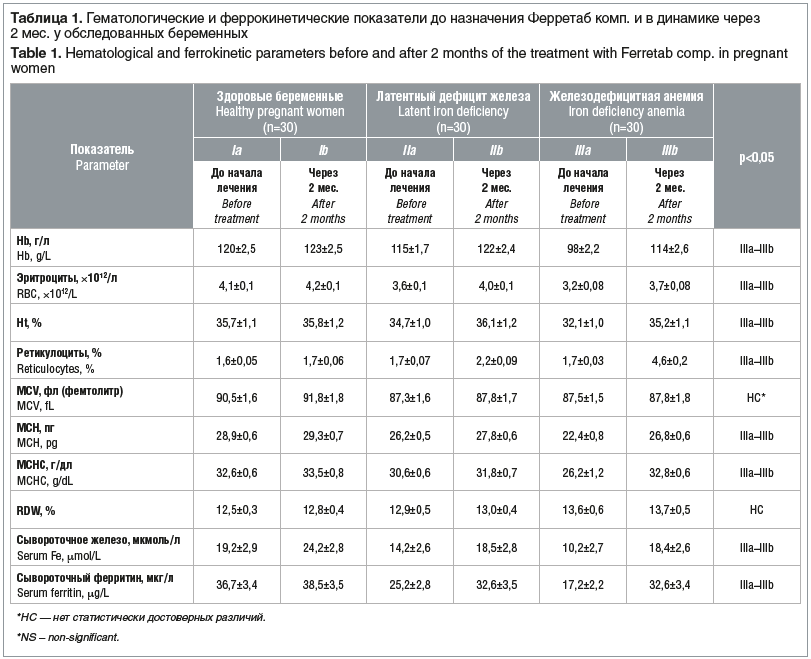
–Т I –≥—А—Г–њ–њ–µ –Ј–і–Њ—А–Њ–≤—Л—Е –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –і–Њ –љ–∞—З–∞–ї–∞ —Д–µ—А—А–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –Є —Д–µ—А—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –±—Л–ї–Є –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. (1 –Ї–∞–њ—Б./—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 2 –Љ–µ—Б.) —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М —Б—В–∞–±–Є–ї—М–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –≤—Б–µ—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —Е–Њ—А–Њ—И–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —А–∞–Ј–≤–Є—В–Є—П –∞–љ–µ–Љ–Є–Є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –±–µ—А–µ–Љ–µ–љ–љ—Л—Е (—Б–Љ. —В–∞–±–ї. 1).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±–µ—А–µ–Љ–µ–љ–љ—Л—Е II –≥—А—Г–њ–њ—Л —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ –ї–∞—В–µ–љ—В–љ—Л–є –і–µ—Д–Є—Ж–Є—В –ґ–µ–ї–µ–Ј–∞, –і–ї—П –Ї–Њ—В–Њ—А–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –°–§ –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–Є –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–Њ—А–Љ—Л –Њ—Б–љ–Њ–≤–љ—Л—Е –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є (Hb, Ht, RBC, MCV, –Ь–°–Э, –Ь–°–Э–° –Є RDW). –Я–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. (1 –Ї–∞–њ—Б./—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 2 –Љ–µ—Б.) –Њ—В–Љ–µ—З–µ–љ —А–Њ—Б—В –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, –∞ —Д–µ—А—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Њ—Б—В–∞–ї–Є—Б—М –љ–∞ —В–Њ–Љ –ґ–µ —Г—А–Њ–≤–љ–µ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. –љ–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г–µ—В –і–∞–ї—М–љ–µ–є—И–µ–µ –Є—Б—В–Њ—Й–µ–љ–Є–µ —А–µ–Ј–µ—А–≤–Њ–≤ –ґ–µ–ї–µ–Ј–∞ –њ—А–Є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, —З—В–Њ –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –Ц–Ф–Р —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б –ї–∞—В–µ–љ—В–љ—Л–Љ –і–µ—Д–Є—Ж–Є—В–Њ–Љ –ґ–µ–ї–µ–Ј–∞ (—Б–Љ. —В–∞–±–ї. 1).
–£ –±–µ—А–µ–Љ–µ–љ–љ—Л—Е III –≥—А—Г–њ–њ—Л –≤ –љ–∞—З–∞–ї–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Є —Б–љ–Є–ґ–µ–љ—Л –Ї–∞–Ї –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ, —В–∞–Ї –Є —Д–µ—А—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —А–∞–Ј–≤–Є—В–Є–Є –Ц–Ф–Р; —Г –≤—Б–µ—Е –±–µ—А–µ–Љ–µ–љ–љ—Л—Е —Н—В–Њ–є –≥—А—Г–њ–њ—Л –±—Л–ї–∞ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–∞ –∞–љ–µ–Љ–Є—П –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є. –Я–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. (2 –Ї–∞–њ—Б./—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 2 –Љ–µ—Б.) –њ–Њ–ї—Г—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–∞–Ї –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е, —В–∞–Ї –Є —Д–µ—А—А–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є (Hb, —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤, Ht, —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞, –°–§) (—Б–Љ. —В–∞–±–ї. 1).
–°–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–ї—Б—П –њ–∞—Ж–Є–µ–љ—В–Ї–∞–Љ–Є –≤—Б–µ—Е –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –≥—А—Г–њ–њ, –љ–µ –≤—Л–Ј—Л–≤–∞–ї –і–Є—Б–њ–µ–њ—Б–Є—З–µ—Б–Ї–Є—Е —П–≤–ї–µ–љ–Є–є –Є –љ–∞—А—Г—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞, –±—Л–ї —Б–Њ–≤–Љ–µ—Б—В–Є–Љ —Б –і—А—Г–≥–Є–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –љ–∞–Ј–љ–∞—З–µ–љ–љ—Л–Љ–Є –і–ї—П –ї–µ—З–µ–љ–Є—П —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є. –Э–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –љ–∞ —Д–Њ–љ–µ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ –љ–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ.
–Т—Л–≤–Њ–і—Л
–Р–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ј–≤–Њ–ї–Є–ї —Б–і–µ–ї–∞—В—М —Б–ї–µ–і—Г—О—Й–Є–µ –≤—Л–≤–Њ–і—Л.
–Я—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. вАФ –ґ–µ–ї–µ–Ј–∞ (II) —Д—Г–Љ–∞—А–∞—В–∞ –≤ –і–Њ–Ј–µ 152,1 –Љ–≥ –Є —Д–Њ–ї–Є–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –і–Њ–Ј–µ 500 –Љ–Ї–≥ (1 –Ї–∞–њ—Б—Г–ї–∞ вАФ 50 –Љ–≥ —Н–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞) –Ј–і–Њ—А–Њ–≤—Л–Љ –±–µ—А–µ–Љ–µ–љ–љ—Л–Љ –≤–Њ IIвАУIII —В—А–Є–Љ–µ—Б—В—А–∞—Е –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –ї–∞—В–µ–љ—В–љ–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ –ґ–µ–ї–µ–Ј–∞ –Є –Ц–Ф–Р, –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–Љ–Є —П–≤–ї–µ–љ–Є—П–Љ–Є –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –њ–∞—Ж–Є–µ–љ—В–Ї–∞–Љ–Є. –Т–Ї–ї—О—З–µ–љ–Є–µ —Д–Њ–ї–Є–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л 500 –Љ–Ї–≥ –≤ —Б–Њ—Б—В–∞–≤ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г—Б–Є–ї–µ–љ–Є—О –≥–µ–Љ–Њ–њ–Њ—Н–Ј–∞, —Г—В–Є–ї–Є–Ј–∞—Ж–Є–Є –Є –≤—Б–∞—Б—Л–≤–∞–љ–Є—О –ґ–µ–ї–µ–Ј–∞, —З—В–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –∞–љ–µ–Љ–Є–Є.
–Ф–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –ї–∞—В–µ–љ—В–љ–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ –ґ–µ–ї–µ–Ј–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –≤ I —В—А–Є–Љ–µ—Б—В—А–µ —Г—А–Њ–≤–љ—П –°–§ –Є –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ –љ–∞—З–∞—В—М –ї–µ—З–µ–љ–Є–µ –ї–∞—В–µ–љ—В–љ–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ –ґ–µ–ї–µ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. (1 –Ї–∞–њ—Б./—Б—Г—В) –Є –њ—А–µ–і—Г–њ—А–µ–і–Є—В—М —А–∞–Ј–≤–Є—В–Є–µ –Ц–Ф–Р –Є –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є.
–Ф–ї—П –ї–µ—З–µ–љ–Є—П –Ц–Ф–Р –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г–≤–µ–ї–Є—З–Є—В—М –і–Њ 2 –Ї–∞–њ—Б./—Б—Г—В (100 –Љ–≥ —Н–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞), –њ—А–Є —Н—В–Њ–Љ —З–µ—А–µ–Ј 2 –Љ–µ—Б. –ї–µ—З–µ–љ–Є—П –љ–∞–±–ї—О–і–∞—О—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Є —А–Њ—Б—В –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є; –њ–Њ—Б–ї–µ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Г—А–Њ–≤–љ—П –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ –і–ї—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –і–µ–њ–Њ –ґ–µ–ї–µ–Ј–∞ —В–µ—А–∞–њ–Є—О –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–і–Њ–ї–ґ–∞—В—М –≤ —В–µ—З–µ–љ–Є–µ 2вАУ3 –Љ–µ—Б. –≤ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–µ–є –і–Њ–Ј–µ –Є –≤ —В–µ—З–µ–љ–Є–µ 6 –љ–µ–і. –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ (1 –Ї–∞–њ—Б./—Б—Г—В вАФ 50 –Љ–≥ —Н–ї–µ–Љ–µ–љ—В–∞—А–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤—Л—Б–Њ–Ї–∞—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –§–µ—А—А–µ—В–∞–± –Ї–Њ–Љ–њ. –Є –µ–≥–Њ —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –µ–≥–Њ –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В –≤—Л–±–Њ—А–∞ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –∞–љ–µ–Љ–Є–Є, –ї–µ—З–µ–љ–Є—П –ї–∞—В–µ–љ—В–љ–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ –ґ–µ–ї–µ–Ј–∞ –Є –Ц–Ф–Р –њ—А–Є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є.
–°–≤–µ–і–µ–љ–Є—П –Њ–± –∞–≤—В–Њ—А–µ:
–С–∞—Е–∞—А–µ–≤–∞ –Ш—А–Є–љ–∞ –Т–Є–Ї—В–Њ—А–Њ–≤–љ–∞ вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А –Ї–∞—Д–µ–і—А—Л –∞–Ї—Г—И–µ—А—Б—В–≤–∞ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є –ї–µ—З–µ–±–љ–Њ–≥–Њ —Д–∞–Ї—Г–ї—М—В–µ—В–∞, ODCID iD 0000-0002-3078-0744.
–§–У–С–Ю–£ –Т–Ю –†–Э–Ш–Ь–£ –Є–Љ. –Э.–Ш. –Я–Є—А–Њ–≥–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є. 117997, –†–Њ—Б—Б–Є—П, –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –Ю—Б—В—А–Њ–≤–Є—В—П–љ–Њ–≤–∞, –і. 1.
–Ъ–Њ–љ—В–∞–Ї—В–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П: –С–∞—Е–∞—А–µ–≤–∞ –Ш—А–Є–љ–∞ –Т–Є–Ї—В–Њ—А–Њ–≤–љ–∞, e-mail: iribakhareva@yandex.ru. –Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є: –∞–≤—В–Њ—А –љ–µ –Є–Љ–µ–µ—В —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –Є–ї–Є –Љ–µ—В–Њ–і–∞—Е. –Ъ–Њ–љ—Д–ї–Є–Ї—В –Є–љ—В–µ—А–µ—Б–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В. –°—В–∞—В—М—П –њ–Њ—Б—В—Г–њ–Є–ї–∞ 20.04.2019.
About the authors:
Irina V. Bakhareva вАФ MD, PhD, Professor of the Department of Obstetrics and Gynecology, ODCID iD 0000-0002-3078-0744.
Pirogov Russian National Research Medical University. 1, Ostrovityanov str., Moscow, 117997, Russian Federation.
Contact information: Irina V. Bakhareva, e-mail: iribakhareva@yandex.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 20.04.2019.












