–Т–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л (–Т–Ч–Ю–Ь–Ґ) —П–≤–ї—П—О—В—Б—П –Њ–і–љ–Њ–є –Є–Ј —Б–∞–Љ—Л—Е —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –њ—А–Є—З–Є–љ –Њ–±—А–∞—Й–µ–љ–Є—П –ґ–µ–љ—Й–Є–љ –Ї –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥—Г. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ–µ—А–µ–і–∞—О—Й–Є–µ—Б—П –њ–Њ–ї–Њ–≤—Л–Љ –њ—Г—В–µ–Љ, –Њ–Ї–∞–Ј—Л–≤–∞—О—В –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–є –љ–∞ –Ј–і–Њ—А–Њ–≤—М–µ —З–µ–ї–Њ–≤–µ–Ї–∞, –љ–Њ –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–Љ –Є–Ј –љ–Є—Е —П–≤–ї—П–µ—В—Б—П —Г—А–Њ–љ, –љ–∞–љ–Њ—Б–Є–Љ—Л–є —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є. –°—В—А–∞–і–∞—О—В –Ї–∞–Ї –Љ—Г–ґ—З–Є–љ—Л, —В–∞–Ї –Є –ґ–µ–љ—Й–Є–љ—Л, –Њ–і–љ–∞–Ї–Њ –љ–∞–і–Њ –њ—А–Є–Ј–љ–∞—В—М, —З—В–Њ –ґ–µ–љ—Б–Ї–Њ–µ –Ј–і–Њ—А–Њ–≤—М–µ –≤ –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є–Є —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Є–≥—А–∞–µ—В –±–Њ–ї—М—И—Г—О —А–Њ–ї—М. –Ъ–∞–Ї–Њ–≤–∞ –ґ–µ —Б–Є—В—Г–∞—Ж–Є—П? –С–Њ–ї—М–љ—Л–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–Њ—Б—В–∞–≤–ї—П—О—В 60–65% –≤—Б–µ—Е –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е. –Я—А–Є–љ–Є–Љ–∞—П –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ —А–Њ–ї—М –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є —В–∞–Ї–Є—Е –њ–∞—В–Њ–ї–Њ–≥–Є–є, –Ї–∞–Ї —Н–Ї—В–Њ–њ–Є—П —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є – 15% –Њ—В —З–Є—Б–ї–∞ –≤—Б–µ—Е –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е, –ї–µ–є–Њ–Љ–Є–Њ–Љ–∞ –Љ–∞—В–Ї–Є – 30%, —Н–љ–і–Њ–Љ–µ—В—А–Є–Њ–Ј – 25%, –њ–Њ–ї—Г—З–∞–µ—В—Б—П, —З—В–Њ –≤ —Б—Г–Љ–Љ–µ –њ–µ—А–µ–Ї—А—Л–≤–∞–µ—В—Б—П –њ–Њ—З—В–Є –≤–µ—Б—М —Б–њ–µ–Ї—В—А –±–Њ–ї—М–љ—Л—Е, –Њ–±—А–∞—Й–∞—О—Й–Є—Е—Б—П –≤ –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –Ї–ї–Є–љ–Є–Ї—Г. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —П–≤–ї—П—О—В—Б—П —Б–∞–Љ–Њ–є —З–∞—Б—В–Њ–є –њ—А–Є—З–Є–љ–Њ–є –љ–µ–≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –±–µ—Б–њ–ї–Њ–і–Є—П, —Н–Ї—В–Њ–њ–Є—З–µ—Б–Ї–Є—Е –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–µ–є, –љ–µ–≤—Л–љ–∞—И–Є–≤–∞–љ–Є—П, –±–Њ–ї–µ–Ј–љ–µ–є –Є –њ–Њ—А–Њ–Ї–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –њ–ї–Њ–і–∞, –Є –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ – –±–Њ–ї—М—И–Њ–≥–Њ —З–Є—Б–ї–∞ –Њ–њ–µ—А–∞—В–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤.
–Ю—Б–љ–Њ–≤–љ–Њ–є —Б–њ–µ–Ї—В—А –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л—Е –Ј–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≥–µ–љ–Є—В–∞–ї–Є–є, —Б–Њ—Б—В–Њ–Є—В –Є–Ј —Б–ї–µ–і—Г—О—Й–Є—Е –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є: —Е–ї–∞–Љ–Є–і–Є–Є, –≥–Њ–љ–Њ–Ї–Њ–Ї–Ї–Є, –Љ–Є–Ї–Њ–њ–ї–∞–Ј–Љ—Л, —Г—А–µ–∞–њ–ї–∞–Ј–Љ—Л –Є —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і—Л. –Х–ґ–µ–≥–Њ–і–љ–Њ –≤ –Љ–Є—А–µ —А–µ–≥–Є—Б—В—А–Є—А—Г–µ—В—Б—П 100 –Љ–Є–ї–ї–Є–Њ–љ–Њ–≤ —Б–ї—Г—З–∞–µ–≤ –Ј–∞—А–∞–ґ–µ–љ–Є—П —Е–ї–∞–Љ–Є–і–Є–Њ–Ј–Њ–Љ, 62 –Љ–Є–ї–ї–Є–Њ–љ–Њ–≤ – –≥–Њ–љ–Њ—А–µ–µ–є, 170 –Љ–Є–ї–ї–Є–Њ–љ–Њ–≤ – —В—А–Є—Е–Њ–Љ–Њ–љ–Є–∞–Ј–Њ–Љ. –Ъ–∞–ґ–і–Њ–µ –Є–Ј —Н—В–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–∞–љ–Њ—Б–Є—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –≤—А–µ–і –Ј–і–Њ—А–Њ–≤—М—О —З–µ–ї–Њ–≤–µ–Ї–∞, –Њ–і–љ–∞–Ї–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–∞–µ—В—Б—П –љ–µ—Г–Ї–ї–Њ–љ–љ–∞—П —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є —Н—В–Є—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–є, —З—В–Њ, –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г—Е—Г–і—И–∞–µ—В —В–µ—З–µ–љ–Є–µ –Є –њ—А–Њ–≥–љ–Њ–Ј –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Я–Њ –љ–∞—И–Є–Љ –і–∞–љ–љ—Л–Љ, —Б–Њ—З–µ—В–∞–љ–Є–µ —Е–ї–∞–Љ–Є–і–Є–є —Б –≥–Њ–љ–Њ–Ї–Њ–Ї–Ї–Њ–Љ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г 33,7% –њ–∞—Ж–Є–µ–љ—В–Њ–Ї, —Б —Г—А–µ–∞–њ–ї–∞–Ј–Љ–Њ–є – 19,1%, —Б —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і–Њ–є – 31,3%, —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ––Ї–∞–љ–і–Є–і–Њ–Ј–љ–∞—П –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—П – —Г 9%. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —В—А–Є —А–∞–Ј–ї–Є—З–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –≤—Б—В—А–µ—З–∞—О—В—Б—П —Г 10,6%, 4–5 –Є–љ—Д–µ–Ї—Ж–Є–є – —Г 5,6%. –Э–µ–ї—М–Ј—П –љ–µ –Њ—В–Љ–µ—В–Є—В—М —В–Њ—В —Д–∞–Ї—В, —З—В–Њ —Г–Ї–∞–Ј–∞–љ–љ—Л–µ –≤—Л—И–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ–±–ї–µ–≥—З–∞—О—В –њ–µ—А–µ–і–∞—З—Г –Т–Ш–І––Є–љ—Д–µ–Ї—Ж–Є–Є –Є —Б—В–∞–љ–Њ–≤—П—В—Б—П –Ї–Њ—Д–∞–Ї—В–Њ—А–Њ–Љ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Т–Ш–І/–°–Я–Ш–Ф–∞.
–Т–µ—А–Њ—П—В–љ–µ–µ –≤—Б–µ–≥–Њ, –њ—А–Є—З–Є–љ–Њ–є —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–є —П–≤–ї—П–µ—В—Б—П –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Э–µ–њ—А–∞–≤–Є–ї—М–љ–Њ –њ–Њ–і–Њ–±—А–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В, –і–Њ–Ј–∞, —А–µ–ґ–Є–Љ –њ—А–Є–µ–Љ–∞, –љ–µ–±—А–µ–ґ–љ–Њ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –ї–µ—З–µ–љ–Є—П – –≤—Б–µ —Н—В–Њ –њ—А–Є–≤–Њ–і–Є—В –ї–Є—И—М –Ї —Б—В–Є—Е–∞–љ–Є—О –Њ—Б—В—А—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є –Ї —А–∞–Ј–≤–Є—В–Є—О —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞. –Т –і–∞–ї—М–љ–µ–є—И–µ–Љ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–µ –Ј–∞—А–∞–ґ–µ–љ–Є—П –і—А—Г–≥–Є–Љ–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є —Д–Њ—А–Љ–Є—А—Г—О—В –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—О, –Ї–Њ—В–Њ—А–∞—П, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, —Ж–µ–ї–Є–Ї–Њ–Љ –Љ–Њ–ґ–µ—В –њ–µ—А–µ–і–∞–≤–∞—В—М—Б—П –њ–∞—А—В–љ–µ—А—Г.
–Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ —А–∞–љ–љ–µ–µ –∞–і–µ–Ї–≤–∞—В–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б–њ–Њ—Б–Њ–±–љ–Њ –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М —А–∞–Ј–≤–Є—В–Є–µ –Љ–љ–Њ–ґ–µ—Б—В–≤–∞ —В—П–ґ–µ–ї—Л—Е –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–є –і–ї—П –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —З–µ–ї–Њ–≤–µ–Ї–∞, –∞ –Њ—Б–Њ–±–µ–љ–љ–Њ –і–ї—П –µ–≥–Њ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є. –Х—Й–µ –±–Њ–ї–µ–µ –≤–∞–ґ–љ–Њ–є –Ј–∞–і–∞—З–µ–є —П–≤–ї—П–µ—В—Б—П –≥—А–∞–Љ–Њ—В–љ–∞—П –њ—А–Њ—Б–≤–µ—В–Є—В–µ–ї—М—Б–Ї–∞—П —А–∞–±–Њ—В–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ —Б –Љ–Њ–ї–Њ–і—Л–Љ–Є –ї—О–і—М–Љ–Є, –Ї–∞–Ї –љ–∞–Є–±–Њ–ї–µ–µ —Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ –∞–Ї—В–Є–≤–љ–Њ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –≥—А—Г–њ–њ–Њ–є. –Ю—З–µ–љ—М –≤–∞–ґ–љ–Њ –і–µ–ї–∞—В—М –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є –∞–Ї—Ж–µ–љ—В –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –±–∞—А—М–µ—А–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є. –®–Є—А–Њ–Ї–∞—П –њ–Њ–њ—Г–ї—П—А–Є–Ј–∞—Ж–Є—П –Љ–µ—В–Њ–і–Њ–≤ –Њ—А–∞–ї—М–љ–Њ–є –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є —Б—А–µ–і–Є –Љ–Њ–ї–Њ–і–µ–ґ–Є –њ—А–Є–≤–µ–ї–∞ –Ї —В–Њ–Љ—Г, —З—В–Њ –Љ–љ–Њ–≥–Є–µ –Њ—В–Ї–∞–Ј—Л–≤–∞—О—В—Б—П –Њ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–Ј–µ—А–≤–∞—В–Є–≤–Њ–≤. –†–µ—И–∞—П —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –њ—А–Њ–±–ї–µ–Љ—Г –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ–є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, –Њ–љ–Є —Б–Њ–≤–µ—А—И–µ–љ–љ–Њ –љ–µ –Ј–∞–±–Њ—В—П—В—Б—П –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Ј–∞—А–∞–ґ–µ–љ–Є—П. –Я—А–Є —Н—В–Њ–Љ –љ–∞–Є–±–Њ–ї—М—И–∞—П —З–∞—Б—В–Њ—В–∞ —Б–Љ–µ–љ—Л –њ–∞—А—В–љ–µ—А–Њ–≤ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Є–Љ–µ–љ–љ–Њ —Б—А–µ–і–Є –Љ–Њ–ї–Њ–і–µ–ґ–Є, —З—В–Њ –≤–Њ –Љ–љ–Њ–≥–Њ —А–∞–Ј –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П. –Ч–∞–±–Њ–ї–µ–≤–∞—П —А–∞–љ–Њ, –≤ 16–18 –ї–µ—В, –Ї 22–25 –≥–Њ–і–∞–Љ –Љ–љ–Њ–≥–Є–µ —Г–ґ–µ –љ–µ –Љ–Њ–≥—Г—В –њ–Њ–ї–љ–Њ—Ж–µ–љ–љ–Њ —А–µ–∞–ї–Є–Ј–Њ–≤–∞—В—М —Б–≤–Њ—О —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О, –њ—А–Є—З–Є–љ–Њ–є —З–µ–≥–Њ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –і–ї–Є—В–µ–ї—М–љ–Њ —В–µ–Ї—Г—Й–Є–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б, –њ–Њ–і—З–∞—Б –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–є. –Т –њ–Њ–і–Њ–±–љ—Л—Е —Б–ї—Г—З–∞—П—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –Є–Ј–±–µ–≥–∞—П –љ–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Љ–љ–Њ–ґ–µ—Б—В–≤–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Г—З–Є—В—Л–≤–∞—П —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –њ–Њ–і–Њ–±–љ—Л–µ –њ–∞—Ж–Є–µ–љ—В–Ї–Є –њ—А–µ–ґ–і–µ –њ–Њ–ї—Г—З–∞–ї–Є –ї–µ—З–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є.
–Ґ–∞–Ї –Ї–∞–Ї –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–Є, –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤, –њ–µ—А–µ–і–∞—О—В—Б—П –њ–Њ–ї–Њ–≤—Л–Љ –њ—Г—В–µ–Љ, –њ–µ—А–≤—Л–Љ–Є –њ–Њ—А–∞–ґ–∞—О—В—Б—П –љ–Є–ґ–љ–Є–µ –Њ—В–і–µ–ї—Л –≥–µ–љ–Є—В–∞–ї–Є–є. –Т –љ–Њ—А–Љ–µ –≤–Њ –≤–ї–∞–≥–∞–ї–Є—Й–µ —Б—Г—Й–µ—Б—В–≤—Г—О—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –љ–∞–і–µ–ґ–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Ј–∞—Й–Є—В—Л –Њ—В –Є–љ–≤–∞–Ј–Є–Є –њ–∞—В–Њ–≥–µ–љ–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –≠—В–Њ –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Љ–Є–Ї—А–Њ–±–Є–Њ—Ж–µ–љ–Њ–Ј –≤–ї–∞–≥–∞–ї–Є—Й–∞, –Ї–Њ—В–Њ—А—Л–є –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —А—П–і–∞ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї —Б–Њ–Ј–і–∞–љ–Є–µ –Ї–Є—Б–ї–Њ–є —Б—А–µ–і—Л, –Ї–Њ–љ–Ї—Г—А–µ–љ—Ж–Є–Є –љ–∞ —Г—А–Њ–≤–љ–µ –њ–Є—Й–µ–≤—Л—Е —Б—Г–±—Б—В–∞–љ—Ж–Є–є –Є –і—А., –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є—П –њ–∞—В–Њ–≥–µ–љ–Њ–≤. –§–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –і–µ—Б–Ї–≤–∞–Љ–∞—Ж–Є—П —Н–њ–Є—В–µ–ї–Є—П –≤–ї–∞–≥–∞–ї–Є—Й–∞, —Б–Є–љ—В–µ–Ј –Є–Љ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е –≤–µ—Й–µ—Б—В–≤, –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –ї–Њ–Ї–∞–ї—М–љ–Њ–є –Є–Љ–Љ—Г–љ–љ–Њ–є –Ј–∞—Й–Є—В—Л, –Ї–∞–Ї –Ї–ї–µ—В–Њ—З–љ–Њ–є, —В–∞–Ї –Є –≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–є, —В–∞–Ї–ґ–µ –≤–љ–Њ—Б–Є—В —Б–≤–Њ–є –≤–Ї–ї–∞–і –≤ –Ј–∞—Й–Є—В—Г –Њ—В –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –∞–≥–µ–љ—В–Њ–≤. –Я—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–µ –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –≤ –≤–µ—А—Е–љ–Є–µ –Њ—В–і–µ–ї—Л –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–∞—П —Б–ї–Є–Ј—М, –Ї–Њ—В–Њ—А–∞—П –±–Њ–≥–∞—В–∞ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л–Љ–Є —Б—Г–±—Б—В–∞–љ—Ж–Є—П–Љ–Є –Є –∞–љ—В–Є—В–µ–ї–∞–Љ–Є, –∞ —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±–љ–∞ —Б–Њ–Ј–і–∞–≤–∞—В—М –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–µ–њ—П—В—Б—В–≤–Є–µ. –Т–∞–ґ–љ—Г—О –Ј–∞—Й–Є—В–љ—Г—О —А–Њ–ї—М –Є–≥—А–∞–µ—В –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є—П, –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–Њ—В–Њ—А–Њ–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Њ—В—В–Њ—А–ґ–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П —Н–љ–і–Њ–Љ–µ—В—А–Є—П, —З—В–Њ –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –і–ї–Є—В–µ–ї—М–љ–Њ–Љ—Г –њ—А–µ–±—Л–≤–∞–љ–Є—О –њ–∞—В–Њ–≥–µ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є, —В–µ–Љ —Б–∞–Љ—Л–Љ –њ—А–µ–њ—П—В—Б—В–≤—Г—П —Б–Њ–Ј–і–∞–љ–Є—О —Г—Б–ї–Њ–≤–Є–є –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–є –њ–µ—А—Б–Є—Б—В–µ–љ—Ж–Є–Є, –њ—А–Є —Н—В–Њ–Љ –ї–µ–є–Ї–Њ—Ж–Є—В–∞—А–љ–∞—П –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є—П –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Б–Є–ї–Є–≤–∞–µ—В —Н—В–Њ—В –Љ–µ—Е–∞–љ–Є–Ј–Љ.
–†–∞–Ј–ї–Є—З–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л, –Ї–∞–Ї —Н–Ї–Ј–Њ–≥–µ–љ–љ—Л–µ, —В–∞–Ї –Є —Н–љ–і–Њ–≥–µ–љ–љ—Л–µ, —Б–њ–Њ—Б–Њ–±–љ—Л –љ–∞—А—Г—И–∞—В—М –Ј–∞—Й–Є—В–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, –њ–Њ–≤—Л—И–∞—П —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ъ —Н–љ–і–Њ–≥–µ–љ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–∞–Љ –Љ–Њ–ґ–љ–Њ –Њ—В–љ–µ—Б—В–Є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л–µ –≤–ї–Є—П–љ–Є—П, –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В—Л —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї –њ—А–Є–Љ–µ—А—Г, —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В; –Ї —Н–Ї–Ј–Њ–≥–µ–љ–љ—Л–Љ – —З–∞—Б—В—Л–µ, –љ–µ–Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–µ —Б–њ—А–Є–љ—Ж–µ–≤–∞–љ–Є—П, –≤–≤–µ–і–µ–љ–Є–µ –≤–Њ –≤–ї–∞–≥–∞–ї–Є—Й–µ –Є–љ–Њ—А–Њ–і–љ—Л—Е –њ—А–µ–і–Љ–µ—В–Њ–≤, –љ–µ–Ї–Њ—В–Њ—А—Л–µ –≤–Є–і—Л –Љ–µ—Б—В–љ–Њ–є –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є, –љ–µ—Б–Њ–±–ї—О–і–µ–љ–Є–µ –ї–Є—З–љ–Њ–є –≥–Є–≥–Є–µ–љ—Л.
–Я–Њ —В–Њ–њ–Њ–≥—А–∞—Д–Є–Є –Љ–Њ–ґ–љ–Њ –≤—Л–і–µ–ї–Є—В—М –њ–Њ—А–∞–ґ–µ–љ–Є–µ –љ–Є–ґ–љ–µ–≥–Њ –Њ—В–і–µ–ї–∞ —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Є –≤–Њ—Б—Е–Њ–і—П—Й—Г—О –Є–љ—Д–µ–Ї—Ж–Є—О. –Ъ –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ –љ–Є–ґ–љ–µ–≥–Њ –Њ—В–і–µ–ї–∞ —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Њ—В–љ–Њ—Б—П—В —Г—А–µ—В—А–Є—В, –њ–∞—А–∞—Г—А–µ—В—А–Є—В, –±–∞—А—В–Њ–ї–Є–љ–Є—В, –Ї–Њ–ї—М–њ–Є—В –Є —Н–љ–і–Њ—Ж–µ—А–≤–Є—Ж–Є—В. –Я—А–Є –≥–µ–љ–Є—В–∞–ї—М–љ–Њ––Њ—А–∞–ї—М–љ—Л—Е –Ї–Њ–љ—В–∞–Ї—В–∞—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е —Д–∞—А–Є–љ–≥–Є—В–Њ–≤ –Є —В–Њ–љ–Ј–Є–ї–ї–Є—В–Њ–≤, –∞ –њ—А–Є –≥–µ–љ–Є—В–∞–ї—М–љ–Њ––∞–љ–∞–ї—М–љ—Л—Е – –њ—А–Њ–Ї—В–Є—В–Њ–≤.
–†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—О –Є–љ—Д–µ–Ї—Ж–Є–Є –Є–Ј –Њ—З–∞–≥–Њ–≤, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –≤ –љ–Є–ґ–љ–Є—Е –Њ—В–і–µ–ї–∞—Е —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–µ –њ—А–µ—А—Л–≤–∞–љ–Є–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –Є –Ї–Њ–љ—В—А–∞—Ж–µ–њ—В–Є–≤—Л, –Њ–њ–µ—А–∞—Ж–Є–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –љ–µ —В–Њ–ї—М–Ї–Њ –љ–∞ –≥–µ–љ–Є—В–∞–ї–Є—П—Е. –Ъ –њ—А–Є–Љ–µ—А—Г, –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ–Њ–є –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є (–Т–Ь–Ъ), —А–Є—Б–Ї –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ—А–≥–∞–љ–Њ–≤ –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞ –≤ 4–7 —А–∞–Ј –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї.
–Т–Њ—Б—Е–Њ–і—П—Й–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П —З–∞—Й–µ –≤—Б–µ–≥–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П–µ—В—Б—П:
- –Ї–∞–љ–∞–ї–Є–Ї—Г–ї—П—А–љ–Њ, —В–Њ –µ—Б—В—М —З–µ—А–µ–Ј —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ—Л–є –Ї–∞–љ–∞–ї, –њ–Њ–ї–Њ—Б—В—М –Љ–∞—В–Ї–Є, –Љ–∞—В–Њ—З–љ—Л–µ —В—А—Г–±—Л –љ–∞ –±—А—О—И–Є–љ—Г –Є –Њ—А–≥–∞–љ—Л –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є;
- –ї–Є–Љ—Д–Њ–≥–µ–љ–љ–Њ, —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –њ–µ–ї—М–≤–Є–Њ–њ–µ—А–Є—В–Њ–љ–Є—В–Њ–≤ –Є –і–∞–ї—М–љ–µ–є—И–Є–Љ –ї–Є–Љ—Д–Њ–≥–µ–љ–љ—Л–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ–Љ (–Њ—Б–Њ–±–µ–љ–љ–Њ —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є) –љ–∞ –±—А—О—И–Є–љ—Г –њ–Њ–і–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є (–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–є —Б–Є–љ–і—А–Њ–Љ –Ъ—Г—А—В–Є—Б–∞––§–Є—В—Ж–∞––•—М—О, –∞–њ–њ–µ–љ–і–Є—Ж–Є—В, —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В, –њ–µ—А–Є–≥–µ–њ–∞—В–Є—В, –њ–ї–µ–≤—А–Є—В);
- –≥–µ–Љ–∞—В–Њ–≥–µ–љ–љ–Њ, –Њ —З–µ–Љ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –љ–∞–ї–Є—З–Є–µ —Н–Ї—Б—В—А–∞–≥–µ–љ–Є—В–∞–ї—М–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (—Б—Г—Б—В–∞–≤–љ—Л–µ —Б—Г–Љ–Ї–Є).
–Т –≤–Њ—Б—Е–Њ–ґ–і–µ–љ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ–≥—Г—В —В–∞–Ї–ґ–µ –Є–≥—А–∞—В—М —А–Њ–ї—М —Б–њ–µ—А–Љ–∞—В–Њ–Ј–Њ–Є–і—Л –Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Т–Ь–°.
–Ь–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л, –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ—Л–µ –Є–Ј –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –≥–µ–љ–Є—В–∞–ї–Є–є –Є –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є, –Љ–Њ–≥—Г—В –±—Л—В—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л, –Ї–∞–Ї:
1. –≠–Ї–Ј–Њ–≥–µ–љ–љ—Л–µ –Њ—А–≥–∞–љ–Є–Ј–Љ—Л (–Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л, –њ–µ—А–µ–і–∞—О—Й–Є–µ—Б—П –њ–Њ–ї–Њ–≤—Л–Љ –њ—Г—В–µ–Љ, –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—А–≥–∞–љ–Њ–≤ –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞ –≤ 2/3 —Б–ї—Г—З–∞–µ–≤):
– C. trachomatis
– N. gonorrhoeae
– Genitalium mycoplasma
– Ureaplasma urealyticum
– Trichomonas vaginalis
2. –≠–љ–і–Њ–≥–µ–љ–љ—Л–µ –Њ—А–≥–∞–љ–Є–Ј–Љ—Л:
–Р) –С–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є –≤–∞–≥–Є–љ–Њ–Ј:
– Gardnerella vaginalis
– Bacteroides
– Peptostreptococcus
– Mobiluncus
– Streptococcus
– Mycoplasma hominis
– Fusobacterium
–С) –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –±–∞–Ї—В–µ—А–Є–Є:
– E.coli
– Haemophilus spp.
– Pneumococcus
– Campylobacter foetus
– Staphylococcus
–Т–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Њ—А–≥–∞–љ–Њ–≤ –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞ (–Т–Ч–Ю–Ь–Ґ) –≤—Л—П–≤–ї—П–µ—В—Б—П –њ–Њ–ї–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —Д–ї–Њ—А–∞, –њ—А–Є—З–µ–Љ –≤–µ–і—Г—Й—Г—О —А–Њ–ї—М –Є–≥—А–∞—О—В –≥–Њ–љ–Њ–Ї–Њ–Ї–Ї–Є –Є —Е–ї–∞–Љ–Є–і–Є–Є, –≤—Л–і–µ–ї—П–µ–Љ—Л–µ –Є–Ј –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –њ–Њ–ї–Њ–≤–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–≤ 28% –Є 23% —Б–ї—Г—З–∞–µ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Я—А–Є –љ–∞–ї–Є—З–Є–Є –Т–Ч–Ю–Ь–Ґ –≥–Њ–љ–Њ–Ї–Њ–Ї–Ї–Є –Є–Ј —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –≤—Л–і–µ–ї—П—О—В—Б—П –≤ 25–50% —Б–ї—Г—З–∞–µ–≤, –∞ —Е–ї–∞–Љ–Є–і–Є–Є –≤ 22–47%. –Ю–і–љ–∞–Ї–Њ —Г 1/3 –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –Т–Ч–Ю–Ь–Ґ –Є–Ј —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –љ–µ —Г–і–∞–µ—В—Б—П –≤—Л–і–µ–ї–Є—В—М –љ–Є–Ї–∞–Ї–Є—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤. –Т 65% —Б–ї—Г—З–∞–µ–≤ –Є–Ј –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –њ–Њ–ї–Њ–≤–Њ–≥–Њ —В—А–∞–Ї—В–∞ –≤—Л—Б–µ–≤–∞–µ—В—Б—П —А–∞–Ј–ї–Є—З–љ–∞—П –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–∞—П –Є –∞–љ–∞—Н—А–Њ–±–љ–∞—П —Д–ї–Њ—А–∞. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, —З—В–Њ –≤ –љ–∞—З–∞–ї–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –ї–Є—И—М –Њ–і–Є–љ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–є –∞–≥–µ–љ—В –Є–љ–Є—Ж–Є–Є—А—Г–µ—В –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б, –Є–Ј–Љ–µ–љ—П–µ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ –ї–Њ–Ї–∞–ї—М–љ—Л—Е –Є–Љ–Љ—Г–љ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, –њ–Њ–і–≥–Њ—В–∞–≤–ї–Є–≤–∞—П —В–µ–Љ —Б–∞–Љ—Л–Љ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Г—О –њ–Њ—З–≤—Г –і–ї—П –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П –і—А—Г–≥–Є–Љ–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞–Љ–Є. –°—Г–і—П –њ–Њ –≤—Б–µ–Љ—Г, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ —В–∞–Ї–Є–Љ–Є «–Є–љ–Є—Ж–Є–∞—В–Њ—А–∞–Љ–Є» –≤—Л—Б—В—Г–њ–∞—О—В –≥–Њ–љ–Њ–Ї–Њ–Ї–Ї–Є, —Е–ї–∞–Љ–Є–і–Є–Є –Є —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і—Л.
–Я–Њ—А–∞–ґ–µ–љ–Є–µ –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –њ–Њ–ї–Њ–≤–Њ–≥–Њ —В—А–∞–Ї—В–∞ –њ—А–Є –Т–Ч–Ю–Ь–Ґ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –≤–љ–∞—З–∞–ї–µ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Ї–ї–µ—В–Њ–Ї —Н–љ–і–Њ—Б–∞–ї—М–њ–Є–љ–≥—Б–∞, –Ї–Њ—В–Њ—А—Л–µ –≤—Л—Б—В–Є–ї–∞—О—В –Љ–∞—В–Њ—З–љ—Л–µ —В—А—Г–±—Л. –Ш–љ—Д–µ–Ї—Ж–Є—П –Љ–Њ–ґ–µ—В –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—В—М—Б—П —В—А—Г–±–∞–Љ–Є (—Б–∞–ї—М–њ–Є–љ–≥–Є—В) –Є–ї–Є –Ј–∞—В—А–∞–≥–Є–≤–∞—В—М —В–∞–Ї–ґ–µ –Є —П–Є—З–љ–Є–Ї–Є (—Б–∞–ї—М–њ–Є–љ–≥–Њ–Њ–Њ—Д–Њ—А–Є—В). –°–ї–µ–і—Б—В–≤–Є–µ–Љ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П —А–∞–Ј—А—Г—И–µ–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –Є —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –љ–∞ –Љ–∞–Ї—А–Њ– –Є –Љ–Є–Ї—А–Њ—Г—А–Њ–≤–љ–µ. –Ф–∞–ґ–µ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ. –Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –Ј–∞—В—А–∞–≥–Є–≤–∞—О—Й–µ–µ –Є–љ—В—А–∞–њ–µ—А–Є—В–Њ–љ–µ–∞–ї—М–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л, –≤–µ–і–µ—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О —В—Г–±–Њ–Њ–≤–∞—А–Є–∞–ї—М–љ–Њ–≥–Њ –∞–±—Б—Ж–µ—Б—Б–∞, —З—В–Њ –≤—Л–Ј—Л–≤–∞–µ—В –њ–Њ–ї–љ–Њ–µ —А–∞–Ј—А—Г—И–µ–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –Є —Д—Г–љ–Ї—Ж–Є–Є —В–∞–Ј–Њ–≤—Л—Е —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤.
–Т–Ч–Ю–Ь–Ґ – –±–Њ–ї–µ–Ј–љ—М —Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ –∞–Ї—В–Є–≤–љ—Л—Е –ґ–µ–љ—Й–Є–љ. –Т–Ч–Ю–Ь–Ґ —А–µ–і–Ї–Њ –≤—Б—В—А–µ—З–∞—О—В—Б—П –≤–Њ –≤—А–µ–Љ—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, –≤ –њ—А–µ–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–Љ –Є –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–Љ –њ–µ—А–Є–Њ–і–∞—Е. –Х—Б–ї–Є –ґ–µ –Т–Ч–Ю–Ь–Ґ –≤–Њ–Ј–љ–Є–Ї–∞—О—В —Г –ґ–µ–љ—Й–Є–љ —Н—В–Є—Е –≥—А—Г–њ–њ, —В–Њ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ —П–≤–ї—П—О—В—Б—П –≤—В–Њ—А–Є—З–љ—Л–Љ–Є –Є–ї–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П—О—Й–Є–Љ–Є—Б—П –Є–Ј –і—А—Г–≥–Є—Е –Њ—З–∞–≥–Њ–≤ –Є–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –Ї –њ—А–Є–Љ–µ—А—Г, –≤—Б–ї–µ–і—Б—В–≤–Є–µ —А–∞–Ј—А—Л–≤–∞ –∞–њ–њ–µ–љ–і–Є–Ї—Г–ї—П—А–љ–Њ–≥–Њ –∞–±—Б—Ж–µ—Б—Б–∞.
–†–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Т–Ч–Ю–Ь–Ґ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —З–∞—Б—В–Њ—В—Л —Б–Љ–µ–љ—Л –њ–∞—А—В–љ–µ—А–∞, –≤–Њ–Ј—А–∞—Б—В–∞, —Б–њ–Њ—Б–Њ–±–∞ –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є, –Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, –љ–µ–і–∞–≤–љ–Є–µ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Л—П–≤–Є–ї–Є –њ—А—П–Љ—Г—О –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –Љ–µ–ґ–і—Г –Ї—Г—А–µ–љ–Є–µ–Љ –Є —З–∞—Б—В–Њ—В–Њ–є —А–∞–Ј–≤–Є—В–Є—П –Т–Ч–Ю–Ь–Ґ.
–Я–Њ–≤—Л—И–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л —А–∞–Ј–≤–Є—В–Є—П –Т–Ч–Ю–Ь–Ґ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В: —А–∞–љ–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –њ–µ—А–≤–Њ–≥–Њ –њ–Њ–ї–Њ–≤–Њ–≥–Њ –Ї–Њ–љ—В–∞–Ї—В–∞, –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ –њ–∞—А—В–љ–µ—А–Њ–≤, –љ–µ–і–∞–≤–љ—П—П —Б–Љ–µ–љ–∞ –њ–∞—А—В–љ–µ—А–∞, —З–∞—Б—В–Њ—В–∞ –њ–Њ–ї–Њ–≤—Л—Е –Ї–Њ–љ—В–∞–Ї—В–Њ–≤ –і–∞–ґ–µ –≤ –Љ–Њ–љ–Њ–≥–∞–Љ–љ–Њ–є —Б–≤—П–Ј–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–∞–ї–Є—З–Є–µ —Г –ґ–µ–љ—Й–Є–љ—Л –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –≤–∞–≥–Є–љ–Њ–Ј–∞ –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–љ–Є—П –Т–Ч–Ю–Ь–Ґ.
–Ъ–∞–Ї –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –≤—Л—И–µ, –≤–∞–ґ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Т–Ч–Ю–Ь–Ґ —П–≤–ї—П–µ—В—Б—П –≤–Њ–Ј—А–∞—Б—В. –Я–Є–Ї –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –њ—А–Є—Е–Њ–і–Є—В—Б—П –љ–∞ –њ–µ—А–Є–Њ–і —Б 15 –і–Њ 24–—Е –ї–µ—В. –Я–Њ—Б–ї–µ 20 (–Є –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–Њ—Б–ї–µ 30 –ї–µ—В) —З–∞—Б—В–Њ—В–∞ —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –Т–Ч–Ю–Ь–Ґ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П. –Э–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –њ—А–Є—З–Є–љ–Њ–є –њ–Њ–і–Њ–±–љ–Њ–є —Б–≤—П–Ј–Є –≤–Њ–Ј—А–∞—Б—В–∞ —Б –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М—О –Т–Ч–Ю–Ь–Ґ, –љ–Њ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, —З—В–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О —А–Њ–ї—М –Є–≥—А–∞—О—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Њ–ї–Њ–≤–Њ–≥–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П –Є/–Є–ї–Є –њ–Њ—П–≤–ї–µ–љ–Є–µ –Ј–∞—Й–Є—В–љ—Л—Е –∞–љ—В–Є—В–µ–ї –≤ —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–Љ –Ї–∞–љ–∞–ї–µ.
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Њ—А–∞–ї—М–љ—Л—Е –Ї–Њ–љ—В—А–∞—Ж–µ–њ—В–Є–≤–Њ–≤ –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –Љ–µ—А–µ —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –њ–Њ–ї–Њ–≤–Њ–≥–Њ —В—А–∞–Ї—В–∞. –Т —Б–ї—Г—З–∞—П—Е –ґ–µ —А–∞–Ј–≤–Є—В–Є—П –Т–Ч–Ю–Ь–Ґ —Г –ґ–µ–љ—Й–Є–љ, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Њ—А–∞–ї—М–љ—Л–µ –Ї–Њ–љ—В—А–∞—Ж–µ–њ—В–Є–≤—Л, –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –њ—А–Њ—В–µ–Ї–∞–µ—В –Љ–µ–љ–µ–µ –∞–≥—А–µ—Б—Б–Є–≤–љ–Њ. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ —Ж–µ–ї—П—Е –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л—Е —Б—А–µ–і—Б—В–≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Т–Ч–Ю–Ь–Ґ, –Ї–Њ—В–Њ—А—Л–є –њ—А–µ–≤—Л—И–∞–µ—В —В–∞–Ї–Њ–≤–Њ–є –і–∞–ґ–µ —Б—А–µ–і–Є –ґ–µ–љ—Й–Є–љ, –љ–µ –Є—Б–њ–Њ–ї—М–Ј—Г—О—Й–Є—Е –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –≤–Є–і–Њ–≤ –Ї–Њ–љ—В—А–∞—Ж–µ–њ—Ж–Є–Є.
Gardnerella vaginalis —В–∞–Ї–ґ–µ –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ —Г—З–∞—Б—В–≤—Г–µ—В –≤ —А–∞–Ј–≤–Є—В–Є–Є –Т–Ч–Ю–Ь–Ґ. –Ш–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ —П–≤–ї—П–µ—В—Б—П —Б–ї–µ–і—Б—В–≤–Є–µ–Љ —Д–µ—А–Љ–µ–љ—В–∞—В–Є–≤–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–ї–Є–Ј–Є —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –Є–Ј-–Ј–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –љ–∞—А—Г—И–µ–љ–Є—П –≤–ї–∞–≥–∞–ї–Є—Й–љ–Њ–є —Д–ї–Њ—А—Л.
–Я–Њ –і–∞–љ–љ—Л–Љ –Т.–Ш. –Ъ—Г–ї–∞–Ї–Њ–≤–∞ –Є –Х.–Ь. –Т–Є—Е–ї—П–µ–≤–Њ–є (1995), –≤ —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –ґ–µ–љ—Й–Є–љ—Л —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–∞—П —А–Њ–ї—М –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–є –њ—А–Є—А–Њ–і–µ —Б —Г—З–∞—Б—В–Є–µ–Љ 2–6 –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, –љ–µ—А–µ–і–Ї–Њ –њ—А–Є –≤–µ–і—Г—Й–µ–є —А–Њ–ї–Є –љ–µ—Б–њ–Њ—А–Њ–Њ–±—А–∞–Ј—Г—О—Й–Є—Е –Њ–±–ї–Є–≥–∞—В–љ–Њ––∞–љ–∞—Н—А–Њ–±–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є. –Ф–ї–Є—В–µ–ї—М–љ–∞—П –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П –њ–µ—А—Б–Є—Б—В–µ–љ—Ж–Є—П –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤—Л—П–≤–ї—П–µ—В—Б—П –≤ 67,2% –љ–∞–±–ї—О–і–µ–љ–Є–є.
–Ь–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П —П–≤–ї—П–µ—В—Б—П —Б–µ—А—М–µ–Ј–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є, –Є–±–Њ –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –њ–∞—В–Њ–≥–µ–љ–љ–Њ—Б—В—М –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –Т —В–∞–Ї–Є—Е —Б–ї—Г—З–∞—П—Е –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –≤—Л–Ј—Л–≤–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ—Г—О —А–µ–∞–Ї—Ж–Є—О —В–Ї–∞–љ–µ–є (—Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –≤–ї–∞–≥–∞–ї–Є—Й–∞, —Н–Ї—В–Њ—Ж–µ—А–≤–Є–Ї—Б–∞, –≤—Л–≤–Њ–і–љ—Л—Е –њ—А–Њ—В–Њ–Ї–Њ–≤ –±–Њ–ї—М—И–Є—Е –≤–µ—Б—В–Є–±—Г–ї—П—А–љ—Л—Е –ґ–µ–ї–µ–Ј, –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞—В–µ–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –њ—А—П–Љ–Њ–є –Ї–Є—И–Ї–Є, –Љ–∞—В–Ї–Є, –Љ–∞—В–Њ—З–љ—Л—Е —В—А—Г–±, —П–Є—З–љ–Є–Ї–Њ–≤), —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й—Г—О—Б—П –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ —Н–њ–Є—В–µ–ї–Є—П, –і–µ—Б—В—А—Г–Ї—Ж–Є–µ–є –Є –і–Є—Б–њ–ї–∞–Ј–Є–µ–є. –Я—А–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б–µ –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Б–љ–Є–ґ–µ–љ–Є—П –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –њ—А–Є –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–Є —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –Ї—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є—П, –њ–Њ–≤—А–µ–ґ–і–∞—О—В—Б—П –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л–µ —Б–ї–Њ–Є, –њ—А–Є–ї–µ–≥–∞—О—Й–Є–µ –Ї –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ, –Њ–±—А–∞–Ј—Г–µ—В—Б—П –≥—А–∞–љ—Г–ї—П—Ж–Є–Њ–љ–љ–∞—П —В–Ї–∞–љ—М. –≠—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О –љ–µ —В–Њ–ї—М–Ї–Њ –Ї–Њ–ї—М–њ–Є—В–∞, —Н–љ–і–Њ—Ж–µ—А–≤–Є—Ж–Є—В–∞, —Ж–Є—Б—В–Є—В–∞ –Є –њ—А–Њ–Ї—В–Є—В–∞, –љ–Њ –Љ–Њ–ґ–µ—В –Є–≥—А–∞—В—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Г—О —А–Њ–ї—М –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є —Н–Ї—В–Њ–њ–Є–є —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є, –њ–Њ —Б–≤–Њ–є —Б—Г—В–Є —П–≤–ї—П—О—Й–Є—Е—Б—П —Д–Њ–љ–Њ–≤—Л–Љ–Є –њ—А–µ–і—А–∞–Ї–Њ–≤—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, —В—Г–±–Њ–Њ–≤–∞—А–Є–∞–ї—М–љ—Л—Е –≥–љ–Њ–є–љ—Л—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є, –Љ–Є–Њ–Љ—Л –Љ–∞—В–Ї–Є, –≥—А–Њ–Ј—П—Й–Є—Е –ґ–µ–љ—Й–Є–љ–∞–Љ —А–∞–і–Є–Ї–∞–ї—М–љ—Л–Љ–Є –Њ–њ–µ—А–∞—Ж–Є—П–Љ–Є —Б –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –њ–Њ—В–µ—А–µ–є –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е —Д—Г–љ–Ї—Ж–Є–є –ґ–µ–љ—Б–Ї–Њ–≥–Њ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞.
–Я–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –∞–≥–µ–љ—В–Њ–≤ –њ—А–Њ–Є—Б—Е–Њ–і—П—В –љ–µ —В–Њ–ї—М–Ї–Њ –і–µ—Б—В—А—Г–Ї—В–Є–≤–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П, –љ–Њ –Є –њ–Њ–і–∞–≤–ї—П–µ—В—Б—П —Д–∞–≥–Њ—Ж–Є—В–∞—А–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О —В–Њ—А–њ–Є–і–љ—Л—Е —Д–Њ—А–Љ –Є —Д–∞–≥–Њ—Ж–Є—В–Њ–Ј—Г –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–ї–Є–Љ–Њ—А—Д–љ–Њ–—П–і–µ—А–љ—Л–Љ–Є –ї–µ–є–Ї–Њ—Ж–Є—В–∞–Љ–Є –њ–Њ —В–Є–њ—Г –љ–µ–Ј–∞–≤–µ—А—И–µ–љ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є. –•—А–Њ–љ–Є–Ј–∞—Ж–Є—П –і–µ—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ–Њ—Б—В–Є –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–∞—А–љ—Л—Е —Д–∞–≥–Њ—Ж–Є—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ–љ–Є–Ї–∞—О—В –≤ –Њ—З–∞–≥ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –≤—Б–ї–µ–і –Ј–∞ –њ–Њ–ї–Є–Љ–Њ—А—Д–љ–Њ–—П–і–µ—А–љ—Л–Љ–Є –ї–µ–є–Ї–Њ—Ж–Є—В–∞–Љ–Є. –Т–∞–ґ–љ–µ–є—И–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –≤ —Н—В–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б–µ —П–≤–ї—П–µ—В—Б—П –≤–Ї–ї—О—З–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, —В–Њ –µ—Б—В—М —Д–Є–Ї—Б–∞—Ж–Є—П –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ G –Є M –Є –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞ –≤ —Б—В–µ–љ–Ї–∞—Е –Љ–µ–ї–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤ –Є –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е, –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є –Ґ–—Е–µ–ї–њ–µ—А–Њ–≤ –Є –њ–Њ–≤—Л—И–µ–љ–Є–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ґ–—Б—Г–њ—А–µ—Б—Б–Њ—А–Њ–≤, —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –≤—В–Њ—А–Є—З–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Њ–і–µ—Д–Є—Ж–Є—В–∞. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, —Г —А—П–і–∞ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –µ—Б—В—М –∞–љ—В–Є–≥–µ–љ—Л, —А–Њ–і—Б—В–≤–µ–љ–љ—Л–µ —В–Ї–∞–љ—П–Љ –≥–µ–љ–Є—В–∞–ї–Є–є, —З—В–Њ –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –Љ–Њ–ґ–µ—В —Б–Њ–Ј–і–∞—В—М —Г—Б–ї–Њ–≤–Є—П –і–ї—П —А–∞–Ј–≤–Є—В–Є—П –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤.
–Т–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤—Л–Ј–≤–∞–љ–љ—Л–Љ –њ–Њ–ї–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —Д–ї–Њ—А–Њ–є, –Њ—В–≤–Њ–і–Є—В—Б—П –±–Њ–ї—М—И–∞—П —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є —В–∞–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –Ї–∞–Ї —Н–Ї—В–Њ–њ–Є—П —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є, –ї–µ–є–Њ–Љ–Є–Њ–Љ–∞ –Љ–∞—В–Ї–Є, —Н–љ–і–Њ–Љ–µ—В—А–Є–Њ–Ј.
–£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Г 1/3 –±–Њ–ї—М–љ—Л—Е –ї–µ–є–Њ–Љ–Є–Њ–Љ–Њ–є –Љ–∞—В–Ї–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—О –њ—А–µ–і—И–µ—Б—В–≤–Њ–≤–∞–ї–Є –Є —Б–Њ–њ—Г—В—Б—В–≤–Њ–≤–∞–ї–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –њ—А–Є–і–∞—В–Ї–∞—Е –Љ–∞—В–Ї–Є, —Г 60% – —А–∞–Ј–ї–Є—З–љ—Л–µ —Б–Њ—З–µ—В–∞–љ–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ—А–≥–∞–љ–Њ–≤ –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞. –Ю—В–Љ–µ—З–µ–љ–Њ —В–∞–Ї–ґ–µ, —З—В–Њ –Ј–∞ 7–10 –ї–µ—В –і–Њ –њ–µ—А–≤–Њ–≥–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –ї–µ–є–Њ–Љ–Є–Њ–Љ—Л –Љ–∞—В–Ї–Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е —А–∞–Ј–Љ–µ—А–Њ–≤, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –і–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є, —Г —Н—В–Є—Е –ґ–µ–љ—Й–Є–љ –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –њ–Њ–ї–Є–≥–∞–Љ–Є—П. –Я–Њ—Б–ї–µ–і–љ—П—П –љ–µ –±–µ–Ј—А–∞–Ј–ї–Є—З–љ–∞ –і–ї—П –ґ–µ–љ—Й–Є–љ, –≤ —Б–≤—П–Ј–Є —Б —В–µ–Љ, —З—В–Њ —Б–њ–µ—А–Љ–∞—В–Њ–Ј–Њ–Є–і—Л –Љ–Њ–≥—Г—В –љ–µ —В–Њ–ї—М–Ї–Њ —В—А–∞–љ—Б–њ–Њ—А—В–Є—А–Њ–≤–∞—В—М –Љ–Є–Ї—Б—В–Є–љ—Д–µ–Ї—Ж–Є—О –Њ—В —А–∞–Ј–љ—Л—Е –њ–∞—А—В–љ–µ—А–Њ–≤, –љ–Њ –Є –≤—Л–Ј—Л–≤–∞—В—М –Љ–µ—Б—В–љ—Л–µ –Є–Љ–Љ—Г–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є —Б –њ—А–Є–≤–ї–µ—З–µ–љ–Є–µ–Љ –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤.
–° –њ–Њ–Љ–Њ—Й—М—О –Я–¶–† –Љ–µ—В–Њ–і–Є–Ї –љ–∞–Љ —Г–і–∞–ї–Њ—Б—М –≤—Л—П–≤–Є—В—М, —З—В–Њ –≤ —В–Њ–ї—Й–µ –Љ–Є–Њ–Љ–∞—В–Њ–Ј–љ—Л—Е —Г–Ј–ї–Њ–≤ –Є –Э–∞–±–Њ—В–Њ–≤—Л—Е –Ї–Є—Б—В–∞—Е —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ –њ–Њ–≤—Л—И–µ–љ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–ї–Њ—А—Л –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Њ–Ї—А—Г–ґ–∞—О—Й–Є–Љ–Є —В–Ї–∞–љ—П–Љ–Є.
–Т —А–∞–Ј–≤–Є—В–Є–Є —Н–љ–і–Њ–Љ–µ—В—А–Є–Њ–Ј–∞ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л —В–∞–Ї–ґ–µ –Є–≥—А–∞—О—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Г—О —А–Њ–ї—М, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—П –љ–∞—А—Г—И–µ–љ–Є—О –ї–Њ–Ї–∞–ї—М–љ—Л—Е –Є–Љ–Љ—Г–љ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –≤ –њ–µ—А–Є—В–Њ–љ–µ–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –±–Њ–ї–µ–µ —Б–ї–Њ–ґ–љ—Г—О –њ—А–Њ–±–ї–µ–Љ—Г, —З–µ–Љ —Н—В–Њ –Ї–∞–ґ–µ—В—Б—П –љ–∞ –њ–µ—А–≤—Л–є –≤–Ј–≥–ї—П–і. –Т—Л—Б—В—Г–њ–∞—О—Й–∞—П –љ–∞ –њ–µ—А–≤—Л–є –њ–ї–∞–љ –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є—П –≤–љ–Њ—Б–Є—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –Ї–Њ—А—А–µ–Ї—В–Є–≤—Л –≤ –њ–Њ–љ–Є–Љ–∞–љ–Є–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —В—А–µ–±—Г–µ—В –±–Њ–ї–µ–µ –≤–љ–Є–Љ–∞—В–µ–ї—М–љ–Њ–≥–Њ –Њ—В–љ–Њ—И–µ–љ–Є—П –Ї –њ–Њ–і–±–Њ—А—Г —В–µ—А–∞–њ–Є–Є –Є –Љ–µ—В–Њ–і–∞–Љ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є.
–Э–∞ –љ–∞—З–∞–ї—М–љ—Л—Е —Н—В–∞–њ–∞—Е –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–љ—Д–µ–Ї—Ж–Є–є, –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤, –њ—А–Њ—В–µ–Ї–∞—О—В –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ. –Ю—В—Б—Г—В—Б—В–≤–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г–Ї–∞–Ј—Л–≤–∞–µ—В –ї–Є—И—М –љ–∞ –≤—А–µ–Љ–µ–љ–љ–Њ–µ —А–∞–≤–љ–Њ–≤–µ—Б–Є–µ –Љ–µ–ґ–і—Г –њ–∞—А–∞–Ј–Є—В–∞–Љ–Є –Є «—Е–Њ–Ј—П–Є–љ–Њ–Љ» –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—О—Й–Є—Е, –љ–Њ –љ–µ –њ—А–µ–њ—П—В—Б—В–≤—Г—О—Й–Є—Е —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є—О. –Ш–љ—Д–µ–Ї—Ж–Є—П —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–Љ —В–µ—З–µ–љ–Є–µ–Љ —П–≤–ї—П–µ—В—Б—П –љ–µ –Љ–µ–љ–µ–µ –Њ–њ–∞—Б–љ–Њ–є, —З–µ–Љ –µ–µ –Љ–∞–љ–Є—Д–µ—Б—В–љ—Л–µ —Д–Њ—А–Љ—Л.
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–Є –њ–Њ—А–∞–ґ–∞—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Ї–ї–µ—В–Ї–Є —Ж–Є–ї–Є–љ–і—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П, –Є—Б–Ї–ї—О—З–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–ї—П—О—В —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і—Л, –≥–∞—А–і–љ–µ—А–µ–ї–ї—Л –Є –≥—А–Є–±–Ї–Є, —Б–њ–Њ—Б–Њ–±–љ—Л–µ —А–∞–Ј–Љ–љ–Њ–ґ–∞—В—М—Б—П –≤ –Љ–љ–Њ–≥–Њ—Б–ї–Њ–є–љ–Њ–Љ –њ–ї–Њ—Б–Ї–Њ–Љ —Н–њ–Є—В–µ–ї–Є–Є. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –љ–µ—А–µ–і–Ї–Њ –±—Л–≤–∞—О—В —Б—Г–±–Љ–∞–љ–Є—Д–µ—Б—В–љ—Л–Љ–Є –Є–ї–Є –∞—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–Љ–Є. –Я–Њ–ї–Њ–≤–Є–љ–∞ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ –љ–µ –Є–Љ–µ—О—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є, –Ї–Њ—В–Њ—А—Л–µ –Ј–∞–≤–Є—Б—П—В –Њ—В –≤–Є—А—Г–ї–µ–љ—В–љ–Њ—Б—В–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ—А–µ–±—Л–≤–∞–љ–Є—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, —В–Њ–њ–Њ–≥—А–∞—Д–Є–Є –њ–Њ—А–∞–ґ–µ–љ–Є–є, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Љ–µ—Б—В–љ—Л—Е –Є –Њ–±—Й–Є—Е —А–µ–∞–Ї—Ж–Є–є –Љ–∞–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞.
–Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Т–Ч–Ю–Ь–Ґ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –њ–Њ–ї–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–µ–є. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л, –њ—А–Є—Б—Г—В—Б—В–≤—Г—О—Й–Є–µ –≤–Њ –≤–ї–∞–≥–∞–ї–Є—Й–µ (–Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –ї–∞–Ї—В–Њ– –Є –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є), –Љ–Њ–≥—Г—В –њ—А–Є–љ–Є–Љ–∞—В—М —Г—З–∞—Б—В–Є–µ –≤ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б–µ. –Ю–і–љ–∞–Ї–Њ –≤–µ–і—Г—Й–∞—П —А–Њ–ї—М –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –љ–∞–Є–±–Њ–ї–µ–µ –≤–Є—А—Г–ї–µ–љ—В–љ—Л–Љ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞–Љ: –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—П–Љ —Б–µ–Љ–µ–є—Б—В–≤–∞ Enterobacteriaceae (–њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–µ) –Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї—Г. –†–Њ–ї—М –∞–љ–∞—Н—А–Њ–±–Њ–≤, –Ї–∞–Ї –Ї–Њ-–њ–∞—В–Њ–≥–µ–љ–Њ–≤, —В–∞–Ї–ґ–µ —П–≤–ї—П–µ—В—Б—П –Њ–±—Й–µ–њ—А–Є–Ј–љ–∞–љ–љ–Њ–є, –Њ–і–љ–∞–Ї–Њ –µ–µ –љ–µ —Б–ї–µ–і—Г–µ—В –њ–µ—А–µ–Њ—Ж–µ–љ–Є–≤–∞—В—М, —В–∞–Ї –Ї–∞–Ї –≤–µ–і—Г—Й–Є–Љ–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є —Н—В–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л –љ–µ —П–≤–ї—П—О—В—Б—П.
–Ь–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є –Т–Ю–Ч –і–ї—П –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –і–Є–∞–≥–љ–Њ–Ј–∞ –Т–Ч–Ю–Ь–Ґ —П–≤–ї—П—О—В—Б—П:
– –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є –ґ–Є–≤–Њ—В–∞
– –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –≤ –Њ–±–ї–∞—Б—В–Є –њ—А–Є–і–∞—В–Ї–Њ–≤ –Љ–∞—В–Ї–Є
– –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л–µ —В—А–∞–Ї—Ж–Є–Є —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є.
–Ф–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Б—Г—Й–µ—Б—В–≤—Г—О—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –Ї—А–Є—В–µ—А–Є–Є:
– —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —В–µ–ї–∞ –≤—Л—И–µ 38,3°–°
– –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –≤—Л–і–µ–ї–µ–љ–Є—П –Є–Ј —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є –Є –≤–ї–∞–≥–∞–ї–Є—Й–∞
– –њ–Њ–≤—Л—И–µ–љ–Є–µ –°–Ю–≠
– –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –°–—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞
– –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є –≥–Њ–љ–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є, —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і–∞–Љ–Є, —Е–ї–∞–Љ–Є–і–Є—П–Љ–Є.
–Ф–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є –Т–Ч–Ю–Ь–Ґ —П–≤–ї—П—О—В—Б—П:
– –≥–Є—Б—В–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є–µ —Н–љ–і–Њ–Љ–µ—В—А–Є—В–∞ –њ—А–Є –±–Є–Њ–њ—Б–Є–Є —Н–љ–і–Њ–Љ–µ—В—А–Є—П
– —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л–µ –і–∞–љ–љ—Л–µ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —В—А–∞–љ—Б–≤–∞–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П, –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—Й–Є–µ —Г—В–Њ–ї—Й–µ–љ–љ—Л–µ, –љ–∞–њ–Њ–ї–љ–µ–љ–љ—Л–µ –ґ–Є–і–Ї–Њ—Б—В–љ—Л–Љ —Б–Њ–і–µ—А–ґ–Є–Љ—Л–Љ –Љ–∞—В–Њ—З–љ—Л–µ —В—А—Г–±—Л —Б –Є–ї–Є –±–µ–Ј —Б–≤–Њ–±–Њ–і–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є; –љ–∞–ї–Є—З–Є–µ —В—Г–±–Њ–Њ–≤–∞—А–Є–∞–ї—М–љ–Њ–≥–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П
– –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П, –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ—Л–µ –њ—А–Є –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є–Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ –Т–Ч–Ю–Ь–Ґ.
–Э–∞–Є–±–Њ–ї–µ–µ –Њ–њ–∞—Б–љ—Л–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ–Љ –Т–Ч–Ю–Ь–Ґ —П–≤–ї—П–µ—В—Б—П –±–µ—Б–њ–ї–Њ–і–Є–µ. –І–∞—Б—В–Њ—В–∞ –µ–≥–Њ –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –њ—А—П–Љ–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є –Ї—А–∞—В–љ–Њ—Б—В–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–є —В–∞–Ј–Њ–≤—Л—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –ґ–∞–ї–Њ–±–∞–Љ–Є —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е —П–≤–ї—П—О—В—Б—П: –±–µ—Б–њ–ї–Њ–і–Є–µ (–њ–µ—А–≤–Є—З–љ–Њ–µ –Є–ї–Є –≤—В–Њ—А–Є—З–љ–Њ–µ), —Г 12% – –±–Њ–ї–Є –≤–љ–Є–Ј—Г –ґ–Є–≤–Њ—В–∞ —Б –Є—Е —Г—Б–Є–ї–µ–љ–Є–µ–Љ –њ–µ—А–µ–і –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–µ–є, –љ–∞–ї–Є—З–Є–µ –ґ–Є–і–Ї–Є—Е –≤—Л–і–µ–ї–µ–љ–Є–є –±–µ–Ј –Ј–∞–њ–∞—Е–∞ –Њ–±—Л—З–љ–Њ –Ј–∞ 4–5 –і–љ–µ–є –њ–µ—А–µ–і –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–µ–є, 3–4 —А–∞–Ј–∞ –≤ –≥–Њ–і —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –≤ 3–4 –Љ–µ—Б—П—Ж–∞, —Г 70% – –њ—Б–Є—Е–Њ—Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ (–љ–∞—А—Г—И–µ–љ–Є–µ —Б–љ–∞, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М).
–Ф—А—Г–≥–Є–Љ–Є –љ–µ –Љ–µ–љ–µ–µ —В—П–ґ–µ–ї—Л–Љ–Є –Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ–Є –Т–Ч–Ю–Ь–Ґ —П–≤–ї—П—О—В—Б—П –≤–љ–µ–Љ–∞—В–Њ—З–љ–∞—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М –Є —Б–њ–∞–µ—З–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –Ї–Є—И–µ—З–љ–Є–Ї–∞.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б —Ж–µ–ї—М—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П —А—П–і –Љ–µ—В–Њ–і–Є–Ї, –Ї–Њ—В–Њ—А—Л–µ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О, —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М—О, —Г–і–Њ–±—Б—В–≤–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П, –і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О –Є —Ж–µ–љ–Њ–є. –Ю—Б–љ–Њ–≤–љ—Л–Љ –Є –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —П–≤–ї—П–µ—В—Б—П –Я–¶–† (–њ–Њ–ї–Є–Љ–µ—А–∞–Ј–љ–∞—П —Ж–µ–њ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П), –њ–Њ–Ј–≤–Њ–ї—П—О—Й–∞—П –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –≤ –ґ–Є–і–Ї–Њ—Б—В—П—Е –Є —В–Ї–∞–љ—П—Е –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е —Е–ї–∞–Љ–Є–і–Є–Є, —Г—А–µ–∞–њ–ї–∞–Ј–Љ—Л, –Љ–Є–Ї–Њ–њ–ї–∞–Ј–Љ—Л, –≥–∞—А–і–љ–µ—А–µ–ї–ї—Л, —Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б—Л, –≤–Є—А—Г—Б—Л –≥–µ—А–њ–µ—Б–∞ 1 –Є 2, –≥–Њ–љ–Њ–Ї–Њ–Ї–Ї–Є, —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і—Л, –Т–Ш–І, –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–Є —В—Г–±–µ—А–Ї—Г–ї–µ–Ј–∞ –Є —Б–Є—Д–Є–ї–Є—Б–∞. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –Є–Љ–Љ—Г–љ–Њ—Д–ї—О–Њ—А–µ—Б—Ж–µ–љ—В–љ—Л–є –∞–љ–∞–ї–Є–Ј, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–є –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞, –Љ–µ—З–µ–љ–љ—Л–µ —Д–ї—О–Њ—А–µ—Б—Ж–µ–љ—В–Њ–Љ. –І—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–∞–љ–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 98%, –∞ —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М 90%. –° –њ–Њ–Љ–Њ—Й—М—О —Н—В–Њ–є –Љ–µ—В–Њ–і–Є–Ї–Є –Љ–Њ–ґ–љ–Њ —В–∞–Ї–ґ–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞—В—М —Е–ї–∞–Љ–Є–і–Є–Њ–Ј –Є –Љ–Є–Ї–Њ–њ–ї–∞–Ј–Љ–µ–љ–љ—Г—О –Є–љ—Д–µ–Ї—Ж–Є—О.
–Т–ї–∞–≥–∞–ї–Є—Й–љ—Г—О —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і—Г –Љ–Њ–ґ–љ–Њ –Њ–±–љ–∞—А—Г–ґ–Є—В—М –≤ –љ–∞—В–Є–≤–љ–Њ–Љ –њ—А–µ–њ–∞—А–∞—В–µ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ –Є–Ј —Б–≤–Њ–і–∞ –≤–ї–∞–≥–∞–ї–Є—Й–∞, —Г—А–µ—В—А—Л, —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –∞ —В–∞–Ї–ґ–µ –њ—А–Є –Њ–Ї—А–∞—Б–Ї–µ –Є–љ–і–Є–Ї–∞—В–Њ—А–Њ–Љ – –Љ–µ—В–Є–ї–µ–љ–Њ–≤—Л–Љ —Б–Є–љ–Є–Љ. –У–Њ–љ–Њ–Ї–Њ–Ї–Ї –≤—Л—П–≤–ї—П–µ—В—Б—П –≤ –Њ—В–і–µ–ї—П–µ–Љ–Њ–Љ —Г—А–µ—В—А—Л, —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –∞ —В–∞–Ї–ґ–µ –≤—Л–≤–Њ–і–љ—Л—Е –њ—А–Њ—В–Њ–Ї–Њ–≤ –±–Њ–ї—М—И–Є—Е –≤–µ—Б—В–Є–±—Г–ї—П—А–љ—Л—Е –ґ–µ–ї–µ–Ј –њ—А–Є –Њ–Ї—А–∞—Б–µ –њ–Њ –У—А–∞–Љ—Г.
–°—В–∞–љ–і–∞—А—В–Њ–Љ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П –≤—Б–µ—Е –≤–Є–і–Њ–≤ –Є–љ—Д–µ–Ї—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –Ї—Г–ї—М—В—Г—А–∞–ї—М–љ—Л–є –Љ–µ—В–Њ–і, –Њ–і–љ–∞–Ї–Њ –µ–≥–Њ —И–Є—А–Њ–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В—Б—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О, —Б–ї–Њ–ґ–љ–Њ—Б—В—М—О –Є –љ–µ—Г–і–Њ–±—Б—В–≤–Њ–Љ –≤ —Е—А–∞–љ–µ–љ–Є–Є –Є —В—А–∞–љ—Б–њ–Њ—А—В–Є—А–Њ–≤–Ї–µ –Љ–∞—В–µ—А–Є–∞–ї–∞.
–Ч–∞ —А—Г–±–µ–ґ–Њ–Љ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ –∞–Љ–њ–ї–Є—Д–Є–Ї–∞—Ж–Є–Њ–љ–љ—Л–µ –Љ–µ—В–Њ–і—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є. –Я–Њ–Љ–Є–Љ–Њ –Я–¶–†, –≤ –≥—А—Г–њ–њ—Г —Н—В–Є—Е –Љ–µ—В–Њ–і–Є–Ї –≤—Е–Њ–і—П—В: –ї–Є–≥–∞–Ј–љ–∞—П —Ж–µ–њ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –Є —А–Є–±–Њ—Б–Њ–Љ–∞–ї—М–љ–∞—П –†–Э–Ъ –∞–Љ–њ–ї–Є—Д–Є–Ї–∞—Ж–Є—П (TMA – «transcription–mediated amplification»). –Э–∞ –Њ—Б–љ–Њ–≤–µ –∞–Љ–њ–ї–Є—Д–Є–Ї–∞—Ж–Є–Њ–љ–љ—Л—Е –Љ–µ—В–Њ–і–Є–Ї —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л –Љ–Њ—З–µ–≤—Л–µ —В–µ—Б—В—Л, –і–Њ–≤–Њ–ї—М–љ–Њ —Г–і–Њ–±–љ—Л–µ –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, –Њ–і–љ–∞–Ї–Њ –Њ–љ–Є –њ–Њ–Ї–∞ –љ–µ –њ–Њ–ї—Г—З–Є–ї–Є —И–Є—А–Њ–Ї–Њ–≥–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ.
–°–ї–µ–і—Г–µ—В –Њ—Б–Њ–±–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–∞—В–µ—А–Є–∞–ї–∞ –Є–Ј —Г—А–µ—В—А—Л, —Б–≤–Њ–і–Њ–≤ –≤–ї–∞–≥–∞–ї–Є—Й–∞ –Є —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –љ–µ–ї—М–Ј—П —Б—З–Є—В–∞—В—М –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є –і–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П –њ–Њ—А–∞–ґ–µ–љ–Є—П —Н–љ–і–Њ–Љ–µ—В—А–Є—П, –Љ–Є–Њ–Љ–µ—В—А–Є—П –Є –Љ–∞—В–Њ—З–љ—Л—Е —В—А—Г–±. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ —Б–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–Є–Є –Є –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є–Є, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–µ–љ –Ј–∞–±–Њ—А –Љ–∞—В–µ—А–Є–∞–ї–∞ –Є–Ј –Љ–∞—В–Ї–Є, –Љ–∞—В–Њ—З–љ—Л—Е —В—А—Г–± –Є –њ–µ—А–Є—В–Њ–љ–µ–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤–Њ –≤—А–µ–Љ—П —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П —Б–Њ—Б—В–Њ—П–љ–Є–µ –Љ–∞—В–Ї–Є, —Н–љ–і–Њ–Љ–µ—В—А–Є—П –Є –Љ–∞—В–Њ—З–љ—Л—Е —В—А—Г–±. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б —Е–ї–∞–Љ–Є–і–Є–Њ–Ј–Њ–Љ –≤ 71% —Б–ї—Г—З–∞–µ–≤ –Љ–∞—В–Њ—З–љ—Л–µ —В—А—Г–±—Л –љ–µ–њ—А–Њ—Е–Њ–і–Є–Љ—Л –≤ –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ–Њ–Љ –Њ—В–і–µ–ї–µ, —В–Њ–≥–і–∞ –Ї–∞–Ї —Г –±–Њ–ї—М–љ—Л—Е —Б –±–∞–љ–∞–ї—М–љ—Л–Љ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ –≤ 53% –љ–∞–±–ї—О–і–µ–љ–Є–є —В—А—Г–±—Л –љ–µ–њ—А–Њ—Е–Њ–і–Є–Љ—Л –≤ –∞–Љ–њ—Г–ї—П—А–љ—Л—Е –Њ—В–і–µ–ї–∞—Е.
–Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ —А—Г—В–Є–љ–љ–Њ–µ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–∞—В–µ—А–Є–∞–ї–∞, –њ–Њ–ї—Г—З–∞–µ–Љ–Њ–≥–Њ –і–∞–ґ–µ –њ—А–Є –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є–Є, –Њ—В–ї–Є—З–∞–µ—В—Б—П –љ–Є–Ј–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О. –Я—А–Є –Є–Ј—Г—З–µ–љ–Є–Є –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є –њ–Њ–ї—Г—З–µ–љ–љ–Њ–≥–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –≤–Є–Ј—Г–∞–ї—М–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ 63% —Б–ї—Г—З–∞–µ–≤ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А–∞ –љ–µ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П. –Ю–љ–∞ –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –≤ —В–Њ–ї—Й–µ –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ —В–Ї–∞–љ–µ–є, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є —Г–і–∞–ї—П–µ–Љ—Л—Е –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ –ї–∞–њ–∞—А–Њ—В–Њ–Љ–Є—З–µ—Б–Ї–Є –њ—А–Є–і–∞—В–Ї–Њ–≤ –Є –Љ–∞—В–Ї–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–ї–µ–і—Г–µ—В –њ—А–Є–Ј–љ–∞—В—М, —З—В–Њ –≤ —А–µ–∞–ї—М–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є—П –Т–Ч–Ю–Ь–Ґ –њ–Њ –±–Њ–ї—М—И–µ–є —З–∞—Б—В–Є —П–≤–ї—П–µ—В—Б—П —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є, –∞ —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–µ–Ї–Њ—А—А–µ–Ї—В–љ—Л—Е –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –≤–≤–Њ–і—П—В –≤ –Ј–∞–±–ї—Г–ґ–і–µ–љ–Є–µ –Є –Љ–Њ–≥—Г—В –њ—А–Є–≤–Њ–і–Є—В—М, —Б–Ї–Њ—А–µ–µ, –Ї –њ—А–Њ–≤–µ–і–µ–љ–Є—О –Ї–∞—Б—В—А–∞—Ж–Є–Є, –љ–µ–ґ–µ–ї–Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П.
–°–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —В–µ–љ–і–µ–љ—Ж–Є—П —В–µ—А–∞–њ–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ—А–Њ–≤–Њ–Ј–≥–ї–∞—И–∞–µ—В –њ—А–Є–љ—Ж–Є–њ «–љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є» –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤—Л–±–Њ—А–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –љ–µ –≤—Б–µ–≥–і–∞ –Є–Љ–µ–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤ —Б—Е–µ–Љ–µ –ї–µ—З–µ–љ–Є—П –Њ–і–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞, –Є–љ–Њ–≥–і–∞ –Є—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–Њ—Е–Њ–і–Є—В –і–Њ –і–µ—Б—П—В–Є. –° –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –њ—А–Є–љ–Є–Љ–∞–µ–Љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞—В—М –Є—Е —Н—Д—Д–µ–Ї—В —Б—В–∞–љ–Њ–≤–Є—В—Б—П –≤—Б–µ —В—А—Г–і–љ–µ–µ, –∞ –њ–Њ–і—З–∞—Б –Є –≤–Њ–≤—Б–µ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –љ–∞–ї–Є—З–Є–µ–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є, –Ї–Њ—В–Њ—А—Л–µ –і–Њ —Б–Є—Е –њ–Њ—А –Є–Ј—Г—З–µ–љ—Л –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ. –Ф—А—Г–≥–Є–Љ –љ–µ –Љ–µ–љ–µ–µ –≤–∞–ґ–љ—Л–Љ —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –њ–Њ–ї–Є–њ—А–∞–≥–Љ–∞–Ј–Є–Є —П–≤–ї—П–µ—В—Б—П –љ–µ—Г–і–Њ–±—Б—В–≤–Њ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–∞. –Я–Њ–ї—Г—З–Є–≤ –Є–Ј —А—Г–Ї –≤—А–∞—З–∞ –њ–Њ–і—А–Њ–±–љ—Г—О —Б—Е–µ–Љ—Г —Б–≤–Њ–µ–≥–Њ –ї–µ—З–µ–љ–Є—П, –њ–∞—Ж–Є–µ–љ—В –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –≤ –≤–µ—Б—М–Љ–∞ —Б–ї–Њ–ґ–љ–Њ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є: –≥–і–µ –љ–∞–є—В–Є –≤—Б–µ —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л, –≥–і–µ –≤–Ј—П—В—М —Б—В–Њ–ї—М–Ї–Њ –і–µ–љ–µ–≥, —З—В–Њ–±—Л –Є—Е –Њ–њ–ї–∞—В–Є—В—М, –Ї–∞–Ї –±–µ–Ј–Њ—И–Є–±–Њ—З–љ–Њ –≤—Л–њ–Њ–ї–љ–Є—В—М –њ—А–µ–і–њ–Є—Б–∞–љ–Є—П –њ–Њ –њ—А–Є–µ–Љ—Г –Є —З—В–Њ –±—Г–і–µ—В —Б –Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–Љ –њ–Њ—Б–ї–µ —Н—В–Њ–≥–Њ?..
–†–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—П –≤–Њ–њ—А–Њ—Б —В–µ—А–∞–њ–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤, —Б–µ–≥–Њ–і–љ—П —В–∞–Ї –Є–ї–Є –Є–љ–∞—З–µ –њ—А–Є—Е–Њ–і–Є—В—Б—П —Б—В–∞–ї–Ї–Є–≤–∞—В—М—Б—П —Б –њ—А–Њ–±–ї–µ–Љ–Њ–є –њ–Њ–ї–Є–њ—А–∞–≥–Љ–∞–Ј–Є–Є. –° —З–µ–Љ —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ? –Ъ–∞–Ї –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –≤—Л—И–µ, —Б—В—А–µ–Љ–Є—В–µ–ї—М–љ–Њ —А–∞—Б—В–µ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б–ї—Г—З–∞–µ–≤ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, –≤—Л–Ј–≤–∞–љ–љ—Л—Е –љ–µ –Њ–і–љ–Є–Љ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–Љ, –∞ –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–µ–є 2–6 –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є. –Т —В–∞–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е —Б—В–∞–љ–Њ–≤–Є—В—Б—П –Њ—З–µ–≤–Є–і–љ—Л–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Б–Є–ї—М–љ—Л—Е –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–∞–Ї –љ–Є —Б—В—А–∞–љ–љ–Њ, —И–Є—А–Њ–Ї–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –і–µ–є—Б—В–≤–Є—П, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤ –Є—Е «—И–Є—А–Њ–Ї–Є–µ —Б–њ–µ–Ї—В—А—Л» –љ–µ —Г–Ї–ї–∞–і—Л–≤–∞—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–µ –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ —А–∞–Ј—А–∞–±–Њ—В–Ї–∞ –љ–Њ–≤–Њ–є —Б—Е–µ–Љ—Л —В–µ—А–∞–њ–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤ – —Б –њ—А–Є–≤–ї–µ—З–µ–љ–Є–µ–Љ –љ–Њ–≤—Л—Е –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –і–µ–є—Б—В–≤–Є—П, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–µ–≥–Њ –≤–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е –њ—А–Є–±–µ–≥–∞—В—М –Ї –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –і–ї—П –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –і–Њ–ї–ґ–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і –Є –∞–љ–∞—Н—А–Њ–±–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є –≤ —Б—Е–µ–Љ—Л –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ —Б –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤–Ї–ї—О—З–∞—В—М –Ґ–Є–±–µ—А–∞–ї (–Њ—А–љ–Є–і–∞–Ј–Њ–ї) –≤ —Б–≤—П–Ј–Є —Б –µ–≥–Њ –љ–µ—Б–Њ–Є–Ј–Љ–µ—А–Є–Љ–Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і –Є –≤–і–≤–Њ–µ –±–Њ–ї—М—И–Є–Љ –њ–µ—А–Є–Њ–і–Њ–Љ —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї–Њ–Љ.
–Ф–ї—П –ї–µ—З–µ–љ–Є—П –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е —Б–ї—Г—З–∞–µ–≤ –≥–Њ–љ–Њ—А–µ–Є –Љ–Њ–ґ–љ–Њ –њ—А–µ–і–ї–Њ–ґ–Є—В—М –Њ–і–љ–Њ–Ї—А–∞—В–љ—Л–є –њ—А–Є–µ–Љ 400 –Љ–≥ –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞. –Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ –Ї —В–µ—А–∞–њ–Є–Є –≥–Њ–љ–Њ—А–µ–Є —П–≤–ї—П–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –Њ–і–љ–Є–Љ –Є–Ј –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–є –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П–µ—В—Б—П —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ (–†–Њ—Ж–µ—Д–Є–љ). –Ф–ї—П –ї–µ—З–µ–љ–Є—П –≥–Њ–љ–Њ—А–µ–Є –†–Њ—Ж–µ—Д–Є–љ –љ–∞–Ј–љ–∞—З–∞—О—В –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –≤ –і–Њ–Ј–µ 1 –≥ –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ –Є–ї–Є 0,5 –≥ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ. –Т —Б–≤—П–Ј–Є —Б —В–µ–Љ, —З—В–Њ –і–Њ–≤–Њ–ї—М–љ–Њ —З–∞—Б—В–Њ –≥–Њ–љ–Њ–Ї–Њ–Ї–Ї–Є —Б–Њ—З–µ—В–∞—О—В—Б—П —Б —В—А–Є—Е–Њ–Љ–Њ–љ–∞–і–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –Ј–∞ —Б—З–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Ї —Д–∞–≥–Њ—Ж–Є—В–Њ–Ј—Г —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–љ–Є—О –≥–Њ–љ–Њ—А–µ–Є, –∞ —В–∞–Ї–ґ–µ –≤–Њ—Б—Е–Њ–ґ–і–µ–љ–Є—О –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ –≤–µ—А—Е–љ–Є–µ –Њ—В–і–µ–ї—Л –њ–Њ–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л, —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ–µ—А–µ–і –≤–≤–µ–і–µ–љ–Є–µ–Љ –†–Њ—Ж–µ—Д–Є–љ–∞ –љ–∞–Ј–љ–∞—З–Є—В—М –њ—П—В–Є–і–љ–µ–≤–љ—Л–є –Ї—Г—А—Б —В–µ—А–∞–њ–Є–Є –Ґ–Є–±–µ—А–∞–ї–Њ–Љ –њ–Њ 500 –Љ–≥ –і–≤–∞ —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є.
–Ф–ї—П —В–µ—А–∞–њ–Є–Є —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є –Є –Љ–Є–Ї–Њ–њ–ї–∞–Ј–Љ–µ–љ–љ–Њ–є/—Г—А–µ–∞–њ–ї–∞–Ј–Љ–µ–љ–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –љ–∞–Ј–љ–∞—З–∞—О—В –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ 200–300 –Љ–≥ 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М – 7 –і–љ–µ–є (–њ—А–Є –Є–Ј–≤–µ—Б—В–љ–Њ–є –Є–ї–Є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–є –і–∞—В–µ –Ј–∞—А–∞–ґ–µ–љ–Є—П, –≤ –Њ—Б—В–∞–ї—М–љ—Л—Е —Б–ї—Г—З–∞—П—Е 20–21 –і–µ–љ—М).
–Я—А–Є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–Љ –≤–∞–≥–Є–љ–Њ–Ј–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–∞ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –і–≤—Г—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤: –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ (300 –Љ–≥ 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М) + –Ґ–Є–±–µ—А–∞–ї (500 –Љ–≥ 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М) –≤ —В–µ—З–µ–љ–Є–µ 7 –і–љ–µ–є. –Я–Њ –Њ–Ї–Њ–љ—З–∞–љ–Є–Є —В–µ—А–∞–њ–Є–Є —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–∞ –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є—П –Є –ї–µ—З–µ–љ–Є–µ —Г –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–∞, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј—Г –Ї–Є—И–µ—З–љ–Є–Ї–∞ –њ—А–Є–њ–Є—Б—Л–≤–∞–µ—В—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–∞—П —А–Њ–ї—М –≤ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –і–∞–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Э–µ—В—А—Г–і–љ–Њ –Ј–∞–Љ–µ—В–Є—В—М, —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—П –њ—А–Є–≤–µ–і–µ–љ–љ—Л–µ –≤—Л—И–µ —Б—Е–µ–Љ—Л, —З—В–Њ –≤ —Б–ї—Г—З–∞–µ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Љ–Є–Ї—Б—В-–Є–љ—Д–µ–Ї—Ж–Є–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –±—Г–і–µ—В –њ—А–Є–Љ–µ–љ–Є—В—М —В–Њ–ї—М–Ї–Њ –і–≤–∞ –њ—А–µ–њ–∞—А–∞—В–∞ (–Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ –Є –Ґ–Є–±–µ—А–∞–ї) –≤–Ј–∞–Љ–µ–љ —В—А–µ—Е –Є–ї–Є —З–µ—В—Л—А–µ—Е. –Т —В–∞–Ї–Њ–Љ —Б–ї—Г—З–∞–µ —Б—Е–µ–Љ–∞ —В–µ—А–∞–њ–Є–Є –±—Г–і–µ—В –≤—Л–≥–ї—П–і–µ—В—М —В–∞–Ї –ґ–µ, –Ї–∞–Ї –Є –њ—А–Є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–Љ –≤–∞–≥–Є–љ–Њ–Ј–µ.
–° –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Љ–µ–љ—П–µ—В—Б—П –њ–Њ–і—Е–Њ–і –Ї —В–µ—А–∞–њ–Є–Є –Т–Ч–Ю–Ь–Ґ. –Ы–µ—З–µ–љ–Є–µ –Т–Ч–Ю–Ь–Ґ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –љ–∞—З–∞—В–Њ —Б—А–∞–Ј—Г –ґ–µ –њ–Њ—Б–ї–µ —Г—Б—В–∞–љ–Њ–≤–Ї–Є –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–Є–∞–≥–љ–Њ–Ј–∞, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–≥–Њ –љ–∞ –љ–∞–ї–Є—З–Є–Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л—Е –Ї—А–Є—В–µ—А–Є–µ–≤ –Т–Ю–Ч, —В–∞–Ї –Ї–∞–Ї –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Њ—В–і–∞–ї–µ–љ–љ—Л—Е –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–є, —А–∞–Ј–≤–Є—В–Є—П —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤–Њ–≥–Њ –Ї–∞—Б–Ї–∞–і–∞ –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–∞–љ–∞ —Б–Њ —Б—А–Њ–Ї–∞–Љ–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞. –Ш—Б—Е–Њ–і—П –Є–Ј —Н—В–Њ–≥–Њ –≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –ї–µ—З–µ–љ–Є–µ –і–Њ–ї–ґ–љ–Њ –љ–∞—З–Є–љ–∞—В—М—Б—П —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Є, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤—А–µ–Љ—П, –њ–Њ—В—А–∞—З–µ–љ–љ–Њ–µ –љ–∞ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є—О, –Љ–Њ–ґ–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г—Е—Г–і—И–Є—В—М —А–µ–Ј—Г–ї—М—В–∞—В.
–Т –љ–∞—И–µ–є –њ—А–∞–Ї—В–Є–Ї–µ –Љ—Л –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –њ—А–Є–љ—Ж–Є–њ—Л —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Т–Ч–Ю–Ь–Ґ, —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л–µ –¶–µ–љ—В—А–Њ–Љ –њ–Њ –Ї–Њ–љ—В—А–Њ–ї—О –Ј–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М—О –°–®–Р (CDC), –њ—А–µ–і–њ–Є—Б—Л–≤–∞—О—Й–Є–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–ї–µ–і—Г—О—Й–µ–є —Б—Е–µ–Љ—Л:
–Ю—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ (400 –Љ–≥ 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М) + –Ґ–Є–±–µ—А–∞–ї (500 –Љ–≥ 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М) = 15 –і–љ–µ–є
–Ю—З–µ–≤–Є–і–љ–Њ—Б—В—М –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є—П –Є–Љ–µ–љ–љ–Њ —Н—В–Њ–є —Б—Е–µ–Љ—Л –њ—А–Є —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Т–Ч–Ю–Ь–Ґ –љ–∞–≥–ї—П–і–љ–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –≤ —В–∞–±–ї. 1. –Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —В–∞–±–ї–Є—Ж—Л, —Б–Њ—З–µ—В–∞–љ–Є–µ –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–∞ —Б –Ґ–Є–±–µ—А–∞–ї–Њ–Љ –љ–∞–Є–±–Њ–ї–µ–µ –њ–Њ–ї–љ–Њ –њ–µ—А–µ–Ї—А—Л–≤–∞–µ—В –≤–µ—Б—М —Б–њ–µ–Ї—В—А –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Т–Ч–Ю–Ь–Ґ, —А–µ–∞–ї–Є–Ј—Г—П –њ—А–Є —Н—В–Њ–Љ –њ—А–Є–љ—Ж–Є–њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –Є–Ј–±–µ–≥–∞—П –њ–Њ–ї–Є–њ—А–∞–≥–Љ–∞–Ј–Є–Є –њ—А–Є –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є.
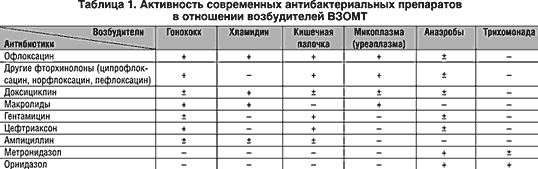
–†–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –≤—Л–Ј–і–Њ—А–Њ–≤–ї–µ–љ–Є–µ –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е: –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –±–Њ–ї–µ–є –≤ –љ–Є–Ј—Г –ґ–Є–≤–Њ—В–∞, —В–Њ—И–љ–Њ—В—Л, –≥–љ–Њ–є–љ—Л—Е –Є –Ї—А–Њ–≤—П–љ–Є—Б—В—Л—Е –≤—Л–і–µ–ї–µ–љ–Є–є –Є–Ј –њ–Њ–ї–Њ–≤—Л—Е –њ—Г—В–µ–є, –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –Є —З–Є—Б–ї–∞ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ –Ї—А–Њ–≤–Є, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –°–Ю–≠. –Я–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П –≤ –Љ–∞–Ј–Ї–∞—Е –Є–Ј —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞–ї–Њ—Б—М —З–Є—Б–ї–Њ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤, –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є –њ–∞—В–Њ–≥–µ–љ–љ—Л–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Б –±–Њ–ї—М—И–Є–Љ —Г—Б–њ–µ—Е–Њ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Ґ–Є–±–µ—А–∞–ї–∞ —Б –Њ—Д–ї–Њ–Ї—Б–∞—Ж–Є–љ–Њ–Љ. –•–Њ—В—П –і–Њ —Б–Є—Е –њ–Њ—А –љ–µ —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ –њ—А–µ–њ–∞—А–∞—В, –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—Й–Є–є –љ–∞ –≤—Б–µ—Е –±–µ–Ј –Є—Б–Ї–ї—О—З–µ–љ–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤, —Г–ґ–µ —Б–µ–є—З–∞—Б –њ—А–µ–і–ї–∞–≥–∞–µ–Љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б–њ–Њ—Б–Њ–±–љ–∞ –Њ–±–µ—Б–њ–µ—З–Є—В—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ–≥—А–µ—Б—Б –≤ —А–µ—И–µ–љ–Є–Є —Б–ї–Њ–ґ–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ—Л –њ–Њ–ї–Є–њ—А–∞–≥–Љ–∞–Ј–Є–Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –≥–µ–љ–Є—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –Я—А–Є —Н—В–Њ–Љ —А–µ–∞–ї–Є–Ј—Г–µ—В—Б—П –њ—А–Є–љ—Ж–Є–њ –±–µ—А–µ–ґ–љ–Њ–≥–Њ –Њ—В–љ–Њ—И–µ–љ–Є—П –Ї –њ–∞—Ж–Є–µ–љ—В—Г –Є –±–µ–Ј–ґ–∞–ї–Њ—Б—В–љ–Њ–≥–Њ – –Ї –±–∞–Ї—В–µ—А–Є—П–Љ, –Ї–Њ—В–Њ—А—Л–є —Б–Њ—З–µ—В–∞–µ—В –≤ —Б–µ–±–µ —А–∞–Ј—Г–Љ–љ—Г—О –∞–≥—А–µ—Б—Б–Є–≤–љ–Њ—Б—В—М –Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї—Г—О —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М.












