–°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Њ–є –≤–µ—В–≤–Є –Р–љ–≥–ї–Њ–—Б–Ї–∞–љ–і–Є–љ–∞–≤—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є—Б—Е–Њ–і–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б–µ—А–і—Ж–∞ (ASCOT–LLA) —Г –ї–Є—Ж —Б –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є –±–µ–Ј –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є —Б–µ—А–і—Ж–∞ (–Ш–С–°) –ї–µ—З–µ–љ–Є–µ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–µ—В —З–∞—Б—В–Њ—В—Г –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Є–љ—Б—Г–ї—М—В–Њ–≤ –Є –њ—А–Є—Б—В—Г–њ–Њ–≤ –Ш–С–° [1]. –Т —В–µ—З–µ–љ–Є–µ —Б—А–µ–і–љ–µ–≥–Њ —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є–є 3,3 –≥–Њ–і–∞ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–µ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ —З–Є—Б–ї–∞ —Б–Њ–±—Л—В–Є–є –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є (–Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –±–µ–Ј —Б–Љ–µ—А—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ –Є –Ш–С–° —Б–Њ —Б–Љ–µ—А—В–µ–ї—М–љ—Л–Љ –Є—Б—Е–Њ–і–Њ–Љ) –љ–∞ 36% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ, —З—В–Њ –Ї–Њ—А—А–µ–ї–Є—А–Њ–≤–∞–ї–Њ —Б —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Є –Ы–Я–Э–Я –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 1,1 –Є 1,0 –Љ–Љ–Њ–ї—М/–ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –≠—В–Є –і–∞–љ–љ—Л–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –љ–∞–±–ї—О–і–µ–љ–Є—П, —Б–і–µ–ї–∞–љ–љ—Л–µ –≤ —Е–Њ–і–µ –і—А—Г–≥–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Б—В–∞—В–Є–љ–Њ–≤ [2], —А–∞—Б—И–Є—А—П—П —В–µ–Љ —Б–∞–Љ—Л–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Г—О –±–∞–Ј—Г, –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Ї–Њ—В–Њ—А–Њ–є —А–∞–Ј—А–∞–±–∞—В—Л–≤–∞—О—В—Б—П —Б—Е–µ–Љ—Л –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ш–С–° —Г –±–Њ–ї—М–љ—Л—Е –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є —Б –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–Р–Ф) –Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ –Ш–С–° (–Њ–Ї–Њ–ї–Њ 10% –≤ —В–µ—З–µ–љ–Є–µ 10 –ї–µ—В).
–° –њ–Њ–Љ–Њ—Й—М—О 2×2 —Д–∞–Ї—В–Њ—А–љ–Њ–≥–Њ –њ–ї–∞–љ–∞ ASCOT-LLA –Њ–±—К–µ–і–Є–љ–Є–ї–Є —Б –µ—Й–µ –±–Њ–ї–µ–µ –Ї—А—Г–њ–љ–Њ–Љ–∞—Б—И—В–∞–±–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Є—Б–њ—Л—В–∞–љ–Є–µ–Љ – –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є –≤–µ—В–≤—М—О –Р–љ–≥–ї–Њ–—Б–Ї–∞–љ–і–Є–љ–∞–≤—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є—Б—Е–Њ–і–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б–µ—А–і—Ж–∞ (ASCOT–BPLA), –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ 19257 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ї—Г—З–∞–ї–Є –ї–µ—З–µ–љ–Є–µ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Њ–і–љ–Њ–є –Є–Ј –і–≤—Г—Е —Б—В—А–∞—В–µ–≥–Є–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є [3]. –Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є ASCOT–BPLA —Б—А–∞–≤–љ–Є–≤–∞–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–Њ–≤–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ш–С–° –Є –і—А—Г–≥–Є—Е —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —П–≤–ї–µ–љ–Є–є, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–≥–Њ –љ–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –±–ї–Њ–Ї–∞—В–Њ—А–∞ –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (–Р–Я–§) –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–Њ–Љ (–і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф), –Є —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–є —Б—Е–µ–Љ—Л, –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—О—Й–µ–є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ β––±–ї–Њ–Ї–∞—В–Њ—А–∞ –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –Є –і–Є—Г—А–µ—В–Є–Ї–∞ –±–µ–љ–і—А–Њ—Д–ї—Г–Љ–µ—В–Є–∞–Ј–Є–і–∞ —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Ї–∞–ї–Є—П.
ASCOT–BPLA –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Њ—Б—М –Є –њ–Њ—Б–ї–µ –і–Њ—Б—А–Њ—З–љ–Њ–≥–Њ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П ASCOT-LLA, –Њ–і–љ–∞–Ї–Њ –Є –Њ–љ–Њ –±—Л–ї–Њ –Ј–∞–≤–µ—А—И–µ–љ–Њ –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ–Њ (—Б—А–µ–і–љ–Є–є —Б—А–Њ–Ї –љ–∞–±–ї—О–і–µ–љ–Є—П –њ—А–Є–Љ–µ—А–љ–Њ 5,5 –ї–µ—В) [4]. –£ –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ —Б –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–Њ–Љ, –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —П–≤–ї–µ–љ–Є–є (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –≤—Б–µ—Е –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є, –Є–љ—Б—Г–ї—М—В–Њ–≤, –≤—Б–µ—Е –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є –Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤, —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Љ–µ—А—В–Є) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –∞—В–µ–љ–Њ–ї–Њ–ї –Є –і–Є—Г—А–µ—В–Є–Ї. –Т –љ–∞—Б—В–Њ—П—Й–µ–Љ –Њ–±–Ј–Њ—А–µ –њ—А–µ–і–њ—А–Є–љ—П—В–∞ –њ–Њ–њ—Л—В–Ї–∞ –њ–Њ–љ—П—В—М, –≤–ї–Є—П—О—В –ї–Є —А–∞–Ј–ї–Є—З–љ—Л–µ –≤–∞—А–Є–∞–љ—В—Л –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –Є –і—А—Г–≥–Є—Е —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —П–≤–ї–µ–љ–Є–є.
–Ь–µ—В–Њ–і—Л
–Я–Њ–і—А–Њ–±–љ–Њ–µ –Њ–њ–Є—Б–∞–љ–Є–µ –њ—А–Њ—В–Њ–Ї–Њ–ї–∞ ASCOT –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–Њ —А–∞–љ–µ–µ [3], –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П —В–∞–Ї–ґ–µ –і–Њ—Б—В—Г–њ–љ–∞ –љ–∞ –≤–µ–±–—Б–∞–є—В–µ www.ascotstudy.org. –Ш—Б–њ—Л—В—Г–µ–Љ—Л—Е –Њ—В–±–Є—А–∞–ї–Є —Б —Д–µ–≤—А–∞–ї—П
–Я–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –њ–Њ–і–≥–Њ—В–Њ–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ —Н—В–∞–њ–∞ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О 4 –љ–µ–і–µ–ї–Є, –≤ —Е–Њ–і–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –Њ–њ—А–µ–і–µ–ї—П–ї–Є —Б—В–µ–њ–µ–љ—М –≥–Њ–і–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–∞ –і–ї—П –і–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –њ–Њ–ї—Г—З–∞–ї–Є –µ–≥–Њ —Б–Њ–≥–ї–∞—Б–Є–µ –љ–∞ —Г—З–∞—Б—В–Є–µ, –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –њ–Њ–і–≤–µ—А–≥–∞–ї–Є –њ–µ—А–≤–Њ–є —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є (BPLA) –Є —А–∞–Ј–і–µ–ї—П–ї–Є –љ–∞ 2 –Ї–Њ–≥–Њ—А—В—Л – –≥—А—Г–њ–њ–∞ –ї–µ—З–µ–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –≥—А—Г–њ–њ–∞ –ї–µ—З–µ–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞—В–µ–љ–Њ–ї–Њ–ї–∞. –С–Њ–ї—М–љ—Л—Е —Б –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–µ–є –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –љ–∞—В–Њ—Й–∞–Ї –Љ–µ–љ–µ–µ 6,5 –Љ–Љ–Њ–ї—М (250 –Љ–≥/–і–ї), –љ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–≤—И–Є—Е –љ–∞ –Љ–Њ–Љ–µ–љ—В –Њ—Б–Љ–Њ—В—А–∞ —Б—В–∞—В–Є–љ–Њ–≤ –Є–ї–Є —Д–Є–±—А–∞—В–Њ–≤, –њ–Њ–і–≤–µ—А–≥–∞–ї–Є –≤—В–Њ—А–Њ–є —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Д–∞–Ї—В–Њ—А–љ–Њ–≥–Њ –њ–ї–∞–љ–∞ –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –і–Њ–Ј–µ 10 –Љ–≥ –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ (ASCOT–LLA). –Т —Ж–µ–ї–Њ–Љ –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В–µ—А–∞–њ–Є–Є –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є–ї–Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –±—Л–ї–Њ –Њ—В–Њ–±—А–∞–љ–Њ 19257 —З–µ–ї–Њ–≤–µ–Ї, –Є–Ј –љ–Є—Е 10305 –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е –њ—А–Є–љ–Є–Љ–∞–ї–Є –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ. –Я—А–Њ—В–Њ–Ї–Њ–ї –≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г—З–∞—Б—В–≤–Њ–≤–∞–≤—И–Є—Е –≤ —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є ASCOT–BPLA, –і–µ—В–∞–ї—М–љ–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –≤ –і—А—Г–≥–Є—Е —А–∞–±–Њ—В–∞—Е [3]. –Т –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–∞–ґ–і–Њ–≥–Њ –≤–Є–Ј–Є—В–∞ –Ї –≤—А–∞—З—Г –і–Њ–Ј—Г –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —В–Є—В—А–Њ–≤–∞–ї–Є, –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф (–Љ–µ–љ–µ–µ 140/90 –Љ–Љ —А—В.—Б—В. –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –°–Ф, –Љ–µ–љ–µ–µ 130/80 –Љ–Љ —А—В.—Б—В. –њ—А–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–Љ –°–Ф) –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –і–Њ–±–∞–≤–ї—П–ї–Є –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї, –∞ –≤ –≥—А—Г–њ–њ–µ –∞—В–µ–љ–Њ–ї–Њ–ї–∞ – –±–µ–љ–і—А–Њ—Д–ї—Г–Љ–µ—В–Є–∞–Ј–Є–і —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Ї–∞–ї–Є—П.
–Я–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –њ—А–Њ—Ж–µ–і—Г—А—Л —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є —Д–Є–Ї—Б–Є—А–Њ–≤–∞–ї–Є –і–∞–љ–љ—Л–µ –Њ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є —А–∞–Ј–≤–Є—В–Є–Є –ї—О–±—Л—Е –љ–Њ–≤—Л—Е –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є –Є–ї–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є —Б–ї—Г—З–∞–Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ –ї—О–±–Њ–є –њ—А–Є—З–Є–љ–µ). –Ъ–Њ–љ–µ—З–љ—Л–µ —В–Њ—З–Ї–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М —З–ї–µ–љ–∞–Љ–Є –Ъ–Њ–Љ–Є—В–µ—В–∞ –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї –≤—Б–ї–µ–њ—Г—О –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї—А–Є—В–µ—А–Є–µ–≤ –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –і–Є–∞–≥–љ–Њ–Ј–∞, –њ—А–Є–≤–Њ–і–Є–Љ—Л—Е –љ–∞ –≤–µ–±–—Б–∞–є—В–µ www.ascotstudy.org. –Я–µ—А–≤–Є—З–љ—Л–Љ–Є –Ї–Њ–љ–µ—З–љ—Л–Љ–Є —В–Њ—З–Ї–∞–Љ–Є ASCOT–LLA –Є ASCOT–BPLA —П–≤–ї—П–ї–Є—Б—М –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –±–µ–Ј —Б–Љ–µ—А—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –±–µ–Ј–±–Њ–ї–µ–≤–∞—П —Д–Њ—А–Љ–∞) –Є –Ш–С–° —Б–Њ —Б–Љ–µ—А—В–µ–ї—М–љ—Л–Љ –Є—Б—Е–Њ–і–Њ–Љ (—Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–∞—П —Б–Љ–µ—А—В—М). –Т—В–Њ—А–Є—З–љ—Л–µ –Ї–Њ–љ–µ—З–љ—Л–µ —В–Њ—З–Ї–Є –≤–Ї–ї—О—З–∞–ї–Є –Є–љ—Б—Г–ї—М—В —Б–Њ —Б–Љ–µ—А—В–µ–ї—М–љ—Л–Љ –Є—Б—Е–Њ–і–Њ–Љ –Є–ї–Є –±–µ–Ј, –∞ —В–∞–Ї–ґ–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–µ –Ї–Њ–љ–µ—З–љ—Л–µ —В–Њ—З–Ї–Є. –Т –Ї–∞—З–µ—Б—В–≤–µ —В—А–µ—В–Є—З–љ–Њ–є —В–Њ—З–Ї–Є –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ –Ј–∞–і–∞–≤–∞–ї–Њ—Б—М –≤—Л—П–≤–ї–µ–љ–Є–µ –ї—О–±–Њ–≥–Њ —А–Њ–і–∞ —Б–Є–љ–µ—А–≥–Є–Є –Љ–µ–ґ–і—Г –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ –Є –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –ї–µ—З–µ–љ–Є–µ–Љ.
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л
–Ь–µ—В–Њ–і—Л —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞–±–Њ—В–Ї–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Њ–њ–Є—Б–∞–љ—Л –љ–∞ –≤–µ–±–—Б–∞–є—В–µ www.ascotstudy.org. –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤—Г—П—Б—М –њ—А–Є–љ—Ж–Є–њ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ –Є –≥—А—Г–њ–њ–µ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ —Б—А–∞–≤–љ–Є–≤–∞–ї–Є –≤—А–µ–Љ—П, –њ—А–Њ—Е–Њ–і–Є–≤—И–µ–µ –і–Њ –Љ–Њ–Љ–µ–љ—В–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–µ—А–≤–Њ–≥–Њ —Н–њ–Є–Ј–Њ–і–∞ –°–°–Ч (–≤–њ–ї–Њ—В—М –і–Њ –њ—А–Є–Њ—Б—В–∞–љ–Њ–≤–Ї–Є ASCOT–LLA, —Б—А–µ–і–љ–Є–є —Б—А–Њ–Ї –љ–∞–±–ї—О–і–µ–љ–Є–є 3,3 –≥–Њ–і–∞), —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –ї–Њ–≥–∞—А–Є—Д–Љ–Є—А–Њ–≤–∞–љ–Є—П —А–∞–љ–≥–Њ–≤ –Є –Љ–Њ–і–µ–ї–µ–є –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ –Ъ–Њ–Ї—Б–∞. –Ф–ї—П –њ—А–Њ–≤–µ—А–Ї–Є –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –і–Њ–њ—Г—Й–µ–љ–Є–є —А–Є—Б–Ї–∞ –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ—Б—В—М –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є—П –Њ —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –Є–љ–і–Є–Ї–∞—В–Њ—А–∞–Љ–Є –ї–µ—З–µ–љ–Є—П –Є –≤—А–µ–Љ–µ–љ–µ–Љ. –Ф–ї—П –≤—Б–µ—Е –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї –Ј–љ–∞—З–µ–љ–Є–µ –† –њ—А–µ–≤—Л—Б–Є–ї–Њ 0,30. –Ґ–µ—Б—В –Т–∞–ї—М–і–∞ –і–ї—П –Њ—Ж–µ–љ–Ї–Є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Є –Љ–µ–ґ–і—Г –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ –Є –і–≤—Г–Љ—П —Б—В—А–∞—В–µ–≥–Є—П–Љ–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤ –њ–Њ–ї–љ–Њ–є –Љ–Њ–і–µ–ї–Є –Ъ–Њ–Ї—Б–∞. –Т—Б–µ –Ї—А–Є—В–µ—А–Є–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В–Є –≤—Л—З–Є—Б–ї—П–ї–Є—Б—М –љ–∞ –Њ—Б–љ–Њ–≤–µ –і–≤–Њ–є–љ–Њ–є –≤—Л–±–Њ—А–Ї–Є –њ—А–Є —Г—А–Њ–≤–љ–µ –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є 0,05.
–†–µ–Ј—Г–ї—М—В–∞—В—Л
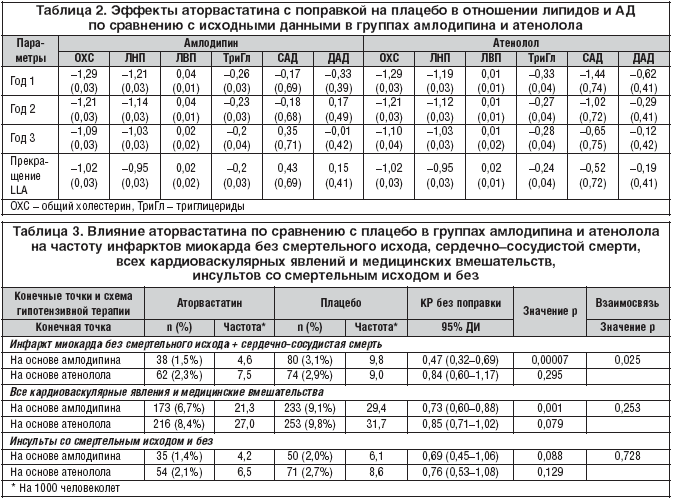
–Ф–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –ї–Є—Ж, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —Г—З–∞—Б—В–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ASCOT–LLA, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ—Л –≤ —А–∞–љ–љ–Є—Е —А–∞–±–Њ—В–∞—Е [1]. –Т –≥—А—Г–њ–њ–∞—Е –ї–µ—З–µ–љ–Є—П —Н—В–Є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –±—Л–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л (—В–∞–±–ї. 1). –Ъ –Љ–Њ–Љ–µ–љ—В—Г –Ј–∞–≤–µ—А—И–µ–љ–Є—П ASCOT–LLA –њ–Њ–ї–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –±—Л–ї–∞ —Б–Њ–±—А–∞–љ–∞ –њ–Њ 98,8% —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (10305 —З–µ–ї–Њ–≤–µ–Ї). –Я—А–Є–µ–Љ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–ї —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Є –Ы–Я–Э–Я –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –љ–∞ 1,3 –Є 1,2 –Љ–Љ–Њ–ї—М/–ї —З–µ—А–µ–Ј –≥–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є–є –Є 1,0 –Є 1,0 –Љ–Љ–Њ–ї—М/–ї —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ – –Ї –Љ–Њ–Љ–µ–љ—В—Г –Ј–∞–≤–µ—А—И–µ–љ–Є—П –Є—Б–њ—Л—В–∞–љ–Є–є [1]. –Я—А–Є —Н—В–Њ–Љ —П–≤–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –њ–Њ —Б—В–µ–њ–µ–љ–Є —Б–љ–Є–ґ–µ–љ–Є—П —В–Є—В—А–Њ–≤ –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Є –Ы–Я–Э–Я –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ (—А–Є—Б. 1–Р –Є 1–С). –Т –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —А–Њ—Б—В—Г –Ы–Я–Э–Я —Б—А–µ–і–Є –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Ї–∞–Ї –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ, —В–∞–Ї –Є –њ–ї–∞—Ж–µ–±–Њ, –∞ –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞—В–µ–љ–Њ–ї–Њ–ї–∞ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ы–Я–Э–Я —Б–Њ–Ї—А–∞—Й–∞–ї–Њ—Б—М –њ—А–Є –њ—А–Є–µ–Љ–µ –Є –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞, –Є –њ–ї–∞—Ж–µ–±–Њ (—А–Є—Б. 1–Т). –Ю–і–љ–∞–Ї–Њ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–ї –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–µ (—Е–Њ—В—П –Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ) –∞–±—Б–Њ–ї—О—В–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ы–Я–Э–Я –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е (—А–Є—Б. 1–Т, —В–∞–±–ї. 2). –Т –њ—А–Њ—Ж–µ—Б—Б–µ –ї–µ—З–µ–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ —Г—А–Њ–≤–µ–љ—М —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ —Б–љ–Є–ґ–∞–ї—Б—П —Б —Б–∞–Љ–Њ–≥–Њ –љ–∞—З–∞–ї–∞, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —В–µ—А–∞–њ–Є—П –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ —Б–љ–∞—З–∞–ї–∞ —Б–њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞–ї–∞ –њ–Њ–і—К–µ–Љ —Б—А–µ–і–љ–Є—Е –Ј–љ–∞—З–µ–љ–Є–є —Н—В–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П, –∞ —Г–Љ–µ–љ—М—И–Є–ї–Є—Б—М –Њ–љ–Є —З–µ—А–µ–Ј –≥–Њ–і (—А–Є—Б. 1–У). –Э–Њ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –њ—А–Є–≤–µ–ї–Њ –Ї –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О —В–Є—В—А–Њ–≤ —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –≤ –≥—А—Г–њ–њ–∞—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞ (—В–∞–±–ї. 2).
–Ъ –Ї–Њ–љ—Ж—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П ASCOT–LLA –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –ї–µ—З–µ–љ–Є—П –њ–Њ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є —Б—А–µ–і–љ–Є–є —Г—А–Њ–≤–µ–љ—М –Р–Ф –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ –Є –њ–ї–∞—Ж–µ–±–Њ –Њ–Ї–∞–Ј–∞–ї—Б—П —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л–Љ (138,3/80,4 –Є 138,4/80,4 –Љ–Љ —А—В.—Б—В. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –¶–µ–ї–µ–≤–Њ–µ –Р–Ф —Г–і–∞–≤–∞–ї–Њ—Б—М –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—В—М —Г 58,8% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–≥–Њ –°–Ф (–Љ–µ–љ–µ–µ 140/90 –Љ–Љ —А—В.—Б—В.) –Є —Г 31% –±–Њ–ї—М–љ—Л—Е –°–Ф (–Љ–µ–љ–µ–µ 130/80 –Љ–Љ —А—В.—Б—В.). –Т –Ї–∞–ґ–і–Њ–є –Є–Ј –≥—А—Г–њ–њ –њ–Њ –Њ—В–і–µ–ї—М–љ–Њ—Б—В–Є —А–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г –≤–µ–ї–Є—З–Є–љ–∞–Љ–Є –Р–Ф —Г –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ –Є –њ–ї–∞—Ж–µ–±–Њ –±—Л–ї–∞ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є (—А–Є—Б. 2). –Т –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –Р–Ф –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–љ–Є–Ј–Є–ї–Њ—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 2,9/2,0 –Љ–Љ —А—В.—Б—В. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –љ–Њ –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –Є –њ–ї–∞—Ж–µ–±–Њ —Н—В–Є –Ј–љ–∞—З–µ–љ–Є—П –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –≤–µ—Б—М–Љ–∞ –±–ї–Є–Ј–Ї–Є (—А–Є—Б. 2, —В–∞–±–ї. 2).
–Т –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ–Њ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є —З–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –њ–µ—А–≤–Є—З–љ—Л—Е –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї (–Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –±–µ–Ј —Б–Љ–µ—А—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ –Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–∞—П —Б–Љ–µ—А—В—М) –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–Є–ґ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ (–Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В —А–Є—Б–Ї–∞/–Ъ–†=0,64; 95% –Ф–Ш 0,50–0,83 –њ—А–Є p=0,0005) [1]. –°—А–µ–і–Є –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ –њ–Њ–Ј–≤–Њ–ї–Є–ї –і–Њ–±–Є—В—М—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–≥–Њ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є –љ–∞ 53% (–Ъ–†=0,47; 95% –Ф–Ш 0,32–0,69 –њ—А–Є p<0,0001), –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –≥—А—Г–њ–њ–µ –∞—В–µ–љ–Њ–ї–Њ–ї–∞ —Н—В–Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —Б–Њ—Б—В–∞–≤–Є–ї –ї–Є—И—М 16% (–Ъ–†=0,84; 95% –Ф–Ш 0,60–1,17 –њ—А–Є p=0,30; —В–∞–±–ї. 3, —А–Є—Б. 3). –†–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г —Г–Ї–∞–Ј–∞–љ–љ—Л–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є —А–Є—Б–Ї–∞ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ –љ–∞—Е–Њ–і–Є–ї–∞—Б—М –≤ –≥—А–∞–љ–Є—Ж–∞—Е —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є (–≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М p=0,025).
–Х—Б–ї–Є —Б—А–∞–≤–љ–Є–≤–∞—В—М —Б –њ–ї–∞—Ж–µ–±–Њ, —В–Њ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ —Г–Љ–µ–љ—М—И–∞–ї –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї –≤—Б–µ—Е –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —П–≤–ї–µ–љ–Є–є –Є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –љ–∞ 27% –≤ —Б–ї—Г—З–∞–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ (–Ъ–†=0,73; 95% –Ф–Ш 0,60–0,88 –њ—А–Є p=0,001) –Є –љ–∞ 15% –≤ —Б–ї—Г—З–∞–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞—В–µ–љ–Њ–ї–Њ–ї–∞ (–Ъ–†=0,85; 95% –Ф–Ш 0,71–1,02 –њ—А–Є p=0,079; —А–Є—Б. 4). –†–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г —Н—В–Є–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –љ–µ –Є–Љ–µ–ї–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В–Є (–≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М p=0,25), —З—В–Њ –Њ–±—К—П—Б–љ—П–µ—В—Б—П –Њ—В–ї–Є—З–Є—П–Љ–Є –њ–Њ –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–µ. –Т–ї–Є—П–љ–Є–µ –љ–∞ —З–∞—Б—В–Њ—В—Г –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Є–љ—Б—Г–ї—М—В–Њ–≤ —Б–Њ —Б–Љ–µ—А—В–µ–ї—М–љ—Л–Љ –Є—Б—Е–Њ–і–Њ–Љ –Є–ї–Є –±–µ–Ј –≤ –≥—А—Г–њ–њ–∞—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞ (–Ъ–†=0,69; 95% –Ф–Ш 0,45–1,06 –њ—А–Є p=0,09; –Є –Ъ–† =0,76; 95% –Ф–Ш 0,53–1,08 –њ—А–Є p=0,13, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) –±—Л–ї–Њ –≤—Л—А–∞–ґ–µ–љ–Њ –≤ —А–∞–≤–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є (–≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М p=0,73; —А–Є—Б. 5).
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Т –±–Њ–ї–µ–µ —А–∞–љ–љ–Є—Е –Њ—В—З–µ—В–∞—Е –њ–Њ ASCOT–BPLA –і–µ–ї–∞–ї–Є—Б—М –њ–Њ–њ—Л—В–Ї–Є –Њ—Ж–µ–љ–Є—В—М, –Љ–Њ–ґ–љ–Њ –ї–Є –Њ–±—К—П—Б–љ–Є—В—М —А–∞–Ј–љ–Є—Ж—Г –≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б—В—А–∞—В–µ–≥–Є–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—В–ї–Є—З–Є—П–Љ–Є –≤ —Г—А–Њ–≤–љ–µ –Р–Ф –Є –і—А—Г–≥–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ–≤–Њ—Ж–Є—А—Г–µ—В –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–µ –њ–Њ—Б–ї–µ —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є –ї–µ—З–µ–љ–Є–µ [5]. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –љ–µ–і–Њ—З–µ—В—Л, —А–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ, –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ, –Њ—В—З–∞—Б—В–Є —А–∞–Ј–љ–Є—Ж–∞ –њ–Њ —З–∞—Б—В–Њ—В–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Н–њ–Є–Ј–Њ–і–Њ–≤ –Ш–С–° –Є –Є–љ—Б—Г–ї—М—В–∞ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –Є–Ј––Ј–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Г—А–Њ–≤–љ—П –Њ—Б—В–∞–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, –њ–Њ–Љ–Є–Љ–Њ –Р–Ф (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ы–Я–Т–Я). –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Њ–і–љ–∞–Ї–Њ, —З—В–Њ —Н—В–Њ –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–Њ –Є –Ї–∞–Ї–Є–Љ–Є–—В–Њ –і—А—Г–≥–Є–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є. –Т —Е–Њ–і–µ —Н—В–Њ–≥–Њ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ –Ј–∞–і–∞–љ–љ–Њ–є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М—О –Є–Ј—Г—З–∞–ї–Є—Б—М –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –і–≤—Г—Е —А–∞–Ј–љ—Л—Е –≥—А—Г–њ–њ–∞—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Б —В–µ–Љ, —З—В–Њ–±—Л –њ–Њ–љ—П—В—М, –Љ–Њ–ґ–љ–Њ –ї–Є —Б—З–Є—В–∞—В—М —А–∞–Ј–љ–Є—Ж—Г —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –≤ —Е–Њ–і–µ ASCOT–BPLA, —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Є –Љ–µ–ґ–і—Г –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є –Є –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–µ–є.
–Х—Б–ї–Є —Б—А–∞–≤–љ–Є–≤–∞—В—М —Б –њ–ї–∞—Ж–µ–±–Њ, –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —А–Є—Б–Ї–∞ —Б–Њ–±—Л—В–Є–є –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є (–Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –±–µ–Ј —Б–Љ–µ—А—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ –Є–ї–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–∞—П —Б–Љ–µ—А—В—М) –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –Њ–Ї–∞–Ј–∞–ї—Б—П –≤—Л—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –∞—В–µ–љ–Њ–ї–Њ–ї–∞. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ—Л —В–Њ—А–Љ–Њ–Ј—П—В —А–∞–Ј–≤–Є—В–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ [6], –∞ –њ–Њ –і–∞–љ–љ—Л–Љ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є, –∞–љ—В–Є–∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –Њ–±–ї–∞–і–∞—О—В –Є –±–ї–Њ–Ї–∞—В–Њ—А—Л –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ [7,8]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Б–љ–Є–ґ–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —П–≤–ї–µ–љ–Є–є –±–ї–∞–≥–Њ–і–∞—А—П –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ, –љ–µ —Б–≤—П–Ј–∞–љ–љ—Л–Љ —Б –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ –Р–Ф [9,10], –Ї —В–Њ–Љ—Г –ґ–µ –≤ —Е–Њ–і–µ –Њ–і–љ–Њ–≥–Њ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ –≤ –њ–Њ–ї—М–Ј—Г –Є—Е —Б–Є–љ–µ—А–≥–Є–Є —Б–Њ —Б—В–∞—В–Є–љ–∞–Љ–Є [11].
–Ґ–Њ—В —Д–∞–Ї—В, —З—В–Њ –Њ—Б–љ–Њ–≤–Њ–є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–є —Б–Є–љ–µ—А–≥–Є–Є —П–≤–ї—П–µ—В—Б—П –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –Љ–µ–ґ–і—Г —Б—В–∞—В–Є–љ–∞–Љ–Є –Є –і–Є–≥–Є–і—А–Њ–њ–Є—А–Є–і–Є–љ–Њ–≤—Л–Љ–Є –±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤, –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –љ–∞–ї–Є—З–Є–µ–Љ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ –њ–µ—А–≤—Л–µ 3 –Љ–µ—Б—П—Ж–∞ –Њ—В –љ–∞—З–∞–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В–µ—А–∞–њ–Є–Є (p=0,02) [12, –љ–µ–Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л–µ –і–∞–љ–љ—Л–µ]. –Ч–∞ —Н—В–Њ –≤—А–µ–Љ—П –Љ–µ–љ—М—И–µ–є —З–∞—Б—В–Є –±–Њ–ї—М–љ—Л—Е –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –і–Њ–±–∞–≤–Є—В—М –Ї –ї–µ—З–µ–љ–Є—О –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –љ–∞–ї–Є—З–Є–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ –Є —Б—В–∞—В–Є–љ–∞–Љ–Є –і–Њ–Ї–∞–Ј–∞–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є –љ–∞ –Ї–ї–µ—В–Њ—З–љ–Њ–Љ –Є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–Љ —Г—А–Њ–≤–љ–µ [13,14].
–Ш–љ—В–µ—А–њ—А–µ—В–Є—А—Г—П –∞—А–≥—Г–Љ–µ–љ—В—Л –≤ –њ–Њ–ї—М–Ј—Г —Б–Є–љ–µ—А–≥–Є–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ, —З—В–Њ –Њ–љ–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –ї–Є—И—М —Б–ї–µ–і—Б—В–≤–Є–µ–Љ —Б–ї—Г—З–∞–є–љ—Л—Е —Б–Њ–≤–њ–∞–і–µ–љ–Є–є. –ѓ–≤–љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є—П –Љ–µ–ґ–і—Г —Н—Д—Д–µ–Ї—В–∞–Љ–Є –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –њ–µ—А–≤–Є—З–љ—Л—Е –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї –≤ –≥—А—Г–њ–њ–∞—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –љ–∞—Е–Њ–і–Є–ї–∞—Б—М –≤ –≥—А–∞–љ–Є—Ж–∞—Е —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –і–ї—П —В—А–µ—В–Є—З–љ—Л—Е –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї (p=0,025). –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –∞–Љ–ї–Њ–і–Є–њ–Є–љ –Є –∞—В–µ–љ–Њ–ї–Њ–ї –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –Є–љ—Б—Г–ї—М—В–Њ–≤ –Є –≤—Б–µ—Е –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —П–≤–ї–µ–љ–Є–є –Є–ї–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ. –Ю–і–љ–∞–Ї–Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј –Є–љ—Б—Г–ї—М—В–∞ –Є –Ш–С–° –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤. –Х—Б–ї–Є —Б—А–∞–≤–љ–Є–≤–∞—В—М —Б –њ–ї–∞—Ж–µ–±–Њ, —В–Њ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ –≤–ї–Є—П–ї –љ–∞ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Є –Ы–Я–Э–Я. –†–∞–Ј–љ–Є—Ж—Г –Љ–µ–ґ–і—Г —Б–Њ–±—Л—В–Є—П–Љ–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї –љ–µ–ї—М–Ј—П –Њ–±—К—П—Б–љ–Є—В—М –љ–µ–Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —В–Є—В—А–Њ–≤ –Ы–Я–Т–Я –Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –±–Њ–ї–µ–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ (–њ—А–Є –µ–≥–Њ –љ–∞–ї–Є—З–Є–Є) –њ—А–µ–њ–∞—А–∞—В –Њ–Ї–∞–Ј—Л–≤–∞–ї –≤ –≥—А—Г–њ–њ–µ –∞—В–µ–љ–Њ–ї–Њ–ї–∞ (—В–∞–±–ї. 2). –Э–µ –≤—Л—П–≤–ї–µ–љ–Њ –Є —П–≤–љ–Њ–є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Є –Љ–µ–ґ–і—Г –≤–ї–Є—П–љ–Є–µ–Љ –≥–Є–њ–Њ–ї–Є–њ–Є–і–µ–Љ–Є—З–µ—Б–Ї–Њ–є –Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞ —Г—А–Њ–≤–µ–љ—М –Р–Ф.
–°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ю–±—К–µ–і–Є–љ–µ–љ–љ–Њ–≥–Њ –њ—А–Њ–µ–Ї—В–∞ –њ–Њ –њ—А–∞–≤–∞—Б—В–∞—В–Є–љ—Г, –Њ–±–Њ–±—Й–Є–≤—И–µ–≥–Њ –і–∞–љ–љ—Л–µ —В—А–µ—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –њ—А–∞–≤–∞—Б—В–∞—В–Є–љ–∞ –Ї–∞–Ї –≥–Є–њ–Њ—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ [15], —Г –ї–Є—Ж, –љ–∞—Е–Њ–і—П—Й–Є—Е—Б—П –љ–∞ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ї –Љ–Њ–Љ–µ–љ—В—Г –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Н–њ–Є–Ј–Њ–і–Њ–≤ –Ш–С–° –±—Л–ї–Њ –≤—Л—А–∞–ґ–µ–љ–Њ –≤ –≥–Њ—А–∞–Ј–і–Њ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –±–Њ–ї—М–љ—Л–Љ–Є, –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є–Љ–Є —В–∞–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–љ–∞ 14 –Є 33%, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ; –≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М p=0,003). –Ю–і–љ–∞–Ї–Њ —А–∞–Ј—А–∞–±–Њ—В—З–Є–Ї–∞–Љ –њ—А–Њ–µ–Ї—В–∞ –љ–µ —Г–і–∞–ї–Њ—Б—М –і–Њ–Ї–∞–Ј–∞—В—М —Б–≤—П–Ј—М —Н—В–Є—Е –Њ—В–ї–Є—З–Є–є —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Ї–∞–Ї–Њ–≥–Њ––ї–Є–±–Њ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –Т —Е–Њ–і–µ –Ї—А—Г–њ–љ–Њ–Љ–∞—Б—И—В–∞–±–љ–Њ–≥–Њ –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ј–∞—Й–Є—В—Л —Б–µ—А–і—Ж–∞ (HPS) –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ –≤ –µ–ґ–µ–і–љ–µ–≤–љ–Њ–є –і–Њ–Ј–µ 40 –Љ–≥ –≤—Л–Ј—Л–≤–∞–µ—В –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є–ї–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Љ–µ—А—В–Є –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–≥–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П [16]. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –≤ –≥—А—Г–њ–њ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –±–ї–Њ–Ї–∞—В–Њ—А—Л –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ –љ–∞ –Љ–Њ–Љ–µ–љ—В —Б—В–∞—А—В–∞ –Є—Б–њ—Л—В–∞–љ–Є–є –Є –≤ –≥—А—Г–њ–њ–µ –љ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–≤—И–Є—Е —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–∞—П —З–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –∞–Љ–≤–∞—Б—В–∞—В–Є–љ–Њ–Љ —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ (–љ–∞ 25 –Є 30% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ; –≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М χ2/1=0,41), –∞ –µ—Б–ї–Є —А–∞–Ј–љ–Є—Ж–∞ –Є –љ–∞–±–ї—О–і–∞–ї–∞—Б—М, —В–Њ –Њ–љ–∞ –±—Л–ї–∞ –≤ –њ–Њ–ї—М–Ј—Г –њ–µ—А–≤–Њ–є –Ї–Њ–≥–Њ—А—В—Л –±–Њ–ї—М–љ—Л—Е (40 –Є 24% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ; –≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ—Б—В—М χ2/1=5,8). –Т –і–Њ–Ї–ї–∞–і–µ –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –≥—А—Г–њ–њ—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –њ–Њ –ї–µ—З–µ–љ–Є—О —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ (–°–Ґ–Ґ), –њ—А–Њ–≤–µ–і—И–µ–є –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ 14 –Ї—А—Г–њ–љ–Њ–Љ–∞—Б—И—В–∞–±–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є —Б—В–∞—В–Є–љ–Њ–≤, –љ–µ—В —Г–Ї–∞–Ј–∞–љ–Є–є –љ–∞ —В–Њ, —З—В–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—В –Ї–∞–Ї–Є–µ–—В–Њ –Њ—В–ї–Є—З–Є—П –њ–Њ —З–∞—Б—В–Њ—В–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –Є –і—А—Г–≥–Є—Е —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ—А–Њ–≤–µ–і–µ–љ–Є—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Є–ї–Є –µ–≥–Њ –Њ—В—Б—Г—В—Б—В–≤–Є—П [2].
–†–µ–Ј—Г–ї—М—В–∞—В—Л ASCOT–BPLA –Є —А—П–і–∞ –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [17–20] —Б—В–∞–≤—П—В –њ–Њ–і —Б–Њ–Љ–љ–µ–љ–Є–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П β––±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤ –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –°–°–Ч, —Е–Њ—В—П –і–ї—П —Ж–µ–ї–µ–є –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –°–°–Ч –Є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Њ–љ–Є –њ–Њ––њ—А–µ–ґ–љ–µ–Љ—Г –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л. –Ь–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ –љ–∞ —З–∞—Б—В–Њ—В—Г –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —П–≤–ї–µ–љ–Є–є (ASCOT–LLA) –њ–Њ–і–љ–Є–Љ–∞–µ—В –≤–Њ–њ—А–Њ—Б –Њ —В–Њ–Љ, –љ–µ —Б–љ–Є–ґ–∞–µ—В—Б—П –ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О —Б—В–∞—В–Є–љ–Њ–≤ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П β––±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є (–Є–ї–Є –і–∞–ґ–µ –і–Є—Г—А–µ—В–Є–Ї–∞–Љ–Є). –Ю–і–љ–∞–Ї–Њ –і–∞–љ–љ—Л–µ –њ–Њ —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ—Г –Є –і—А—Г–≥–Є–Љ —Б—В–∞—В–Є–љ–∞–Љ, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ HPS –Є –°–Ґ–Ґ, –љ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В —Н—В–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, –Є –њ–Њ—Н—В–Њ–Љ—Г —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —В–Њ–≥–Њ, —З—В–Њ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –∞—В–µ–љ–Њ–ї–Њ–ї–Њ–Љ, –љ–∞–±–ї—О–і–∞–µ–Љ–Њ–µ –≤ —Е–Њ–і–µ ASCOT–LLA, –≤—Б–µ –ґ–µ —П–≤–ї—П–µ—В—Б—П —Б–ї–µ–і—Б—В–≤–Є–µ–Љ —Б–ї—Г—З–∞–є–љ–Њ—Б—В–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–µ–ґ–і—Г –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ –ї–µ—З–µ–љ–Є–µ–Љ –Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —Б—В–∞—В–Є–љ–Њ–≤ —Б—Г—Й–µ—Б—В–≤—Г–µ—В –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є—П. –Ш —Е–Њ—В—П –њ—А–Є–≤–µ–і–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –Љ–Њ–≥—Г—В –±—Л—В—М –≤—Б–µ–≥–Њ –ї–Є—И—М —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ —Б–ї—Г—З–∞–є–љ—Л—Е —Б–Њ–≤–њ–∞–і–µ–љ–Є–є (—З—В–Њ –µ—Й–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–Њ–Ї–∞–Ј–∞—В—М), –Љ—Л –њ–Њ–ї–∞–≥–∞–µ–Љ, —З—В–Њ –≤—Б–µ –ґ–µ –і–Њ–ї–ґ–љ—Л —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞—В—М —Г–±–µ–і–Є—В–µ–ї—М–љ—Л–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –≤ –њ–Њ–ї—М–Ј—Г —Н—В–Њ–є –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –љ–∞ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–Љ —Г—А–Њ–≤–љ–µ. –≠—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є—В –њ–Њ–љ—П—В—М, –њ–Њ—З–µ–Љ—Г –Њ–њ–Є—Б–∞–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Њ—П–≤–ї—П—О—В—Б—П –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —З–∞—Б—В–Њ—В—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Б–Њ–±—Л—В–Є–є –Ш–С–°, –∞ –љ–µ –і—А—Г–≥–Є—Е –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї, –њ–∞—В–Њ–≥–µ–љ–µ–Ј –Ї–Њ—В–Њ—А—Л—Е –±–Њ–ї–µ–µ —Б–ї–Њ–ґ–µ–љ.
–†–µ—Д–µ—А–∞—В –њ–Њ–і–≥–Њ—В–Њ–≤–ї–µ–љ –Х.–С. –Ґ—А–µ—В—М—П–Ї
–њ–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ —Б—В–∞—В—М–Є
P. Sever, B. Dahlof, H. Wedel et al.
«Potential synergy between lipid–lowering
and blood–pressure–lowering
In the Anglo–Scandinavian
Cardiac Outcomes Trial»
European Heart Journal, 2006, 27: 2982–2988



–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Sever PS, Dahlof B, Poulter NR, Wedel H, Beevers G, Caulfield M, Collins R, Kjeldsen SE, Kristinsson A, McInnes GT, Mehlsen J, Nieminen M, O’Brien E, Ostergren J, for the ASCOT investigators. Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower–than–average cholesterol concentrations, in the Anglo–Scandinavian Cardiac Outcomes Trial–Lipid Lowering Arm (ASCOT–LLA): a multicentre randomised controlled trial. Lancet 2003;361:1149–1158.
2. Cholesterol Treatment Trialists’ (CTT) Collaboration. Efficacy and safety of cholesterol–lowering treatment: prospective meta–analysis of data from 90,056 participants in 14 randomised trials of statins. Lancet 2005; 366:1267–1278.
3. Sever PS, Dahlo?f B, Poulter NR, Wedel H, Beevers G, Caulfield M, Collins R, Kjeldsen SE, McInnes GT, Mehlsen J, Nieminen M, O’Brien E, O?stergren J, for the ASCOT investigators. Rationale, design, methods and baseline demography of participants of the Anglo–Scandinavian Cardiac Outcomes Trial. J Hypertens 2001;6:1139–1147.
4. Dahlo?f B, Sever PS, Poulter NR, Wedel H, Beevers DG, Caulfield M, Collins R, Kjeldsen SE, Kristinsson A, McInnes GT, Mehlsen J, Nieminen M, O’Brien E, O?stergren J, for the ASCOT Investigators. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo–Scandinavian Cardiac Outcomes Trial–Blood Pressure Lowering Arm (ASCOT–BPLA): a multicentre randomised controlled trial. Lancet 2005;366:895–906.
5. Poulter NR, Wedel H, Dahlo?f B, Sever PS, Beevers DG, Caulfield M, Kjeldsen SE, Kristinsson A, McInnes GT, Mehlsen J, Nieminen M, O’Brien E, O?stergren J, Pocock S, for the ASCOT Investigators. Role of blood pressure and other variables in the differential cardiovascular event rates noted in the Anglo–Scandinavian Cardiac Outcomes Trial–Blood Pressure Lowering Arm (ASCOT–BPLA). Lancet. 2005;366:907–913.
6. Henry PD. Calcium channel blockers and atherosclerosis. J Cardiovasc Pharmacol 1990;16(Suppl.) 1):S12–S15.
7. Lichtlen PR, Hugenholtz PG, Rafflenbeul W, Hecker H, Jost S, Deckers JW. Retardation of angiographic progression of coronary artery disease by nifedipine. Results of the International Nifedipine Trial on Antiatherosclerotic Therapy (INTACT). INTACT Group Investigators. Lancet 1990;335:1109–1113.
8. Nissen SE, Murat Tuzcu E, Libby P, Thompson PD, Ghali M, Garza D. Effect of antihypertensive agents on cardiovascular events in patients with coronary disease and normal blood pressure. The CAMELOT Study: a randomised controlled trial. JAMA 2004;292:2217–2225.
9. Verdecchia P, Reboldi G, Angeli F, Gattobigio R, Bentivoglio M, Thijs L, Staessen JA, Porcellati C. Angiotensin–converting enzyme inhibitors and calcium channel blockers for coronary heart disease and stroke prevention. Hypertension 2005;46:386–392.
10. Sever PS, Poulter NR. Blood pressure reduction is not the only determinant of outcome. Circulation 2006;113:2754–2774.
11. Athyros VG, Mikhailidis DP, Papageorgiou AA, Bouloukos VI, Pehlivanidis AN, Symeonidis AN, GREACE Study Collaborative Group. Effect of statins and ACE inhibitions alone and in combination on clinical outcome in patients with coronary heart disease. J Hum Hypertens 2004;11:781–788.
12. Sever PS. Lipid–lowering therapy and the patient with multiple risk factors: what have we learned from the Anglo–Scandinavian Cardiac Outcomes Trial (ASCOT)? Am J Med 2005;118(Suppl. 12A):3S–9S.
13. Munro E, Patel M, Chan P, Betteridge L, Clunn G, Gallagher K, Hughes A, Schachter M, Wolfe J, Sever P. Inhibition of human vascular smooth muscle cell proliferation by lovastatin: the role of isoprenoid intermediates of cholesterol synthesis. Eur J Clin Invest 1994;24:766–772.
14. Preston Mason R, Walter MF, Day CA, Jacob RF. Intermolecular differences of 3–hydroxy–3–methylglutaryl coenzyme A reductase inhibitors contribute to distinct pharmacologic and pleiotropic action. Am J Cardiol 2005; 96(Suppl.):11F–23F.
15. Sacks FM, Tonkin AM, Shepherd J, Braunwald E, Cobbe S, Morton Hawkins C, Keech A, Packard C, Simes J, Byington R, Furberg CD. Effect of pravastatin on coronary disease events in subgroups defined by coronary risk factors: The Prospective Pravastatin Pooling Project. Circulation 2000;102:1893–1900.
16. Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol–lowering with simvastatin in 5963 people with diabetes: a randomised placebo–controlled trial. Lancet 2003;361:2005–2015.
17. Medical Research Council trial of treatment of mild hypertension: principal results. Medical Research Council Working Party. BMJ 1985;291:97–104.
18. Medical Research Council trial of treatment of hypertension in older adults: principal results. MRC Working Party. BMJ 1992;304:405–412.
19. Neumann BI, Montero LJ, Carlberg B, Samuelsson O, Lindholm L. Critical appraisal: Should atenolol be the first choice for primary hypertension? Atenolol in hypertension: is it a wise choice? Lancet 2004;364:1684–1689.
20. Beevers DG. The end of beta blockers for uncomplicated hypertension? Lancet 2005;366:1510–1512.








.gif)



