Крупнейшее российское эпидемиологическое исследование ЭПОХА-ХСН, выполненное в 8 регионах страны и включившее в себя 19 500 респондентов, впервые позволило определить распространенность ХСН в нашей стране.
ЭПОХА-О-ХСН [2] – одномоментное госпитальное исследование в 22 регионах РФ (n=6884), которое выявило, что распространенность ХСН в стране составляет 7%, это соответствует 7,9х106 пациентов. Клинически манифестировавшая ХСН выявлена у 4,5% населения, что соответствует 5,1х106 человек. Для рассматриваемого в этой статье вопроса гораздо важнее знать уровень встречаемости III–IV ФК (NYHA) ХСН. Именно эта когорта пациентов является основным источником для госпитализаций по поводу декомпенсации ХСН. Результаты эпидемиологических исследований показали, что встречаемость III–IV ФК (NYHA) ХСН в РФ составляет 2,1%, что соответствует 2,4х106 человек. Декомпенсация кровообращения стала причиной госпитализации в кардиологические и терапевтические стационары в 4,9% всех случаев, а ХСН включалась в диагноз в 92% всех случаев.
Крупнейшее европейское исследование EHFS II [3], включившее в себя в 30 странах Европы 3580 пациентов, выявило, что в течение 2005 г. причинами госпитализаций стали: впервые возникший синдром острой декомпенсации (de novo) – 37%; декомпенсация кровообращения – 65%; отек легких – 16%; кардиогенный шок – 4%; правожелудочковая недостаточность – 3%. Митральная регургитация отмечена у 80% пациентов. Госпитальная летальность составила 6,7%.
Главный вывод эпидемиологических исследований:
• госпитализации по поводу ХСН доминируют в современных стационарах;
• факт госпитализации является независимым фактором увеличения риска смертности у пациентов с ХСН;
• новый параметр, выявленный в ходе исследований – частота повторных госпитализаций, рассматривается в настоящее время как новый, независимый прогностический фактор.
В ходе анализа результатов эпидемиологических исследований пришло осознание того факта, что исходы у стабильных амбулаторных больных с ХСН и пациентов, перенесших хотя бы одну госпитализацию по поводу декомпенсации ХСН, – принципиально разнятся. Сам факт госпитализации, и тем более повторной госпитализации, достоверно повышает риск смерти пациента, что стало основанием для разработки новой цели в лечении больных ХСН – снижения числа повторных госпитализаций (до этого периода главной целью в лечении ХСН провозглашалось только снижение риска смерти).
Хорошо известно, что с 1991 по 2011 г. смена главного принципа лечения ХСН у амбулаторных пациентов с использования мочегонных + нитратов + положительных ионотропных препаратов на лечение, основанное на применении иАПФ, β-блокаторов и антагонистов рецепторов минералокортикоидов, привела к снижению риска смерти на 59%. На фоне этого успеха следует констатировать, что у больных с декомпенсированным течением ХСН, потребовавших госпитализации, смертность и повторная госпитализация составили соответственно 15 и 30%. Более того, на ранний прогноз после выписки из стационара традиционные препараты оказывают влияние, отличное от аналогичного влияния на прогноз стабильных амбулаторных пациентов.
Так, в работе G.C. Fonarow [7] были проанализированы данные 5791 пациента в 91 клинике США, госпитализированных по поводу декомпенсации ХСН. Госпитальная летальность составила 8,6%, частота повторных госпитализаций в интервале 60–90 дней – 36,2%. Тяжесть состояния в момент госпитализации не коррелировала со смертностью после выписки. Выраженное положительное влияние на прогноз после выписки оказали иАПФ. β–блокаторы обладали меньшим влиянием. Клиницисту важно понимать, что первая, вторая и последующая госпитализации вслед за синдромом острой декомпенсации оказывают разное по величине, но неуклонно возрастающее негативное прогностическое влияние.
В наблюдательном исследовании S. Setoguchi [4] установил, что 895 пациентов с диагнозом ХСН за 4,7 года имели 4359 госпитализаций. Из них 17% (713) госпитализаций были связаны с декомпенсацией ХСН. Всего 69% пациентов были госпитализированы после выписки из стационара за последний год. В течение 2 мес. регоспитализированы 30%, 3 мес. – 27%, 6 мес. – 38%, что означает, что риск смерти значимо возрастает с каждой последующей регоспитализацией. В другом наблюдательном исследовании из 14 374 пациентов, выписанных после госпитализации по поводу декомпенсации ХСН, до 4-й регоспитализации дожили 417 пациентов [5].
Таким образом, в современных клинических исследованиях сформировался новый параметр анализа эффективности лечения: частота и срок наступления повторной госпитализации после выписки из стационара по поводу декомпенсации ХСН. Этот же параметр рекомендован врачу первичного звена в качестве интегрального критерия комплаентности пациента и эффективности индивидуального плана лечения ХСН у конкретного пациента.
Каковы особенности пациентов,
госпитализируемых по поводу
декомпенсации кровообращения?
Как уже упоминалось, доля госпитализированных пациентов с ухудшением клинической картины ХСН составляет 80%, а с впервые возникшей недостаточностью – 15%.
Большинство госпитализированных пациентов не имеют признаков тяжелой декомпенсации и быстро отвечают на лечение. Это пациенты, отвечающие критериям «сухой–теплый», в противовес пациентам с выраженной клинической картиной, отвечающие критериям «мокрый–холодный» [6]. Терминами «сухой–мокрый» качественно отмечен застой в малом круге кровообращения. «Сухой» – означает отсутствие влажных хрипов, «мокрый» – наличие влажных симметричных хрипов. Термины «теплый»–«холодный» оценивают выраженность гипоперфузии периферических тканей. Так, «холодный» подразумевает наличие холодного диффузного цианоза, сочетающегося с плотными симметричными отеками, «теплый» – наличие адекватной перфузии тканей. Сочетание «влажный» + «холодный» самое неблагоприятное. Пациенты с такой характеристикой, как правило, имеют сниженную ФВ ЛЖ, снижение СКФ, высокий уровень ЧСС, высокое число дыхательных движений и низкое АД [7]. Анализ когорты больных с выраженной симптоматикой показал, что суммарная госпитальная смертность составляет 7%, однако она значимо возрастает до 20% у больных с низкой СКФ.
В исследовании EVEREST [13–15] 40% летальных исходов после выписки было обусловлено очередной декомпенсацией кровообращения, а 30% – внезапной смертью.
В 1993 г. 18% всех регоспитализаций происходило до 30-го дня после выписки; в 2005 г. этот параметр составил 20%.
Таким образом, ни смертность, ни ранние повторные госпитализации за 22 года не изменили свою выраженность. Следует признать, что отдельные результаты (частота повторных госпитализаций) за этот период вообще не изучались в клинических исследованиях как первичная конечная точка.
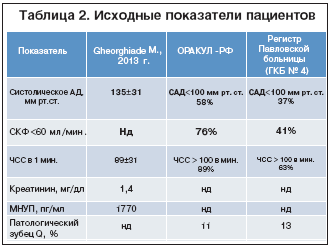
Представляет особый интерес сравнение анамнестических клинических параметров у госпитализируемых в стационар по поводу декомпенсации кровообращения. В представленном материале проанализированы следующие базы данных: регистр, сформированный под руководством M. Gheorghiade (n=20118) [7], регистр Павловской больницы Москвы (n=617), регистр ОРАКУЛ (РФ) (n=2496). Сравнительный анализ представлен в таблицах 1–4. Данные таблиц показывают, что пациенты, госпитализируемые в стационар в РФ, имеют существенно более тяжелое течение ХСН. Так, 72% больных в регистре M. Gheorghiade [7] имели в течение предшествующего года 1 госпитализацию, 53% в исследовании ОРАКУЛ – ≥2 госпитализаций. Среди больных ФВ <40% в исследовании ОРАКУЛ встречалась в 1,89 раза чаще, чем в цитируемом регистре [7].
Таким образом, большее число пациентов, госпитализированных в РФ, соответствуют критерию «мокрый–холодный» и имеют меньшую ФВ, СКФ, меньшую приверженность научно-обоснованному лечению и большее ЧСС.
Другой особенностью российской популяции было большое количество пневмоний в момент госпитализации пациента с декомпенсацией ХСН. Спектр бактериальной флоры у этих пациентов не соответствует классическому спектру внегоспитальной пневмонии. Значительный процент в спектре флоры занимает флора, типичная для госпитальной пневмонии. Факт пневмонии оказывал негативное влияние на уровень СКФ, снижая в среднем на 5,6 мл/мин. и повышая ФК ХСН в период после выписки. Важно отметить, что старт антибактериальной терапии происходил с задержкой на 72 ч от дебюта симптоматики декомпенсации, что было связано с трудностью распознавания пневмонии на фоне застоя в малом круге кровообращения.
Прогностические маркеры
повторных госпитализаций
Первая прогностическая многофакторная модель была выведена в ходе исследования OPTIMIZE-HF. В этом регистре исследовалось 19 параметров с целью выявить факторы, определяющие вероятность регоспитализаций в течение 60–90 дней после выписки. Анализ 4402 пациентов (10% от включенных в регистр) показал, что 29,6% (n=1715 пациентов) были регоспитализированы в течение 90 дней после выписки. Самыми мощными предикторами комбинированного показателя «смерть + регоспитализация» (в ходе наблюдения умер 481(8,6%) пациент) были: уровень креатинина в момент госпитализации, систолическое АД менее 120 мм рт.ст., уровень гемоглобина, регулярный прием иАПФ в момент выписки, наличие ХОБЛ [8].
В рамках этого же регистра анализ данных 48 612 пациентов из 259 стационаров США показал, что наличие ИБС в момент госпитализации проводило к росту госпитальной (3,7% против 2,9%) и постгоспитальной смертности – 10,6% против 6,9%. Причем этот показатель был одинаковым у лиц с сохраненной ФВ и ФВ <40%. Наличие реваскуляризации не улучшало прогноз [9]. В рамках этого же регистра анализ уровня в момент госпитализации показал, что пациенты с уровнем Na+ <135 ммоль/л и >135 ммоль/л имеют различный прогноз. Так, риск госпитальной и постгоспитальной смерти возрастал соответственно на 19 и 10%, а риск развития комбинированного показателя смерть + регоспитализация – на 8% при снижении уровня Na+ на каждые 3 ммоль/л ниже уровня 140 ммоль/л [10].
Первым, кто обратил внимание на ухудшение функции почек у больных с ХСН еще в 1946 г., был Arthur Merril [11]. Он описал снижение плазмотока через почку на 1/3 у больных с недостаточностью кровообращения и снижением сердечного выброса на 50%. Несмотря на такое снижение плазмотока, СКФ снижалась существенно меньше. Этот феномен получил название почечного парадокса и объясняется развитием внутриклубочковой гипертензии и увеличением фильтрации. Следует пояснить, что такое изменение с современной точки зрения обусловлено гиперактивацией РААС, что помимо внутриклубочковой гипертензии приводит к увеличению ретенции Na+, а, следовательно, к увеличению ОЦК. Прогноз при снижении СКФ ниже 60 мл/мин. значительно ухудшается [7, 12].
В рамках исследования EVEREST [13] было определено влияние продолжительности комплекса QRS на госпитальную и постгоспитальную смертность. Из 2962 включенных в исследование у 1321 длительность QRS была более 120 мс. Смертность в когорте больных с длительностью QRS менее 120 мс и более 120 мс была 18,7 и 28,1% соответственно. Эта же тенденция сохранилась до 9 мес.
Анализ клинической картины [14] пациентов, включенных в исследование EVEREST, показал, что такие параметры, как увеличение массы тела, признаки застоя, тахикардия являются неблагоприятными маркерами, увеличивающими вероятность регоспитализации. Так, из 635 повторных госпитализаций за 60 дней в исследовании EVEREST 184 были у пациентов с прибавкой в весе менее 2 кг и 401 – более 2 кг. Следует помнить, что даже отсутствие симптомов застоя при выписке не исключает плохой прогноз. Так, post hoc анализ исследования EVEREST показал, что в популяции больных 0 баллов (по 3-балльной шкале – отеки ног, ортопноэ, набухание вен шеи) при выписке показатель смертности за 9,9 мес. равен 19,1%, а регоспитализации – 26,2% [15].
Так, анализ ряда параметров через 1 нед. после стабилизации состояния показал, что наличие отеков, тахикардии, влажных хрипов и анемии резко увеличивает вероятность регоспитализации.
Группа исследователей, выполнивших исследование OPTIMIZE-HF [8], предложила учитывать факторы, ускоряющие регоспитализацию, выделив пять дополнительных факторов:
1) миокардиальные, включающие в себя ишемию миокарда, фибрилляцию предсердий, неконтролируемую АГ, стойкую тахикардию;
2) немиокардиальные факторы – обострение ХОБЛ, инфекции;
3) личностные особенности – низкая комплаентность, несоблюдение диеты, злоупотребление алкоголем, курение;
4) ятрогенные факторы – назначение НПВП;
5) системные факторы – в первую очередь, отсутствие преемственности в ведении пациента. Анализ популяции российских пациентов позволил отметить негативное влияние крайне низкой комплаентности и инфекции.
Ведущий кардиологический механизм,
приводящий к повторным госпитализациям
Основной причиной повторной госпитализации является застой, а не низкая ФВ. Высокий уровень давления заполнения ЛЖ развивается в результате формирования порока сердца, инфаркта миокарда, тахикардии, приводящих к сокращению диастолы. Как правило, повышение давления заполнения начинает развиваться задолго до декомпенсации кровообращения, т.е. в отсутствие клинических симптомов одышки, периферических отеков, однако сам факт повышения давления приводит к развитию субэндокардиальной ишемии, изменяет геометрию ЛЖ, усиливает митральную регургитацию, активизирует РААС и усиливает застой в легочных венах. Уровень давления заполнения коррелирует с уровнем мозгового натрийуретического пептида. Очевидно, что снижение ЧСС и удлинение диастолы приводят к снижению давления заполнения. Таким образом, «гемодинамический» застой предшествует клиническому и требует раннего выявления и коррекции. Лечащий врач уже с первых часов контакта с пациентом может применить шестифакторную модель для оценки тяжести состояния пациента:
1) тяжесть клинического состояния;
2) СН de novo;
3) ХСН;
4) АД;
5) сопутствующие заболевания;
6) ЧСС. Чем больше баллов, тем вероятнее госпитализация или летальный исход.
Пути коррекции застоя:
• Центральным механизмом в коррекции содержания жидкости в организме остается комплекс мер по снижению потребления NaCl и прием мочегонных препаратов (петлевых диуретиков). Применение мочегонных препаратов ухудшает функцию клубочка, в этой связи целесообразно применять их вместе с иАПФ.
• Применение антагонистов рецепторов минералокортикоидов существенно снижает число повторных госпитализаций.
• Вопросы воздействия на коронарные артерии решаются всегда индивидуально на основе анализа распространенности зон гибернации.
• Клапанные пороки должны быть устранены хирургически.
• Жесткий контроль АД обязателен.
• Контроль ХОБЛ, уровня глюкозы крови обязателен.
• Обязательность обучения пациента.
Контроль ЧСС как один
из эффективных путей снижения
риска повторных госпитализаций
Основные данные, подтверждающие влияние ЧСС на количество госпитализаций, были получены в рамках исследования SHIFT. Это исследование было рандомизированным двойным слепым плацебо-контролируемым клиническим в параллельных группах с участием пациентов с синусовым ритмом и умеренной или тяжелой систолической дисфункцией левого желудочка. В исследование включены 6505 пациентов из 37 стран (677 медицинских центров), которые были рандомизированы в группы плацебо или ивабрадина (стартовая доза 5 мг 2 раза/сут. с последующим титрованием до 7,5 или 2,5 мг 2 раза/сут. либо отменой препарата в зависимости от ЧСС и переносимости лечения).
В исследование включали мужчин или женщин в возрасте ≥18 лет, имевших стабильную симптоматику ХСН давностью ≥4 нед. с фракцией выброса левого желудочка (ФВЛЖ) ≤35%, имевших госпитализации в связи с ухудшением СН за предыдущие 12 мес. и синусовым ритмом с ЧСС в покое ≥70 уд./мин. (по данным электрокардиографии в 12 отведениях на двух последовательных визитах). Все пациенты получали научно-обоснованное базовое лечение ХСН. Если пациент не получал β-адреноблокатор или получал его в дозе меньшей, чем рекомендуемая в руководствах, то перед включением в исследование предпринимались попытки титрации дозы на повышение. В случаях, когда на максимально переносимой дозе β-адреноблокатора ЧСС превышала 70 уд./мин., пациент включался в исследование.
Первичной конечной точкой в исследовании был комбинированный показатель «сердечно-сосудистая смерть и госпитализации в связи с ухудшением СН».
Вторичные конечные точки включали отдельные компоненты первичной конечной точки, смерть от СН, госпитализацию в связи с любой причиной, а также комбинации каждого из этих показателей.
В исследовании регистрировали все случаи регоспитализаций и летальные исходы.
В ходе исследования были проанализированы госпитализации по причине декомпенсации ХСН как минимум 1 раз в ходе исследования. Таким образом, анализируемые пациенты были госпитализированы в связи с ухудшением СН как минимум дважды, учитывая критерий включения – наличие как минимум одной госпитализации в связи с ухудшением СН за 12 мес. до включения в исследование. Были проанализированы также пациенты, которые за период исследования имели как минимум 2 и 3 госпитализации.
Влияние ивабрадина на повторные госпитализации в связи с ухудшением СН изучали в следующих аспектах:
1) анализ общего внегоспитального времени – учитывалось время с момента рандомизации до наступления первой, второй, третьей и каждой последующей госпитализации с помощью модели Вэя, Лина и Вейсфельда (Wei, Lin, Weissfeld).
Эта модель сохраняет принципы рандомизации, примененные в исследовании, и используется, когда сравнивают результаты в группах, различающихся по методам лечения, что позволило осуществить анализ кумулятивного действия ивабрадина по сравнению с плацебо на госпитализации с момента рандомизации. Результатом являются соответствующие кумулятивные отношения рисков (ОР), 95% доверительные интервалы (ДИ) и значения p для сравнения групп лечения на момент первой, второй и третьей госпитализации.
2) анализ времени между событиями использовали у пациентов как минимум с одной госпитализацией в ходе исследования. Этот подход учитывает время от начала первой госпитализации после рандомизации до второй госпитализации с помощью модели пропорциональных рисков Кокса и позволяет проводить нерандомизированное сравнение времени до второго события между группами лечения. Результатом являются соответствующие ОР, 95% ДИ и значения p.
Итогом анализа стало общее число дней, когда пациенты жили вне стационара. Этот параметр вычисляли как период времени наблюдения (дата рандомизации до закрытия исследования 31 марта 2010 г.) минус число дней в госпитале минус число дней после смерти до окончания исследования.
У пациентов с одной (n=714), двумя (n=254) и тремя или более (n=218) госпитализациями в связи с декомпенсацией СН отмечалось соответственно большее количество маркеров риска неблагоприятного исхода на момент госпитализации (т.е. больший возраст, наличие сахарного диабета, снижения СКФ, перенесенный инсульт, большее ЧСС), чем у пациентов без госпитализации в связи с декомпенсацией ХСН (n=5319) (табл. 1–4).
У 1186 из 6505 рандомизированных пациентов была зафиксирована как минимум одна госпитализация в связи с декомпесацией ХСН. Из них у 472 в ходе исследования было как минимум 2 госпитализации, у 218 пациентов – как минимум 3 госпитализации в связи с декомпенсацией ХСН. Госпитализация в связи с любой причиной отмечалась у 2587 пациентов после рандомизации, у 1328 пациентов было как минимум 2 таких госпитализации, у 718 пациентов – три и более.
По сравнению с эффектом плацебо прием ивабрадина ассоциировался с меньшим числом госпитализаций в связи с декомпенсацией ХСН (902 в группе ивабрадина против 1211 в группе плацебо, отношение частот 0,75, 95% ДИ: 0,65–0,87, p=0,0002) за период наблюдения 22,9 мес.
Наиболее значимое снижение риска госпитализаций было отмечено у пациентов с ЧСС >75 уд./мин. (n=4150) (отношение рисков 0,73, 95% ДИ: 0,61–0,87, p=0,0006).
В группе пациентов с ЧСС 70–74 уд./мин. были получены одинаково направленные и качественно похожие результаты, как и в группе пациентов с ЧСС ≥75 уд./мин.; хотя различие в группе с более низкой ЧСС не достигало порога статистической значимости.
Госпитализации в связи с любой причиной (2661 против 3110; отношение рисков 0,85, 95% ДИ: 0,78–0,94, p=0,001) и госпитализации в связи с сердечно-сосудистой причиной (1909 против 2272; отношение рисков 0,84, 95% ДИ: 0,76–0,94, p=0,002) были достоверно реже в группе ивабрадина, чем в группе плацебо. Важно отметить, что при использовании ивабрадина число госпитализаций в связи с другими причинами, кроме декомпенсации ХСН (1759 в группе ивабрадина против 1899 в группе плацебо, отношение рисков 0,92, 95% ДИ: 0,83–1,02, p=0,12), не увеличилось. Начиная с 6 мес. достоверно снижается число госпитализаций в группе ивабрадина, а, следовательно, увеличивается внегоспитальное время.
Таким образом, в современной клинической практике появилась новая цель в лечении – уменьшение числа повторных госпитализаций, что увеличивает не только продолжительность жизни пациента с ХСН, но и ее качество.



Литература
1. Fang J., Mensah G., Groft J., Keenan N. Heart Failure-Related Hospitalization in the U.S., 1979 to 2004 // J. Am. Coll. Cardiol. 2008. Vol. 52(6). P. 428–434.
2. Мареев В.Ю., Даниелян М.О., Беленков Ю.Н. От имени рабочей группы Первые результаты национального эпидемиологического исследования –Эпидемиологическое обследование больных ХСН в реальной практике (по Обращаемости) ЭПОХА-О-ХСН // Сердечная недостаточность. 2003. Т. 4(3). С. 116–120.
3. Nieminen M., Brutsaert D., Dickstain K. et al. EuroHeart Failure Survey II (EHFS II): a survey on hospitalized acute heart failure patients: description of population // Eur. Heart J. 2006. Vol. 27 (22). P. 2725–2736.
4. Setoguchi S., Stevenson L. Hospitalizations in Patients With Heart Failure: Who and Why // J. Am. Coll. Cardiol. 2009. Vol. 54(18). P. 1703–1705.
5. Gheorghiade M., Mebasaa A. Introduction to acute HF syndrome // Am. J. Cardiol. 2005. Vol. 96(6A). P. 1–4.
6. Guidelines of diagnosis and treatment of acute heart failure of European Society of Cardiology, 2008. available at http://www.escardio.org/guidelines-surveys/esc-guidelines//Pages/acute-chronic-heart-failure.aspx
7. Gheorghiade M., Vaduganathan M., Fonarow G. et al. Rehospitalization for Heart FailureProblems and Perspectives // J. Am. Coll. Cardiol. 2013. Vol. 61(4). P. 391–403.
8. O'Connor C.M., Abraham W.T., Albert N.M. at al. Predictors of mortality after discharge in patients hospitalized with heart failure: an analysis from the Organized Program to Initiate Lifesaving Treatment in Hospitalized Patients with Heart Failure (OPTIMIZE-HF) // Am. Heart J. 2008. Vol.156(4). P. 662–673.
9. Rossi J.S., Flaherty J.D., Fonarow G.C. et al. Influence of coronary artery disease and coronary revascularization status on outcomes in patients with acute heart failure syndromes: a report from OPTIMIZE-HF (Organized Program to Initiate Lifesaving Treatment in Hospitalized Patients with Heart Failure) // Eur. J. Heart Fail. 2008. Vol. 10. P. 1215–1223.
10. Gheorghiade M . Abraham http://eurheartj.oxfordjournals.org/ content/28/8/ 980.long - aff-2 Albert N. et al. Relationship between admission serum sodium concentration and clinical outcomes in patients hospitalized for heart failure: an analysis from the OPTIMIZE-HF registry // Eur. Heart J. 2007. Vol. 28 (8). P. 980–988.
11. Merrill A.J. Edema and decreased renal blood flow in patients with chronic congestive heart failure; evidence of forward failure as the primary cause of edema // J. Clin. Invest. 1946. Vol. 25. P. 389–400.
12. Ruggenenti P., Remuzzi G. Worsening kidney function in decompensated heart failure: treat the heart, don't mind the kidney // Eur. Heart J. 2011. Vol. 32 (20). P. 2476–2478.
13. Wang N.C., Maggioni A.P., Konstam M.A. et al. For the Efficacy of Vasopressin Antagonism in Heart Failure Outcome Study With Tolvaptan (EVEREST) Investigators. Clinical Implications of QRS Duration in Patients Hospitalized With Worsening Heart Failure and Reduced Left Ventricular Ejection Fraction // JAMA. 2008. Vol. 299, № 22. P. 2656–2666.
14. Dunlay S.M., Gheorghiade M., Reid K.J. Critical elements of clinical follow-up after hospital discharge for heart failure: insights from the EVEREST trial // Eur. J. Heart Fail. 2010. Vol. 12. P. 367–374.
15. Ambrosy A. Pang P. Khan S. Clinical course and predictive value of congestion during hospitalization in patients admitted for worsening signs and symptoms of heart failure with reduced ejection fraction: findings from the EVEREST trial // Eur. Heart J. 2013. Vol. 34 (11). P. 835–843.












