При стабильной стенокардии напряжения хирургическое лечение (аорто–коронарное шунтирование (АКШ) или ЧКВ) рекомендовано пациентам с многососудистым поражением и сниженной систолической функцией левого желудочка [4]. Однако в последние годы увеличивается число пациентов, имеющих минимальные симптомы ИБС, которым проводится ЧКВ (по крайней мере, 1/3 из 758 тыс. ЧКВ в США за 2005 г.) [5]. До последнего времени оставалось неясным, является ли предпочтительной (в отношении уменьшения риска неблагоприятных сердечно–сосудистых событий) для больных со стабильной коронарной болезнью начальная стратегия лечения, включающая ЧКВ и оптимальную медикаментозную терапию по сравнению с оптимальной медикаментозной терапией без оперативного лечения. Оптимальная медикаментозная терапия стабильной коронарной болезни сердца – это сочетание интенсивной фармакотерапии (с обязательным длительным назначением дезагрегантов, β–адреноблокаторов, статинов, ингибиторов АПФ у больных с сердечной недостаточностью или артериальной гипертонией) и воздействие на образ жизни [4]. Обязательным компонентом оптимальной медикаментозной терапии пациентов со стенокардией напряжения и гиперхолестеринемией являются гиполипидемические препараты.
Нарушение липидного обмена является общепризнанным фактором риска сердечно–сосудистых заболеваний (ССЗ), в том числе ИБС. Коррекция дислипидемий (в частности, снижение повышенного уровня холестерина липопротеидов низкой плотности (ХС ЛПНП) – наиболее атерогенной фракции холестерина) уменьшает риск развития ИБС, снижает смертность и риск других неблагоприятных сердечно–сосудистых событий. По данным мета–анализа 28 крупных клинических исследований (49 тысяч пациентов) и 10 проспективных когортных исследований, было показано, что снижение уровня общего ХС (ОХС) на 10% (на 0,6 ммоль/л) и ХС ЛПНП на 15% в течение 5 лет уменьшает смертность от ИБС на 25–30%, риск нефатального инфаркта миокарда – на 21 % [6]. Наиболее эффективные препараты, снижающие уровень холестерина и улучшающие прогноз пациентов с ИБС – ингибиторы 3–гидрокси–3–метилглутарил–коэнзим А (ГМГ–КоА)–редуктазы – статины. Высокая эффективность (ввиду не только гиполипидемического действия, но и уникальных плейотропных эффектов) и доказанная безопасность этой группы препаратов делает их важнейшей частью комплексной медикаментозной терапии пациентов с ИБС.
Крупные рандомизированные исследования последних лет COURAGE (The Clinical Outcomes Utilizing Revascularization and Aggressive Drug Evaluation) и MAAS–II (Five–Year Follow–Up of the Medicine, Angioplasty, or Surgery Study) продемонстрировали, что реваскуляризация (ЧКВ и АКШ) у пациентов со стабильной стенокардией напряжения не улучшает 5–летнюю выживаемость по сравнению с группой оптимальной медикаментозной терапии [7,8]. Только АКШ уменьшало число нефатальных инфарктов миокарда и дополнительных процедур реваскуляризации миокарда, а между группами медикаментозного лечения и эндоваскулярных коронарных вмешательств достоверных различий по этим конечным точкам выявлено не было. Эти данные согласуются с результатами других исследований: ЧКВ не уменьшает смертность или риск инфаркта миокарда по сравнению с оптимальной лекарственной терапией у пациентов со стабильной стенокардией [9]. Таким образом, если пациенту со стабильной ИБС и многососудистым поражением не проводится ЧКВ, то «агрессивная» медикаментозная терапия с обязательным использованием статинов улучшает прогноз, снижает риск смерти и нефатального инфаркта миокарда в той же степени, что и при применении эндоваскулярных коронарных вмешательств. Необходимо отметить, что в этих исследованиях была очень высокой приверженность больных к лечению (превышала 90%) и эффективность медикаментозной терапии (целевые цифры холестерина были достигнуты более чем у 70% больных, целевые показатели АД – у 65–90%). Естественно, что подобные хорошие результаты от медикаментозного лечения больных со стабильной стенокардией можно ожидать только при такой же «агрессивности» фармакологической терапии и такой же высокой приверженности больных к лечению.
К сожалению, приходится констатировать, что в России статины применяются лишь у небольшой части пациентов с ИБС, которым они показаны, и у еще меньшей части пациентов достигаются целевые цифры холестерина [10]. Так, по данным Moscow Statin Survey (2004–2005 гг.), в Москве статины получали только около 30% от числа тех, кому они были показаны, а среди пациентов, получавших статины, целевой уровень ХС ЛПНП был достигнут только у 29,8% [11]. Меньше всего процент лечения статинами и достижения целевого уровня XC ЛПНП был отмечен у лиц со стабильной ИБС без осложнений и у пациентов с сахарным диабетом (СД) 2 типа. Еще хуже положение дел по России в целом: как было показано в эпидемиологической части исследования ОСКАР–2006, пациентам высокого риска в общей поликлинической практике статины назначали чуть более 5%, а целевых значений ХС ЛПНП достигли только 4,3% больных [12].
Механизмы действия статинов
Механизм гиполипидемического действия статинов обусловлен ингибированием ГМГ–КоА–редуктазы, в результате чего снижается синтез эндогенного холестерина в печени, повышается образование рецепторов к ЛПНП на гепатоцитах, что приводит к удалению атерогенных ЛПНП из кровотока. Таким образом, гиполипидемический эффект статинов выражается прежде всего в снижении холестерина липопротеидов низкой плотности (на 25–50%, в зависимости от препарата и суточной дозы). Также при применении статинов снижается содержание общего холестерина (на 25–40%), холестерина липопротеидов очень низкой плотности (ЛПОНП) и триглицеридов (ТГ). Статины умеренно повышают содержание холестерина липопротеидов высокой плотности (ХС ЛПВП), уменьшая соотношение ХС ЛПНП/ХС ЛПВП (до 50%) [13]. При постоянной дозе статинов максимальный гиполипидемический эффект наступает через 4–8 недель [14]. Наряду с гиполипидемическим действием, статины обладают целым рядом дополнительных положительных свойств – это плейотропные эффекты статинов, изучению которых было посвящено большое количество работ в последние годы.
Статины улучшают эндотелиальную функцию, уменьшают вазоспастические реакции в коронарных артериях; стабилизируют атеросклеротические бляшки, уменьшают их склонность к разрыву; подавляют реакции воспаления; благоприятно влияют на вязкость крови, снижают агрегацию тромбоцитов [15]. Показано, что статины (в частности, симвастатин) оказывают антиишемический эффект за счет уменьшения эндотелиальной дисфункции коронарных артерий. Так, в группе пациентов с ИБС, получавших симвастатин (по сравнению с группой плацебо), при проведении нагрузочной пробы увеличилось время до наступления ишемии и уменьшилась величина депрессии сегмента ST; а по данным Холтеровского ЭКГ–мониторирования было отмечено уменьшение числа эпизодов ишемии миокарда [16]. Статины активируют эндотелиальную NO–синтетазу, тем самым увеличивая продукцию окиси азота (NO) и усиливая эндотелий–зависимую вазодилатацию [17]. Вазодилатирующий эффект статинов усиливается за счет их способности снижать продукцию эндотелина – мощного вазоконстрикторного фактора [18]. Для большинства статинов (исследования in vitro) доказана способность уменьшать пролиферацию и миграцию гладкомышечных клеток, которые играют важную роль в атерогенезе и в патогенезе рестеноза после ЧКВ [19]. Установлено участие в процессе атерогенеза окисленных ЛПНП (заряжены отрицательно). Статины оказывают прямой антиоксидантный эффект на ЛПНП [20]. У пациентов с семейной гиперхолестеринемией лечение симвастатином существенно снижало пропорцию окисленных ЛПНП [21].
В последнее десятилетие было доказано влияние воспаления на развитие атеросклероза. Повышенные уровни маркеров воспаления, таких как С–реактивный белок (СРБ), интерлейкин–6, ассоциируются с увеличенным риском первичных и последующих сердечно–сосудистых событий. По данным исследования CARE (Cholesterol and Recurrent Events trial), лечение правастатином постинфарктных пациентов снижало повышенный уровень СРБ; относительный риск последующих неблагоприятных коронарных событий уменьшался на 54% [22]. Снижение уровня воспалительных маркеров не коррелировало с уменьшением уровня ХС ЛПНП. Быстрое снижение уровня СРБ при применении статинов отчасти может объяснить ранние положительные эффекты этих препаратов при остром коронарном синдроме [23].
Статины обладают уникальной способностью стабилизировать атеросклеротические бляшки, уменьшают их склонность к разрыву. Несколько механизмов могут объяснить эффект статинов, стабилизирующий бляшку. Снижение ХС ЛПНП способствует уменьшению размеров липидного ядра атеросклеротической бляшки [24]. Повышенный плазменный уровень маркеров воспалительного каскада (Р–селектин, интерлейкин–6,
Исследования плейотропных эффектов статинов доказали, что некоторые из них не связаны с гиполипидемическими свойствами этих препаратов: проявляются при очень низких дозах статинов, раньше, чем снижается уровень ХС, слабо коррелируют или вообще не коррелируют с уровнем ХС ЛПНП [15]. Понимание всего спектра преимуществ терапии статинами, возможно, расширит область их терапевтического применения в будущем.
Стратегия гиполипидемической
терапии у пациентов со стенокардией напряжения (отечественные
и зарубежные рекомендации)
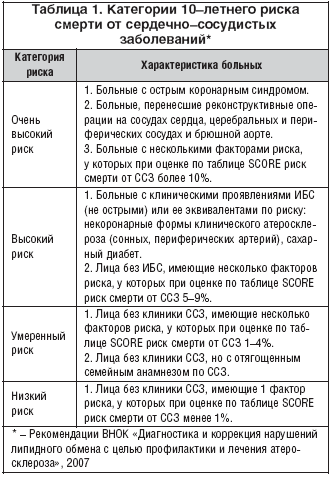
При выборе алгоритма гиполипидемической терапии необходимо учитывать, к какой категории, определяемой по 10–летнему риску смерти от сердечно–сосудистых заболеваний (ССЗ), относится пациент (табл. 1) [26,27].
Шкала SCORE (Systematic COronary Risk Evaluation), принятая Европейским конгрессом кардиологов, разработана для оценки риска смертельного исхода ССЗ в течение 10 лет [28]. Эта шкала предназначена для оценки риска у лиц без клинических проявлений ИБС и других ССЗ. Основными факторами риска по шкале SCORE являются гиперхолестеринемия, артериальная гипертония, курение, а также возраст и пол больного. К категории высокого риска относятся пациенты с установленным диагнозом сердечно–сосудистых заболеваний, сахарным диабетом, повышением уровня общего холестерина выше 8,0 ммоль/л или АД больше 180/110 мм рт.ст. У лиц умеренного и низкого риска можно в начале лечения дислипидемий использовать немедикаментозные меры профилактики атеросклероза: назначение гипохолестеринемической диеты, коррекцию массы тела, повышение физической активности, прекращение курения [26]. При отсутствии эффекта для достижения целевых цифр липидов следует назначать медикаментозную терапию (табл. 2).
Медикаментозную терапию дислипидемий следует проводить у всех лиц высокого и очень высокого риска, совмещая ее с немедикаментозными мерами профилактики атеросклероза [26].
Результаты крупных исследований последних лет подтвердили преимущества гиполипидемической терапии у пациентов ИБС из группы высокого риска. Для пациентов из группы высокого риска как целевой был определен уровень ХС ЛПНП менее 2,5 ммоль/л (100 мг/дл) [26]. Было подчеркнуто, что пациенты с сахарным диабетом отнесены к группе высокого риска и должны получать гиполипидемическую терапию. Доказана польза гиполипидемической терапии статинами пациентов с ИБС пожилого возраста. Для пациентов, относящихся к группе очень высокого риска (острые коронарные синдромы) целевым предложено признать уровень ХС ЛПНП менее 2,0 ммоль/л (70 мг/дл).
Лечение гиперлипидемий IIa, IIb и III типов (с преимущественным повышением ХС ЛПНП и общего ХС) рекомендовано начинать с ингибиторов ГМГ–КоА-редуктазы (статинов).
Эффективность статинов доказана в многочисленных рандомизированных клинических исследованиях. Так, в исследовании 4S (Scandinavian Simvastatin Survival Study) длительное (5–летнее) применение симвастатина (20–40 мг/сут.) у пациентов с ИБС и гиперхолестеринемией (общий ХС 5,5–8,0 ммоль/л) позволило по сравнению с плацебо снизить общую смертность на 30%, смертность от ИБС на 42%, частоту нефатальных инфарктов миокарда на 37%, необходимость в АКШ или ЧКВ на 37% [29]. В исследовании HPS (Heart Protection Study) также была подтверждена высокая эффективность симвастатина у пациентов с ИБС или в группе высокого риска развития ИБС [30]. Применение симвастатина в дозе 40 мг/сут. снижало общую смертность и риск основных сердечно–сосудистых событий, а также потребность в оперативных вмешательствах по восстановлению коронарного кровотока (АКШ и ЧКВ). При применении статинов замедляется прогрессирование атеросклероза коронарных артерий и снижается частота неблагоприятных сердечно–сосудистых событий [31].
За последние годы в результате проведенных клинических исследований были получены новые данные, потребовавшие внесения изменений и дополнений в существовавшие ранее руководства по лечению пациентов с нарушениями липидного обмена [30,32]. В первую очередь это коснулось изменений целевых уровней ХС ЛПНП у больных высокого и очень высокого риска – целесообразно снижение ХС ЛПНП ниже 70 мг/дл [33].
Применение Вазилипа в лечении больных со стабильной стенокардией напряжения и гиперхолестеринемией
При проведении гиполипидемической терапии врачу приходится решать проблему выбора препарата, основываясь на данных о его клинической эффективности и принимая во внимание стоимость лечения. Генерики и оригинальные препараты должны быть эквиваленты по своим терапевтическим параметрам, т.е. они должны иметь одинаковый клинический эффект и профиль безопасности при использовании пациентами. Важной положительной чертой препаратов–генериков является их более доступная цена по сравнению с оригинальным препаратом. Одним из современных и хорошо изученных на российских пациентах симвастатином является Вазилип (компания KRKA, Словения). У большинства пациентов с ИБС эффективная доза Вазилипа, позволяющая достичь целевых значений ХС ЛПНП, составляет 20–40 мг/сут. При необходимости доза Вазилипа может быть увеличена до 80 мг/сут. Лечение препаратом рекомендуется начинать с дозы 20 мг/сут. и дальнейшее титрование проводить, увеличивая дозу с интервалами в 4 недели. Гиполипидемический эффект проявляется через 2 недели от начала лечения, а максимальная эффективность достигается спустя 4–6 недель. Вазилип принимают 1 раз в сутки, лучше вечером, ввиду того, что синтез ХС наиболее интенсивно происходит в ночное время.
Анализ данных многочисленных исследований показал, что результаты, полученные для Вазилипа, воспроизводят известные закономерности, характерные для оригинального препарата симвастатина. Так, в открытом исследовании ОСКАР, в котором участвовали 7098 пациентов с ИБС в возрасте 57,7±0,2 лет, 86,9% больных принимали в течение 8 недель Вазилип в дозе 20 мг/сут. ОХС снизился на 22,7%, ХС ЛПНП на 26,7% и ТГ на 24%, что сопровождалось уменьшением расчетного суммарного риска сердечно–сосудистых осложнений на 33% [34]. При использовании небольших доз Вазилипа (10 мг) у больных пожилого возраста со стенокардией напряжения уровень общего ХС снижался на 13%, улучшались вазодилатирующие свойства эндотелия; все пациенты хорошо переносили лечение [35]. О.М. Драпкина и соавт. в 2007 г. провели длительное лечение Вазилипом (20 мг/сут.) пациентов с дислипидемией IIa и IIb типов, имеющих жировой гепатоз печени. Применение Вазилипа достоверно снижало уровень ХС ЛПНП на 27,8%, ОХС – на 17,5%, индекс атерогенности на 36,7%. Все пациенты хорошо перенесли 12–месячный прием Вазилипа, несмотря на наличие сопутствующей патологии печени [36].
При исследовании клинической эффективности Вазилипа (в низких дозах 10–20 мг/сут.) у пациентов с артериальной гипертензией и сахарным диабетом, помимо гиполипидемического действия, подтвердились плейотропные эффекты препарата на эндотелиальную функцию (увеличивался синтез NO), снизился уровень провоспалительных цитокинов (TNF– α). Плейотропные эффекты Вазилипа не зависели от выраженности гиполипидемического действия препарата. Эти данные согласуются с результатами других исследований, изучавших плейотропные свойства статинов [37].
Таким образом, Вазилип – высококачественный симвастатин, аналогичный по эффективности и безопасности оригинальному препарату. По данным фармакоэкономического исследования (2003 г.), замена оригинального препарата симвастатина на Вазилип приводит к снижению дополнительных затрат на лечение пациентов до 744 долларов США в расчете на одну дополнительно предотвращенную двойную конечную точку (смерть или нефатальный инфаркт миокарда) и до 1595 долларов США в расчете на один дополнительно предотвращенный летальный исход [38].
Побочные эффекты
Статины хорошо переносятся пациентами и, по данным многочисленных клинических исследований, могут считаться одним из самых безопасных классов лекарственных препаратов [26]. Длительное (5–летнее) применение симвастатина не вызывало серьезных побочных эффектов, в том числе со стороны мышечной системы (статистически незначимое увеличение частоты миопатии до 0,01% в год при р=0,2) или других побочных реакций [30]. Прием статинов иногда может сопровождаться болями в животе, метеоризмом, запорами. В целях обеспечения безопасности лечения статинами необходимо проводить регулярный контроль побочных эффектов. До начала лечения, а также каждые 6 недель (в первые 3 месяца лечения) и далее каждые 8 недель (в течение первого года), а затем 1 раз в полгода необходимо определять уровень креатинфосфокиназы (КФК), печеночных ферментов (АСТ, АЛТ). Бессимптомное повышение уровня печеночных ферментов наблюдается у 1–5% больных. Если уровень хотя бы одного из ферментов превышает норму в 3 раза при двух последовательных измерениях, лечение статинами прекращают, что приводит к нормализации трансаминаз [26,39]. Факторами риска появления осложнений со стороны печени являются гепатит в анамнезе, употребление алкоголя. Редким осложнением (0,1–0,5%) лечения статинами является миопатия. О появлении миопатии свидетельствует следующая клиническая симптоматика: боли в мышцах, мышечная слабость, возможны лихорадка, увеличение КФК (при увеличении КФК более чем в 10 раз выше нормы, лечение прекращают). Наиболее опасное, но чрезвычайно редкое осложнение терапии статинами – рабдомиолиз, риск которого возрастает при совместном применении статинов с фибратами, циклоспорином, макролидами. У пациентов, получающих такую комбинацию лекарств, клинический и лабораторный контроль побочных эффектов проводится не реже 1 раза в месяц. Так, по данным мета–анализа более 50 крупных исследований, было зарегистрировано 8 случаев нефатального рабдомиолиза на 35 тыс. пролеченных пациентов [40].
Таким образом, Вазилип (фармацевтическая компания KRKA, Словения) – симвастатин, эффективность и безопасность которого доказана многочисленными исследованиями, может широко применяться для длительного лечения больных со стабильной стенокардией напряжения. Длительное лечение этим препаратом улучшает прогноз пациентов, снижая общую и сердечно–сосудистую смертность, улучшает клиническое течение заболевания.

Литература
1. Centers for Disease Control and Prevention Prevalence of heart disease MMWR. Surveill Summ 2007; 56:113–118.
2. Харченко В.И., Кокорина Е.П., Корякин М.В., и др. Смертность от основных болезней системы кровообращения в России. Российский кардиологический журнал. 2005; 1(51):5–15.
3. ACC/AHA guidelines for the management of patients with ST–elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Revise the 1999 Guidelines for the Management of Patients With Acute Myocardial Infarction). J Am Coll Cardiol. 2004; 44(3): E1–E211.
4. ACC/AHA 2002 guideline update for the management of patients with chronic stable angina—summary article: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on the Management of Patients With Chronic Stable Angina). Circulation. 2003; 107(1): 149–158.
5. Levit K., Ryan K., Elixhauser A. et al. HCUP Facts and Figures: Statistics on Hospital–based Care in the United States, 2005. Agency for Healthcare Research and Quality Web site. http://www.hcup–us.ahrq.gov/reports/annualreport/HAR 2005. Accessed June 2, 2008.
6. Law M.R., N J Wald, S G Thompson. By how much and how quickly does reduction in serum cholesterol concentration lower risk of ischemic heart disease? Br. Med. J. 1994. V. 308. P.367–372.
7. Kereiakes D.J., Teirstein P.S., Sarembock I.J. The Truth and Consequences of the COURAGE Trial. J Am Coll Cardiol. 2007; 50: 1598–1603.
8. Hueb W., Lopes N.H., Gersh B.J. Five–Year Follow–Up of the Medicine, Angioplasty, or Surgery Study (MASS II): A Randomized Controlled Clinical Trial of 3 Therapeutic Strategies for Multivessel Coronary Artery Disease. Circulation. 2007; 115: 1082–1089.
9. Coylewright M., Blumenthal R. S., Post W. Placing COURAGE in Context: Review of the Recent Literature on Managing Stable Coronary Artery Disease. Mayo Clin. Proc. 2008; 83(7): 799 – 805.
10. Оганов Р.Г., Лепахин В.К., Фитилев С.Б. и др. Особенности диагностики и терапии стабильной стенокардии в Российской Федерации (международное исследование ATP–Angina Treatment Pattern). Кардиология 2003; № 5: 9–15.
11. Сусеков А.В., Зубарева М.Ю., Деев А.Д. и др. Основные результаты Московского Исследования по Статинам (Moscow Statin Survey, MSS). Сердце. 2006; 6.
12. Шальнова СА, Деев АД. Характеристика пациентов высокого риска. Результаты эпидемиологической части научно–образовательной программы ОСКАР. Кардиоваскулярная терапия и профилактика. 2006; 5.
13. Marchioli R., Investigators G.T. Beneficial effects of statins. The Lancet 1996; 348:1582.
14. Grines C.L. The role of statins in reversing atherosclerosis: what the latest regression studies show. J Interv Cardiol. 2006; 19(1): 3–9.
15. Davignon J. Beneficial Cardiovascular Pleiotropic Effects of Statins. Circulation. 2004; 109: III39–III43.
16. De Devitiis M., Pubba P., Di Sommas S. et al. Effects of short term reduction in serum cholesterol with simvastatin in patients with stable angina pectoris and mild to moderate hypercholesterolemia. Am J Cardiol. 1996; 78: 763–768.
17. Bates K., Ruggeroli C.E., Goldman S., Gaballa M.A. Simvastatin restores endothelial NO–mediated vasorelaxation in large arteries after myocardial infarction. Am J Physiol Heart Circ Physiol. 2002; 283: H768–75.
18. Hernandez–Perera O., Perez–Sala D., Navarro–Antolin J. et al. Effects of the 3–hydroxy–3–methylglutaryl–CoA reductase inhibitors, atorvastatin and simvastatin, on the expression of endothelin–1 and endothelial nitric oxide synthase in vascular endothelial cells. J Clin Invest 1998; 101: 2711–2719.
19. Conti CR. Updated pathophysiologic concepts in unstable coronary artery disease. Am Heart J 2001; 141 (2 Suppl): S12–14.
20. Suzumura K., Yasuhara M., Tanaka K., et al. Protective effect of fluvastatin sodium, HMG–CoA reductase inhibitor, on oxidative modification of human low–density lipoprotein in vitro. Biochem Pharmacol. 1999; 57: 697–703.
21. Sanchez–Quesada J.L., Otal–Entraigas C., Franco M., et al. Effect of simvastatin treatment on the electronegative low–density lipoprotein present in patients with heterozygous familiar hypercholesterolemia. Am J Cardiol. 1999; 84: 655–659.
22. Ridker P.M., Rifai N., Pfeffer M.A., et al. Тhe Cholesterol and Recurrent Events (CARE) Investigators. Inflammation, pravastatin, and the risk of coronary events after myocardial infarction in patients with average cholesterol levels. Circulation. 1998; 98: 839–844.
23. Olsson A.G., Schwartz G.G.. Early initiation of treatment with statins in acute coronary syndromes. Ann Med. 2002; 34: 37–41.
24. Llorente–Cortes V/, Martinez–Gonzalez J/, Badimon L. Esterified cholesterol accumulation induced by aggregated LDL uptake in human vascular smooth muscle cells is reduced by HMG–CoA reductase inhibitors. Arterioscler Thromb Vasc Biol. 1998; 18: 738–746.
25. Bellosta S, Via D, Canavesi M, et al. HMG–CoA reductase inhibitors reduce MMP–9 secretion by macrophages. Arterioscler Thromb Vasc Biol. 1998; 18: 1671–1678.
26. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации, разработанные группой экспертов ВНОК, III пересмотр. М., 2007 г.
27. Grundy S.M.; Cleeman J.I.; Brewer H.B. Implications of Recent Clinical Trials for the National Cholesterol Education Program Adult Treatment Panel III Guidelines. Circulation. 2004;110: 227–239.
28. Conroy RM, Pyorala K, Fitzgerald AP, et al. Estimation of ten–year risk of fatal cardiovascular disease in Europe: the SCORE project. Eur Heart J 2003;24:987–1003.
29. Randomised trial of cholesterol lowering in 4,444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S): Scandinavian Simvastatin Survival study Group. Lancet 1994; 344: 1383–1389.
30. Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20 536 high–risk individuals: a randomised placebo–controlled trial. Lancet 2002; 360: 7–22.
31. Карпов Ю.А. Статины в профилактике и лечении связанных с атеросклерозом заболеваний; эффективность и безопасность. Рациональная Фармакотерапия в Кардиологии 2005; № 2: 48–53.
32. Cannon C.P., Braunwald E., McCabe C.H. et al. Pravastatin or Atorvastatin Evalua












