От 600 тыс. до 2,5 млн. людей в мире страдают хроническими трофическими язвами стоп и голеней [Токмакова А.Ю.]. В среднем, по данным различных источников, трофические язвы венозной этиологии составляют более 70% от всех язв нижних конечностей. Облитерирующий атеросклероз является причиной возникновения трофических язв нижних конечностей в 8% случаев (кроме того, он может сопутствовать ХВН). Диабетическая микро–, макроангиопатия и дистальная нейропатия становится причиной трофических язв в 3% случаев, а среди больных сахарным диабетом число лиц, имеющих язвенные дефекты стоп, достигает 15%. Малигнизация трофических язв отмечается в 1,6–3,5 % случаев.
В руководстве «Флебология» (2001 г.) под редакцией академика Савельева В.С. приводится следующая примерная этиологическая частота трофических язв: варикозные – 52 %, артериальные – 14%; смешанные – 13%, посттромбофлебитические – 7%, посттравматические – 6%, диабетические – 5%, нейротрофические – 1% и прочие – 2%.
Этиология и патогенез
Этиологию и патогенез трофической язвы можно представить в виде пирамиды, на вершине которой тяжелый раневой сепсис и синдром полиорганной дисфункции, а в основании – множество врожденных и приобретенных заболеваний и травм, запускающих различные патологические процессы на тканевом (ишемия, гипоксия), микроциркуляторном (микротромбозы и сладж форменных элементов крови, экстравазация белка в перивазальное пространство с накоплением фибрина в тканях и с образованием «фибриновых манжет» вокруг капилляров, что усугубляет метаболические нарушения в тканях, стимулируя эпидермальный некроз) и клеточном (активизация лейкоцитов с выбросом ими лизосомальных ферментов) уровнях.
Дополнительно происходят локальные и системные сдвиги, формирующие синдром гипервязкости крови. В ответ на выраженную локальную гипоксию тканей в области трофической венозной язвы активируются процессы свободнорадикального перекисного окисления липидов, приводящие к системному истощению с развитием цитокин опосредованного повреждающего воздействия на ткани дистальных сегментов конечности. В результате возникновения первичного аффекта нарушается барьерная функция кожи. Повреждение ее слоев сопровождается некрозом мягких тканей и массивным экссудативным процессом. В дальнейшем происходит быстрая бактериальная контаминация трофической язвы, которая в ряде случаев может приобретать генерализованный характер.
Заболевания, приводящие
к образованию трофических язв
Трофические язвы на нижних конечностях являются следствием разнообразных заболеваний, нарушающих локальную гемодинамику артериальной, венозной, лимфатической систем, включая микроциркуляторный уровень поражения. Кроме этих факторов, причиной появления трофических язв могут быть различные травмы кожи, мягких тканей и периферических нервов.
Этиологически трофические язвы могут быть:
– венозные (хроническая венозная недостаточность (ХВН) при варикозной болезни (ВБ) и/или посттромботической болезни (ПТБ));
– артериальные (хроническая артериальная недостаточность (ХАН) при облитерирующих заболеваниях артериального русла);
– диабетические (на фоне диабетической микро–, макроангиопатии и нейропатии при синдроме диабетической стопы (СДС));
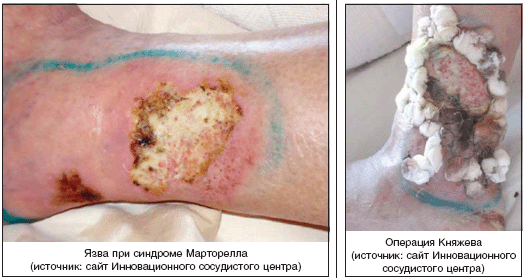
– гипертонические (синдром Марторелла – локальные артериовенозные шунты);
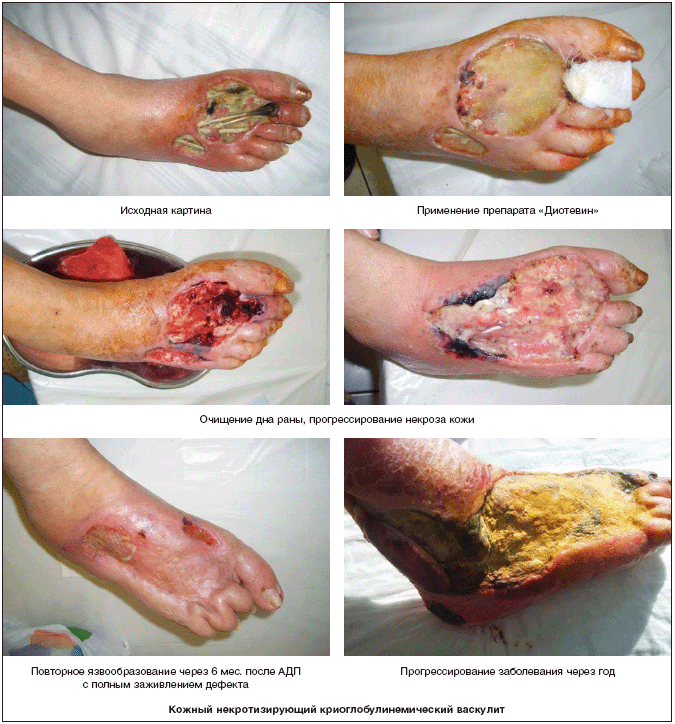
– при системных заболеваниях [болезни крови, обмена веществ, коллагенозы, васкулиты – например, ливедо–васкулит (обусловленный одновременно васкулитом и тромбозом мелких сосудов: характерно сочетание геморрагической сыпи и ливедо с болезненными язвами ног; чаще всего встречается идиопатическая форма заболевания; кроме того, ливедо–васкулит наблюдают при СКВ, антифосфолипидном синдроме, системной склеродермии, криоглобулинемии и криофибриногенемии) или кожная некротизирующая форма криоглобулинемического васкулита (КГВ)];
– нейротрофические (при деиннервации на фоне заболеваний или травм нервных стволов в зонах избыточного давления (НЯ));
– рубцово–трофические (образующиеся на поверхности послеоперационных или посттравматических рубцов);
– фагеденические (прогрессирующая эпифасциальная гангрена);
– застойные (образуются на фоне недостаточности кровообращения (НК) и отечного синдрома при сердечно–сосудистой патологии, достаточно быстро регрессируют при компенсации основного заболевания и купировании отеков);
– пиогенные (на фоне гнойных заболеваний кожи конечностей при несоблюдении правил личной гигиены, как правило – у асоциального контингента);
– специфические и инфекционные (сифилитические; туберкулезные (болезнь Базена); лепрозные; язва Бурули – инфекционная тропическая болезнь, вызываемая Mycobacterium ulcerans; тропическая язва или язва Нага – кожное заболевание, часто встречающееся в регионах с влажным тропическим климатом; характеризуется появлением большой открытой, покрытой струпьями язвы на месте недавно полученной раны или ссадины чаще всего на ногах; тропические фагеденические язвы; лейшманиоз, риккетсиоз; онхоцеркоз);
– малигнизированные (новообразования кожи);
– при токсическом эпидермальном некролизе Лайелла (самая тяжелая, порой смертельная форма лекарственной токсидермии – острое началом и отслойка всех слоев эпидермиса на 30% поверхности тела и более; у взрослых синдром Лайелла чаще всего обусловлен лекарственными средствами – противосудорожными средствами, сульфаниламидами, аминопенициллинами, НПВП и аллопуринолом; риск повышен у иммуноскомпроментированных больных; характерен положительный симптом Никольского – при легком потирании здоровой кожи происходит десквамация эпидермиса и обнажение мокнущей поверхности; могут присоединяться токсико–аллергические поражения сердца, печени, органов брюшной полости, почек);
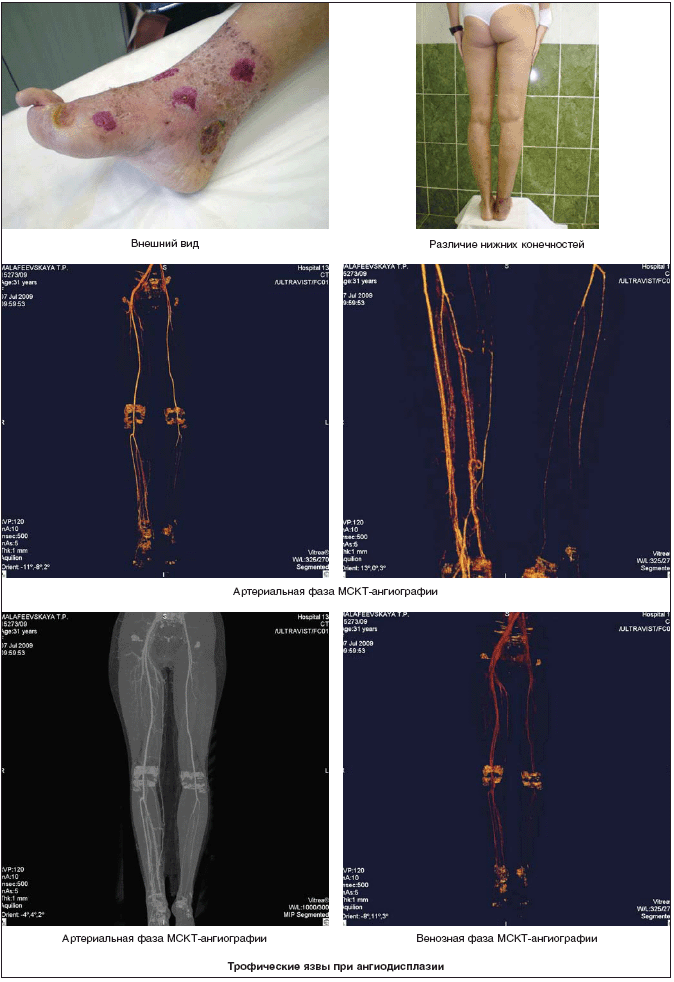
– при врожденных пороках развития сосудистой системы – ангиодисплазиях;
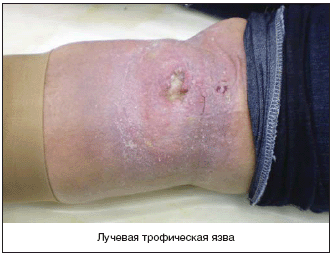
– лучевые;
– язвы, развившиеся вследствие воздействия физических факторов (ожоги и отморожения);
– артифициальные (искусственные язвы с целью симуляции и членовредительства).
Классификация
Практически повсеместно приняты следующие классификации трех основных патологий (ХВН, ХАН, СДС), приводящих на определенной стадии к образованию трофических язв нижних конечностей в подавляющем большинстве случаев – суммарно более 90% всех трофических язв нижних конечностей: классификация хронической венозной недостаточности СЕАР, классификация облитерирующих заболеваний периферических артерий по Фонтейну–Покровскому, степень выраженности поражения тканей при СДС [Wagner F.W., 1979]. Кроме того, используются классификация диабетических язв Техасского Университета и классификация язвенных дефектов у больных с СДС PEDIS (The Consensus of diabetic foot Supplement, Amsterdam, 2003) и другие.
Дополнительно могут быть использованы классификации, описывающие глубину язвенного дефекта и его площадь. По глубине различают: I степень – поверхностную язву (эрозию) в пределах дермы; II степень – язву, достигающую подкожной клетчатки; III степень – язву, пенетрирующую до фасции или субфасциальных структур (мышцы, сухожилия, связки, кости), в полость суставной сумки или сустава; по площади: малые, площадью до 5 см2; средние – от 5 до 20 см2; обширные (гигантские) – свыше 50 см2.
Диагностика
В диагностике заболеваний, приводящих к образованию трофических язв нижних конечностей, помимо стандартных лабораторных анализов, используются бактериологические, гистологические и цитологические исследования, исследование цитокинового профиля, оценка показателей перекисного окисления липидов и антиоксидантной системы защиты тканей, ревмопробы, определение титра антител ANCA и криоглобулинов.
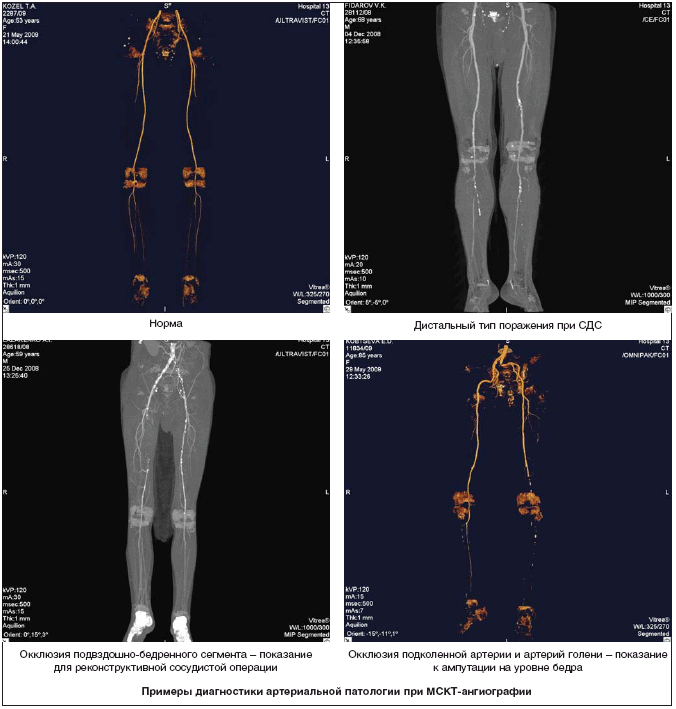
Среди инструментальных методов исследований применяются ультразвуковое ангиосканирование (УЗАС), ультразвуковая допплерография (УЗДГ), интраваскулярная ультрасонография, УЗИ мягких тканей, мультиспиральная компьютерная томография–ангиография (МСКТ–ангиография), рентген–контрастная ангиография, магнито–резонансная томография, определение плече–лодыжечного индекса (ПЛИ), реолимфовазография, денситометрия, исследование вибрационной чувствительности (камертон, биотензиометр), измерение распределения плантарного давления, педография, электромиография, Холтеровское мониторирование, мониторинг АД, транскутанное определение напряжения кислорода и углекислого газа в тканях, лазерная флоуметрия, плетизмография (окклюзионная, воздушная, фото–), рентгеноконтрастная и радиоизотопная флебография, флеботонография.
Дифференциальный диагноз
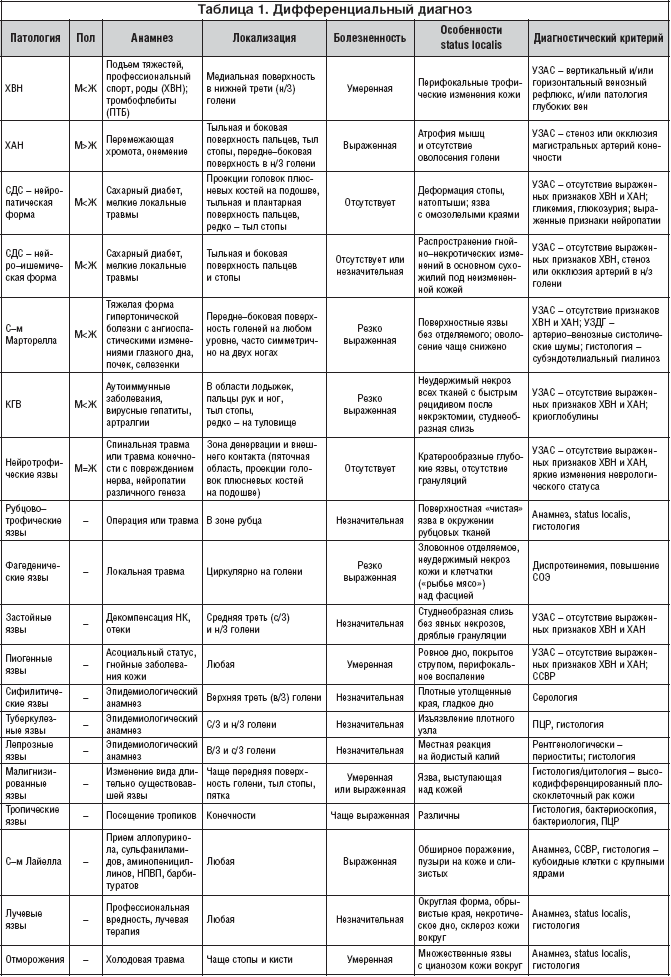
Схематично дифференциальный диагноз трофических язв различной этиологии с учетом особенностей анамнеза, локализации, болевого синдрома, местного статуса и основного диагностического критерия представлен в таблице 1.
Лечение
Не потеряли актуальности слова С.И. Спасокукоцкого: «Язвы голени представляют истинный крест хирургов по своему громадному упорству и трудности лечения». Общее число методов лечения трофических язв приближается к 10 тыс. [Кованов В.В., Сыченникова И.А.].
Хирургические методы лечения
Симптоматические хирургические методы достаточно широко используются российскими хирургами. Обоснованием их применения и модернизации является постулат о необходимости иссечения нежизнеспособных тканей и радикального удаления очага хронической инфекции [Хохлов А.М., 2002; Аскеров Н.Г., Светухин А.М. с соавт., 2003].
В литературе можно встретить диаметрально противоположные мнения о применении того или иного метода. Так, например, такие методы местного воздействия на язву, как кюретаж и вакуумирование, сразу после процедуры приводят к кажущемуся освобождению трофической язвы от некротических тканей и наложений фибрина; на самом деле грубое и не дозированное механическое воздействие вызывает значительное увеличение площади и глубины повреждения кожи Савельев В.С. и соавт., 2000; Богачев В.Ю. и соавт., 2001], в результате разрушается ростковый слой кожи и нарушается процесс синтеза коллагена и по этой причине заживление трофической язвы затягивается [Моrison М., Moffat C., 1995].
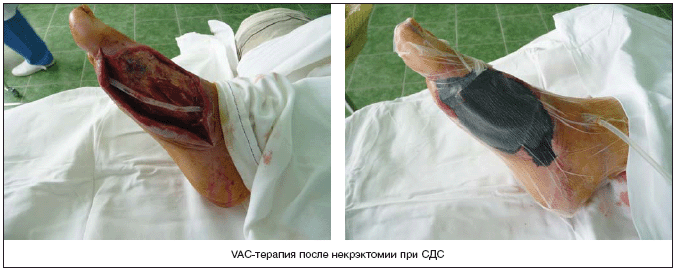
С другой стороны, VAC–терапия – метод локального лечения инфицированных раневых дефектов, позволяющий эффективно и быстро очистить, снизить контаминацию раны, уменьшить ее объем, ускорить образование грануляционной ткани, экономически эффективен ввиду отсутствия необходимости перевязок в течение 3–7 дней. Считается, что отрицательное давление способствует удалению интерстициальной жидкости, снижению локального отека, стимуляции локальной микроциркуляции, снижению уровня микробной контаминации. Кроме того, в условиях дозированного отрицательного давления в ране увеличивается скорость пролиферации клеток.
Существуют VAC–системы фирмы «KСI», США, которые, однако, не представлены на рынке России. Нами используется оригинальный аналог: повязка состоит из подведенной к ране через контрапертуру дренажной трубки с дополнительными сечениями для лучшего оттока из раны, поролона, который укладывается в рану двумя слоями, чтобы покрыть всю поверхность раны, причем дренаж располагается между слоями поролона (другой вариант – один слой поролона на рану с подведением дренажа к его поверхности с помощью плоского переходника); далее выполняется закрытие раны пленкой для операционного поля фирмы «3М»; дренажная трубка подсоединяется к медицинскому отсосу В–40А (Беларусь) для активной аспирации в режиме non stop. Одним из важных условий является герметичность системы; оптимальный уровень негативного давления, который должен создаваться в повязке – около 125 мм рт.ст.
Метод катетеризации a. еpigastrica позволяет проводить регионарную инфузионную терапию пораженной конечности с помощью инфузомата в режиме non–stop; противопоказаниями являются тяжелая общая инфекция, окклюзия артерий конечности.
Метод «виртуальной ампутации», предложенный Калабрезе Э. при лечении нейропатической формы СДС, предполагает резекцию плюсневой кости и плюсне–фалангового сустава с сохранением внешней анатомической целостности стопы и в то же время ликвидирует проблемную зону избыточного давления, приводящую к образованию язвы, и очаг костного инфекционного процесса.
При синдроме Марторелла, для которого характерно образование артерио–венозных шунтов, используется предложенная болгарским хирургом Княжевым В. операция, заключающаяся в разобщении артерио–венозных фистул по периферии язвы путем их чрескожного прошивания.
Описаны методы эспандерной дермотензии (применяемые больше в детской хирургии); нами при обширных раневых дефектах чаще используется дермотензия на спицах Киршнера; в настоящее время на Российском рынке появились израильские мини–дермотензионные системы с дозатором натяжения тканей.
Лечение язв на фоне ангиодисплазий заключается в микрохирургических, сосудистых, эндоваскулярных и пластических вмешательствах.
Склерооблитерация. Необходимо помнить о наличии противопоказаний – как абсолютных (известная аллергия на склеропрепарат, тяжелые заболевания, острый варикотромбофлебит или тромбоз глубоких вен, тяжелая общая инфекция, недостаточная подвижность пациента, облитерирующей атеросклероз артерий нижних конечностей с ХАН 3 и 4 стадии, беременность), так и относительных (выраженные отеки нижних конечностей, местная инфекция в области предполагаемой склеротерапии, осложнения диабета (полинейропатия), облитерирующий атеросклероз артерий нижних конечностей с ХАН 2 стадии, бронхиальная астма, аллергический диатез, тромбофилия с тромбозом глубоких вен в анамнезе).
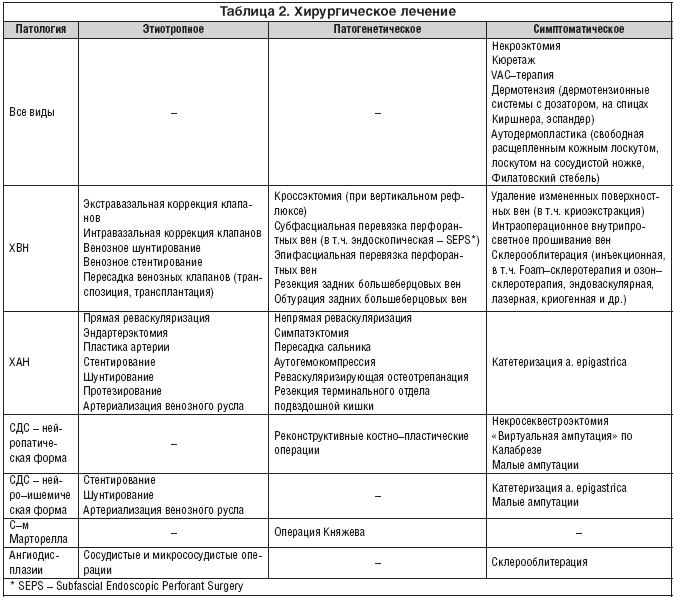
Хирургические методы лечения представлены в таблице 2.
Фармакотерапия
Лекарственные препараты определенных групп могут быть использованы в лечении трофических язв практически любой этиологии, воздействуя на сходные патогенетические механизмы или в качестве симптоматического лечения; другие применяются по показаниям лишь при определенных заболеваниях.
С целью коррекции нарушений свертывающей системы и сосудорасширяющего воздействия применяются ангиопротекторы, дезагреганты и реологические препараты – ацетилсалициловая к–та, пентоксифиллин, дипиридамол, клопидогрел, тиклопидин, простагландины Е1, гепарин, низкомолекулярные гепарины, не требующие постоянного лабораторного мониторинга, гепарин–сульфаты – ломопоран, сулодексид, реополиглюкин; спазмолитики – папаверин, дротаверин, никотиновая кислота.
Пентоксифиллин представляет собой вазоактивное соединение, улучшающее реологические свойства крови и оказывающее легкое фибринолитическое действие, обладает выраженным венотонизирующим действием, высоким лимфодренирующим эффектом, а также предотвращает миграцию, адгезию и активацию лейкоцитов – важного звена патогенеза трофических расстройств [Богданец Л.И. с соавт., 2000].
Простагландины расширяют артерии малого калибра, усиливают кровоток в капиллярах, повышают фибринолитическую активность крови, подавляют агрегацию и адгезию тромбоцитов и лейкоцитов.
Пентоксифиллин и простагландины используют, как правило, в лечении критической ишемии нижних конечностей и трофических язв, связанных с нарушением артериального кровообращения, в лечении нейро–ишемической формы СДС, при КГВ, синдроме Марторелла. Хронические венозные язвы также можно рассматривать в качестве показания к применению простагландинов и пентоксифиллина.
Необходимость устранения местной гипоксии тканей делает актуальным вопрос поиска препаратов, способствующих улучшению транспорта кислорода в клетку. Депротеинизированный дериват крови телят (Актовегин) получаемый посредством диализа и ультрафильтрации гомогената, которые обеспечивают наличие в препарате только соединений с молекулярной массой менее 5000 дальтон. Препарат содержит пептиды, аминокислоты, нуклеозиды, липиды, олигосахариды, а также неорганические электролиты и микроэлементы (натрий, кальций, фосфор, магний, кремний, медь); существенно увеличивает поглощение кислорода и обмен веществ и таким образом ускоряет репаративные процессы. Особенно следует выделить наличие в составе препарата магния, который является компонентом 13 металлопротеинов и более 300 ферментов в организме и необходим для синтеза клеточных пептидов. Микроэлементы имеют большое значение для активности супероксиддисмутазы – одного из ключевых ферментов антиоксидантной защиты, который способствует превращению супероксидного радикала в его электронейтральную форму Н2О2. Кроме того, магний входит в состав глутатионпероксидазы, принимающей участие в дальнейшем метаболизме Н2О2, приводящем к образованию глутатиона [Ушкалова Е.А., 2005]. Таким образом, Актовегин обладает выраженными антиоксидантными свойствами.
Активная фракция Актовегина обладает инсулиноподобным действием: увеличивает поступление глюкозы в клетки, активирует процессы аэробного и анаэробного окисления глюкозы, повышает обмен высокоэнергетических фосфатов (АТФ, АДФ, фосфокреатина). Анаболическое и энергетическое действие активных компонентов Актовегина опосредовано воздействием на пострецепторные механизмы действия инсулина: активируя пируватдегидрогеназу, участвующую в метаболическом каскаде окисления глюкозы, он увеличивает утилизацию глюкозы клетками. Под действием Актовегина в клетке возрастает аэроб¬ное окисление глюкозы, которое является наиболее энергетически выгодным, активируются ферменты окислительного фосфорилирования (сукцинатдегидрогеназа, цитохром–С–оксидаза), ускоряется процесс распада продуктов анаэробного гликолиза (лактата, гидроксибитурата). В эксперименте с применением хроматографических методов было показано, что под влиянием Актовегина биосинтез липидов может возрасти в 5 раз. Актовегин увеличивает потребление кислорода тканями, повышает устойчивость к гипоксии. Под влиянием препарата значительно улучшается диффузия и утилизация кислорода в нейрональных структурах.
Комплексное и ступенчатое применение препарата Актовегин (парентеральные, пероральные, местные формы) позволяет сохранить преемственность лечения и достичь отличного результата [Гусева С.Л. с соавт.; Учкин И.Г. с соавт.; Шипилов Г.Ф., 2008] однако следует помнить и о дозозависимости эффекта: по мнению многих отечественных и зарубежных авторов, суточная доза Актовегина должна составлять не менее 1000 мг [Балаболкин М.И. с соавт., 2000; Креминская В.М. с соавт., 2006; Львова Л.В., 2003 и др.]. Нами используется следующая схема введения препарата: в/в инфузия в течение 10 дней по 1000–2000 мг (инфузионные флаконы или ампулы по 5–10 мл) с последующим переходом на пероральную форму по 6 таб./сут. на 20 дней. По данным проведенного в 2008 г. в 26 центрах России, Украины и Казахстана мультицентрового рандомизированного двойного слепого плацебо–контролируемого исследования, у больных сахарным диабетом пероральный прием препарата рекомендован на срок до 5 месяцев («Diabetes Care», май 2009 г.).
Флеботропные препараты защищают от гипоксии венозный эндотелий; предупреждают появление рефлюкса, подавляя адгезию лейкоцитов к венозному эндотелию стенки и клапана (препятствуют патологическому ремоделированию венозной стенки); увеличивают резистентность капилляров и снижают их патологическую проницаемость; улучшают лимфодренаж; уменьшают воспалительный ответ за счет подавления активности свободных радикалов и ферментов: эластазы и гиалуронидазы; улучшают гемореологию за счет уменьшения агрегации эритроцитов, снижения вязкости крови и повышения скорости движения эритроцитов.
В лечении диабетической нейропатии при СДС применяются препараты a–липоевой кислоты – улучшение трофики нейронов, регулирование липидного и углеводного обмена, антиоксидантное, гепатопротекторное и дезинтоксикационное действие; препараты витаминов группы В; толперизон – миорелаксант центрального действия, усиливающий периферический кровоток; антидепрессанты, противосудорожные, нейролептики, ингибиторы альдоредуктазы, g–линолевая к–та. Необходимо отметить, что препараты указанных групп не являются альтернативой назначению Актовегина – их комплексное применение потенцирует клинический эффект. Бенфотиамин влияет не только на нормализацию функций вегетативной нервной системы, уменьшение проявлений нейропатии (болевой синдром, парестезии, чувствительность), но и уменьшает активность перекисного окисления липидов и увеличивает активность антиоксидантной защиты. Аналогичная терапия может быть показана и при нейротрофических язвах.
Также с целью снижения активности перекисного окисления липидов применяют антиоксиданты.
Антибактериальные препараты. Показанием к проведению антибактериальной терапии служат синдром системной воспалительной реакции, признаки острого инфекционного воспаления мягких тканей, окружающих трофическую язву, или высокая степень ее бактериальной контаминации, составляющая 107 и более микробных тел на грамм ткани. Возможно эмпирическое назначение препаратов с учетом наиболее вероятных штаммов микроорганизмов, вегетирующих в трофических язвах (фторхинолоны, защищенные b–лактамные препараты) с последующей идентификацией микробной флоры и определением ее чувствительности к антибактериальным препаратам и коррекцией терапии. Клинически и экономически целесообразно придерживаться принципов деэскалации и ступенчатой терапии; длительность антибиотикотерапии в некоторых случаях может достигать 2 месяцев (например, при обширных гнойно–некротических процессах при нейро–ишемической форме СДС). Следует воздерживаться от применения аминогликозидов ввиду их нефротоксичности у больных с диабетической или токсической нефропатией и при заинтересованности почек при системных заболеваниях.
Антимикотики. Хронические язвы, особенно на фоне сахарного диабета, гематологических и онкологических заболеваний, ВИЧ–инфекций, приема стероидов, помимо микробных ассоциаций, как правило, контаминированы и грибами, чаще дрожжами (различные виды Candida), поэтому необходима их верификация и назначение соответствующего антимикотика (флуконазол, вориконазол, каспофунгин и др.).
В лечении специфических и инфекционных трофических язв, а также язв при системных заболеваниях в первую очередь необходима терапия основного заболевания – например, антибактериальная терапия рифампицином в случае язвы Бурули. В лечении токсического эпидермального некролиза Лайелла, при КГВ и ливедо–васкулитах рекомендовано применение цитостатиков, кортикостероидов, НПВП, интерферонов, гепарина, проведение мощной детоксикационной терапии.
Местное лечение
Туалет трофической язвы. При обработке трофической язвы оптимальным можно считать струйное промывание ее поверхности стерильным охлажденным озонированным физиологическим раствором (первая фаза раневого процесса), или подогретым до 37°С физиологическим раствором (вторая и третья фаза раневого процесса). Следует избегать применения концентрированных антисептиков (йод–повидон, перекись водорода, мирамистин, гипохлорид натрия и др.), традиционно используемых при острых ранах. В условиях трофических язв они не только уничтожают микроорганизмы, но и оказывают цитотоксическое действие, повреждая грануляционную ткань.
Препараты местного действия. Несколько лет назад была сформулирована теория обработки основания раны «Wound Bed Preparation» [Falanga V., 2002]. «Wound Bed Preparation» – стратегия обработки основания раны с целью перевода хронической раны в острую и удаления как некротического компонента, состоящего из некротической ткани, так и фенотипически измененных клеток края и основания раны и продуцируемого ими экссудата.
Необходимость подобной агрессивной обработки диктуется целым рядом причин: наличие некротических тканей, фибринной пленки является потенциальным субстратом развития инфекционных осложнений; клеточные линии, находящиеся в крае хронической раны, претерпевают фенотипическую трансформацию, что ведет к нарушению процессов регенерации. Применение любых перевязочных материалов – и самых простых, и ультрасовременных – не даст положительных результатов без предварительной подготовки раны. Дебридмент (удаление некротических тканей и экссудата) занимает одно из ключевых мест в реализации препарирования раневого ложа. Для этого широко используют разнообразные протеолитические ферменты. Одним из первых начали применять растительный фермент папаин, затем препараты, созданные из продуктов жизнедеятельности стрептококка (рибонуклеаза, гиалуронидаза, нуклеотидаза и нуклеозидаза, ультрализин).
В 70–80 годы прошлого века в нашей стране были весьма популярны выкристаллизованные трипсин и химотрипсин [Григорян А.В. и соавт., 1979; 1985; Хохлов А.М., 1989; Васютков В.Я. и соавт., 1993]. Несмотря на оптимистические прогнозы, кристаллическая форма протеолитических ферментов не нашла широкого клинического применения – они активны лишь во влажной среде при фиксированном значении рН=6 [Torrance C., 1985; Taylor S. et al., 1986; Stuck J., 1995], расщепляют только компоненты раневого экссудата, не оказывая никакого действия на коллаген, а также повреждают компоненты регенерирующего соединительнотканного матрикса [Flanga V., 2002].
Коллагеназа – водорастворимый фермент, избирательно расщепляет лишенный мукополисахаридного футляра «мертвый» коллаген на границе живых и девитализированных тканей, которые быстро и атравматично отделяются от раневого ложа. Коллагеназа не только не повреждает компоненты соединительнотканного матрикса, но и увеличивает пролиферацию кератиноцитов почти в 10 раз [Flanga V., 2002]. Коллагеназа входит в состав мази «Ируксол», широко применяемой для лечения трофических язв [Липницкий М.Е. и соавт. 1981, 1987, 2001].
Хорошо зарекомендовала себя в клинической практике отечественная мазь Стрептолавен, содержащая антисептик мирамистин и коллагенолитический фермент ультрализин.
В первой фазе раневого процесса целесообразно применение не только антисептиков и протеолитических ферментов, но и сорбентов; мы используем и рекомендуем отечественные препараты Диoтeвин – дpeниpующий copбeнт c aнтиceптикoм (диоксидин) и пpoтeoлитичecким фepмeнтoм (террилитин) для лeчeния гнoйнo–нeкpoтичecкиx paн paзличнoй этиoлoгии.
Во вторую и третью фазы раневого процесса с целью ускорения пролиферации и регенерации тканей на фоне антимикробного воздействия целесообразно применение гиалуроната цинка и мази Эбермин, а также местных форм Актовегина (во вторую фазу – в форме геля, в третью – мази).
Для симптоматического лечения при ХВН можно использовать местные лекарственные препараты, в состав которых включены флеботропные препараты и гепарин. Эффективность местных лекарственных препаратов в значительной мере зависит от концентрации действующего вещества. Гепарин в концентрации не менее 500 МЕ в 1 г оказывает противовоспалительное и анальгезирующее действие за счет инактивации гистамина и гиалуронидазы, а также потенцирует антитромботический эффект. Гели, содержащие 1000 МЕ гепарина в 1 г, демонстрируют более выраженный терапевтический эффект.
Раневые покрытия. Выбор того или иного перевязочного средства требует обязательного учета фазы течения раневого процесса и степени экссудации. Так, повязки, применение которых рационально в фазу воспаления, благодаря структуре своего материала способны инактивировать раневой экссудат, способствуют необратимой элиминации микроорганизмов, токсинов и тканевого детрита, стимулируя при этом процесс отторжения некротизированных тканей. В свою очередь покрытия, используемые при лечении «чистых» заживающих язв, поддерживают необходимую влажность и аэрацию, надежно защищают от механических повреждений и вторичной контаминации, стимулируют репаративные процессы.
В настоящее время в международной практике доминирует концепция заживления трофических язв во влажной среде [Winter G., 1962; Maibach J., 1963]. Для этого применяют разнообразные раневые покрытия, обеспечивающие: аутолитическую очистку язвы и поглощение раневого экссудата; влажную среду для миграции клеток, пролиферации, дифференциации и образования новых сосудов; термозащиту и температурную стабильность язвенной поверхности; защиту от внешней суперинфекции; безболезненное и атравматичное удаление повязки; гипоаллергенность. Эти покрытия просты в использовании, экономичны по стоимости и затратам времени.
Раневые покрытия в зависимости от их состава, физико–химических свойств и особенностей клинического применения представлены в таблице 3.
Биопрепараты. Принципиально новым и весьма перспективным направлением в лечении рефрактерных трофических язв может стать применение различных факторов роста, избирательно воздействующих на тот или иной компонент соединительной ткани (тромбоцит–синтезирующий фактор роста – PDGF; фактор роста фибробластов – FGF; эпидермальный фактор роста – EGF; трансформирующий фактор роста b–типа – TGF).
Leigh J.M., Purkis P.E., Navsaria H.A. et al. сообщили в 1987 г. о применении культивированных клеток (кератиноцитов) при лечении трофических язв, развившихся вследствие хронической венозной недостаточности, не получивших широкого распространения ввиду высокой стоимости. В 1993 г. в Институте хирургии им. А.В. Вишневского РАМН был разработан оригинальный и эффективный способ лечения ожоговых ран на основе применения культивированных фибробластов [Саркисов Д.С. с соавт.,1991; Федоров В.Д. с соавт., 1993], что в 10–15 раз дешевле, чем применение кератиноцитов. В 1998 г. в США впервые в мире был лицензирован и получил разрешение FDA к применению в клинической практике первый коммерческий тканевой продукт Apligraf, состоящий из биодеградируемой коллагеновой матрицы на основе бычьего коллагена, аллогенных донорских кератиноцитов и фибробластов.
Экономически более оправдано применение ксеногенной твердой мозговой оболочки животных [Родин Ю.А., Родин А.Ю., 2003], а также обогащенной тромбоцитами плазмы (БоТП) [Зинин В.Ю. с соавт., 2007].
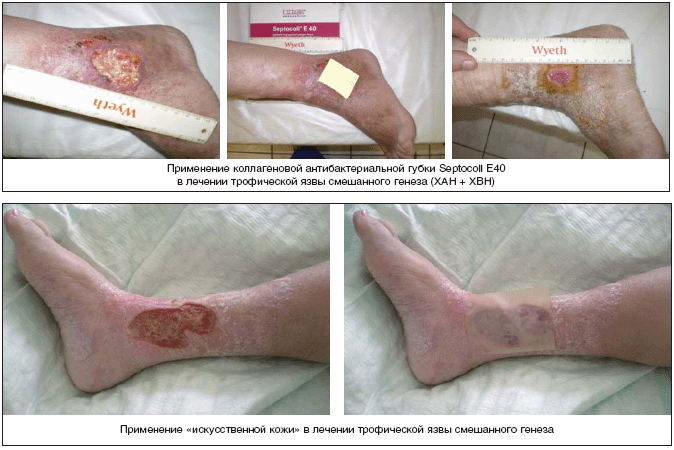
Нами апробировано применение импрегнированной двумя солями гентамицина коллагеновой губки Septocoll Е, а также отечественной пленки «искусственная кожа».
Дополнительные методы лечения
Гипербарическая оксигенация (ГБО) нарушает процессы жизнедеятельности микробов и снижает их резистентность к антибактериальной терапии. Также отмечено положительное влияние ГБО на состояние свертывающей системы крови в плане снижения концентрации фибриногена и повышения фибринолитической активности [Ефунин С.Н., 1986].
Баротерапия в камере Кравченко (камера локального отрицательно давления) показана при облитерирующем эндартериите и атеросклерозе артерий конечностей при ХАН I–II стадии, ангиоспазме, синдроме Рейно. Противопоказаниями являются ХАН III и IV стадии, ХВН, злокачественные опухоли, туберкулез, инфекционные болезни, декомпенсация сердечной деятельности, выраженные явления склероза сосудов головного мозга/сердца/почек, гипертоническая болезнь I и II стадии с высокими цифрами давления и наклонностью к гипертоническим кризам, ИБС, последствия ОНМК.
УЗ–кавитация ран. Наряду с собственным бактерицидным эффектом низкочастотный УЗ существенно усиливает действие многих антибиотиков и антисептиков на различные микроорганизмы. Ультразвук стимулирует внутриклеточный биосинтез и регенераторные процессы, вызывает расширение кровеносных сосудов и увеличение регионарного кровотока в 2–3 раза, инициирует благоприятные изменения в микроциркуляторном русле и адвентиции сосудов, развитие коллатералей, что очень важно при воспалительных и гнойно–деструктивных процессах. УЗ оказывает противовоспалительное действие за счет улучшения устранения застойных явлений, рассасывания инфильтратов, повышения фагоцитарной активности лейкоцитов и уровня неспецифической защиты. Активизация ультразвуком лизосомальных ферментов макрофагов приводит к очищению воспалительного очага от клеточного детрита и патогенной микрофлоры в экссудативной стадии. Также УЗ–волны ускоряют синтез коллагена фибробластами и образование грануляционной ткани в пролиферативной стадии воспаления.
Лазеротерапия обладает спазмолитическим, обезболивающим, противовоспалительным и биостимулирующим эффектами. Однако следует помнить о статистически достоверном увеличении количества атипичных клеток в зоне лазерного облучения [Rick K., 1999].
Магнитотерапию назначают для оказания сосудорасширяющего, обезболивающего, противоотечного и седативного действия.
Ультрафиолетовое облучение с длиной волны 297 нм вызывает расширение сосудов микроциркуляторного русла, повышает фагоцитарную активность лейкоцитов, усиливает общую сопротивляемость организма неблагоприятным факторам за счет по¬вышения адаптационных возможностей.
Озонотерапия оказывает бактерицидный и бактериостатический эффект, усиливает микроциркуляцию, улучшает реологические свойства крови, способствует очищению ран и ускорению эпителизации, нормализует соотношение процессов перекисного окисления липидов и антиоксидантной защиты, обладает противовоспалительным и иммуномоделирующим действием.
NO–терапию используют в лечении хронических заболеваний периферических сосудов. Экзогенный оксид азота, получаемый из атмосферного воздуха, оказывает эндотелий–протективное действие, стимулирует рост соединительной ткани, а также обладает бактерицидным эффектом. Монооксид азота увеличивает скорость регенерации кожи и усвоение тканями кислорода, кроме того, он убивает всех известных бактерий.
Бальнеотерапия. В отсутствие острых воспалительных процессов при лечении больных с ХЗВ и ХВН могут быть использованы грязелечение, гидро– и бальнеотерапия. Грязелечение применяют при ХВН в стадии трофических расстройств, при липодерматосклерозе, экссудативном дерматите и экземе.
Биологическая санация трофических язв. В настоящее время возрождается интерес к методу очищения гнойно–некротических язв с использованием личинок зеленых мух (Larval therapy). Специально выращенные личинки при помещении в рану оказывают очищающее воздействие посредством выделения мощных протеаз. Под их воздействием девитализированные ткани подвергаются некролизу, становятся аморфными и поглощаются личинками. Основная проблема биологической санации трофических язв заключается в неоднозначном этическом и эстетическом восприятии метода врачами и пациентами.
Лечение трофических язв в управляемой абактериальной среде. Метод бесповязочного лечения обширных гнойных ран в управляемой абактериальной среде основан на принципе гнотобиологической изоляции. Область язвенных дефектов изолируют от внешней среды в прозрачной пластиковой камере и постоянно подают в нее поток стерильного воздуха, создавая оптимальную для заживления раны среду. Недостатком метода является его громоздкость, возможность проведения только в стационарных условиях, а также значительное снижения качества жизни пациента, вынужденного длительное время соблюдать строгий постельный режим.
Экстракорпоральная детоксикация – лимфоцитаферез, регионарное внутриартериальное введение модифицированных иммуномодулятором аутолимфоцитов; плазмаферез, УФО аутокрови, инфузии гипохлорита Na. Особенностью плазмафереза является возможность улучшения реологических свойств крови за счет удаления вместе с плазмой крупнодисперсных белков, в том числе фибриногена, способного образовывать крупные гемопротеиновые конгломераты.
С целью коррекции нарушений гемолимфоциркуляции применяют физиотерапевтическое воздействие с помощью аппратов «Лимовижин» и «Пролонг».
В лечении нейропатии используют магнитотерапию, электростимуляцию поясничного нервного сплетения и мышц голени, периневральный электрофорез толперизона на пораженной конечности.
Заслуживают пристального внимания и внедрения предложенные Яншиным Д.В. (НИИСП им. Н.В. Склифасовского) методы регионарной эндолимфатической терапии и раневой оксигенации, использование оригинальных оксигенизированных микроэмульсий.
Компрессионная терапия является необходимым компонентом лечения венозных трофических язв и предотвращения их рецидива. При открытой язве с явлениями венозного отека, целлюлита и экссудации предпочтение отдают многослойным бандажам, сформированным из бинтов ограниченной растяжимости. Для профилактики рецидива, как правило, используют медицинский компрессионный трикотаж.
По мнению Partsch H., применение компрессионной терапии приводит к следующим 10 эффектам: уменьшению отека; редукции липодермосклероза; сокращению диаметра вен; увеличению скорости венозного кровотока; улучшению центральной гемодинамики; уменьшению венозного рефлюкса; улучшению функции венозной помпы; влиянию на артериальный кровоток; улучшению микроциркуляции; увеличению дренажной функции лимфатической системы.
Механизм действия компрессии при отсутствии венозного рефлюкса реализуется за счет усиления капиллярного кровотока, снижения проницаемости истонченной основной мембраны сосудов, уменьшения внутрилимфатического и интерстициального давления, уменьшения интерстициального отека, уменьшения выраженности венозной симптоматики. В случае наличия венозного рефлюкса компрессия дополнительно обеспечивает устранение или значительное уменьшение ретроградного кровотока, устранение патологической венозной емкости, уменьшение отека, лечение трофических нарушений при ХВН, их профилактика.
Перманентная эластическая компрессия показана в ряде случаев при варикозной болезни (категорический отказ пациента от хирургического лечения, наличие абсолютных противопоказаний к последнему, а также до– и послеоперационный период), при всех формах посттромбофлебитической болезни и врожденных ангиодисплазиях. Для этой цели наиболее эффективен медицинский трикотаж «Меди» или «Сигварис» II–III компрессионного класса.
Постоянная компрессия противопоказана пациентам с заболеванием периферических артерий на поздних стадиях (снижение ЛПИ ниже 0,7), при тяжелых неврологических нарушениях, лимфангиите, аллергии к компонентам компрессионного изделия. При снижении давления на лодыжке ниже 100 мм рт.ст. (но выше 60 мм рт.ст.) могут быть использованы изделия I класса компрессии. Относительными противопоказаниями к назначению компрессии являются суб– и декомпенсация кровообращения из–за опасности развития острой сердечной недостаточности, острый экссудативный дерматит.
К компрессионным повязкам относятся цинк–желатиновая повязка, предложенная Унна («сапожок Унна») и усовершенствованная Кефером, компрессионный сапожок AirCast, системы прерывистой пневматической компрессии.
Высоко эффективен применяемый нами в третьей фазе раневого процесса у больных с трофическими язвами венозной этиологии в качестве многодневного бандажа бинт Varolast, сочетающий в себе эластическую компрессию и местное лечебное воздействие на язву и окружающие ткани за счет пропитывания цинковой массой. Продольно– и поперечно–эластичный бинт со способностью к двухмерной деформации позволяет осуществить точное наложение повязки без надрезания бинта даже на трудных анатомических переходах, в результате чего возможно выравнивание непрерывного падения давления в дистальном направлении. Также в последнее время для лечения больных с трофическими язвами венозной этиологии предложена принципиально новая компрессионная система SaphenaMed UCV, представленная двумя компрессионными чулками.
Алгоритмы фармакотерапии, местных и дополнительных методов лечения указаны в таблице 4.
Подиатрия
Одним из основных моментов в лечении язвенных дефектов стоп у пациентов с нейропатической и нейроостеоартропатической формами СДС и нейротрофическими язвами является разгрузка зоны поражения. Снижение плантарного давления достигается применением ортопедической обуви (традиционно применяется «полубашмак») или индивидуальных разгрузочных ортопедических стелек (предпочтительно из термопластичных материалов) и силиконовых корректоров, или индивидуальной иммобилизирующей разгрузочной повязки Total Contact Cast.
Профилактика
1. Раннее выявление и радикальная хирургическая коррекция основного заболевания (это положение в основном справедливо в отношении варикозной болезни и облитерирующих заболеваний магистральных артерий).
2. Адекватная эластическая компрессия (при ХВН), ортопедическая обувь (при СДС).
3. Медикаментозное лечение. Целесообразно проведение поддерживающих курсов медикаментозного лечения основного заболевания (например, с применением флеботонических препаратов поливалентного механизма действия при ХВН, ангиопротекторов и дезагрегантов при ХАН и т.д.) или препаратов универсального действия (Актовегин). Продолжительность таких курсов должна быть 1–2 месяца, а их кратность зависит от тяжести заболевания и обычно составляет 2–3 раза в год.
В перерыве между курсами приема медикаментов целесообразно проводить физиотерапевтическое (магнитотерапия, лазеротерапия, квантовая аутогемотерапия и др.) и санаторно–курортное (по сердечно–сосудистому профилю) лечение.
4. Рациональная организация труда и отдыха имеет свои особенности в зависимости от основного заболевания. Так, пациенты с ХВН не могут выполнять тяжелую статическую физическую нагрузку, работать на вредных производствах (горячие цеха), длительно пребывать в неподвижном состоянии (как стоя, так и сидя). Во время отдыха оптимальным является элевация нижних конечностей выше уровня сердца, ежедневное выполнение (в горизонтальном положении) упражнений, направленных на стимуляцию работы мышечно–венозной помпы голени («велосипед», «ножницы», «березка» и др.). Из занятий физической культурой оптимальным является плавание.
5. Рациональная организация питания преследует целью контроль массы тела, исключение приема острой и соленой пищи (во избежание чрезмерной водной нагрузки, провоцирующей отечный синдром).



Литература
1. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Микроангиопатия – одно из сосудистых осложнений сахарного диабета. // Consilium medicum. – 2000. – Т. 2. – № 5.
2. Богачев В.Ю., Богданец Л.И., Кириенко А.И., Брюшков А.Ю., Журавлева О.В. Местное лечение венозных трофических язв. // Consilium medicum. – 2001. – №2. – С. 45–50.
3. Богданец Л.И., Кириенко А.И., Алексеева Е.А. Местное лечение венозных трофических язв. // Журн. «Гедеон Рихтер» в СНГ. – 2000. – № 2. – С. 58 – 60.
4. Богданец Л.И., Кошкин В.М., Кириенко А.И. Роль пентоксифиллина в лечении и профилактике трофических язв сосудистого генеза. / «Трудный пациент», Архив. – 2006. – №1.
5. Гусева С.Л., Макарова Н.Н., Трухова В.В., Хисматов Р.Р. Актовегин в лечении трофических язв нижних конечностей венозной этиологии. / РМЖ, 2008, том 16, № 29.
6. Дифференциальная диагностика кожных болезней. (Под ред. Б.А. Беренбейна и А.А. Студницина). – М. – 1989.
7. Ефунин С.Н. Руководство по гипербарической оксигенации. / М., Медицина. – 1986.
8. Захарова Е.В. ANCA–ассоциированные и криоглобулинемические васкулиты – диагностика и лечение (обзор литературы). – 2006.
9. Кириенко А.И., Богачев В.Ю., Богданец Л.И. Лечение трофических язв венозной этиологии. / Consilium medicum. – 2000. – Т. 2. – № 4.
10. Креминская В.М., Гурьева И.В. Возможность применения Актовегина при поздних осложнениях сахарного диабета. // РМЖ. – 2006.
11. Кривощеков Е.П., Яремин Б. И., Атаманов Е. В. Лечение хронической венозной недостаточности в поликлинике. / Самара, 2000. – С. 69–77.
12. Липницкий Е.М. Лечение трофических язв нижних конечностей // Москва. – 2001. – 160 с.
13. Львова Л.В. В центре внимания. // Провизор. – 2003. – № 6.
14. Любарский М.С., Смагин А.А., Хабаров Д.В., Ракитин А.А., Титова Л.В. Возможности экстракорпоральных методов в лечении трофических язв. // Матер. VIII Всеросс. съезда анестезиологов–реаниматологов. – 2002.
15. Материалы IX съезда Российского Общества Эндоскопических Хирургов.
16. Родин Ю. А., Родин А. Ю. Лечение варикозных язв голеней с помощью ксеногенной твердой мозговой оболочки животных. / Хирургия. – 2003.
17. Савельев В.С., Гологорский В.А., Кириенко А.И. и др. Флебология. Руководство для врачей. под ред. В. С. Савельева. / М., Медицина. – 2001. – 664 с.
18. Самцов В.И., Подвысоцкая И.И. Токсический эпидермальный некролиз. / Вестн. дерм. и вен. – 1979. – № 12. – С. 16.
19. Ушкалова Е.А. Антиоксидантные и антигипоксические и свойства актовегина у кардиологических больных. / Трудный пациент. – 2005. – № 3.
20. Шипилов Г.Ф. Применение Актовегина при лечении трофических язв нижних конечностей. / Издание ЦКБ ПМЦ РФ г. Москва.
21. Falanga V. Wound Bed Preparation and the Role of Enzymes: A Case for Multiple Actions of Therapeutic gents». / Wounds. 2002. – 14(2). – Р. 47–57.
22. Wagner F.W. A classification and treatment program for diabetic, neuropatic and dysvascular foot problems. / In The American Academy of Ortopaedic Surgeons instructional course lectures. – St. Louis. – Mosby Year Book. – 1979. – P. 143 – 165.












