–С–Њ–ї–µ–Ј–љ—М –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞ (–С–Я) - —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–µ –љ–µ—Г–Ї–ї–Њ–љ–љ–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–µ –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –Є–Ј–±–Є—А–∞—В–µ–ї—М–љ–Њ –њ–Њ—А–∞–ґ–∞—О—В—Б—П –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–µ –љ–µ–є—А–Њ–љ—Л –Ї–Њ–Љ–њ–∞–Ї—В–љ–Њ–є —З–∞—Б—В–Є —З–µ—А–љ–Њ–є —Б—Г–±—Б—В–∞–љ—Ж–Є–Є. –С–Я –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –Є —П–≤–ї—П–µ—В—Б—П –њ—А–Є—З–Є–љ–Њ–є –±–Њ–ї–µ–µ 80% —Б–ї—Г—З–∞–µ–≤ –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ–∞. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В —Г –Ї–∞–ґ–і–Њ–≥–Њ —Б–Њ—В–Њ–≥–Њ —З–µ–ї–Њ–≤–µ–Ї–∞ –Є, –љ–µ—Г–Ї–ї–Њ–љ–љ–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—П, –њ—А–Є–≤–Њ–і–Є—В –Ї –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є. –Ю—Б–љ–Њ–≤–љ—Л–µ –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –С–Я: –∞–Ї–Є–љ–µ–Ј–Є—П, —А–Є–≥–Є–і–љ–Њ—Б—В—М, —В—А–µ–Љ–Њ—А –њ–Њ–Ї–Њ—П –Є –њ–Њ—Б—В—Г—А–∞–ї—М–љ–∞—П –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М - —Б–≤—П–Ј–∞–љ—Л –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –і–Њ—Д–∞–Љ–Є–љ–∞ –≤ —Б—В—А–Є–∞—В—Г–Љ–µ, –Є –µ–≥–Њ –Ї–Њ—А—А–µ–Ї—Ж–Є—П, —Е–Њ—В—П –Є –љ–µ –≤–ї–Є—П–µ—В –љ–∞ –њ–µ—А–≤–Є—З–љ—Л–є –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б, –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—Б–ї–∞–±–Є—В—М –Љ–љ–Њ–≥–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –С–Я. –°—Г—Й–µ—Б—В–≤—Г—О—В 3 –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ—Л–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –≤–Њ—Б–њ–Њ–ї–љ–µ–љ–Є—П –і–µ—Д–Є—Ж–Є—В–∞ –і–Њ—Д–∞–Љ–Є–љ–∞: –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–∞ –і–Њ—Д–∞–Љ–Є–љ–∞, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б—А–µ–і—Б—В–≤, —В–Њ—А–Љ–Њ–Ј—П—Й–Є—Е —А–∞—Б–њ–∞–і –і–Њ—Д–∞–Љ–Є–љ–∞, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б—А–µ–і—Б—В–≤ - “–Ј–∞–Љ–µ–љ–Є—В–µ–ї–µ–є” –і–Њ—Д–∞–Љ–Є–љ–∞, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –њ–Њ–і–Њ–±–љ–Њ –µ–Љ—Г —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л [1, 3].
–Я–Њ—П–≤–ї–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ L-–Ф–Ю–§–Р (–ї–µ–≤–Њ–і–Њ–њ—Л) –њ—А–Њ–Є–Ј–≤–µ–ї–Њ –Ї–∞—А–і–Є–љ–∞–ї—М–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –ґ–Є–Ј–љ–Є –Љ–Є–ї–ї–Є–Њ–љ–Њ–≤ –±–Њ–ї—М–љ—Л—Е —Б –С–Я. –Ю–љ–Є –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –Њ—Б—В–∞–≤–∞—В—М—Б—П –±–∞–Ј–Є—Б–љ—Л–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ –≤ –ї–µ—З–µ–љ–Є–Є —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Э–Њ —Б–Њ –≤—А–µ–Љ–µ–љ–µ–Љ —Б—В–∞–ї–Њ —П—Б–љ–Њ, —З—В–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —А–µ—Б—Г—А—Б –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л –Њ–≥—А–∞–љ–Є—З–µ–љ, –Є —Б–њ—Г—Б—В—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –ї–µ—В –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–Њ—З—В–Є –љ–µ–Є–Ј–±–µ–ґ–љ–Њ —Б–љ–Є–ґ–∞–µ—В—Б—П, —З—В–Њ –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ–±—К—П—Б–љ—П–µ—В—Б—П –њ—А–Њ–і–Њ–ї–ґ–∞—О—Й–µ–є—Б—П –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–µ–є –љ–µ–є—А–Њ–љ–Њ–≤ —З–µ—А–љ–Њ–є —Б—Г–±—Б—В–∞–љ—Ж–Є–Є, –Ї–Њ—В–Њ—А—Г—О –њ—А–µ–њ–∞—А–∞—В—Л –ї–µ–≤–Њ–і–Њ–њ—Л –љ–µ –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—О—В. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —З–Є—Б–ї–µ–љ–љ–Њ—Б—В–Є –љ–µ–є—А–Њ–љ–Њ–≤ —Б–љ–Є–ґ–∞–µ—В—Б—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –Њ–Ї–Њ–љ—З–∞–љ–Є–є –≤ —Б—В—А–Є–∞—В—Г–Љ–µ –Ј–∞—Е–≤–∞—В—Л–≤–∞—В—М –ї–µ–≤–Њ–і–Њ–њ—Г, –њ—А–µ–≤—А–∞—Й–∞—В—М –µ–µ –≤ –і–Њ—Д–∞–Љ–Є–љ, –љ–∞–Ї–∞–њ–ї–Є–≤–∞—В—М –Љ–µ–і–Є–∞—В–Њ—А –Є –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –≤—Л–±—А–∞—Б—Л–≤–∞—В—М –µ–≥–Њ –≤ —Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї—Г—О —Й–µ–ї—М. –Я—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –ї–µ–≤–Њ–і–Њ–њ—Л –Є–Ј–Љ–µ–љ—П–µ—В—Б—П –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Т—Б–µ —Н—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –њ–Њ—А–Њ–≥–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –і–Є—Б–Ї–Є–љ–µ–Ј–Є–є –Є –љ–µ—А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ—Б—В–Є —Н—Д—Д–µ–Ї—В–∞ –ї–µ–≤–Њ–і–Њ–њ—Л - –Љ–Њ—В–Њ—А–љ—Л–Љ —Д–ї—Г–Ї—В—Г–∞—Ж–Є—П–Љ.
–С–Њ–ї–µ–µ —В–Њ–≥–Њ, —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –і–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –ї–µ–≤–Њ–і–Њ–њ–∞, –Ї–∞–Ї –Є —Б–∞–Љ –і–Њ—Д–∞–Љ–Є–љ, –Њ–Ї–∞–Ј—Л–≤–∞—О—В —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –Ї—Г–ї—М—В—Г—А—Г –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –љ–µ–є—А–Њ–љ–Њ–≤, –≤—Л–Ј—Л–≤–∞—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤. –Ш —Е–Њ—В—П –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Ж–µ–ї–Њ—Б—В–љ–Њ–≥–Њ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —Н—В–Њ—В –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Љ–Њ–ґ–µ—В –љ–Є–≤–µ–ї–Є—А–Њ–≤–∞—В—М—Б—П —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–Љ–Є –Ј–∞—Й–Є—В–љ—Л–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є –Є –Њ–±–љ–∞—А—Г–ґ–Є—В—М –µ–≥–Њ –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –Є–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–µ —Г–і–∞–µ—В—Б—П, –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л —Б–ї–µ–і—Г–µ—В –њ—А–Є–і–µ—А–ґ–Є–≤–∞—В—М—Б—П –њ—А–Є–љ—Ж–Є–њ–∞ —А–∞–Ј—Г–Љ–љ–Њ–≥–Њ –Љ–Є–љ–Є–Љ—Г–Љ–∞.
–Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –Њ—Б–Њ–±–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ—А–Є–Њ–±—А–µ—В–∞–µ—В –њ–Њ–Є—Б–Ї —Б—А–µ–і—Б—В–≤, –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л –≤ –Њ–±—Е–Њ–і –љ–µ—Г–Ї–ї–Њ–љ–љ–Њ –і–µ–≥–µ–љ–µ—А–Є—А—Г—О—Й–Є—Е –љ–Є–≥—А–Њ—Б—В—А–Є–∞—А–љ—Л—Е –љ–µ–є—А–Њ–љ–Њ–≤. –Р–≥–Њ–љ–Є—Б—В—Л –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–Р–Ф–†) –Ї–∞–Ї —А–∞–Ј –Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –Ї–ї–∞—Б—Б –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ –Є –і—А—Г–≥–Є—Е —В–Ї–∞–љ—П—Е –Њ—А–≥–∞–љ–Є–Ј–Љ–∞.
–Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Р–Ф–†
–Т—Л–і–µ–ї—П—О—В 2 –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–Њ–і–Ї–ї–∞—Б—Б–∞ –Р–Ф–†: —Н—А–≥–Њ–ї–Є–љ–Њ–≤—Л–µ –∞–≥–Њ–љ–Є—Б—В—Л, —П–≤–ї—П—О—Й–Є–µ—Б—П –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ–Є —Б–њ–Њ—А—Л–љ—М–Є (–±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ, –њ–µ—А–≥–Њ–ї–Є–і, –ї–Є–Ј—Г—А–Є–і, –Ї–∞–±–µ—А–≥–Њ–ї–Є–љ) –Є –љ–µ—Н—А–≥–Њ–ї–Є–љ–Њ–≤—Л–µ –∞–≥–Њ–љ–Є—Б—В—Л (–∞–њ–Њ–Љ–Њ—А—Д–Є–љ, –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї, —А–Њ–њ–Є–љ–Є—А–Њ–ї).
–≠—Д—Д–µ–Ї—В –Р–Ф–† –Ј–∞–≤–Є—Б–Є—В –Њ—В —В–Є–њ–∞ –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –љ–∞ –Ї–Њ—В–Њ—А—Л–µ –Њ–љ–Є –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—В. –Ґ—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ –≤—Л–і–µ–ї—П—О—В –і–≤–∞ –Њ—Б–љ–Њ–≤–љ—Л—Е —В–Є–њ–∞ –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (D1 –Є D2), –Ї–Њ—В–Њ—А—Л–µ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –њ–Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ-–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ —Г–і–∞–ї–Њ—Б—М –≤—Л—П–≤–Є—В—М –љ–µ –Љ–µ–љ–µ–µ 5 —В–Є–њ–Њ–≤ –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤: –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Є–Ј –љ–Є—Е –Є–Љ–µ—О—В —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ D1 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (D1, D5), –і—А—Г–≥–Є–µ - —Б–≤–Њ–є—Б—В–≤–∞ D2 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (D2, D3, D4). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Є–љ—П—В–Њ –≥–Њ–≤–Њ—А–Є—В—М –Њ 2 –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–µ–Љ–µ–є—Б—В–≤–∞—Е –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (D1 –Є D2). –≠—Д—Д–µ–Ї—В—Л —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є D1 –Є D2 –Њ–Ї–∞–Ј—Л–≤–∞—О—В—Б—П —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –љ–µ —В–Њ–ї—М–Ї–Њ –≤ —Б–Є–ї—Г –љ–µ–Њ–і–Є–љ–∞–Ї–Њ–≤—Л—Е –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, –Ј–∞–њ—Г—Б–Ї–∞–µ–Љ—Л—Е —Б—В–Є–Љ—Г–ї—П—Ж–Є–µ–є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –љ–Њ –Є –≤ —Б–Є–ї—Г —А–∞–Ј–ї–Є—З–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, —Б—В–Є–Љ—Г–ї—П—Ж–Є—П D1 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —З–µ—А–µ–Ј –∞–Ї—В–Є–≤–∞—Ж–Є—О –њ—А—П–Љ–Њ–≥–Њ –њ—Г—В–Є, —Б–ї–µ–і—Г—О—Й–µ–≥–Њ –Њ—В —Б—В—А–Є–∞—В—Г–Љ–∞ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Ї –≤—Л—Е–Њ–і–љ—Л–Љ —Б—В—А—Г–Ї—В—Г—А–∞–Љ –±–∞–Ј–∞–ї—М–љ—Л—Е –≥–∞–љ–≥–ї–Є–µ–≤ –Є –і–∞–ї–µ–µ —З–µ—А–µ–Ј —В–∞–ї–∞–Љ—Г—Б –Ї –Ї–Њ—А–µ, –Њ–±–ї–µ–≥—З–∞–µ—В –∞–і–µ–Ї–≤–∞—В–љ—Л–µ –≤ –і–∞–љ–љ—Л–є –Љ–Њ–Љ–µ–љ—В –і–≤–Є–ґ–µ–љ–Є—П, –Є–љ–Є—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–µ –≤ –њ—А–µ–Љ–Њ—В–Њ—А–љ–Њ–є –Ї–Њ—А–µ. –°—В–Є–Љ—Г–ї—П—Ж–Є—П D2 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —З–µ—А–µ–Ј —В–Њ—А–Љ–Њ–ґ–µ–љ–Є–µ “–љ–µ–њ—А—П–Љ–Њ–≥–Њ” –њ—Г—В–Є, —Б–ї–µ–і—Г—О—Й–µ–≥–Њ –Њ—В —Б—В—А–Є–∞—В—Г–Љ–∞ –Ї –≤—Л—Е–Њ–і–љ—Л–Љ —Б—В—А—Г–Ї—В—Г—А–∞–Љ –±–∞–Ј–∞–ї—М–љ—Л—Е –≥–∞–љ–≥–ї–Є–µ–≤ —З–µ—А–µ–Ј –ї–∞—В–µ—А–∞–ї—М–љ—Л–є —Б–µ–≥–Љ–µ–љ—В –±–ї–µ–і–љ–Њ–≥–Њ —И–∞—А–∞ –Є —Б—Г–±—В–∞–ї–∞–Љ–Є—З–µ—Б–Ї–Њ–µ —П–і—А–Њ, –Є –≤ –љ–Њ—А–Љ–µ —В–Њ—А–Љ–Њ–Ј—П—Й–µ–≥–Њ –љ–µ–∞–і–µ–Ї–≤–∞—В–љ—Л–µ –і–≤–Є–ґ–µ–љ–Є—П, —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є. –С–Њ–ї—М—И–∞—П —З–∞—Б—В—М –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –љ–µ–є—А–Њ–љ–Њ–≤ –Є–Љ–µ–µ—В –њ—А–µ—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є–µ –∞—Г—В–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л, —А–Њ–ї—М –Ї–Њ—В–Њ—А—Л—Е –≤—Л–њ–Њ–ї–љ—П—О—В D2 –Є D3 —А–µ—Ж–µ–њ—В–Њ—А—Л: –Є—Е –∞–Ї—В–Є–≤–∞—Ж–Є—П —Б–љ–Є–ґ–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–є—А–Њ–љ–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Б–Є–љ—В–µ–Ј –Є –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –і–Њ—Д–∞–Љ–Є–љ–∞. –І–µ—А–µ–Ј –∞–Ї—В–Є–≤–∞—Ж–Є—О –∞—Г—В–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Љ–Њ–ґ–µ—В –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—В—М—Б—П –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Р–Ф–†.
–Я—А–Є –С–Я –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Э–∞ –љ–∞—З–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–љ–Є–ґ–∞–µ—В—Б—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–µ—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є—Е D2 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ –љ–µ–є—А–Њ–љ–∞—Е —З–µ—А–љ–Њ–є —Б—Г–±—Б—В–∞–љ—Ж–Є–Є, –љ–Њ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –і–µ–љ–µ—А–≤–∞—Ж–Є–Њ–љ–љ–∞—П –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–Њ—Б—В—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ D2) –≤ —Б—В—А–Є–∞—В—Г–Љ–µ. –Я—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Р–Ф–† —Б–≤—П–Ј—Л–≤–∞—О—В –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б–Њ —Б—В–Є–Љ—Г–ї—П—Ж–Є–µ–є D2 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Э–Њ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –Є–Ј—Г—З–∞–µ—В—Б—П –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–≥–Њ–љ–Є—Б—В–Њ–≤ D1 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —А–µ–ґ–µ –≤—Л–Ј—Л–≤–∞—О—В –і–Є—Б–Ї–Є–љ–µ–Ј–Є–Є, —З–µ–Љ –∞–≥–Њ–љ–Є—Б—В—Л D2 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–Ф–† –љ–∞ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –С–Я
–Ю–≥—А–∞–љ–Є—З–µ–љ–љ–Њ—Б—В—М –њ–µ—А–Є–Њ–і–∞ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л –Ј–∞—Б—В–∞–≤–ї—П–µ—В –Њ—В–Ї–ї–∞–і—Л–≤–∞—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л –≤–њ–ї–Њ—В—М –і–Њ —В–Њ–≥–Њ –Љ–Њ–Љ–µ–љ—В–∞, –Ї–Њ–≥–і–∞ –і—А—Г–≥–Є–µ –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞ –Њ–Ї–∞–ґ—Г—В—Б—П –љ–µ –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є —Б–Ї–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–∞—В—М –љ–∞—А–∞—Б—В–∞—О—Й–Є–є –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–є –і–µ—Д–µ–Ї—В. –†—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –љ–∞ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –С–Я –Р–Ф–† —Г —З–∞—Б—В–Є –±–Њ–ї—М–љ—Л—Е –љ–µ —Г—Б—В—Г–њ–∞—О—В –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ –ї–µ–≤–Њ–і–Њ–њ—Л –Є –њ–Њ–Ј–≤–Њ–ї—П—О—В –Њ—В—Б—А–Њ—З–Є—В—М –Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ—Б—П—Ж–µ–≤, –∞ –Є–љ–Њ–≥–і–∞ –Є –ї–µ—В [17, 19].
–Т—Л–њ–Њ–ї–љ–µ–љ–љ—Л–µ –љ–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –Р–Ф–† (–±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ, –њ–µ—А–≥–Њ–ї–Є–і –Є –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї), –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л–µ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є, —Б–њ–Њ—Б–Њ–±–љ—Л –≤—Л–Ј–≤–∞—В—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —Г –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —З–∞—Б—В–Є –±–Њ–ї—М–љ—Л—Е —Б —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–µ–є –С–Я. –Ґ–∞–Ї, –љ–∞ —Д–Њ–љ–µ 3 –Љ–µ—Б—П—З–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ–Њ–Љ (–≤ –і–Њ–Ј–µ –і–Њ 20 –Љ–≥/—Б—Г—В) —Б—А–µ–і–љ—П—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ–∞, –Њ—Ж–µ–љ–Є–≤–∞–µ–Љ–∞—П —Б –њ–Њ–Љ–Њ—Й—М—О –£–љ–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є —А–µ–є—В–Є–љ–≥–Њ–≤–Њ–є —И–Ї–∞–ї—Л –С–Я, —Б–љ–Є–Ј–Є–ї–∞—Б—М –љ–∞ 25%. –Х—Й–µ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–Њ–Ї–∞–Ј–∞–ї –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї: –Ї –Ї–Њ–љ—Ж—Г 4-–Љ–µ—Б—П—З–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П (–≤ –і–Њ–Ј–µ –і–Њ 4,5 –Љ–≥/—Б—Г—В) –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –љ–∞ 47,7%.
–Ю—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –Р–Ф–† –Љ–Њ–≥—Г—В —Б—Л–≥—А–∞—В—М –≤ –љ–∞—З–∞–ї—М–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –Љ–Њ–ї–Њ–і—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –С–Я (–Љ–Њ–ї–Њ–ґ–µ 50 –ї–µ—В). –Я—А–Є —Н—В–Њ–Љ —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М 2 —Д–∞–Ї—В–Њ—А–∞. –Т–Њ-–њ–µ—А–≤—Л—Е, —Г –Љ–Њ–ї–Њ–і—Л—Е –±–Њ–ї—М–љ—Л—Е –≤—Л—И–µ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –ґ–Є–Ј–љ–Є –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Њ–љ–Є –њ–Њ—З—В–Є –љ–µ–Є–Ј–±–µ–ґ–љ–Њ —Б—В–Њ–ї–Ї–љ—Г—В—Б—П —Б –Є—Б—В–Њ—Й–µ–љ–Є–µ–Љ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л. –Т–Њ-–≤—В–Њ—А—Л—Е, –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –ї–µ–≤–Њ–і–Њ–њ—Л —Г –љ–Є—Е –±—Л—Б—В—А–µ–µ, —З–µ–Љ —Г –њ–Њ–ґ–Є–ї—Л—Е, —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –Љ–Њ—В–Њ—А–љ—Л–µ —Д–ї—Г–Ї—В—Г–∞—Ж–Є–Є –Є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–Є. –Ш–Љ–µ–љ–љ–Њ –≤ —Н—В–Њ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е –Њ—В—Б—А–Њ—З–Є—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л. –С–ї–∞–≥–Њ–і–∞—А—П –і–ї–Є—В–µ–ї—М–љ–Њ–Љ—Г –њ–µ—А–Є–Њ–і—Г –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є (–Њ—В 5-6 –і–Њ 24 —З —Г —А–∞–Ј–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Р–Ф–†, —Г –ї–µ–≤–Њ–і–Њ–њ—Л - 60-90 –Љ–Є–љ) –Є –Њ—В—Б—Г—В—Б—В–≤–Є—О –Ї–Њ–љ–Ї—Г—А–µ–љ—Ж–Є–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –њ–Є—Й–µ–≤—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Ј–∞ –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –≤ –Ї—А–Њ–≤—М –Є–ї–Є –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А, –Р–Ф–† –≤—Л–Ј—Л–≤–∞—О—В –±–Њ–ї–µ–µ —Б—В–∞–±–Є–ї—М–љ—Г—О –Є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —Б—В–Є–Љ—Г–ї—П—Ж–Є—О –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —З—В–Њ —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Љ–Њ—В–Њ—А–љ—Л—Е —Д–ї—Г–Ї—В—Г–∞—Ж–Є–є –Є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–є, –Ї–Њ—В–Њ—А—Л–µ –≤–Њ –Љ–љ–Њ–≥–Њ–Љ —Б–≤—П–Ј–∞–љ—Л —Б –љ–µ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–µ—А—Л–≤–Є—Б—В–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–µ–є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –ї–µ–≤–Њ–і–Њ–њ–Њ–є.
–Ш —В–Њ–ї—М–Ї–Њ –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –Р–Ф–† –Є–ї–Є –Є—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б –∞–Љ–∞–љ—В–∞–і–Є–љ–Њ–Љ, —Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є–Ї–∞–Љ–Є –Є–ї–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –Ь–Р–Ю –Т —Б–µ–ї–µ–≥–Є–ї–Є–љ–Њ–Љ –љ–µ –њ—А–Є–љ–µ—Б–ї–∞ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П, —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –ї–µ–≤–Њ–і–Њ–њ—Л. –Э–Њ –Є –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–Ф–† –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–∞ –і–ї–Є—В–µ–ї—М–љ—Л–є —Б—А–Њ–Ї –Њ–≥—А–∞–љ–Є—З–Є—В—М –і–Њ–Ј—Г –ї–µ–≤–Њ–і–Њ–њ—Л —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ –љ–µ–±–Њ–ї—М—И–Њ–є –≤–µ–ї–Є—З–Є–љ–Њ–є (100-200 –Љ–≥/—Б—Г—В), —З—В–Њ —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е —Д–ї—Г–Ї—В—Г–∞—Ж–Є–є –Є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–є [10].
–Э–µ—Б–Ї–Њ–ї—М–Ї–Њ –Є–љ–∞—П —В–∞–Ї—В–Є–Ї–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –≤ –і—А—Г–≥–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –Ї–∞—В–µ–≥–Њ—А–Є—П—Е. –Т –≤–Њ–Ј—А–∞—Б—В–µ 50 - 70 –ї–µ—В –ї–µ—З–µ–љ–Є–µ –љ–∞—З–Є–љ–∞—О—В —Б –Р–Ф–† —В–Њ–ї—М–Ї–Њ –њ—А–Є –Љ–∞–ї–Њ–є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –і–µ—Д–µ–Ї—В–∞ –Є –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є—Е –Ї —А–∞–Ј–≤–Є—В–Є—О –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Э–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є —Б–Њ–≤–µ—В—Г—О—В –љ–∞—З–Є–љ–∞—В—М –ї–µ—З–µ–љ–Є–µ —Б –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л, –Є –ї–Є—И—М –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Љ–∞–ї—Л–µ –µ–µ –і–Њ–Ј—Л (300-400 –Љ–≥/—Б—Г—В) –љ–µ –њ—А–Є–љ–Њ—Б—П—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, –і–Њ–±–∞–≤–Є—В—М –Р–Ф–†, —З—В–Њ–±—Л –Є–Ј–±–µ–ґ–∞—В—М –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–Є—П –і–Њ–Ј—Л –ї–µ–≤–Њ–і–Њ–њ—Л [9]. –Ф–Њ–±–∞–≤–ї–µ–љ–Є–µ –Р–Ф–† –Ї –њ—А–µ–њ–∞—А–∞—В–∞–Љ –ї–µ–≤–Њ–і–Њ–њ—Л –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–љ–Є–Ј–Є—В—М –і–Њ–Ј—Г –ї–µ–≤–Њ–і–Њ–њ—Л –±–µ–Ј –њ–Њ—В–µ—А–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–∞ 10-30% –Є —В–µ–Љ —Б–∞–Љ—Л–Љ –Њ—В—Б—А–Њ—З–Є—В—М —А–∞–Ј–≤–Є—В–Є–µ –Љ–Њ—В–Њ—А–љ—Л—Е —Д–ї—Г–Ї—В—Г–∞—Ж–Є–є.
–Т –≤–Њ–Ј—А–∞—Б—В–µ —Б—В–∞—А—И–µ 70 –ї–µ—В –њ—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –ї–µ—З–µ–љ–Є–µ –љ—Г–ґ–љ–Њ —Б—А–∞–Ј—Г –ґ–µ –љ–∞—З–Є–љ–∞—В—М —Б –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л. –£ –±–Њ–ї—М–љ—Л—Е —Н—В–Њ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ—Л –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Є –і–µ–Љ–µ–љ—Ж–Є—П, –њ–Њ—Н—В–Њ–Љ—Г —Г –љ–Є—Е —З–∞—Й–µ –≤–Њ–Ј–љ–Є–Ї–∞—О—В –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П (–≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –≥–∞–ї–ї—О—Ж–Є–љ–∞—Ж–Є–Є) –њ—А–Є –ї–µ—З–µ–љ–Є–Є –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –Р–Ф–†. –Ъ —В–Њ–Љ—Г –ґ–µ —А–Є—Б–Ї —А–∞–љ–љ–µ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П —Д–ї—Г–Ї—В—Г–∞—Ж–Є–є –Є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–є —Г –љ–Є—Е –Љ–µ–љ—М—И–µ, –∞ –Њ–ґ–Є–і–∞–µ–Љ–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –ґ–Є–Ј–љ–Є –љ–µ –љ–∞—Б—В–Њ–ї—М–Ї–Њ –≤—Л—Б–Њ–Ї–∞, —З—В–Њ–±—Л —Г—Б–њ–µ—В—М –Є–Ј—А–∞—Б—Е–Њ–і–Њ–≤–∞—В—М —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —А–µ—Б—Г—А—Б –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л. –Р–Ф–† —Г –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е –і–Њ–±–∞–≤–ї—П—О—В –њ—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е —Д–ї—Г–Ї—В—Г–∞—Ж–Є–є –Є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–є –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –і–µ–Љ–µ–љ—Ж–Є–Є.
–Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ –і–Њ–≤–Њ–і–Њ–Љ –≤ –њ–Њ–ї—М–Ј—Г —А–∞–љ–љ–µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Р–Ф–† —П–≤–ї—П–µ—В—Б—П –Є—Е –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–µ –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ [18]. –Т—Л–≤–Њ–і –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–Љ –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–Љ –і–µ–є—Б—В–≤–Є–Є –Р–Ф–† –Њ—Б–љ–Њ–≤–∞–љ –љ–∞ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е, –∞ —В–∞–Ї–ґ–µ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —В–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–і–њ–Њ—Б—Л–ї–Ї–∞—Е. –Ь–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Р–Ф–† –љ–µ —Б–≤—П–Ј–∞–љ —Б –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –њ—А–Њ—Ж–µ—Б—Б–∞–Љ–Є –Є –љ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О —В–Њ–Ї—Б–Є—З–љ—Л—Е —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Р–Ф–† –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ: —Б —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї—А—Г–≥–Њ–Њ–±—А–Њ—В–∞ –і–Њ—Д–∞–Љ–Є–љ–∞ (–±–ї–∞–≥–Њ–і–∞—А—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О –љ–∞ D2 –∞—Г—В–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л); —Б –њ—А—П–Љ—Л–Љ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ —З–µ—А–µ–Ј —Б—В–Є–Љ—Г–ї—П—Ж–Є—О D1 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Є —Б–Є–љ—В–µ–Ј –±–µ–ї–Ї–Њ–≤ c –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є, —П–≤–ї—П—О—Й–Є—Е—Б—П ‘’—З–Є—Б—В–Є–ї—М—Й–Є–Ї–∞–Љ–Є’’ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤, –∞ —В–∞–Ї–ґ–µ –Є–љ–і—Г–Ї—Ж–Є—О —Д–µ—А–Љ–µ–љ—В–Њ–≤ —Б –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є; —Б–Њ —Б—В–Є–Љ—Г–ї—П—Ж–Є–µ–є –∞—Г—В–Њ—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–µ–є—А–Њ–љ–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —В–Њ–љ—Г—Б–∞ —А–∞—Б—В–Њ—А–Љ–Њ–ґ–µ–љ–љ—Л—Е –њ—А–Є –С–Я —Б—В—А—Г–Ї—В—Г—А, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Б—Г–±—В–∞–ї–∞–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —П–і—А–∞, –љ–µ–є—А–Њ–љ—Л –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤—Л–і–µ–ї—П—О—В –љ–∞ —Б–≤–Њ–Є—Е –Њ–Ї–Њ–љ—З–∞–љ–Є—П—Е (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –≤ —З–µ—А–љ–Њ–є —Б—Г–±—Б—В–∞–љ—Ж–Є–Є) –≥–ї—Г—В–∞–Љ–∞—В –Є —В–µ–Љ —Б–∞–Љ—Л–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ —А–∞–Ј–≤–Є—В–Є—О —Н–Ї—Б—Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –љ–µ–є—А–Њ–љ–Њ–≤. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–µ in vitro –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —А–∞–Ј–ї–Є—З–љ—Л–µ –Р–Ф–† —Г—Б–Є–ї–Є–≤–∞—О—В —А–Њ—Б—В –Є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –Ї—Г–ї—М—В—Г—А –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –љ–µ–є—А–Њ–љ–Њ–≤ [7]. –Х—Б–ї–Є –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Р–Ф–† –±—Г–і–µ—В —З–µ—В–Ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –≤ —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, —В–Њ –њ—А–µ–њ–∞—А–∞—В—Л –Р–Ф–† –і–Њ–ї–ґ–љ—Л –±—Г–і—Г—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ —А–∞–љ—М—И–µ - –њ—А–Є –њ–µ—А–≤—Л—Е –њ—А–Є–Ј–љ–∞–Ї–∞—Е –±–Њ–ї–µ–Ј–љ–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Р–Ф–† –њ–Њ–Ј–≤–Њ–ї—П—О—В –Њ—В—Б—А–Њ—З–Є—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л –Є–ї–Є –Ј–∞–Љ–µ–і–ї–Є—В—М —Н—Б–Ї–∞–ї–∞—Ж–Є—О –µ–µ –і–Њ–Ј—Л –Є —В–µ–Љ —Б–∞–Љ—Л–Љ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–і–ї–Є–љ–Є—В—М –њ–µ—А–Є–Њ–і, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –Љ—Л –Љ–Њ–ґ–µ–Љ –∞–і–µ–Ї–≤–∞—В–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–Ф–† –љ–∞ –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–Є –С–Я
–Э–∞ –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–Є –С–Я –Њ—Б–љ–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П–µ—В—Б—П –ї–µ–≤–Њ–і–Њ–њ–∞ - –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–є –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ—А–µ–њ–∞—А–∞—В. –Ю–і–љ–∞–Ї–Њ –µ–≥–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ, –Ї–∞–Ї —Г–ґ–µ —Г–Ї–∞–Ј—Л–≤–∞–ї–Њ—Б—М, –њ–Њ—З—В–Є –љ–µ–Є–Ј–±–µ–ґ–љ–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ —Д–ї—Г–Ї—В—Г–∞—Ж–Є–є –Є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–є, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Ј–∞—В—А—Г–і–љ—П—О—Й–Є—Е –ї–µ—З–µ–љ–Є–µ –Є —В—А–µ–±—Г—О—Й–Є—Е –Њ—В –≤—А–∞—З–∞ –Њ—Б–Њ–±–Њ–≥–Њ –Љ–∞—Б—В–µ—А—Б—В–≤–∞. –Ф–Њ–±–∞–≤–ї–µ–љ–Є–µ –Р–Ф–† –Ї –њ—А–µ–њ–∞—А–∞—В—Г –ї–µ–≤–Њ–і–Њ–њ—Л –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ–±–ї–µ–≥—З–∞–µ—В —А–µ—И–µ–љ–Є–µ —Н—В–Њ–є —В—А—Г–і–љ–Њ–є –Ј–∞–і–∞—З–Є. –С–Њ–ї–µ–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–∞—П –Є —Б—В–∞–±–Є–ї—М–љ–∞—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –њ–Њ—Б—В—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г–µ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —Г—Б–Є–ї–Є–≤–∞–µ—В –Є —Г–і–ї–Є–љ—П–µ—В —Н—Д—Д–µ–Ї—В –ї–µ–≤–Њ–і–Њ–њ—Л. –Ф–Њ–±–∞–≤–ї–µ–љ–Є–µ –Р–Ф–† –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–љ–Є–Ј–Є—В—М –і–Њ–Ј—Г –ї–µ–≤–Њ–і–Њ–њ—Л –њ–Њ—З—В–Є –љ–∞ 30%, —Г–Љ–µ–љ—М—И–∞—П –њ—А–Є —Н—В–Њ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є —Г–≤–µ–ї–Є—З–Є–≤–∞—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —Н—Д—Д–µ–Ї—В–∞ –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і—Б—В–≤. –≠—В–Њ –≤–µ–і–µ—В –Ї —Г–ї—Г—З—И–µ–љ–Є—О –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Є—Е –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –≤ –њ–Њ—Б—В–Њ—А–Њ–љ–љ–µ–Љ —Г—Е–Њ–і–µ. –Т –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–Љ –≤—Л—А–∞–ґ–µ–љ–Є–Є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Р–Ф–† —Г–Љ–µ–љ—М—И–∞—В—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Д–ї—Г–Ї—В—Г–∞—Ж–Є–є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–∞ —Б —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –і—А—Г–≥–Є—Е —Б—А–µ–і—Б—В–≤, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –і–ї—П –Є—Е –Ї–Њ—А—А–µ–Ї—Ж–Є–Є - –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –ї–µ–≤–Њ–і–Њ–њ—Л –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Ї–∞—В–µ—Е–Њ–ї-–Ю-–∞–Љ–Є–љ–Њ—В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л (–Ъ–Ю–Ь–Ґ). –Ю–і–љ–∞–Ї–Њ —Б—Г—Й–µ—Б—В–≤—Г–µ—В —Ж–µ–ї—Л–є —А—П–і –њ—А–Њ—П–≤–ї–µ–љ–Є–є –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–Є –С–Я (–љ–µ–њ—А–µ–і—Б–Ї–∞–Ј—Г–µ–Љ—Л–µ —Д–ї—Г–Ї—В—Г–∞—Ж–Є–Є –Є–ї–Є –і–≤—Г—Е—Д–∞–Ј–љ—Л–µ –і–Є—Б–Ї–Є–љ–µ–Ј–Є–Є), –Ї–Њ–≥–і–∞ –Р–Ф–†, –њ–Њ-–≤–Є–і–Є–Љ–Њ–Љ—Г, –Є–Љ–µ–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –њ–µ—А–µ–і –і—А—Г–≥–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є.
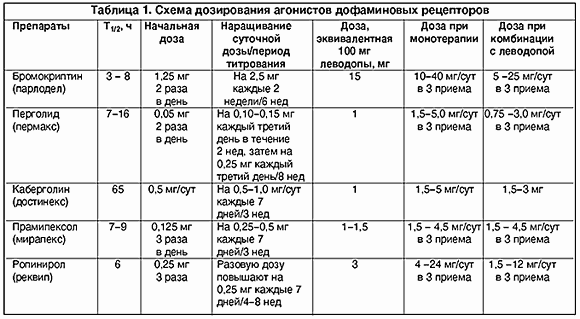
–Я–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Р–Ф–† —Б—Е–Њ–і–љ—Л —Б –њ–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –ї–µ–≤–Њ–і–Њ–њ—Л –Є –≤–Ї–ї—О—З–∞—О—В —В–Њ—И–љ–Њ—В—Г, —А–≤–Њ—В—Г, –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї—Г—О –≥–Є–њ–Њ—В–µ–љ–Ј–Є—О, –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –љ–Њ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П —З–∞—Й–µ, —З–µ–Љ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –ї–µ–≤–Њ–і–Њ–њ—Л. –Т–Њ–Ј–љ–Є–Ї–љ—Г–≤ –≤ –љ–∞—З–∞–ї–µ –ї–µ—З–µ–љ–Є—П, –≤ –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ –Њ–љ–Є –Є–Љ–µ—О—В —В–µ–љ–і–µ–љ—Ж–Є—О –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О. –Ф–ї—П —Г–Љ–µ–љ—М—И–µ–љ–Є—П –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Р–Ф–† –≤–љ–∞—З–∞–ї–µ –љ–∞–Ј–љ–∞—З–∞—О—В –≤ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј–µ, –∞ –Ј–∞—В–µ–Љ –і–Њ–Ј—Г –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —В–Є—В—А—Г—О—В, —Б—В—А–µ–Љ—П—Б—М –њ–Њ–ї—Г—З–Є—В—М –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В (—В–∞–±–ї–Є—Ж–∞ 1). –Э—Г–ґ–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Р–Ф–† –≤ –Љ–∞–ї—Л—Е –і–Њ–Ј–∞—Е –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї –љ–∞—А–∞—Б—В–∞–љ–Є—О –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –Ј–∞ —Б—З–µ—В –∞–Ї—В–Є–≤–∞—Ж–Є–Є –њ—А–µ—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є—Е –∞—Г—В–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Є —Г—Б–Є–ї–µ–љ–Є—П –Њ–±—А–∞—В–љ–Њ–≥–Њ –Ј–∞—Е–≤–∞—В–∞, —Б–љ–Є–ґ–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –Є –≤—Л–і–µ–ї–µ–љ–Є—П –і–Њ—Д–∞–Љ–Є–љ–∞ –≤ —Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї—Г—О —Й–µ–ї—М. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –і–Њ–Љ–њ–µ—А–Є–і–Њ–љ–∞ –≤ –љ–∞—З–∞–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –ї–µ—З–µ–љ–Є—П (–Њ–±—Л—З–љ–Њ –≤ –њ–µ—А–≤—Л–µ 2 –љ–µ–і–µ–ї–Є) —Г–Љ–µ–љ—М—И–∞–µ—В —В–Њ—И–љ–Њ—В—Г –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–∞—А–∞—Й–Є–≤–∞—В—М –і–Њ–Ј—Г –±—Л—Б—В—А–µ–µ. –Х—Б–ї–Є –љ–µ —Г–і–∞–µ—В—Б—П –і–Њ—Б—В–Є—З—М —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј—Л –Р–Ф–† –Є–Ј-–Ј–∞ —Г—Б–Є–ї–µ–љ–Є—П –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–Є, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Г–≤–µ–ї–Є—З–Є—В—М –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ —Б–Њ–ї–Є –Є –ґ–Є–і–Ї–Њ—Б—В–Є, –љ–Њ—Б–Є—В—М —Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–µ —З—Г–ї–Ї–Є, —Б–њ–∞—В—М —Б –≤—Л—Б–Њ–Ї–Њ –њ–Њ–і–љ—П—В–Њ–є –≥–Њ–ї–Њ–≤–Њ–є, –њ—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Є—Е –Љ–µ—А - –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –љ–∞–Ј–љ–∞—З–Є—В—М —Д–ї—Г–і—А–Њ–Ї–Њ—А—В–Є–Ј–Њ–љ. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Р–Ф–† —З–∞—Й–µ, —З–µ–Љ –њ—А–µ–њ–∞—А–∞—В—Л –ї–µ–≤–Њ–і–Њ–њ—Л, –≤—Л–Ј—Л–≤–∞—О—В –њ—Б–Є—Е–Њ—В–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Є–ї–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ–Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є. –Я—А–Є —А–∞–љ–љ–µ–Љ —А–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–љ–Є–Є —Н—В–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –Њ—В–Љ–µ–љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –±—Л—Б—В—А–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–є —Б—В–∞—В—Г—Б.
–•–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –Р–Ф–†
–С—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ (–њ–∞—А–ї–Њ–і–µ–ї) - –њ—А–Њ–Є–Ј–≤–Њ–і–љ–Њ–µ —Б–њ–Њ—А—Л–љ—М–Є —Б –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Є–Ј–±–Є—А–∞—В–µ–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ D2 —А–µ—Ж–µ–њ—В–Њ—А—Л, —П–≤–ї—П—О—Й–Є–є—Б—П —В–∞–Ї–ґ–µ —Б–ї–∞–±—Л–Љ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–Љ D1 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Э–∞ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –С–Я –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–є –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є, –≤—Л–Ј—Л–≤–∞–ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –Є —Б—В–Њ–є–Ї–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ, —Б–Њ—Е—А–∞–љ—П–≤—И–µ–µ—Б—П –љ–µ –Љ–µ–љ–µ–µ 1 –≥–Њ–і–∞ —В–Њ–ї—М–Ї–Њ —Г —В—А–µ—В–Є –±–Њ–ї—М–љ—Л—Е [15, 16, 20]. –Я—А–Є —Н—В–Њ–Љ –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–≥–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –і–Њ–Ј—Г –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ–∞ –Є–љ–Њ–≥–і–∞ –њ—А–Є—Е–Њ–і–Є—В—Б—П —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –і–Њ 30 –Љ–≥/—Б—Г—В. –Я—А–Є –і–∞–ї—М–љ–µ–є—И–µ–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –і–Њ–Ј—Л (–і–Њ 40 –Љ–≥/—Б—Г—В) –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—О –Є–љ–Њ–≥–і–∞ —Г–і–∞–≤–∞–ї–Њ—Б—М –њ—А–Њ–і–Њ–ї–ґ–∞—В—М –≤ —В–µ—З–µ–љ–Є–µ 3-5 –ї–µ—В. –Э–Њ –њ—А–Є —Н—В–Њ–Љ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –≤—Л—И–µ, —З–µ–Љ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –ї–µ–≤–Њ–і–Њ–њ—Л. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б—А–µ–і–љ–Є—Е –і–Њ–Ј –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ–∞ (–≤ –≤–Є–і–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Є–ї–Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є–Ї–∞–Љ–Є, —Б–µ–ї–µ–≥–Є–ї–Є–љ–Њ–Љ, –∞–Љ–∞–љ—В–∞–і–Є–љ–Њ–Љ) –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Љ–∞–ї—Л–Љ–Є –і–Њ–Ј–∞–Љ–Є –ї–µ–≤–Њ–і–Њ–њ—Л. –Ф–Њ–±–∞–≤–ї–µ–љ–Є–µ –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ–∞ –Ї –ї–µ–≤–Њ–і–Њ–њ–µ —Г –±–Њ–ї—М–љ—Л—Е —Б –Љ–Њ—В–Њ—А–љ—Л–Љ–Є —Д–ї—Г–Ї—В—Г–∞—Ж–Є—П–Љ–Є –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є “–≤–Ї–ї—О—З–µ–љ–Є—П - –≤—Л–Ї–ї—О—З–µ–љ–Є—П” –Є —Б–љ–Є–ґ–µ–љ–Є—О –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –∞–Ї–Є–љ–µ–Ј–Є–Є –Ї–Њ–љ—Ж–∞ –і–Њ–Ј—Л, –∞ –Ј–∞ —Б—З–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—П –і–Њ–Ј—Л –ї–µ–≤–Њ–і–Њ–њ—Л (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 10%) - –Є –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –і–Є—Б–Ї–Є–љ–µ–Ј–Є–є [11]. –Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –≤–Ї–ї—О—З–∞—О—В —В–Њ—И–љ–Њ—В—Г, –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї—Г—О –≥–Є–њ–Њ—В–µ–љ–Ј–Є—О, —Б–њ—Г—В–∞–љ–љ–Њ—Б—В—М —Б–Њ–Ј–љ–∞–љ–Є—П –Є –≥–∞–ї–ї—О—Ж–Є–љ–∞—Ж–Є–Є. –Ъ–∞–Ї –Є –і—А—Г–≥–Є–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ —Б–њ–Њ—А—Л–љ—М–Є, –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ –Љ–Њ–ґ–µ—В –≤—Л–Ј—Л–≤–∞—В—М –ї–µ–≥–Њ—З–љ—Л–є –Є –Ј–∞–±—А—О—И–Є–љ–љ—Л–є —Д–Є–±—А–Њ–Ј, —Н—А–Є—В—А–Њ–Љ–µ–ї–∞–ї–≥–Є—О, –≤–∞–Ј–Њ—Б–њ–∞–Ј–Љ. –Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ –і–Є—Б–Ї–Є–љ–µ–Ј–Є–Є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ–∞ –≤–Њ–Ј–љ–Є–Ї–∞—О—В —А–µ–і–Ї–Њ.
–Я–µ—А–≥–Њ–ї–Є–і (–њ–µ—А–Љ–∞–Ї—Б) - –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Њ–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ–Њ–µ —Б–њ–Њ—А—Л–љ—М–Є. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ–∞, –Њ–љ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –Ї–∞–Ї D2 (D3), —В–∞–Ї –Є D1 —А–µ—Ж–µ–њ—В–Њ—А—Л. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ–µ—А–≥–Њ–ї–Є–і–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–µ–є –С–Я –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О –њ–Њ—З—В–Є —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е, –њ—А–Є—З–µ–Љ —Б–њ—Г—Б—В—П 3 –≥–Њ–і–∞ —Г–ї—Г—З—И–µ–љ–Є–µ —Б–Њ—Е—А–∞–љ—П–ї–Њ—Б—М –Љ–µ–љ–µ–µ —З–µ–Љ —Г —В—А–µ—В–Є –±–Њ–ї—М–љ—Л—Е [20]. –Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ–µ—А–≥–Њ–ї–Є–і–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–µ–є –С–Я —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Љ–Њ–≥—Г—В –±—Л—В—М —В–∞–Ї–Є–Љ–Є –ґ–µ, –Ї–∞–Ї –Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –ї–µ–≤–Њ–і–Њ–њ—Л. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ–µ—А–≥–Њ–ї–Є–і–∞ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –ї–µ–≤–Њ–і–Њ–њ–Њ–є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–љ–Є–Ј–Є—В—М –і–Њ–Ј—Г –ї–µ–≤–Њ–і–Њ–њ—Л –љ–∞ 20- 30 % –Є —Г–Љ–µ–љ—М—И–Є—В—М –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–µ—А–Є–Њ–і–∞ –≤—Л–Ї–ї—О—З–µ–љ–Є—П –љ–∞ 30 % [18]. –Т–∞–ґ–љ–Њ–є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –њ–µ—А–≥–Њ–ї–Є–і–∞ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–µ —В–Њ–ї—М–Ї–Њ –љ–∞ –і–Є—Б–Ї–Є–љ–µ–Ј–Є–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–µ –ї–µ–≤–Њ–і–Њ–њ–Њ–є, –љ–Њ –Є –љ–∞ —Б–њ–Њ–љ—В–∞–љ–љ—Г—О –і–Є—Б—В–Њ–љ–Є—О. –Т–∞–ґ–љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ —А–µ–∞–Ї—Ж–Є—П –љ–∞ –Р–Ф–† –Є–Љ–µ–µ—В –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А: –љ–µ–Ї–Њ—В–Њ—А—Л–µ –±–Њ–ї—М–љ—Л–µ –Њ—В–Љ–µ—З–∞—О—В —Г–ї—Г—З—И–µ–љ–Є–µ –њ—А–Є –њ–µ—А–µ—Е–Њ–і–µ —Б –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ–∞ –љ–∞ –њ–µ—А–≥–Њ–ї–Є–і, –љ–µ–Ї–Њ—В–Њ—А—Л–µ - –њ—А–Є –Њ–±—А–∞—В–љ–Њ–Љ –њ–µ—А–µ—Е–Њ–і–µ [8]. –Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Є –њ—А–Є–µ–Љ–µ –њ–µ—А–≥–Њ–ї–Є–і–∞: –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ, –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є—П, —А–Є–љ–Є—В, –∞—Б—В–µ–љ–Є—П, –≥–∞–ї–ї—О—Ж–Є–љ–∞—Ж–Є–Є, –љ–∞—А—Г—И–µ–љ–Є—П —Б–љ–∞, –≤–∞–Ј–Њ—Б–њ–∞–Ј–Љ, —Н—А–Є—В—А–Њ–Љ–µ–ї–∞–ї–≥–Є—П, –Ј–∞–±—А—О—И–Є–љ–љ—Л–є –Є –ї–µ–≥–Њ—З–љ—Л–є —Д–Є–±—А–Њ–Ј.
–Я—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї (–Љ–Є—А–∞–њ–µ–Ї—Б) - —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Њ–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ–Њ–µ –±–µ–љ–Ј–Њ—В–Є–∞–Ј–Њ–ї–∞, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –і–µ–є—Б—В–≤—Г—О—Й–Є–є –љ–∞ D3 –њ–Њ–і—В–Є–њ D2 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї–∞ —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Ї–Њ—В–Њ—А–∞—П –њ–Њ —Б–Є–ї–µ –њ—А–Є–±–ї–Є–ґ–∞–µ—В—Б—П –Ї –і–Њ—Д–∞–Љ–Є–љ—Г. –Я—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Њ—В–Ї—А—Л—В—Л—Е –Є –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –∞ —В–∞–Ї–ґ–µ –љ–∞—И —Б–Њ–±—Б—В–≤–µ–љ–љ—Л–є –Њ–њ—Л—В –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е —Б —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–µ–є –С–Я –њ—А–µ–њ–∞—А–∞—В –≤ –і–Њ–Ј–µ 1,5-4,5 –Љ–≥/—Б—Г—В —Б–њ–Њ—Б–Њ–±–µ–љ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є—В—М —Б–Є–Љ–њ—В–Њ–Љ—Л –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ–∞. –Я—А–Є—З–µ–Љ –µ–≥–Њ —Н—Д—Д–µ–Ї—В –Љ–Њ–ґ–љ–Њ —Б–Њ—Е—А–∞–љ—П—В—М—Б—П –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 2-4 –ї–µ—В, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Њ—В—Б—А–Њ—З–Є—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –ї–µ–≤–Њ–і–Њ–њ—Л –Є —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Љ–Њ—В–Њ—А–љ—Л—Е —Д–ї—Г–Ї—В—Г–∞—Ж–Є–є –Є –і–Є—Б–Ї–Є–љ–µ–Ј–Є–є [6]. –Я–Њ –і–∞–љ–љ—Л–Љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї –≤ –≤ –і–Њ–Ј–µ 4,5 –Љ–≥/—Б—Г—В –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ, —З–µ–Љ –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ –≤ –і–Њ–Ј–µ 20-30 –Љ–≥/—Б—Г—В. –£ –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–µ–є –С–Я –і–Њ–±–∞–≤–ї–µ–љ–Є–µ –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–љ–Є–Ј–Є—В—М –і–Њ–Ј—Г –ї–µ–≤–Њ–і–Њ–њ—Л –љ–∞ 27 %, —Г–Љ–µ–љ—М—И–∞—П –њ—А–Є —Н—В–Њ–Љ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–µ—А–Є–Њ–і–∞ –≤—Л–Ї–ї—О—З–µ–љ–Є—П –љ–∞ 31 % [14]. –С–ї–∞–≥–Њ–і–∞—А—П —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є D3 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ –ї–Є–Љ–±–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ–µ –њ—А–µ–њ–∞—А–∞—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–µ–є –С–Я –Є –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ–ї–µ–Ј–µ–љ –≤ –ї–µ—З–µ–љ–Є–Є –і–µ–њ—А–µ—Б—Б–Є–Є, –Ї–Њ—В–Њ—А–∞—П —З–∞—Б—В–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г –±–Њ–ї—М–љ—Л—Е –С–Я. –Я—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ, —З–µ–Љ –і—А—Г–≥–Є–µ –Р–Ф–†, —Г–Љ–µ–љ—М—И–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —В—А–µ–Љ–Њ—А–∞ –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ–±–Є—В—М—Б—П —Г–ї—Г—З—И–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —В—А—Г–і–љ–Њ –Ї—Г—А–∞–±–µ–ї—М–љ–Њ–є –і—А–Њ–ґ–∞—В–µ–ї—М–љ–Њ–є —Д–Њ—А–Љ–Њ–є –С–Я.
–Я—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ, —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –љ–µ–і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–µ —А–µ—Ж–µ–њ—В–Њ—А—Л (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –∞–ї—М—Д–∞-–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л, —Б–µ—А–Њ—В–Њ–љ–Є–љ–Њ–≤—Л–µ, –Љ—Г—Б–Ї–∞—А–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л), —А–µ–ґ–µ –≤—Л–Ј—Л–≤–∞–µ—В –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л (–ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л–µ –Є–ї–Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–µ) –Є –ї—Г—З—И–µ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –±–Њ–ї—М–љ—Л–Љ–Є. –Э–µ—Н—А–≥–Њ–ї–Є–љ–Њ–≤–∞—П –њ—А–Є—А–Њ–і–∞ –Є—Б–Ї–ї—О—З–∞–µ—В —В–∞–Ї–ґ–µ —В–∞–Ї–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П, –Ї–∞–Ї —П–Ј–≤–∞ –ґ–µ–ї—Г–і–Ї–∞, –≤–∞–Ј–Њ—Б–њ–∞–Ј–Љ, –ї–µ–≥–Њ—З–љ—Л–є —Д–Є–±—А–Њ–Ј –Є —В.–і. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї –Є–Љ–µ–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–µ—А–µ–і –і—А—Г–≥–Є–Љ–Є –Р–Ф–†, –Ї–∞–Ї –љ–∞ —А–∞–љ–љ–µ–є, —В–∞–Ї –Є –љ–∞ —А–∞–Ј–≤–µ—А–љ—Г—В–Њ–є —Б—В–∞–і–Є–Є –С–Я.
–Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤ —Б—В—А—Г–Ї—В—Г—А–µ –њ–Њ–±–Њ—З–љ—Л—Е –і–µ–є—Б—В–≤–Є–є –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї–∞ –±–Њ–ї–µ–µ –≤–µ—Б–Њ–Љ–Њ–µ –Љ–µ—Б—В–Њ –Ј–∞–љ–Є–Љ–∞—О—В —Ж–µ–љ—В—А–∞–ї—М–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л (–≥–∞–ї–ї—О—Ж–Є–љ–∞—Ж–Є–Є, –љ–∞—А—Г—И–µ–љ–Є—П —Б–љ–∞, –і–Є—Б–Ї–Є–љ–µ–Ј–Є–Є). –У–∞–ї–ї—О—Ж–Є–љ–∞—Ж–Є–Є –Є —Б–њ—Г—В–∞–љ–љ–Њ—Б—В—М —Б–Њ–Ј–љ–∞–љ–Є—П —З–∞—Й–µ –≤–Њ–Ј–љ–Є–Ї–∞—О—В –њ—А–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї–∞ –Є –ї–µ–≤–Њ–і–Њ–њ—Л –љ–∞ –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–Є –С–Я - —Г –±–Њ–ї—М–љ—Л—Е —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї–∞, –њ—А–µ–≤—Л—И–∞—О—Й–Є—Е 4,5 –Љ–≥, —В—А–µ–±—Г–µ—В –Њ—Б–Њ–±–Њ–є –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ—Б—В–Є –Є–Ј-–Ј–∞ —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ—А–Є—Б—В—Г–њ–Њ–≤ –љ–µ–њ—А–µ–Њ–і–Њ–ї–Є–Љ–Њ–є —Б–Њ–љ–ї–Є–≤–Њ—Б—В–Є. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –Њ–њ–Є—Б–∞–љ—Л –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–ї—Г—З–∞–µ–≤, –Ї–Њ–≥–і–∞ –њ—А–Є—Б—В—Г–њ –Ј–∞—Б—Л–њ–∞–љ–Є—П –Ј–∞ —А—Г–ї–µ–Љ, –≤–Њ–Ј–љ–Є–Ї—И–Є–є –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї–Њ–Љ, –њ—А–Є–≤–µ–ї –Ї –і–Њ—А–Њ–ґ–љ–Њ-—В—А–∞–љ—Б–њ–Њ—А—В–љ—Л–Љ –њ—А–Њ–Є—Б—И–µ—Б—В–≤–Є—П–Љ. –Э—Г–ґ–љ–Њ, –Њ–і–љ–∞–Ї–Њ, –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–є —Н—Д—Д–µ–Ї—В –≤–Њ–Ј–Љ–Њ–ґ–µ–љ –Є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –і—А—Г–≥–Є—Е –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і—Б—В–≤. –Ю—Б—В–Њ—А–Њ–ґ–љ–Њ—Б—В—М —Б–ї–µ–і—Г–µ—В —Б–Њ–±–ї—О–і–∞—В—М –Є –њ—А–Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, —В—А–µ–±—Г—О—Й–µ–є —Б–љ–Є–ґ–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –њ—А–Є–µ–Љ–∞ –Є —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞. –Ъ–∞–Ї –Є –і—А—Г–≥–Є–µ –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞, –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї –Љ–Њ–ґ–µ—В –≤—Л–Ј—Л–≤–∞—В—М —Г—Б–Є–ї–µ–љ–Є–µ –ї–Є–±–Є–і–Њ, —З—В–Њ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б–Њ—Б—В–Њ—П–љ–Є—П –±–Њ–ї—М–љ—Л—Е –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М –Ї–∞–Ї –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ, —В–∞–Ї –Є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П.
–†–Њ–њ–Є–љ–Є—А–Њ–ї (—А–µ–Ї–≤–Є–њ) - –љ–Њ–≤—Л–є –љ–µ—Н—А–≥–Њ–ї–Є–љ–Њ–≤—Л–є –њ—А–µ–њ–∞—А–∞—В. –Я–Њ —Б—В—А—Г–Ї—В—Г—А–µ –Њ–љ –љ–∞–њ–Њ–Љ–Є–љ–∞–µ—В –і–Њ—Д–∞–Љ–Є–љ –Є –Њ—Б–Њ–±–µ–љ–љ–Њ –∞–Ї—В–Є–≤–љ–Њ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б D2 –Є D3 —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є, –і–µ–є—Б—В–≤—Г—П, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –љ–∞ –њ—А–µ—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є–µ –∞—Г—В–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л. –Э–∞ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є —А–Њ–њ–Є–љ–Є—А–Њ–ї –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–µ —Г—Б—В—Г–њ–∞–µ—В –ї–µ–≤–Њ–і–Њ–њ–µ –Є –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ, —З–µ–Љ –±—А–Њ–Љ–Њ–Ї—А–Є–њ—В–Є–љ [5]. –Т —В–µ—З–µ–љ–Є–µ 3-–ї–µ—В–љ–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —А–Њ–њ–Є–љ–Є—А–Њ–ї –Њ–±–µ—Б–њ–µ—З–Є–ї –∞–і–µ–Ї–≤–∞—В–љ—Г—О –Ї–Њ—А—А–µ–Ї—Ж–Є—О –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Г 60% –±–Њ–ї—М–љ—Л—Е. –Э–∞ –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–Є –С–Я —А–Њ–њ–Є–љ–Є—А–Њ–ї –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –ї–µ–≤–Њ–і–Њ–њ–Њ–є —Г–Љ–µ–љ—М—И–∞–ї –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–µ—А–Є–Њ–і–∞ –≤—Л–Ї–ї—О—З–µ–љ–Є—П –љ–∞ 12% –Є –њ–Њ–Ј–≤–Њ–ї—П–ї —Б–љ–Є–Ј–Є—В—М –і–Њ–Ј—Г –ї–µ–≤–Њ–і–Њ–њ—Л –љ–∞ 31%. –Ш–Ј –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ —З–∞—Б—В–Њ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –љ–∞—А—Г—И–µ–љ–Є—П —Б–љ–∞ –Є —В–Њ—И–љ–Њ—В–∞, –Њ–±—Л—З–љ–Њ –њ—А–µ—Е–Њ–і—П—Й–∞—П.
–Р–њ–Њ–Љ–Њ—А—Д–Є–љ - –љ–µ—Н—А–≥–Њ–ї–Є–љ–Њ–≤—Л–є –∞–≥–Њ–љ–Є—Б—В, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–є D1, D2 –Є D3 —А–µ—Ж–µ–њ—В–Њ—А—Л. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –і—А—Г–≥–Є—Е –Р–Ф–†, –∞–њ–Њ–Љ–Њ—А—Д–Є–љ –≤—Л–њ—Г—Б–Ї–∞–µ—В—Б—П –≤ —А–∞—Б—В–≤–Њ—А–µ –Є –Љ–Њ–ґ–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ. –І–∞—Й–µ –≤—Б–µ–≥–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –љ–∞ –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞—О—Й–Є—Е —В—П–ґ–µ–ї—Л–Љ–Є –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–Љ–Є —Д–ї—Г–Ї—В—Г–∞—Ж–Є—П–Љ–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ ‘’–≤–Ї–ї—О—З–µ–љ–Є—П-–≤—Л–Ї–ї—О—З–µ–љ–Є—П”. –Я—А–Є –њ–Њ–і–Ї–Њ–ґ–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є —Н—Д—Д–µ–Ї—В –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —З–µ—А–µ–Ј 10-15 –Љ–Є–љ—Г—В –Є —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П 1-2 —З–∞—Б–∞.
–Ъ–∞–±–µ—А–≥–Њ–ї–Є–љ (–і–Њ—Б—В–Є–љ–µ–Ї—Б) - —Н—А–≥–Њ–ї–Є–љ–Њ–≤—Л–є –њ—А–µ–њ–∞—А–∞—В, —П–≤–ї—П—О—Й–Є–є—Б—П –≤—Л—Б–Њ–Ї–Њ–∞–Ї—В–Є–≤–љ—Л–Љ –∞–≥–Њ–љ–Є—Б—В–Њ–Љ D2 —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Ь–Њ–ґ–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П 1 —А–∞–Ј –≤ –і–µ–љ—М. –£ –±–Њ–ї—М–љ—Л—Е —Б —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–µ–є –С–Я –њ—А–µ–њ–∞—А–∞—В –≤ —Б—А–µ–і–љ–µ–є –і–Њ–Ј–µ 2,8 –Љ–≥/—Б—Г—В —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б –ї–µ–≤–Њ–і–Њ–њ–Њ–є. –Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ї–∞–±–µ—А–≥–Њ–ї–Є–љ–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –і–ї–Є—В–µ–ї—М–љ—Л–Љ –ї–µ—З–µ–љ–Є–µ–Љ –ї–µ–≤–Њ–і–Њ–њ–Њ–є, –≤–Њ–Ј–љ–Є–Ї–∞—О—В –њ–Њ–Ј–і–љ–µ–µ. –Э–∞ –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–Є –С–Я –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –ї–µ–≤–Њ–і–Њ–њ–Њ–є –Ї–∞–±–µ—А–≥–Њ–ї–Є–љ —Г–Љ–µ–љ—М—И–∞–µ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–µ—А–Є–Њ–і–∞ –≤—Л–Ї–ї—О—З–µ–љ–Є—П –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–љ–Є–Ј–Є—В—М –і–Њ–Ј—Г –ї–µ–≤–Њ–і–Њ–њ—Л –љ–∞ 18 % [13]. –Я–Њ–±–Њ—З–љ—Л–µ –і–µ–є—Б—В–≤–Є—П —В–µ –ґ–µ, —З—В–Њ –Є —Г –і—А—Г–≥–Є—Е —Н—А–≥–Њ–ї–Є–љ–Њ–≤—Л—Е –Р–Ф–†.
–°–њ–Є—Б–Њ–Ї –ї–Є—В–µ—А–∞—В—Г—А—Л –Т—Л –Љ–Њ–ґ–µ—В–µ –љ–∞–є—В–Є –љ–∞ —Б–∞–є—В–µ http://www.rmj.ru
–Я—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї –
–Ь–Є—А–∞–њ–µ–Ї—Б (—В–Њ—А–≥–Њ–≤–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ)
(Pharmacia & Upjohn)
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –У–Њ–ї—Г–±–µ–≤ –Т.–Ы., –Ы–µ–≤–Є–љ –ѓ.–Ш., –Т–µ–є–љ –Р.–Ь. –С–Њ–ї–µ–Ј–љ—М –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞ –Є —Б–Є–љ–і—А–Њ–Љ –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ–∞. –Ь, 1999.416 –°.
2. –§–µ–і–Њ—А–Њ–≤–∞ –Э.–Т., –®—В–Њ–Ї –Т.–Э. –≠—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ–∞ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –њ–∞—В–Њ–Љ–Њ—А—Д–Њ–Ј –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є.// –Т–µ—Б—В–љ–Є–Ї –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є.-1995.- —Ф1.-–°.87-88.
3. –®—В–Њ–Ї –Т.–Э., –§–µ–і–Њ—А–Њ–≤–∞ –Э.–Т. –Ы–µ—З–µ–љ–Є–µ –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ–∞. –Ь.1997. 196 —Б.
4. –®—В—Г–ї—М–Љ–∞–љ –Ф.–†., –Ы–µ–≤–Є–љ –Ю.–°. –Я–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ. –°–њ—А–∞–≤–Њ—З–љ–Є–Ї –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤—А–∞—З–∞. –Ь., 1999. –°. 419-436
5. Adler C.H., Sethi K.D., Hauser R.A., et al: Ropinirole for the treatment of early Parkinson’s disease//Neurology49:393,1997.
6. Bressman S., Shulman L.M., Tanner C., Rajput A., Shannon K., Borchert L., Wright E.C. Long-term safety and efficacy of pramipexole in early Parkinson’s disease.//6th International congress of Parkinson’s disease and movement disorders Barcelona, Spain;2000.
7. Carvey P.M., Fieri S., Ling Z.D. Attenuation of levodopa-induced toxicity in mesencephalic cultures by pramipexole.//J Neural Transm 1997;104:209-228.
8. Factor S.A., Sanchez-Ramos J.R., Weiner W.J. Parkinson’s disease: An open-label trial of pergolide in patients failing bromocriptine therapy // J Neurol Neurosurg Psychiatry 1988;51:529-533.
9. Gawel M., Riopelle R., Libman I. Bromocriptine in the treatment of Parkinson’s disease. A double-blind study against L-dopa/carbidopa//Adv Neurol 1986;45:535-538.
10. Gimenez-Roldan S., Tolosa E., Burguera J., et al. Early combination of bromocriptine and levodopa in Parkinson’s disease: a prospective randomized study of two parallel groups over a total follow-up period of 44 months including an initial 8-month double-blind stage//Clin Neuropharmacol 1997;20:67-76.
11. Guttman M. International Pramipexole-Bromocriptine Study Group: Double-blind comparison of pramipexole and bromocriptine treatment with placebo in advanced Parkinson’s disease//Neurology 49:1060,1997.
12. Kostic V., Przedborski S., Flaster E., Sternic N. Early development of levodopa-induced dyskinesias and response fluctuations in young-onset Parkinson’s disease//Neurology 1991;41:202-205.
13. Lieberman A.N., Olanow C.W., Sethi K., et al. A multicenter trial of ropinirole as adjunct treatment for Parkinson’s disease//Neurology51:1057-1062,1998.
14. Lieberman A.N., Ranhosky A., Korts D: Clinical evaluation of pramipexole in advanced Parkinson’s disease: Results of a double-blind, placebo-controlled, parallel-group study//Neurology49:162,1997.
15. Mannen T., Mizuno Y., Iwata M., Goto I., Kanazawa I., Kowa H., et al. A multi-center, double-blind study on slow-release bromocriptine in the treatment of Parkinson’s disease//Neurology 1991;41:1598-602:issue:10.
16. Montastruc J.L., Rascol O., Senard J.M., et al. A randomized controlled study comparing bromocriptine to which levodopa was later added, with levodopa alone in previously untreated patients with Parkinson’s disease: a five year follow-up//J Neurol Neurosug Pschiatry 1994;57:1034-1038.
17. Nakanishi T., Iwata M., Goto I., et al. Nationwide collaborative study on the long-term effects of bromocriptine in the treatment of parkinsonian patients//Eur Neurol 1991;32(Suppl 1):9-22.
18. Olanow C.W., Fahn S., Muenter M., et al. A multicenter, double-blind, placebo-controlled trial of pergolide as an adjunct to Sinemet in Parkinson’s disease//Mov Disord 1994;9:40-47.
19. Rinne U.K. Combined bromocriptine-levodopa therapy early in Parkinson’s disease//Neurology 1985;35:1196-1198.
20. Rinne U.K. Dopamine agonists in the treatment of Parkinson’s disease. In: Rinne UK, Yanagisawa N, eds. Controversies in Treatment of Parkinson’s Disease. PMSI: Tokyo, Japan, 1992:49-60.
21. Watts R.L. The role of dopamine agonists in early Parkinson’s disease//Neurology 1997;49(Suppl 1):S34-48.
| –Я—А–Є–ї–Њ–ґ–µ–љ–Є—П –Ї —Б—В–∞—В—М–µ |








.gif)



