В современной практике терапевта лечение хронических заболеваний является важной составляющей повседневной клинической работы. Принятие решения о выборе тактики медикаментозной терапии не всегда является легкой задачей, особенно если речь идет о сочетанной патологии и различных коморбидных состояниях. Именно таким, малопонятным, «коморбидным» заболеванием является «инсомния» (на бытовом языке – бессонница). Однажды к нам в клинику обратилась женщина 46 лет с жалобами на болезненное состояние, заставившее нас более тщательно «распутывать клубок» существующих у нее проблем.
Клинический случай
Елизавета П., 46 лет, обратилась в лабораторию по изучению расстройств сна ФГУ НИИ пульмонологии г. Москвы 20/IХ 2005 г. по поводу очередного 6–месячного ухудшения сна. Свои проблемы она описывала, как трудности с засыпанием и частыми пробуждениями в период сна. Впервые нарушения сна она стала замечать после рождения второго ребенка 15 лет назад. В это же время проявляется послеродовая депрессия, клинически документированная. В последующие годы, несмотря на отсутствие повторов депрессивных состояний, больших психологических стрессов, Елизавете П. требовалось более 2 часов, чтобы уснуть. Когда же ей удавалось необычно быстро уснуть, она пробуждалась в 2 часа ночи и более уже не спала. По совету друзей, для улучшения засыпания Елизавета П. пробовала ложиться в кровать значительно позже 11–12 часов вечера – времени, которое для нее было привычным. Однако сон не наступал раньше, а мучительность засыпания оставалась прежней. Условия жизни и работы пациентки можно расценивать как хорошие. Врачебный осмотр и специализированный опрос (анкетирование) не обнаруживали значимых системных заболеваний, а также симптомов дыхательных расстройств в период сна или синдрома беспокойных ног.
Перед нами возникли закономерные вопросы: «Какое расстройство сна существует у Елизаветы П.? Какова в этом случае лечебная тактика? Какую медикаментозную терапию необходимо проводить у таких пациентов?»
Инсомния – современная
клиническая проблема
Что такое инсомния (бытовое выражение – «бессонница»)? В Руководстве по диагностике и статистике психических расстройств (DSM–4) инсомния определяется как дефицит качества и количества сна, необходимых для нормальной дневной деятельности. В МКБ–10 группа заболеваний, таких как инсомния, гиперсомния и нарушения ритма сна, определяются как «первично психогенные состояния с эмоционально обусловленным нарушением качества, длительности или ритма сна».
Характерным для инсомнии является трудность засыпания, частые спонтанные пробуждения, уменьшение длительности сна и ухудшение его качества. Последствиями плохого сна является низкая повседневная активность пациента, несмотря на сохраненную возможность сна и благоприятные для него условия [1,2].
Существует четкий диагностический критерий – «маркер инсомнии»: задержка в наступлении сна более чем на 30 минут (увеличение времени засыпания) и эффективность сна менее 85%. Эффективность сна вычисляется, как отношение времени сна ко всему времени пребывания в кровати. Однако в клинической практике наиболее важным остается субъективное мнение пациента о качестве и количестве своего сна. По клиническим критериям инсомнию разделяют на преходящую (транзиторную) – длящуюся менее одной недели, кратковременную – продолжительностью от одной до четырех недель и хроническую [3].
Хроническая инсомния – расстройство сна, длительностью более одного месяца, распространена у 10–15% лиц в популяции, чаще развивается у женщин детородного возраста, пожилых, и пациентов с хроническими соматическими или психическими нарушениями [1,4].
Обычно хроническая инсомния развивается после нескольких эпизодов острой, особенно у предрасположенных лиц. Расстройства сна становятся хроническими, когда существуют предрасполагающие психические и поведенческие факторы, такие как тревога, беспокойство, искаженные представления о «хорошем сне». Характерными последствиями хронической инсомнии являются: длительно существующая усталость, частые расстройства настроения, проблемы межличностных отношений, «непривычные трудности» выполнения профессиональной работы, сниженное качество жизни [5].
Для установления диагноза важным является тщательный сбор анамнеза заболевания непосредственно у пациента, а при отсутствии такой возможности – у его партнера. Это позволит правильно установить причины инсомнии, определит путь дальнейшей коррекции. Чрезвычайно полезным является заполнение пациентом дневника «бодрствование/сон» с регистрацией в нем времени засыпания и пробуждения в течение 4–х недель. Полисомнография (ночное исследование сна) в таких случаях не требуется. Тем не менее полисомнография, как важнейшая диагностическая процедура, будет необходима у пациентов с инсомнией при подозрении на наличие у них расстройств дыхания в период сна (синдром обструктивного апноэ сна), нарушений двигательной активности в период сна (синдром периодического движения конечностей) или при отсутствии эффекта от медикаментозной терапии [6,7].
В соответствии с причинным фактором инсомнию классифицируют на первичную и вторичную (табл. 1).
Принято считать, что патогенез первичной инсомнии неизвестен. Между тем в исследованиях последних лет установлено, что у большинства таких пациентов отмечается состояние повышенной активации в период сна. В контролируемом исследовании, изучающем метаболизм глюкозы головного мозга методом позитронно–эмиссионной томографии, у пациентов исследуемой группы отмечался ее повышенный метаболизм как в состоянии бодрствования, так и во время сна. При полисомнографическом исследовании у таких пациентов определялась повышенная бета–активность и сниженные тета– и дельта–активности головного мозга. В то же время при исследовании уровня секреции гормонов в исследуемой группе наблюдались высокие уровни адренокортикотропного гормона и кортизола [8].
Вторичная инсомния более распространена, чем первичная. В связи со схожестью клинической картины важно не совершить ошибку, расценив вторичную инсомнию как первичную, и наоборот. Правило достаточно простое – «если симптомы заболевания сохраняются, несмотря на устранение вторичных причин, необходимо лечение первичной инсомнии». Однако стоит помнить о том, что несколько причин заболевания могут присутствовать у одного и того же пациента. Хочется отметить, что расстройства циркадного ритма, к которым относят расстройства сна в результате сменной работы, синдром запаздывающего сна (наступление сна с опозданием более 2 часов от обычного времени сна), синдром добровольной депривации сна (добровольное лишение себя сна в установленное время), обязательно должны рассматриваться при диагностике инсомнии, но они не могут расцениваться как инсомния!
Лечебная стратегия:
клинические доказательства
На сегодняшний день не существует неоспариваемой лечебной доктрины инсомнии. Однако повсеместно признается, что основными способами коррекции расстройств сна являются поведенческая психотерапия и фармакологическое лечение.
Поведенческая психотерапия
Терминологически «поведенческая психотерапия» означает набор методик, способных устранить факторы «укоренения» инсомнии, независимо от ее причины (табл. 2). По воздействию на причинный фактор их разделяют на несколько групп.
В первую группу включены психотерапевтические методики, устраняющие неадекватное поведение пациента в кровати во время приготовления ко сну (регулярное чтение лежа, еда в постели или просмотр телепередач) и формирующие у них правильную ассоциацию между постелью и сном [9].
Вторая группа включает методы «добровольного ограничения сна». Они основаны на предположении, что пациенты с инсомнией могут научиться удлинять свой сон, искусственно вызывая эпизоды его укорочения посредством малого нахождения в постели [10].
Третья группа релаксационных методик предполагает связь инсомнии с чрезмерными мозговыми активациями. Психологический компонент таких методов подразумевает коррекцию несбыточных ожиданий, устранение тревоги и преувеличенного восприятия последствий плохого сна. Физическая компонента направлена на обучение пациента методам аутотренинга и релаксации с элементами обратной связи. Обучение правильной гигиене сна позволяет устранить воздействие основных внешних факторов, способствующих регулярности инсомнии, таких как шум, неприятный свет или запахи, чрезмерное употребление кофеина [11].
В серии рандомизированных контролируемых исследований (РКИ) отмечена эффективность методов поведенческой психотерапии при первичной бессоннице. Ряд крупных мета–анализов последних лет убедительно показывают, что у пациентов с первичной инсомнией поведенческая психотерапия улучшает показатель латенции ко сну и увеличивает общее время сна на 30 минут. При этом достоверно уменьшаются количество и длительность мозговых активаций [4,12]. В половине случаев присутствуют достоверные клинические улучшения самочувствия [13].
В большинстве случаев поведенческая психотерапия сочетает несколько разных методик. В РКИ, изучавших возможности композиционной психотерапии, достоверно показаны ее высокая эффективность в сравнении с монотерапией. Исключение составили отдельные методики, связанные с обучением испытуемых гигиене сна и психотерпевтическим воздействием, по своей эффективности не уступавшие композиционному подходу [14]. Даже после прекращения композиционной психотерапии устойчивое положительное воздействие на сон испытуемых сохранялось в течение 6 месяцев [1].
Выбор способа обучения и его длительность также представляют неподдельный интерес. Обратимся к ряду исследований, изучавших данный вопрос. В большинстве из них поведенческая психотерапия осуществлялась психологами за 6 занятий в среднем по 5,8 часов на пациента [1]. Проведенный мета–анализ свидетельствует, что индивидуальная терапия значительно эффективнее, чем групповая [4]. Интересно, что стажеры в области психологии и психиатрии [15], медсестры [13] и консультанты [16] также могли успешно проводить коррекцию за 4–6 занятий по 20–50 минут каждое. Положительными результаты были и тогда, когда поведенческая психотерапия, состоящая из 3–10 занятий, осуществлялась терапевтами первичного звена, прошедшими специальную 3–часовую подготовку у психолога с опытом в лечении инсомнии [17]. Не менее интересно исследование укороченного курса поведенческой психотерапии, проводимого младшими клиническими психологами за 2 занятия продолжительностью по 25 минут каждое с двухнедельным перерывом. Оно показало достоверный положительный эффект, сохраняющийся в течение 3 месяцев после окончания курса [18]. Самообучение посредством просмотра видеокассет [19] или печатных материалов [20] также было эффективным.
Фармакологические методы терапии
Фармакологическая коррекция инсомнии активно проводится на протяжении уже 100 лет и включает различные группы лекарственных препаратов. По доступности для самостоятельного использования пациентом лекарственные средства подразделяются на препараты рецептурного и безрецептурного отпуска.
К препаратам рецептурного отпуска относят группу бензодиазепинов, непрямых агонистов бензодиазепиновых рецепторов и антидепрессантов с седативным действием. В связи с серьезными побочными эффектами препаратов предпочтительными являются средства, одобренные органами надзора в сфере лекарственных препаратов (например, Администрацией по контролю за продуктами питания и лекарствами – FDA), к использованию у пациентов с инсомнией. Так, в группу разрешенных бензодиазепинов включены препараты длительного, среднего и короткого периода полувыведения, тогда как разрешенные непрямые агонисты бензодиазепиновых рецепторов включили в себя только лекарственные средства короткого и ультракороткого периода полувыведения (табл. 3).
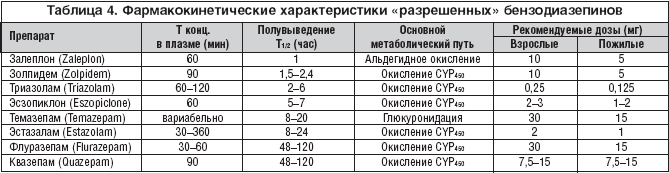
Прямые бензодиазепины через рецепторы бензодиазепин–g–аминомасляной кислоты воздействуют на хлорные каналы. Непрямые агонисты бензодиазепиновых рецепторов воздействуют аналогично, но отличаются другой степенью сродства к рецептору. Основные фармакокинетические характеристики «одобренных» бензодиазепинов приведены в таблице 4.
Большинство РКИ демонстрируют эффективность бензодиазепинов и непрямых агонистов бензодиазепиновых рецепторов в устранении кратковременной бессонницы. Однако ни одно из исследований, вошедших в анализ, не продолжалось более 6 месяцев.
Интерес представляет мета–анализ, включающий 22 РКИ, изучавших действие бензодиазепинов и непрямых агонистов бензодиазепиновых рецепторов. Данные убедительно показывают достоверное улучшение латентности ко сну, возрастание общего времени сна, уменьшение количества пробуждений и улучшение качества сна [23]. Исследуемая группа, получающая данный класс препаратов, имела процентный прирост по многим основным показателям. Так, они на 29% быстрее засыпали, на 24% дольше спали, на 28% реже просыпались и имели на 27% более высокое качество сна. Препараты с коротким периодом полувыведения оказывали преимущественное действие на латентность ко сну, тогда как препараты со средним и продолжительным периодом полувыведения достоверно увеличивали общее время сна.
В другой мета–анализ, оценивающий эффективность терапии бензодиазепинами, были включены препараты короткого, среднего и длительного периода полувыведения. Обнаружено положительное влияние данного класса препаратов на общее время сна, но не выявлено достоверных изменений латентности ко сну [24].
Исследование непрямого агониста бензодиазепиновых рецепторов залеплона (zaleplon) обнаружило снижение показателя латентности ко сну на 50% по сравнению с исходным уровнем, но не выявило достоверного изменения общего времени сна. Выявленное действие объясняется коротким временем полувыведения препарата. Однако залеплон, назначаемый спустя 3,5 часа после наступления сна, увеличивал общее время сна на 4 часа, не вызывая дневной сонливости или нарушений когнитивной функции днем [25,26].
Шестимесячное исследование непрямого агониста рецепторов бензодиазепина со средним периодом полувыведения эсзопиклона (eszopiclone) выявило 50%–е снижение латентности ко сну и 65%–е снижение времени пробуждений в период сна по сравнению с исходным уровнем. В исследовании было показано, что использование препарата с регулярностью 3–5 раз в неделю высокоэффективно при хронической бессоннице. Интересно, что ухудшение сна не происходило даже в те дни недели, когда препарат не назначался [28–30].
Отмена лекарственной терапии может провоцировать «рикошетную инсомнию». Такие случаи крайне редки при отмене терапии бензодиазепинами длительного периода полувыведения, редко встречаются после отмены бензодиазепинов среднего периода полувыведения [31,33]. Однако обнаружена выраженная рикошетная инсомния после отмены бензодиазепина короткого периода полувыведения триазолама длительностью от одной до трех ночей [34,35]. В противоположность сказанному исследование бензодиазепина короткого периода полувыведения золпидема не обнаружило рикошетной инсомнии при отмене препарата [31,34,37]. Аналогичный результат наблюдался при исследовании залеплона [25,27].
Проведенные исследования свидетельствуют о необходимости индивидуального подбора лекарственного препарата. Решение о назначении того или иного препарата во многом будет зависеть от периода его полувыведения и дозы, длительности курсового лечения и характера инсомнии (острая или хроническая) [36].
Имеются сообщения о нескольких случаях антероградной амнезии на следующий день после назначения триазолама, однако распространенность этого побочного эффекта неизвестна. Несмотря на то, что ряд исследований демонстрируют различной степени выраженности дефициты памяти при использовании всех бензодиазепинов [39], клинически значимая амнезия присуща препаратам короткого периода полувыведения. Амнезия, включая ассоциированную со сном булимию, чаще наблюдается при использовании золпидема [40,41] и намного реже при назначении более продолжительного по периоду полувыведения триазолама. Наиболее частыми побочными эффектами бензодиазепинов длительного периода полувыведения являются избыточная дневная сонливость и нарушение координации движений [33]. Крайне редко они отмечаются у препаратов среднего периода полувыведения. Практически никогда они не наблюдаются у препаратов короткого периода полувыведения. К сожалению, резкое возрастание побочных эффектов становится возможным при использовании высоких доз препаратов, например, триазолама (triazolam) [33]. Побочные эффекты чаще наблюдаются у пожилых пациентов и обычно требуют снижения дозы. В ряде исследований назначение бензодиазепинов продолжительного периода полувыведения пожилым лицам было ассоциировано с повышением риска травм от падений (переломы бедра) [42].
Проблемой большинства исследований препаратов группы бензодиазепинов является ограниченная продолжительность наблюдения за пациентами. Так, средняя продолжительность в 22 РКИ, включенных в вышеупомянутый мета–анализ, составила всего 12 дней (максимальный период 35 дней). Кратковременная устойчивость к препарату, измеряемая как ухудшение сна во время его назначения, не отмечалась при 8–недельном назначении темазепама, 5–недельного ежедневного [37,43] или 12–недельного периодического назначения золпидема [30] или залепона [25,27]. Наиболее продолжительное наблюдение – 6–месячное исследование эсзопиклона продемонстрировало устойчивые положительные эффекты на сон без развития толерантности к препарату [28].
В последнее время участились случаи назначения антидепрессантов с седативным эффектом [44], несмотря на малочисленность данных РКИ в поддержку такой практики. Так, лишь некоторые рандомизированные исследования отмечают эффективность тразодона (trazodone) при лечении вторичной инсомнии у пациентов с депрессией [44,45].
В 14–дневном исследовании латентности и длительности сна у пациентов с первичной инсомнией назначение золпидема оказывало больший положительный эффект, чем тразодон и плацебо [47]. 4–недельное исследование трициклического антидепрессанта доксепина у пациентов с первичной инсомнией продемонстрировало достоверное влияние препарата на: латентность ко сну (уменьшение на 21% от исходного), эффективность сна (повышение на 13% от исходного), общее время сна (повышение на 13% от исходного) [48]. Однако трициклические антидепрессанты обладают целым спектром побочных эффектов, таких как сухость во рту, ортостатическая артериальная гипотензия, сонливость, сердечные аритмии, увеличение веса тела, запоры и приапизм. Тетрациклический антидепрессант миртазапин, обладающий свойствами адренергического и серотонинергического антагониста, уменьшает время бодрствования во время сна, увеличивает эффективность сна, увеличивает продолжительность медленно–волнового сна у здоровых людей [49]. Однако для него отсутствуют убедительные данные об эффективности при первичной инсомнии.
Основными субстанциями в лечении инсомнии считаются седативный блокатор H1–гистаминовых рецепторов доксиламин и гормональный препарат мелатонин.
Доксиламин (Донормил) – блокатор H1–гистаминовых рецепторов из группы этаноламинов, известен начиная с 1948 года. Он оказывает выраженное М–холинолитическое действие. Достоверно сокращает время засыпания, повышает длительность и качество сна, не нарушает структуры и фаз сна. Хорошо абсорбируется из ЖКТ. Проходит гистогематические барьеры (включая ГЭБ) и распределяется по тканям и органам. Метаболизируется в печени. Экскретируется почками (60% в неизмененном виде).
В ряде работ было показано, что доксиламин составляет достойную альтернативу бензодиазепинам. Так, в многоцентровом рандомизированном двойном слепом исследовании с 3 параллельными группами и участием 338 пациентов в возрасте от 18 до 73 лет сравнивалась эффективность и переносимость доксиламина (15 мг) с золпидемом (10 мг) и плацебо при лечении инсомнии (с изучением синдрома отмены). Исследование подтвердило преимущество доксиламина над плацебо в отношении снотворного действия. С другой стороны, была продемонстрирована как высокая эффективность доксиламина и золпидема, так и хорошая переносимость препаратов без развития синдрома отмены. Доксиламин был эффективнее плацебо в отношении большинства симптомов инсомнии (время засыпания, качество и продолжительность сна, частота пробуждений) и не отличался от золпидема по влиянию на дневную сонливость. Интересно, что высокое качество сна, отмечаемое на терапии доксиламином и золпидемом, сохранялось в течение 1 недели после отмены препаратов. Положительный терапевтический эффект тем не менее сопровождался незначительными побочными эффектами, не требовавшими отмены лекарственного препарата и самостоятельно проходящими при прекращении курсовой терапии. Так, сонливость, астения, усталость были отмечены у 13,5% пациентов, получавших доксиламин, и у 6,7% пациентов, получавших золпидем. Функциональные гастроинтестинальные нарушения чаще отмечались при приеме золпидема (9,3%), чем плацебо (7,3%) и доксиламина (7,2%). Общая оценка исследователей в отношении переносимости препаратов после 2 недель терапии была положительной в 85% случаев. При приеме доксиламина не обнаружен «синдром отмены» [50].
Учитывая высокую безопасность доксиламина, возможно рекомендовать его в качестве препарата «первой линии» в лечении первичной инсомнии при отсутствии у пациента очевидных противопоказаний к его назначению (гиперчувствительность, закрытоугольная глаукома, аденома предстательной железы, нарушения мочеиспускания различного генеза, беременность, кормление грудью, возраст до 15 лет) [21].
Рандомизированные исследования мелатонина включали малое количество пациентов, имели кратковременный период наблюдения и разнообразие в дозах. Кроме того, они продемонстрировали достаточно противоречивые результаты [22].
Вопросы, на которые
нет определенного ответа
Несмотря на то, что поведенческая психотерапия признается эффективной при первичной инсомнии, ее роль при вторичной инсомнии, особенно вызванной психиатрическими расстройствами, систематически не исследована. Необходимо ясное представление о том, смогут ли практикующие терапевты, учитывая их большую занятость, добиться устойчивых результатов в обучении пациентов за малое число занятий. Для пациентов с хронической инсомнией, устойчивой к поведенческой психотерапии, остается неясной роль длительной лекарственной терапии. Несмотря на имеющиеся 6–месячные исследования назначения непрямых агонистов бензодиазепиновых рецепторов, показавших свою эффективность без развития лекарственной устойчивости, остаются невыясненными последствия терапии длительностью 1 год и более. К сожалению, место агонистов мелатониновых рецепторов в лечении как острой, так и хронической инсомнии остается малопонятным.
Руководства по лечению
инсомнии профессиональных обществ
В 2006 г. Американская академия медицины сна (American Academy of Sleep Medicine – AASM) опубликовала рекомендуемые ею алгоритмы диагностики и лечения хронической инсомнии, основанные на большой доказательной базе. Указанная терапия включала фармакологические и нефармакологические методы коррекции. В нефармакологической терапии инсомнии рекомендовались мультикомпонентная поведенческая психотерапия, использующая методики контроля стимулов, прогрессирующая мышечная релаксация, метод аутотренинга с обратной связью. В качестве базовой медикаментозной терапии хронической инсомнии рекомендован индивидуальный подбор разрешенных лекарственных средств: бензодиазепинов, непрямых агонистов бензодиазепиновых рецепторов и антидепрессантов с седативным действием [51].
Заключение и рекомендации
Изложив свои доводы и предоставив, на наш взгляд, достаточные аргументы, мы хотели бы ответить на поставленные вопросы: «Какое расстройство сна существует у Елизаветы П.? Какова в этом случае лечебная тактика? Какую медикаментозную терапию необходимо проводить у таких пациентов?»
Совокупность анамнестических данных и характер заболевания у Елизаветы П. свидетельствовали о наличии первичной инсомнии. Тем не менее перед постановкой диагноза первичной инсомнии необходимо установить все вторичные причины заболевания. Начиная терапию, мы располагали данными о том, что эффективное лечение возможно для большинства пациентов с хронической инсомнией, несмотря на то, что доказательная база поведенческой психотерапии и фармакологической коррекции не располагала данными об отдаленных результатах.
Мы рекомендовали начать терапию с курса поведенческой психотерапии, включающей контроль стимулов, релаксацию, обучение правильной гигиене сна и другие описанные выше методы. Для этого нами самостоятельно был осуществлен короткий вводный курс. Пациентка получила соответствующие печатные материалы для самостоятельного ознакомления и обучения. Хочется отметить, что мы не встретили серьезных препятствий при проведении указанной терапии. Думается, что врачи первичной практики смогут самостоятельно применять эти методы к своим пациентам или направлять пациентов с инсомнией к специалистам медицины сна или подготовленным психологам. Следует помнить, что поведенческую психотерапию не следует сочетать со снотворными препаратами, так как они могут снижать ее эффективность.
Подавляющее большинство специалистов рекомендуют долговременное применение фармакотерапии в подгруппе пациентов с хронической первичной бессонницей, плохо отвечающей на поведенческую психотерапию. Наиболее тщательный мониторинг эффективности, толерантности и побочных действий лекарственных препаратов необходимо осуществлять в группе пожилых пациентов. При инсомнии, затрагивающей процессы инициации сна, рационально применение золпидема и залеплона. При инсомнии, проявляющейся гиперактивациями в период сна, возможно назначение бензодиазепинов среднего периода полувыведения, таких как темазепам. Бензодиазепин с коротким периодом полувыведения залеплон эффективен при частых пробуждениях во второй половине ночи. Бензодиазепины длительного периода полувыведения не являются препаратами выбора в терапии хронической инсомнии (за исключением случаев ее сочетания с сопутствующим тревожным расстройством). Альтернативу бензодиазепинам составляет Донормил. Учитывая высокую безопасность доксиламина, возможно рекомендовать его в качестве препарата «первой линии» в лечении первичной инсомнии.



Литература
1. Morin CM, Hauri PJ, Espie CA, Spielman AJ, Buysse DJ, Bootzin RR. Nonpharmacologic treatment of chronic insomnia: an American Academy of Sleep Medicine review. Sleep 1999; 22: 1134–56.
2. Costa e Silva JA, Chase M, Sartorius M, Roth T. Special report from a symposium held by the World Health Organization and the World Federation of Sleep Research Societies: an overview of insomnias and related disorders – recognition, epidemiology, and rational management. Sleep 1996; 19: 412–6.
3. The international classification of sleep disorders, revised: diagnostic and coding manual. Rochester, Minn.: American Sleep Disorders Association, 1997.
4. Morin CM, Culbert JP, Schwartz SM. Nonpharmacological interventions for insomnia: a meta–analysis of treatment efficacy. Am J Psychiatry 1994; 151:1172–80.
5. Spielman AJ, Caruso LS, Glovinsky PB. A behavioral perspective on insomnia treatment. Psychiatr Clin North Am 1987; 10:541–53.
6. Littner M, Hirshkowitz M, Kramer M, et al. Practice parameters for using polysomnography to evaluate insomnia: an update. Sleep 2003; 26:754–60.
7. The international classification of sleep disorders: diagnostic & coding manual, ICDS–2. 2nded. Westchester, Ill.: American Academy of Sleep Medicine, 2005.
8. Perlis ML, Smith MT, Pigeon WR. Etiology and pathophysiology of insomnia. In: KrygerMH, RothT, Dement WC, eds. Principles and practice of sleep medicine. 4th ed. Philadelphia: Elsevier/Saunders, 2005: 714–25.
9. Bootzin RR, Epstein D, Wood JM. Stimulus control instructions. In: Hauri PJ, ed. Case studies in insomnia. New York: Plenum Medical Book, 1991:19–28.
10. Spielman AJ, Saskin P, Thorpy MJ. Treatment of chronic insomnia by restriction of time in bed. Sleep 1987; 10:45–56.
11. Hauri PJ. Sleep hygiene, relaxation therapy, and cognitive interventions. In: Hauri PJ, ed. Case studies in insomnia. New York: Plenum Medical Book, 1991:65–84.
12. Murtagh DRR, Greenwood KM. Identifying effective psychological treatments for insomnia: a meta–analysis. J Consult Clin Psychol 1995;63:79–89.
13. Espie CA, Inglis SJ, Tessier S, Harvey L. The clinical effectiveness of cognitive behaviour therapy for chronic insomnia: implementation and evaluation of a sleep clinic in general medical practice. Behav Res Ther 2001;39:45–60.
14. Edinger JD, Wohlgemuth WK, Radtke RA, Marsh GR, Quillian RE. Cognitive be havioral therapy for treatment of chronic primary insomnia: a randomized controlled trial. JAMA 2001; 285:1856–64.
15. Turner RM, Ascher LM. Therapist factor in the treatment of insomnia. Behav Res Ther 1982;20:33–40.
16. Morgan K, Dixon S, Mather N, Thompson J, Tomeny M. Psychological treatment for insomnia in the management of long–term hypnotic drug use: a pragmatic randomised controlled trial. Br J Gen Pract 2003;53:923–8.
17. Baillargeon L, Demers L, Ladouceur R. Stimulus–control: nonpharmacologic treatment for insomnia. Can Fam Physician 1998; 44:73–9.
18. Edinger JD, Sampson WS. A primary care «friendly» cognitive behavioral insomnia therapy. Sleep 2003; 26:177–82.
19. Riedel BW, Lichstein KL, Dwyer WO. Sleep compression and sleep education for older insomniacs: self–help versus therapist guidance. Psychol Aging 1995; 10:54–63.
20. Mimeault V, Morin CM. Self–help treatment for insomnia: bibliotherapy with and without professional guidance. J Consult Clin Psychol 1999;67:511–9.
21. Meoli AL, Rosen CL, Kristo D, etal. Oral nonprescription treatment for insomnia: an evaluation of products with limited evidence. J Clin Sleep Med 2005;1:173–87.
22. Rogers NL, Dinges DF, Kennaway DJ, Dawson D. Potential action of melatonin in insomnia. Sleep 2003; 26:1058–9.
23. Nowell PD, Mazumdar S, Buysse DJ, Dew MA, Reynolds CF III, Kupfer DJ. Benzodiazepines and zolpidem for chronic insomnia: a meta–analysis of treatment efficacy. JAMA 1997; 278:2170–7.
24. Holbrook AM, Crowther R, Lotter A, Cheng C, King D. Meta–analysis of benzodiazepine use in the treatment of insomnia. CMAJ 2000;162:225–33.
25. Elie R, Ruther E, Farr I, Elilien G, Salinas E. Sleep latency is shortened during 4 weeks of treatment with zaleplon, a novel nonbenzodiazepine hypnotic. J Clin Psychiatry 1999; 60:536–44.
26. Walsh JK, Vogel GW, Scharf M, et al. A five week, polysomnographic assessment of zaleplon 10 mg for the treatment of primary insomnia. Sleep Med 2000; 1:41–9.
27. Walsh JK, Pollak CP, Scharf MB, Schweitzer PK, Vogel GW. Lack of residual sedation following middle–of–the–night zaleplon administration in sleep maintenance insomnia. Clin Neuropharmacol 2000; 23:17–21.
28. Krystal AD, Walsh JK, Laska E, et al. Sustained efficacy of eszopiclone over 6 months of nightly treatment: results of a randomized, double–blind, placebo–controlled study of adults with chronic insomnia. Sleep 2003; 26:793–9.
29. Walsh JK, Roth T, Randazzo A, et al. Eight weeks of non–nightly use of zolpidem for primary insomnia. Sleep 2000; 23:1087–96.
30. Perlis ML, McCall WV, Krystal AD, Walsh JK. Long–term, non–nightly administration of zolpidem in the treatment of patients with primary insomnia. J Clin Psychiatry 2004; 65:1128–37.
31. Voshaar RC, van Balkom AJ, Zitman FG. Zolpidem is not superior to temazepam with respect to rebound insomnia: a controlled study. Eur Neuropsychopharmacol 2004; 14:301–6.
32. Vogel GW, Morris D. The effects of estazolam on sleep, performance, and memory: a long–term sleep laboratory study of elderly insomniacs. J Clin Pharmacol 1992;32:647–51.
33. Roth T, Roehrs TA. A review of the safety profiles of benzodiazepine hypnotics. J Clin Psychiatry 1991; 52: Suppl:38–41.
34. Monti JM, Attali P, Monti D, Zipfel A, de la Giclais B, Morselli PL. Zolpidem and rebound insomnia – a double–blind, controlled polysomnographic study in chronic insomniac patients. Pharmacopsychiatry 1994;27:166–75.
35. Soldatos CR, Dikeos DG, Whitehead A. Tolerance and rebound insomnia with rapidly eliminated hypnotics: a meta–analysis of sleep laboratory studies. Int Clin Psychopharmacol 1999;14:287–303.
36. Greenblatt DJ, Harmatz JS, Zinny MA, Shader RI. Effect of gradual withdrawal on the rebound sleep disorder after discontinuation of triazolam. N Engl J Med 1987; 317: 722–8.
37. ScharfMB, Roth T, Vogel GW, Walsh JK. A multicenter, placebo–controlled study evaluating zolpidem in the treatment of chronic insomnia. J Clin Psychiatry 1994; 55:192–9.
38. Rothschild AJ. Disinhibition, amnestic reactions, and other adverse reactions secondary to triazolam: a review of the literature. J Clin Psychiatry 1992; 53:Suppl:69–79.
39. Roth T, Hartse KM, Saab PG, Piccione PM, Kramer M. The effects of flurazepam, lorazepam, and triazolam on sleep and memory. Psychopharmacology (Berl) 1980; 70:231–7.
40. Canaday BR. Amnesia possibly associated with zolpidem administration. Pharmacotherapy 1996;16 :687–9.
41. Morgenthaler TI, Silber MH. Amnestic sleep–related eating disorder associated with zolpidem. Sleep Med 2002; 3:323–7.
42. Mendelson WB. Clinical distinctions between long–acting and short–acting benzodiazepines. J Clin Psychiatry 1992; 53: Suppl: 4–7.
43. Morin CM, Colecchi C, Stone J, Sood R, Brink D. Behavioral and pharmacological therapies for late–life insomnia: a randomized controlled trial. JAMA 1999; 281:991–9.
44. Walsh JK, Schweitzer PK. Ten–year trends in the pharmacological treatment of insomnia. Sleep 1999; 22:371–5.
45. Kaynak H, Kaynak D, Gozukirmizi E, Guilleminault С. The effects of trazodone on sleep in patients treated with stimulant antidepressants. Sleep Med 2004; 5:15–20.
46. Nierenberg AA, Adler LA, Peselow E, Zornberg G, Rosenthal M. Trazodone for antidepressant–associated insomnia. Am J Psychiatry 1994;151:1069–72.
47. Walsh JK, Erman M, Erwin CW, et al. Subjective hypnotic efficacy of trazodone in DSM3–R primary insomnia. Hum Psycho pharmacol 1998;13:191–8.
48. Hajak G, Rodenbeck A, Voderholzer U, et al. Doxepin in the treatment of primary insomnia: a placebo–controlled, double–blind, polysomnographic study. J Clin Psychiatry 2001;62:453–63.
49. Aslan S, Isik E, Cosar B. The effects of mirtazapine on sleep: a placebo controlled, double–blind study in young healthy volunteers. Sleep 2002; 25:677–9.
50. Hausser–Hauw et al. Effect on sleep architecture and residual effect of a dose of 15 mg of Doxylamine versus triazolam treatment in persistent sleep–onset insomnia. Sep Hop Paris 1995; 71: no 23–24, 742–750.
51. Practice Parameters for the Psychological and Behavioral Treatment of Insomnia: An Update. An American Academy of Sleep Medicine Report. Sleep 2006; 29: 650–9.












