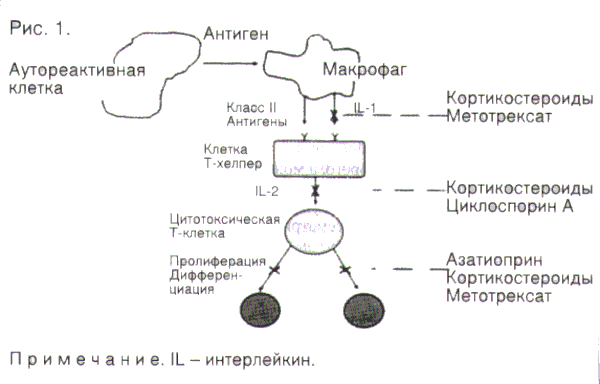
МТ вначале использовался как химиотерапевтический препарат для лечения лейкемии. В обычных условиях фолиевая кислота превращается в клетках в восстановленную активную форму витамина, которая называется тетрагидрофолатом (FH4). Этот FH4 является важной молекулой-носителем для одноуглеродных соединений и играет первичную роль в синтезе пиримидинов, пуринов и аминокислот. Превращение фолиевой кислоты в ее активную форму происходит при участии катализатора дигидрофолатредуктазы. МТ является сильным ингибитором этого фермента и, таким образом, препятствует образованию активного тетрагидрофолата. В результате он затрагивает синтез ДНК, РНК и протеинов. Наличие таких характеристик объясняет использование МТ у больных раком или псориазом, у которых отмечается быстрая пролиферация эпидермальных клеток. Ингибиторные свойства также частично объясняют токсичность МТ для нормальных тканей.
В
противоположность его хорошо
известной противораковой
активности механизм действия МТ в
качестве противовоспалительного и
иммуносупрессивного препарата
изучен недостаточно.
Эти свойства МТ в основном
наблюдаются при лечении пациентов
с ревматоидныи артритом.
И здесь антагонизм фолата может
играть важную роль, ингибируя
пролиферацию мононуклеарных
лейкоцитов путем подавления
реакции метилирования, что
приводит к уменьшению образования
токсических медиаторов в участках
воспаления, вызывая накопление
аденозиновых радикалов,
сопровождаемое снижением функции
клеток воспаления.
Важным аргументом,
подтверждающим существенную роль
антагонизма фолата, является тот
факт, что МТ утрачивает свою
активность в тех случаях, когда
пациенты с ревматоидным артритом
получают лечение МТ в сочетании с
высокими дозами активного
восстановленого тетрафолата или
лейковорина (leucovorin). Более того, МТ
существенным образом воздействует
на различные цетокины, такие как
интерлейкины-1, 2 и 6, которые играют
важную роль в иммунорегуляции и
патогенезе так называемых иммунных
нарушений. Подавление активности
интерлейкина-1 можно объяснить
структурной аналогией между
интерлейкином-lp и ферментом
дегидрофолатредуктазой.
Экскреция МТ происходит в
основном в интактной форме с мочой,
более 80% принятой дозы выводится в
течение первых суток после приема.
Небольшая фракция
метаболизируется в печени
альдегидоксидазой и этот метаболит
также выделяется мочой. Небольшая
фракция выводится через желчные
пути и метаболизируется кишечными
бактериями. Однако более важное
значение имеет внутриклеточное
превращение МТ в депонированную
форму - полиглутамат. Эта форма
препарата задерживается в клетке
гораздо дольше и является более
эффективным ингибитором зависимых
от фолата ферментов, чем сама
родительская молекула МТ.
Полиглутамация может наблюдаться в
клетках печени, лейкемических
клетках и в различных
новообразованиях у человека.
В нормальном костном мозге и
клетках кишечника глутамация
наблюдается лишь в незначительной
степени. Эти особенности
метаболизма МТ позволяют
объяснить, почему недельная
пульсирующая доза препарата
обеспечивает постоянную
эффективность; этим же объясняется
выраженная чувствительность к
препарату некоторых
злокачественных клеточных линий и
ограниченная токсичность для таких
тканей, как костный мозг и мукоза
кишечни ка, в которых отмечается
низкий уровень образования
полиглутамата. Токсичность
является важным моментом, который
необходимо учитывать при лечении
МТ пациентов с заболеваниями
печени. Дефицит фолата,
сопровождаемый
желудочно-кишечными нарушениями,
стоматитом, и уменьшение числа
лейкоцитов и тромбоцитов в
сочетании с иммуноаллергически
индуцированным внутритканевым
пневмонитом являются наиболее
значимыми токсическими побочными
явлениями. Другие осложнения
связаны с наличием
условно-патогенных инфекций, таких
как гепатит В и инфекция вирусом
Эпштейна - Барр. Механизм,
приводящий к развитию фиброза
печени, изучен недостаточно.
Результаты нескольких
исследований показывают, что
токсичность для печени не является
значимой клинической проблемой и
что риск развития фиброза печени
подвержен значительному влиянию
других факторов, таких как наличие
диабета, ожирение, употребление
алкоголя.
Противопоказаниями к
назначению МТ являются
беременность, злоупотребление
алкоголем, ожирение и диабет,
наличие персистирующей инфекции
вирусом гепатита В и нахождение в
условиях высокого риска заражения.
Во время лечения МТ следует
избегать приема таких препаратов,
как котримоксазол (из-за его
противофолатного действия) и
различных средств, могущих
повлиять на экскрецию почками МТ.
Токсичность может быть предупреждена путем назначения небольших доз фолиевой кислоты или уменьшением дозы МТ.
МТ не следует
назначать пациентам с нарушенной
функцией почек. Во всех
исследованиях, посвященных
использованию МТ у пациентов с
заболеваниями печени, препарат
назначали в дозе 15 мг в неделю в 3
приема, интервалы между которыми
составляли 12 ч. Однако такая схема
лечения была разработана для
больных псориазом и при таком
способе введения препарат
является, по крайней мере
теоретически, более токсичным, чем
при однократном приеме. Принято
считать, что продление присутствия
препарата в сыворотке, что и
обеспечивается повторным
введением, увеличивает образование
активных, но и токсичных,
полиглутамированных производных в
клетках. Для пациентов с
ревматоидным артритом некоторые
авторы рекомендуют еженедельный
однократный прием препарата в дозе
от 5 до 15 мг. Недавно опубликованные
результаты клинического
плацебо-контролированного
испытания МТ при ПСХ, выполненного
Kaplan, показали, что значимое влияние
препарата на гистологию печени,
холангиографические данные и
печеночные тесты отсутствуют. Было
обнаружено только значимое
улучшение активности щелочной
фосфатазы. Однако у 12 из 24
пациентов, принимавших участие в
исследовании, была уже
цирротическая стадия заболевания,
поэтому их включение в испытание
представляется неправомерным.
Дальнейшие контролированнные
исследования необходимы для того,
чтобы определить терапевтическую
роль МТ у пациентов с ПСХ без
цирроза. В Лёвене было выполнено
небольшое рандомизированное
контролированное испытание МТ у
пациентов с ПБЦ без цирроза. 8
пациентов получали
комбинированное лечение МТ (15 мг в
неделю) и урсодезоксихолевой
кислотой (УДОХК) в дозе 500 мг в день. 6
пациентов не получали никакого
лечения. Все пациенты наблюдались в
течение 2 лет; сравнивали динамику
клинических, биохимических и
гистологических показателей в этих
двух группах.
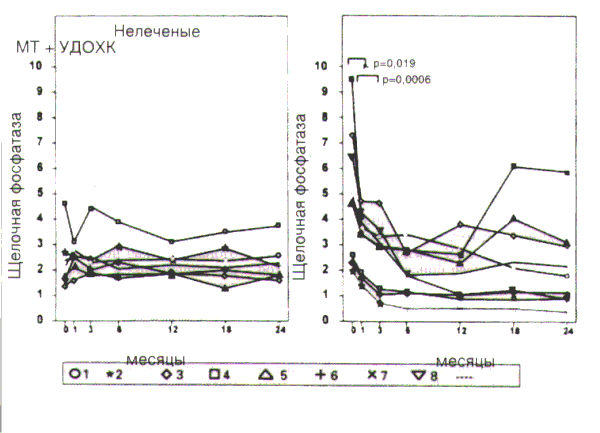
Судя по результатам этого
контролированного ис следования, лечение МТ
и УДОХК не оказывало значимого
влияния на динамику клинических и
биохимических показателей;
отмечалось лишь значимое снижение активности
щелочной фосфатазы в группе больных, получавших
активное лечение, однако значение
этого остается неясным, поскольку
активность щелочной
фосфатазы не является
прогностическим фактором у пациентов с
ПБЦ.
В нашем
исследовании токсичность
проявлялась временным повышением
уровня сывороточных трансаминаз у 5
из 8 пациентов, серьезным
внутритканевым пневмонитом,
потребовавшим отмены МТ, а также значительным
уменьшением числа лейкоцитов и
тромбоцитов. Таким образом, МТ
представляет собой
противораковый антагонист фолата,
проявляющий противовоспалительную
и иммуномодулирующую активность, в
связи с чем может быть успешно использован для
лечения острого ревматоидного
артрита и, возможно, так называемых
иммуноопосредованных
холестатических заболеваний
печени. Прием МТ
приводит к внутриклеточному
образованию очень
активных МТ-полиглутаматов,
сохраняющихся в
клетке в течение длительного
времени. Этим объясняется
эффективность импульсной терапии
низкими дозами
препарата (5 - 15 мг), которые,
возможно, следует
вводить за один прием.
Препарат
преимущественно выводится с мочой
и его не следует
назначать пациентам с нарушенной
функцией почек. При ПБЦ и ПСХ
препарат следует назначать лишь
пациентам с начальными стадиями
заболевания (гистологические
стадии I и II), которые характеризуются
иммуноопосредованным повреждением
желчных протоков. Принимая во
внимание потенциально
существенное побочное действие
препарата и отсутствие значимого
эффекта в небольших контролированных
клинических исследованиях, мы полагаем, что
использование МТ следует
ограничить большими
контролированными клиническими
испытаниями.
Взято из
"Clinical Hepatology 1995; a report of the 10th
Rotterdam Liver Day" с
разрешения главной редакции.








.gif)