Введение
Изучение эпидемиологии офтальмологических заболеваний с учетом этиопатогенеза является одним из перспективных направлений здравоохранения. Большой вклад в данный раздел фундаментальной науки вносят генетико-эпидемиологические исследования. В настоящее время в России подобные работы проводятся в ограниченном формате в отдельных регионах страны. Изучению детского населения уделяется повышенное внимание ввиду формирования нозологического спектра и груза патологии,
в т. ч. и наследственных форм офтальмологических заболеваний. В настоящее время на долю генетических форм офтальмопатологии в России приходится более 30% [1, 2]. Наследственная офтальмопатология относится к группе редких болезней с частотой встречаемости от 1:15 000 и реже [3].
С учетом клинического полиморфизма генетически гетерогенной группы заболеваний генетико-эпидемиологические исследования позволяют определить особенности нозологического спектра, отягощенность и распространенность регион-специфичных наследственных патологий. С развитием молекулярной генетики появляются новые возможности диагностики, и расширяется понимание этиопатогенеза на клеточном уровне. Полученные результаты помогают скорректировать объем и качество медико-генетической помощи населению.
Цель работы: изучить отягощенность наследственной несиндромальной офтальмологической патологией среди населения Карачаево-Черкесской Республики (КЧР) и провести молекулярно-генетическое исследование детского населения с глазной патологией.
Данная статья представляет собой первую часть комплексного офтальмо-генетического и генетико-эпидемиологического обследования детского населения КЧР, сфокусированную на оценке отягощенности регион-специфичной наследственной глазной патологии, а также полученные данные молекулярно-генетической диагностики. Вторая часть, характеризующая структуры нозологического спектра и распространенность наследственной несиндромальной офтальмологической патологии, будет опубликована позднее.
Материал и методы
Выполнено генетико-эпидемиологическое обследование населения КЧР, общая численность — 410 367 человек. Доля детского населения составила 22,1% (90 739 человек) (табл. 1). Национальный состав КЧР представлен 5 основными этносами: карачаевцами (41%), русскими (31,6%), черкесами (11,9%), абазинами (7,8%), ногайцами (3,3%); 4,4% составляют другие национальности.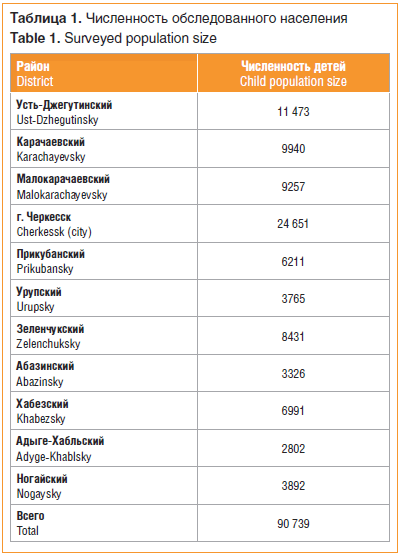
В выборку включен 121 пациент из 109 семей в возрасте от 0 до 17,9 года, средний возраст — 10,5 года. Для возможности проведения молекулярно-генетического исследования собраны образцы биоматериала (крови). От всех официальных представителей детей (родителей) получено письменное информированное согласие на обработку персональных данных, проведение обследования, выполнение исследований и публикацию в средствах массовой информации. Исследование одобрено этическим комитетом ФГБНУ «МГНЦ».
Для решения поставленной задачи использовались генетико-эпидемиологические, статистические, молекулярно-генетические методы обследования. Основными источниками регистрации больных являлись анкеты ФГБНУ «МГНЦ», заполненные медицинскими работниками республики, данные регистра инвалидов и специализированных коррекционных учебных заведений. Необходимо отметить, что метод анкетирования является наиболее эффективным при выявлении больных. Для клинико-генеалогического изучения использован обзорный метод. При эпидемиологических исследованиях необходимо придерживаться единого протокола обследования, что позволяет проводить сравнение полученных результатов. Коллектив ФГБНУ «МГНЦ» использует формат обследования населения и сбора материала, разработанный сотрудниками лаборатории генетической эпидемиологии более 35 лет назад [4–7]. Настоящий протокол позволяет выявлять широкий спектр наследственных заболеваний человека, включающий в себя всю известную изолированную наследственную патологию глаз. Протокол включает в себя комплексное обследование популяций и состоит из трех основных этапов: медико-генетического обследования популяций; изучения генетической структуры популяций прямым методом через условно-нейтральные генетические системы, а также при помощи стандартных методов популяционной генетики (F-статистики Райта, изоляция расстоянием Малеко, индекс Кроу, этническая ассортативность и т. д.); сопоставления результатов, полученных через различные генетические системы.
Статистическая обработка полученных данных проведена с помощью компьютерной программы Statistica 10.0 на персональном компьютере. С учетом клинического полиморфизма заболеваний, наличия генетической гетерогенности (локусной, аллельной) и различных видов мутаций частично проведены секвенирование кодирующих последовательностей по Сэнгеру, анализ MLPA (мультиплексная лигазозависимая амплификация зондов) для идентификации крупных делеций, анализ мутаций в интронной зоне части генов. При отсутствии идентифицированных нарушений нуклеотидной последовательности предполагается проведение секвенирования нового
поколения (NGS анализа). Отягощенность аутосомно-
доминантной и аутосомно-рецессивной патологией рассчитана как соотношение числа больных к численности обследованной популяции (на 1000 детей), Х-сцепленной на мужское население (на 1000 мальчиков). Сравнительный анализ отягощенности выполнен при помощи t-критерия Стьюдента [8]. Достоверным считался уровень значимости p<0,05.
Результаты и обсуждение
Оценка груза наследственной офтальмологической патологии органа зрения
В результате генетико-эпидемиологического обследования детского населения КЧР выявлен 121 ребенок из 109 семей с несиндромальной наследственной офтальмопатологией. У 78 детей из 67 семей диагностирована аутосомно-доминантная (АД) патология органа зрения, аутосомно-рецессивные (АР) заболевания выявлены у 40 детей из 39 семей, Х-сцепленные болезни — у 3 пациентов из 3 семей.Значение отягощенности детского населения обследованных районов КЧР наследственной офтальмопатологией составило 1,33±0,12, при сравнении вклада АР-патологии с АД-заболеваниями выявлено преобладание последних (t=3,44) (табл. 2).
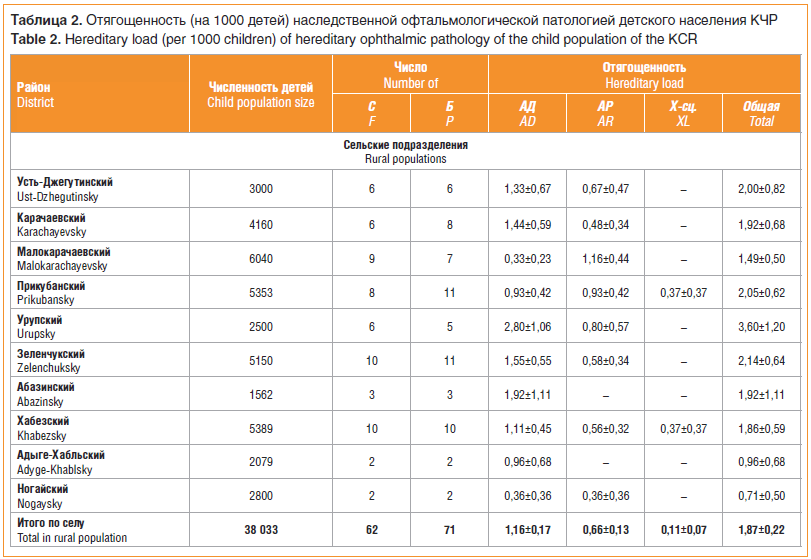
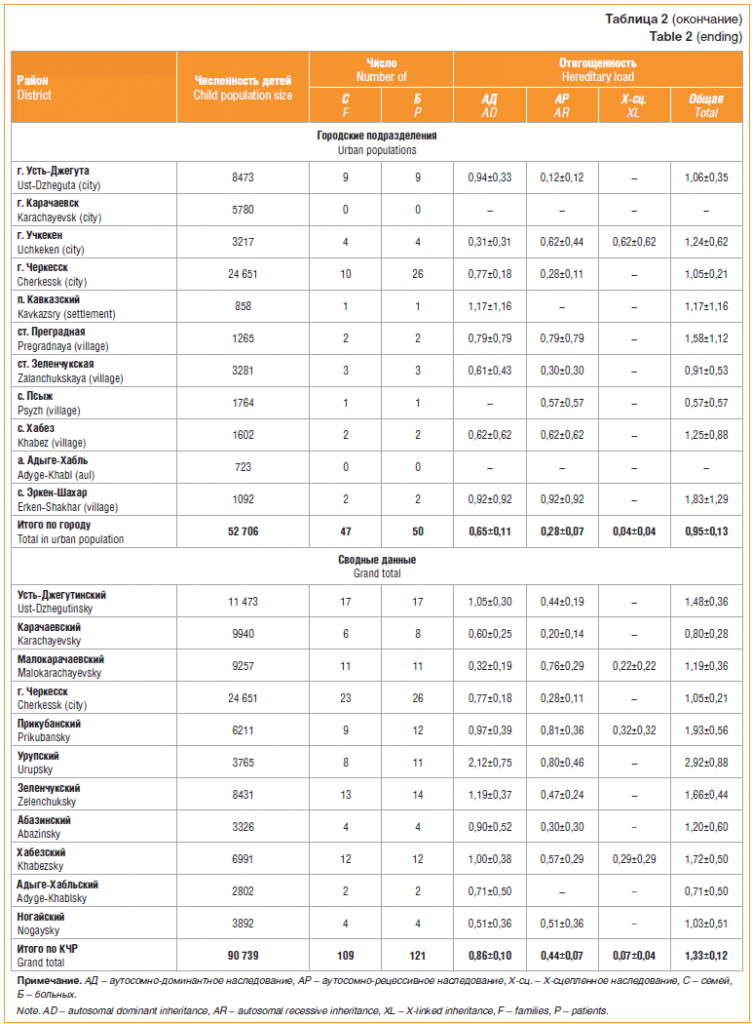
В результате статистического анализа полученных данных выявлены статистически достоверные различия между аутосомно-доминантной патологией у сельского и у городского населения (t=2,5). Аналогичная закономерность наблюдалась при аутосомно-рецессивной патологии (t=2,5). Выявлено преобладание АД-патологии над заболеваниями с АР-наследованием как в сельской (t=2,3), так и в городской субпопуляции (t=2,8). При сравнении суммарных данных отягощенности сельского и городского населения выявлены более высокие значения у больных из сельской местности (t=3,6).
Статистически значимых различий отягощенности между районами не выявлено, что характеризуется относительно равномерным распределением заболеваемости наследственной офтальмопатологией детского населения обследованного региона. Из-за малого количества пациентов с Х-сцепленной патологией статистически достоверных различий между районами выявить не удалось.
Полученные результаты показывают высокую отягощенность детского населения КЧР наследственной офтальмопатологией и указывают на необходимость проведения корректировки медико-реабилитационной помощи.
Результаты молекулярно-генетической диагностики
Группе пациентов проведена молекулярно-генетическая диагностика с целью возможной верификации клинико-генетической формы заболевания.В качестве клинических примеров приведем несколько случаев.
Семья К. из Зеленчукского района с больным ребенком 14 лет, диагноз при направлении: кератопатия. Акушерский анамнез без особенностей. Синдромальная патология на момент осмотра не выявлена. Острота зрения обоих глаз — светоощущение. Уровень внутриглазного давления (ВГД) — в пределах возрастной нормы.
При биомикроскопии на обеих роговицах выявлены помутнения средней интенсивности в центральных и парацентральных отделах с плотными очагами в центре. В патологический процесс вовлечены передний эпителий роговицы и часть стромального слоя. Остальные структуры органа зрения — без видимой патологии. По клиническим данным диагностирована центральная дистрофия роговицы, тип Гренуа. В результате молекулярно-генетической диагностики выявлены патологические варианты нуклеотидной последовательности в гене CHST6 (описанный NM_021615.4 (CHST6_v001): c.610C>T, p.Pro204Ser [10] и ранее не описанный c.1124delT, p.Val375Glyfs*6) в компаунд-гетерозиготном состоянии. Таким образом, диагноз «центральная дистрофия роговицы, тип Гренуа, с аутосомно-рецессивным типом наследования» подтвержден. Пациенту проведено медико-генетическое консультирование и скорректирована консервативная терапия.
В семье К. из Зеленчукского района (3 больных) и семье А. (1 больной) из г. Черкесска выявлена аниридия. Для этих больных проведена подтверждающая ДНК-диагностика. В результате секвенирования кодирующей последовательности гена PAX6 и MLPA анализа выявлены мутации в гене в обеих семьях. В первой семье (аниридией поражены 2 сибса и их мать) в экзоне 8 гена PAX6 найдена известная по литературным данным 1 из 3 частых мутаций, встречающихся в различных популяциях человека [11], нонсенс-мутация c.607C>T, p.Arg203Ter, в гетерозиготном состоянии. Во второй семье — в единичном случае врожденной аниридии — обнаружена ранее не описанная гетерозиготная делеция 5 экзонов гена PAX6: hg18: chr11:31778912_31794631del.
Семья К. из г. Черкесска, обследованная в Урупском
районе, с больным ребенком 11 лет. Из анамнеза установлено, что снижение зрения отмечалось с 7 лет. Экзогенного воздействия на зрительный анализатор не было. Синдромальной наследственной патологии на момент осмотра не выявлено. Акушерский анамнез не отягощен. Роды в срок. Рост и развитие — в соответствии с возрастом. При офтальмологическом обследовании обоих глаз выявлено: острота зрения — счет пальцев у лица, коррекции не поддается; уровень ВГД — норма; передний отрезок глаз — вариант возрастной нормы; на глазном дне в макулярной области рефлекс сглажен, очаговая депигментация — со сливными очажками атрофии, кольцевое отграничение макулы слабо-пигментным кольцом, по ходу сосудистых аркад — белесоватые очаги мелких размеров, пигментные депозиты отсутствуют. Выполнено молекулярно-генетическое исследование. Выявлен ранее описанный патогенный вариант нуклеотидной последовательности в гене ABCA4 (NM_000350.2 (ABCA4_v001): c.2966T>C) в гетерозиготном состоянии [12].
Вторая мутация не обнаружена с помощью высокопроизводительного секвенирования, что может быть вызвано ограничением метода. C учетом полученных данных установлен клинико-генетический диагноз: беспигментная тапеторетинальная абиотрофия. Проведено медико-
генетическое консультирование.
В настоящее время часть биоматериала пациентов находится в процессе исследования. Затруднения верификации генетического варианта связаны с клиническим полиморфизмом и генетической гетерогенностью данной группы заболеваний.
В результате генетико-эпидемиологического обследования детского населения КЧР установлено, что большую часть наследственной глазной патологии составляют аутосомно-доминантные формы (t=2,3). Суммарное значение отягощенности детского населения КЧР составило 1,33±0,12 (1:671). Выявлены статистически достоверные различия отягощенности между сельской
и городской популяциями региона для аутосомно-доминантной и аутосомно-рецессивной патологии (t=2,5). Выявлено, что более высокие значения отягощенности — у больных из сельской местности (t=3,6). В результате молекулярно-генетических исследований группе пациентов установлены клинико-генетические формы патологий. Регион-специфических патологических нуклеотидных последовательностей не выявлено. Комплексное генетико-эпидемиологическое обследование детского населения КЧР позволяет разработать регион-специфичную педиатрическую медико-реабилитационную программу и проводить корректные профилактические мероприятия.
Сведения об авторах: 1Кадышев Виталий Викторович — к.м.н., ст. науч. сотр. лаборатории генетической эпидемиологии. 1Марахонов Андрей Владимирович — к.б.н., ст. науч. сотр. лаборатории генетической эпидемиологии. 1,2Куцев Сергей Иванович — д.м.н., профессор, член-корр. РАН, директор ФГБНУ «МГНЦ», зав. кафедрой молекулярной и клеточной генетики МБФ, главный внештатный специалист по медицинской генетике Минздрава России. 1,3Зинченко Рена Абульфазовна — д.м.н., профессор, зам. директора по научно-клинической работе; зав. лабораторией генетической эпидемиологии, профессор курса клинической фармакологии кафедры организационно-правого обеспечения медицинской и фармацевтической деятельности. 1ФГБНУ «МГНЦ». 115522, Российская Федерация, г. Москва, ул. Москворечье, д. 1. 2ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. 117997, Российская Федерация, г. Москва, ул. Островитянова, д. 1. 3ГБУЗ МО МОНИКИ им. М.Ф. Владимирского. 129110, Российская Федерация, г. Москва, ул. Щепкина, д. 61/2. Контактная информация: Кадышев Виталий Викторович, e-mail: vvh.kad@gmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 23.04.2018.
Исследование выполнено при финансовой поддержке гранта РФФИ № 18–015–00090.
About the authors: 1Vitaly V. Kadyshev — PhD, MD, Senior Research Scientist in Laboratory of Genetic Epidemiology. 1Andrey V. Marakhonov — PhD, MD, Senior Research Scientist in Laboratory of Genetic Epidemiology. 1,2Sergey I. Kutsev – professor, Dr. Sci., MD, corresponding member of RAS, director of the Research Centre for Medical Genetics, head of the Department of molecular and cell genetics. 1,3Rena A. Zinchenko — professor, Dr. Sci., MD, vice director, head of the Laboratory of Genetic Epidemiology. 1Research Center for Medical Genetics. 1, Moskvorechie Str., Moscow, 115522, Russian Federation. 2Pirogov Russian National Research Medical University. 1, Ostrovitianova st., Moscow,117997, Russian Federation. 3Moscow Regional research and clinical Institute. 61/2, Shepkina str., Moscow, 129110, Russian Federation. Contact information: Vitaly V. Kadyshev, e-mail: vvh.kad@gmail.com. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 23.04.2018.
Supported by Russian Foundation for Basic Research grant № 18–015–00090.












