E.B. Tretyak, I.N. Efremov,
A.A. Ryabtseva, S.V. Suchkov
The present review summarizes data on modern and perspective approaches to the treatment of isolated forms of autoimmune uveitis using pharmacological preparations with a broad spectrum of activity. The current progress in understanding molecular–cellular mechanisms of immunoregulation allows to concentrate on the correction of immune disorders and suppression of aggression of autoreactive T–lymphocytes clones to uveoretinal tissue. Nowadays, corticosteroids remain the basic medication in the treatment of uveitis. However most of these preparations are rather toxic for the whole organism. When used at doses, that allow to achieve stable remission, they cause numerous side effects. At smaller doses – allowing to minimize harmful side effects – it is not possible to control the course of the disease. Hence optimal immunosuppressors are those that are characterized by significant anti–inflammatory action and minimal risk in respect to side effects. Among several modern approaches to the therapy of autoimmune uveitis, immunosuppressors with a more specific effect on the damaged uveoretinal tissue are most promising for the everyday clinical practice. Their application would help reduce harmful side effect that are characteristic of the group of nonspecific immunosuppressors.
Введение
Понимание молекулярно–клеточных механизмов иммунорегуляции раскрывает уникальные возможности для создания и развития новейших лечебно–реабилитационных технологий в практике заболеваний аутоиммунной природы, к которым принадлежит аутоиммунный увеит [Mochizuki M., 1987; Chan C.C. and Li Q., 1998; Zierhut M. et al., 2000; Foxman E.F. et al., 2002; Morgan J.P et al., 2002; Zhang X. et al., 2002].
Известно, что в контроле аутореактивности у больных с аутоиммунным увеитом участвуют два основных вида иммунного ответа – генетически детерминированный (наследственный) и приобретенный (адаптивный). Последний, в основе которого лежат механизмы Т–клеточной и антителоопосредованной иммунологической реактивности, играет в патогенезе аутоиммунных нарушений у больных с увеитами ключевую роль [Mochizuki M., 1987; Chan C.C. and Li Q., 1998; Streilein J.W., 2001; Foxman E.F. et al., 2002]. Вполне вероятно, что терапевтические фармакоконструкции и современные программы иммуно– и генотерапии аутоиммунного увеита, разрабатываемые как в целях предотвращения гиперактивации клеточного и гуморального звеньев иммунитета, так и для контроля уровней активности этих звеньев в постактивационном периоде, составят основу того ближайшего будущего, которое определит клинический успех лечебно–реабилитационных мероприятий у больных с аутоиммунными увеитами.
В настоящем обзоре мы ограничились рассмотрением вопросов, связанных с современными подходами и перспективными разработками в лечении самостоятельных или изолированных форм аутоиммунных увеитов, и не касались проблем терапии увеитов, развивающихся при системных аутоиммунных или инфекционных заболеваниях (саркоидоз, болезнь Бехчета и др.), а также увеитов при раковоассоциированной ретинопатии [Huober J. et al., 1997; Ohguro H. et al., 1997; Salgia R. et al., 1998]. Вместе с тем схемы иммуно– и генотерапии аутоиммунных заболеваний в концептуальном понимании имеют много общего, независимо от нозологической формы заболевания и локализации органа– или ткани–мишени, в связи с чем при дальнейшем изложении материала и анализе конкретной лечебной схемы мы можем использовать клинические модели, имеющие существенные отличия от классического аутоиммунного увеита [Dick A.D., 1998; Dick A.D., 2000; Zervos T. and Tsiaras W., 1999].
В первой части статьи будет рассмотрено лечение аутоиммунных увеитов препаратами широкого спектра действия, использующимися в офтальмологической практике в настоящее время. Во второй части предлагается ряд новых программ иммунотерапии увеитов, которые еще не получили широкого применения в клинике, однако в будущем могут стать альтернативой традиционным иммунофармакопрепаратам.
Иммунотерапия с использованием иммунофармакологических препаратов
широкого спектра действия
Среди различных направлений в лечении аутоиммунных увеитов, получивших в последнее время весьма активное развитие и исследования в рамках которых приобрели сегодня весьма интенсивный характер, традиционным является иммунотерапия с использованием иммунофармакологических препаратов широкого механизма действия, обладающих в организме больного масштабным спектром молекулярных и клеточных мишеней [Caspi R.R., 1999; Pleyer U. et al., 1999; Chan C.C. and Mochizuki M., 1999; Morgan J.P. et al., 2002].
Известно, однако, что такого рода терапия, особенно в лечении тяжелых или осложненных форм увеитов, течение которых имеет торпидный и весьма агрессивный характер, потенциально является очень токсичной (табл. 1). А с учетом того, что ключевая роль в патогенезе аутоиммунных увеитов принадлежит увеаретинальным аутоантителам и аутореактивным Т–клеткам соответствующей специфичности, осуществляющим в тандеме с аутоантителами контроль за прогрессированием аутоиммунного воспаления в области увеаретинального тракта, можно предположить, что одним из наиболее результативных путей в совершенствовании технологий лечения аутоиммунных увеитов может стать разработка средств и методов прицельной коррекции нарушений функции Т–звена иммунитета, в частности, его эффекторного крыла, где в качестве основного патогенетического инструмента фигурируют аутореактивные Т–лимфоциты [Becker M.D. et al., 2000; Dick A.D., 2000; Pleyer U. et al., 1999; Zhang X. et al., 2002].
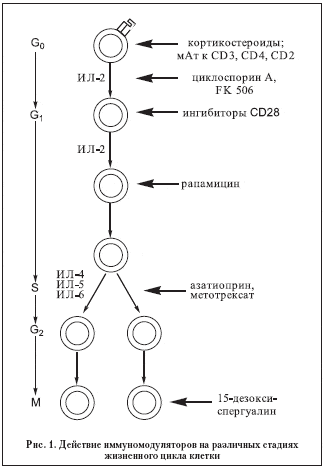
При разработке препаратов этой категории следует в обязательном порядке учитывать ключевые особенности жизненного цикла Т–лимфоцитов (рис. 1), в отношении которых возможна реализация иммуномодулирующих эффектов лекарственных средств рассматриваемой группы:
• подавление антигенспецифической активации лимфоцитов (кортикостероиды и моноклональные антитела к CD2, CD3 и CD4 маркерам субпопуляций лимфоцитов);
• подавление продукции цитокинов (циклоспорин А, FK 506);
• препятствие передачи трансдуцирующего сигнала (рапамицин);
• подавление интенсивности пролиферации лимфоцитов (азатиоприн, циклофосфамид, метотрексат) или процессов дифференцировки иммунокомпетентных клеток (15–дезоксиспергуалин).
Вышеуказанные лекарственные препараты могут действовать на различных стадиях клеточного цикла клеток, задействованных в реализации иммунного ответа при формировании и развитии аутоиммунного синдрома с эволюцией последнего в полномасштабную картину аутоиммунного заболевания, в данном случае, аутоиммунного увеита (рис. 1).
Особенности иммуномодулирующего действия традиционных фармакопрепаратов на лимфоциты
Кортикостероиды (КС)
Механизм действия КС. КС, образуя комплексы с цитоплазматическими рецепторами, достаточно легко проникают через наружную клеточную мембрану и после пенетрации клеточного ядра связываются с соответствующей регуляторной областью ДНК. Одним из важнейших итогов этого связывания является заметное снижение антиген–презентирующими клетками синтеза цитокинов, определяющих интенсивность секреции ИЛ–2, а следовательно, и масштаб подавления объема и набора Т–клеточных реакций [Pleyer U. et al., 1999].
Следует, однако, учитывать тот факт, что, помимо КС, высокой степенью гомологии к вышеуказанной регуляторной области ДНК обладают рецепторы других гормонов [Pleyer U. et al., 1999], способных провоцировать в процессе лечебного действия КС развитие ряда побочных эффектов, обусловленных перекрестной специфичностью между такими рецепторами и соответствующими гормонами.
Показания к использованию КС при лечении заболеваний глаз. Использование КС может иметь как локальный характер, так и системный, что следует учитывать при разработке комбинированных программ иммунотерапии аутоиммунных увеитов.
При местном использовании КС противовоспалительные свойства препаратов заметно доминируют над их потенциальным иммуносупрессивным ресурсом и соответствующими иммуносупрессивными фармакоэффектами. В этой связи формы КС, предназначенные для локального применения, могут быть использованы в лечении аутоиммунных воспалительных процессов, ограниченных передним отрезком увеаретинального тракта, в том числе в схемах лечения передних и промежуточных увеитов.
При системном использовании КС иммуносупрессивный эффект явно преобладает над противовоспалительным действием препарата и реализуется в достаточно полном объеме. В этом случае прямыми показаниями к системному применению КС служат поражения органа зрения и увеаретинального тракта, в частности, возникающие при системных аутоиммунных заболеваниях, а также те конкретные клинические ситуации, когда местное применение КС для коррекции аутоиммунного дисбаланса при увеитах не дает желаемого эффекта, что, например, характерно для системных ревматических процессов и других системных формах аутоиммунной патологии, а также в запущенных или осложненных случаях задних увеитов или панувеитов [Pleyer U. et al., 1999].
Циклоспорин А и такролимус (FK 506)
Механизм действия циклоспорина А и FK 506. Циклоспорин А и FK 506 являются иммунофармакологическими препаратами, которые оказывают супрессорное влияние на раннюю и предранние стадии активации Т–клеток [Zervos T and Tsiaras W., 1999].
Последние достижения в клинической иммунологии и иммунопатологии воспалительных заболеваний органа зрения и высокая информативность ряда экспериментальных моделей аутоиммунных увеитов сделали возможным и патогенетически обоснованным эффективное использование в комплексном лечении увеитов циклоспорина и FK 506.
В комплексе с соответствующими рецепторами указанные препараты подавляют активность кальцийнейрина, следствием чего является резкое падение уровня секреции ИЛ–2 – провоспалительного цитокина, играющего немаловажную роль в патогенезе аутоиммунного увеита [Pleyer U. et al., 1999; Rizzo L.V. et al., 1994; Rizzo L.V. and Caspi R.R., 1995; Silver P.B. et al., 2000; Foxman E.F. et al., 2002]. Важнейшим завершающим итогом этой цепи событий является угнетение клональной пролиферации аутореактивных к антигенам сетчатки и увеа Т–лимфоцитов, что ведет к торможению прогрессирования аутоиммунных нарушений и воспаления при увеите и, как следствие, – к положительной динамике клинико–иммунологических показателей и клинической картины аутоиммунного увеита в целом [Pleyer U. et al., 1999].
Показания к применению. Рассматривая использование циклоспорина А в клинической практике офтальмолога, необходимо учитывать тот факт, что доза, применяемая сегодня и достаточная для надежного и эффективного контроля течения и развития заболевания и аутоиммунного увеита, в частности, слишком токсична. Использование в лечебных схемах меньшей дозы, при которой побочные эффекты отсутствуют, напротив, не позволяет достигнуть желаемого лечебного эффекта, длительной и стабильной ремиссии [Becker M.D. et al., 2000]. По этой причине циклоспорин А, как фармакотерапевтический компонент в сложных лечебных программах, используется в комбинации с преднизолоном. Однако при этом ряд неблагоприятных эффектов циклоспорина А все же сохраняется. Вместе с тем не следует забывать о том, что лечение аутоиммунных увеитов циклоспорином А в дополнение к преднизолону позволяет не только заметно снизить темпы развития и прогрессирования заболевания в целом, но и свести с минимуму побочные эффекты, возникающие при использовании преднизолона (артериальная гипертония, токсическое воздействие на почки) [Pleyer U. et al., 1999; Lightman S., 1997].
FK 506 оказался весьма эффективен в комплексной терапии хронически–рецидивирующих задних увеитов, где он стал средством выбора в повседневной практике западного офтальмолога. Так, у пациентов, пролеченных FK 506, такие препараты, как преднизолон, циклоспорин А и колхицин, зачастую оказываются неэффективны [Ishioka M. et al., 1994].
Рапамицин
Рапамицин был получен в 1975 г. из гриба Streptomyces hydrosopicus, хотя широко использовать его в качестве иммуносупрессивного препарата специалисты начали лишь в начале 90–х гг. [Kahan B.D. et al., 1991].
Механизм фармакотерапевтического действия рапамицина заключается в эффекте подавлении активации Т–лимфоцитов путем предотвращения процессов трансдукции сигнала от ИЛ–2 на Т–клеточный рецептор (рис. 1).
Сходным с ним фармакоэффектом обладает лефлуномид, который блокирует секрецию сразу трех цитокинов – ИЛ–2, ИЛ–3 и ФНО–a, но не ИЛ–1. В то же время весьма выраженное токсическое действие указанного препарата на гемопоэтические клетки и на эмбриогенез в целом лишает возможности провести широкомасштабные клинические испытания эффектов лефлуномида [Zervos T. and Tsiaras W., 1999; Pleyer U. et al., 1999].
Бромокриптин
Многочисленными исследованиями показано, что в патогенезе некоторых аутоиммунных заболеваний (в том числе аутоиммунных увеитов) определенная роль принадлежит гормону передней доли гипофиза – пролактину. Следовательно, бромокриптин, являющийся антагонистом допамина, может иметь определенную терапевтическую ценность, как лечебный фармакопрепарат при лечении больных с аутоиммунными увеитами [Nagy E. et al., 1983]. Постулируемый на сегодня возможный механизм фармакотерапевтического действия бромокриптина заключается в подавлении синтеза пролактина и в модулирующем эффекте на периферические рецепторы дофамина [McMurray R.W., 2001].
Интересным оказался тот факт, что действие бромокриптина является синергичным с эффектами циклоспорина А; это позволяет при определенных обстоятельствах снижать дозу последнего, применяя в сложных комбинированных схемах иммунотерапии увеитов сочетание двух иммуносупрессантов – циклоспорина А и бромокриптина. В монотерапии аутоиммунных увеитов бромокриптин, как правило, используется редко. Подробный механизм действия этого препарата неизвестен, однако доказанным является тот факт, что на внешней клеточной мембране Т–лимфоцитов, играющих, как известно, ключевую роль в патогенезе аутоиммунных увеитов, имеются рецепторы к бромокриптину [Pleyer U. et al., 1999]. Это обстоятельство может послужить в дальнейшем основой для разработки на основе бромокриптина и его рецептора нового класса биотехнологических фармакоконструкций, позволяющих в ходе лечения аутоиммунных увеитов тонко регулировать эффекты индуцирующих сигналов в отношении аутореактивных Т–клеток.
Азатиоприн и метотрексат
Антиметаболиты и алкилирующие субстанции, применяемые в онкологической практике, также могут занять важное место в комбинированной терапии воспалительных процессов, протекающих с картиной аутоиммунного синдрома. Привыкание организма к этой группе препаратов развивается медленнее, чем к КС, что немаловажно для использования антиметаболитов и алкилирующих субстанций в длительных лечебных схемах [Pleyer U. et al., 1999].
Принцип действия вышеуказанных препаратов, обладающих цитотоксическими свойствами, заключается в подавлении синтеза геномной ДНК или РНК и, следовательно, торможении пролиферации и дифференцировки лимфоцитов. При этом на систему Т–лимфоцитов антиметаболиты и алкилирующие агенты действуют значительно эффективнее и стабильнее, чем на систему гуморального иммунитета [Pleyer U. et al., 1999].
Из алкилирующих субстанций подробнее всего изучен циклофосфамид, а наибольшее применение в широкой клинической практике, в том числе при лечении аутоиммунных увеитов, получили азатиоприн и метотрексат. Наиболее эффективным и безопасным для пациента является метотрексат; он с успехом используется для лечения тяжелых и осложненных форм хронических увеитов [Deschenes J., 2000].
Азатиоприн по сравнению с циклофосфамидом и в особенности преднизолоном как, представителем КС, обладает гораздо меньшим спектром побочных эффектов. Более того, азатиоприн в значительной степени и за гораздо меньшее время снижает интенсивность и площадь интраокулярного воспаления, способствуя тем самым сохранению остроты зрения [Flores M. et al., 2001].
Аллопуринол
Аллопуринол оказывает положительный лечебный эффект в комбинированной терапии увеитов. Принято считать, что наличие такого эффекта связано с иммуномодулирущими свойствами аллопуринола, а также с тем, что этот препарат уменьшает объем окислительных повреждений тканей путем инактивации свободных радикалов [Grus F.H. et al., 2001].
Кроме того, аллопуринол тормозит пролиферацию полиморфноядерных лейкоцитов, играющих немаловажную роль в индукции повреждения тканей глаза при аутоиммунных увеитах [Matuura G. et al., 1999]. В серии экспериментов доказано, что аллопуринол значительно уменьшает уровень липидных перекисей, а также тормозит миелопероксидазную активность.
Перечисленные эффекты аллопуринола сходны с фармакотерапевтическими эффектами КС (в частности, преднизолона), однако патоморфологическая картина пораженных тканей заметно меняется в позитивном направлении лишь при использовании аллопуринола [Augustin A.J. et al., 1999]. Более того, на экспериментальной модели аутоиммунного увеита у крыс линии Lewis показано, что в ходе проводимого лечения аллопуринол оказывает гораздо более сильный иммуномодулирующий эффект, чем КС [Grus F.H. et al., 2000].
Все эти данные позволяют считать, что аллопуринол может стать новым, альтернативным КС, препаратом выбора для использования в комплексных схемах лечения аутоиммунных увеитов.
FTY 720
Одним из иммуносупрессантов, полученных в последние годы, является FTY 720. Клиническими и патоморфологическими исследованиями доказано, что FTY 720 ослабляет тяжесть и интенсивность аутоиммунного увеита на экспериментальных моделях у крыс Lewis. Этот иммунофармакопрепарат снижает сывороточный уровень аутоантител к S–антигену и подавляет пролиферацию антиген–специфических аутореактивных Т–лимфоцитов. Результаты предварительных клинических исследований гласят, что FTY 720 может стать альтернативой традиционным иммуносупрессантам, широко применяемым сегодня, в частности, в офтальмологии [Kurose S. et al., 2000].
Микофенолат
Микофенолат – это иммуносупрессант, который с успехом используется при трансплантации органов и тканей, а также в лечении целого ряда аутоиммунных заболеваний (в том числе и аутоиммунных увеитов). Его преимуществом является гораздо меньшая частота побочных эффектов, чем у прочих иммуносупрессантов. Более того, у большинства пациентов, пролеченных микофенолатом, достигается продолжительная и стабильная ремиссия заболевания [Larkin G. and Lightman S., 1999; Zierhut M. et al., 2001].
a–МСГ (a–меланоцитстимулирующий гормон)
Ранее было показано, что a–МСГ подавляет продукцию ИФН–g активированными Т–эффекторами, а затем и то, что этот гормон опосредует индукцию продуцирующих ФНО–b Т–клеток, которые в этом случае могут действовать, как регуляторные Т–лимфоциты [Taylor A.W. et al., 2000]. Эти данные послужили толчком к дальнейшему исследованию способности a–МСГ подавлять воспалительный процесс, индуцированный и поддерживаемый аутореактивными Т–лимфоцитами или, иными словами, аутоиммунное воспаление, а также регулировать продукцию лимфокинов регуляторными и эффекторными Т–клетками.
Было установлено, что если экспериментальным мышам с индуцированным аутоиммунным увеитом на пике развития клинической картины увеоретинита инъецировать a–МСГ, тяжесть увеита значительно снижается. В присутствии a–МСГ эффекторные Т–клетки активируются, интенсивно пролиферируют и начинают продуцировать ИЛ–4 и ФНО–b, относящиеся к группе противовоспалительных цитокинов, тогда как как интенсивность секреции важнейших провоспалительных цитокинов – ИФН–g и ИЛ–10 – в это время падает [Taylor A.W. et al., 2000]. Накопленные к настоящему времени факты позволяют считать, что a–МСГ принимает участие в реализации местных эффектов иммуносупрессии и, возможно, в формировании зоны периферической толерантности. Отсюда следует, что a–МСГ может быть успешно использован как лечебный фармакопрепарат, способный подавлять уровень активности аутоиммунного воспаления при различных формах аутоиммунной патологии, в том числе при аутоиммунных увеитах, восстанавливая при этом утраченную толерантность к криптическим детерминантам аутоантигенов.
Как уже говорилось, подавляющее большинство используемых в настоящее время иммуносупрессантов являются токсичными. Так, дозы, которые позволяют достигать стойкой ремиссии, вызывают многочисленные побочные эффекты, тогда как меньшие по объему дозы, при использовании которых нежелательные эффекты сведены к минимуму, не позволяют адекватно контролировать течение заболевания. Исходя из этого, оптимальными следует считать иммуносупрессанты, сочетающие в себе наиболее выраженное противовоспалительное действие и минимальную опасность для пациента с точки зрения выраженности побочных эффектов. На практике, однако, это труднодостижимо, ибо часто используемые и наиболее эффективные иммуносупрессанты (например, КС, антиметаболиты) вызывают такой объем всевозможных побочных действий, который при определенных обстоятельствах может привести к гибели пациента. Реальным путем в этом направлении является, видимо, комбинация препаратов с различным механизмом иммуносупрессивного эффекта, которые действуют на разных этапах жизненного цикла Т–лимфоцитов, что ведет к нивелированию основных побочных действий указанных лечебных средств.

Литература
1. Augustin A.J., Loeffler K.U., Sekundo W., Grus F.H., Lutz J. «Effects of systemically applied allopurinol and prednisolone on experimental autoimmune uveitis.» Graefes. Arch. Clin. Exp. Ophthalmol. Vol. 237 (No. 6): 508–512, 1999.
2. Becker M.D., Adamus G., Davey M.D., Rosenbaum J.T. «The role of T–cells in autoimmune uveitis.» Ocul. Immunol. and Inflam. Vol. 8 (No 2): 93–100, 2000.
3. Caspi R.R. «Immune mechanisms of uveitis.» Springer Semin. Immunopathol. Vol. 21: 113–124, 1999.
4. Chan C.C., Li Q. «Immunopathology of uveitis.» Br. J. Ophthalmol. Vol. 82: 91–96, 1998.
5. Chan C.C., Mochizuki M. «Sympathetic ophthalmia: an autoimmune ocular inflammatory disease.» Springer Semin Immunopathol. Vol. 21: 125–134, 1999.
6. Deschenes J. «Therapeutics for future treatment of uveitis.» Bull. Soc. Belge Ophtalmol. Vol. 276: 7–11, 2000.
7. Dick A.D. «Immune mechanisms of uveitis: insights into disease pathogenesis and treatment.» Int. Ophthalmol. Clin. Vol. 40: 1–18, 2000.
8. Dick A.D. «Serological tests for monitoring and predicting disease severity, course and outcome of autoimmune intraocular inflammation.» Br. J. Ophthalmol. Vol. 82: 856–857, 1998.
9. Flores M., Gudino Perez R., Rios Prado R., Almedia Arvizu V.M., Castrejon Vazquez M.I., Ocampo A.A. «Comparative study of the treatment of autoimmune uveitis with prednisone and with cyclophosphamide and azathioprin.» Rev. Alerg. Mex. Vol. 48 (No. 3): 75–79, 2001.
10. Foxman E.F., Zhang M., Hurst S.D., Muchamuel T., Shen D., Wawrousek E.F., Chan C.C., Gery I. «Inflammatory mediators in uveitis: differential induction of cytokines and chemokines in Th1– versus Th2–mediated ocular inflammation.» J. Immunol. Vol. 168 (No. 5): 2483–2492, 2002.
11. Grus F.H., Augustin A.J., Loeffler K., Dick B., Lutz J., Pfeiffer N. «Allopurinol has immunomodulating activity following topical and systemic application in experimental autoimmune uveitis.» Eur. J. Ophthalmol. Vol. 11 (No. 3): 252–260, 2001.
12. Grus F.H., Augustin A.J., Sekundo W., Loeffler K. «Immunological effect of systemically administered allopurinol in experimental autoimmune uveitis.» Klin. Monatsbl. Augenheilkd. Vol. 216 (No. 3): 165–171, 2000.
13. Huober J., Holz F.G., Schmid H., Nolle B., Bellman C., Krastel H., Wallwiener D., Bastert G. «Paraneoplastic retinopathy in 2 patients with breast carcinoma.» Zentralbl. Gynakol. Vol. 119 (No. 3): 278–281, 1997.
14. Ishioka M., Ohno S., Nakamura S., Isobe K., Watanabe N., Tanaka S. «FK 506 treatment of non–infectious uveitis.» Am. J. Ophtalmol. Vol. 118: 723–729, 1994.
15. Kahan B.D., Chang J.Y., Seghal S.N. «Preclinical evaluation of a new potent immunosupressive agent, rapamycin.» Transplantation Vol. : 185–191, 1991.
16. Kurose S., Ikeda E., Tokiwa M., Hikita N., Mochizuki M. «Effects of FTY 720, a novel immunosuppressant, on experimental autoimmune uveoretinitis in rats.» Exp. Eye Res. Vol. 70 (No. 1): 7–15, 2000.
17. Larkin G., Lightman S.L. «Mycophenolate motefil: a useful immunosupressive in inflammatory eye disease.» Ophthalmology Vol. 106: 370–375, 1999.
18. Lightman S.L. «New therapeutic options in uveitis.» Eye Vol. 11: 222–226, 1997.
19. Matuura G., Goto H., Kezuka T., Yamakawa N., Usui M. «Suppression of experimental autoimmune uveoretinitis with a combination of cyclosporin and allopurinol.» Nippon Ganka Gakkai Zasshi Vol. 103 (No. 1): 26–33, 1999.
20. McMurray R.W. «Bromocriptine in rheumatic and autoimmune diseases.» Semin. Arthritis Rheum. Vol. 31 (No. 1): 21–32, 2001.
21. Morgan J.P., Robins R.A., Dua H.S., Tighe P.J. « S antigen specific effector T cell activation detected by cytokine flow cytometry.» Br. J. Ophthalmol. Vol. 86 (No. 5): 517–520, 2002.
22. Nagy E., Berczi I., Wren G.E., Asa S.L., Kovacs K. «Immunomodulation by bromocriptine.» Immunopharmacology Vol. 6: 231–243, 1983.
23. Ohguro H., Takaya T., Ogawa K., Suzuki J., Nakagawa T. «Cancer–associated retinopathy.» Nippon Ganka Gakkai Zasshi Vol. 101 (No. 4): 283–287, 1997.
24. Pleyer U., Liekfeld A., Baatz H., Hartmann C. «Pharmakologische Modulation immunmediierter Erkrankungen des Auges.» Klin. Monatsbl. Augenheilk. Vol. 214: 160–170, 1999.
25. Rizzo L.V., Caspi R.R. «Immunotolerance and prevention of ocular autoimmune disease.» Current Eye Res. Vol. 14: 857–864, 1995.
26. Rizzo L.V., Miller–Rivero N.E., Chan C.C., Wiggert B., Nussenblatt R.B., Caspi R.R. «Interleukin–2 treatment potentiates induction of oral tolerance in a murine model of autoimmunity.» J. Clin. Invest. Vol. 94 (No. 4): 1668–1672, 1994.
27. Salgia R., Hedges T.R., Rizk M., Reimer R.H., Skarin A.T. «Cancer–associated retinopathy in a patient with non–small–cell lung carcinoma.» Lung cancer Vol. 22 (No. 2): 149–152, 1998.
28. Streilein J.W. «Ocular immune privilege – protection that preserves sight!» Karger Gazette «The Eye in Focus» No 64: 5–8, 2001.
29. Taylor A.W., Yee D.G., Nishida T., Namba K. «Neuropeptide regulation of immunity. The immunosuppressive activity of alpha–melanocyte–stimulating hormone (alpha–MSH).» Ann. N. Y. Acad. Sci. Vol. 917: 239–247, 2000.
30. Zervos T., Tsiaras W. «Systemic autoimmune diseases and their effect on the eye.» Med. Health R. I. Vol. 82: 53–57, 1999.
31. Zhang X., Jiang S., Manczak M., Sugden B., Adamus G. «Phenotypes of T cells infiltrating the eyes in autoimmune anterior uveitis associated with EAE.» Invest. Ophthalmol. Vis. Sci. Vol. 43 (No. 5): 1499–1508, 2002.
32. Zierhut M., Schlote T., Tomida J., Stiemer R. «Immunology of uveitis and ocular allergy.» Acta Ophthalmol. Scand. Vol. 78: 22–25, 2000.
33. Zierhut M., Stubiger N., Aboalchamat W., Landenberger H., Bialasiewicz A.A., Engelmann K. «Immunosuppressive therapy with mycophenolate mofetil (CellCept) in treatment of uveitis.» Ophthalmologe Vol. 98 (No. 7): 647–651, 2001.












