Методы: проанализированы 30 историй болезни пациентов СОКОБ им. Т.И. Ерошевского в 2012–2013 гг. с патологией роговицы, которым была произведена повторная кератопластика в связи с отторжением или мутным приживлением донорского трансплантата после хирургического лечения гнойной язвы роговицы (23 пациента), герпетического кератоувеита (4 пациента), вторичной ЭЭД (3 пациента).
В послеоперационном периоде всем пациентам общепринятая схема лечения дополнялась местным применением дважды в день препарата Рестасис (глазные капли 0,05% циклоспорина 0,4 мл).
Результаты и заключение: большая вероятность получения предметного зрения после рекератопластики возможна при выполнении хирургического вмешательства не ранее чем через 12 и более месяцев. Включение в схему лечения больных данной группы иммуносупрессора позволяет получить у большей части пациентов (80% случаев) прозрачное приживление и предметное зрение.
Ключевые слова: циклоспорин, Рестасис, кератопластика, роговичный трансплантат.
Abstract
Possibilities of local immunosuppression in repeated
keratoplasty
Milyudin E.S., Zolotarev A.V., Milyudin A.E.
Scientific Research Institute of Eye Diseases of Samara State Medical University
Samara Clinical Ophthalmologic hospital named after Eroshevskii T.I., Samara
Purpose: to study possibilities of usage of cyclosporine 0.005% eye drops in complex treatment of patients after repeated keratoplasty.
Methods: 30 case histories of patients with corneal pathology operated on in 2012- 2013 because of graft rejection or opaque engraftment after surgical treatment of corneal purulent ulcer, herpetic keratouveitis or secondary epithelial dystrophy were analyzed. In a postoperative period all patients were treated with additional instillations of Restasis eye drops (cyclosporine 0.005%).
Results and conclusion: restoring of central vision after the repeated keratoplasty has a bigger probability if the surgery is performed not earlier than in 12 months. Immunosupressive thereapy results in the engraftment with corneal transparency and restoring the central vision in 80% of patients.
Key words: cyclosporin, Restasis, keratoplasty, corneal graft.
Актуальность
Пересадка роговицы во многих случаях и по разным причинам может закончиться формированием бельма. Прежде всего это может произойти в результате кератопластики, выполненной у больных с выраженным воспалительным синдромом. Операция у данной группы больных позволяет надеяться лишь на восстановление фиброзной оболочки глаза (Elliot J.H., 1971) и не более чем в 50% случаев – на какой-либо функциональный результат (Слонимский А.Ю., 2010). Следовательно, через определенный период времени будет необходимо оперировать данного пациента в плановом порядке.
Повторная кератопластика может быть проведена также и по экстренным показаниям, когда вследствие развившегося иммунного конфликта либо активно продолжающегося бактериального процесса происходит первичное отторжение донорского трансплантата.
Наименее часто выполняются повторные кератопластики после операции по оптическим показаниям, т. к. помутнение трансплантата в послеоперационном периоде в данной группе пациентов происходит лишь в 5–10% случаев (Thiell M.A., 2003).
Любое повторное хирургическое вмешательство, особенно повторное использование донорских тканевых материалов, значительно утяжеляет послеоперационное течение, увеличивает риск развития послеоперационных осложнений, частота которых достигает 25,1–32,1%, что приводит к ухудшению функциональных результатов операций (Труфакина М.В., 1999). У больных, которым предстоит выполнить повторную кератопластику, наибольшую опасность представляет вероятность развития иммунологического конфликта после операции. В большинстве случаев результатами будут помутнение или отторжение роговичного трансплантата, развитие вторичной глаукомы либо рецидив первичного основного заболевания роговицы (Pleyer U., Bertelmann E., 2005). Традиционное в послеоперационном периоде медикаментозное лечение антибактериальными, стероидными и нестероидными противовоспалительными препаратами, стимуляторами регенерации и заменителями слезной жидкости, направленное на приживление донорского трансплантата при повторных операциях, недостаточно эффективно у данной группы пациентов.
Наличие системного иммунологического дисбаланса, характерного для больных с высоким риском отторжения трансплантата при кератопластике, предполагает применение цитостатиков (циклофосфамид, 6-меркаптопурин, азатиоприн, 5-фторурацил). Однако серьезные побочные эффекты, вызываемые ими (нарушение гемопоэза и регенерации тканей, угнетение всех форм иммунного ответа), значительно ограничивают их применение (Warrington J.S., Shaw L.M., 2005).
Препаратом выбора в офтальмологии стал селективный иммуносупрессивный препарат – циклоспорин А, механизм действия которого обусловлен торможением экспрессии цитокинов, активаторов отторжения, в т. ч. IL-2 и IFN-γ. В отличие от стероидов циклоспорин А не только уменьшает высвобождение IL-2, но и блокирует связывание его с рецепторами на клеточной мембране, в результате чего блокируется активация Т- и В-лимфоцитов и подавляются клеточные иммунные реакции. В отличие от цитостатиков циклоспорин А не угнетает гемопоэз и не влияет на функции фагоцитов, не нарушает противоинфекционный иммунитет (Балаян Т.Г., 2008). Комбинированное применение малых доз цитостатиков с кортикостероидом возможно даже у пациентов детского возраста. Системное применение метипреда и циклоспорина в малых дозах не предотвращает у детей развитие реакции отторжения, но существенно уменьшает ее частоту – с 87,5% случаев в контрольной группе до 45% – в опытной группе (Плескова А.В., 2008).
Несомненно, наиболее эффективным представляется местное сочетанное применение циклоспорина А и глюкокортикоидов, которое более чем в 2 раза увеличивает вероятность прозрачного приживления роговичного трансплантата по сравнению с местным применением только глюкокортикоидов (M.O. Price и F.W. Price, 2003).
В России с сентября 2011 г. стал доступен препарат Рестасис (глазные капли 0,05% циклоспорина 0,4 мл). В связи с этим нами в данной работе была поставлена цель: изучить возможность применения 0,05% циклоспорина в виде глазных капель у больных после повторной кератопластики в составе комплексной терапии.
Методы
Проанализированы 30 историй болезни пациентов СОКОБ им. Т.И. Ерошевского с патологией роговицы, которым в 2012–2013 гг. была проведена повторная кератопластика: в связи с отторжением или мутным приживлением донорского трансплантата после хирургического лечения гнойной язвы роговицы (23 пациента), герпетического кератоувеита (4 пациента), вторичной ЭЭД (3 пациента). В зависимости от сроков выполнения повторной кератопластики больные были разделены на 4 группы (табл. 1).
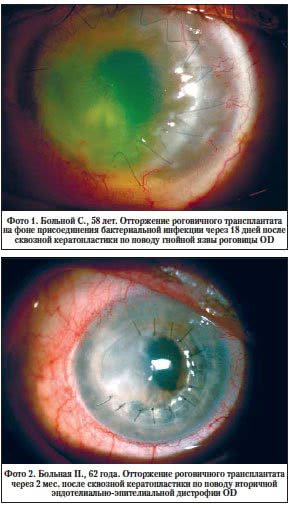
Основными причинами повторной операции в 1-й группе были лизис роговичного трансплантата (фото 1) и резко выраженная активность инфекционного процесса. Во 2-й группе основной причиной реоперации была несостоятельность трансплантата без выраженных инфекционных осложнений (фото 2). В 3-й и 4-й группах главными причинами ретрансплантации роговичного диска являлись помутнение роговичного трансплантата, отсутствие предметного зрения (фото 3).
Пациенты 1-й и 2-й групп перед операцией получали как местно, так и парентерально антибиотики, кортикостероиды и нестероидные противовоспалительные препараты. Больным 3-й и 4-й групп предоперационное лечение не проводилось.
В послеоперационном периоде у всех пациентов общепринятая схема лечения дополнялась местным применением 2 р./сут препарата Рестасис (глазные капли 0,05% циклоспорина 0,4 мл).
Результаты и обсуждение
Особенностью повторной кератопластики у больных 1–й и 2-й групп была необходимость безотлагательного выполнения операции. В 3-й и 4-й группах повторная трансплантация роговицы выполнялась в плановом порядке. В зависимости от сроков выполнения повторной кератопластики мы придерживались следующих правил выбора диаметра трепанов. В ранние сроки – до 6 мес. после первой кератопластики использовался больший – на 0,5–1,5 мм – трепан, в сроки от 6 мес. до 1 года пораженная роговица иссекалась в пределах границ старого трансплантата. Иссечение патологически измененной роговицы трепаном у больных 1-й и 2-й групп осложнялось гипотонией, наличием вновь образованных сосудов, неравномерной толщиной трансплантата и его сращением с подлежащими тканями. В каждом случае выполнялся большой объем реконструктивных мероприятий, который включал в себя разделение передних, гонио- и задних синехий, удаление ретрокорнеальных и зрачковых пленок, в 3-х случаях – экстракцию набухающей катаракты с имплантацией ИОЛ и ее фиксацией узловыми швами к радужке.
В более поздние сроки границы удаления бельма определялись индивидуально для каждого больного в зависимости от наличия и выраженности тех или иных факторов, осложняющих выполнение операции. У больных 3-й и 4-й групп наиболее часто встречающимся фактором, осложняющим выполнение повторной кератопластики, являлось наличие вновь образованных сосудов.
Во всех 4-х группах оперированных повторно у 27 пациентов (90%) одинаково часто выявлены заращение зрачка и прорастание сосудов в ткань роговицы. Ретрокорнеальные мембраны и синехии угла передней камеры встречались реже и в более тяжелых случаях – у 17 (55%) и 21 (70%) соответственно.
У пациентов, не входящих в группу высокого риска отторжения кератотрансплантата, при отсутствии признаков системного иммунологического дисбаланса характер приживления кератотрансплантата в 70–80% случаев находится в прямой зависимости от послеоперационной динамики показателей иммунитета. При лечении в таких случаях общепринято ограничиваться местным применением глюкокортикоидов. Между тем локальная стероидная терапия оказывается явно недостаточной при наличии осложняющих выполнение операции факторов и системного иммунологического дисбаланса, характерного для больных с высоким риском отторжения трансплантата.
В связи с этим у наших пациентов схема послеоперационного лечения дополнялась иммуносупрессивным препаратом – глазными каплями 0,05% циклоспорина. Закапывание препарата проводилось 2 р./сут с 1-го до 30-го дня послеоперационного периода. У 1 пациента возникли неприятные ощущения в виде жжения и покраснения глаза, в связи с чем препарат был отменен. Послеоперационный период у больных, получавших 0,05% циклоспорин, протекал спокойно, эпителизация роговичного трансплантата у большей части оперированных больных заканчивалась в обычные сроки – на 3–5-е сут послеоперационного периода. Купирование воспалительных явлений в 1-й и 2–й группах достигалось к 10–15 сут послеоперационного периода, в 3-й и 4-й группах – к 7–8 сут.
В 2-х случаях (у ВИЧ-инфицированных пациентов, оба – из 1-й группы, причиной сквозной кератопластики у них была гнойная язва роговицы) к 7–10 сут послеоперационного периода наблюдалась картина первичного отторжения роговичного трансплантата.
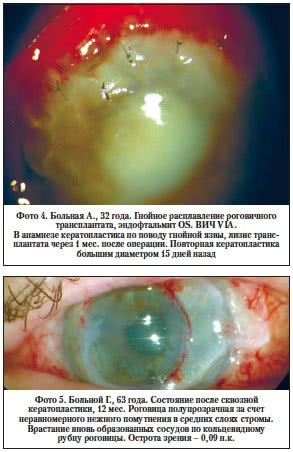
Также на фоне закапывания 0,05% циклоспорина отторжение донорского трансплантата с расширением зоны лизиса на склеру произошло у 2-х пациентов 2-й группы, которым повторная кератопластика была выполнена по поводу несостоятельности роговичного трансплантата после хирургического лечения гнойной язвы. Всем пациентам с лизисом роговичного трансплантата проведена лечебная кератопластика. Однако у ВИЧ-инфицированных больных в обоих случаях, несмотря на отмену 0,05% циклоспорина, повторно развились лизис роговичного трансплантата и эндофтальмит (фото 4). В дальнейшем обоим больным была выполнена энуклеация.
Следовательно, повторная кератопластика при расплавлении донорского трансплантата в сроки до 30 сут после предыдущей кератопластики является малоперспективной с целью сохранения анатомической целостности глазного яблока и абсолютно неперспективной с целью получения предметного зрения, несмотря на усиление иммуносупрессивной терапии 0,05% раствором циклоспорина.
Вероятность сохранения целостности глазного яблока у больных, которым выполнялась повторная кератопластика не ранее чем через 2–6 мес., увеличивается при местном применении 0,05% циклоспорина до 77%. В данной группе пациентов не наблюдалось ни одного случая приживления роговичного трансплантата с сохранением его прозрачности, и, соответственно, ни у одного пациента не было получено предметное зрение.
Местное применение циклоспорина у больных в 3-й группе, которым была выполнена рекератопластика по истечении 6–12 мес., позволило полностью исключить вероятность отторжения и лизиса роговичного трансплантата, но в 14% случаев получено мутное и в 43% случаев – полупрозрачное приживление и, соответственно, только у 3 (43%) больных из 7 получено предметное зрение (фото 5).
Большая вероятность получения предметного зрения после рекератопластики возможна при выполнении хирургического вмешательства не ранее чем через 12 мес. и более. Включение в схему лечения больных данной группы иммуносупрессора позволяет получить у большей части пациентов (80% случаев) прозрачное приживление и предметное зрение (фото 6).
Выводы
По результатам нашего исследования можно утверждать, что местное применение циклоспорина 0,05% в виде глазных капель обоснованно и может в большинстве случаев повысить эффективность хирургического лечения больных при повторной кератопластике.




Литература.
1. Балаян Т.Г. Дифференцированная тактика иммуносупрессивного лечения при кератопластике высокого риска: Автореф. дис. … канд. мед. наук. М., 2008. 26 с.
2. Плескова А.В. Сквозная кератопластика при помутнениях роговицы у детей: субъективные, объективные и информационные основания // Российская педиатрическая офтальмология. 2009. № 2. С. 55–56.
3. Слонимский А.Ю., Слонимский Ю.Б., Долгий С.С. Сквозная пересадка роговицы при гнойных процессах переднего отрезка глазного яблока // Клиническая офтальмология. 2010. № 1. С. 11–14.
4. Труфакина М.В. Иммунопатогенетические механизмы повторной хирургической травмы глаза: Автореф. дисс. ... канд. мед. наук. Новосибирск, 1999. 24 с.
5. Elliot J.H. Immune factors in corneal graft rejection // Invest. Ophthal. 1971. Vol. 10. Р. 216–234.
6. Hirst L.W., Quigley H.A., Stark W.J. Specular microscopy of iridocorneal endothelial syndrome // Am J Ophthalmol. 1980. Vol. 89. Р. 11–21.
7. Li X. Q., Schlickeiser S., Pleyer U. Current Aspects of the Immunobiology and Prevention of Corneal Graft Rejection: What Have We Learned from 100 Years of Keratoplasty? 2007.
8. Pleyer U., Bertelmann E. Differential diagnosis and therapy of graft rejection after keratoplasty // Klin. Monatsbl. Augenheilkd. 2005. Vol. 222. № 11. Р. 863–869.
9. Thiell M.A., Coster D.J., Williams K.A. The potential of antibody-based immunosuppressive agents for corneal transplantation // Immunology and Cell Biology. 2003. Vol. 81. Р. 93–105.








.gif)



