Department of Ophthalmology of Medical Faculty
GOU VPO Russian State Medical University of Roszdrav, Moscow
Literary review is devoted to age–related macular degeneration, questions of its pathogenesis,diagnostics and treatment.
Возрастная макулярная дегенерация (ВМД) характеризуется необратимым прогрессирующим поражением центральной фотоактивной зоны сетчатки и является одной из нозологических форм, наиболее часто вызывающих потерю зрения среди населения развитых стран мира [1]. В России заболеваемость ВМД составляет более 15 на 1000 населения [2]. В структуре первичной инвалидности по ВМД больные в трудоспособном возрасте составляют 21%, а в пенсионном возрасте – 32% [3].
Частота ВМД растет параллельно с увеличением возраста больных. Так, в возрастной группе от 52 до 64 лет она составляет 1,6%, от 65 до 74 лет – 15%, от 75 до 84 лет – 25%, а среди лиц старше 85 лет – 30%. По данным ВОЗ, доля населения старшей возрастной группы в экономически развитых странах составляет около 20%, а к 2050 г. возрастет, вероятно, до 33% [2]. Соответственно, в связи с ожидаемым увеличением продолжительности жизни, неуклонным ростом атеросклероза и сопутствующей патологии проблема ВМД остается наиболее актуальной. К тому же в последние годы наметилась отчетливая тенденция к «омоложению» данного заболевания [4]. Социально–медицинская значимость этой патологии обусловлена быстрой потерей центрального зрения и утратой общей работоспособности. Степень тяжести процесса и потери центрального зрения зависит от формы ВМД и близости процесса к центральной ямке сетчатки. Замечено, что парный глаз поражается не позднее, чем через 5 лет после заболевания первого [5].
Этиопатогенез
Несмотря на многочисленные исследования, посвященные ВМД, этиопатогенез этого заболевания остается до настоящего времени окончательно не выясненным. ВМД относится к многофакторным заболеваниям. Прежде всего это инволюционный процесс, о чем свидетельствует прямая зависимость частоты возникновения заболевания от возраста.
Выявлению факторов риска развития данного заболевания было посвящено много различных работ. Полученные результаты позволяют утверждать, что курение, помимо возраста и этнического происхождения, является единственным фактором риска, значимость которого подтверждалась во всех исследованиях. Прекращение курения может снижать риск развития ВМД.
В настоящее время интенсивно изучается роль наследственных факторов в возникновении этого заболевания. Многие исследователи указывают на аутосомно–доминантный тип наследования данной патологии [8]. Возникновение ВМД связывают с мутациями в генах ARMD1 [1q25–q31], FBLN6 [1q24–q25], ARMD3 [14q32.1] [2]. По мнению J.D. Gass, семейный анамнез является важным фактором риска у 20% больных ВМД. Установлено трехкратное возрастание риска развития ВМД, если заболевание встречается у родственников в первом поколении [10].
Существенная роль в развитии ВМД отводится сердечно–сосудистым заболеваниям. E.F. Cherney (2001) отмечает, что при атеросклерозе риск поражения макулярной области возрастает в 3 раза, а при наличии гипертонической болезни – в 7 раз [6]. Атеросклеротические бляшки общей сонной артерии увеличивают риск развития ВМД в 2,5 раза, бляшки в области бифуркации сонных артерий – в 4,7 раза [8]. Кроме того, установлено снижение регионального кровоснабжения у большей части больных ВМД. Так, по данным Г.Д. Михайловой (1986), снижение линейной скорости кровотока в глазничной артерии у больных ВМД отмечается в 78,7% случаев. Т.В. Мельникова (1998) в своих исследованиях c использованием метода импульс¬но–волновой допплерографии выявила значительное снижение объемной скорости кровотока в системе задних коротких цилиарных артерий. Отмечена тенденция к снижению гемодинамических показателей по мере прогрессирования дистрофического процесса [9].
В ряде исследований была установлена связь между уровнем потребления жиров с пищей и развитием поздней стадии ВМД. Риск ВМД выше у людей, которые употребляют в пищу больше насыщенных жиров и холестерина, а также при повышенном индексе массы тела, и ниже у тех, в чьем пищевом рационе имеется достаточное количество омега–3 длинноцепочечных полиненасыщенных жирных кислот (они содержатся в рыбе).
В разных исследованиях рассматривались и другие факторы, включая гормональный статус, экспозицию воздействия солнечных лучей, употребление алкоголя.
В последнее время существенную роль в патогенезе ВМД отводят окислительному стрессу, заключающемуся в повреждении тканей глаза вследствие дисбаланса в системе образования свободных радикалов и антиоксидантной защиты. Токсическое действие свободных радикалов реализуется через повреждение липидов мембраны, поверхностных протеинов и трансмембранных гликопротеидов. Увеличение энергии фотосенсибилизатора приводит к образованию синглетного кислорода, способного разрушать мембраны клетки и другие ее структуры. Фототоксичной для сетчатки является коротковолновая часть спектра видимого света, инфракрасные и ультрафиолетовые лучи [11]. Чувствительность сетчатки к продуктам окислительного стресса и свободным радикалам определяется тремя основными факторами: во–первых, сетчатка постоянно подвергается сочетанному воздействию света и кислорода, что создает идеальные условия для синтеза свободных радикалов; во–вторых, она содержит в большом количестве полиненасыщенные жирные кислоты, которые наиболее чувствительны к окислению; в–третьих, сетчатка, как производное нервной ткани, особенно чувствительна к гипоксии [12].
Защита сетчатки от фотоповреждения обеспечивается за счет постоянного обновления светочувствительного наружного сегмента фоторецепторной клетки, системы антиоксидантной защиты и светофильтрующей системы глаза (роговица, хрусталик, макулярный пигмент, меланин). Ослабление или нарушение любого из звеньев этой тонко сбалансированной защитной системы ведет к дистрофическим изменениям в сетчатке.
Классификация ВМД
Классификация ВМД строится в основном на этапах развития дистрофического процесса. Кацнельсон Л.А. с соавт. различают 3 формы заболевания [13]:
1. Неэкссудативная (сухая) форма: ретинальные друзы, дефекты пигментного эпителия, перераспределение пигмента, атрофия пигментного эпителия и хориокапиллярного слоя.
2. Экссудативная (влажная) форма: стадия экссудативной отслойки пигментного эпителия; стадия экссудативной отслойки нейроэпителия; неоваскулярная стадия; стадия экссудативно–геморрагической отслойки пигментного эпителия и нейроэпителия.
3. Рубцовая стадия.
Другие авторы предлагают выделять раннюю и позднюю стадию ВМД [14]. В ранней стадии отмечаются фокальные друзы и неравномерность пигментации РПЭ. Для поздней стадии характерны отслойка и разрыв РПЭ, хориоидальная неоваскуляризация (ХНВ), дисковидный (фиброваскулярный) рубец, географическая атрофия РПЭ.
Американская академия офтальмологии рекомендует классификацию, разработанную в ходе исследования возрастной глазной патологии (Age–Related Eye Disease Study – AREDS) [15]:
Отсутствие ВМД (категория 1 AREDS) – отсутствие или небольшое количество твердых друз (диаметр <63 микрон).
Ранняя стадия ВМД (категория 2 AREDS) – множественные твердые друзы, небольшое число мягких друз (диаметр от 63 до 124 микрон) или изменения РПЭ. В исследовании AREDS у пациентов с данной стадией 5–летний риск развития поздней стадии ВМД любого глаза составлял 1,3%.
Промежуточная стадия ВМД (категория 3 AREDS) – множество мягких друз, по крайней мере, одна сливная друза (диаметр ³ 125 микрон) или географическая атрофия, не затрагивающая центральной ямки. 5–летний риск развития поздней стадии ВМД составляет примерно 18%, причем для пациентов с наличием сливной друзы на одном глазу риск равен 6,3%, а при аналогичном поражении обоих глаз – 26%.
Поздняя стадия ВМД (категория 4 AREDS) характеризуется одним или несколькими из следующих признаков (при отсутствии других причин):
• географическая атрофия РПЭ и хориокапиллярного слоя в области центральной ямки сетчатки;
• неоваскулярная макулопатия: ХНВ, серозная и/или геморрагическая отслойка нейроэпителия или РПЭ, липидные отложения, субретинальная и субпигментная неоваскуляризация, образование дисковидного рубца.
Подсчитано, что в течение 5 лет приблизительно в 22% парных (лучших) глаз у пациентов с поздней стадией ВМД могут появиться неоваскулярные изменения или географическая атрофия в области центральной ямки [15].
Диагностика ВМД
Диагностика ВМД базируется на данных анамнеза, жалобах пациента, оценке зрительных функций и данных офтальмоскопии (предпочтительнее стереоскопическая биомикроскопия).
В настоящее время одним из самых информативных методов при выявлении патологии сетчатки признана флюоресцентная ангиография глазного дна (ФАГД). Для проведения ФАГД применяют различные модели фотокамер и флюоресцеин, молекула которого имеет небольшой размер и низкую молекулярную массу, что позволяет ей легко проникать через большинство биологических мембран путем диффузии [13]. Однако при планировании ФАГД необходимо учесть все возможные риски, связанные с этой процедурой. Могут возникнуть тяжелые медицинские осложнения, вплоть до летального исхода (1 случай на 200 000 пациентов).
При проведении ангиографии обычно делают стереоскопические цветные снимки глазного дна, так как они помогают исследовать центральные отделы глазного дна и серозные отслойки нейроэпителия и РПЭ, а также определить причину блокированной флюоресценции или экстравазации из неизвестного источника в поздней фазе ангиографии. Стереоскопические снимки также могут быть использованы как исходные для динамического наблюдения за рядом пациентов с выраженной сухой фомой ВМД и за пациентами в процессе лечения.
Ангиография с индоцианин зеленым приобрела популярность после внедрения цифровых фундус–камер. Индоцианин зеленый имеет пики абсорбции вблизи красного спектра. Большие длины волн лучше проникают в РПЭ или в субретинально расположенную кровь, или серозную жидкость. Поэтому сосуды хориоидеи лучше видны с индоцианин зеленым, чем с флюоресцеином. Кроме того, в отличие от флюоресцеина, индоцианин зеленый практически полностью связывается с белками и поэтому не дает пропотевания из нормальных сосудов хориоидеи и ХНВ. Ангиография с индоцианин зеленым удобна для выявления субретинальной неоваскуляризации при наличии отслойки РПЭ, непрозрачной субретинальной жидкости или геморрагии [2]. К сожалению, индоцианин зеленый в нашей стране не разрешен для медицинского применения.
Для оценки топографии и морфологии макулы применяют OCT (оптическая когерентная томография), что позволяет выявлять структурные изменения на самых ранних стадиях дегенерации сетчатки. Основным достоинством томографов является возможность дифференцировать оптическую структуру сетчатки, выявить недоступные при офтальмоскопии утолщения сетчатки, интраретинальные патологические процессы, а также помощь в оценке реакции сетчатки и РПЭ на лечение.
Большое распространение в диагностике макулярной патологии получили электрофизиологические методы исследования. Изменения ритмичной ЭРГ наиболее выражены при отечных формах заболевания. На ранних стадиях отмечается снижение амплитуды и увеличение латентности при макулярной ЭРГ [16, 22].
Медикаментозное лечение сухой формы ВМД
Несмотря на огромные успехи в усовершенствовании методов диагностики ВМД, ее лечение остается достаточно сложной проблемой. В терапии сухих форм ВМД и при высоком риске развития заболевания с целью нормализации обменных процессов в сетчатке рекомендуют проводить курсы антиоксидантной терапии.
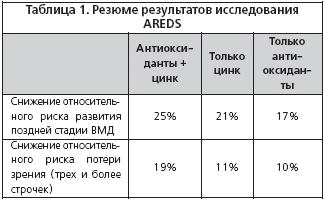
По данным исследования AREDS, полезный эффект от приема антиоксидантов был достигнут у тех участников, у которых была промежуточная или поздняя стадия ВМД хотя бы на одном глазу. Комбинированная терапия антиоксидантами, цинком и медью за 5 лет снизила частоту развития поздней стадии ВМД на 25%, а риск потери остроты зрения на 3 и более строчек на 19% (табл. 1) [15].
Среди соединений, способных защитить сетчатку от окислительного стресса и развития ВМД, особую роль в последнее время отводят каротиноидам. Около 50 каротиноидов обнаружены в желто–оранжевых фруктах и темно–зеленых овощах. Человек не способен синтезировать каротиноиды, поэтому их поступление в организм напрямую связано с питанием.
Плазма человека в значительных количествах содержит 6 каротиноидов: a– и b–каротин (из моркови), b–криптоксантин (из цитрусов), ликопин (из томатов), лютеин (из шпината) и зеаксантин (из кукурузы). Только лютеин и зеаксантин транспортируются в сетчатку, где они формируют желтый макулярный пигмент или макулярный ксантофилл [17, 18].
По данным гистологического исследования, макулярные пигменты расположены в слое волокон Генле или аксонов фоторецепторов. В результате свет, прежде чем попадает на светочувствительный наружный сегмент фоторецепторов, сначала проходит через желтый пигмент. Таким образом, макулярный пигмент осуществляет функцию внутриглазного и пререцепторного ультрафиолетового фильтра. Лютеин и зеаксантин располагаются не только перед фоторецепторами в качестве пассивного оптического фильтра. Они обнаружены, хотя и в меньших концентрациях, в наружном сегменте фоторецепторов [17].
В настоящее время в РФ зарегистрированы витаминно–минеральные комплексы, содержащие каротиноиды, экстракт черники, микроэлементы, предназначенные для профилактической и заместительной терапии при сухой форме ВМД.
Каротиноиды. В адекватных дозах они дополнительно снижают риск возникновения катаракты. Ликопин, который усиливает действие лютеина, также защищает сетчатку и является хорошим средством профилактики возрастной макулодистрофии. Как показали многочисленные исследования, подобный эффект при данной патологии оказывают витамины А, С и Е, b–каротин и цинк.
Также следует остановиться на антоцианах. Они содержатся в экстракте плодов черники, которая давно известна своим благотворным влиянием на зрение и издавна использовалась с этой целью в народной медицине. Лишь в 80–е годы прошлого века было установлено, что основными действующими на зрение веществами черники являются антоцианозиды, обладающие выраженным антиоксидантным и ангиопротективным действием. Они способствуют улучшению реологических свойств крови, снижая тонус сосудистой стенки и уменьшая тромбообразование, а также укрепляют стенку кровеносных сосудов за счет способности этих веществ влиять на регуляцию биосинтеза коллагена.
Важно, чтобы все эти компоненты содержались в витаминно–минеральном комплексе в рациональном соотношении. Так, лютеина должно быть минимум 2 мг, так как суточная доза для профилактики ВМД в группе риска – не менее 6,0 мг (рекомендация российского Экспертного совета по ВМД, 2009). Эффективность усвоения и действия повышают ликопин и b–каротин. Содержание антоцианов должно быть выше 10 мг. Важно получение достаточного количества микроэлементов, в первую очередь таких, как цинк – более 10 мг в день, медь – не менее 1 мг. Полезную роль играют такие витамины, как А, В, С, и Е.
Следует помнить, что заместительная терапия для профилактики и лечения сухой формы ВМД не может быть курсовой, ее использование возможно только на постоянной основе. Она должна применяться у лиц старше 50 лет, а при наличии факторов риска (курение, избыточный вес, отягощенный анамнез, экстракция катаракты), то и ранее.
Наиболее соответствуют этим требованиям лютеин–содержащие препараты фирм «АКВИОН» – Фокус, а также «Экомир» – Лютеин–Комплекс, из зарубежных – Окувайт Лютеин (Бауш и Ломб). Однако последние комплексы не содержат антоцианов черники. Отечественная разработка Фокус («АКВИОН») содержит и антоцианы черники (12,5 мг), и лютеин, а также ликопин, который способствует лучшему усвоению лютеина, и β-каротин. Кроме того, в нем содержатся витамины А, В2, С, Е и цинк, то есть все необходимые вещества для профилактики ВМД.
Литература
1. Будзинская М.В., Воробьева М.В., Киселева Т.Н., Лагутина Ю.М., Полунин Г.С. Современные подходы к лечению и профилактике возрастной макулярной дегенерации // Клиническая офтальмология. – 2007. – Т. 8. – № 2. – С. 78–82.
2. Еднева Я.Н., Миронова Э.М., Абрамова О.С. Гемодинамика глаза у больных «сухой» формой склеротической макулодистрофии до и после комбинированной аргонлазерной стимуляции // Лазерные методы лечения и ангиографические исследования в офтальмологии: Сб. науч. тр. – М., 1983. – С. 85–88.
3. Ермакова Н.А., Рабданова О.Ц. Основные этиологические факторы и патогенетические механизмы развития возрастной макулярной дегенерации // Клиническая офтальмология. – 2007. – Т. 8. – № 3. – С. 125–128.
4. Ермакова Н.А., Рабданова О.Ц. Современные методы диагностики и лечения возрастной макулярной дистрофии // VI Всероссийск. школа офтальмол.: Сб. науч. тр. – М., 2007. – С. 416–422.
5. Журавлева Л.В., Бойко Э.В., Чурилова И.В. и др. // VI Всероссийск. школа офтальмол.: Сб. науч. тр. – М., 2007. – С. 275–283.
6. Кацнельсон Л.А., Лысенко В.С., Балишанская Т.И. Клинический атлас патологии глазного дна. – 3–е изд., стер. – М.: ГЭОТАР–МЕД, 2004. – 152 с.
7. Киселева Т.Н., Кравчук Е.А., Лагутина Ю.М. Современные аспекты патогенеза, клиники и медикаментозного лечения неэкссудативных форм возрастной макулярной дегенерации // Клиническая офтальмология. – 2006. – Т. 7. – № 3. – С. 99–102.
8. Клинические рекомендации. Офтальмология // Под ред. Л.К. Мошетовой, А.П. Нестерова, Е.А. Егорова. – М.: ГЭОТАР–Медиа, 2007. – 256 с.
9. Либман Е.С., Шахова Е.В. Слепота, слабовидение и инвалидность по зрению в Российской Федерации. Ликвидация устранимой слепоты. Всемирная инициатива ВОЗ // Мат. Росс. межрегион. симпозиума. – Уфа, 2003. – С. 38–42.
10. Нащенкова О.В. Медикаментозное лечение возрастных макулярных дегенераций // III Всероссийск. школа офтальмол.: Сб. науч. тр. – М., 2004. – С. 281–289.
11. Age–Related Eye Disease Study Research Group. A randomized, placebo–controlled, clinical trial of high–dose supplementation with vitamins C and E and beta carotene for age–related cataract and vision loss: AREDS report no. 9 // Arch Ophthalmol. – 2001. – Vol. 119. – № 10. – Р. 1439–1452.
12. Cherney E.F. Патогенез сосудистой макулодистрофии // Офтальмологический конгресс «Белые ночи», 28–31 мая 2001. Тез. докладов. – 2001. – С. 3 –5.
13. Clemons T.E., Milton R.C., Klein R., Seddon J.M., Ferris F.L. 3rd. Risk factors for the incidence of Advanced Age–Related Macular Degeneration in the Age–Related Eye Disease Study (AREDS) AREDS report no. 19 // Ophthalmology. – 2005. – Vol. 112. – № 4. – Р. 33–99.
14. Ding X., Patel M., Chan C.C. Molecular pathology of age–related macular degeneration // Prog Retin Eye Res. – 2008 Nov 6. [Epub ahead of print]
15. Ehrlich R., Harris A., Kheradiya N.S., Winston D.M., Ciulla T.A., Wirostko B. Age–related macular degeneration and the aging eye // Clin Interv Aging. – 2008. – Vol. 3. – № 3. – P. 473–482.
16. Floyd R.A., Carney J.M. Free radical damage to protein and DNA: mechanisms involved and relevant observations on brain undergoing oxidative stress // Ann. Neurol. – 1992. – Vol. 32 Suppl. – P. 22–27.
17. Gass J.D. Choroidal neovascular membranes their visualization and treatment // Trans.Am.Acad. Ophthal. Otolaryng. – 1973. Vol. 77 – P. 310–320.
18. Holz F., Pauleikhoff D., Spaide R.F., Bird A.S. age–related macular degeneration. – Berlin; Heidelberg: Springer–Verlag, 2004. – 238 p.
19. Rehak M, Fric E, Wiedemann P. Lutein and antioxidants in the prevention of age–related macular degeneration // Ophthalmologe. – 2008. – Vol. 105. – № 1. – Р. 40–45.
20. Szostak W.B., Szostak–Wegierek D. Nutrition in prevention of age–related macular degeneration // Przegl Lek. – 2008. – Vol. 65. – № 6. – P. 308–311.
21. Zweng H.C., Little H.L., Vassiliadis A. Argon laser photocoagulation. – St. Louis: Mosby, 1977. – P. 127–162.
22. Клиническая физиология зрения. // Под ред. А.М. Шамшиновой. – М.: Научно–мед. фирма МБН, 2006. 944 с.
23. А.П. Нестеров, Л.М. Балашова, Е.П. Кантаржи, А.В. Попов. Изучение влияния витаминно–минерального комплекса «ФОКУС» на клиническую картину и зрительные функции больных, страдающих патологией макулярной области сетчатки // «Офтальмология»,– 2007, Т. 4, № 2, июнь, с. 59–66.












