of infectious complications of ophthalmic surgery
(literary review)
A.V. Vohmyakov, I.N. Okolov, P.A. Gurchenok
St.-Petersburg department of FGU MNTK «Eye Microsurgery» named after acad. Fedorov S.N.
Authors give the review of some results of comparative studies of antibiotics in preoperative and postoperative ophthalmic surgery in USA, Europe, Finland and Russia. There is also data devoted to the resistance level of microorganisms to levofloxacin and other antibiotics and schemes of prescription of levofloxacin before and after ophthalmic surgery.
Поскольку наиболее часто послеоперационные эндофтальмиты вызываются микрофлорой век и конъюнктивы [7, 39], одним из направлений профилактики инфекции в офтальмохирургии является сокращение количества бактериальной флоры на поверхности глазного яблока [4]. Для минимизации риска развития инфекционных осложнений, помимо соблюдения правил асептики и антисептики, необходимо назначение антибиотиков до, во время и после операции [37].
При отсутствии профилактической санации конъюнктивального мешка с использованием антибактериальных препаратов до операции потенциальные возбудители инфекции высеваются из конъюнктивальной полости в 41,8% [3]. В подавляющем большинстве случаев это грамположительные микроорганизмы: S.epidermidis (75,0%), S.aureus (14,1%), Streptococcus spp. (6,2%), Micrococcus spp. (1,6%) и Enterococcus spp. (3,1%) [3].
По данным Endophthalmitis Vitrectomy Study, возбудителями эндофтальмитов в США в 75%-95% случаев являются грамположительные кокки: S. aureus, S. epidermidis и другие коагулазанегативные стафилококки (КНС) [7, 20].
Критериями выбора офтальмологических антибиотиков местного применения, используемых для периоперативной профилактики инфекции, являются следующие их характеристики: бактерицидное действие, высокая проникающая способность, широкий спектр действия, низкая токсичность, хорошая переносимость, а также удобство использования и дозировки [4].
Большинство применяемых в офтальмологии антибиотиков имеют доказанную эффективность в отношении сокращения количества бактериальной флоры на поверхности конъюнктивы. Тем не менее, не все группы препаратов способны предотвращать внутриглазную контаминацию во время операции. В частности, исследования, оценивающие аспираты влаги передней камеры глаза, не выявили существенного эффекта левомицетина, фузидиевой кислоты, неомицина и норфлоксацина на количество колониеобразующих единиц при контаминации передней камеры микроорганизмами во время офтальмологических операций [14, 16, 17, 31, 37]. Также имеются сведения, что глазные капли гентамицина и тобрамицина не создают терапевтической концентрации в водянистой влаге [11, 41].
Длительное использование некоторых антибактериальных препаратов в офтальмологии не могло не изменить степень чувствительности к ним микроорганизмов. Так, большинство обычных возбудителей глазных инфекций, включая H. influenzae, Ps. aeruginosa и S. viridans, имеют высокую резистентность к эритромицину, Ps.aeruginosa, кроме того, устойчив к левомицетину, а около 50% стафилококков не чувствительны к сульфаниламидам [8, 33]. Аминогликозиды – гентамицин и тобрамицин, обычно резервируются для грамотрицательной флоры, они не обладают высокой эффективностью против стрептококков, также возросла резистентность к этим антибиотикам со стороны стафилококков [33]. Несмотря на то, что исследования, проведенные в Санкт-Петербурге, показали, что резистентность КНС к тобрамицину и гентамицину в последние годы была относительно невысокой и, составляла 10,7% и 12,7%, соответственно [2], по данным зарубежных авторов, только 64% изолятов микроорганизмов возбудителей глазных инфекций оказались чувствительны к тобрамицину [28].
Активность современных фторхинолонов в отношении как грамположительных, так и грамотрицательных бактерий и высокая проникающая способность антибиотиков этого класса во влагу передней камеры являются основными аргументами для активного их использования с целью профилактики послеоперационных осложнений в офтальмохирургии [21, 27, 29, 30]. По сведениям Американского общества катарактальных и рефракционных хирургов (ASCRS), 93% оперирующих офтальмологов в США предпочитают использовать именно фторхинолоны [26].
Тем не менее, в отечественной и зарубежной литературе имеются публикации, что в период с 1993 по 2000 гг. было отмечено возрастание резистентности к ципрофлоксацину и офлоксацину среди S. aureus, КНС, Streptococcus spp. и Ps. aeruginosa. Доля резистентных изолятов этих микроорганизмов достигала 50% [1, 6, 13, 18].
Для предотвращения дальнейшего развития резистентности и инфицирования устойчивыми штаммами бактерий необходимо внедрять в практику новые антибактериальные препараты, в том числе и новые фторхинолоны. В отличие от фторхинолонов прежнего поколения, левофлоксацин ингибирует не только бактериальную ДНК-гиразу (топоизомеразу II), но и второй фермент, ответственный за синтез бактериальной ДНК, – топоизомеразу IV. Считается, что воздействие на этот фермент объясняет высокую его активность в отношении стафилококков и стрептококков и более низкие показатели резистентности [34].
По сравнению с предшествующими фторхинолонами, левофлоксацин имеет наивысшую проникающую способность в передний сегмент глаза [15, 22, 43], более широкий спектр действия против Streptococcus spp. и некоторых штаммов атипичных микобактерий и обладает низкой вероятностью возникновения резистентных штаммов возбудителей [19, 33, 34].
Результаты многоцентрового исследования, проведенного в 2004 году в Германии [33], свидетельствуют, что левофлоксацин обладает самым широким среди сравниваемых офтальмологических антибиотиков спектром действия против возбудителей глазных инфекций. Кроме того, по данным национального исследования по надзору за резистентностью в США TRUST (Tracking Resistance in the USA Today), левофлоксацин сохраняет этот спектр в течение последних десяти лет, что является безусловным преимуществом, по сравнению с фторхинолонами предшествующих поколений, такими как ципрофлоксацин и офлоксацин [8, 19].
Результаты исследований, проведенных в 2002-2003 годах в Санкт-Петербурге, по определению резистентности к фторхинолонам КНС основных возбудителей, выделенных у больных бактериальными конъюнктивитами, представлены на рисунке 1. Анализ антимикробного действия четырех фторхинолонов показал, что ко всем препаратам имелось нарастание устойчивости. При этом к левофлоксацину увеличение числа резистентных штаммов, по сравнению с другими фторхинолонами, было наименьшим [1].
Для достижения терапевтических уровней концентрации фторхинолонов во влаге передней камеры требуется определенное время, чтобы антибиотик проник через конъюнктиву и роговицу. В многоцентровом исследовании, проведенном в Японии, были получены данные, что назначение левофлоксацина за три дня до операции по одной капле 3 раза в день давало достоверно высший уровень эрадикации микроорганизмов, чем его применение в течение 1 дня или за 1 час перед операцией (p<0.05) [24]. По сообщению R.Uusitalo, 2006 г. использование левофлоксацина в университетской клинике г. Хельсинки, начиная за 2 дня до операции по 1 капле 5 раз в день и продолжая после нее, позволило сократить показатель развития послеоперационных эндофтальмитов с 2-5 на 1000 операций по поводу катаракты до нуля на 5500 операций [42].
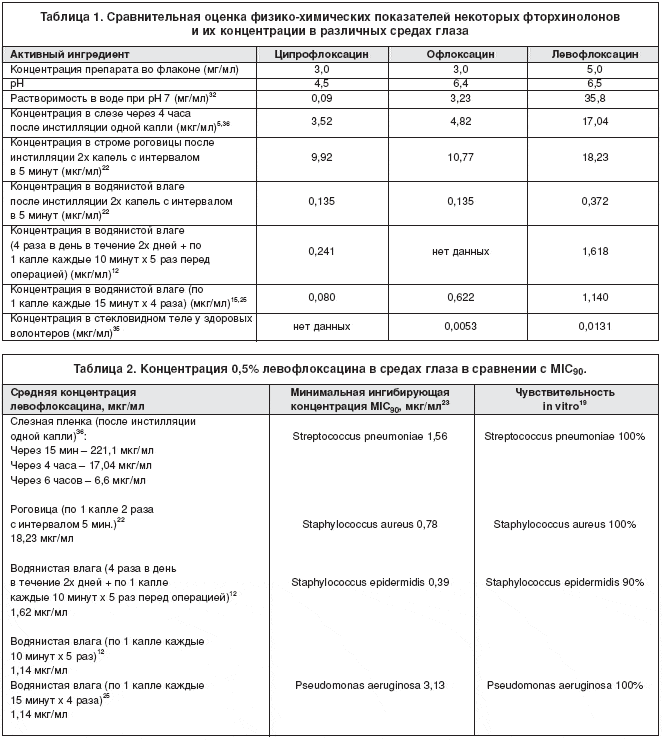
Уровень концентрации левофлоксацина в роговице и водянистой влаге при различных режимах назначения перед операцией превосходит концентрацию ципрофлоксацина и офлоксацина, назначенных в эквивалентных дозировках (табл. 1).
При этом назначение левофлоксацина за 2-3 дня до операции позволяет к моменту ее начала достичь уровня концентрации антибиотика в роговице и влаге передней камеры, превосходящего минимальную ингибирующую концентрацию MIC90 для наиболее частых возбудителей послеоперационного эндофтальмита (табл. 2).
В доступной литературе опубликованы следующие схемы применения левофлоксацина в предоперационном периоде (табл. 3).
В послеоперационном периоде левофлоксацин необходимо продолжать применять в течение 7-14 дней, начиная непосредственно после операции, по рекомендованной производителями схеме (по 1 капле до 8 раз в день в период бодрствования в течение первых двух дней, затем до 4 раз в день в период бодрствования в течение последующих 5-12 дней) [38].
Европейское общество катарактальных и рефракционных хирургов (ESCRS) в рамках многоцентрового исследования, проведенного с сентября 2003 по январь 2006 года с участием около 16 тысяч пациентов, рекомендовало применять левофлоксацин для периоперативной профилактики инфекций по следующей схеме: по 1 капле 2 раза за 1 час и 30 минут до операции, затем 1 капля сразу после окончания операции (на операционном столе), далее – по 1 капле через 5 и 10 минут после операции, и затем по 1 капле 4 раза в день в течение 7-14 дней [10, 38].
Таким образом, применение глазных капель 0,5% левофлоксацина – офтальмологического антибиотика с широким спектром действия, высокой растворимостью и проникающей способностью, низкой резистентностью и хорошей переносимостью, обеспечивающего достаточный уровень микробиологической эрадикации возбудителей в комплексе с асептическими и антисептическими мероприятиями является одним из эффективных путей периоперативной профилактики инфекции в офтальмохирургии.


Литература
1. Околов И.Н., Кафтырева Л.А., Каргальцева Н.М. Резистентность к фтохинолонам микроорганизмов, выделенных от больных с конъюнктивитами. // Офтальмохирургия и терапия. -2004.-№4.-Т.-4.-С.21-24.
2. Околов И.Н., Кафтырева Л.А. Резистентность коагулазанегативных стафилококков, выделенных от больных с конъюнктивитами к антибактериальным препаратам. // Новое в офтальмологии.-2006.-№4.-С.34-36.
3. Сергиенко Н.М. и соавт. Профилактика послеоперационного эндофтальмита. // Офтальмологический журнал. – 2006. - №3 (II). – С. 151-152.
4. Aguirre-Romo I. Comparison of Conjunctival Application of Topical 0.5 % Levofloxacin and 1% Povidone-Iodine Flushing versus Povidone-Iodine alone in Patients undergoing Intraocular Surgery: A Prospective Randomized Study. Dissertation zum Erwerb des Doktorgrades der Medizin an der Medizinischen Fakult?t der Ludwig-Maximilians-Universit?t zu M?nchen. 2006. 66 p.
5. Akkan A.G. et al. Comparative tear concentrations of topically applied ciprofloxacin, ofloxacin and norfloxacin in human eyes. // International Journal of Clinical Pharmacology and Therapeutics. - 1997. - Vol. 35, № 5. - P. 214-217.
6. Alexandrakis G., Alfonso E.C., Miller D. Shifting trends in bacterial keratitis in south Florida and emerging resistance to fluoroquinolones. // Ophthalmology 2000;107:1497-502.
7. Ariyasu RG, Nakamura T, Trousdale MD, Smith RE. Intraoperative bacterial contamination of the aqueous humor. Ophthalmic Surg 1993;24:367-73.
8. Asbell P.A. Recent levofloxacin susceptibility data. // Eurotimes. Supplement, November 2006.- Vol. 11, Issue 11. - P. 3-4.
9. Bannerman T.L., Rhoden D.L., McAllister S.K. et al. The source of coagulase-negative staphylococci in the Endophthalmitis Vitrectomy Study. A comparison of eyelid and intraocular isolates using pulsed-field gel electrophoresis. // Arch. Ophthalmol. 1997;115:357-61.
10. Barry P. et al. ESCRS study of prophylaxis of postoperative endophthalmitis after cataract surgery. // J. Cataract. Refract. Surg. 2006;32:407-10 (updated patient numbers and percentages).
11. Behrens-Baumann W. Absorption of topically administered ciprofloxacin, ofloxacin and gentamicin in the inflamed rabbit eye. // Ophthalmologica. 1996; Vol.210, №2. P.119-122.
12. Bucci F.A. Jr. An in vivo study comparing the ocular absorption of levofloxacin and ciprofloxacin prior to phacoemulsification. // Am. J. Ophthalmol. 2004 Feb;137(2):308-12.
13. Chaudhry N.A., Flynn H.W., Jr., Murray T.G. et al. Emerging ciprofloxacin-resistant Pseudomonas aeruginosa. // Am. J. Ophthalmol. 1999;128:509-10.
14. Chitkara D.K., Manners T., Chapman F. et al. Lack of effect of preoperative norfloxacin on bacterial contamination of anterior chamber aspirates after cataract surgery. // Br. J. Ophthalmol. 1994;78:772-4.
15. Colin J., Simonpoli S., Geldsetzer K., Ropo A. Corneal penetration of levofloxacin into the human aqueous humour: a comparison with ciprofloxacin. // Acta Ophthalmologica Scandinavica. – 2003. – Vol. 81. – P. 611-613.
16. Dallison I.W., Simpson A.J., Keenan J.I. et al. Topical antibiotic prophylaxis for cataract surgery: a controlled trial of fusidic acid and chloramphenicol. // Aust. N Z J Ophthalmol. 1989;17:289-93.
17. Gelfand Y.A., Mezer E., Linn S., Miller B. Lack of effect of prophylactic gentamicin treatment on intraocular and extraocular fluid cultures after pars plana vitrectomy. // Ophthalmic Surg. Lasers 1998;29:497-501.
18. Goldstein M.H., Kowalski R.P., Gordon Y.J. Emerging fluoroquinolone resistance in bacterial keratitis: a 5-year review. // Ophthalmology 1999;106:1313-8.
19. Graves A., Henry M., O’Brien T.P. et al. In vitro susceptibilities of bacterial ocular isolates to fluoroquinolones. // Cornea. – 2001. – Vol. 20., № 3. – P. 301-305.
20. Han D.P., Wisniewski S.R., Wilson L.A. et al. Spectrum and susceptibilities of microbiologic isolates in the Endophthalmitis Vitrectomy Study. // Am. J. Ophthalmol. 1996;122:1-17.
21. Hanioglu-Kargi S., Basci N., Soysal H. et al. The penetration of ofloxacin into human aqueous humor given by various routes. // Eur. J. Ophthalmol. 1998;8:33-6.
22. Healy D.P., Holland E.J. et al. Concentrations of levofloxacin, ofloxacin, and ciprofloxacin in human corneal stromal tissue and aqueous humor after topical administration. // Cornea. 2004 Apr;23(3):255-63.
23. Holland E.J. New Options for Preventing Infection. // Ocular Surgery News. – Sept., 2002. – P. 5-6.
24. Inoue Y. Multicentre study of levofloxacin pre-operative use in Japan. // Eurotimes. Supplement, November 2006.- Vol. 11, Issue 11. - P. 5-6.
25. Koch H.R., Kulus S.C., Roessler M., Ropo A., Geldsetzer K. Corneal penetration of fluoroquinolones: aqueous humor concentrations after topical application of levofloxacin 0.5% and ofloxacin 0.3% eyedrops. // J. Cataract Refract. Surg. 2005 Jul;31(7):1377-85.
26. Leaming D.V. Practice styles and preferences of ASCRS members–2003 survey. // J. Cataract Refract. Surg. 2004;30:892-900.
27. Liesegang T.J. Use of antimicrobials to prevent postoperative infection in patients with cataracts. // Curr Opin Ophthalmol 2001;12:68-74.
28. Milazzo G. et al. // Int. J. Clin. Pharmacol. Ther. - 1999; Vol. 37. P. 243-248.
29. Mi?o de Kaspar H., Chang R.T., Shriver E.M. et al. Three-day application of topical ofloxacin reduces the contamination rate of microsurgical knives in cataract surgery: a prospective randomized study. // Ophthalmology 2004;111:1352-5.
30. Mi?o de Kaspar H. et al. A prospective randomised study determining the efficacy of preoperative topical levofloxacin in eliminating conjunctival bacterial flora. Poster at XXIII ESCRS, Lisbon, Sep 2005.
31. Mistlberger A., Ruckhofer J., Raithel E. et al. Anterior chamber contamination during cataract surgery with intraocular lens implantation. // J. Cataract. Refract. Surg. 1997;23:1064-9.
32. Mitsui Y. et al. AQCmax as a Pharmacokinetic Parameter of Ophthalmic Solution. // Atarashii Ganka (Journal of the Eye) – 1995. – Vol. 12, № 5. – P. 783-786.
33. Multicentre study to determine the prevalence of resistance among isolates of various bacterial pathogens against antibiotics obtained from patients with eye infections in Germany (ophthalmics study). Antiinfectives Intelligence GmbH Rheinbach, Germany, December 2005.
34. Neu H.C., Chin N. In vitro activity of S-ofloxacin. // Antimicrob. Agents Chemother. 1989;33:1105-7.
35. Puustjarvi T. et al. Penetration of topically applied levofloxacin 0.5% and ofloxacin 0.3% into the vitreous of the non-inflamed human eye. // Graefes Arch. Clin. Exp. Ophthalmol. 2006 May 20; [Epub ahead of print]
36. Raizman M.B., Rubin J.M., Graves A.L., Rinehart M. Tear Concentrations of Levofloxacin Following Topical Administration of a Single Dose of 0.5% Levofloxacin Ophthalmic Solution in Healthy Volunteers. // Clinical Therapeutics. – 2002.– Vol. 24, № 9.– P. 1439-1450.
37. Saint-Blancat P., Burucoa C., Boissonnot M. et al. Search for bacterial contamination of the aqueous humor during cataract surgery with and without local antibiotic prophylaxis. // J. Fr. Ophtalmol 1995;18:650-5.
38. Seal D.V. The case for use of levofloxacin in cataract surgery. // Eurotimes. Supplement, November 2006.- Vol. 11, Issue 11. - P. 6-7.
39. Speaker M.G., Milch F.A., Shah M.K. et al. Role of external bacterial flora in the pathogenesis of acute postoperative endophthalmitis. // Ophthalmology 1991;98:639-49.
40. Ta C.N., Egbert P.R., Singh K. et al. Prospective randomized comparison of 3-day versus 1-hour preoperative ofloxacin prophylaxis for cataract surgery. // Ophthalmology 2002;109:2036-40.
41. Taravella M., Stepp P., Young D. Collagen shield delivery of tobramycin to the human eye. // CLAO J.- 1998 Jul; Vol.24, № 3. P.166-168.
42. Uusitalo R. The prophylaxis of endophthalmitis in cataract surgery with levofloxacin. // XI Congress ophthalmologists of Ukraine Abstracts. 16-19 May, 2006. Odessa, Ukraine. P.141.
43. Yamada M., Mochizuki H., Yamada K., et al. Aqueous humor levels of topically applied levofloxacin, norfloxacin, and lomefloxacin in the same human eyes. // J Cataract Refract Surg 2003;29:1771-5.








.gif)



