Актуальность
Юношеская ангиофиброма основания черепа (ЮАОЧ) – это редкая доброкачественная васкуляризированная опухоль, которая обычно развивается у мальчиков-подростков и характеризуется агрессивным ростом. Разрушая структуры основания черепа, ЮАОЧ распространяется в околоносовые пазухи, крылонебную и подвисочную ямки, орбиту, а также интракраниально. Клиническими проявлениями ЮАОЧ являются затруднение носового дыхания; частые, иногда профузные носовые кровотечения; нарушение слуха (при обтурации опухолью носоглотки); деформация лицевого скелета (при прорастании латерально); экзофтальм, зрительные и глазодвигательные нарушения (при распространении в орбиту); различные неврологические симптомы (при интракраниальном распространении). При длительном существовании заболевания развиваются тяжелая анемия и истощение. ЮАОЧ может быть причиной летального исхода [1].Основным методом лечения ЮАОЧ является хирургическое удаление [2–4]. Операции очень часто сопровождаются выраженным кровотечением, для уменьшения которого применяют предварительную эмболизацию сосудов опухоли [5]. При наличии остаточной ткани и развитии продолженного роста, кровоснабжение ЮАОЧ восстанавливается при помощи коллатералей в течение нескольких суток [6–8]. ЮАОЧ – исключительно часто рецидивирующая опухоль. Многие авторы с большими сериями наблюдений, длительно занимающиеся проблемой ЮАОЧ, утверждают, что в ряде случаев резидуальная ЮАОЧ не только не подвергается обратному развитию, но и ведет себя более агрессивно [6, 9–12]. Lloyd et al. в серии из 72 пациентов отметили рецидивы в 39,5% случаев, 14% из которых были неоднократными [13]. Herman et al. наблюдали продолженный рост ангиофибром с интракраниальным распространением у 9 из 44 пациентов [14]. Кроме того, в литературе представлены случаи озлокачествления ЮАОЧ, а также отдельные случаи развития рецидивов через десятки лет после лечения [6].
Проведение повторной операции, как правило, затруднено из-за выраженного рубцового процесса и профузного, а иногда стремительного кровотечения из-за развития коллатералей с внутренней сонной артерий (ВСА). Такие операции всегда сопровождаются массивной кровопотерей до двух объемов циркулирующей крови [15, 16]. Таким образом, при наличии рецидива, особенно при его расположении в области кавернозного синуса, который считается неоперабельным, в крылонебной и подвисочной ямках, оправдано проведение лучевого лечения [17].
Современные аппаратные и программные возможности позволяют проводить конформное стереотаксическое облучение ЮАОЧ в альтернативных режимах – радиохирургии и гипофракционирования. В данной работе мы представляем наш опыт проведения облучения в режиме гипофракционирования при ЮАОЧ, как обоснование применения новых современных методов лучевого лечения у больных с неоперабельной юношеской ангиофибромой основания черепа.
В НМИЦ нейрохирургии им. акад. Н.Н. Бурденко накоплен большой опыт хирургического лечения рецидивов и продолженного роста ЮАОЧ. С 2002 г. по 2017 г. 133 больным с ЮАОЧ, большинство из которых поступали в институт из других клиник уже с рецидивом, проведено хирургическое лечение с применением эндоскопической оптики (всего 156 операций) [5, 18]. В связи с нерезектабельной остаточной опухолью или же по поводу продолженного роста ЮАОЧ 14 пациентам проведено лучевое лечение в отделении радиологии и радиохирургии с 2006 г. по 2017 г. У одного пациента ранее уже был проведен курс лучевой терапии в другом учреждении. Облучение проводилось на аппаратах «КиберНож» (1 пациент), «Новалис» (8 пациентов) и «Примус» (5 пациентов). В 12 случаях облучение проводилось в режиме стандартного фракционирования, в 2-х случаях – в режиме гипофракционирования, при небольшом объеме мишени и при отсутствии вовлечения в опухоль критических структур.
Рассмотрим оба случая гипофракционированного облучения подробно.
Клинический случай 1
У пациента Р. в возрасте 17 лет в 2013 г. появились заложенность носа, носовые кровотечения. При обследовании выявлено образование «задних клеток решетчатого лабиринта и хоан». По месту жительства в августе 2013 г. выполнена эмболизация сосудов опухоли и опухоль была удалена. Гистологическое исследование подтвердило диагноз «ангиофиброма». Через год пациента продолжали беспокоить носовые кровотечения, затруднение носового дыхания, гипестезия верхней губы. На спиральной компьютерной томографии (СКТ) выявлен продолженный рост ЮАОЧ с распространением из носоглотки в крылонебную ямку и интракраниально в среднюю черепную ямку в области большого крыла клиновидной кости. При анализе ангиограмм, выполненных по месту жительства, выявлено, что кровоснабжение опухоль получает из системы наружной сонной артерии (НСА) и ВСА слева. Учитывая, что окклюзия опухоли была проведена микроспиралями, проведение повторной эмболизации было невозможно. В сентябре 2014 г. в НМИЦ нейрохирургии им. акад. Н.Н. Бурденко проведено эндоскопическое эндоназальное удаление краниофациальной юношеской ангиофибромы основания черепа. На операции отмечалось выраженное кровотечение из ветвей каменистого отдела ВСА и ветвей НСА, проводилась реинфузия аутокрови. При контрольном обследовании через 3 и 6 мес. отмечен продолженный рост резидуальной ЮАОЧ в области клиновидной пазухи, крылонебной ямки и принято решение о проведении лучевой терапии. К остатку ангиофибромы объемом 15,2 см3 на аппарате «КиберНож» за 5 сеансов подведена средняя суммарная очаговая доза (СОД) 25 Гр. Через 6 и 12 мес. выявлено выраженное уменьшение объема опухоли (рис. 1).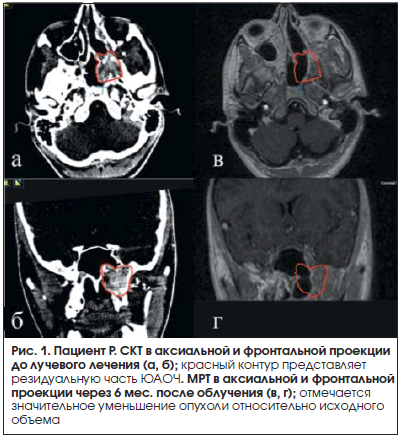
Клинический случай 2
Пациент М. в возрасте 10 лет в начале 2011 г. отметил затруднение носового дыхания, сукровичные выделения из носа. На СКТ выявлена опухоль носоглотки и клиновидной пазухи. Пациент был госпитализирован в больницу по месту жительства в сентябре 2011 г., где была проведена эмболизация сосудов и удаление опухоли – юношеской ангиофибромы, подтвержденной гистологически. После операции носовое дыхание улучшилось, однако на контрольных снимках отмечен продолженный рост резидуальной части ЮАОЧ, распространившейся из носоглотки клиновидной пазухи в клетки решетчатого лабиринта и крылонебную ямку. В декабре 2011 г. пациент был госпитализирован в НМИЦ нейрохирургии им. акад. Н.Н. Бурденко. При проведении ангиографии выявлено кровоснабжение из систем обеих НСА и ВСА. После эмболизации ветвей НСА произведено эндоскопическое эндоназальное удаление ЮАОЧ. Операция сопровождалась выраженным кровотечением из коллатералей системы ВСА, общая кровопотеря составила 3200 мл. Через год после операции выявлен рецидив ЮАОЧ в области клиновидной пазухи, с разрушением ее латеральной стенки и распространением в кавернозный синус. Учитывая невозможность адекватной эмболизации и высокий риск ранения ВСА в ходе операции, пациенту проведена лучевая терапия в режиме гипофракционирования на аппарате «Новалис» в режиме 5 фракций по 5 Гр. Объем опухоли на момент облучения составил 12,5 см3. При катамнестическом наблюдении в течение 3,5 года состояние пациента оставалось стабильным. При магнитно-резонансной томографии (МРТ) отмечено уменьшение объема опухоли (рис. 2).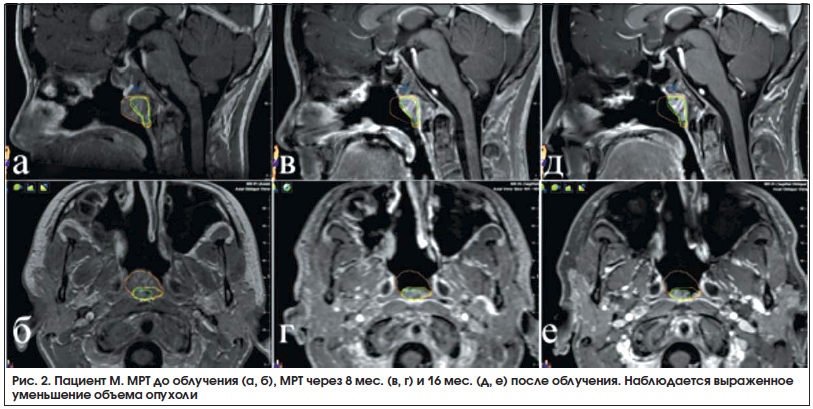
Обсуждение
Хирургическое лечение ЮАОЧ сопряжено с определенными сложностями, в т. ч. с ожидаемой массивной кровопотерей [15, 16, 19, 20]. Развитие эндоваскулярных и эндоскопических методик, кровесберегающих технологий значительно улучшило исходы хирургического лечения ЮАОЧ [5]. Однако высокая склонность ЮАОЧ к рецидивированию, быстрая реваскуляризация и рост опухоли в кавернозный синус ограничивают возможности оперативного лечения рецидивов [17]. По этой причине лучевое лечение активно используется при частичном удалении или рецидиве ЮАОЧ, а также в качестве первичного метода лечения ЮАОЧ в центрах, где нет необходимого опыта и оборудования для проведения таких операций [6]. В последние годы для облучения ЮАОЧ применяются различные методики дистанционного облучения, в т. ч. лучевая терапия в различных режимах и радиохирургия.Большинство публикаций мировой литературы посвящены в основном лучевой терапии в режиме классического фракционирования. До 1990-х годов облучение проводилось до СОД 50–55 Гр [21, 22]. В настоящее время при облучении ЮАОЧ в режиме классического фракционирования стандартными являются суммарные дозы 30–46 Гр [21]. С появлением новых технических возможностей появились работы по стереотаксическому конформному облучению ЮАОЧ [23].
В последние годы стали появляться публикации, демонстрирующие эффективность альтернативных методов фракционирования (гипофракционирования и радиохирургии) при ЮАОЧ [24–26]. Большая часть этих работ представлена описанием отдельных клинических наблюдений. В работе Alvarez et al. радиохирургическое лечение проведено у 10 пациентов с ЮАОЧ с краевыми дозами 14–20 Гр [27].
Практически во всех исследованиях была продемонстрирована высокая эффективность лучевого лечения при ЮАОЧ. Наибольшее количество наблюдений (55 пациентов) представлено в работе Cummings et al. [28]. Контроль роста опухолей в этом исследовании составил 80% при периоде наблюдения от 3 до 26 лет. В диссертационной работе М.В. Родионова продолженный рост был выявлен у 4–х из 51 пациента (т. е. контроль роста опухоли составил 74,5%) при медиане наблюдения 4,4 года (2–16 лет) [29]. В работе McAfee et al. в группе из 22 пациентов получен контроль роста опухоли в 91% при медиане наблюдения 12,7 года [30]. В работе Lee et al. безрецидивная выживаемость составила 85% в группе из 26 больных ЮАОЧ, при среднем периоде наблюдения 6 лет [21]. Mallick et al. представили результаты облучения 31 пациента. При медиане наблюдения 3 года контроль роста опухоли составил 94% [31]. Было высказано предположение о влиянии СОД на безрецидивную выживаемость. В работе Admur при облучении ЮАОЧ с СОД 30–32 Гр контроль роста опухоли составил 77%, а с СОД 35–36 Гр – 91% [32]. В единственной радиохирургической серии из 10 пациентов не было выявлено рецидивов при среднем периоде наблюдения 8 лет [27].
В большинстве работ авторы отмечают, что все выявленные рецидивы происходили в течение 5 лет после проведенной лучевой терапии. Все авторы единодушны во мнении, что пациенты, прошедшие облучение, нуждаются в длительном нейровизуализационном наблюдении [29, 32].
ЮАОЧ являются достаточно радиочувствительными опухолями. В большей части случаев, описанных в литературе, после облучения отмечается выраженное уменьшение опухоли. Admur et al. отметили постепенное уменьшение опухоли (как минимум на 50% объема через год после облучения) вплоть до ее полного регресса у всех пациентов без рецидива [32]. В другой работе полный ответ опухоли на облучение (исчезновение очага) отмечался реже – в 41% случаев [33]. Данная разница, вероятнее всего, определяется разными сроками наблюдения и применяемыми методами нейровизуализации. Следует заметить, что в редких случаях при ЮАОЧ описано развитие массивных кровотечений, несмотря на проведенное облучение и стабилизацию размеров опухоли [23].
Облучение ЮАОЧ сопряжено с определенными рисками. Различают ранние и поздние осложнения лучевой терапии.
К ранним осложнениям следует отнести острые реакции, возникающие во время лечения или в ближайшее время после него. Это в первую очередь реакция слизистых оболочек в виде мукозита. При применении лучевой терапии с относительно небольшими суммарными дозами (до 30–46 Гр), которые приняты в настоящее время, эти реакции выражены минимально [28, 29, 31].
К поздним осложнениям относят повреждение тканей, которое возникает через годы после лечения. В работе Lee et al. при длительном наблюдении у 15% пациентов были зафиксированы поздние осложнения, среди них: катаракта, кератопатия, пангипопитуитаризм, задержка роста, некроз височной доли [21]. Об этом же сообщают и другие авторы [28, 34]. Указанные поздние осложнения характерны для устаревших неизбирательных методик конвенционального облучения, которые использовались в 1960–1970-е годы. При использовании современных стереотаксических методик облучения данные осложнения практически исключены [23, 33]. Дополнительные риски создает повторное облучение ЮАОЧ, при котором возможно развитие деформации (недоразвития) верхнечелюстной кости, лучевого некроза с образованием язвенных дефектов слизистой оболочки полости носа и носоглотки, атрофии зрительного нерва, лучевого фиброза подкожно-жировой клетчатки [29].
Самым грозным поздним эффектом лучевого воздействия является развитие вторичных (радиоиндуцированных) опухолей, а также возможность малигнизации ЮАОЧ. Появление вторичных опухолей является поздним эффектом лучевого воздействия и возникает через много лет после лечения. Тщательное отслеживание данного эффекта особенно актуально у пациентов с ЮАОЧ, т. к. в связи с доброкачественным характером опухоли и эффективностью лечебных мероприятий через 10–15 лет после проведенного облучения, т. е. в 30–35 лет, у этих пациентов могут проявляться вторичные злокачественные опухоли. Из-за разных объемов выборки и периода наблюдения в нескольких исследованиях отмечена разная частота этого грозного осложнения.
В работе Cummings et al. среди 55 пациентов (катамнез 3 года – 26 лет) было выявлено 2 случая развития вторичных опухолей (рак щитовидной железы и базально-клеточный рак кожи) [28]. В исследовании Mallick et al. вторичная опухоль выявлена у 1 из 31 пациента (плоскоклеточный рак) при медиане наблюдения 36 мес. [31]. В работе М.В. Родионова выявлено 3 случая развития вторичной злокачественной опухоли в зоне облучения (обызвествляющаяся эпителиома Малерба, злокачественная опухоль нижней челюсти, базально-клеточный рак кожи щеки) при медиане наблюдения 4,4 года [29]. Существует опасение, что при увеличении периода наблюдения количество этих опухолей может возрастать.
К другим поздним осложнениям, которые обсуждаются в литературе, можно отнести возможность злокачественной трансформации ЮАОЧ. В обзоре Makek 1989 г. собраны опубликованные случаи, которые были расценены как злокачественные трансформации ЮАОЧ [35]. В обзоре собрано 6 наблюдений, опубликованных в 1950–1980-х годах. При этом в 5 из 6 случаев трансформация наблюдалась у пациентов, ранее получивших облучение. Гистологически у 5 из 6 пациентов была диагностирована фибросаркома, у одного – гистиоцитома. Сложно однозначно говорить о прямой гистологической связи фибросарком и гистиоцитомы с исходной ангиофибромой и утверждать, что произошла трансформация. Вполне вероятно, что в данных случаях произошло развитие радиоиндуцированной опухоли. Интересно, что с тех пор в литературе не опубликовано наблюдений злокачественной трансформации ЮАОЧ. В нашей клинике проходил хирургическое лечение больной 36 лет, с фибросаркомой, которому в 16 лет было проведено хирургическое и лучевое лечение по поводу юношеской ангиофибромы.
Одним из способов снижения риска развития вторичных опухолей является применение более коротких режимов фракционирования, т. е. радиохирургии и гипофракционирования [36, 37]. Считается, что радиохирургическое лечение на аппарате «Гамма-нож» не увеличивает или минимально увеличивает такой риск. Кроме того, возможно, применение протонного облучения вместо фотонного также может снизить риск развития вторичных опухолей [38].












