–í–≤–Ķ–ī–Ķ–Ĺ–ł–Ķ
–õ–ĺ–ļ–į–Ľ—Ć–Ĺ—č–Ķ –ł –Ľ–ĺ–ļ–ĺ—Ä–Ķ–≥–ł–ĺ–Ĺ–į—Ä–Ĺ—č–Ķ —Ä–Ķ—Ü–ł–ī–ł–≤—č —Ä–į–ļ–į –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł –Ņ–ĺ—Ā–Ľ–Ķ –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–≥–ĺ —Ä–į–ī–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź —Ä–į–∑–≤–ł–≤–į—é—ā—Ā—Ź –Ņ—Ä–ł–Ī–Ľ–ł–∑–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –≤ –Ņ–ĺ–Ľ–ĺ–≤–ł–Ĺ–Ķ —Ā–Ľ—É—á–į–Ķ–≤ –≤ —Ā—Ä–ĺ–ļ–ł –ĺ—ā 6 –ľ–Ķ—Ā. –ī–ĺ 5 –Ľ–Ķ—ā [1]. –í –į–Ĺ–į–ľ–Ĺ–Ķ–∑–Ķ —É –ī–į–Ĺ–Ĺ—č—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –ļ–į–ļ –Ņ—Ä–į–≤–ł–Ľ–ĺ, –Ņ—Ä–ł—Ā—É—ā—Ā—ā–≤—É–Ķ—ā –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ–Ķ —Ä–į–ī–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł, –≤–ļ–Ľ—é—á–į—é—Č–Ķ–Ķ —Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ĺ–Ķ –≤–ľ–Ķ—ą–į—ā–Ķ–Ľ—Ć—Ā—ā–≤–ĺ, –Ľ—É—á–Ķ–≤—É—é —ā–Ķ—Ä–į–Ņ–ł—é —Ā –ļ–ĺ–Ĺ–ļ—É—Ä–Ķ–Ĺ—ā–Ĺ–ĺ–Ļ —Ö–ł–ľ–ł–ĺ—ā–Ķ—Ä–į–Ņ–ł–Ķ–Ļ –ł–Ľ–ł –Ī–Ķ–∑ –Ĺ–Ķ–Ķ.–•–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ĺ–Ķ –≤–ľ–Ķ—ą–į—ā–Ķ–Ľ—Ć—Ā—ā–≤–ĺ –Ņ–ĺ –Ņ–ĺ–≤–ĺ–ī—É —Ä–Ķ—Ü–ł–ī–ł–≤–į –Ņ—Ä–ł –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–ł –Ķ–≥–ĺ –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ–ł—Ź —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ—č–ľ —Ā–Ņ–ĺ—Ā–ĺ–Ī–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ł –ľ–ĺ–∂–Ķ—ā –ĺ–Ī–Ķ—Ā–Ņ–Ķ—á–ł—ā—Ć 2-–Ľ–Ķ—ā–Ĺ—é—é –Ī–Ķ–∑—Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ—É—é –≤—č–∂–ł–≤–į–Ķ–ľ–ĺ—Ā—ā—Ć –ī–ĺ 36% [2]. –ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ –ľ–Ķ—ā–į–į–Ĺ–į–Ľ–ł–∑–į 32 –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ļ (1080 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤), –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –≤ 2011 –≥., –ĺ–Ī—Č–į—Ź 5-–Ľ–Ķ—ā–Ĺ—Ź—Ź –≤—č–∂–ł–≤–į–Ķ–ľ–ĺ—Ā—ā—Ć –Ņ—Ä–ł —Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł —Ä–Ķ—Ü–ł–ī–ł–≤–į —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–į 39% [1]. –ü–į–Ľ–Ľ–ł–į—ā–ł–≤–Ĺ–į—Ź —Ö–ł–ľ–ł–ĺ—ā–Ķ—Ä–į–Ņ–ł—Ź –ł —ā–į—Ä–≥–Ķ—ā–Ĺ–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź (—Ü–ł—Ā–Ņ–Ľ–į—ā–ł–Ĺ, 5-—Ą—ā–ĺ—Ä—É—Ä–į—Ü–ł–Ľ –ł —Ü–Ķ—ā—É–ļ—Ā–ł–ľ–į–Ī) –Ĺ–Ķ –ĺ—ā–Ľ–ł—á–į—é—ā—Ā—Ź –≤—č—Ā–ĺ–ļ–ĺ–Ļ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć—é –ł –ĺ–Ī–Ķ—Ā–Ņ–Ķ—á–ł–≤–į—é—ā –ľ–Ķ–ī–ł–į–Ĺ—É –Ī–Ķ–∑—Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–ĺ–Ļ –ł –ĺ–Ī—Č–Ķ–Ļ –≤—č–∂–ł–≤–į–Ķ–ľ–ĺ—Ā—ā–ł 5,6 –ł 10,1 –ľ–Ķ—Ā. —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ [3].
–Ě–Ķ—Ā–ľ–ĺ—ā—Ä—Ź –Ĺ–į –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā –≤ —Ö–ł—Ä—É—Ä–≥–ł–ł —Ä–Ķ—Ü–ł–ī–ł–≤–ĺ–≤ –ĺ–Ņ—É—Ö–ĺ–Ľ–Ķ–Ļ –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł, –≤ –į–Ī—Ā–ĺ–Ľ—é—ā–Ĺ–ĺ–ľ –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–Ķ —Ā–Ľ—É—á–į–Ķ–≤ —ć—ā–ł –Ī–ĺ–Ľ—Ć–Ĺ—č–Ķ –Ĺ–Ķ–ĺ–Ņ–Ķ—Ä–į–Ī–Ķ–Ľ—Ć–Ĺ—č –Ņ–ĺ –Ņ—Ä–ł—á–ł–Ĺ–Ķ —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā–ł –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į, –Ĺ–į–Ľ–ł—á–ł—Ź —ā—Ź–∂–Ķ–Ľ–ĺ–Ļ —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–Ķ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–ł –Ľ–ł–Ī–ĺ —ā–Ķ—Ö–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ĺ–Ķ–≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–ł –≤—č–Ņ–ĺ–Ľ–Ĺ–ł—ā—Ć —É—Ā–Ľ–ĺ–≤–Ĺ–ĺ —Ä–į–ī–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–Ķ –ĺ–Ņ–Ķ—Ä–į—ā–ł–≤–Ĺ–ĺ–Ķ –≤–ľ–Ķ—ą–į—ā–Ķ–Ľ—Ć—Ā—ā–≤–ĺ, –ł –Ľ—É—á–Ķ–≤–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź –ĺ—Ā—ā–į–Ķ—ā—Ā—Ź –ĺ—Ā–Ĺ–ĺ–≤–Ĺ—č–ľ –ľ–Ķ—ā–ĺ–ī–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–į –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —Ä–Ķ—Ü–ł–ī–ł–≤–į–ľ–ł —Ä–į–ļ–į –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł –Ņ–ĺ—Ā–Ľ–Ķ –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–≥–ĺ –ĺ–Ņ–Ķ—Ä–į—ā–ł–≤–Ĺ–ĺ–≥–ĺ, –Ľ—É—á–Ķ–≤–ĺ–≥–ĺ, —Ö–ł–ľ–ł–ĺ—ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ł–Ľ–ł –ł—Ö –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–Ļ [4].
–Ě–į —Ā–Ķ–≥–ĺ–ī–Ĺ—Ź—ą–Ĺ–ł–Ļ –ī–Ķ–Ĺ—Ć —Ā—É—Č–Ķ—Ā—ā–≤—É–Ķ—ā –ĺ–Ņ—č—ā —É—Ā–Ņ–Ķ—ą–Ĺ–ĺ–≥–ĺ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź —Ā–ĺ–≤—Ä–Ķ–ľ–Ķ–Ĺ–Ĺ—č—Ö –ľ–Ķ—ā–ĺ–ī–ł–ļ –ļ–ĺ–Ĺ—Ą–ĺ—Ä–ľ–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź IMRT (Intensity Modulated Radiation Therapy) –ł VMAT (Volumetric Modulated Arc Therapy) –≤ —Ä–Ķ–∂–ł–ľ–Ķ –ĺ–Ī—č—á–Ĺ–ĺ–≥–ĺ —Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ņ—Ä–ł –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —Ä–Ķ—Ü–ł–ī–ł–≤–į–ľ–ł —Ä–į–ļ–į –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł [5]. –ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ —Ä—Ź–ī–į –į–≤—ā–ĺ—Ä–ĺ–≤, –ī–į–Ĺ–Ĺ—č–Ķ –ľ–Ķ—ā–ĺ–ī–ł–ļ–ł –ĺ–Ī–Ķ—Ā–Ņ–Ķ—á–ł–≤–į—é—ā –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–ł –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ź –ī–ĺ 80% –ł 2-–Ľ–Ķ—ā–Ĺ–Ķ–Ļ –Ī–Ķ–∑—Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–ĺ–Ļ –≤—č–∂–ł–≤–į–Ķ–ľ–ĺ—Ā—ā–ł –ī–ĺ 50% [6].
–° –Ņ–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ–ľ —ā–Ķ—Ö–Ĺ–ł—á–Ķ—Ā–ļ–ł—Ö –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–Ķ–Ļ –ļ–ĺ–Ĺ—Ą–ĺ—Ä–ľ–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź —Ā —Ā–ĺ–∑–ī–į–Ĺ–ł–Ķ–ľ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö –ī–ĺ–∑–Ĺ—č—Ö –≥—Ä–į–ī–ł–Ķ–Ĺ—ā–ĺ–≤ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ —Ä–į–∑–≤–ł—ā–ł–Ķ –Ņ–ĺ–Ľ—É—á–ł–Ľ–į —Ā—ā–Ķ—Ä–Ķ–ĺ—ā–į–ļ—Ā–ł—á–Ķ—Ā–ļ–į—Ź –Ľ—É—á–Ķ–≤–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź –≤ —Ä–Ķ–∂–ł–ľ–Ķ –≥–ł–Ņ–ĺ—Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź. –Ē–į–Ĺ–Ĺ–į—Ź –ľ–Ķ—ā–ĺ–ī–ł–ļ–į —Ö–ĺ—Ä–ĺ—ą–ĺ –∑–į—Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–ĺ–≤–į–Ľ–į —Ā–Ķ–Ī—Ź –Ņ—Ä–ł —Ä–į–ī–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł –Ľ–ĺ–ļ–į–Ľ–ł–∑–ĺ–≤–į–Ĺ–Ĺ—č—Ö —Ą–ĺ—Ä–ľ —Ä–į–ļ–į –Ņ—Ä–Ķ–ī—Ā—ā–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ –∂–Ķ–Ľ–Ķ–∑—č [7], –Ľ–Ķ–≥–ļ–ĺ–≥–ĺ [8], –į —ā–į–ļ–∂–Ķ –Ņ—Ä–ł –Ņ–į–Ľ–Ľ–ł–į—ā–ł–≤–Ĺ–ĺ–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–ł –ľ–Ķ—ā–į—Ā—ā–į–∑–ĺ–≤ –≤ –Ľ–Ķ–≥–ļ–ł–Ķ, –Ņ–Ķ—á–Ķ–Ĺ—Ć, –≥–ĺ–Ľ–ĺ–≤–Ĺ–ĺ–Ļ –ľ–ĺ–∑–≥ –ł –ļ–ĺ—Ā—ā–ł [9].
–ė–∑-–∑–į –Ĺ–į–Ľ–ł—á–ł—Ź –Ī–ĺ–Ľ—Ć—ą–ĺ–≥–ĺ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–į –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ĺ—Ä–≥–į–Ĺ–ĺ–≤ –ł —Ā—ā—Ä—É–ļ—ā—É—Ä –≤ –ĺ–Ī–Ľ–į—Ā—ā–ł –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł, –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ—Ā—ā–ł –Ņ–ĺ–ī–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –≤—č—Ā–ĺ–ļ–ĺ–Ļ —Ā—É–ľ–ľ–į—Ä–Ĺ–ĺ–Ļ –ī–ĺ–∑—č –ļ –Ņ–ĺ—ā–Ķ–Ĺ—Ü–ł–į–Ľ—Ć–Ĺ–ĺ —Ä–į–ī–ł–ĺ—Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ–Ļ —Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ —Ā—ā–Ķ—Ä–Ķ–ĺ—ā–į–ļ—Ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ—Ä–ł —Ä–Ķ—Ü–ł–ī–ł–≤–į—Ö —Ä–į–ļ–į –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ—Ź–Ķ—ā –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –ł–Ĺ—ā–Ķ—Ä–Ķ—Ā [10]. –Ě–į —Ā–Ķ–≥–ĺ–ī–Ĺ—Ź—ą–Ĺ–ł–Ļ –ī–Ķ–Ĺ—Ć –ĺ—ā—Ā—É—ā—Ā—ā–≤—É—é—ā –ļ–į–ļ–ł–Ķ-–Ľ–ł–Ī–ĺ —á–Ķ—ā–ļ–ł–Ķ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł–ł –Ņ–ĺ —Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ĺ–ł—é —Ä–į–ī–ł–ĺ—ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ĺ–Ī—ä–Ķ–ľ–ĺ–≤ –ł –Ņ—Ä–Ķ–ī–Ņ–ł—Ā–į–Ĺ–ł—é –ī–ĺ–∑ –Ņ—Ä–ł –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–ł –≤ —Ä–Ķ–∂–ł–ľ–Ķ –≥–ł–Ņ–ĺ—Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź, –≤ —Ā–≤—Ź–∑–ł —Ā —á–Ķ–ľ —ā—Ä–Ķ–Ī—É–Ķ—ā—Ā—Ź –ī–į–Ľ—Ć–Ĺ–Ķ–Ļ—ą–Ķ–Ķ –ł–∑—É—á–Ķ–Ĺ–ł–Ķ –≤–ĺ–∑–ľ–ĺ–∂–Ĺ–ĺ—Ā—ā–Ķ–Ļ –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –ī–į–Ĺ–Ĺ–ĺ–Ļ –Ľ–Ķ—á–Ķ–Ī–Ĺ–ĺ–Ļ –ĺ–Ņ—Ü–ł–ł —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö —Ā —Ä–Ķ—Ü–ł–ī–ł–≤–į–ľ–ł —Ä–į–ļ–į –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł.
–¶–Ķ–Ľ—Ć: –ł–∑—É—á–Ķ–Ĺ–ł–Ķ –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā–ł –ł–Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ–Ļ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ņ–ĺ –ļ—Ä–ł—ā–Ķ—Ä–ł—é –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ź –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–Ļ —Ā—ā–Ķ—Ä–Ķ–ĺ—ā–į–ļ—Ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –≤ —Ä–Ķ–∂–ł–ľ–Ķ –≥–ł–Ņ–ĺ—Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö —Ā –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ—č–ľ–ł –ł —Ä–Ķ–≥–ł–ĺ–Ĺ–į—Ä–Ĺ—č–ľ–ł —Ä–Ķ—Ü–ł–ī–ł–≤–į–ľ–ł —Ä–į–ļ–į –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł.
–ú–į—ā–Ķ—Ä–ł–į–Ľ –ł –ľ–Ķ—ā–ĺ–ī—č
–í –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –≤–ļ–Ľ—é—á–Ķ–Ĺ—č 8 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ (5 –ľ—É–∂—á–ł–Ĺ, 3 –∂–Ķ–Ĺ—Č–ł–Ĺ—č) —Ā –ľ–ĺ—Ä—Ą–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł –Ņ–ĺ–ī—ā–≤–Ķ—Ä–∂–ī–Ķ–Ĺ–Ĺ—č–ľ–ł —Ä–Ķ—Ü–ł–ī–ł–≤–į–ľ–ł —Ä–į–ļ–į –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł, –Ņ–ĺ–Ľ—É—á–ł–≤—ą–ł–Ķ –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–Ķ —Ā—ā–Ķ—Ä–Ķ–ĺ—ā–į–ļ—Ā–ł—á–Ķ—Ā–ļ–ĺ–Ķ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–Ķ –≤ –õ–Ē–¶ –ú–ė–Ď–° –ł–ľ. –°. –Ď–Ķ—Ä–Ķ–∑–ł–Ĺ–į —Ā 2013 –Ņ–ĺ 2017 –≥. –í–ĺ–∑—Ä–į—Ā—ā –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā–ĺ—Ā—ā–į–≤–ł–Ľ 38 –Ľ–Ķ—ā ‚Äď 72 –≥–ĺ–ī–į. –Ē–į–Ĺ–Ĺ—č–Ķ –Ņ–ĺ –Ľ–ĺ–ļ–į–Ľ–ł–∑–į—Ü–ł–ł –ĺ–Ņ—É—Ö–ĺ–Ľ–ł –Ņ—Ä–ł–≤–Ķ–ī–Ķ–Ĺ—č –≤ —ā–į–Ī–Ľ–ł—Ü–Ķ 1, –≥–ł—Ā—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–ľ—É —ā–ł–Ņ—É —Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł ‚Äď –≤ —ā–į–Ī–Ľ–ł—Ü–Ķ 2. –ü–Ķ—Ä–ł–ĺ–ī –≤—Ä–Ķ–ľ–Ķ–Ĺ–ł —Ā –ľ–ĺ–ľ–Ķ–Ĺ—ā–į –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź —Ā–ĺ—Ā—ā–į–≤–ł–Ľ –ĺ—ā 6 –ī–ĺ 38 –ľ–Ķ—Ā. –°—É–ľ–ľ–į—Ä–Ĺ–į—Ź –ī–ĺ–∑–į –Ņ—Ä–ł –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–ł –≤–į—Ä—Ć–ł—Ä–ĺ–≤–į–Ľ–į –ĺ—ā 44 –ī–ĺ 66 –ď—Ä –≤ —Ä–Ķ–∂–ł–ľ–Ķ –ĺ–Ī—č—á–Ĺ–ĺ–≥–ĺ —Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź.
–° —Ü–Ķ–Ľ—Ć—é –ł—Ā–ļ–Ľ—é—á–Ķ–Ĺ–ł—Ź –ĺ—ā–ī–į–Ľ–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –ľ–Ķ—ā–į—Ā—ā–į–∑–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź, –į —ā–į–ļ–∂–Ķ –ī–Ľ—Ź –Ī–ĺ–Ľ–Ķ–Ķ —ā–ĺ—á–Ĺ–ĺ–≥–ĺ –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –≥—Ä–į–Ĺ–ł—Ü –ĺ–Ī–Ľ–į—Ā—ā–ł —Ä–Ķ—Ü–ł–ī–ł–≤–į –Ĺ–į —Ą–ĺ–Ĺ–Ķ –Ņ–ĺ—Ā—ā–Ľ—É—á–Ķ–≤—č—Ö –ł –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ—č—Ö —Ą–ł–Ī—Ä–ĺ–∑–Ĺ—č—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ –≤—Ā–Ķ–ľ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ –≤—č–Ņ–ĺ–Ľ–Ĺ—Ź–Ľ–į—Ā—Ć –Ņ–ĺ–∑–ł—ā—Ä–ĺ–Ĺ–Ĺ–ĺ-—ć–ľ–ł—Ā—Ā–ł–ĺ–Ĺ–Ĺ–į—Ź —ā–ĺ–ľ–ĺ–≥—Ä–į—Ą–ł—Ź, —Ā–ĺ–≤–ľ–Ķ—Č–Ķ–Ĺ–Ĺ–į—Ź —Ā –ļ–ĺ–ľ–Ņ—Ć—é—ā–Ķ—Ä–Ĺ–ĺ–Ļ —ā–ĺ–ľ–ĺ–≥—Ä–į—Ą–ł–Ķ–Ļ (–ü–≠–Ę-–ö–Ę) –≤—Ā–Ķ–≥–ĺ —ā–Ķ–Ľ–į —Ā 18F-—Ą—ā–ĺ—Ä–ī–Ķ–∑–ĺ–ļ—Ā–ł–≥–Ľ—é–ļ–ĺ–∑–ĺ–Ļ (18F-–§–Ē–ď).
–Ē–Ľ—Ź –ł–ľ–ľ–ĺ–Ī–ł–Ľ–ł–∑–į—Ü–ł–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ–ł—Ā—Ć —ā–Ķ—Ä–ľ–ĺ–Ņ–Ľ–į—Ā—ā–ł—á–Ķ—Ā–ļ–ł–Ķ –ľ–į—Ā–ļ–ł. –ü—Ä–ł –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ł–ł –Ņ—Ä–Ķ–ī–Ľ—É—á–Ķ–≤–ĺ–Ļ –Ņ–ĺ–ī–≥–ĺ—ā–ĺ–≤–ļ–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ –≤—č–Ņ–ĺ–Ľ–Ĺ—Ź–Ľ–ł—Ā—Ć –ö–Ę, –ú–†–Ę —Ā –ļ–ĺ–Ĺ—ā—Ä–į—Ā—ā–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ–ľ –ł –ü–≠–Ę-–ö–Ę —Ā 18F-–§–Ē–ď —Ā –Ņ–ĺ—Ā–Ľ–Ķ–ī—É—é—Č–ł–ľ —Ā–ĺ–≤–ľ–Ķ—Č–Ķ–Ĺ–ł–Ķ–ľ –ł–∑–ĺ–Ī—Ä–į–∂–Ķ–Ĺ–ł–Ļ. –ě–Ī—ä–Ķ–ľ GTV (Gross Tumor Volume) —Ą–ĺ—Ä–ľ–ł—Ä–ĺ–≤–į–Ľ—Ā—Ź –Ĺ–į –ĺ—Ā–Ĺ–ĺ–≤–į–Ĺ–ł–ł –ī–į–Ĺ–Ĺ—č—Ö –ü–≠–Ę-–ö–Ę (—Ä–ł—Ā. 1), –ĺ–ļ–ĺ–Ĺ—ā—É—Ä–ł–≤–į–Ĺ–ł–Ķ –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ĺ—Ä–≥–į–Ĺ–ĺ–≤ –ł —Ā—ā—Ä—É–ļ—ā—É—Ä –≤—č–Ņ–ĺ–Ľ–Ĺ—Ź–Ľ–ĺ—Ā—Ć –Ņ–ĺ –ö–Ę –ł –ú–†–Ę. –° —Ü–Ķ–Ľ—Ć—é –ļ–ĺ–ľ–Ņ–Ķ–Ĺ—Ā–į—Ü–ł–ł –Ķ–∂–Ķ–ī–Ĺ–Ķ–≤–Ĺ—č—Ö –Ņ–ĺ–≥—Ä–Ķ—ą–Ĺ–ĺ—Ā—ā–Ķ–Ļ –Ņ–ĺ–∑–ł—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź —Ā–ĺ–∑–ī–į–≤–į–Ľ—Ā—Ź –ĺ—ā—Ā—ā—É–Ņ –ī–Ľ—Ź PTV (Planned Treatment Volume) –ī–ĺ 5 –ľ–ľ –ĺ—ā GTV —Ā —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ–ľ –ī–ĺ 1 –ľ–ľ –≤ –ĺ–Ī–Ľ–į—Ā—ā–ł –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ł—Ö —Ā—ā—Ä—É–ļ—ā—É—Ä.

–ü—Ä–Ķ–ī–Ņ–ł—Ā–į–Ĺ–Ĺ–į—Ź —Ā—É–ľ–ľ–į—Ä–Ĺ–į—Ź –ī–ĺ–∑–į —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–į 35 –ď—Ä, –ī–ĺ–∑–į –∑–į —Ą—Ä–į–ļ—Ü–ł—é ‚Äď 7 –ď—Ä, —á–ł—Ā–Ľ–ĺ —Ą—Ä–į–ļ—Ü–ł–Ļ ‚Äď 5, —Ä–ł—ā–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź ‚Äď –Ķ–∂–Ķ–ī–Ĺ–Ķ–≤–Ĺ–ĺ. –Ē–į–Ĺ–Ĺ—č–Ļ —Ä–Ķ–∂–ł–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź —ć–ļ–≤–ł–≤–į–Ľ–Ķ–Ĺ—ā–Ķ–Ĺ 70 –ď—Ä –≤ —Ä–Ķ–∂–ł–ľ–Ķ –ĺ–Ī—č—á–Ĺ–ĺ–≥–ĺ —Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ņ–ĺ –Ņ–ĺ–∑–ī–Ĺ–ł–ľ –Ľ—É—á–Ķ–≤—č–ľ –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł—Ź–ľ.
–†–į—Ā—á–Ķ—ā —ć–ļ–≤–ł–≤–į–Ľ–Ķ–Ĺ—ā–Ĺ—č—Ö –ī–ĺ–∑ –ī–Ľ—Ź –Ņ–ĺ–∑–ī–Ĺ–ł—Ö –Ľ—É—á–Ķ–≤—č—Ö –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ļ –Ņ—Ä–ĺ–ł–∑–≤–ĺ–ī–ł–Ľ—Ā—Ź –Ņ–ĺ –Ľ–ł–Ĺ–Ķ–Ļ–Ĺ–ĺ-–ļ–≤–į–ī—Ä–į—ā–ł—á–Ĺ–ĺ–Ļ –ľ–ĺ–ī–Ķ–Ľ–ł —Ā –Ņ–ĺ–ľ–ĺ—Č—Ć—é —Ą–ĺ—Ä–ľ—É–Ľ—č

–≥–ī–Ķ D1 ‚Äď —Ā—É–ľ–ľ–į—Ä–Ĺ–į—Ź –ī–ĺ–∑–į –≤ —Ä–Ķ–∂–ł–ľ–Ķ –ĺ–Ī—č—á–Ĺ–ĺ–≥–ĺ —Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź, D2 ‚Äď —Ā—É–ľ–ľ–į—Ä–Ĺ–į—Ź –ī–ĺ–∑–į –≤ —Ä–Ķ–∂–ł–ľ–Ķ –ľ–ĺ–ī–ł—Ą–ł—Ü–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–≥–ĺ —Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź, d1 ‚Äď –ī–ĺ–∑–į –∑–į —Ą—Ä–į–ļ—Ü–ł—é –≤ —Ä–Ķ–∂–ł–ľ–Ķ –ĺ–Ī—č—á–Ĺ–ĺ–≥–ĺ —Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź, d2 ‚Äď –ī–ĺ–∑–į –∑–į —Ą—Ä–į–ļ—Ü–ł—é.
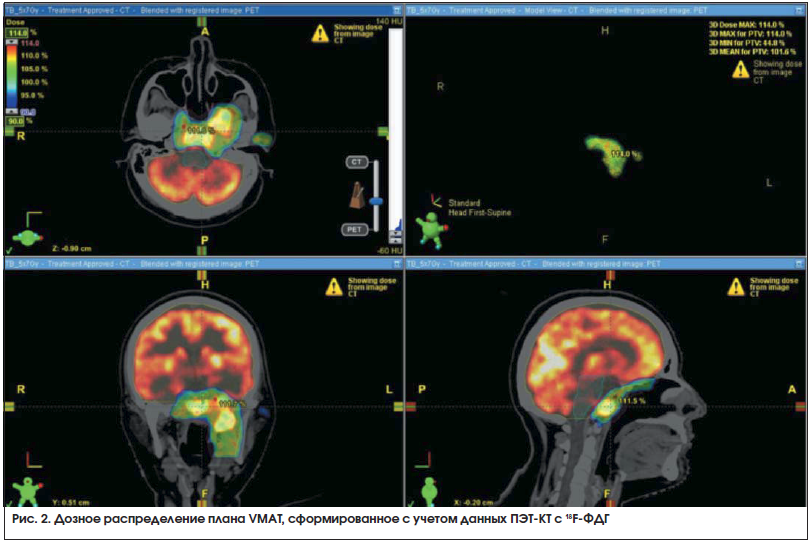
–Ē–ĺ–∑–ł–ľ–Ķ—ā—Ä–ł—á–Ķ—Ā–ļ–ĺ–Ķ –Ņ–Ľ–į–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ĺ—Ā—Ć —Ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ–ľ –Ņ—Ä–ĺ–≥—Ä–į–ľ–ľ–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ķ—Ā–Ņ–Ķ—á–Ķ–Ĺ–ł—Ź Eclipse 10 (Varian) –ł Multiplan 8.0 (Accuray). –ü—Ä–ł–ľ–Ķ—Ä –ī–ĺ–∑–Ĺ–ĺ–≥–ĺ —Ä–į—Ā–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –Ņ—Ä–ł –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–ł —Ä–Ķ—Ü–ł–ī–ł–≤–į –Ĺ–į–∑–ĺ—Ą–į—Ä–ł–Ĺ–≥–Ķ–į–Ľ—Ć–Ĺ–ĺ–Ļ –ļ–į—Ä—Ü–ł–Ĺ–ĺ–ľ—č –Ĺ–ĺ—Ā–ĺ–≥–Ľ–ĺ—ā–ļ–ł –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ–Ķ–Ĺ –Ĺ–į —Ä–ł—Ā. 2. –ě–Ņ—Ä–Ķ–ī–Ķ–Ľ—Ź—Ź –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–ĺ –ī–ĺ–Ņ—É—Ā—ā–ł–ľ—č–Ķ –ī–ĺ–∑—č –Ĺ–į –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ł–Ķ –ĺ—Ä–≥–į–Ĺ—č –Ņ—Ä–ł –Ņ–Ľ–į–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł–ł –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź, –ľ—č —Ä—É–ļ–ĺ–≤–ĺ–ī—Ā—ā–≤–ĺ–≤–į–Ľ–ł—Ā—Ć –Ľ–ł—ā–Ķ—Ä–į—ā—É—Ä–Ĺ—č–ľ–ł –ī–į–Ĺ–Ĺ—č–ľ–ł [11], —Ā–ĺ–≥–Ľ–į—Ā–Ĺ–ĺ –ļ–ĺ—ā–ĺ—Ä—č–ľ —Ā—á–ł—ā–į–Ķ—ā—Ā—Ź, —á—ā–ĺ –Ņ—Ä–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł –Ņ–ĺ–Ľ–Ĺ–ĺ–Ķ –≤–ĺ—Ā—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ł–Ķ —ā–ĺ–Ľ–Ķ—Ä–į–Ĺ—ā–Ĺ—č—Ö –ī–ĺ–∑ –ī–Ľ—Ź —Ā—ā—Ä—É–ļ—ā—É—Ä –¶–Ě–° (—Ā—ā–≤–ĺ–Ľ –ľ–ĺ–∑–≥–į, –∑—Ä–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ķ –Ĺ–Ķ—Ä–≤—č –ł –ł—Ö –Ņ–Ķ—Ä–Ķ–ļ—Ä–Ķ—Ā—ā, —Ā–Ņ–ł–Ĺ–Ĺ–ĺ–Ļ –ľ–ĺ–∑–≥) –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī–ł—ā –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 1,5‚Äď2 –Ľ–Ķ—ā —Ā –ľ–ĺ–ľ–Ķ–Ĺ—ā–į –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź. –Ē—Ä—É–≥–ł–Ķ –į–≤—ā–ĺ—Ä—č –ĺ–Ņ–ł—Ā—č–≤–į—é—ā –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ–Ķ –Ņ–ĺ–ī–≤–Ķ–ī–Ķ–Ĺ–ł–Ķ –ļ –ľ—Ź–≥–ļ–ł–ľ —ā–ļ–į–Ĺ—Ź–ľ —ą–Ķ–ł –ī–ĺ 60 –ď—Ä –Ņ—Ä–ł –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–ł —á–Ķ—Ä–Ķ–∑ –≥–ĺ–ī –Ņ–ĺ—Ā–Ľ–Ķ –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–Ļ –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł [12]. –ü—Ä–ł –Ņ–Ľ–į–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł–ł –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł —ā–ĺ–Ľ–Ķ—Ä–į–Ĺ—ā–Ĺ—č–Ķ –ī–ĺ–∑—č –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ĺ—Ä–≥–į–Ĺ–ĺ–≤ –ł —ā–ļ–į–Ĺ–Ķ–Ļ –Ī—č–Ľ–ł —Ā–ĺ–Ī–Ľ—é–ī–Ķ–Ĺ—č.
–ě–Ī–Ľ—É—á–Ķ–Ĺ–ł–Ķ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ĺ –Ĺ–į —É—Ā—ā–į–Ĺ–ĺ–≤–ļ–į—Ö TrueBeam STx (Varian) –ł CyberKnife (Accuray). –Ē–Ľ—Ź –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ź —ā–ĺ—á–Ĺ–ĺ—Ā—ā–ł –Ņ–ĺ–∑–ł—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ľ–ł—Ā—Ć –ĺ—Ä—ā–ĺ–≥–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–Ķ —Ä–Ķ–Ĺ—ā–≥–Ķ–Ĺ–ĺ–≤—Ā–ļ–ł–Ķ —Ā–Ĺ–ł–ľ–ļ–ł –ł –ö–Ę –≤ –ļ–ĺ–Ĺ—É—Ā–Ĺ–ĺ–ľ –Ņ—É—á–ļ–Ķ –Ķ–∂–Ķ–ī–Ĺ–Ķ–≤–Ĺ–ĺ, –ĺ—ā–ļ–Ľ–ĺ–Ĺ–Ķ–Ĺ–ł—Ź –Ĺ–Ķ –Ņ—Ä–Ķ–≤—č—Ā–ł–Ľ–ł 1 –ľ–ľ.
–õ—É—á–Ķ–≤—č–Ķ —Ä–Ķ–į–ļ—Ü–ł–ł –ł –Ņ–ĺ–∑–ī–Ĺ–ł–Ķ –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł—Ā—Ć –Ņ–ĺ –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ EORTC/RTOG. –Ě–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ļ —ć—Ą—Ą–Ķ–ļ—ā –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ—Ā—Ź —á–Ķ—Ä–Ķ–∑ –ľ–Ķ—Ā—Ź—Ü –Ņ–ĺ—Ā–Ľ–Ķ –ĺ–ļ–ĺ–Ĺ—á–į–Ĺ–ł—Ź –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –≤ —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤–ł–ł —Ā –ļ—Ä–ł—ā–Ķ—Ä–ł—Ź–ľ–ł RECIST –Ņ–ĺ –ī–į–Ĺ–Ĺ—č–ľ –ö–Ę –ł –ú–†–Ę-–ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł —É —á–į—Ā—ā–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ņ–ĺ –ī–į–Ĺ–Ĺ—č–ľ –ü–≠–Ę-–ö–Ę —Ā 18F-–§–Ē–ď.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č
–í—Ā–Ķ–ľ 8 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ —É–ī–į–Ľ–ĺ—Ā—Ć –≤—č–Ņ–ĺ–Ľ–Ĺ–ł—ā—Ć –∑–į–Ņ–Ľ–į–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ. –í–ĺ –≤—Ä–Ķ–ľ—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź —É 2-—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ —É—Ā–ł–Ľ–Ķ–Ĺ–ł–Ķ –Ī–ĺ–Ľ–Ķ–≤–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į, –ļ—É–Ņ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ķ –Ĺ–į–∑–Ĺ–į—á–Ķ–Ĺ–ł–Ķ–ľ –Ĺ–Ķ—Ā—ā–Ķ—Ä–ĺ–ł–ī–Ĺ—č—Ö –Ņ—Ä–ĺ—ā–ł–≤–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ā—Ä–Ķ–ī—Ā—ā–≤, —É 1 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ —Ä–į–∑–≤–ł—ā–ł–Ķ –Ľ—É—á–Ķ–≤–ĺ–≥–ĺ –ī–Ķ—Ä–ľ–į—ā–ł—ā–į I —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł (–≥–ł–Ņ–Ķ—Ä–Ķ–ľ–ł—Ź –ļ–ĺ–∂–ł –≤ –ĺ–Ī–Ľ–į—Ā—ā–ł –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź). –í –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–Ķ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź –∑–į –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ–ł –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 2-—Ö –Ĺ–Ķ–ī–Ķ–Ľ—Ć —Ā –ľ–ĺ–ľ–Ķ–Ĺ—ā–į –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź —É 6 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ —Ä–į–∑–≤–ł—ā–ł–Ķ –Ľ—É—á–Ķ–≤–ĺ–≥–ĺ —ć–Ņ–ł—ā–Ķ–Ľ–ł–ł—ā–į —Ā–Ľ–ł–∑–ł—Ā—ā–ĺ–Ļ –≥–Ľ–ĺ—ā–ļ–ł II —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł, —Ä–į–∑—Ä–Ķ—ą–ł–≤—ą–Ķ–≥–ĺ—Ā—Ź –ļ 4-–Ļ –Ĺ–Ķ–ī–Ķ–Ľ–Ķ —Ā –ľ–ĺ–ľ–Ķ–Ĺ—ā–į –ĺ–ļ–ĺ–Ĺ—á–į–Ĺ–ł—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź.–ü—Ä–ł –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–ľ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł —á–Ķ—Ä–Ķ–∑ –ľ–Ķ—Ā—Ź—Ü –ĺ–Ī—ä–Ķ–ļ—ā–ł–≤–Ĺ—č–Ļ –ĺ—ā–≤–Ķ—ā –Ī—č–Ľ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ —É –≤—Ā–Ķ—Ö 8 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≤–ł–ī–Ķ —á–į—Ā—ā–ł—á–Ĺ–ĺ–≥–ĺ —Ä–Ķ–≥—Ä–Ķ—Ā—Ā–į –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł (5 –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö) –ł —Ā—ā–į–Ī–ł–Ľ–ł–∑–į—Ü–ł–ł —Ä–į–∑–ľ–Ķ—Ä–ĺ–≤ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł —Ā –Ņ–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ–ľ –Ĺ–Ķ–ĺ–ī–Ĺ–ĺ—Ä–ĺ–ī–Ĺ–ĺ—Ā—ā–ł —Ā—ā—Ä—É–ļ—ā—É—Ä—č, —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É—é—Č–Ķ–Ļ –Ņ–ĺ—Ā—ā–Ľ—É—á–Ķ–≤—č–ľ –Ĺ–Ķ–ļ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ł–ľ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź–ľ (3 –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö). –ü—Ä–ł –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–ľ –ĺ–Ī—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł —á–Ķ—Ä–Ķ–∑ 3 –ľ–Ķ—Ā. —Ā –ľ–ĺ–ľ–Ķ–Ĺ—ā–į –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź —Ā–ĺ—Ö—Ä–į–Ĺ—Ź–Ľ–į—Ā—Ć —ā–Ķ–Ĺ–ī–Ķ–Ĺ—Ü–ł—Ź –ļ —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł—é —Ä–į–∑–ľ–Ķ—Ä–ĺ–≤ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–Ĺ—č—Ö –ĺ—á–į–≥–ĺ–≤. –£ 4-—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ĺ–į –ī–į–Ĺ–Ĺ–ĺ–ľ —Ā—Ä–ĺ–ļ–Ķ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź –Ņ–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ –ü–≠–Ę-–ö–Ę —Ā 18F-–§–Ē–ď –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ SUVmax (Standardized Uptake Value) –ī–ĺ –∑–Ĺ–į—á–Ķ–Ĺ–ł–Ļ, —Ā–ĺ–ĺ—ā–≤–Ķ—ā—Ā—ā–≤—É—é—Č–ł—Ö –Ņ–ĺ—Ā—ā–Ľ—É—á–Ķ–≤—č–ľ –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź–ľ (SUVmax 4,0‚Äď5,0).
–ö –Ĺ–į—Ā—ā–ĺ—Ź—Č–Ķ–ľ—É –ľ–ĺ–ľ–Ķ–Ĺ—ā—É –∂–ł–≤—č 6 –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö. –ú–Ķ–ī–ł–į–Ĺ–į –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–į 11 –ľ–Ķ—Ā., —É –≤—č–∂–ł–≤—ą–ł—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ĺ–Ķ—ā –Ņ—Ä–ł–∑–Ĺ–į–ļ–ĺ–≤ –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ —Ä–ĺ—Ā—ā–į –ł–Ľ–ł —Ä–Ķ—Ü–ł–ī–ł–≤–į –≤ –ĺ–Ī–Ľ–į—Ā—ā–ł –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź. –£ 1 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź —Ā –Ņ–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł–Ķ–ľ –ĺ—ā–ī–į–Ľ–Ķ–Ĺ–Ĺ—č—Ö –ľ–Ķ—ā–į—Ā—ā–į–∑–ĺ–≤ –≤ –Ľ–Ķ–≥–ļ–ł—Ö. –ě–ī–ł–Ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā –Ņ–ĺ–≥–ł–Ī –ĺ—ā –Ņ—Ä–ĺ—Ą—É–∑–Ĺ–ĺ–≥–ĺ –ļ—Ä–ĺ–≤–ĺ—ā–Ķ—á–Ķ–Ĺ–ł—Ź –ł–∑ –ļ—Ä—É–Ņ–Ĺ—č—Ö —Ā–ĺ—Ā—É–ī–ĺ–≤ —á–Ķ—Ä–Ķ–∑ 3 –Ĺ–Ķ–ī. –Ņ–ĺ—Ā–Ľ–Ķ –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź, –Ķ—Č–Ķ –ĺ–ī–ł–Ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā –Ņ–ĺ–≥–ł–Ī –≤—Ā–Ľ–Ķ–ī—Ā—ā–≤–ł–Ķ —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–Ķ–Ļ –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł–ł (–ĺ—Ā—ā—Ä–į—Ź –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ—Ā—ā—Ć –ľ–ĺ–∑–≥–ĺ–≤–ĺ–≥–ĺ –ļ—Ä–ĺ–≤–ĺ–ĺ–Ī—Ä–į—Č–Ķ–Ĺ–ł—Ź) —á–Ķ—Ä–Ķ–∑ 4 –ľ–Ķ—Ā. –Ņ–ĺ—Ā–Ľ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź.
–ó–į –Ņ–Ķ—Ä–ł–ĺ–ī –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź —É –≤—č–∂–ł–≤—ą–ł—Ö –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –Ĺ–Ķ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ —Ä–į–∑–≤–ł—ā–ł—Ź –Ņ–ĺ–∑–ī–Ĺ–ł—Ö –Ľ—É—á–Ķ–≤—č—Ö –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ļ –ł —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—Ź –ļ–į—á–Ķ—Ā—ā–≤–į –∂–ł–∑–Ĺ–ł.
–ě–Ī—Ā—É–∂–ī–Ķ–Ĺ–ł–Ķ
–ü–ĺ –Ľ–ł—ā–Ķ—Ä–į—ā—É—Ä–Ĺ—č–ľ –ī–į–Ĺ–Ĺ—č–ľ, –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ł–Ķ –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–Ļ –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł —Ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ–ľ –ļ–ĺ–Ĺ–≤–Ķ–Ĺ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č—Ö –ľ–Ķ—ā–ĺ–ī–ł–ļ –Ĺ–Ķ –ĺ–Ī–Ķ—Ā–Ņ–Ķ—á–ł–≤–į–Ķ—ā —É–ī–ĺ–≤–Ľ–Ķ—ā–≤–ĺ—Ä–ł—ā–Ķ–Ľ—Ć–Ĺ—č—Ö —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤ –Ņ–ĺ –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–ľ—É –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—é –ł –≤—č–∂–ł–≤–į–Ķ–ľ–ĺ—Ā—ā–ł [13]. –Ę–į–ļ, –Ņ–ĺ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź RTOG 9911 2-–Ľ–Ķ—ā–Ĺ—Ź—Ź –Ī–Ķ–∑—Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–į—Ź –≤—č–∂–ł–≤–į–Ķ–ľ–ĺ—Ā—ā—Ć —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–į 16%, 2-–Ľ–Ķ—ā–Ĺ—Ź—Ź –ĺ–Ī—Č–į—Ź –≤—č–∂–ł–≤–į–Ķ–ľ–ĺ—Ā—ā—Ć ‚Äď 26% [14]. –ě–Ī–Ľ—É—á–Ķ–Ĺ–ł–Ķ —Ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ–ľ –ļ–ĺ–Ĺ–≤–Ķ–Ĺ—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č—Ö –ľ–Ķ—ā–ĺ–ī–ł–ļ —Ö–į—Ä–į–ļ—ā–Ķ—Ä–ł–∑—É–Ķ—ā—Ā—Ź –≤—č—Ā–ĺ–ļ–ĺ–Ļ —á–į—Ā—ā–ĺ—ā–ĺ–Ļ —Ä–į–∑–≤–ł—ā–ł—Ź –Ņ–ĺ–∑–ī–Ĺ–ł—Ö –Ľ—É—á–Ķ–≤—č—Ö –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ļ III –ł IV —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł, –Ņ—Ä–ĺ—Ź–≤–Ľ—Ź—é—Č–ł—Ö—Ā—Ź –ĺ—Ā—ā–Ķ–ĺ—Ä–į–ī–ł–ĺ–Ĺ–Ķ–ļ—Ä–ĺ–∑–į–ľ–ł, –Ĺ–Ķ–ļ—Ä–ĺ–∑–į–ľ–ł —Ö—Ä—Ź—Č–Ķ–Ļ –≥–ĺ—Ä—ā–į–Ĺ–ł, —ā—Ä–ł–∑–ľ–ĺ–ľ –∂–Ķ–≤–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ –ľ—É—Ā–ļ—É–Ľ–į—ā—É—Ä—č –ł –Ľ—É—á–Ķ–≤—č–ľ–ł –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł—Ź–ľ–ł –ļ–ĺ–Ĺ—Ā—ā—Ä–ł–ļ—ā–ĺ—Ä–ĺ–≤ –≥–Ľ–ĺ—ā–ļ–ł [15].–ė—Ā—Ö–ĺ–ī—Ź –ł–∑ –Ņ—Ä–Ķ–ī–Ņ–ĺ–Ľ–ĺ–∂–Ķ–Ĺ–ł—Ź –ĺ —ā–ĺ–ľ, —á—ā–ĺ —Ä–Ķ—Ü–ł–ī–ł–≤ –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī–ł—ā –ł–∑ –ļ–Ľ–ĺ–Ĺ–į –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —Ä–į–ī–ł–ĺ—Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ—č—Ö –ļ–Ľ–Ķ—ā–ĺ–ļ, –Ņ–Ķ—Ä–Ķ–∂–ł–≤—ą–ł—Ö –Ľ—É—á–Ķ–≤—É—é —ā–Ķ—Ä–į–Ņ–ł—é –Ņ—Ä–ł –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–ľ –Ľ–Ķ—á–Ķ–Ĺ–ł–ł, –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–Ķ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–Ķ –ī–ĺ–Ľ–∂–Ĺ–ĺ –Ņ—Ä–ĺ–≤–ĺ–ī–ł—ā—Ć—Ā—Ź —Ā –Ņ–ĺ–ī–≤–Ķ–ī–Ķ–Ĺ–ł–Ķ–ľ –≤—č—Ā–ĺ–ļ–ł—Ö —Ā—É–ľ–ľ–į—Ä–Ĺ—č—Ö –ī–ĺ–∑ —Ā —Ü–Ķ–Ľ—Ć—é –Ņ—Ä–Ķ–ĺ–ī–ĺ–Ľ–Ķ–Ĺ–ł—Ź —Ä–į–ī–ł–ĺ—Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł [16]. –Ě–į –Ņ—Ä–į–ļ—ā–ł–ļ–Ķ —ć—ā–ĺ —ā—Ä—É–ī–Ĺ–ĺ–≤—č–Ņ–ĺ–Ľ–Ĺ–ł–ľ–į—Ź –∑–į–ī–į—á–į –ł–∑-–∑–į –Ī–ĺ–Ľ–Ķ–Ķ –Ĺ–ł–∑–ļ–ł—Ö —ā–ĺ–Ľ–Ķ—Ä–į–Ĺ—ā–Ĺ—č—Ö –ī–ĺ–∑ –ĺ–ļ—Ä—É–∂–į—é—Č–ł—Ö —ā–ļ–į–Ĺ–Ķ–Ļ –ł –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ł—Ö —Ā—ā—Ä—É–ļ—ā—É—Ä –Ņ–ĺ—Ā–Ľ–Ķ –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź.
–Ę–į–ļ–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ, —Ä–Ķ—ą–Ķ–Ĺ–ł–Ķ —ć—ā–ĺ–Ļ –∑–į–ī–į—á–ł, —Ā –ĺ–ī–Ĺ–ĺ–Ļ —Ā—ā–ĺ—Ä–ĺ–Ĺ—č, —ā—Ä–Ķ–Ī—É–Ķ—ā —É–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł—Ź –ĺ–Ī—ä–Ķ–ľ–į –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź –∑–į —Ā—á–Ķ—ā –Ī–ĺ–Ľ–Ķ–Ķ —ā–ĺ—á–Ĺ–ĺ–≥–ĺ –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź –≥—Ä–į–Ĺ–ł—Ü —Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł, –į —Ā –ī—Ä—É–≥–ĺ–Ļ ‚Äď –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –≤—č—Ā–ĺ–ļ–ĺ—ā–ĺ—á–Ĺ—č—Ö –ļ–ĺ–Ĺ—Ą–ĺ—Ä–ľ–Ĺ—č—Ö –ľ–Ķ—ā–ĺ–ī–ł–ļ —Ą–ĺ—ā–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź –ł–Ľ–ł –Ľ–ĺ–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –Ņ–ĺ–ī–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –≤—č—Ā–ĺ–ļ–ł—Ö –ī–ĺ–∑ —Ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ–ľ –Ī—Ä–į—Ö–ł—ā–Ķ—Ä–į–Ņ–ł–ł [17]. –Ē—Ä—É–≥–ł–ľ —Ā–Ņ–ĺ—Ā–ĺ–Ī–ĺ–ľ –Ņ—Ä–Ķ–ĺ–ī–ĺ–Ľ–Ķ–Ĺ–ł—Ź —Ä–į–ī–ł–ĺ—Ä–Ķ–∑–ł—Ā—ā–Ķ–Ĺ—ā–Ĺ–ĺ—Ā—ā–ł —Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ –Ĺ–Ķ—Ā—ā–į–Ĺ–ī–į—Ä—ā–Ĺ—č—Ö —Ä–Ķ–∂–ł–ľ–ĺ–≤ —Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –ī–ĺ–∑—č, –Ĺ–į–Ņ—Ä–ł–ľ–Ķ—Ä —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł—Ź –ī–ĺ–∑—č –∑–į —Ą—Ä–į–ļ—Ü–ł—é [18].
–ě–ī–Ĺ–į –ł–∑ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ—č—Ö –∑–į–ī–į—á –Ņ—Ä–ł –Ņ–Ľ–į–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł–ł –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź –∑–į–ļ–Ľ—é—á–į–Ķ—ā—Ā—Ź –≤ —ā–ĺ—á–Ĺ–ĺ–ľ –ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–ł–ł –≥—Ä–į–Ĺ–ł—Ü —Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł, —á—ā–ĺ –≤ –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–Ķ —Ā–Ľ—É—á–į–Ķ–≤ –Ī—č–≤–į–Ķ—ā –∑–į—ā—Ä—É–ī–Ĺ–Ķ–Ĺ–ĺ –≤ —Ā–≤—Ź–∑–ł —Ā –Ĺ–į–Ľ–ł—á–ł–Ķ–ľ –≤ –∑–ĺ–Ĺ–Ķ —Ä–Ķ—Ü–ł–ī–ł–≤–į —Ą–ł–Ī—Ä–ĺ–∑–Ĺ—č—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ –Ņ–ĺ—Ā–Ľ–Ķ —Ä–į–Ĺ–Ķ–Ķ –Ņ–Ķ—Ä–Ķ–Ĺ–Ķ—Ā–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ —Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –≤–ľ–Ķ—ą–į—ā–Ķ–Ľ—Ć—Ā—ā–≤–į –ł–Ľ–ł —Ä–į–ī–ł–ļ–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ –ļ—É—Ä—Ā–į –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł [19]. –Ě–į —Ą–ĺ–Ĺ–Ķ —ā–į–ļ–ł—Ö –ł–∑–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ļ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ —ā—Ä–į–ī–ł—Ü–ł–ĺ–Ĺ–Ĺ—č—Ö –ľ–Ķ—ā–ĺ–ī–ĺ–≤ –≤–ł–∑—É–į–Ľ–ł–∑–į—Ü–ł–ł –≤ –≤–ł–ī–Ķ –ö–Ę –ł –ú–†–Ę —Ā –ļ–ĺ–Ĺ—ā—Ä–į—Ā—ā–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ–ľ –Ĺ–Ķ –≤—Ā–Ķ–≥–ī–į –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ķ—ā –≤–ł–∑—É–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į—ā—Ć —Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ—É—é –ĺ–Ņ—É—Ö–ĺ–Ľ—Ć. –°–Ņ–ĺ—Ā–ĺ–Ī–ĺ–ľ —Ä–Ķ—ą–Ķ–Ĺ–ł—Ź —ć—ā–ĺ–Ļ –Ņ—Ä–ĺ–Ī–Ľ–Ķ–ľ—č —Ā—ā–į–Ľ–ĺ –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ —Ā–ĺ–≤–ľ–Ķ—Č–Ķ–Ĺ–Ĺ—č—Ö —Ä–į–ī–ł–ĺ–ł–∑–ĺ—ā–ĺ–Ņ–Ĺ—č—Ö –ľ–Ķ—ā–ĺ–ī–ĺ–≤ –Ľ—É—á–Ķ–≤–ĺ–Ļ –ī–ł–į–≥–Ĺ–ĺ—Ā—ā–ł–ļ–ł, –≤–ł–∑—É–į–Ľ–ł–∑–ł—Ä—É—é—Č–ł—Ö –ľ–Ķ—ā–į–Ī–ĺ–Ľ–ł–∑–ľ –ĺ–Ņ—É—Ö–ĺ–Ľ–Ķ–≤–ĺ–Ļ —ā–ļ–į–Ĺ–ł, –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –ī–ĺ—Ā—ā—É–Ņ–Ĺ—č–Ļ –ł–∑ –ļ–ĺ—ā–ĺ—Ä—č—Ö ‚Äď –ü–≠–Ę-–ö–Ę —Ā 18F‚Äď–§–Ē–ď [20]. –Ē–į–Ĺ–Ĺ—č–Ļ –ľ–Ķ—ā–ĺ–ī –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ķ—ā –≤–ł–∑—É–į–Ľ–ł–∑–ł—Ä–ĺ–≤–į—ā—Ć –ĺ–Ī—ä–Ķ–ľ –ľ–Ķ—ā–į–Ī–ĺ–Ľ–ł—á–Ķ—Ā–ļ–ł –į–ļ—ā–ł–≤–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł –ł –Ņ–ĺ –ö–Ę-—Ā–ĺ—Ā—ā–į–≤–Ľ—Ź—é—Č–Ķ–Ļ —ā–ĺ—á–Ĺ–ĺ –Ľ–ĺ–ļ–į–Ľ–ł–∑–ĺ–≤–į—ā—Ć –Ķ–≥–ĺ, —á—ā–ĺ —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź –ļ—Ä–ł—ā–ł—á–Ĺ—č–ľ –Ņ—Ä–ł –ĺ–ļ–ĺ–Ĺ—ā—É—Ä–ł–≤–į–Ĺ–ł–ł –ĺ–Ī—ä–Ķ–ľ–į –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź.
–í –Ĺ–į—ą–Ķ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł –ľ—č –ĺ—Ü–Ķ–Ĺ–ł–Ľ–ł –Ņ–Ķ—Ä–Ķ–Ĺ–ĺ—Ā–ł–ľ–ĺ—Ā—ā—Ć, –Ĺ–Ķ–Ņ–ĺ—Ā—Ä–Ķ–ī—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ķ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–ł—Ź –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–Ļ –ļ–ĺ–Ĺ—Ą–ĺ—Ä–ľ–Ĺ–ĺ–Ļ –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł –≤ —Ä–Ķ–∂–ł–ľ–Ķ –≥–ł–Ņ–ĺ—Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ņ—Ä–ł –Ľ–ĺ–ļ–ĺ—Ä–Ķ–≥–ł–ĺ–Ĺ–į—Ä–Ĺ—č—Ö —Ä–Ķ—Ü–ł–ī–ł–≤–į—Ö —Ä–į–ļ–į –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł, –į —ā–į–ļ–∂–Ķ —á–į—Ā—ā–ĺ—ā—É —Ä–į–∑–≤–ł—ā–ł—Ź –Ņ–ĺ–∑–ī–Ĺ–ł—Ö –Ľ—É—á–Ķ–≤—č—Ö —Ä–Ķ–į–ļ—Ü–ł–Ļ –ł –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ļ.
–ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ –Ĺ–į—ą–Ķ–≥–ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź, –Ņ—Ä–ł –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–ľ –ļ–ĺ–Ĺ—Ą–ĺ—Ä–ľ–Ĺ–ĺ–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–ł —Ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ–ľ –≥–ł–Ņ–ĺ—Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ĺ–Ķ –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī–ł–Ľ–ĺ –Ņ–ĺ–≤—č—ą–Ķ–Ĺ–ł—Ź —á–į—Ā—ā–ĺ—ā—č —Ä–į–∑–≤–ł—ā–ł—Ź —Ä–į–Ĺ–Ĺ–ł—Ö –Ľ—É—á–Ķ–≤—č—Ö —Ä–Ķ–į–ļ—Ü–ł–Ļ (–ľ—É–ļ–ĺ–∑–ł—ā—č, –Ľ—É—á–Ķ–≤–ĺ–Ļ –ī–Ķ—Ä–ľ–į—ā–ł—ā) –≤ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł —Ā –Ņ–Ķ—Ä–≤–ł—á–Ĺ—č–ľ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–Ķ–ľ —Ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł–Ķ–ľ —ā–Ķ—Ö –∂–Ķ –ľ–Ķ—ā–ĺ–ī–ł–ļ –ł —Ä–Ķ–∂–ł–ľ–į —Ą—Ä–į–ļ—Ü–ł–ĺ–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź. –ě—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ —É—Ā–ł–Ľ–Ķ–Ĺ–ł—Ź —Ä–į–Ĺ–Ĺ–Ķ–Ļ –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–ĺ–ļ—Ā–ł—á–Ĺ–ĺ—Ā—ā–ł —Ā–ĺ–≥–Ľ–į—Ā—É–Ķ—ā—Ā—Ź —Ā –ł–ľ–Ķ—é—Č–ł–ľ–ł—Ā—Ź –Ľ–ł—ā–Ķ—Ä–į—ā—É—Ä–Ĺ—č–ľ–ł –ī–į–Ĺ–Ĺ—č–ľ–ł [21].
–Ě–į–ł–Ī–ĺ–Ľ–Ķ–Ķ –≤–Ķ—Ä–ĺ—Ź—ā–Ĺ–ĺ, –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ —É—Ā–ł–Ľ–Ķ–Ĺ–ł—Ź —Ä–į–Ĺ–Ĺ–Ķ–Ļ –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–ĺ–ļ—Ā–ł—á–Ĺ–ĺ—Ā—ā–ł –≤ –Ĺ–į—ą–Ķ–ľ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–ł —Ā–≤—Ź–∑–į–Ĺ–ĺ —Ā –ľ–Ķ–Ĺ—Ć—ą–ł–ľ–ł –∑–Ĺ–į—á–Ķ–Ĺ–ł—Ź–ľ–ł –ĺ–Ī—ä–Ķ–ľ–ĺ–≤ –≤—č—Ā–ĺ–ļ–ĺ–ī–ĺ–∑–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź. –£–ľ–Ķ–Ĺ—Ć—ą–Ķ–Ĺ–ł–Ķ –ĺ–Ī—ä–Ķ–ľ–ĺ–≤ –Ī—č–Ľ–ĺ –ī–ĺ—Ā—ā–ł–≥–Ĺ—É—ā–ĺ –∑–į —Ā—á–Ķ—ā –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—Ź –ü–≠–Ę-–ö–Ę —Ā 18F-–§–Ē–ď –Ņ—Ä–ł –ĺ–ļ–ĺ–Ĺ—ā—É—Ä–ł–≤–į–Ĺ–ł–ł GTV, –≤ —Ā–≤—Ź–∑–ł —Ā —á–Ķ–ľ –Ĺ–Ķ –Ī—č–Ľ–ĺ –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–ĺ—Ā—ā–ł –≤ —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł–ł –ĺ—ā—Ā—ā—É–Ņ–į –ī–Ľ—Ź CTV, —Ā–≤—Ź–∑–į–Ĺ–Ĺ–ĺ–≥–ĺ —Ā –Ĺ–Ķ–ĺ–Ņ—Ä–Ķ–ī–Ķ–Ľ–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć—é –≤–ł–∑—É–į–Ľ–ł–∑–į—Ü–ł–ł –≥—Ä–į–Ĺ–ł—Ü —Ä–Ķ—Ü–ł–ī–ł–≤–Ĺ–ĺ–Ļ –ĺ–Ņ—É—Ö–ĺ–Ľ–ł. –Ę–į–ļ–∂–Ķ –Ī–Ľ–į–≥–ĺ–ī–į—Ä—Ź –Ņ—Ä–ł–ľ–Ķ–Ĺ–Ķ–Ĺ–ł—é —Ā—Ä–Ķ–ī—Ā—ā–≤ IGRT (–ļ–ł–Ľ–ĺ–≤–ĺ–Ľ—Ć—ā–Ĺ—č–Ķ —Ā–Ĺ–ł–ľ–ļ–ł –ł –ö–Ę –≤ –ļ–ĺ–Ĺ—É—Ā–Ĺ–ĺ–ľ –Ņ—É—á–ļ–Ķ) —É–ī–į–Ľ–ĺ—Ā—Ć —Ā–ĺ–ļ—Ä–į—ā–ł—ā—Ć –ĺ—ā—Ā—ā—É–Ņ PTV –ī–ĺ 5 –ľ–ľ, –į –≤ –ĺ–Ī–Ľ–į—Ā—ā–ł –ļ—Ä–ł—ā–ł—á–Ķ—Ā–ļ–ł—Ö —Ā—ā—Ä—É–ļ—ā—É—Ä —Ü–Ķ–Ĺ—ā—Ä–į–Ľ—Ć–Ĺ–ĺ–Ļ –Ĺ–Ķ—Ä–≤–Ĺ–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č –ī–ĺ 1 –ľ–ľ.
–ü—Ä–ł –ľ–Ķ–ī–ł–į–Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź –≤ 11 –ľ–Ķ—Ā. —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ĺ—Ā—Ć –Ņ–ĺ–∑–ī–Ĺ–Ķ–Ļ –Ľ—É—á–Ķ–≤–ĺ–Ļ —ā–ĺ–ļ—Ā–ł—á–Ĺ–ĺ—Ā—ā–ł –≤ –≤–ł–ī–Ķ –ĺ—Ā—ā–Ķ–ĺ–Ĺ–Ķ–ļ—Ä–ĺ–∑–ĺ–≤, –Ĺ–Ķ–ļ—Ä–ĺ–∑–ĺ–≤ –ľ—Ź–≥–ļ–ł—Ö —ā–ļ–į–Ĺ–Ķ–Ļ –ł —Ä–į–ī–ł–į—Ü–ł–ĺ–Ĺ–Ĺ—č—Ö –Ņ–ĺ–≤—Ä–Ķ–∂–ī–Ķ–Ĺ–ł–Ļ —Ā—ā—Ä—É–ļ—ā—É—Ä —Ü–Ķ–Ĺ—ā—Ä–į–Ľ—Ć–Ĺ–ĺ–Ļ –Ĺ–Ķ—Ä–≤–Ĺ–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č. –Ě–į—ą–ł –ī–į–Ĺ–Ĺ—č–Ķ —Ā–ĺ–≥–Ľ–į—Ā—É—é—ā—Ā—Ź —Ā —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–į–ľ–ł —Ä–į–Ī–ĺ—ā –ī—Ä—É–≥–ł—Ö –į–≤—ā–ĺ—Ä–ĺ–≤, –Ņ—Ä–ĺ–≤–ĺ–ī–ł–≤—ą–ł—Ö –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ–ĺ–Ķ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł–Ķ –Ņ—Ä–ł —Ä–Ķ—Ü–ł–ī–ł–≤–į—Ö –ł–Ľ–ł –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ-–ľ–Ĺ–ĺ–∂–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö –ľ–Ķ—ā–į—Ö—Ä–ĺ–Ĺ–Ĺ—č—Ö –ĺ–Ņ—É—Ö–ĺ–Ľ—Ź—Ö –ĺ–Ī–Ľ–į—Ā—ā–ł –≥–ĺ–Ľ–ĺ–≤—č –ł —ą–Ķ–ł, –≤ –ļ–ĺ—ā–ĺ—Ä—č—Ö –Ņ–ĺ–ļ–į–∑–į–Ĺ–ĺ –Ņ—Ä–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł –Ņ–ĺ–Ľ–Ĺ–ĺ–Ķ –≤–ĺ—Ā—Ā—ā–į–Ĺ–ĺ–≤–Ľ–Ķ–Ĺ–ł–Ķ —ā–ĺ–Ľ–Ķ—Ä–į–Ĺ—ā–Ĺ—č—Ö –ī–ĺ–∑ —Ā–Ņ–ł–Ĺ–Ĺ–ĺ–≥–ĺ –ľ–ĺ–∑–≥–į, –ļ–ĺ–∂–ł –ł –ľ—Ź–≥–ļ–ł—Ö —ā–ļ–į–Ĺ–Ķ–Ļ —á–Ķ—Ä–Ķ–∑ –≥–ĺ–ī –Ņ–ĺ—Ā–Ľ–Ķ –Ņ–Ķ—Ä–≤–ł—á–Ĺ–ĺ–≥–ĺ –ĺ–Ī–Ľ—É—á–Ķ–Ĺ–ł—Ź [22].












