–Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≤—Б–µ —З–∞—Й–µ –≥–Њ–≤–Њ—А—П—В –Њ –і–µ—Д–Є—Ж–Є—В–µ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е —Н—Б—Б–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е –љ—Г—В—А–Є–µ–љ—В–Њ–≤.
–Э–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –њ–Є—В–∞–љ–Є—П –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –Њ—З–µ–≤–Є–і–љ–∞. –Э–µ –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Љ–љ–µ–љ–Є–є —В–∞–Ї–ґ–µ –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ –Ї–ї–µ—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Ю—А–≥–∞–љ–Є–Ј–Љ –±–Њ–ї—М–љ–Њ–≥–Њ —А–∞–Ї–Њ–Љ –љ–µ –∞–і–∞–њ—В–Є—А—Г–µ—В—Б—П –Ї –љ–Њ–≤—Л–Љ —Г—Б–ї–Њ–≤–Є—П–Љ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Є –љ–µ –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є —Б–Њ—Е—А–∞–љ–Є—В—М –Є–ї–Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В—М –љ–Њ—А–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Њ–±–Љ–µ–љ–∞.
–Я–Њ –і–∞–љ–љ—Л–Љ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Є–Љ–Є —Г—З–µ–љ—Л–Љ–Є –≤ 80–—Е –≥–Њ–і–∞—Е –њ—А–Њ—И–ї–Њ–≥–Њ –≤–µ–Ї–∞, 50% –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е, –љ–∞–њ—А–∞–≤–ї—П–µ–Љ—Л—Е –љ–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ, –Є–Љ–µ–ї–Є –і–µ—Д–Є—Ж–Є—В –Љ–∞—Б—Б—Л —В–µ–ї–∞ —А–∞–Ј–љ–Њ–є —Б—В–µ–њ–µ–љ–Є, –∞ —Г 15% – –і–Њ 10% –Њ—В —Г—А–Њ–≤–љ—П –і–Њ –љ–∞—З–∞–ї–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Я–Њ –і–∞–љ–љ—Л–Љ ECOG 2003 –≥. (–Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Њ 3047 –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е), —З–∞—Б—В–Њ—В–∞ –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, —В.–µ. –і–µ—Д–Є—Ж–Є—В –±–µ–ї–Ї–Њ–≤, –ґ–Є—А–Њ–≤, —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –Є –Љ–Є–љ–µ—А–∞–ї–Њ–≤, –њ—А–Є –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Њ—А–≥–∞–љ–Њ–≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –Њ—В 70 –і–Њ 83%. –Я—А–Є —Н—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –≤–Њ–Ј—А–∞—Б—В–∞—О—Й–Є–µ –љ–∞ 60% —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –Є –≤—В–Њ—А–Є—З–љ—Г—О (—П—В—А–Њ–≥–µ–љ–љ—Г—О) –љ—Г—В—А–Є—В–Є–≤–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, —А–∞–Ј–≤–Є–≤–∞—О—Й—Г—О—Б—П –≤ —Е–Њ–і–µ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ, –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є–ї–Є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П [1].
–Э—Г—В—А–Є—В–Є–≤–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М —Г –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е —В–∞–Ї–ґ–µ —Б–≤—П–Ј–∞–љ–∞ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–Љ–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ–Є: –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ–Њ–є –њ–љ–µ–≤–Љ–Њ–љ–Є–µ–є, –љ–∞–≥–љ–Њ–µ–љ–Є–µ–Љ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е —А–∞–љ, —Б–≤–Є—Й–∞–Љ–Є, —Н—А–Њ–Ј–Є–≤–љ—Л–Љ–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П–Љ–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Є –і—А. [1]. –Ъ–Њ—А—А–µ–Ї—Ж–Є—П –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Љ–Њ–ґ–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М—Б—П —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ, –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –Є–ї–Є –Є—Е —Б–Њ—З–µ—В–∞–љ–Є—П.
–Я—А–Њ–Њ–±—А–∞–Ј–Њ–Љ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М –і–Њ–Ї—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ—Л–є —Д–∞–Ї—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –µ–≥–Є–њ—В—П–љ–∞–Љ–Є 3500 –ї–µ—В –љ–∞–Ј–∞–і —А–µ–Ї—В–∞–ї—М–љ—Л—Е –Ї–ї–Є–Ј–Љ (–Ї–∞–Ї —З–∞—Б—В—М —А–Є—В—Г–∞–ї—М–љ–Њ–≥–Њ –≥–Њ–ї–Њ–і–∞–љ–Є—П), –њ—А–Є–µ–Љ —Б–ї–∞–±–Є—В–µ–ї—М–љ—Л—Е –Є —А–µ–Ї—В–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ —Б —Ж–µ–ї—М—О —Б–Њ—Е—А–∞–љ–µ–љ–Є—П –Ј–і–Њ—А–Њ–≤—М—П [2].
–•–Њ—В—П –њ–µ—А–≤—Л–µ –Њ–њ–Є—Б–∞–љ–Є—П –Њ—А–Њ—Д–∞—А–Є–љ–≥–µ–∞–ї—М–љ–Њ–≥–Њ –Є–ї–Є —Д–∞—А–Є–љ–≥–µ–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –Њ—В–љ–Њ—Б—П—В—Б—П –Ї XII –≤–µ–Ї—Г, —В–Њ–ї—М–Ї–Њ –≤ 1617 –≥–Њ–і—Г Fabricius –і–µ—В–∞–ї—М–љ–Њ –Њ–њ–Є—Б–∞–ї –≤–≤–µ–і–µ–љ–Є–µ –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е —Б–Љ–µ—Б–µ–є —Б –њ–Њ–Љ–Њ—Й—М—О —Б–µ—А–µ–±—А—П–љ–Њ–є —В—А—Г–±–Ї–Є, –≤—Б—В–∞–≤–ї–µ–љ–љ–Њ–є –≤ –њ–Є—Й–µ–≤–Њ–і –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—В–Њ–ї–±–љ—П–Ї–Њ–Љ [3]. –Э–∞—З–∞–ї–Њ–Љ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М 1793 –≥–Њ–і, –Ї–Њ–≥–і–∞ –≤ –Ы–Њ–љ–і–Њ–љ–µ J. Hunter, —Е–Є—А—Г—А–≥ –Ї–Њ—А–Њ–ї—П –У–µ–Њ—А–≥–∞ III, –њ—А–Є–Љ–µ–љ–Є–ї –і–ї—П –њ–Є—В–∞–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ —Б «–њ–∞—А–∞–ї–Є–Ј–Є—Б–Њ–Љ —П–≥–Њ–і–Є—З–љ–Њ–є –Љ—Л—И—Ж—Л» –Ї–Є—В–Њ–≤—Л–є —Г—Б, –Њ–±–µ—А–љ—Г—В—Л–є –Ї–Њ–ґ–µ–є —Г–≥—А—П, –∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б–Љ–µ—Б–µ–є –і–ї—П —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –Ј–Њ–љ–і–Њ–≤–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –±—Л–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л —Б—В—Г–і–љ–Є –Є —П–є—Ж–∞, –≤–Ј–±–Є—В—Л–µ —Б –≤–Њ–і–Њ–є, —Б–∞—Е–∞—А–Њ–Љ –Є–ї–Є –≤–Є–љ–Њ–Љ [3].
–Э–∞—З–Є–љ–∞—П —Б —Н—В–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є, –±–µ—А–µ—В —Б–≤–Њ–є –Њ—В—З–µ—В —Н–њ–Њ—Е–∞ —А–∞–Ј–≤–Є—В–Є—П —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П. –Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ – —Н—В–Њ –≤–≤–µ–і–µ–љ–Є–µ –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е —Б–Љ–µ—Б–µ–є –≤ —В–Њ—В —Г—З–∞—Б—В–Њ–Ї –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –≥–і–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Є—Е –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ. –Т –Њ—Б–љ–Њ–≤–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –ї–µ–ґ–∞—В –Љ–µ–і–Є–Ї–Њ––±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–і–њ–Њ—Б—Л–ї–Ї–Є:
– –њ–Њ–њ–∞–і–∞–љ–Є–µ –љ—Г—В—А–Є–µ–љ—В–Њ–≤ —З–µ—А–µ–Ј —Б–Є—Б—В–µ–Љ—Г –≤–Њ—А–Њ—В–љ–Њ–є –≤–µ–љ—Л –≤ –њ–µ—З–µ–љ—М –±–Њ–ї–µ–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–љ–Њ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В —Б–Є–љ—В–µ–Ј –±–µ–ї–Ї–∞ –Є —А–µ–≥—Г–ї—П—Ж–Є—О –Њ–±–Љ–µ–љ–∞ –≤–µ—Й–µ—Б—В–≤ –≤ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ—Л—Е –Њ—А–≥–∞–љ–∞—Е –Є –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –њ–µ—З–µ–љ–Є;
– –љ–µ–Ї–Њ—В–Њ—А—Л–µ –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є–µ –≤ —Б—В–µ–љ–Ї–µ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –љ–∞–њ—А–Є–Љ–µ—А, —В—А–∞–љ—Б–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–Є–µ, –Є—Б–Ї–ї—О—З–∞—О—В—Б—П –њ—А–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–Љ –њ–Є—В–∞–љ–Є–Є;
– –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л–є –њ—Г—В—М –∞–ї–Є–Љ–µ–љ—В–∞—Ж–Є–Є –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –Њ–±—К–µ–Љ–∞ —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–Є–є –ґ–Є–і–Ї–Њ—Б—В–Є –Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –љ–∞–≥—А—Г–Ј–Ї—Г –љ–∞ —Б–µ—А–і—Ж–µ, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ —А–∞—Б—Е–Њ–і–Њ–Љ —Н–љ–µ—А–≥–Є–Є;
– —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–Љ –Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є –Є–Ј–Њ–Ї–∞–ї–Њ—А–Є–є–љ—Л—Е, –Є–Ј–Њ–∞–Ј–Њ—В–Є—Б—В—Л—Е —А–∞—Б—В–≤–Њ—А–Њ–≤ –њ–Є—Й–µ–≤—Л—Е –≤–µ—Й–µ—Б—В–≤ –≤—Л—П–≤–Є–ї–Њ –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ –њ—А–Є–±–∞–≤–Ї–Є –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є —А–µ—В–µ–љ—Ж–Є–Є –∞–Ј–Њ—В–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–µ—А–≤–Њ–≥–Њ —Б–њ–Њ—Б–Њ–±–∞;
– –Љ–µ—В–Њ–і–Є–Ї–Є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –Њ—В–ї–Є—З–∞—О—В—Б—П –њ—А–Њ—Б—В–Њ—В–Њ–є –≤ –Є—Б–њ–Њ–ї–љ–µ–љ–Є–Є –Є –і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О –љ–µ —В–Њ–ї—М–Ї–Њ –і–ї—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е —Г—З—А–µ–ґ–і–µ–љ–Є–є —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П, –Њ—Б–љ–∞—Й–µ–љ–љ–Њ—Б—В–Є –Є –≤–Љ–µ—Б—В–Є–Љ–Њ—Б—В–Є, –љ–Њ –Є –≤ –і–Њ–Љ–∞—И–љ–Є—Е –Є –і–∞–ґ–µ –њ–Њ–ї–µ–≤—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е.
–С–ї–∞–≥–Њ–і–∞—А—П —Д—Г–љ–і–∞–Љ–µ–љ—В–∞–ї—М–љ—Л–Љ —А–∞–±–Њ—В–∞–Љ –∞–Ї–∞–і–µ–Љ–Є–Ї–∞ –Р.–Ь. –£–≥–Њ–ї–µ–≤–∞ –≤ 1960 –≥. —Б–Њ–Ј–і–∞–µ—В—Б—П —В–µ–Њ—А–Є—П –Њ–± –∞–і–µ–Ї–≤–∞—В–љ–Њ–Љ –њ–Є—В–∞–љ–Є–Є [4]. –Т 1972 –≥–Њ–і—Г —А—Г—Б—Б–Ї–Є–є —Д–Є–Ј–Є–Њ–ї–Њ–≥ –Ѓ.–Ь. –У–∞–ї—М–њ–µ—А–Є–љ [5] –Њ—В–Ї—А—Л–ї –≥–µ—В–µ—А–Њ—Д–∞–Ј–љ–Њ–µ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є–µ, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н—В–Њ–є —А–∞–±–Њ—В—Л –±—Л–ї–Є —В–∞–Ї–ґ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –≤–∞–ґ–љ—Л–µ –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ—Б—В–Є –Њ–±–Љ–µ–љ–∞ –љ—Г—В—А–Є–µ–љ—В–∞–Љ–Є –Љ–µ–ґ–і—Г —Н–љ—В–µ—А–∞–ї—М–љ–Њ–є –Є –≤–љ—Г—В—А–µ–љ–љ–µ–є —Б—А–µ–і–Њ–є –Є –њ–Њ–Ї–∞–Ј–∞–љ–∞ —А–Њ–ї—М —Б–ї–Є–Ј–Є—Б—В—Л—Е –љ–∞–ї–Њ–ґ–µ–љ–Є–є. –Ш–Љ–µ–љ–љ–Њ —Н—В–Є —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –њ–Њ—Б–ї—Г–ґ–Є–ї–Є –Њ—Б–љ–Њ–≤–Њ–є –і–ї—П —Б–Њ–Ј–і–∞–љ–Є—П —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е —Б–Љ–µ—Б–µ–є –і–ї—П —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ –±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ–Љ—Г –≤–љ–µ–і—А–µ–љ–Є—О —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –≤ –Љ–µ–і–Є—Ж–Є–љ–µ. –Р–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е —А–∞–±–Њ—В Bristol J.B. et al. [6] –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ —Г —В–Њ–љ–Ї–Њ–≥–Њ –Ї–Є—И–µ—З–љ–Є–Ї–∞, –Ї–∞–Ї –Є —Г —Б–µ—А–і—Ж–∞, –Є–Љ–µ–µ—В—Б—П —А–µ–Ј–µ—А–≤–љ–∞—П —Н–љ–µ—А–≥–Є—П, –∞ –њ—А–Њ—Ж–µ—Б—Б—Л —Б–µ–Ї—А–µ—Ж–Є–Є –±–∞–ї–∞–љ—Б–Є—А—Г—О—В—Б—П –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ–Љ. –Ъ —В–Њ–Љ—Г –ґ–µ —Н—В–Є —Д—Г–љ–Ї—Ж–Є–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –∞–≤—В–Њ–љ–Њ–Љ–љ—Л –Њ—В –Љ–Њ—В–Њ—А–љ–Њ–—Н–≤–∞–Ї—Г–∞—В–Њ—А–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —В–Њ–љ–Ї—Г—О –Ї–Є—И–Ї—Г –і–ї—П –њ–Є—В–∞–љ–Є—П –і–∞–ґ–µ –і–Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї–Є.
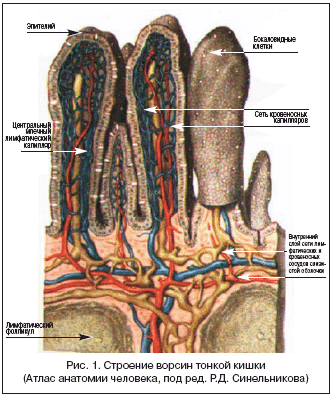
–Э–∞—З–Є–љ–∞—П —Б 80–—Е –≥–Њ–і–Њ–≤ XX –≤–µ–Ї–∞, –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –Є–љ—В–µ—А–µ—Б –Ї —Н–љ—В–µ—А–∞–ї—М–љ–Њ–Љ—Г –Ј–Њ–љ–і–Њ–≤–Њ–Љ—Г –њ–Є—В–∞–љ–Є—О –≤ —Б–≤–µ—В–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –Њ –Ї–Є—И–µ—З–љ–Є–Ї–µ, –Ї–∞–Ї –Є–љ—В–µ–≥—А–∞–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ, –Є–Љ–µ—О—Й–µ–Љ —Б–ї–µ–і—Г—О—Й–Є–µ —Д—Г–љ–Ї—Ж–Є–Є: 1) —Н–љ–і–Њ–Ї—А–Є–љ–љ—Г—О; 2) –Є–Љ–Љ—Г–љ–љ—Г—О; 3) –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї—Г—О; 4) –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї—Г—О; 5) –≥–Њ–Љ–µ–Њ—Б—В–∞—В–Є—З–µ—Б–Ї—Г—О; 6) –±–∞—А—М–µ—А–љ—Г—О. –Ю–і–љ–Њ–є –Є–Ј –≤–∞–ґ–љ—Л—Е —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е —Н—В–Є—Е —Д—Г–љ–Ї—Ж–Є–є —П–≤–ї—П–µ—В—Б—П —Ж–µ–ї–Њ—Б—В–љ–Њ—Б—В—М —Б–ї–Є–Ј–Є—Б—В–Њ–є –Ї–Є—И–µ—З–љ–Є–Ї–∞. –Ь–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Њ—Б–љ–Њ–≤–∞ —В–Ї–∞–љ–µ–≤–Њ–є –Љ–∞—Б—Б—Л —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є – —Н—В–Њ –ї–Є–Љ—Д–Њ–Є–і–љ–∞—П —В–Ї–∞–љ—М. –Я—А–Є–Љ–µ—А–љ–Њ 20% –Ї–ї–µ—В–Њ–Ї –≤ —Н–њ–Є—В–µ–ї–Є–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –њ—А–Є—Е–Њ–і–Є—В—Б—П –љ–∞ –ї–Є–Љ—Д–Њ—Ж–Є—В—Л. –І–Є—Б–ї–Њ –≤–љ—Г—В—А–Є—Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –≤ —Б—А–µ–і–љ–µ–Љ 21 –љ–∞ 100 —Н–љ—В–µ—А–Њ—Ж–Є—В–Њ–≤ (—А–Є—Б. 1), –њ–Њ—Н—В–Њ–Љ—Г —В–Њ–љ–Ї–∞—П –Ї–Є—И–Ї–∞ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П, –Ї–∞–Ї —Ж–µ–љ—В—А–∞–ї—М–љ—Л–є –Њ—А–≥–∞–љ –Т––Є–Љ–Љ—Г–љ–Є—В–µ—В–∞. –Ґ–∞–Ї–ґ–µ –≤ 1 –Љ–Љ3 —В–Ї–∞–љ–Є —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є —Б–Њ–і–µ—А–ґ–Є—В—Б—П –Њ–Ї–Њ–ї–Њ 430 —В—Л—Б—П—З –њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ —В–Њ–љ–Ї–∞—П –Ї–Є—И–Ї–∞ —П–≤–ї—П–µ—В—Б—П –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤. –Т –Ї–Є—И–Ї–µ –љ–∞—Е–Њ–і—П—В—Б—П –Ґ––ї–Є–Љ—Д–Њ—Ж–Є—В—Л –Є –Љ–∞–Ї—А–Њ—Д–∞–≥–Є, —Б–њ–Њ—Б–Њ–±–љ—Л–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Њ–≤–∞—В—М —Б –ї–Є–Љ—Д–Њ—Ж–Є—В–∞–Љ–Є, –≤—Л—А–∞–±–∞—В—Л–≤–∞—В—М –ї–Є–Ј–Њ—Ж–Є–Љ, –Є–љ—В–µ—А—Д–µ—А–Њ–љ [7].
–Я–Є—В–∞–љ–Є–µ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Ї–Є—И–µ—З–љ–Є–Ї–∞, —З—В–Њ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –±–∞–Ї—В–µ—А–Є–є, —Н–љ–і–Њ—В–Њ–Ї—Б–Є–љ–Њ–≤ –Є –∞–љ—В–Є–≥–µ–љ–Њ–≤ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ. –°—З–Є—В–∞–µ—В—Б—П, —З—В–Њ —Н—В–Њ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В, –Ї–Њ–≥–і–∞ —Д–∞–≥–Њ—Ж–Є—В—Л –Ј–∞—Е–≤–∞—В—Л–≤–∞—О—В –±–∞–Ї—В–µ—А–Є–Є, —В—А–∞–љ—Б–њ–Њ—А—В–Є—А—Г—О—В –Є—Е –≤ —В–Ї–∞–љ–Є –Ј–∞ –њ—А–µ–і–µ–ї–∞–Љ–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є, –±—Г–і—Г—З–Є –љ–µ –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –Є—Е —Д–∞–≥–Њ—Ж–Є—В–Є—А–Њ–≤–∞—В—М, –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞—О—В –±–∞–Ї—В–µ—А–Є–Є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–і–∞–≤–ї–µ–љ–Є—О –Њ–і–љ–Њ–≥–Њ –Є–ї–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –≤–Є–і–Њ–≤ –±–∞–Ї—В–µ—А–Є–є –Є –Є–Ј–±—Л—В–Њ—З–љ–Њ–Љ—Г —А–Њ—Б—В—Г –і—А—Г–≥–Є—Е, –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л, —З—А–µ–Ј–Љ–µ—А–љ—Л–є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є —А–Њ—Б—В –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ, —Б –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ –њ–Њ—Б–ї–µ–і–љ–Є—Е –≤ –ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є–µ —Г–Ј–ї—Л [8].
–Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—В –Є –Ј–∞—Й–Є—В–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, –∞–Ї—В–Є–≤–Є–Ј–Є—А—Г—О—Й–Є–µ—Б—П —Н–љ—В–µ—А–∞–ї—М–љ—Л–Љ –њ–Є—В–∞–љ–Є–µ–Љ [8]: 1) —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є–µ –Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є–Є; 2) –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–∞—П –Ј–∞—Й–Є—В–∞: –Ї–Є—И–µ—З–љ–∞—П –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї–∞, –≤—Л—А–∞–±–Њ—В–Ї–∞ —Б–ї–Є–Ј–Є, —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ–∞—П –і–µ—Б–Ї–≤–∞–Љ–∞—Ж–Є—П; 3) —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–µ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ—Л A, —Б–≤—П–Ј—Л–≤–∞—П—Б—М —Б –±–∞–Ї—В–µ—А–Є—П–Љ–Є, –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—В —А–∞–Ј–≤–Є—В–Є–µ –Љ–µ—Б—В–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞.
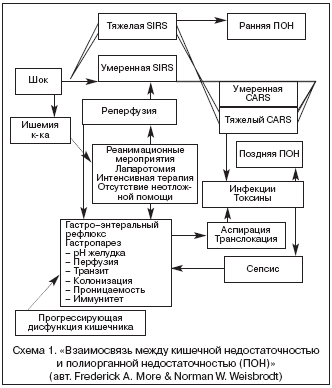
–Э–∞–±–ї—О–і–µ–љ–Є—П –Є —А–∞–±–Њ—В—Л –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е —Г—З–µ–љ—Л—Е –і–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ—А–Є –Ї–Є—И–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (—Б—Е–µ–Љ–∞ 1) —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Є—Б—В–Њ—Й–µ–љ–Є–µ —Н–љ—В–µ—А–Њ—Ж–Є—В–Њ–≤, –Љ–µ–љ—П–µ—В—Б—П –Љ–Є–Ї—А–Њ—Д–ї–Њ—А–∞ –Є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –Є—И–µ–Љ–Є—П —Б—В–µ–љ–Ї–Є –Ї–Є—И–Ї–Є, –∞ –њ–Њ—Б—В—Г–њ–∞—О—Й–Є–µ –њ–Є—В–∞—В–µ–ї—М–љ—Л–µ —Б—Г–±—Б—В—А–∞—В—Л —Б—В–Є–Љ—Г–ї–Є—А—Г—О—В —А–Њ—Б—В –Є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—О –Ї–ї–µ—В–Њ—З–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Ј–∞ —Б—З–µ—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤ –љ–µ–µ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П, –∞–Ї—В–Є–≤–Є—А—Г—О—В —Д–µ—А–Љ–µ–љ—В–∞—В–Є–≤–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ—Л—Е —Б–Њ–Ї–Њ–≤, –Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ—Л—Е –≥–Њ—А–Љ–Њ–љ–Њ–≤ –Є —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –Љ–µ–Ј–µ–љ—В–µ—А–Є–∞–ї—М–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї. –Т—Б–µ —Н—В–Є –њ–Њ–ї–Њ–ґ–µ–љ–Є—П –µ—Й–µ —А–∞–Ј –і–Њ–Ї–∞–Ј—Л–≤–∞—О—В —В–Њ, —З—В–Њ –Ї–Є—И–µ—З–љ–Є–Ї (—А–Є—Б. 2) – —Н—В–Њ –љ–µ —В–Њ–ї—М–Ї–Њ –Љ–µ—Б—В–Њ –≥–Є–і—А–Њ–ї–Є–Ј–∞ –њ–Њ—Б—В—Г–њ–∞—О—Й–Є—Е –љ—Г—В—А–Є–µ–љ—В–Њ–≤, –љ–Њ –Є –≤–∞–ґ–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–є –Њ—А–≥–∞–љ.
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, –Ї–∞–Ї –ї—О–±–Њ–є –Љ–µ—В–Њ–і–Є–Ї–Є —В–µ—А–∞–њ–Є–Є, –Є–Љ–µ–µ—В —Б–ї–µ–і—Г—О—Й–Є–µ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П:
– —И–Њ–Ї–Њ–≤–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ,
– —В—А–Њ–Љ–±–Њ–Ј –Љ–µ–Ј–µ–љ—В–µ—А–Є–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤,
– –≥–Є–њ–Њ–Ї—Б–Є—П – —А–∞–Ю2 < 50 –Љ–Љ —А—В.—Б—В.,
– –і—Л—Е–∞—В–µ–ї—М–љ—Л–є –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–є –∞—Ж–Є–і–Њ–Ј
—Б —А–∞–Э < 7,2 –Љ–Љ–Њ–ї—М/–ї; —А–∞–°–Ю2 > 80 –Љ–Љ —А—В.—Б—В.,
– –њ–µ—А—Д–Њ—А–∞—Ж–Є—П –Ї–Є—И–µ—З–љ–Є–Ї–∞,
– –Њ—Б—В—А–Њ–µ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–µ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ,
– –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–∞—П –Ї–Є—И–µ—З–љ–∞—П –љ–µ–њ—А–Њ—Е–Њ–і–Є–Љ–Њ—Б—В—М.
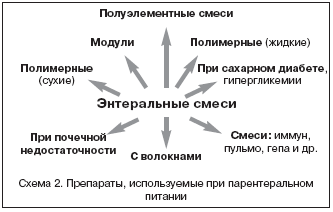
–Я—А–Є —Н—В–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ. –Ю—Б–љ–Њ–≤–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П —П–≤–ї—П–µ—В—Б—П –љ—Г—В—А–Є—В–Є–≤–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Є–ї–Є –Ј–∞—Й–Є—В–∞ –Њ—В —А–∞–Ј–≤–Є—В–Є—П –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ф–ї—П —В–Њ–≥–Њ —З—В–Њ–±—Л —Г—Б–њ–µ—И–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤—Л–±—А–∞—В—М –њ–Є—В–∞—В–µ–ї—М–љ—Г—О —Б–Љ–µ—Б—М. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤—Л–±–Њ—А –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –†–Њ—Б—Б–Є–Є –≤–µ—Б—М–Љ–∞ —И–Є—А–Њ–Ї (—Б—Е–µ–Љ–∞ 2), —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Н—В—Г –Љ–µ—В–Њ–і–Є–Ї—Г –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е.
–•–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—П —Н—В–Є —Б–Љ–µ—Б–Є –і–ї—П —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –Ї–∞–ґ–і–Њ–є –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –Љ–Њ–ґ–µ—В –њ–Њ—В—А–µ–±–Њ–≤–∞—В—М—Б—П –љ–µ –Њ–і–Є–љ –≤–Є–і –њ—А–µ–њ–∞—А–∞—В–∞, –∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ, –њ–Њ—Н—В–Њ–Љ—Г –≤ –Ї–ї–Є–љ–Є–Ї–µ –ґ–µ–ї–∞—В–µ–ї—М–љ–Њ –Є–Љ–µ—В—М –≤–µ—Б—М —Б–њ–µ–Ї—В—А —Н–љ—В–µ—А–∞–ї—М–љ—Л—Е —Б–Љ–µ—Б–µ–є.
–Я–Њ–ї–Є–Љ–µ—А–љ—Л–µ (—Б—Г—Е–Є–µ) –Є –ґ–Є–і–Ї–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ—Л–µ —Б–Љ–µ—Б–Є –і–Њ–ї–ґ–љ—Л —Б–Њ–і–µ—А–ґ–∞—В—М –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–µ–ї–Ї–Њ–≤, –ґ–Є—А–Њ–≤, —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –≤–Є—В–∞–Љ–Є–љ–Њ–≤, –Љ–Є–Ї—А–Њ– –Є –Љ–∞–Ї—А–Њ—Н–ї–µ–Љ–µ–љ—В–Њ–≤. –Ю—Б–љ–Њ–≤–љ–Њ–µ –Њ—В–ї–Є—З–Є–µ –Љ–µ–ґ–і—Г —Н—В–Є–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ —В–Њ–Љ, —З—В–Њ –ґ–Є–і–Ї–Є–µ –њ–Њ–ї–Є–Љ–µ—А–љ—Л–µ —Б–Љ–µ—Б–Є –љ–µ —В—А–µ–±—Г—О—В —А–∞–Ј–≤–µ–і–µ–љ–Є—П –≤–Њ–і–Њ–є –Є –≥–Њ—В–Њ–≤—Л –Ї —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—О. –°—Г—Е–Є–µ –њ–Њ–ї–Є–Љ–µ—А–љ—Л–µ —Б–Љ–µ—Б–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —А–∞–Ј–≤–µ—Б—В–Є –≤–Њ–і–Њ–є –њ–µ—А–µ–і –≤–≤–µ–і–µ–љ–Є–µ–Љ –Є–ї–Є —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е –±–Њ–ї–µ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–Љ–Є –Љ–Њ–≥—Г—В –Њ–Ї–∞–Ј–∞—В—М—Б—П —Б—Г—Е–Є–µ –њ–Њ–ї–Є–Љ–µ—А–љ—Л–µ —Б–Љ–µ—Б–Є, —В–∞–Ї –Ї–∞–Ї —А–∞–Ј–≤–µ–і–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е –Љ–Њ–ґ–µ—В –±—Л—В—М —А–∞–Ј–ї–Є—З–љ—Л–Љ – 0,25/0,5/0,75 –Ї–Ї–∞–ї/–Љ–ї, –∞ —Н—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ–±–Є—В—М—Б—П –±–Њ–ї–µ–µ –њ–ї–∞–≤–љ–Њ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤–≤–Њ–і–Є–Љ–Њ–є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–є —Б–Љ–µ—Б–Є –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ —Н—В–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ.
–Я–Њ–ї—Г—Н–ї–µ–Љ–µ–љ—В–љ—Л–µ —Н–љ—В–µ—А–∞–ї—М–љ—Л–µ —Б–Љ–µ—Б–Є –≤ —Ж–µ–ї–Њ–Љ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є —Б—В–µ–њ–µ–љ—М—О –≥–Є–і—А–Њ–ї–Є–Ј–∞. –Ь–Њ–і—Г–ї—М–љ—Л–µ —Б–Љ–µ—Б–Є —Б–Њ–і–µ—А–ґ–∞—В –Ї–∞–Ї—Г—О–—В–Њ –Њ–і–љ—Г —Б–Њ—Б—В–∞–≤–ї—П—О—Й—Г—О: –±–µ–ї–Њ–Ї, —Г–≥–ї–µ–≤–Њ–і—Л –Є –і—А. –Ю–±–ї–∞—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і—А—Г–≥–Є—Е —Б–Љ–µ—Б–µ–є —Г–Ї–∞–Ј–∞–љ–∞ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –Є—Е –љ–∞–Ј–≤–∞–љ–Є–Є.
–Ю—Б–љ–Њ–≤–љ—Л–µ –Љ–µ—В–Њ–і–Є–Ї–Є –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –њ–Њ–і–і–µ—А–ґ–Ї–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П:
• –°–Є–њ–Є–љ–≥ (sip feeding) – –њ—А–Є–µ–Љ —Н–љ—В–µ—А–∞–ї—М–љ—Л—Е —Б–Љ–µ—Б–µ–є —З–µ—А–µ–Ј —В—А—Г–±–Њ—З–Ї—Г –Љ–µ–ї–Ї–Є–Љ–Є –≥–ї–Њ—В–Ї–∞–Љ–Є
• –°–Њ—З–µ—В–∞–љ–Є–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–є –і–Є–µ—В—Л —Б –њ—А–Є–µ–Љ–Њ–Љ —Н–љ—В–µ—А–∞–ї—М–љ—Л—Е —Б–Љ–µ—Б–µ–є
• –Ю–±–Њ–≥–∞—Й–µ–љ–Є–µ –љ–∞—В—Г—А–∞–ї—М–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ —Н–љ—В–µ—А–∞–ї—М–љ—Л–Љ–Є —Б–Љ–µ—Б—П–Љ–Є ± –њ–Њ–і–і–µ—А–ґ–Ї–∞ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л–Љ –њ–Є—В–∞–љ–Є–µ–Љ
• –°–Њ—З–µ—В–∞–љ–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –Ј–Њ–љ–і–Њ–≤–Њ–≥–Њ –Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П
• –≠–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Ј–Њ–љ–і–Њ–≤–Њ–µ –њ–Є—В–∞–љ–Є–µ: —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Њ–µ, –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Њ–µ, –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ, –±–Њ–ї—О—Б–љ–Њ–µ.
–Т—Л–±–Њ—А –Љ–µ—В–Њ–і–Є–Ї–Є —В–∞–Ї–ґ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Б–Є–њ–Є–љ–≥ –Є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Ј–Њ–љ–і–Њ–≤–Њ–µ –њ–Є—В–∞–љ–Є–µ. –Т —Ж–µ–ї–Њ–Љ –Љ–µ—В–Њ–і–Є–Ї–∞ —Б–Є–њ–Є–љ–≥–∞ –њ—А–Њ—Б—В–∞ –Є –њ–Њ–љ—П—В–љ–∞, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –Ј–Њ–љ–і–Њ–≤–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П —В—А–µ–±—Г–µ—В –њ–ї–∞–≤–љ–Њ—Б—В–Є –Є —З–µ—В–Ї–Њ—Б—В–Є –Є –љ–µ —В–µ—А–њ–Є—В —Б–њ–µ—И–Ї–Є. –Т —Ж–µ–ї–Њ–Љ –∞–ї–≥–Њ—А–Є—В–Љ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –Ј–Њ–љ–і–Њ–≤–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П (–≠–Ч–Я) –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –≤ —В–∞–±–ї–Є—Ж–µ 1.
–Ю—Ж–µ–љ–Ї–∞ –≤—Б–∞—Б—Л–≤–∞—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –Њ—Б–љ–Њ–≤–∞–љ–∞ –љ–∞ –≤–≤–µ–і–µ–љ–Є–Є –≤ –Ј–Њ–љ–і —Н–љ—В–µ—А–∞–ї—М–љ—Л—Е —Б–Љ–µ—Б–µ–є —Б–Њ —Б–Ї–Њ—А–Њ—Б—В—М—О 20 –Љ–ї/—З (–і–ї—П —Н—В–Њ–≥–Њ –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Б—В–∞–љ–і–∞—А—В–љ—Л–µ –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Л–µ —Б–Є—Б—В–µ–Љ—Л –Р–Ю «–Ъ—Г—А–≥–∞–љ—Б–Є–љ—В–µ–Ј» –Є–ї–Є «Exadrop», –Є–ї–Є –њ–µ—А–Є—Б—В–∞–ї—М—В–Є—З–µ—Б–Ї–Є–µ –љ–∞—Б–Њ—Б—Л), –Њ–±—К–µ–Љ–Њ–Љ 400 –Љ–ї. –Я–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –≤ –Ј–Њ–љ–і —Г–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞ —Н–љ—В–µ—А–∞–ї—М–љ—Л—Е —Б–Љ–µ—Б–µ–є –Ј–Њ–љ–і –њ–µ—А–µ–Ї—А—Л–≤–∞—О—В –љ–∞ 30–40 –Љ–Є–љ—Г—В. –Ч–∞—В–µ–Љ –Ј–Њ–љ–і –Њ—В–Ї—А—Л–≤–∞—О—В –Є –µ—Б–ї–Є —Н–≤–∞–Ї—Г–Є—А—Г–µ–Љ–Њ–µ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–µ –Є–Ј –Ј–Њ–љ–і–∞ –Љ–µ–љ–µ–µ 50% –Њ—В –Њ–±—К–µ–Љ–∞ –≤–≤–Њ–і–Є–Љ–Њ–є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–є —Б–Љ–µ—Б–Є, —В–Њ –њ—А–Њ–і–Њ–ї–ґ–∞—О—В —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Ј–Њ–љ–і–Њ–≤–Њ–µ –њ–Є—В–∞–љ–Є–µ. –Т —В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ —Н–≤–∞–Ї—Г–Є—А—Г–µ–Љ–Њ–µ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–µ –Є–Ј –Ј–Њ–љ–і–∞ –±–Њ–ї–µ–µ 50% –Њ—В –Њ–±—К–µ–Љ–∞ –≤–≤–Њ–і–Є–Љ–Њ–є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–є —Б–Љ–µ—Б–Є, —В–Њ –њ–µ—А–µ—Е–Њ–і—П—В –љ–∞ «–Ї–Є—И–µ—З–љ—Л–є –ї–∞–≤–∞–ґ»: 2 –ї–Є—В—А–∞ —Н–љ—В–µ—А–∞–ї—М–љ—Л—Е —А–∞—Б—В–≤–Њ—А–Њ–≤ –≤–≤–Њ–і—П—В –Ї–∞–њ–µ–ї—М–љ–Њ, —З–µ—А–µ–Ј –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Л–є –Ї–∞–љ–∞–ї –і–≤—Г—Е–Ї–∞–љ–∞–ї—М–љ–Њ–≥–Њ –Ј–Њ–љ–і–∞, –Ї –∞—Б–њ–Є—А–Є—А—Г–µ–Љ–Њ–Љ—Г –Ї–∞–љ–∞–ї—Г –њ–Њ–і—Б–Њ–µ–і–Є–љ—П—О—В –Њ—В—Б–Њ—Б «–Ю–Я – 01», —Б —А–∞–Ј—А–µ—И–µ–љ–Є–µ–Љ 10–15 —Б–Љ –≤–Њ–і–љ–Њ–≥–Њ —Б—В–Њ–ї–±–∞ [8].
–С–µ—А–ї–∞–Љ–Є–љ – –Љ–Њ–і—Г–ї—П—А – –Љ–Њ–ї–Њ—З–љ–Њ–—Б–Њ–µ–≤–∞—П —Н–љ—В–µ—А–∞–ї—М–љ–∞—П —Б–Љ–µ—Б—М, —Б–Њ–і–µ—А–ґ–Є—В —А–∞—Б—В–Є—В–µ–ї—М–љ—Л–µ –Є –ґ–Є–≤–Њ—В–љ—Л–µ –±–µ–ї–Ї–Є –≤ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –њ—А–Њ–њ–Њ—А—Ж–Є–Є 50%/50%, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–µ–є –њ–Њ–ї–љ–Њ—Б—В—М—О –Њ–±–µ—Б–њ–µ—З–Є—В—М –њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ:
– —Б–Њ–і–µ—А–ґ–Є—В –Ї–∞–Ї —А–∞—Б—В–Є—В–µ–ї—М–љ—Л–є, —В–∞–Ї –Є –Љ–Њ–ї–Њ—З–љ—Л–є –±–µ–ї–Ї–Є –≤ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–Є 50:50;
– –Є–Ј –ґ–Є—А–Њ–≤ 77% —Б–Њ—Б—В–∞–≤–ї—П—О—В –њ–Њ–ї–Є–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л–µ –ґ–Є—А–љ—Л–µ –Ї–Є—Б–ї–Њ—В—Л, –≤ —В–Њ–Љ —З–Є—Б–ї–µ 50% – –ї–Є–љ–Њ–ї–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, —З—В–Њ —Г–ї—Г—З—И–∞–µ—В –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –ґ–Є—А–∞;
– —Б–Њ–і–µ—А–ґ–Є—В –≤—Б–µ –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–µ –Љ–∞–Ї—А–Њ– –Є –Љ–Є–Ї—А–Њ—Н–ї–µ–Љ–µ–љ—В—Л;
– –Є–Љ–µ–µ—В –≤ —Б–Њ—Б—В–∞–≤–µ –≤—Б–µ –≤–Є—В–∞–Љ–Є–љ—Л: 9 –≤–Њ–і–Њ—А–∞—Б—В–≤–Њ—А–Є–Љ—Л—Е –Є 4 –ґ–Є—А–Њ—А–∞—Б—В–≤–Њ—А–Є–Љ—Л—Е;
– –Њ—Б–Љ–Њ–ї—П—А–љ–Њ—Б—В—М 10–20% —А–∞—Б—В–≤–Њ—А–Њ–≤ –і–∞–љ–љ–Њ–є —Б–Љ–µ—Б–Є –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 300–350 –Љ–Њ—Б–Љ/–ї, —В.–µ. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Њ—Б–Љ–Њ–ї—П—А–љ–Њ—Б—В–Є –њ–ї–∞–Ј–Љ—Л.
–≠—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Є–Ј–Њ—В–Њ–љ–Є—З–µ—Б–Ї–Њ–µ –њ–Є—В–∞–љ–Є–µ, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–µ–µ –Є–Ј–±–µ–ґ–∞—В—М –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –≤—Л—Б–Њ–Ї–Њ–Њ—Б–Љ–Њ–ї—П—А–љ—Л—Е —Б–Љ–µ—Б–µ–є (—В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, –і–Є–∞—А–µ—П, —Б—Г–і–Њ—А–Њ–≥–Є).
–С–µ—А–ї–∞–Љ–Є–љ:
1. –љ–µ —Б–Њ–і–µ—А–ґ–Є—В –≥–ї—О—В–µ–љ–∞, –ї–∞–Ї—В–Њ–Ј—Л, —Б–∞—Е–∞—А–Њ–Ј—Л;
2. –Њ—В—Б—Г—В—Б—В–≤–Є–µ –њ–Є—Й–µ–≤—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ —Б–Љ–µ—Б–Є;
3. –Њ–±—Й–∞—П —Н–љ–µ—А–≥–Њ—Ж–µ–љ–љ–Њ—Б—В—М —Б–Љ–µ—Б–Є 1620 –Ї–Ї–∞–ї (360 –≥ – –Њ–і–љ–∞ —Г–њ–∞–Ї–Њ–≤–Ї–∞).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П (–С–µ—А–ї–∞–Љ–Є–љ) —П–≤–ї—П–µ—В—Б—П –њ—А–Њ—Б—В—Л–Љ –Є –і–Њ—Б—В—Г–њ–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ, –Њ–і–љ–∞–Ї–Њ —В—А–µ–±—Г–µ—В —Б–Њ–±–ї—О–і–µ–љ–Є—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –њ—А–∞–≤–Є–ї.
–Ш–Ј –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є—П –і–Њ–Ї–∞–Ј–∞–љ–љ—Л—Е –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –≤–ї–Є—П–љ–Є—П —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –љ–∞ –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е —Е–Њ—В–µ–ї–Њ—Б—М –±—Л –Њ—В–Љ–µ—В–Є—В—М —Б–ї–µ–і—Г—О—Й–Є–µ:
1. –†–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –њ—А–Њ—Д. –Ь–µ–≥—М—О–і–Њ–Љ –≤ 1988 –≥–Њ–і—Г, –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Є –љ—Г—В—А–Є—В–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О, –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –њ–Њ—Б–ї–µ –њ–ї–∞–љ–Њ–≤—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –Њ–њ—Г—Е–Њ–ї–µ–є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –±—Л–ї–∞ –≤ 6 —А–∞–Ј –љ–Є–ґ–µ, –∞ –њ—А–Њ—Ж–µ–љ—В –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ 2,5 —А–∞–Ј–∞ –Љ–µ–љ—М—И–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –±–Њ–ї—М–љ—Л–Љ–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л, –Ї–Њ—В–Њ—А—Л–Љ –љ–µ –њ—А–Њ–≤–Њ–і–Є–ї–Є –∞–і–µ–Ї–≤–∞—В–љ—Г—О –љ—Г—В—А–Є—Ж–Є–Њ–љ–љ—Г—О —В–µ—А–∞–њ–Є—О [1].
2. –°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –Х–°–ЮG –≤ 21 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є (–Є–Ј –љ–Є—Е 16 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е) —Н—Д—Д–µ–Ї—В—Л –њ—А–µ–і–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –љ—Г—В—А–Є—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Њ—П–≤–Є–ї–Є—Б—М –≤ —Б–љ–Є–ґ–µ–љ–Є–Є —З–∞—Б—В–Њ—В—Л —Б–µ–њ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —Б–љ–Є–ґ–µ–љ–Є–Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є [1].
3. –Я–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–∞—П –љ—Г—В—А–Є—В–Є–≤–љ–∞—П —В–µ—А–∞–њ–Є—П –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –∞–Ј–Њ—В–Є—Б—В—Л–є –±–∞–ї–∞–љ—Б, —Б–љ–Є–ґ–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞ 36%, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞, —Г—А–Њ–≤–љ—П –∞–ї—М–±—Г–Љ–Є–љ–∞, —З–Є—Б–ї–∞ –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є —Г –љ–µ–Њ–њ–µ—А–∞–±–µ–ї—М–љ—Л—Е –±–Њ–ї—М–љ—Л—Е [1].
4. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ—Г—В—А–Є—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ –і–Њ–Љ–∞—И–љ–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В, –њ–Њ –і–∞–љ–љ—Л–Љ Italian Society of Parenteral and Enteral Nutrition 2003 –≥., —Г–≤–µ–ї–Є—З–µ–љ–Є—О –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є –і–Њ 4 –Љ–µ—Б—П—Ж–µ–≤ —Г 12–13% –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е —Б IV —Б—В–∞–і–Є–µ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [1].
5. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞ 837 –±–Њ–ї—М–љ—Л—Е (Lewis et al., 2001) [1], –њ–Њ–ї—Г—З–Є–≤—И–Є—Е —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Ј–Њ–љ–і–Њ–≤–Њ–µ –њ–Є—В–∞–љ–Є–µ –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ–Њ –њ–Њ–≤–Њ–і—Г –Њ–њ—Г—Е–Њ–ї–µ–є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –і–Њ–Ї–∞–Ј–∞–љ–Њ: —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ —З–Є—Б–ї–∞ –Ї–Њ–є–Ї–Њ––і–љ–µ–є, –љ–µ—Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ—Б—В–µ–є —И–≤–Њ–≤ –∞–љ–∞—Б—В–Њ–Љ–Њ–Ј–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є–µ —А–∞–љ–µ–≤–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є, –њ–љ–µ–≤–Љ–Њ–љ–Є–є, –Є–љ—В—А–∞–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л—Е –∞–±—Б—Ж–µ—Б—Б–Њ–≤, –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є.
–Т—Л–≤–Њ–і. –Т–Њ–њ—А–Њ—Б –Њ —В–Њ–Љ, —Б—В–Њ–Є—В –ї–Є –њ—А–Є–Љ–µ–љ—П—В—М —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –≤ –Њ–љ–Ї–Њ–ї–Њ–≥–Є–Є, —А–µ—И–µ–љ –Њ–і–љ–Њ–Ј–љ–∞—З–љ–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є. –Э–Њ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М –љ–∞–ї–Є—З–Є–µ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є, –њ—А–Њ–≤–Њ–і–Є—В—М –∞–і–µ–Ї–≤–∞—В–љ—Л–є –≤—Л–±–Њ—А –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –Љ–µ—В–Њ–і–Є–Ї–Є, —Б–Њ–±–ї—О–і–∞—В—М –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є–є. –Я—А–Є —Н—В–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –њ–Њ–Љ–Њ–ґ–µ—В –≤—А–∞—З—Г––Њ–љ–Ї–Њ–ї–Њ–≥—Г –Ї–Њ—А—А–Є–≥–Є—А–Њ–≤–∞—В—М –љ—Г—В—А–Є—В–Є–≤–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Є–ї–Є –Ј–∞—Й–Є—Й–∞—В—М –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ –Њ—В —А–∞–Ј–≤–Є—В–Є—П –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, —З—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —З–Є—Б–ї–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –ї–µ—З–µ–љ–Є–µ–Љ –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Clinical nutrition, 4th edition, 2004
2. –°–љ–µ–≥–Њ–≤–Њ–є –Р.–Т. / –Ъ–∞–љ–і–Є–і–∞—В—Б–Ї–∞—П –і–Є—Б—Б., 2004
3. –Ы—П—Й–µ–љ–Ї–Њ –Ѓ.–Э. / –Ю—Б–љ–Њ–≤—Л —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, 2001
4. –£–≥–Њ–ї–µ–≤ –Р.–Ь. / –§–Є–Ј–Є–Њ–ї–Њ–≥–Є—П –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П, –Ы––љ–∞—Г–Ї–∞, 1974, 761 —Б.
5. –У–∞–ї—М–њ–µ—А–Є–љ –Ѓ.–Ь. / –Я–Є—Й–µ–≤–∞—А–µ–љ–Є–µ –Є –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј, –Ь––љ–∞—Г–Ї–∞, 1986, 303 —Б.
6. Bristol J.B. et al. / Postoperative adoptation of small intestine, World Journal of Surgery, Vol.9, вДЦ 6, —А.825–832
7. –Ъ–Њ—Б—В—О—З–µ–љ–Ї–Њ –Р.–Ы. / –≠–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –≤ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ–µ, –°–Я–±, –°–њ–µ—Ж.–ї–Є—В.–1996, 392 —Б.
8. –Я–Њ–њ–Њ–≤–∞ –Ґ.–°. / –Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –≤ —Е–Є—А—Г—А–≥–Є–Є, –Ь.:–Ь––°–Ш–Ґ–Ш, 1996, 221 —Б.
9. –°–Є–љ–µ–ї—М–љ–Є–Ї–Њ–≤ –†.–Ф. / –Р—В–ї–∞—Б –∞–љ–∞—В–Њ–Љ–Є–Є —З–µ–ї–Њ–≤–µ–Ї–∞, II —В–Њ–Љ, –Ь–Њ—Б–Ї–≤–∞, 1966








.gif)



