Согласно современным представлениям, любая ОРВИ, сопровождающаяся ринологическими симптомами, является острым вирусным риносинуситом. Острый вирусный риносинусит, как и большинство острых респираторно-вирусных инфекций, имеет склонность к полному саморазрешению заболевания в течение 5–7 дней. Риск развития острого бактериального риносинусита в общей популяции находится на уровне 2–5%. При этом авторами Европейского позиционного документа по вопросам риносинуситов и полипоза (EP3OS) были разработаны четкие критерии для обоснования постановки диагноза «острый бактериальный риносинусит». Данные критерии включают в себя обязательное наличие у пациента 3 и более симптомов, к которым относятся:
• наличие гнойного отделяемого из полости носа;
• лихорадочная реакция ≥38,0°С;
• фасциальные боли;
• наличие «второй волны» в клиническом течении заболевания;
• изменение в клиническом анализе крови (ускорение скорости оседания эритроцитов (СОЭ) и повышение показателя C-реактивного белка).
Если у пациента отмечается усиление выраженности ринологических симптомов спустя 5 дней от начала заболевания или симптомы сохраняются более 10 дней (с полным разрешением в течение 12 нед.), при отсутствии обоснований для констатации бактериальной этиологии ОРС, авторами EP3OS рекомендован диагноз «острый поствирусный риносинусит» [1].
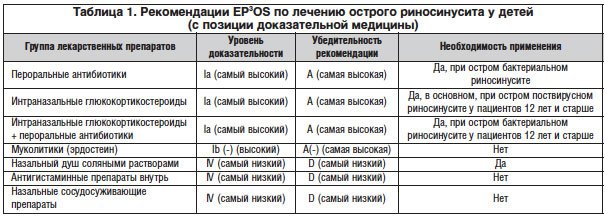
Данная классификация ОРС во многом определяет рекомендации EP3OS по лечению этой патологии у детей (табл. 1). Данные рекомендации, представленные с позиции доказательной медицины, очерчивают четкую границу использования системной антибактериальной терапии (только при остром бактериальном риносинусите), напоминают об актуальности применения назального душа соляными растворами с целью облегчения эвакуации секрета из полости носа (независимо от формы риносинусита) и указывают на главенствующую роль противовоспалительной терапии в виде интраназальных глюкокортикостероидов (ИнГКС) в лечении поствирусного и бактериального риносинусита у детей 12 лет и старше [1]. Однако авторы EP3OS в своих рекомендациях по лечению ОРС у детей не дают ответов на ряд вопросов. Так, остается непонятным, какие препараты следует назначать пациентам младше 12 лет с поствирусным ОРС. Согласно рекомендациям EP3OS, это только назальный душ соляными растворами, что, очевидно, не будет адекватным лечением при наличии у пациента выраженной гиперсекреции и/или назальной обструкции. Без ответа остается и вопрос о возможностях симптоматической терапии острого вирусного риносинусита у детей, при том, что в отечественной литературе существует достаточное количество клинических исследований, доказывающих эффективность и безопасность современных назальных спреев имидазолинов (оксиметазолина и ксилометазолина) в купировании симптома назальной обструкции [2–4].
Достаточно спорными выглядят и рекомендации авторов EP3OS отказаться от использования муколитических препаратов, если учесть, что обоснованием для данного утверждения явился результат лишь одного клинического исследования препарата эрдостеина, являющегося далеко не лучшим с точки зрения фармакокинетики представителем неферментных муколитических препаратов. В противовес данному утверждению в России за последние 10 лет был проведен ряд рандомизированных клинических исследований, доказавших эффективность топических форм N-ацетилцистеина (назальных спреев и ингаляционной терапии) в лечении поствирусных и бактериальных риносинуситов у детей [5–7]. Также непонятно большинству отечественных специалистов отсутствие при рассмотрении вопроса терапии ОРС в педиатрической практике такого класса препаратов, как фитотерапевтические лекарственные средства с секретолитической активностью [5]. И это при том, что в рекомендациях EP3OS по лечению ОРС у лиц старше 18 лет фитотерапевтические лекарственные средства с секретолитической активностью рекомендованы к применению при вирусных и поствирусных формах риносинуситов с высокой степенью достоверности результатов (Ib) при высочайшем уровне рекомендаций (А) [1].
Одним из представителей фитопрепаратов с секретолитической активностью является миртол стандартизированный, представляющий собой комплекс натуральных эфирных масел, полученных в ходе многоступенчатой дистилляции. Точность дозирования действующего вещества в каждой капсуле гарантирована за счет стандартизации миртола по содержанию трех монотерпенов: 1,8-цинеола, d-лимонена и α-пинена. Данные монотерпены в первую очередь являются биологическими маркерами и не охватывают всего спектра фармакологических действий. После приема внутрь капсулы, покрытой кишечнорастворимой оболочкой, ее содержимое всасывается в тонкой кишке и частично выводится через дыхательные пути, где проявляет секретолитические и секретомоторные свойства [8–13].
По данным 98 доклинических исследований и 27 рандомизированных клинических исследований, включивших более 6200 пациентов разных возрастных групп, в т. ч. и детей, было доказано, что препараты миртола обладают выраженным секретолитическим (на 32% превосходя результаты контрольной группы) и секретомоторным действием, облегчая эвакуацию патологического секрета из полости носа и околоносовых пазух [8, 9]. Возможно, не менее важным в патогенетической терапии ОРС у детей до 12 лет и других групп пациентов, которые по тем или иным причинам не имеют возможность применять ИнГКС, может явиться противовоспалительная активность препарата. Данный эффект обеспечивается за счет дозозависимого снижения концентрации лейкотриенов (LTC4/D4/E4) и простагландина Е2 [11]. В одной из экспериментальных работ было показано, что при воспалительном процессе действие миртола стандартизированного нейтрализует агрессивные свободные радикалы кислорода и блокирует активирование лейкоцитов [10].
Также результаты последних исследований установили, что прием препарата миртола стандартизированного приводит к снижению высвобождения гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) на 35,7% и умеренному снижению интерлейкина-8 (IL-8) и фактора некроза опухоли-альфа (TNF-a), что обусловливает противовоспалительную и антиоксидантную активность [12].
Одним из наглядных примеров высокой эффективности миртола стандартизированного в лечении ОРС стал результат рандомизированного плацебо-контролируемого мультицентрового исследования, проведенного группой немецких врачей в университете Гамбурга (Германия). В исследовании принял участие 331 пациент с клиникой ОРС. Пациенты основной группы получали внутрь миртол стандартизированный в капсуле (по 300 мг) 4 р./сут в течение 6±2 сут. Анализ результатов лечения продемонстрировал достоверно менее выраженные клинические симптомы риносинусита в основной группе по сравнению с группой, получавшей плацебо. При этом необходимость дополнительного применения антибиотика в основной группе составила 23% против 40% в группе контроля [13].
Интересен результат одного из отечественных сравнительных исследований препарата миртола стандартизированного. В данную работу были включены 24 пациента с ОРС. 11 человек в основной группе в комплексном лечении риносинусита получали внутрь препарат миртола (по 300 мг 4 р./сут) в течение 10 дней. В группе контроля в качестве муколитической терапии использовался препарат N-ацетилцистеина внутрь по 200 мг 3 р./сут. В результате терапии уже на 3-й день лечения у пациентов, принимавших миртол стандартизированный (ГелоМиртол® форте), стала заметна явная тенденция к выздоровлению (9 из 11 человек), которая оказалась несколько более выраженной, чем в случае приема ацетилцистеина. Что касается признаков исчезновения симптоматики, субъективная оценка эффективности выявила статистически значимые различия между методами лечения на 7-й (p=0,01) и 10-й (p=0,01) дни терапии в пользу миртола стандартизированного. Также при проведении на 20-й день лечения повторного рентгеновского исследования околоносовых пазух автор работы установила статистически значимое изменение рентгенологических результатов анализа состояния околоносовых пазух в пользу миртола стандартизированного (p<0,05).
Отдельным вопросом являются клинические исследования в педиатрической практике. Так, в мультицентровом постмаркетинговом исследовании контролировались изменение симптоматики и переносимость миртола стандартизированного у 511 детей в возрасте от 3 до 17 лет с острым и хроническим синуситом и бронхитом, а также с синубронхиальным синдромом. Из них исследователи выделили 128 детей с ОРС, которые получали миртол стандартизированный в дозе 120 и 300 мг (в зависимости от возраста и массы тела). Все контролируемые в ходе исследования симптомы и клинические признаки показали значительное улучшение. Доля детей, свободных от ключевых симптомов/признаков острого синусита, таких как боль при надавливании в точках выхода нерва, головная боль и боль в придаточных пазухах носа при поколачивании, всегда превышала 95%. Эти данные коррелируют с общей оценкой эффективности всеми участниками исследования: лечащие врачи оценивали эффективность терапии миртолом стандартизированным как «очень хорошую» или «хорошую» в 91,0% случаев, дети оценивали ее подобным же образом в 77,2% наблюдений, а их родители – в 85,5% случаев [15].
Таким образом, исходя из вышеизложенных данных, можно говорить о возможности применения фитотерапевтических лекарственных средств, в частности препаратов миртола стандартизированного, в лечении ОРС. С учетом выраженного секретолитического и секретомоторного действия, а также противовоспалительной активности препараты миртола стандартизированного можно рекомендовать в качестве средства терапии поствирусного риносинусита у детей старше 6 лет. Возможное применение с антибактериальными препаратами дает возможность использовать препараты миртола стандартизированного и для лечения острого бактериального риносинусита. При этом есть необходимость дальнейшего изучения эффективности и безопасности препаратов миртола стандартизированного в лечении ОРС у детей, что требует проведения клинических исследований в будущем.
Литература
1. Fokkens W., Lund V., Mullol J. et al. European position paper on rhinosinusitis and nasal polyps 2012 (EP3OS) // Rhinology. 2012. Vol.50(23). P. 1–299.
2. Заплатников А.Л. Топические деконгестанты в педиатрической практике: безопасность и клиническая эффективность // Педиатрия. 2006. № 6. С. 69–75.
3. Тулупов Д.А., Карпова Е.П. О роли назальных сосудосуживающих препаратов в симптоматическом лечении острых риносинуситов у детей // Российская ринология. 2011. № 2. С. 50.
4. Карпова Е.П., Тулупов Д.А. О безопасности применения назальных сосудосуживающих препаратов в педиатрической практике // Российская ринология. 2014. № 1. С.12–14.
5. Рязанцев С.В. Сравнение российских стандартов лечения острых синуситов с международной программой EPOS // Consilium medicum. 2008. № 10. С.87–90.
6. Колосова Н.Г., Геппе Н.А. Терапия небулайзерами в педиатрической практике // РМЖ. 2011. № 8. С. 514–518.
7. Карпова Е.П., Тулупов Д.А. О возможности небулайзерной терапии в лечении острых риносинуситов у детей // Российская оториноларингология. 2013. № 65(4). С. 160–163.
8. Behrbohm H., Kaschke O., Sydow K. Effect of the phytogenic secretolytic drug Gelomyrtol forte on mucociliary clearance of the maxillary sinus // Laryngorhinootologie. 1995. Vol. 74 (12). P. 733–737.
9. Zimmermann T., Seiberling M., Thomann P., Karabelnik D. The relative bioavailability and pharmacokinetics of standardized myrtol // Arzneimittelforschung. 1995. Vol. 45 (11). P. 1198–1201.
10. Gramann J., Hippeli S., Dornisch K. et al. Antioxidant Properties of Essential Oils, Arzneim. Forsch. // Drug. Res. 2000. Vol. 50 (1). P. 135–139.
11. Beuscher N., Kietzmann M., Bien E., Champeroux P. Interference of myrtol standardized with inflammatory and allergic mediators // Arzneimittelforschung. 1998. Vol. 48 (10). P. 985–989.
12. Rantzsch U., Vacca G., Dück R., Gillissen A. Anti-inflammatory effects of Myrtol standardized and other essential oils on alveolar macrophages from patients with chronic obstructive pulmonary disease // Eur. J. Med. Res. 2009. Vol.14 (Suppl. 4). P. 205–209.
13. Federspil P., Wulkow R., Zimmermann T. Effects of standardized Myrtol in therapy of acute sinusitis – results of a double-blind, randomized multicenter study compared with placebo // Laryngorhinootologie. 1997. Vol. 76 (1). P. 23–27.
14. Зайцева О.В. Роль муколитической терапии при синубронхиальном синдроме // Вестник оториноларингологии. 2012. № 2. С. 63–65.
15. Sengespeik H.C., Zimmermann T., Peiske C., de Mey C. Myrtol standardized in the treatment of acute and chronic respiratory infections in children. A multicenter post-marketing surveillance study // Arzneimittelforschung. 1998. Vol. 48 (10). P. 990–994.












