Предметом обсуждения на симпозиуме явились новейшие исследования по микробиологии и эпидемиологии пневмококка, были рассмотрены меры по совершенствованию лечения инвазивных пневмококковых заболеваний. Неоднократно в докладах на симпозиуме приводились данные о генетических различиях в спектре серотипов пневмококка в зависимости от региона, социально–экономических и других факторов.
Значительная часть сессий была посвящена теме профилактики пневмококковой инфекции с помощью вакцинации. Проблема дальнейшей разработки уже существующих пневмококковых вакцин и создания новых высокоэффективных и безопасных вакцинных препаратов чрезвычайно актуальна в последнее десятилетие. Особая значимость вакцинопрофилактики обусловлена широкой распространенностью пневмококковой заболеваемости в мировом масштабе, а также стремительным ростом антибиотикоустойчивости возбудителя и, как следствие – неэффективностью лечения. Учитывая позицию ВОЗ, что «... вакцинация – единственный способ существенно повлиять на заболеваемость пневмококковой инфекцией», на первый план выступает приоритетность включения современных высокоэффективных и безопасных пневмококковых вакцин в национальные программы иммунизации по всему миру.
Ученые, выступившие на симпозиуме, представили данные о существенных изменениях в последовательностях генома «современного» пневмококка по сравнению с возбудителем двухлетней давности. Характерной чертой процесса эволюции Str. pneumoniae признается приобретение им устойчивости к большинству доступных антибактериальных препаратов, что было продемонстрировано многими учеными – участниками симпозиума. Эксперты отметили, что с повышением антибактериальной резистентности пневмококка, количество новых антибиотиков, приходящих на рынок, фактически уменьшается, потенциально ограничивая доступность необходимых средств для лечения пневмококковых заболеваний. Это затрудняет лечение пациентов с пневмококковой инфекцией, увеличивает продолжительность госпитализации и расходы на лечение. Докладчики подчеркнули необходимость достижения оптимального баланса между наиболее ранним началом терапии заболевания, вызванного пневмококком, и попыткой избежать неразумного применения антибиотиков, что способствует росту антибиотикорезистентности возбудителя и сокращает количество доступных для лечения ресурсов.
Пневмококковая вакцинация:
сегодня и завтра
Как известно, созданная более 20 лет назад полисахаридная пневмококковая вакцина (ППВ), успешно применяемая и в настоящее время, в основном у детей старшего возраста и взрослых, имеющих высокий риск заболевания пневмококковой инфекцией, имеет ряд недостатков – отсутствие иммунологической памяти и бустер–эффекта при ревакцинации, не влияет на бактерионосительство, не предупреждает формирования антибиотикорезистентности. В связи с этим ППВ не может быть использована для массовой вакцинации детей раннего возраста.
Одним из важнейших достижений медицинской науки последних лет является создание 7–валентной конъюгированной пневмококковой вакцины Превенар (ПКВ7) производства компании Pfizer, позволяющей существенно снизить заболеваемость пневмококковой инфекцией. Конъюгированная пневмококковая вакцина способствует формированию Т–клеточного иммунного ответа с индукцией иммунологической памяти, в том числе у детей, начиная с 6 недель жизни. Выработка защитных антител может наблюдаться даже у пациентов с различными вариантами иммунодефицита. Более того, вакцина защищает не только от инфицирования, но и предотвращает назофарингеальную колонизацию, тем самым уменьшая распространение возбудителя в популяции и оказывая позитивное воздействие на заболеваемость пневмококковой инфекцией среди взрослых. В результате такого действия вакцины Превенар создается эффект группового иммунитета, когда «прививая младенцев, мы защищаем от пневмококковых заболеваний взрослых членов их семей».
В рамках симпозиума неоднократно приводились факты резкого снижения частоты инвазивных пневмококковых заболеваний в результате применения ПКВ7 в различных странах мира, а также достоверно значимого снижения уровня заболеваемости другими формами пневмококковой инфекции. На нескольких пленарных сессиях рассматривались результаты исследований, которые продолжают приносить доказательства эффективности ПКВ7 в снижении назофарингеального носительства у привитых детей, а также в уменьшении уровня инвазивных заболеваний у окружающих взрослых в результате прерывания передачи возбудителя от детей ко взрослым («групповой иммунитет»).
В настоящее время разработаны и разрешены к применению три пневмококковые конъюгированные вакцины (табл. 2). Данные вакцины различаются количеством серотипов пневмококка, входящими в ее состав; белком–конъюгатом; количеством полисахарида для каждого конъюгата.
Значимым событием симпозиума стало также представление конъюгированных пневмококковых вакцин следующего поколения, готовящихся к регистрации в России. В состав разработанной ПКВ10 входят дополнительно серотипы 1, 5 и 7F к существующей группе серотипов, включенных в ПКВ7, в то время как в ПКВ13 добавлены также 3, 6A и 19A серотипы пневмококков. Опубликованные данные третьей фазы клинического исследования ПКВ13 свидетельствуют о высокой иммуногенности и хорошей переносимости у младенцев, получивших, как минимум, 3 дозы вакцины [3]. Вакцина Превенар ПКВ13 не препятствует формированию иммунного ответа на сопутствующие педиатрические вакцины, а общий уровень безопасности ПКВ13 сопоставим с ПКВ7. ПКВ13 производится с использованием того же белка–конъюгата, что Превенар, данный белок используется в производстве вакцин для детей уже более 20–и лет и является безопасным биологическим компонентом. Сравнительные данные также показали, что титр защитных антител на серотипы 6А и 19А был выше в сравнении с ПКВ7. Как ожидается, постепенный переход на ПКВ13 позволит предупредить до 90% инвазивных форм пневмококковой инфекции, и, прежде всего, заболеваний, вызванных пневмококком, обладающим высоким уровнем антибактериальной резистентности и способностью к бактерионосительству.
Благодаря данным этих и других исследований докладчики выразили ожидания, что переход от ПКВ7 к ПКВ13 не создает клинических и организационных проблем. Прозвучали упоминания о ходе дополнительных исследований, которые должны определить возможность применения ПКВ13 у взрослых.
В дополнение к успехам, достигнутым в результате разработок пневмококковых конъюгированных вакцин, исследователи представили параллельно развивающиеся технологии создания альтернативных вакцинных препаратов. Одним из самых интересных направлений в создании пневмококковых вакцин являются белковые вакцины на основе различных пневмококковых протеинов. Докладчики обратили внимание на сложность разработки вакцин против пневмококка в связи с тем, что приходится бороться с бактериями более, чем 90 пневмококковых серотипов, которые различаются в зависимости от региона и постоянно подвержены мутации и динамике. Кроме того, существенным является вопрос снижения затрат на производство вакцинных препаратов и его упрощение, что позволит сделать вакцины более доступными, в том числе людям с низким доходом из развивающихся стран.
Таким образом, докладчики особо отметили важность разработки новых вакцин, способных расширить охват серотипов пневмококка, еще более повысить их иммунологическую эффективность, в том числе и на уровне слизистой оболочки, а также поддерживать более продолжительную иммунную защиту (особенно у пациентов из групп риска).
Преимущества различных
схем вакцинации
Результаты многочисленных научных исследований, проведенных в разных странах мира, уже позволили четко обосновать безопасность, иммуногенность и эффективность имеющихся пневмококковых вакцин. Значительную пользу демонстрируют различные графики иммунизации: 3+1, 2+1, 3+0. Согласно рекомендациям ВОЗ в большинстве стран принято использовать 3 дозы ПКВ7 с месячным интервалом и введением ревакцинирующей дозы в возрасте старше 12 месяцев. Однако до сих пор бурную дискуссию вызывает обсуждение наиболее оптимальных схем вакцинации.
Вот лишь несколько доказанных фактов в отношении иммунизации пневмококковой конъюгированной вакциной:
• Одна доза первичной серии – наименьшая за-щита, чем две и более. Проведенное на Фиджи рандомизированное двойное слепое исследование среди 552 детей, привитых ПКВ7, показало, что самый высокий титр антител был достигнут после 3–й дозы вакцины, а наименьший после – первой. Причем соответствующие различия были наиболее заметны в отношении серотипов пневмококка 6В и 23F. Через 12 месяцев уровень иммунной защиты сравнялся у детей, получивших 3 и соответственно 2 дозы, но был достоверно выше, чем у однократно вакцинированных младенцев.
• Интервал между дозами первичной серии – 2 месяца лучше, чем 1 месяц. Исследование вакцины ПКВ10, проведенное в Великобритании среди 284 детей раннего возраста, продемонстрировало наибольшую эффективность 2–месячного интервала между введением доз первичной серии в сравнении с месячным интервалом. Достоверно значимая разница в титре антител отмечена для следующих серотипов пневмококка: 6В, 14 и 23F. Однако после введения бустерной дозы различий в уровне титра пневмококковых антител найдено не было.
• Высокая иммунологическая и клиническая эффективность достигается после введения ревакцинирующей дозы, в большинстве случаев даже выше, чем после первичной серии. Существуют исследования, подтверждающие достоверно значимую эффективность бустера в отношении уровня носительства пневмококка и заболеваемости инвазивными формами инфекции на втором году жизни.
• Полисахаридная пневмококковая вакцина (ППВ) в качестве бустерной дозы не снижает уровня носительства возбудителя [4].
В заключительных сообщениях отмечалось, что разница в эффективности существующих графиков вакцинации незначительна и может быть не заметна с учетом группового эффекта при массовой вакцинации. При этом необходимо подчеркнуть, что не существует достаточных доказательств в поддержку рекомендаций по использовании у детей до 2 лет меньшего количества, чем 2 дозы пневмококковой конъюгированной вакцины.
И все же до сих пор остаются окончательно нерешенными вопросы: какова продолжительность иммунной защиты после различных графиков вакцинации и должны ли различаться схемы иммунизации в развитых и развивающихся странах.
Взаимодействие пневмококка
с другими возбудителями.
Парадигма вируса гриппа
Темой, вызвавшей большой интерес в ходе проведения симпозиума, было взаимодействие между пневмококком и другими возбудителями, и в первую очередь с вирусом гриппа. Серьезная дискуссия была сфокусирована на исследовании, показавшем, что грипп предрасполагает к развитию бактериальной внебольничной пневмонии. На примере каждой из пандемий гриппа ХХ века было установлено, что присоединение вторичной бактериальной инфекции является серьезной причиной заболеваемости и смертности во время пандемий гриппа. Убедительные данные других исследователей наводят на мысль о существовании «окна» в сопротивляемости бактериальным инфекциям, следующим сразу за заражением гриппом, что было достоверно продемонстрировано на ряде моделей млекопитающих, включая мышей, хорьков и обезьян. Так, взаимодействие 2 патогенов приводило к значительному росту уровня смертности животных.
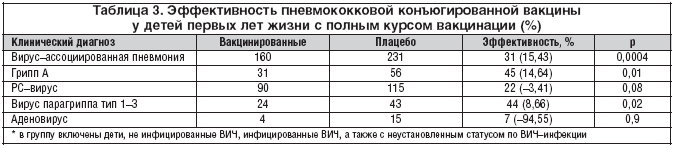
Исследование проведенное в США Центром по контролю и предупреждению заболеваемости (Center of Disease Control and Prevention, 2009), выявило, что приблизительно в одной трети случаев смерти в результате случившейся в 2009 году пандемии гриппа А (H1N1) причиной стала ко–инфекция с пневмококком. Отдельные исследования также демонстрируют, что во время сезонных вспышек гриппа в предыдущие годы заранее проведенная вакцинация ПКВ–7 способствовала снижению риска госпитализации и смерти от гриппа. В частности, была показана высокая эффективность пневмококковой конъюгированной вакцины (ПКВ) среди младенцев в отношении гриппа А и вирус–ассоциированных пневмоний (табл. 3).
Докладчики отметили, что приведенные доказательства подчеркивают необходимость включения пневмококковых вакцин в расширенную стратегию по предотвращению грипп–ассоциируемой заболеваемости и смертности. Участники симпозиума настаивали на применении пневмококковых вакцин, как части плана подготовки к возможной пандемии гриппа.
Таким образом, в ходе 10–летнего применения пневмококковой конъюгированной вакцины значительно снизился уровень заболеваемости пневмококковой инфекцией, вызванной вакцинными серотипами. Одновременно с наблюдаемым снижением пневмококковой заболеваемости в странах, где ПКВ7 включена в Национальные календари вакцинации, на симпозиуме неоднократно подчеркивалась необходимость проведения постоянного мониторинга за уровнем распространенности пневмококков. Целевые серотипы, вызывающие пневмококковые заболевания, постоянно меняются с течением времени и от страны к стране, что придает особую значимость глобальным программам по эффективному наблюдению за ситуацией и определению нужд в области развития будущих пневмококковых конъюгированных вакцин. В качестве резюме участники симпозиума отметили серьезную значимость обмена знаниями о пневмококке и согласились с необходимостью раннего и широкого внедрения пневмококковых конъюгированных вакцин в развивающихся странах с обязательным тщательным отслеживанием новых потенциально опасных серотипов пневмококков для совершенствования вакцинных препаратов и схем иммунизации.
![Таблица 1. Количество смертей, которые можно предотвратить с помощью вакцинации (Vaccine Preventable Deaths) [1]](/data/articles/Image/t18/n20/1228-1.gif)

Литература
1. WHO Global Immunization Vision and Strategy, April 2005 www.who.int/vaccines/GIVS/english/Global_imm._data_EN.pdf.
2. Roman Prymula et al. Pneumococcal capsular polysaccharides conjugated to protein D for prevention of acute otitis media caused by both Str.pneumoniae and non–typable H.influenzae: a randomized double–blind efficacy study. Lancet 2006; 367: 740–48.
3. A. Gurtman et al. Immunogenicity and safety of a 13–valent pneumococcal conjugate vaccine given with routine pediatricvaccinations in the United States. – 7th International Symposium on Pneumococci and Pneumococcal Diseases. Abstract 217.
4. Russel F. Pneumococcal nasopharyngeal carriage following a reduced dose 7–valent pneumococcal conjugate vaccine schedule in infancy and 23–valent pneumococcal polysaccharide vaccine booster. – 7th International Symposium on Pneumococci and Pneumococcal Diseases. Abstract 206.
5. Madhi SA et al. Nat Med. 2004; 10: 811–813.











